Chinese Journal of Tissue Engineering Research ›› 2015, Vol. 19 ›› Issue (10): 1624-1629.doi: 10.3969/j.issn.2095-4344.2015.10.027
Previous Articles Next Articles
Poultry mesenchymal stem cells: exploration and prospects
Li Dong-sheng1, 2, Wang Bing-yun1, Chen Zhi-sheng1, Chen Sheng-feng1, Ji Hui-qin1, Xian Qiong-zhen1, Chen Jin-ding2
- 1College of Life Science, Foshan University, Foshan 5282312, Guangdong Province, China; 2College of Veterinary Medicine, South China Agricultural University, Guangzhou 510642, Guangdong Province, China
-
Online:2015-03-05Published:2015-03-05 -
Contact:Wang Bing-yun, Professor, College of Life Science, Foshan University, Foshan 5282312, Guangdong Province, China -
About author:Li Dong-sheng, Studying for master’s degree, College of Life Science, Foshan University, Foshan 5282312, Guangdong Province, China; College of Veterinary Medicine, South China Agricultural University, Guangzhou 510642, Guangdong Province, China -
Supported by:the National Natural Science Foundation of China, No. 31201871; the Natural Science Foundation of Guangdong Province, No. S2012010010526
CLC Number:
Cite this article
Li Dong-sheng, Wang Bing-yun,Chen Zhi-sheng, Chen Sheng-feng, Ji Hui-qin, Xian Qiong-zhen, Chen Jin-ding. Poultry mesenchymal stem cells: exploration and prospects[J]. Chinese Journal of Tissue Engineering Research, 2015, 19(10): 1624-1629.
share this article
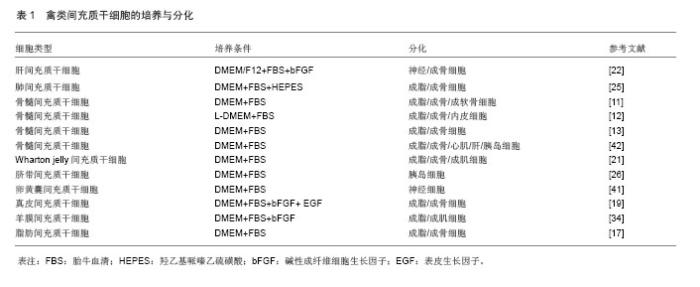
2.1 禽类间充质干细胞的来源 间充质干细胞来源广泛,骨髓、脂肪、皮肤、羊膜、卵黄囊等组织中均能分离到间充质干细胞。 2.1.1 骨髓来源的间充质干细胞 骨髓由3种细胞系统组成:造血系统、内皮系统和基质系统。这3种细胞系统皆存在造血干细胞、内皮祖细胞和间充质干细胞。其中骨髓间充质干细胞具有向多种中胚层和神经外胚层组织细胞分化的能力[9]。 Cohnheim等在1867年通过实验推测骨髓内存在非造血功能的干细胞。Caphan[10]把这些具有一定黏附能力,在体外能高度扩增、并可多向分化的干细胞群命名为间充质干细胞。2009年Mahesh从1-14 d龄的鸡骨髓中分离到间充质干细胞,这些间充质干细胞能在体外很好的培养、增殖和分化[11]。Bai等[12]和李双星等[13]相继于2013年和2014年获得北京油鸡和罗曼鹤鸡的骨髓间充质干细胞。Li等[14]从1 d龄鸭骨髓中获得了鸭的骨髓间充质干细胞,并进行了长期的体外培养。大量研究表明骨髓间充质干细胞具备易于分离培养、增殖纯化、多次传代扩增后仍具有干细胞特性、免疫原性低、体外基因转染率高并能在宿主体内长期存活等优点。 2.1.2 脂肪组织来源的间充质干细胞 脂肪间充质干细胞不仅来源丰富、取材方便,而且同骨髓间充质干细胞有着相似的生物学特性及类似的免疫表型,引起了国内外研究者的广泛关注。2001年Zuk等[15]分离获得了人的脂肪源间充质干细胞。禽类的脂肪间充质干细胞研究相对少,2011年Gong等[16]从1 d龄鸡皮下脂肪组织中首次分离到鸡的脂肪间充质干细胞,唐小洪等[17]于2014年建立鸡的脂肪源间充质干细胞的分离与鉴定方法。这些间充质干细胞表达CD29、CD44及CD71等表型,不表达造血干细胞表面标志CD45、CD34,并具有向脂肪细胞、成骨细胞分化的能力。 2.1.3 皮肤来源的间充质干细胞 随着从骨髓、胎盘、脐带和骨骼肌等组织中分离间充质干细胞的研究日益广泛,人们开始从皮肤组织中分离间充质干细胞。杨立业等[18]从小鼠的皮肤组织中分离到原代的皮肤间充质干细胞,这些细胞多次传代后仍具有形态均一、体外增殖迅速等特征和向成骨细胞、脂肪细胞和神经元样细胞分化的潜能。Gao等[19]从16 d龄鸡的背侧皮肤组织中分离到能表达CD29、CD44及CD71等表面标志和具有成骨、成脂和成神经组织分化能力的鸡皮肤间充质干细胞。 2.1.4 脐带Wharton's Jelly来源的间充质干细胞 1991年Mcelreavey等[20]首次从人脐带的Wharton’s Jelly中分离培养到了一种成纤维样细胞,具有较高的分化潜能,可向多个方向进行分化的间充质干细胞。脐带Wharton's Jelly间充质干细胞不仅自身免疫原性弱,而且可以抑制同种异体免疫反应,降低移植物抗宿主反应。2013年Bai等[21]从鸡的Wharton's Jelly中分离得到鸡的脐带Wharton's Jelly间充质干细胞。脐带Wharton's Jelly间充质干细胞和骨髓间充质干细胞具有很多相似的生物学特性,如在细胞形态学方面均为成纤维细胞样细胞,呈漩涡状生长,具有一定的方向性,都能诱导分化为成骨细胞、成脂细胞和神经细胞。 2.1.5 羊膜来源的间充质干细胞 以往研究从人羊膜培养出间充质干细胞,经免疫表型鉴定与骨髓间充质干细胞相似,并且其比骨髓来源的间充质干细胞具有更强的扩增能力;同时从羊膜中提取间质干细胞来源广泛,受社会伦理学限制较少等优点,成为干细胞来源的主要研究目标。2014年Li等首次分离培养了羊膜间充质干细胞,该羊膜间充质干细胞表达CD29、CD44及CD71等表面标志和干细胞标志基因Oct4,并能诱导分化为成骨细胞、成脂细胞和成肌细胞。 2.1.6 其他来源的间充质干细胞 很多学者报道,从禽类骨组织、卵黄囊、胚胎肺脏和胚胎肝脏等组织器官中均成功分离出禽类间充质干细胞[22-26]。 2.2 禽类间充质干细胞的分离、纯化和培养 由于间充质干细胞在组织中的含量低,获取高纯度的间充质干细胞就显得尤为重要。目前最常用的分离间充质干细胞的方法有组织消化法、全骨髓贴壁法和密度梯度离心法。不同组织来源的间充质干细胞分离方法不同,但是禽类间充质干细胞大多数采用组织消化法+差速贴壁法进行分离培养。对于人和鼠骨髓、外周血和脐血等主要采用Percoll或Ficoll离心方法分离单个核细胞,然后用贴壁法进一步分离纯化间充质干细胞。改进密度梯度离心法,可提高了骨髓源间充质干细胞的分离效率和富集[27]。 间充质干细胞的体外培养,一般都是以DMEM为基础培养基,以经过筛选的胎牛血清为主要营养支持物。为了使间充质干细胞维持更好的生长状态和传代次数,一些研究者在使用血清的时候还要加入一些生长因子,如碱性成纤维细胞生长因子、表皮生长因子和转化生长因子等。田少囡等[24]优化了北京油鸡肺间充质干细胞的培养体系,表明DMEM/F-12基础培养基+体积分数为10%胎牛血清+2 mmol/L L-谷氨酰胺+10 μg/L 碱性成纤维细胞生长因子最有利于北京油鸡肺间充质干细胞的生长增殖。Gao等[19]运用L-DMEM +体积分数为10%胎牛血清+ 2 mmol/L L-谷氨酰胺 +20 μg/L表皮生长因子+ 20 μg/L碱性成纤维细胞生长因子+2 mmol/L 丙酮酸钠来培养皮肤间充质干细胞。而牧仁等[23]运用体积分数为10%胎牛血清+5 μg/L 碱性成纤维细胞生长因子+ DMEM-F12的培养体系来培养胚肝间充质干细胞。在众多生长因子中,碱性成纤维细胞生长因子的作用最突 出[28],作为间充质干细胞有效的有丝分裂原,碱性成纤维细胞生长因子可以保持分化潜能,增加端粒长度。 2.3 禽类间充质干细胞的生物学特性 禽类间充质干细胞广泛存在于全身结缔组织和器官间质中。体外培养的间充质干细胞,相差显微镜下观察到以梭形细胞为主,胞浆丰富,核大,细胞平行或呈漩涡状盘旋排列。间充质干细胞具有高度增殖、自我更新和多向分化的潜能[29]。随着研究的深入发现在不同诱导条件下,可分化为软骨、骨、骨骼肌、肌腱和脂肪等中胚层细胞,同时还可以向外胚层的神经细胞和内胚层的肝卵圆性细胞分化。间充质干细胞是一个异质细胞群,因此至今未发现其特异性抗原表型。一般认为其表达的抗原标记有:SH2、SH3、CD90、CD44、CD29、CD71、CD106、CD120和CD124,不表达其他造血细胞系的表面标记,如CD11b、CD45、CD14和CD34,不表达内皮细胞系的表面标记,如CD31。羊膜来源的鸡间充质干细胞表达CD29、CD44、Vimentin及CD71等表型,不表达上皮细胞标志CK19和造血细胞的表面标记CD34。间充质干细胞不仅能够向多种组织和细胞分化,而且还具有易于分离、培养、扩增和遗传背景相当稳定等特点。 2.4 禽类间充质干细胞的多向分化潜能 间充质干细胞在体外特定诱导环境下,能够分化为脂肪细胞、软骨细胞、成骨细胞、成肌细胞、神经细胞、上皮细胞、胰岛细胞、肾小管细胞和肝细胞等多种功能性细胞。 2.4.1 向脂肪细胞分化 脂肪细胞不仅是机体内主要的能量储存单元,也可以分泌多种细胞因子,在调控机体能量平衡、糖代谢及免疫反应等方面发挥着重要的作用。脂肪细胞是由起源于中胚层的多功能间充质干细胞分化而来,其过程涉及一连串复杂的转录因子级联效应和相关细胞周期蛋白调控,最终导致脂肪细胞分化成熟[30]。 目前对于体外培养的间充质干细胞向成脂分化的研究较多,3-异丁基-1-甲基黄嘌呤(IBMX)、胰岛素、吲哚美辛和地塞米松是诱导骨髓间充质干细胞成脂分化的经典诱导剂,这4种诱导剂合用可诱导间充质干细胞定向分化为成熟脂肪细胞。另外,某些因子如氢化可的松、三碘甲状腺原氨酸、油酸和辛酸也能够诱导骨髓间充质干细胞分化成脂肪细胞。 在哺乳动物上,含有0.1 mmol/L 3-异丁基-1-甲基黄嘌呤、0.1 mmol/L 吲哚美辛、1 μmol/L 地塞米松、不同浓度胰岛素及胎牛血清的DMEM 组方可以定向诱导大鼠骨髓间充质干细胞分化为脂肪细胞[31]。Muraglia等[32]用地塞米松和胰岛素成功分化人骨髓间充质干细胞为脂肪细胞。Du等[33]用成脂诱导液(50 nmol/L胰岛素、50 nmol/L地塞米松、50 μmol/L油酸、0.5 mmol/L辛酸和体积分数为5%胎牛血清的DMEM培养基)对猪骨髓间充质干细胞进行诱导10 d后,检测到脂肪相关基因PPARγ、C/EBPα、aP2和perilipin等的大量表达。在上述成脂分化中,有关学者分别用了含有胰岛素和地塞米松的不同诱导组方来对不同物种不同来源的间充质干细胞进行诱导。胰岛素可通过与骨髓间充质干细胞胰岛素样生长因子1受体结合,促进骨髓间充质干细胞增殖分化。地塞米松能激活骨髓间充质细胞表面的糖皮质激素受体,使其向脂肪细胞分化。基于哺乳动物间充质干细胞向成脂分化的研究结果,鸡间充质干细胞成脂分化的研究相继开展,Bai等[21]选用1 mmol/L地塞米松,0.5 mmol/L IBMX和10 mg/L胰岛素的组合同样可以诱导鸡间充质干细胞分化为脂肪细胞[16];而Li等[34]用 1 mmol/L地塞米松,200 μmol/L吲哚美辛,0.5 mmol/L IBMX和10 μmol/L胰岛素的诱导组方也成功获得成脂细胞。另外有报道称,如果在成脂诱导液中间歇加甲状旁腺激素的话,间充质干细胞向成脂肪细胞的分化将会受到抑制,即甲状旁腺激素可以抑制细胞分化成脂肪细胞[35]。 2.4.2 向肌肉细胞分化 1999年,Makino等最早报道在体外将骨髓间充质干细胞诱导分化为心肌样细胞。Toma等[36]把人骨髓间充质干细胞注射到免疫缺陷鼠的心脏,观察到间充质干细胞分化为心肌样细胞,并表达一定的心肌标志物。Gang等[37]报道,人脐血间充质干细胞在含有地塞米松、氢化可的松和马血清的诱导液作用下可以成功分化成骨骼肌细胞。另一方面,5-氮杂胞苷在间充质干细胞成肌分化过程中扮演重要角色。人或小鼠的间充质干细胞可通过5-氮杂胞苷诱导后能够分化成骨骼肌细胞[38],Du等[33]利用5-氮杂胞苷也成功诱导猪骨髓间充质干细胞分化成骨骼肌细胞。Bai等[21]用10 μmol/L 5-氮杂胞苷处理间充质干细胞24 h后,换用L-DMEM完全培养液培养21 d出现心肌样细胞。5-氮杂胞苷可与 DNA 共价结合形成复合物,抑制其甲基化作用,使其发挥去甲基化作用,促使成肌分化的相关调控基因表达,启动向肌细胞定向分化。 2.4.3 向骨细胞分化 目前研究最多的间充质干细胞诱导分化就是向成骨细胞方向分化,通常采用的诱导剂有地塞米松、β-甘油磷酸钠、抗坏血酸等物质。诱导骨髓间充质干细胞向软骨细胞系分化的生长因子包括碱性成纤维细胞生长因子、转化生长因子β1、胰岛素样生长因子及骨形成蛋白等。转化生长因子β1在成骨分化和骨的改建过程中发挥重要作用。骨形成蛋白可诱导骨髓间充质干细胞经过趋化、分裂、分化等过程不可逆地分化成骨或成软骨,是目前惟一能异位诱导成骨且诱导成骨生成能力最强的细胞因子。转化生长因子β1可以促进间充质干细胞的有丝分裂,大量增殖分化为成骨细胞,增加骨钙盐的沉积含量,同时抑制脂肪细胞生成。 另外,一些中药和植物提取物可以诱导分化为骨细胞。柚皮苷诱导骨髓间充质干细胞后,显著增加细胞的碱性磷酸酶活性[39]。刘钰瑜等[40]报道大黄素的诱导作用主要在骨髓间充质干细胞向成骨细胞分化的骨形成早期,促进成骨细胞成熟和启动钙化。Gao等[41]用补肾中药右归饮的家兔含药血清诱导骨髓间充质干细胞定向分化为软骨细胞。Li等[14]和Gong等[16]分用β-甘油磷酸钠、地塞米松和维生素C成功诱导鸭和鸡的骨髓间充质干细胞分化为成骨细胞。唐小洪等[17]用地塞米松、β-甘油磷酸钠、抗坏血酸的组方诱导鸡的脂肪源间充质干细胞分化为成骨细胞。 2.4.4 向神经细胞分化 抗氧化剂、维甲酸、细胞生长因子、脱甲基试剂、中药单体黄芩苷等常作为间充质干细胞向神经细胞分化的主要诱导试剂。抗氧化剂诱导的具体机制尚不明确,研究表明用表皮生长因子或脑源性神经生长因子与视黄酸等组合将骨髓间充质干细胞诱导为神经元样细胞。Li等[14]用体积分数为20%胎牛血清和3 μmol/L β-巯基乙醇处理鸭间充质干细胞24 h后,改用含有2%二甲基亚砜和200 μmol/L丁基羟基茴香醚(BHA)的无血清培养基培养,能得到神经元样细胞。Gao等[19,41]用维甲酸诱导鸡的间充质干细胞分化成神经细胞。维甲酸主要通过其受体RARs和RXRs起作用,在间充质干细胞诱导分化过程中,有维甲酸受体的大量表达,维甲酸在体内对神经系统的分化发育具有多方面的作用。 2.4.5 向其他细胞分化 国内外一些研究报道禽类间充质干细胞还可以向胰岛样细胞[42]、肝细胞及上皮细胞等多方向分化,具有十分广阔的应用前景。 禽类间充质干细胞的培养与诱导分化条件,见表1,2。 "
| [1]Pittenger MF, Mackay AM, Beck SC,et al. Multilineage potential of adult human mesenchymal stem cells. Science. 1999;284(5411):143-147. [2]Friedenstein AJ, Petrakova KV, Kurolesova AI, et al. Heterotopic of bone marrow. Analysis of precursor cells for osteogenic and hematopoietic tissues. Transplantation. 1968; 6(2):230-247. [3]Flautre B, Anselme K, Delecourt C, et al. Histological aspects in bone regeneration of an association with porous hydroxyapatite and bone marrow cells. J Mater Sci Mater Med. 1999;10(12):811-814. [4]Bosch P, Pratt SL, Stice SL. Isolation, characterization, gene modification, and nuclear reprogramming of porcine mesenchymal stem cells. Biol Reprod. 2006;74(1):46-57. [5]张焱如,刘宗正,韦林盖,等.蒙古马骨髓间充质干细胞的分离培养及多向分化潜能的研究[J].畜牧兽医学报, 2011, 42(10): 1357-1361. [6]华松,武浩,赵慧英,等.山羊骨髓间充质干细胞的分离培养及向神经细胞诱导分化的研究[J].安徽农业大学学报, 2004, 31(3): 273-277. [7]Silveira P, Marin SY, Moreira PA, et al. Interactions of Plasmodium juxtanucleare and chicken anaemia virus: establishing a model. Parasitology. 2013;140(14):1777-1788. [8]Wang JX, Zhou JY, Yang QW, et al. An improved embryonated chicken egg model for the evaluation of antiviral drugs against influenza A virus.J Virol Methods. 2008;153(2): 218-222. [9]张瑞锋,吴金英,姚金凤,等. 间充质干细胞的来源[J]. 中国组织工程研究与临床康复, 2007, 11(15): 2968-2970. [10]Caplan AI.Osteogenesis imperfecta, rehabilitation medicine, fundamental research and mesenchymal stem cells.Connect Tissue Res. 1995;31(4):S9-14. [11]Khatri M, O'Brien TD, Sharma JM. Isolation and differentiation of chicken mesenchymal stem cells from bone marrow. Stem Cells Dev. 2009;18(10):1485-1492. [12]Bai C, Hou L, Ma Y,et al. Isolation and characterization of mesenchymal stem cells from chicken bone marrow. Cell Tissue Bank. 2013;14(3):437-451. [13]李双星,朴丰源,戚媛,等. 罗曼鹤鸡骨髓间充质干细胞的分离培养和鉴定[J]. 山东医药, 2014, 54(11): 1-4. [14]Li L, Bai X, Gong X, et al. Differentiation potential of bone marrow mesenchymal stem cells in duck. J Genet Genomics. 2009;36(3):133-140. [15]Zuk PA, Zhu M, Mizuno H, et al. Multilineage cells from human adipose tissue: implications for cell-based therapies. Tissue Eng. 2001;7(2):211-228. [16]Gong X, Hou L, Bai C, et al. Isolation and biological characteristics of chicken adipose-derived progenitor cells. DNA Cell Biol. 2011;30(7):453-460. [17]唐小洪,叶亚琼,李道通,等. 鸡脂肪源间充质干细胞的分离与鉴定[J]. 华南农业大学学报, 2014, 35(5):1-7. [18]杨立业,刘相名,惠国桢,等. 皮肤间充质干细胞的体外培养和分化[J]. 生物医学工程学杂志, 2005, 22(3): 514-517. [19]Gao Y, Bai C, Xiong H, et al. Isolation and characterization of chicken dermis-derived mesenchymal stem/progenitor cells. Biomed Res Int. 2013;2013:626258. [20]McElreavey KD, Irvine AI, Ennis KT, et al. Isolation, culture and characterisation of fibroblast-like cells derived from the Wharton's jelly portion of human umbilical cord. Biochem Soc Trans. 1991;19(1):29S. [21]Bai C, Li X, Hou L, et al. Biological characterization of chicken mesenchymal stem/progenitor cells from umbilical cord Wharton's jelly. Mol Cell Biochem. 2013;376(1-2):95-102. [22]牧仁,边艳超,浦亚斌,等. 北京油鸡胚胎肝脏间充质干细胞的生物学特性[J]. 华中农业大学学报, 2013, 32(6): 99-105. [23]牧仁,边艳超,浦亚斌,等. 北京油鸡胚胎肝脏来源间充质干细胞的分离培养及生物学特性[J]. 遗传, 2013, 35(3): 365-372. [24]田少囡,侯玲玲,关伟军,等. 北京油鸡肺间充质干细胞的分离培养及鉴定[J].生物技术通报, 2011(12): 139-144. [25]Khatri M, O'Brien TD, Goyal SM, et al. Isolation and characterization of chicken lung mesenchymal stromal cells and their susceptibility to avian influenza virus. Dev Comp Immunol. 2010;34(4):474-479. [26]Bai C, Gao Y, Li Q, et al. Differentiation of chicken umbilical cord mesenchymal stem cells into beta-like pancreatic islet cells.Artif Cells Nanomed Biotechnol. 2013 Dec 5. [Epub ahead of print] [27]李炳尧,武晓云,吴岩. 间充质干细胞的分离与培养:从实验室到临床[J]. 中国组织工程研究,2013,17(14): 2649-2655. [28]Nekanti U, Mohanty L, Venugopal P, et al. Optimization and scale-up of Wharton's jelly-derived mesenchymal stem cells for clinical applications. Stem Cell Res. 2010;5(3):244-254. [29]张凯,王毅,邢国胜.间充质干细胞的生物学特性及多向分化潜能[J].中国组织工程研究与临床康复,2008,12(3): 539-542. [30]Lefterova MI, Lazar MA. New developments in adipogenesis. Trends Endocrinol Metab. 2009;20(3):107-114. [31]徐道华,周晨慧,刘钰瑜,等.大鼠骨髓间充质干细胞分化成脂肪细胞的定向诱导[J]. 中国组织工程研究与临床康复, 2009, 13(1): 125-128. [32]Muraglia A, Cancedda R, Quarto R.Clonal mesenchymal progenitors from human bone marrow differentiate in vitro according to a hierarchical model. J Cell Sci. 2000;113 ( Pt 7):1161-1166. [33]Du MQ, Huang YQ, Lu NS, et al. Characterization and Differentiation into Adipocytes and Myocytes of Porcine Bone Marrow Mesenchymal Stem Cells. Journal of Integrative Agriculture. 2014(4): 837-848. [34]Li X, Gao Y, Hua J, et al. Research potential of multi-lineage chicken amniotic mesenchymal stem cells.Biotech Histochem. 2014;89(3):172-180. [35]Rickard DJ, Wang FL, Rodriguez-Rojas AM, et al. Intermittent treatment with parathyroid hormone (PTH) as well as a non-peptide small molecule agonist of the PTH1 receptor inhibits adipocyte differentiation in human bone marrow stromal cells.Bone. 2006;39(6):1361-1372. [36]Toma C, Pittenger MF, Cahill KS, et al. Human mesenchymal stem cells differentiate to a cardiomyocyte phenotype in the adult murine heart.Circulation. 2002;105(1):93-98. [37]Gang EJ, Jeong JA, Hong SH, et al. Skeletal myogenic differentiation of mesenchymal stem cells isolated from human umbilical cord blood.Stem Cells. 2004;22(4):617-624. [38]Burlacu A, Rosca AM, Maniu H, et al. Promoting effect of 5-azacytidine on the myogenic differentiation of bone marrow stromal cells. Eur J Cell Biol. 2008;87(3):173-184. [39]邓展生,张璇,邹冬青,等.骨碎补有效成分柚皮甙对人骨髓间充质干细胞的影响[J].湘南学院学报:自然科学版, 2005,7(4):5-7. [40]刘钰瑜,崔燎,吴铁,等.大黄素对体外大鼠骨髓基质细胞向脂肪细胞方向分化的影响[J].中国药理学通报, 2005,21(7):842-847. [41]Gao Y, Bai C, Wang K, et al. All-trans retinoic acid promotes nerve cell differentiation of yolk sac-derived mesenchymal stem cells.Appl Biochem Biotechnol. 2014;174(2):682-692. [42]Bhuvanalakshmi G, Arfuso F, Dharmarajan A, et al. Multifunctional properties of chicken embryonic prenatal mesenchymal stem cells- pluripotency, plasticity, and tumor suppression.Stem Cell Rev. 2014;10(6):856-870. |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Lin Qingfan, Xie Yixin, Chen Wanqing, Ye Zhenzhong, Chen Youfang. Human placenta-derived mesenchymal stem cell conditioned medium can upregulate BeWo cell viability and zonula occludens expression under hypoxia [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 4970-4975. |
| [3] | Hou Jingying, Yu Menglei, Guo Tianzhu, Long Huibao, Wu Hao. Hypoxia preconditioning promotes bone marrow mesenchymal stem cells survival and vascularization through the activation of HIF-1α/MALAT1/VEGFA pathway [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 985-990. |
| [4] | Shi Yangyang, Qin Yingfei, Wu Fuling, He Xiao, Zhang Xuejing. Pretreatment of placental mesenchymal stem cells to prevent bronchiolitis in mice [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 991-995. |
| [5] | Liang Xueqi, Guo Lijiao, Chen Hejie, Wu Jie, Sun Yaqi, Xing Zhikun, Zou Hailiang, Chen Xueling, Wu Xiangwei. Alveolar echinococcosis protoscolices inhibits the differentiation of bone marrow mesenchymal stem cells into fibroblasts [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 996-1001. |
| [6] | Fan Quanbao, Luo Huina, Wang Bingyun, Chen Shengfeng, Cui Lianxu, Jiang Wenkang, Zhao Mingming, Wang Jingjing, Luo Dongzhang, Chen Zhisheng, Bai Yinshan, Liu Canying, Zhang Hui. Biological characteristics of canine adipose-derived mesenchymal stem cells cultured in hypoxia [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1002-1007. |
| [7] | Geng Yao, Yin Zhiliang, Li Xingping, Xiao Dongqin, Hou Weiguang. Role of hsa-miRNA-223-3p in regulating osteogenic differentiation of human bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1008-1013. |
| [8] | Lun Zhigang, Jin Jing, Wang Tianyan, Li Aimin. Effect of peroxiredoxin 6 on proliferation and differentiation of bone marrow mesenchymal stem cells into neural lineage in vitro [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1014-1018. |
| [9] | Zhu Xuefen, Huang Cheng, Ding Jian, Dai Yongping, Liu Yuanbing, Le Lixiang, Wang Liangliang, Yang Jiandong. Mechanism of bone marrow mesenchymal stem cells differentiation into functional neurons induced by glial cell line derived neurotrophic factor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1019-1025. |
| [10] | Duan Liyun, Cao Xiaocang. Human placenta mesenchymal stem cells-derived extracellular vesicles regulate collagen deposition in intestinal mucosa of mice with colitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1026-1031. |
| [11] | Pei Lili, Sun Guicai, Wang Di. Salvianolic acid B inhibits oxidative damage of bone marrow mesenchymal stem cells and promotes differentiation into cardiomyocytes [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1032-1036. |
| [12] | Wang Xianyao, Guan Yalin, Liu Zhongshan. Strategies for improving the therapeutic efficacy of mesenchymal stem cells in the treatment of nonhealing wounds [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1081-1087. |
| [13] | Wang Shiqi, Zhang Jinsheng. Effects of Chinese medicine on proliferation, differentiation and aging of bone marrow mesenchymal stem cells regulating ischemia-hypoxia microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1129-1134. |
| [14] | Kong Desheng, He Jingjing, Feng Baofeng, Guo Ruiyun, Asiamah Ernest Amponsah, Lü Fei, Zhang Shuhan, Zhang Xiaolin, Ma Jun, Cui Huixian. Efficacy of mesenchymal stem cells in the spinal cord injury of large animal models: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1142-1148. |
| [15] | Chen Junyi, Wang Ning, Peng Chengfei, Zhu Lunjing, Duan Jiangtao, Wang Ye, Bei Chaoyong. Decalcified bone matrix and lentivirus-mediated silencing of P75 neurotrophin receptor transfected bone marrow mesenchymal stem cells to construct tissue-engineered bone [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 510-515. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||

