Chinese Journal of Tissue Engineering Research
Previous Articles Next Articles
Transforming growth factor beta 1 effects on cartilage tissue metabolism
Guo Tie-feng1, Zhou Ming-wang2, Li Sheng-hua2, Sun Feng-qi1, Mu Huan-xi1
- 1 Gansu University of Traditional Chinese Medicine, Lanzhou 730020, Gansu Province, China
2 Gansu Province Hospital of Traditional Chinese Medicine, Lanzhou 730050, Gansu Province, China
-
Received:2012-07-13Revised:2012-09-26Online:2013-04-09Published:2013-04-09 -
Contact:Zhou Ming-wang, Studying for doctorate, Attending physician, Gansu Province Hospital of Traditional Chinese Medicine, Lanzhou 730050, Gansu Province, China 923433675@qq.com -
About author:Guo Tie-feng★, Studying for master’s degree, Gansu University of Traditional Chinese Medicine, Lanzhou 730020, Gansu Province, China 923433675@qq.com -
Supported by:the Scientific Research Program of Gansu Educational Bureau, No. 1106B-16*
CLC Number:
Cite this article
Guo Tie-feng1, Zhou Ming-wang2, Li Sheng-hua2, Sun Feng-qi1, Mu Huan-xi1. Transforming growth factor beta 1 effects on cartilage tissue metabolism[J]. Chinese Journal of Tissue Engineering Research, doi: 10.3969/j.issn.2095-4344.2013.15.024.
share this article

2.1 转化生长因子β1结构及生物学特性 转化生长因子β超家族除转化生长因子β外,还包括骨形态发生蛋白,缪勒氏管抑制质(MIS) ,AMH[2-3],生长分化因子,抑制素和活化素等30种蛋白。在骨组织中,转化生长因子β1的异构体约占转化生长因子β的80%-90%,不同转化生长因子β基因中因其启动子的差异而表现出不同调节机制[4]。各种异构体在许多生物反应中表现出相似的作用,其中以转化生长因子β1最为重要。 转化生长因子β1是包括受体和配体的超家族中的一员。是一族具有多种功能的蛋白多肽,其基因定位于19q13•1染色体,cDNA 全长2 745 bp,人转化生长因子β1的 cDNA5'端起始码 ATG 位于 842 -844位,终止码 ATG 位于 2 016 -2 018 位,含有 7 个外显子,6 个内含子。人转化生长因子β1 基因 5’端序列包含 5 个明显的调控区: 1 个类增强子 ( enhancer - like) 活性区,2 个负调控区和 2 个启动子区,成熟型转化生长因子β1是相对分子质量为25 000同源二聚体,由两条相同的12.skD亚单位肽链通过二硫键相连结,每条单链含有112个氨基酸。大量存在于骨组织与血小板中,其生物学活性主要包括:促进成纤维细胞和巨噬细胞聚集,细胞的生长增殖,组织损伤的修复,骨质再生[5],免疫抑制,促进细胞外基质的合成,增加金属蛋白酶组织抑制因子活性,下调基质金属蛋白酶活性调节,胚胎发育,抗炎,抑癌以及趋化作用等[6]。 人转化生长因子是调控重组骨髓间充质干细胞的首选生长因子之一[7],可以增强间充质干细胞的增殖,并抑制间充质干细胞向脂肪细胞分化。骨微环境中潜在的转化生长因子β1激活对于调节控制骨再建过程有十分重要的作用[8]。其对软骨代谢的作用主要是:诱导间充质细胞向软骨细胞分化,促进软骨特异性基质的合成[9],如增加成骨细胞Ⅰ型胶原的合成,骨基质蛋白,骨粘连素,蛋白聚糖,纤维结合蛋白的产生,并保护软骨基质不被各种蛋白酶水解破坏,也可诱导滑膜中的间充质细胞持续迁入软骨缺损处[10]。转化生长因子β1可产生抑制或刺激两种作用,对软骨细胞的增殖分化具有双向调节作用[11-14],见表1,其表达时间较转化生长因子β2和转化生长因子β3最长。"

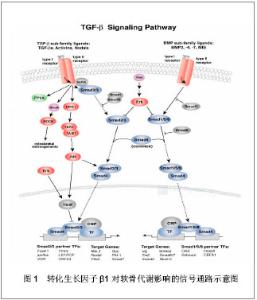
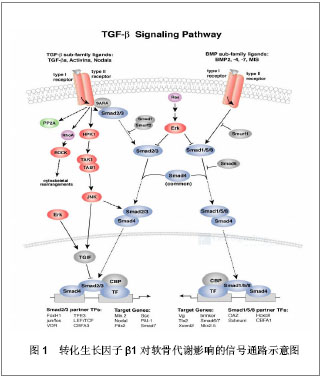
2.2 转化生长因子β1相关生物组织工程与软骨代谢 一般认为,转化生长因子β1呈剂量依赖性增强骨源性间充质细胞向软骨分化的作用,对成骨细胞或成软骨细胞具有促进或降低分化的双重调节作用。在骨关节炎硬化区软骨下高表达的转化生长因子β1可以抑制骨关节炎成骨细胞的矿化[15]。郭静等[16]发现高表达的转化生长因子β1对软骨和滑膜区域细胞凋亡具有负性调节作用。而低剂量转化生长因子β1则可促进其形成破骨细胞。许多研究通过各种方法增强转化生长因子β1的表达来促进成骨及成软骨细胞的分化[17- 18]。有文献报道转化生长因子β1最佳理想质量浓度为100 μg/L[19]。但由于其表达量的不同,软骨分化状态的不同,所产生部位的不同和骨组织内环境的不同,会导致调节作用的不同,所以如何控制转化生长因子β1的表达量使它的成骨效应得到最大的发挥,是值得进一步研究的问题。 转化生长因子β1可以促进骨髓间充质干细胞向软骨细胞分化,早期应用转化生长因子β1可提高骨髓基质干细胞的软骨分化能力,易成清等[20]证实转化生长因子β1基因转染能显著提高间充质干细胞增值能力。转化生长因子β1可能通过蛋白多肽的正性调节作用促进软骨细胞和成骨细胞内的转化生长因子β2发挥其作用[21]。有研究显示转化生长因子β1可促进重组人骨形态发生蛋白2 对 MC3T3-E1的增殖和成骨分化作用[22]。转化生长因子β1能够通过增加Ⅰ型胶原蛋白mRNA、骨桥蛋白及Runx2的表达及碱性磷酸酶活性刺激鼠类骨髓间充质干细胞的成软骨分化。此外,转化生长因子β1还可以促进滑膜细胞的纤维样增殖,使其分化成不同类型的软骨组织,这可能与其组织损伤的修复作用有关;转化生长因子β1可减少滑膜中炎性递质的释放,减轻炎症对滑膜及软骨细胞的损害。 转化生长因子β1促进软骨特异性基质的合成,其可促进合成的细胞外基质有:骨胶原蛋白类,主要是Ⅰ型胶原,还有非胶原蛋白,包括细胞黏附蛋白、骨桥蛋白、骨钙素等。转化生长因子β在促进鼠胚胎肌细胞分化成软骨细胞的同时,可合成其特异性的Ⅱ型胶原及硫酸软骨素蛋白多糖等[22]。有报道称转化生长因子β1在骨基质沉积过程中对早期分化有刺激作用,而对晚期分化的影响很小[23]。郑纪伟等[24]证实转化生长因子β1对钛表面成骨细胞中骨钙素,骨涎蛋白和Ⅰ型胶原蛋白基因表达有促进作用。转化生长因子β1刺激骨形态发生蛋白1 的变化可能直接影响到细胞外基质中活性赖氨酰氧化酶的表达[25]。但也有报道显示转化生长因子β可在培养的胚胎细胞中诱导软骨生成和Ⅱ型胶原合成,而在成熟的软骨细胞中则抑制Ⅱ型胶原的合成[26]。 另一方面,转化生长因子β1保护软骨基质不被各种蛋白酶水解破坏,软骨基质可被金属蛋白酶破坏,转化生长因子β1可以调控基质金属蛋白酶的活性和表达特性,被作为金属蛋白酶的抑制因子,阻止其对细胞外基质的消化。Qureshi等[27]使转化生长因子β1通过PI3K/Akt 通路诱导基质金属蛋白酶组织抑制因子表达,有效阻止了关节软骨的降解。研究发现骨关节炎中转化生长因子β1的高表达下调了关节软骨与滑膜中基质金属蛋白酶基质金属蛋白酶9 的表达,从而抑制了基质金属蛋白酶9对软骨的分解代谢,保护关节软骨,延缓骨关节炎的进展[28]。转化生长因子β1对一氧化氮的拮抗能力对延缓骨关节炎的进展也有重要作用。 转化生长因子β1在细胞内发挥的其生物效应的时间取决于半衰期的长短,而活性转化生长因子β1生物半衰期只有 2.0-3.0 min,只能在细胞内发挥短暂的生物效应,对于各种软骨退行性变或损伤的治疗,需要转化生长因子β1在体内发挥持续稳定的作用,随着组织工程技术的发展,我们可以将转化生长因子β1作为有效目的基因,然后利用基因转移技术将外源基因导入载体细胞,将基因转染后的载体细胞注入体内,使携有转化生长因子β1基因的载体细胞在体内表达治疗产物,转化生长因子β1作为导入靶细胞的具有治疗潜能的外源基因,要能够促进软骨细胞的增殖分化及细胞外基质的合成。这种基因转染的方法可以解决仅靠外源型细胞因子的缺陷,而将编码转化生长因子β1的基因转导入靶细胞内,使靶细胞持续表达合成转化生长因子β1 促进组织修复及愈合。 近年来,国内外学者将寻找多基因转染的种子细胞作为软骨组织工程的重点研究方向,其定向诱导脂肪干细胞向软骨细胞分化及合成细胞外基质的作用远强于单一细胞因子发挥的作用。张平等[29]发现白细胞介素1Ra 与转化生长因子β1 双基因组拮抗白细胞介素1 及 肿瘤坏死因子α的炎性作用优于单基因组。研究表明转化生长因子β1与骨形态发生蛋白2 联合作用更能促进骨髓间充质干细胞向软骨细胞诱导分化及分泌软骨特异性基质[30]。林成等[31]研究发现血管内皮生长因子和转化生长因子β1对NVBG同期种植体骨结合早期(术后一两个月)有明显的促进作用。顾海伦等[12]研究发现应用Ad-BMP-2、Ad-TGF-β转染椎间盘髓核细胞,可促进其中aggrecan 和Ⅱ型胶原合成,同时上调 aggrecan 和Ⅱ型胶原 mRNA 的表达。有实验证明培养的大鼠关节软骨细胞 DNA 合成速度可被转化生长因子β1 和胰岛素样生长因子1复合物提高 10 倍左右,其发挥的作用远强于两种因子单独使用[32]。 但也有一些实验结果显示转化生长因子β1与其他细胞因子的结合可对软骨代谢起到负性调节的作用,如血管内皮生长因子可在骨关节炎病程中发挥炎性递质效应,而抑制转化生长因子β1的炎性调节作用,导致滑膜炎形成及骨关节炎发生。转化生长因子β1和胰岛素样生长因子1 等细胞生长因子在加强软骨修复的作用的同时,也能导致骨赘的形成[33]。由于不明机制作用,使骨形态发生蛋白2/转化生长因子β复合物的成骨功能被部分或完全抵消,其效果不及二者单独使用的效果[34]。 2.3 转化生长因子β1相关基因多态性及与软骨代谢 转化生长因子β1基因定位于19q13,含6个内含子和7个外显子,富含GC和Ap2序列,是通过对Ap2启动子的激活来实现基因水平的调节。国内外的研究证实存在多个可影响转化生长因子β1的转录和表达基因多态性,包括-1348C/T、-765C/T、+29T/C、 + 869T/C、+915G/C、+788C /T、861-20T/C、-988C /A、-800G/A、和-509C/T等。其中转化生长因子β1基因 29T > C 单核苷酸多态性中 TT 基因型就被认为是促进颈椎前路自体髂骨椎间植骨融合的一个重要遗传因素[35]。国外报道称转化生长因子β1 的表达上调与-509 位点 C->T 突变有关。马进峰等[36]研究发现转化生长因子β1基因29T>C单核苷酸多态性中,TT基因型是影响骨肉瘤发病的一个重要遗传因素,与骨循环和易骨折性有关。转化生长因子β1 等位基因的变化与骨质疏松的发生及发展具有相关性[37],可通过上调微管蛋白,肌动蛋白等的基因表达来提高人脐带间充质干细胞的迁移能力,在基因水平上与人脐带间充质干细胞的翻译,转录,代谢,生物合成,信号转导,细胞间连接,细胞迁移具有相关性。 2.4 转化生长因子β1相关信号通路及软骨代谢 转化生长因子β1信号对关节软骨具有的作用主要体现为使软骨细胞维持在未分化状态,抑制其肥大分化。有实验证实被完全敲除Smad3的小鼠的关节软骨肥大分化并最终被骨组织替代,软骨组织被各类组织蛋白酶降解[38]。转化生长因子β1通过与相应受体结合启动信号转导通路,通过胞内信号分子进入细胞核内调节相关基因的表达[39]。转化生长因子β1 信号一方面能够促进软骨细胞的生成,分化,增殖,同时又可使软骨细胞的矿化和肥大作用遭到抑制[40]。这可能与转化生长因子β1 的下游传导因子在不同软骨细胞中的浓度不同有关。转化生长因子β1 信号对维持关节软骨具有很重要的作用,但它的功能和表达是随着年龄的增加而表现为逐渐衰退[41]。 目前发现的转化生长因子β1受体有8种,包括Ⅰ型,Ⅱ型,Ⅲ型,Ⅳ型,Endoglin,PLBPs,GI-210,其中PLBPs可能含有可结合转化生长因子β1 和转化生长因子β2 的两种受体。经大量研究证实Ⅰ型和Ⅱ型受体参与转化生长因子β1的信号传导已知的转化生长因子β信号转导下游途径有两种,分为Smad依赖性和Smad非依赖性。转化生长因子β1Smad依赖性信号转导途径如下: 转化生长因子β1通过与Ⅱ型受体二聚体形成复合物,使受体中的丝氨酸/苏氨酸蛋白激酶结构域发生磷酸化,同时将Ⅰ型受体中的GS结构域丝氨酸/苏氨酸磷酸化,Smad2和Smad3(R-Smads)受到活化的Ⅰ型受体的磷酸化激活,再与Smad4结合,即而经细胞膜将转化生长因子β1信号进入核内,可直接与特定的DNA序列结合,或与转录活化复合物或抑制物结合,亦可与其他转录因子协同作用[42],所以Ⅰ型与Ⅱ型受体是转化生长因子β1信号传导的必需分子。通过R-Smads途径转化生长因子β1可以阻止软骨细胞向成熟方向分化,进而阻止其凋亡发生。常有报道称转化生长因子β1对Ⅱ型受体的刺激往往要强于Ⅰ型受体,这可能与转化生长因子β1激活两种受体的先后顺序有关。Smad2调控软骨形成的效应随着细胞类型,细胞分化阶段和诱导条件差异亦有所区别。 Smad6和Smad7蛋白(I-SmadS)则能拮抗转化生长因子βⅠ型受体丝氨酸/苏氨酸蛋白激酶,它们通过与被激活的Ⅰ型受体结合,阻制R-smads的磷酸化,从而阻断信号通路[43]。有研究发现骨形态发生蛋白7有可能通过抑制了转化生长因子β/Smad通路中Smad3 mRNA表达[44],增加 Smad7 mRNA表达,从而拮抗转化生长因子β1的促纤维化作用。而在对ALK1-Smad158 信号通路的研究中发现此通路可以启动细胞的终末分化以及迁移[45],这可能是Smad蛋白家族成员对转化生长因子β家族的双向调节作用的机制。杨晓等[46]为了证实Smad3介导的转化生长因子β1信号对关节软骨的影响,分析了Smad3 基因敲除小鼠骨骼相关表型,结果发现系统或局部转化生长因子β1表达减少以及关节软骨细胞对转化生长因子β1 的反应性降低与关节软骨的退行性变相关。转化生长因子β1激活的信号转导通路和糖皮质激素之间具有复杂的相互作用,其机制有可能是转化生长因子β1的靶基因转录和信号转导被GC/GR通过与Smad的直接相互作用所抑制。 Smad非依赖性途径有MAPK通路、ERK和JNK、Wnt通路等,有研究表明转化生长因子β1可以诱导ERK信号通路[47],而高浓度的转化生长因子β1则可激活P38MARK信号通路。说明转化生长因子β1可根据其浓度高低诱导不同的通路,从而对破骨细胞的生成产生抑制或促进。另外,转化生长因子β1促使成骨细胞和巨噬细胞释放RANKL和M-CSF等破骨细胞分化因子,以促进破骨细胞的增殖分 化[48]。β-catetenin失活能促进软骨细胞分化,同时也能促进软骨细胞分化中的细胞死亡。并且RANKL与M-CSFmRNA的表达水平与转化生长因子β1的浓度具有相关性。也有文献称在褶皱部位的酸性环境 下[49],转化生长因子β1能够被处于骨吸收中的破骨细胞激活,进一步刺激成骨细胞下调 RANKL的表达,并增加骨保护素的表达。使RANKL/RANK复合体的减少,从而降低了破骨细胞的分化与活化。对转化生长因子β1作用的研究会出现不同甚至有矛盾的结果这可能与转化生长因子β1的来源、浓度及所使用细胞的不同有关。转化生长因子β1对软骨代谢影响的信号通路示意图见图1。"
| [1] Li H, Haudenschild DR, Posey KL, et al. Comparative analysis with collagen type II distinguishes cartilage oligomeric matrix protein as a primary TGFβ-responsive gene. Osteoarthritis Cartilage. 2011; 19(10): 1246-1253..[2] Everett ET. Fluoride's effects on the formation of teeth and bones,and the influence of genetics. Dent Res. 2011;90(5): 552-560.[3] Tachi K,Takami M,Sato H,et al.Enhancement of bone morphogenetic protein-2-induced ectopic bone formation bytransforming growth factor-β1[J]. Tissue Eng Part A. 2011;17(5-6):597-606.[4] 尹君,高传芳. 浅议TGF-β与原发性骨质疏松[J]. 临床医学, 2011, 26:86-87.[5] 王惠娟,董进. 转化生长因子 β 对成骨细胞增殖、BMP- 2及 Cbfal 基因表达的影响[J]. 中国当代医药,2011,18(22):21-23.[6] Wakefield LM, Stuehcn C. Keeping order in the neighborhood: newroles forTGF beta in maintaining epithelial homeostasis. CancerCel,l 2007;4: 293-295.[7] Sila Asna M,Bunyaratvej A,Maeda S,et al.Osteoblast differentiation and bone formation gene expression in stron-tium inducing bone marrow mesenchymal stem cell.Kobe J Med Sci.2007;53(12):25 -35.[8] 王维刚,王志刚,李大鹏,等. 骨肽对骨髓间充质干细胞TGF-β1表达的影响[J].中国实验诊断学,2012,16(4): 607-608.[9] 樊志强,庞炜,杨连甲,等. 白介素 1 受体拮抗剂及转化生长因子 β1 对兔膝关节骨性关节炎(OA)的治疗研究[J].现代生物医学进展,2011,11(13):2447-2450[10] 陈宁杰. 血管内皮细胞生长因子和转化生长因子β1在骨关节炎滑膜组织中的表达及相关性[J].中国组织工程研究与临床康复, 2009,13(2):288-291.[11] 田峰,崔学生,张帅,等.转化生长因子β1及白介素-1β对终板软骨细胞的作用[J]. 重庆医学,2012,41(1): 36-37,39.[12] 顾海伦,刘莉,王欢,等. d-BMP-2和Ad-TGF-β1共转染人退变椎间盘髓核细胞对细胞外基质代谢的影响[J]. 生物医学工程与临床,2009,13(1):58-61.[13] 俞猛,于方,付胜良,等.TGF-β1和bFGF对骨髓基质干细胞增殖、分化的影响[J]. 中国骨肿瘤骨病,2006,5(6): 321-325.[14] 郑丽芳,张小乔,张红,等.Snail基因沉默对转化生长因子- β1促进骨髓间充质干细胞迁移的抑制作用[J]. 解剖学报,2008,39(5): 717-722.[15] Couchourel D, Aubry I, Delalandre A,et al. Altered mineralization of human osteoarthritic osteoblasts is attributable to abnormal type I collagen production. Arthritis Rheum.2009;60(5):1438-1450.[16] 郭静,李琪佳. TGF-β1在骨性关节炎中的表达及与关节软骨和滑膜细胞凋亡的关系[J].中国煤炭工业医学杂志,2008,11(4): 462-465.[17] 孔祥英,万蓉,李莉,等.不同治法方药对激素性股骨头坏死鸡成骨相关因子的影响[J].中国中药杂志,2011,36(5):614-617. [18] 王磊磊,金格勒,任龙龙,等. 不同植骨材料在腰椎融合过程中的应用及转化生长因子β的表达[J].中国组织工程研究与临床康复,2011,15(16):2885-2888.[19] 鲁茂森,夏亚一,袁凌伟,等. 转化生长因子β1与软骨源性形态发生蛋白1修复关节软骨缺损[J]. 中国组织工程研究与临床康复, 2008,12(50):9824-9826[20] 易成清,曹云,马成辉,等.pAD- TGF-β1骨组织工程种子细胞转归的转基因保护[J].国际骨科学杂志,2011,32(2):127-135.[21] 胡振宇. TGF-β1促进rhBMP-2对成骨前体细胞增殖分化的观察[J].口腔颌面外科杂志,2012,22(1):24-26.[22] 杨冠,杨晓.TGF-β超家族在软骨发生、发育和维持中的作用[J].遗传,2008,30(8):953 -959.[23] Cabiling DS, Kim E, Yan D, et al. Differentialeffects of TGF-beta isoforms on murine fetal dural cells and calvarialosteoblasts.Plast Reconstr Surg.2007;120(3): 614-624.[24] 郑纪伟,高玉光,胡温庭,等.骨涎蛋白、骨桥蛋白在小鼠骨组织和牙胚组织发育中的表达[J].中国口腔颌面外科杂志,2009,6(12): 123-128.[25] 尹琳,谢静,蒋稼欢,等. TGF-β1刺激下损伤的前交叉韧带和内侧副韧带中 BMP-1基因的表达[J]. 第三军医大学学报,2012, 34(7): 647-650.[26] 吴剑.转化生长因子β与骨关节炎的研究进展[J].医学综述,2009,15(13):1929-1931.[27] Qureshi HY,Ahmad R,Sylvester J,et al. Re-quirement of phosphatidylinositol 3-kinase/Akt signalingpathway for regulation of tissue inhibitor of metallopro-teinases-3 gene expression by TGF-beta in human chon-drocytes.Cell Signal.2007;19(8): 1643 1651.[28] 郭静,张文丽,李琪佳,等. 基质金属蛋白酶 9 及 TGF-β1mRNA 和蛋白在骨关节炎中的表达[J]. 中国修复重建外科杂志,2011, 25(8): 992-997. [29] 张平,蔡道章,刘斌. 转 IL-1Ra 和 TGF-β1 基因治疗兔骨性关节炎[J]. 中华关节外科杂志,2011,5(3):335-422.[30] 张清林,吕惠成,吴一民. 转化生长因子β1联合骨形态发生蛋白2诱导骨髓间充质干细胞体外向软骨细胞的分化[J].中国组织工程研究与临床康复,2010,14(24):4371-4375.[31] 林成,刘宝林,刘彦普,等. VEGF和TGF-β1促进非血管化骨移植同期种植骨结合的实验研究[J]. 实用口腔医学杂志,2011,27(1): 12-16.[32] Hajishengallis G, Wang M, Liang S. Induction of distinct TLR2- mediated proinflammatory and proadhesive signalingpathways in response to Porphyromonas gingivalis fimbriae. J Immunol.2009;182(1): 6690- 6696. [33] 陈波,谢西梅,李佳霖,等.艾灸治疗对兔 KOA 软骨损伤及 TNF- α、TGF- β1和IGF- 1 表达调节作用的实验研究[J].江苏中医药,2009,41(6):69-71.[34] 蒋滔,程祥荣,夏海滨,等. rhBMP-2/rhTGF-β1联合应用对兔成骨样细胞增殖及分化的影响[J].口腔颌面修复学杂志,2005,6(1): 1-3.[35] 袁百胜,陈晓亮,栾军伟. 转化生长因子β1基因29T >C单核苷酸多态性与脊柱融合的相关性[J].中国组织工程研究与临床康复,2009,13(24):4686-4689.[36] 马进峰,周东生,马学晓,等. TGF-β1基因29T>C单核苷酸多态性与骨肉瘤的关联研究[J]. 中国矫形外科杂志,2010,18(18): 1510-1513.[37] 曲攀,高秀秋. 2型糖尿病伴牙周病大鼠牙槽骨中转化生长因子β1 mRNA的表达[J]. 中国组织工程研究与临床康复,2010, 14(46):8576-8580.[38] Yang X, Chen L, Xu X,et al.TGF-beta/Smad3 signals repress chondrocyte hypertro-phic differentiation and are required for maintaining ar-ticular cartilage. J Cell Biol.2001;153(1): 35-46.[39] Andrew WT.Review of the actvation of TGF-β1 in immunity. LeukoeBiol.2009;85:29-33.[40] Yang X,Chen L,Xu X, ,et al.TGF-beta/ Smad3 signalsrepress chondrocyte hypertrophic differentiation and are required for maintaining articular cartilage.J Cell Biol.2001;153(1):35-46.[41] Blaney Davidson EN,Scharstuhl A,Vitters EL,et al.Reduced transforming growth factor—beta signaling in cartilage of old mice:role in impaired repair capacity.Arthritis ResTher. 2005; 7(6): R1338 -1347.[42] 万晓晨,刘翠平,陈海啸,等.TGF-β/骨形态发生蛋白、Wnt 和 MAPK 信号通路在间充质干细胞向成骨细胞分化中的作用[J]. 细胞生物学杂志,2010,30:697-700.[43] 阎新龙,刘兵,毛宁.间充质干细胞迁移特性的研究进展.[J].中国实验血液学杂志2009,17(4):1101-1105.[44] 武鹏宇,戴立里,唐静,等. 骨形态发生蛋白-7对人肝星状细胞转化生长因子β信号转导的影响[J].第三军医大学学报,2010, 32(13): 1433-1437.[45] 孙啸.骨关节炎进程中软骨细胞膜受体 ALK1在软骨 TGFβ 信号通路中的作用及调控[J]. 中国骨与关节外科,2012,5(1): 88-92.[46] 杨晓. Smad4 介导转化生长因子β 信号调节骨骼发育和稳态维持的功能[J]. 生命科学,2008,20(2):165-169.[47] KaleVP. Differential activation of MAPK signaling pathways by TGF-beta1 forms the molecular mechanism behind its dose-dependent bidirectional effects on hematopoiesis. Stem Cells and Development .2004;13(l):27-38.[48] Janssens,tenDijkeP,JanssensS,et al.Transforming growth faetor-betal to the bone.EndocrReV.2005;26(6):743-774.[49] Quinn JM, Itoh K, Udagawa N,et al.Transforminggrowth factor b affects osteoclast differentiation via direct and indirect actions.Bone Miner Res.2001; 10:1787-1794.[50] 周名亮,李谧,余希杰. 微小RNA对成骨细胞分化成熟的调控及临床意义[J]. 中国修复重建外科杂志,2012,26(6):761-765.[51] Miyaki S, Nakasa T, Otsuki S, et al. MicroRNA-140 is expressed in dif-ferentiated human articular chondrocytes and modulates interleukin-1responses. Arthritis Rheum, 2009, 60(9): 2723-2730.[52] 苏金梅,金晔,曲强,等. 骨髓间充质干细胞向软骨细胞分化过程中miR130a的表达[J]. 基础医学与床,2010,30(5):520-523.[53] Miyaki S, Sato T, Inoue A, et al. MicroRNA-140 plays dual roles inboth cartilage development and homeostasis. Genes Dev, 2010, 24(11):1173-1185[54] 张秀梅,崔亚洲,周小艳,等. microRNAs 参与韧带成纤维细胞成骨分化相关分子表达的调节[J]. 中国生物化学与分子生物学报,2011,27(6):540-547 |
| [1] | Xie Chongxin, Zhang Lei. Comparison of knee degeneration after anterior cruciate ligament reconstruction with or without remnant preservation [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 735-740. |
| [2] | Deng Zhenhan, Huang Yong, Xiao Lulu, Chen Yulin, Zhu Weimin, Lu Wei, Wang Daping. Role and application of bone morphogenetic proteins in articular cartilage regeneration [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 798-806. |
| [3] | Ma Zetao, Zeng Hui, Wang Deli, Weng Jian, Feng Song. MicroRNA-138-5p regulates chondrocyte proliferation and autophagy [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 674-678. |
| [4] | Xie Chengxin, Wang Wei, Wang Chenglong, Li Qinglong, Yin Dong. Systematic review and meta-analysis of bone morphogenetic protein for the treatment of acute tibial fracture [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 486-492. |
| [5] | Zhou Wu, Wang Binping, Wang Yawen, Cheng Yanan, Huang Xieshan. Transforming growth factor beta combined with bone morphogenetic protein-2 induces the proliferation and differentiation of mouse MC3T3-E1 cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(23): 3630-3635. |
| [6] | Yang Caihui, Liu Qicheng, Dong Ming, Wang Lina, Zuo Meina, Lu Ying, Niu Weidong. Serine/threonine protein kinases can promote bone destruction in mouse models of chronic periapical periodontitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(23): 3654-3659. |
| [7] | Tian Guangzhao, Yang Zhen, Zha Kangkang, Sun Zhiqiang, Li Xu, Sui Xiang, Huang Jingxiang, Guo Quanyi, Liu Shuyun. Regulatory effect of decellularized cartilage matrix on macrophage polarization [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3545-3550. |
| [8] | Huo Hua, Cheng Yuting, Zhou Qian, Qi Yuhan, Wu Chao, Shi Qianhui, Yang Tongjing, Liao Jian, Hong Wei. Effects of drug coating on implant surface on the osseointegration [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3558-3564. |
| [9] | Jiang Shengyuan, Li Dan, Jiang Jianhao, Shang-you Yang, Yang Shuye. Biological response of Co2+ to preosteoblasts during aseptic loosening of the prosthesis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(21): 3292-3299. |
| [10] | Tong Jie, Liao Ying, Chen Zhengyu, Sun Guanghua . Osteoarthritic chondrocyte autophagy and regulation of mitogen-activated protein kinase signaling pathway [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(20): 3246-3251. |
| [11] | Wei Qin, Zhang Xue, Ma Lei, Li Zhiqiang, Shou Xi, Duan Mingjun, Wu Shuo, Jia Qiyu, Ma Chuang. Platelet-derived growth factor-BB induces the differentiation of rat bone marrow mesenchymal stem cells into osteoblasts [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(19): 2953-2957. |
| [12] | Guo Zhibin, Wu Chunfang, Liu Zihong, Zhang Yuying, Chi Bojing, Wang Bao, Ma Chao, Zhang Guobin, Tian Faming. Simvastatin stimulates osteogenic differentiation of bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(19): 2963-2968. |
| [13] | Li Xiangze, Bu Xianmin, Li Dongmei, Chi Yulei, Su Qiang, Jin Xintong, Zhao Jian, Zhang Gaotian, Wu Bin, Meng Chunyang . Stem cells, cytokines, hormones, neuropeptides and genes in traumatic brain trauma to promote fracture healing [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(19): 3057-3063. |
| [14] | Wang Liu, Song Dongzhe, Huang Dingming. Bone morphogenetic protein 9 regulates stem cell differentiation and bone regeneration [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(19): 3064-3070. |
| [15] | Liu Yunyi, Wang Bo, Wang Lin. Effects of post-exercise gastrocnemius needling on Achilles tendon degeneration in obese rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(14): 2211-2218. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||