Chinese Journal of Tissue Engineering Research ›› 2022, Vol. 26 ›› Issue (12): 1950-1955.doi: 10.12307/2022.522
Previous Articles Next Articles
Role of TRPV5 and TRPV6 calcium channels in bone metabolism
Li Chao1, Zhang Xian2, Shao Jiahao1
- 1Nanjing University of Chinese Medicine, Nanjing 210023, Jiangsu Province, China; 2Affiliated Wuxi Hospital of Nanjing University of Chinese Medicine, Wuxi 214071, Jiangsu Province, China
-
Received:2021-07-06Revised:2021-07-08Accepted:2021-08-21Online:2022-04-28Published:2021-12-15 -
Contact:Zhang Xian, Chief physician, Master’s supervisor, Affiliated Wuxi Hospital of Nanjing University of Chinese Medicine, Wuxi 214071, Jiangsu Province, China -
About author:Li Chao, Master candidate, Nanjing University of Chinese Medicine, Nanjing 210023, Jiangsu Province, China -
Supported by:the Major Scientific Research Project of Wuxi Municipal Health Commission, No. Z202020 (to ZX); Natural Science Foundation of Nanjing University of Chinese Medicine, No. XZR2020081 (to ZX)
CLC Number:
Cite this article
Li Chao, Zhang Xian, Shao Jiahao. Role of TRPV5 and TRPV6 calcium channels in bone metabolism[J]. Chinese Journal of Tissue Engineering Research, 2022, 26(12): 1950-1955.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
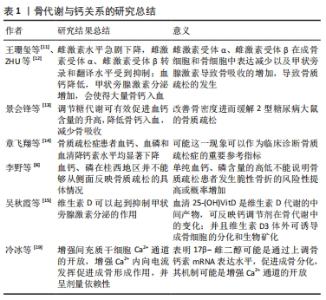
骨代谢贯穿骨质疏松发生发展的全过程,主要包含骨形成、吸收、破坏等因素,Ca2+在细胞内外的转运与这些骨代谢过程密切关系[9]。骨代谢活动维持正常状态的基础是成骨细胞发生的骨形成与破骨细胞发生的骨吸收两者之间保持动态平衡,成骨细胞是骨形成发育过程中最重要的功能细胞,并且一定程度上也调控破骨细胞,因此血钙、磷与骨钙、磷同时也需要保持一定程度的动态平衡[10]。体现骨形成与骨吸收过程的特征性生化指标即为骨代谢指标。雌激素是骨代谢的一个重要调节因素,这主要是由雌激素受体α、β(ERα、ERβ)通过与不同的配体结合产生生物学效应,雌激素水平急剧下降或缺乏导致骨密度降低、机械负荷增加,最终导致骨质疏松的发生[11-12]。血清钙和磷的含量可间接反映骨代谢情况,血钙降低,甲状旁腺激素分泌增加,会使得大量骨钙入血,引发骨质疏松。有研究发现,调节糖代谢可有效提高血钙含量,改善骨密度进而缓解2型糖尿病大鼠的骨质疏松[13]。章飞翔等[14]发现骨质疏松症患者血钙、血磷和血清降钙素水平均显著下降,认为这一现象可以作为临床诊断骨质疏松症的重要参考指标。但李野等[6]在探讨桂西地区骨质疏松患者FRAX评分与体质量指数及外周血中钙、磷指标的相关性中发现,外周血的钙、磷水平与骨折风险概率和体质量指数之间也无显著相关性(P > 0.05),血钙、磷在桂西地区并不能够从侧面反映骨质疏松的具体情况,单纯血中钙、磷含量的高低不能说明骨质疏松患者发生脆性骨折的风险性提高或概率增加。 在人体新陈代谢中维生素D扮演着十分重要的角色,与甲状旁腺激素(PTH)同为人体重要的钙调节激素,维生素D可以起到抑制甲状旁腺激素分泌的作用,以达到促进骨组织矿化的目的,血清25-(OH)VitD是维生素D代谢的中间产物,可反映钙调节剂在骨代谢中的变化[15]。维生素D在血浆中钙、磷的水平维持在正常范围内时,其对于骨骼的生长促进或者矿化的形成并没有直接作用,但是当人体肠道中钙的吸收不足以维持正常条件下血液中血钙的平衡,此时骨吸收的过程和肾脏的重吸收对于血中钙和磷的平衡稳态将发挥更大的作用。这使得血浆中1α,25-(OH)D3和甲状旁腺激素水平得到显著升高,维生素D在骨骼作用中则表现为刺激骨吸收、抑制骨矿化、维持血钙水平,但同时破坏了骨骼的完整性[16]。这显得与目前认为维生素D可以抑制骨吸收相矛盾,研究者认为维生素D虽然是作用于破骨细胞,但是很大程度上是通过成骨细胞发挥作用的,并且药物浓度的1α,25-(OH)D3可通过多种途径调控成骨细胞的成骨作用,并且维生素D3在体外可诱导成骨细胞的分化和生物矿化[17-18]。但是无论钙调节激素是如何影响Ca2+的吸收与排泄,其中都离不开离子通道的影响,离子通道活动是细胞电活动的基础。冷冰等[19]观察17β-雌二醇(17β-E2)对大鼠骨髓间充质干细胞成骨分化过程中Ca2+通道的影响,发现通过增强间充质干细胞Ca2+通道的开放,增强Ca2+内向电流发挥促进成骨形成作用,并呈剂量依赖性[19]。 骨代谢与钙关系研究总结,见表1。"
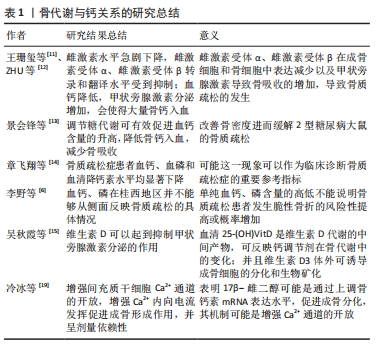
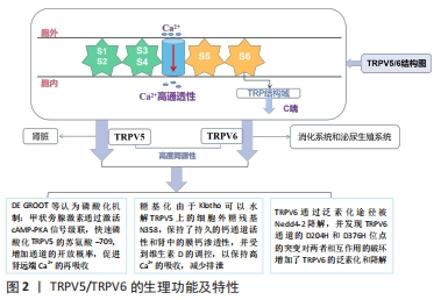
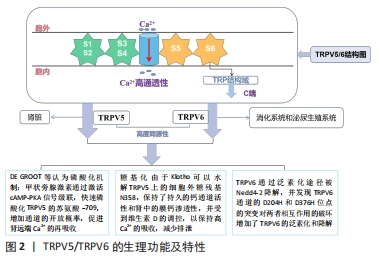
细胞质游离钙浓度(Ca2+)的调节是维持不同细胞类型(包括淋巴细胞)中细胞稳态的关键因素[20]。TRP离子通道广泛分布在人体的各种系统和组织中,其本质是一类阳离子通道,属于非选择性离子通道范畴,能够在较多的信号通路中发挥自身的作用,主要原因是可以参与多种修饰后感知细胞内、外的多种刺激。TRP通道对于大部分Ca2+的渗透性较差,相对于Na+(PCa/PNa)来讲,Ca2+选择性较差,对比范围在0.3-10。但是TRPV5和TRPV6通道是例外,它们是PCa/PNa > 100的两个最高Ca2+选择性TRP通道,在TRP通道中对于Ca2+具有较强的主导和重吸收的作用[21]。因此对于Ca2+通道的分布表达及生理功能的论述更有助于理解并进一步研究发现该通道和骨质疏松间的联系。 2.2.1 TRPV5/TRPV6通道分布表达 TRP家族中,TRPV5和TRPV6形成了最独特的Ca2+选择性通道成员,TRPV5主要分布在肾脏的远曲小管和连接小管中,TRPV6在人体中的分布较TRPV5更为广泛,多存在于人体消化系统和泌尿生殖系统,如胃、肠道、胰腺、前列腺、子宫以及胎盘当中[22-23]。TRPV5和TRPV6在肠道和肾上皮细胞中共同表达,所以又被称为上皮钙离子通道,并能够形成异四聚体通道。TRPV家族中在肾上皮细胞和肠上皮中的主要亚型分别为TRPV5、TRPV6,值得注意的是,TRPV5的表达仅限于肾脏,而TRPV6的表达更为广泛[24]。 研究表明,TRPV5主要特征是一个组成性活性通道,在生理膜电位处具有实质性的Ca2+渗透性[22]。TRPV5表现出由4个天冬氨酸残基(D542)的环组成的选择性过滤序列,形成主细胞外Ca2+结合袋,对许多通道特性至关重要,包括高Ca2+渗透率、镁(Mg2+)阻断和依赖于Ca2+的电流衰变。TRPV5和TRPV6是钙稳态所必需的一种独特的钙选择性TRP通道,与其他TRPV通道不同,TRPV5及其紧密同源物TRPV6不表现出热敏感性或配体依赖的激活,在生理膜电位上呈成倍开放,并由钙调素(CaM)以钙依赖的方式调节[25]。钙转运的过程本质上可认为是一种在肠和肾上皮屏障上的细胞旁被动转运与跨细胞主动转运两种形式,其后者是一个调节的过程,包括3个步骤;顶端钙通过TRPV5或TRPV6进入上皮细胞,钙通过钙结合蛋白-D9k和钙结合蛋白-D28K直接结合,并通过质膜钙ATP酶(PMCA1和PMCA4)和钠钙交换亚型1(NCX1)挤压[26]。因此高选择性离子通道TRPV5和TRPV6参与上皮钙离子转运过程,对维持人类钙稳态做出显著贡献[27]。这是一个重要的过程,因为钙稳态紊乱会导致许多的健康问题,包括结石形成、骨骼紊乱、血栓形成和心电图异常等[28]。上皮钙转运被严格调节,以确保肠道钙吸收、骨骼动态储存和尿排泄的联合过程使血清钙水平维持在狭窄范围内(2.2-2.5 mmol/L)。 2.2.2 TRPV5/TRPV6的生理功能 TRPV5/TRPV6的结构与生理特性:随着科技进步,蛋白质解析技术取得了发展,与所有TRP通道相似,TRPV5和TRPV6通过单个亚基的四聚化形成功能通道[29]。该通道呈三叶草状,具有跨膜茎和四个花瓣,紧密连接并面向细胞质向下形成细胞内结构域,即6个α螺旋组成跨脂质双层的跨膜结构域(S1-S6)、胞内的N末端(N terminal domain,NTD)和C末端(C terminal domain,CTD)构成,在C端紧邻S6跨膜区包含一段α螺旋(25个残基组成),称为TRP结构域(TRP domain),与离子通道门控相关[8]。与所有的TRP通道一样,TRPV5和TRPV6通过对单个亚基的四聚化形成功能通道,S5和S6跨膜之间的循环区域向内和向下面对,被称为孔形成环。通道的离子选择性主要吸引阳离子进入通道孔中,其主要的原因为孔形成环的细胞外结构域控制离子的进出。人们认为羧基末端区域固定在通道的内部,附着在细胞质中,这种方向允许翻译后的修饰和蛋白质的结合[26]。TRPV5和TRPV6中具有高度的序列同源性,TRPV5和TRPV6离子通道的独特特征之一是它们具有高钙选择性的电导率,当调整选择性过滤器序列时,可以发现TRPV5和TRPV6与其他序列不同(TRPV1-4中的T-V/I-I-D与TRPV5/TRPV6中的G-M/L-G-D/E)。NILIUS等[30]已经表明,通过将TRPV5(D542A)和541位置的天冬氨酸替换成丙氨酸,可以消除TRPV5和TRPV6的独特钙选择性,研究者还观察到钙渗透的整体减少。 TRP离子通道本身具有一些独特的功能,并且在修饰后同样可以放大或者改变某些功能。TRPV5介导Ca2+跨细胞膜转运,分布在肾脏,可以调控尿钙水平,肾的远曲小管和集合管是钙的重吸收和Ca2+调节激素作用部位,研究表明,TRPV5基因敲除的小鼠其尿钙排泄量比正常组小鼠高6倍[31]。肠胃对Ca2+的摄取主要是由TRPV6所控制,胃肠道中TRPV6 蛋白的减少会导致骨密度的降低,生育能力随之下降并引发低钙血症[32]。此外,TRPV6在人体许多系统的肿瘤形成发展、增殖、组织间的迁移中同样发挥较大的作用,食管癌、胃癌、结直肠癌、肝癌、胰腺癌与其都具有较高的联系,如胰腺癌患者的生存期预后不佳与TRPV6通道蛋白水平升高联系紧密,并且在大肠癌与恶性细胞增殖机制研究中,TRPV6蛋白的过表达已经取得研究人员的认可[33]。 TRPV5/TRPV6的生理功能:TRP通道能够被理化刺激因素所激活,被称为多觉感受器(polymodal receptors)。TOMILIN等[34]认为,TRPV5/TRPV6的活性对pH值很敏感,体外实验研究发现,细胞内和细胞外pH值直接调节TRPV5/TRPV6的活性,细胞外酸性pH值降低了TRPV5/TRPV6通道的活性,而碱性pH值增加了细胞中TRPV5/TRPV6通道的活性。雌激素的抑制剂他莫昔芬能够降低TRPV6表达,从而抑制Ca2+的转运,这说明TRPV5/TRPV6亦受雌激素的调控[35]。 蛋白质的翻译修饰会贯穿其整个“生命周期”,这个过程是在各种信号通路激活后诱导该蛋白的某个或某几个氨基酸侧链与功能性化学基团进行共价结合,能够在调节蛋白的活性、稳定性、定位、相互作用或折叠中起到作用[36]。TRPV5/TRPV6的翻译修饰主要发生在磷酸化、糖基化和泛素化的几个层面,从而调控通道的表达量和活性。DE GROOT等[37]认为位于甲状旁腺中的Ca2+感受体检测到Ca2+稳态中的轻微扰动,释放甲状旁腺激素到血液循环中,甲状旁腺激素在肾脏中通过刺激肾远端小管对Ca2+的再吸收来减少Ca2+的排泄,具体的机制为甲状旁腺激素通过激活cAMP-PKA信号级联,快速磷酸化TRPV5的苏氨酸-709,增加通道的开放概率,促进肾远端Ca2+的再吸收,这个磷酸化机制中会改变一个固定数量的TRPV5通道的单通道活性,而不会对肠道吸收Ca2+产生影响。蛋白质的N-糖基化从酵母到人类高度保守,对蛋白质结构有稳定作用,Klotho是一种β-葡萄糖醛酸酶,当两者共同定位在肾远曲小管时,Klotho可以水解TRPV5上的细胞外糖残基N358,将该通道包裹在质膜中,这有助于保持持久的钙通道活性和肾中的膜钙渗透性,但两者都会受到维生素D的调控,以保持高Ca2+的吸收,减少排泄,此外在TRPV6通道中N358的同源位点N357也受到Klotho调控的N-糖基化修饰调控[38-39]。 骨量减少是炎性肠道疾病的主要肠外症状之一,研究表明炎症性细胞因子肿瘤坏死因子(TNF)、干扰素(IFN)γ等可降低Klotho的活性,进而降低细胞表面TRPV5水平,加速降解,这是因为TRPV5的泛素化修饰水平提高,使得Ca2+内吞,而不能被肾小管重吸收,而通过敲除UBR4(一种E3泛素连接酶)可以阻止细胞瘤诱导的TRPV5的降解[40]。Nedd4-2是泛素化E3连接酶家族的成员之一,其可以通过向膜蛋白添加泛素链来调节细胞表面的稳定,然后是内吞作用和溶酶体或蛋白酶体降解,TRPV6和Nedd4-2在肠道中共同表达,TRPV6通过泛素化途径被Nedd4-2降解,并发现TRPV6通道的D204H和D376H位点的突变对两者相互作用的破坏增加了TRPV6的泛素化和降解[41]。 TRPV5/TRPV6的生理功能及特性,见图2。"
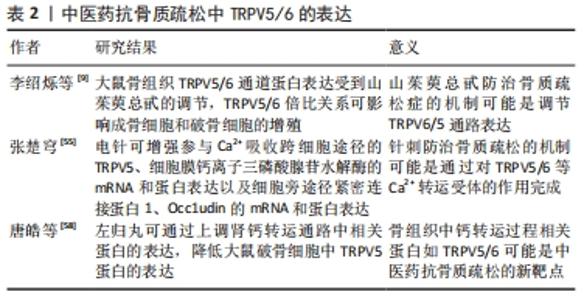
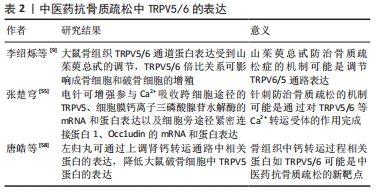
2.3 Ca2+离子通道TRPV5/TRPV6与骨代谢 Ca2+是骨组织的重要组成部分,钙相关调节因子可以通过钙浓度的改变在骨形成和骨吸收中发挥作用,而骨代谢的过程较大程度上就是Ca2+的代谢过程,TRPV5/TRPV6是跨细胞Ca2+转运的重要通道,因此上皮Ca2+通道与骨代谢之间存在着密切关系。通过调节高选择性Ca2+通道TRPV5/TRPV6的通道状态,进而影响成骨细胞、破骨细胞的增殖分化,起到改善骨代谢现状,这可能是调节破骨细胞、成骨细胞生物学功能新兴靶点[42]。 TRPV5在人类和鼠类的骨标本化及培养的破骨细胞中显著表达,存在于破骨细胞的褶皱区,提示RRPV5在破骨细胞骨吸收活动中可能有着重要功能[43]。在骨代谢中破骨细胞的分化离不开核因子κB受体激活蛋白配体(receptor activator of nuclear factor kappa B ligand,RANKL)激活转录因子活化T细胞核因子c1 (nuclear factor of activated T cell c1,NFATc1),RANKL可以使得胞内发生Ca2+震荡,这会有效降低NFATc 1激活所要达到的Ca2+阈值,因此NFATc1更加容易被激活,同时Ca2+信号靶向作用于钙调磷酸酶(Calcineurin)和激活NFATc1,诱导破骨细胞前体分化,改变细胞骨架结构影响破骨细胞的骨吸收能力,因此Ca2+通道TRPV5是介导RANKL诱导人破骨细胞胞浆Ca2+浓度升高的主要原因[44-45]。VAN DER EERDEN等[46]研究发现缺失TRPV5蛋白小鼠外周血的单核细胞中分离诱导出较多的并且更大的破骨细胞,但是其细胞的骨吸收能力却受损,因此破骨细胞的骨吸收过程一定需要TRPV5的参与,并且TRPV6目前只在成骨细胞中发现存在,而未发现TRPV5的存在。Ca2+在肾脏中重吸收过程与在肠道中类似,Ca2+在肾脏远端小管通过TRPV5细胞离子跨膜运输过程进入细胞,进而在胞浆中与CaPB28k结合之后进行输送,通过钠钙交换器(NCX1)和浆膜钙泵(PMCA1b)离开细胞进入血液循环[47]。并且肾脏中的TRPV5表达水平受1α, 25-(OH)2D3调控,如果食物中缺乏1α,25-(OH)2D3,那么肾脏中TRPV5表达水平则会显著降低;反之,肾脏中的TRPV5表达水平明显升高,维生素D作用肾脏下的关键蛋白在TRPV5在肾远端小管中发挥着转运钙离子的重要作用[48]。研究显示TRPV5基因敲除小鼠出现骨小梁、骨皮质厚度降低,同时体外研究也证实TRPV5剔除小鼠单位面积破骨细胞数量及细胞核数量显著升高[49]。 研究表明,糖皮质激素可抑制TRPV6在小肠中的表达,降低肠上皮细胞对于Ca2+的吸收,进而诱导骨质疏松的发生[50]。 此外,TRPV6缺陷小鼠会出现肠道Ca2+吸收障碍、小鼠的体质量下降、骨密度降低等问题的发生,但是TRPV的表达量在男性与年龄无关,而在女性TRPV6的表达量则与年龄有关,这可能与女性绝经后雌激素分泌量减少有关[51-52]。在破骨细胞分化增殖的过程中,巨噬细胞集落刺激因子(M-CSF)和RANKL基本上贯穿破骨细胞形成全过程,PI3K-AKT和MAPK-ERK两个级联反应途径由胰岛素样生长因子(IGF)信号通路转导激活参与骨代谢,胰岛素样生长因子1受体(IGF1R)可参与调控破骨细胞前体细胞的分化能力。研究表明,正常浓度的Ca2+培养液中,TRPV5/TRPV6抑制NaR细胞(Na+-K+-ATP酶丰富细胞)内的IGF1R-PI3K-AKT信号通路,对于NaR细胞的增殖是一种负向调控,而当TRPV5/TRPV6通道的失活或其表达受到抑制时,IGF1R-PI3K-AKT的活性则被激活,会促进NaR细胞的增 殖[53]。马骏[54]研究发现,TRPV6基因敲除小鼠可发生骨质疏松,原因应该是是TRPV6缺乏可导致其骨吸收功能异常,但骨形成功能没有受到显著影响,并且发现破骨细胞随着分化成熟,分布在破骨细胞细胞膜上的破骨细胞重要的调节因子TRPV6表达量会越来越低,非Ca2+振荡/CaN依赖性通路介导TRPV6对破骨细胞形成、骨吸收的负向调控,TRPV6负向调控破骨细胞形成和骨吸收是通过抑制IGF1R-PI3K-AKT信号通路实现的[54]。综上所述,TRPV5/TRPV6可影响体内Ca2+的吸收,参与人体的骨代谢。 2.4 中医药抗骨质疏松与Ca2+通道TRPV5/TRPV6 骨质疏松属于祖国医学中的“骨痿”“骨枯”“痿证”等范畴,中医学认识下的病理机制为“肾藏精,精生髓,髓充骨”与“肾不藏精,不能养骨,使得骨枯髓减”。而中医药在补肾壮骨的治疗方式上具有自身的优势,通过适当的中医药治疗方式,增加体内肠道或者肾脏TRPV5/TRPV6的表达或TRPV5/TRPV6通道开放量增加,进一步提高TRPV5/TRPV6的活性,以达到抑制破骨细胞的骨吸收,促进成骨细胞的骨形成,最终发挥防治骨质疏松的作用。有学者利用补肾壮骨经典中药山茱萸的提取物山茱萸总甙来防治骨质疏松的发生,得出结果发现大鼠骨组织TRPV5/TRPV6通道蛋白表达受到山茱萸总甙的调节,并且改变TRPV5/TRPV6倍比关系可影响成骨细胞和破骨细胞的增殖,起到促成骨方向的骨代谢转变以及提高骨密度[9]。骨质疏松的防治中针刺治疗也可发挥一定的作用,研究者观察针刺在对去卵巢大鼠骨密度及Ca2+转运相关受体的影响中,发现电针能提高去卵巢大鼠的骨密度,增强参与Ca2+吸收跨细胞途径的TRPV5、细胞膜Ca2+三磷酸腺苷水解酶(PMCA1b)的mRNA和蛋白表达以及细胞旁途径紧密连接蛋白1(ZO-1)、Occ1udin的mRNA和蛋白表达[55]。针对骨质疏松的发病原因探讨糖皮质激素性骨质疏松症的发病机制中,有研究者比较补肾、健脾、活血中药的疗效,认为补肾中药通过下调骨组织TRPV5 mRNA与蛋白表达而抑制破骨细胞骨吸收,达到抗骨质疏松的作用,并且疗效优于健脾与活血中药[56]。关于中药对于成骨细胞的研究,MC3T3-E1细胞形态及其增殖活性不受到补肾活血固齿方的干预,补肾固齿方可呈时间依赖性增加MC3T3-E1细胞的碱性磷酸酶活性,研究结果认为补肾活血固齿方促进成骨细胞的增殖分化,上调骨形态发生蛋白2 mRNA的表达通过Ca2+通道TRPV6发挥功能[57]。唐皓等[58]研究发现左归丸可通过上调肾钙转运通路中相关蛋白的表达,达到降低大鼠破骨细胞中TRPV5蛋白的表达,进而发挥抗骨质疏松的作用。因此综上所述,骨组织中钙转运过程相关蛋白如TRPV5/TRPV6可能是中医药抗骨质疏松的新靶点,见表2。"
| [1] FORCIEA MA, MCLEAN RM, QASEEM A. Treatment of Low Bone Density or Osteoporosis to Prevent Fractures in Men and Women: A Clinical Practice Guideline Update From the American College of Physicians. Ann Int Med. 2017;167(12):899. [2] KANIS JA, COOPER C, RIZZOLI R, et al. European guidance for the diagnosis and management of osteoporosis in postmenopausal women. Osteoporos Int. 2019;30(1):3-44. [3] 中华中医药学会.绝经后骨质疏松症(骨痿)中医药诊疗指南(2019年版)[J].中医正骨,2020,32(2):1-13. [4] 中国中西医结合学会骨伤科专业委员会 .骨质疏松症中西医结合诊疗指南[J].中华医学杂志,2019(45):3524-3525-3526-3527-3528-3529-3530-3531-3532-3533. [5] 李福春,马学玲,屈艳萍,等.骨髓间充质干细胞成骨分化过程中瞬时性受体电位香草精受体5的表达[J].中国组织工程研究,2012,16(45): 8361-8366. [6] 李野,董书君,宋成超,等.桂西地区骨质疏松患者FRAX评分与体质量指数及外周血中钙、磷指标的相关性分析[J].中国骨质疏松杂志, 2021,27(1):123-126. [7] YUAN P. Structural biology of thermoTRPV channels. Cell Calcium. 2019; 84:102106 [8] 杨冰洁,田泉,魏鑫,等.翻译后修饰调控TRPV亚家族通道功能的研究进展[J].生物化学与生物物理进展,2021,48(02):171-183. [9] 李绍烁,赵京涛,何昌强,等.山茱萸总甙干预骨质疏松模型大鼠骨代谢:TRPV6、TRPV5通路的变化[J].中国组织工程研究,2019,23(11): 1749-1754. [10] 赖鸿辉,刘跃,李体远,等.外源性硫化氢对双侧卵巢摘除骨质疏松模型大鼠骨代谢的影响[J].中国组织工程研究,2021,25(29): 4632-4637. [11] 王珊玺,谢菊英,谢兴,等.ERα基因过表达对去卵巢骨质疏松小鼠骨密度及钙磷代谢的影响[J/OL].中国应用生理学杂志:1-5[2021-04-26] https://kns.cnki.net/kcms/detail/detail.aspx?dbcode= CAPJ&dbname [12] ZHU H, JIANG J, WANG Q, et al. Associations between ERα/β gene polymorphisms and osteoporosis susceptibility and bone mineral density in postmenopausal women: a systematic review and meta-analysis. BMC Endocr Disord. 2018;18(1):11. [13] 景会锋,王小梅.有氧运动联合褪黑素对Ⅱ型糖尿病 大鼠骨质疏松的影响[J].中国应用生理学杂志,2017,33(3):252-256. [14] 章飞翔,崔海东,吕书军.骨代谢标志物和降钙素在高龄男性骨质疏松症中的诊断价值[J].中国实验诊断学,2020,24(12):1989-1990. [15] 吴秋霞,屈云鹤,徐振华.N-MID、25-(OH)VitD、血清Ca~(2+)与绝经期OP所致髋骨骨折患者骨密度及骨折的关系[J].实验与检验医学,2020, 38(3):478-479+484. [16] 陈阳. TRPV5在维生素D调控破骨细胞分化和骨吸收中的作用[D].扬州:扬州大学,2016. [17] HAUSSLER MR, WHITFIELD GK, KANEKO I, et al. The role of vitamin D in the FGF23, klotho, and phosphate bone-kidney endocrine axis. Rev Endocr Metab Disord. 2012;13(1):57-69. [18] 汪东,杨媛,张峥,等.维生素D_3及其代谢物对成骨细胞分化及生物矿化的实验研究[J].中国骨质疏松杂志,2021,27(3):341-347. [19] 冷冰,王大麟,郑淑云,等.17β-雌二醇对大鼠骨髓间充质干细胞成骨分化过程中Ca~(2+)通道的作用[J].吉林大学学报(医学版),2019, 45(5):1041-1045+1195. [20] TOMILIN VN, CHEREZOVA AL, NEGULYAEV YA, et al. TRPV5/V6 Channels Mediate Ca(2+) Influx in Jurkat T Cells Under the Control of Extracellular pH. J Cell Biochem. 2016;117(1):197-206. [21] DEN DEKKER E, HOENDEROP JG, NILIUS B, et al. The epithelial calcium channels, TRPV5 & TRPV6: from identification towards regulation. Cell Calcium. 2003;33(5-6):497-507. [22] VAN DER WIJST J, LEUNISSEN EH, BLANCHARD MG, et al. A Gate Hinge Controls the Epithelial Calcium Channel TRPV5. Sci Rep. 2017;7:45489. [23] FECHER-TROST C, WISSENBACH U, WEISSGERBER P. TRPV6: from identification to function. Cell Calcium. 2017;67:116-122. [24] NIJENHUIS T, HOENDEROP JG, BINDELS RJ. TRPV5 and TRPV6 in Ca(2+) (re)absorption: regulating Ca(2+) entry at the gate. Pflugers Arch. 2005; 451(1):181-192. [25] DANG S, VAN GOOR MK, ASARNOW D, et al. tructural insight into TRPV5 channel function and modulation. Proc Natl Acad Sci U S A. 2019;116(18): 8869-8878. [26] VAN GOOR MKC, HOENDEROP JGJ, VAN DER WIJST J. TRP channels in calcium homeostasis: from hormonal control to structure-function relationship of TRPV5 and TRPV6. Biochim Biophys Acta Mol Cell Res. 2017;1864(6):883-893. [27] RYAN LE, ING SW. Idiopathic hypercalciuria: Can we prevent stones and protect bones? Cleve Clin J Med. 2018;85(1):47-54. [28] REID IR, BIRSTOW SM, BOLLAND MJ. Calcium and Cardiovascular Disease. Endocrinol Metab (Seoul). 2017;32:339-349. [29] ROMERO-ROMERO S, GOMEZ LAGUNAS F, BALLEZA D. Side chain flexibility and coupling between the S4-S5 linker and the TRP domain in thermo-sensitive TRP channels: insights from protein modeling. Proteins. 2017;85(4):630-646. [30] NILIUS B, VENNEKENS R, PRENEN J, et al. The single pore residue Asp542 determines Ca2+ permeation and Mg2+ block of the epithelial Ca2+ channel. J Biol Chem. 2001;276(2):1020-1025. [31] 陈仲萍,林俊,王群,等.TRPV5信号通路调控尿钙重吸收机制的研究[J].中国当代医药,2018,25(25):8-10+15. [32] 崔军.过表达TRPV6基因对小鼠破骨细胞钙转运及凋亡相关基因表达的影响[D]. 南京:南京农业大学,2016. [33] 吕小斌,罗和生.TRP离子通道家族和消化系统肿瘤相关性研究[J].胃肠病学和肝病学杂志,2021,30(2):194-198. [34] TOMILIN VN, CHEREZOVA AL, NEGULYAEV YA, et al. TRPV5/V6 channels mediate Ca2+ influx in jurkat T cells under the control of extracellular pH. J Cell Biochem. 2016;117(1):197-206. [35] Song T, Lin T, Ma J, et al. Regulation of TRPV5 transcription and expression by E2/ERα signalling contributes to inhibition of osteoclastogenesis. J Cell Mol Med. 2018;22(10):4738-4750. [36] XU Y, WU W, HAN Q, et al. Post-translational modification control of RNA-binding protein hnRNPK function. Open Biology. 2019;9(3):180239. [37] DE GROOT T, LEE K, LANGESLAG M, et al. Parathyroid hormone activates TRPV5 via PKA-dependent phosphorylation. J Am Soc Nephrol. 2009;20(8):1693-1704. [38] CHANG Q, HOEFS S, VAN DER KEMP AW, et al. The betaglucuronidase klotho hydrolyzes and activates the TRPV5 channel. Science. 2005; 310(5747):490-493. [39] BOROS S, XI Q, DIMKE H, et al.Tissue transglutaminase inhibits the TRPV5-dependent calcium transport in an N-glycosylationdependent manner. Cell Mol Life Sci. 2012;69(6):981-992. [40] RADHAKRISHNAN VM, RAMALINGAM R, LARMONIER CB, et al Post-translational loss of renal TRPV5 calcium channel expression, Ca(2+) wasting, and bone loss in experimental colitis. Gastroenterology. 2013;145(3):613-624. [41] ZHANG W, NA T, WU G, et al. Down-regulation of Intestinal Apical Calcium Entry Channel TRPV6 by Ubiquitin E3 Ligase Nedd4-2. J Biol Chem. 2010; 285(47):36586-36596. [42] 郭清河,叶添文.TRPV5/TRPV6调节骨代谢作用的研究进展[J].中国矫形外科杂志,2011,19(23):1976-1978. [43] HOENDEROP JGJ, VRIES TJD, POLS HAP, et al. The epithelial Ca2+ channel TRPVS is essentialfor proper osteoclastic bone resorption [J]. Proc Natl Acad Sci USA. 2005;102(48):17507-17512. [44] 宋腾飞. 雌激素调控破骨细胞TRPV5表达的分子机制研究[D].上海:第二军医大学,2016. [45] CHAMOUX E, BISSON M, PAYET MD, et al. TRPV-5 mediates a receptor activator of NF-kappaB (RANK) ligand-induced increase in cytosolic Ca2+ in human osteoclasts and down-regulates bone resorption. J Biol Chem. 2010;285(33):25354-25362. [46] VAN DER EERDEN BC, HOENDEROP JG, DE VRIES TJ, et al. The epithelial Ca2+ channel TRPVS is essential for proper osteoclastic bone resorption. Proc Natl Acad Sci USA. 2005;102(48):17507-17512. [47] HOENDEROP JG,BINDELS RJ. Calciotropic and magnesiotropic TRP chan- nels. J Physiology(Bethesda). 2008;23:32-40. [48] KO SH, CHOI KC, OH GT, et al. Effect of dietary calcium and 1,25-( OH) 2D3 on the expression of calcium transport genes in calbindin -D9k and -D28k double knockout mice. J Biochem Biophys Res Commun. 2009;379:227-232. [49] VAN DER EERDEN BC, HOENDEROP JG, DE VRIES TJ, et al. The epithelial Ca2+ channel TRPVS is essential for proper osteoclastic bone resorption. Proc Natl Acad Sci U S A. 2005;102(48):17507-17512. [50] HUYBERS S, NABER TH, BINDELS RJ, et al. Prednisolone-induced Ca2+ malabsorption is caused by diminished expression of the epithelial Ca2+ channel TRPV6. Am J Physiol Gastrointest Liver Physiol. 2007;292(1): G92-G97. [51] BIANCO SD, PENG JB, TAKANAGA H, e tal. Marked disturbance of calcium homeostasis in mice with targeted disruption of the Trpv6 calcium channel gene. J Bone Miner Res. 2007;22(2):274-285. [52] WALTERS JR, BALESARIA S, CHAVELE KM, et al. Calcium channel TRPV6 expression inhuman duodenum: different relationships to the vitamin D system and aging in men and women. J Bone Miner Res. 2006;21(11):1770-1777. [53] DAI W, BAI Y, HEBDA L, et al. Calcium deficiency-induced and TRP channel-regulated IGF1R-PI3K-Akt signaling regulates abnormal epithelial cell proliferation. Cell Death Differ. 2014;21(4):568-581. [54] 马骏. 钙离子通道蛋白TRPV6对小鼠骨代谢和破骨细胞形成的调控作用及其机制研究[D].上海:中国人民解放军海军军医大学, 2019. [55] 张楚穹,石娜,欧阳钢.针刺对去卵巢大鼠骨密度及肠黏膜跨膜钙转运相关受体表达的影响[J].针刺研究,2020,45(9):702-707. [56] 朱辉,郑洪新,杨芳,等.补肾、健脾、活血中药对地塞米松诱导骨质疏松大鼠骨组织TRPV5表达的影响[J].中国实验方剂学杂志,2012, 18(6):166-169. [57] 穆春晖. 补肾活血固齿方对成骨细胞增殖、分化,BMP-2表达及TRPV5/TRPV6通道影响的实验研究[D].石家庄:河北医科大学,2014. [58] 唐皓,余娜,仇湘中,等.左归丸对去势大鼠钙转运通路相关蛋白的影响[J].湖南中医药大学学报,2019,39(10):1200-1204. |
| [1] | Jiang Huanchang, Zhang Zhaofei, Liang De, Jiang Xiaobing, Yang Xiaodong, Liu Zhixiang. Comparison of advantages between unilateral multidirectional curved and straight vertebroplasty in the treatment of thoracolumbar osteoporotic vertebral compression fracture [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1407-1411. |
| [2] | Zhu Chan, Han Xuke, Yao Chengjiao, Zhou Qian, Zhang Qiang, Chen Qiu. Human salivary components and osteoporosis/osteopenia [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1439-1444. |
| [3] | Li Wei, Zhu Hanmin, Wang Xin, Gao Xue, Cui Jing, Liu Yuxin, Huang Shuming. Effect of Zuogui Wan on bone morphogenetic protein 2 signaling pathway in ovariectomized osteoporosis mice [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1173-1179. |
| [4] | Xiao Hao, Liu Jing, Zhou Jun. Research progress of pulsed electromagnetic field in the treatment of postmenopausal osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1266-1271. |
| [5] | Gao Yujin, Peng Shuanglin, Ma Zhichao, Lu Shi, Cao Huayue, Wang Lang, Xiao Jingang. Osteogenic ability of adipose stem cells in diabetic osteoporosis mice [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 999-1004. |
| [6] | Peng Kun. Improvement of the treatment effect of osteoporotic fractures: research status and strategy analysis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 980-984. |
| [7] | Shen Song, Xu Bin. Diffuse distribution of bone cement in percutaneous vertebroplasty reduces the incidence of refracture of adjacent vertebral bodies [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 499-503. |
| [8] | Ou Liang, Kong Dezhong, Xu Daoqing, Ni Jing, Fu Xingqian, Huang Weichen. Comparative clinical efficacy of polymethyl methacrylate and self-solidifying calcium phosphate cement in vertebroplasty: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 649-656. |
| [9] | Cai Feng, Yu Bo, Zeng Duo, Chen Qincan, Liao Qi. Cortical bone trajectory in elderly patients with osteoporosis of lumbar disease [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(3): 403-407. |
| [10] | Zhong Yuanming, He Bingkun, Wu Zhuotan, Wu Sixian, Wan Tong, Zhong Xifeng. Meta-analysis of efficacy and safety of Jack kyphoplasty for osteoporotic vertebral compression fractures [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(3): 487-492. |
| [11] | Fan Danyang, Fu Runze, Mi Jiajing, Liu Chunyan. Expression and role of cannabinoid receptors during bone remodeling [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(2): 283-288. |
| [12] | Zeng Xinyu, Chen Xianghe, Liu Bo, Lu Pengcheng, Jin Shengjie, Li Wenxiu, Tian Zhikai, Sun Changliang. Mechanism of exercise improving bone metabolism in type 2 diabetics mellitus based on "Muscle-Bone" Crosstalk [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(2): 289-295. |
| [13] | Chen Yong, Sun Yang. Effect of zoledronic acid on femoral implant subsidence after hip arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(12): 1812-1815. |
| [14] | Tang Yeling, Liang Pengchen, Shi Junfeng, Sun Miaomiao, Zhou Ziyan, Zhu Lisha, Li Tian, Liang Dongyu, Sha Shuang, Yi Qingqing, Chang Qing. Exploring effective components of Guyuling capsule in the treatment of osteoporosis based on bioinformatics analysis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(12): 1899-1906. |
| [15] | Wang Dong, Ding Hai, Chang Wenju, Wang Jinzi. Biological changes and mechanism of salvianolic acid B in ovariectomized osteoporosis rat models [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(12): 1927-1930. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||



