Chinese Journal of Tissue Engineering Research ›› 2022, Vol. 26 ›› Issue (28): 4546-4552.doi: 10.12307/2022.312
Previous Articles Next Articles
Reducing the recurrence of infection after the application of Masquelet technique for osteomyelitis
Ci Wentao, Zhang Xinlong, Yan Shi, Wang Zhao
- Department of Traumatology and Orthopedics, Affiliated Hospital of Chengde Medical University, Chengde 067000, Hebei Province, China
-
Received:2021-02-22Accepted:2021-04-10Online:2022-10-08Published:2022-03-23 -
Contact:Yan Shi, Chief physician, Master’s supervisor, Department of Traumatology and Orthopedics, Affiliated Hospital of Chengde Medical University, Chengde 067000, Hebei Province, China -
About author:Ci Wentao, Master candidate, Department of Traumatology and Orthopedics, Affiliated Hospital of Chengde Medical University, Chengde 067000, Hebei Province, China
CLC Number:
Cite this article
Ci Wentao, Zhang Xinlong, Yan Shi, Wang Zhao. Reducing the recurrence of infection after the application of Masquelet technique for osteomyelitis[J]. Chinese Journal of Tissue Engineering Research, 2022, 26(28): 4546-4552.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
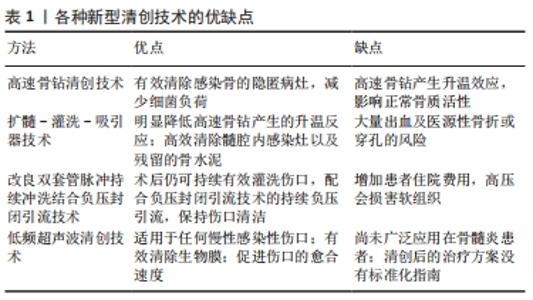
2.1 清创技术的改良 骨髓炎感染灶的彻底清创会极大降低术后感染复发的风险。在慢性骨髓炎病灶中,细菌会形成生物膜,该生物膜保护细菌不被宿主的免疫反应或抗生素所消灭,且病灶处通常伴有死骨的形成,只有清创才能有效地去除感染源,因此感染灶的有效清创是降低骨髓炎术后感染复发的关键环节。 2.1.1 清创范围 彻底、有效的清创有赖于感染部位和感染波及范围的准确判定。术前需要做好充分计划,X射线片有利于明确感染骨的大致范围;CT有助于死骨的判断;MRI能够较准确区分骨皮质与骨膜之间的炎症及髓腔内感染范围,较清晰地显示软组织感染范围;正电子发射断层成像对判断内固定相关感染的准确性更高;Cierny-Mader分型用以明确感染骨的浸润程度;骨髓炎发展时间可以判断生物膜的形成。清创的基础是确保切除所有宏观上失活的组织和生物膜,留下健康的出血组织,细菌以蜉蝣形式存在,残存细菌负荷低于感染阈值[8]。生物膜很难通过大体观察,这无疑增加了清创的难度,为了彻底清除生物膜常常需要扩大清创范围。扩大清创要求有顺序的清除,首先应该清除软组织,对于皮肤的切除范围,坚持扩大清除正常软组织2 mm,显露病灶后切除囊壁组织,也要求扩大切除2 mm正常软组织;软组织清创完毕后,彻底去除炎性肉芽组织、异物及死骨,最后再切除感染骨[9]。对于感染骨的清除,传统清创术认为A类患者切除病灶骨周围3-5 mm范围,B类患者切除5 mm以上范围。杨聪林等[10]扩大清创的经验是只要存在感染骨,松质骨的清创至少要距离病灶边缘0.5 cm以上,皮质骨则扩大切除面到骨面渗血为止。刘兵等[11]认为感染的骨段清创后,确保骨髓腔的通畅、渗血活跃,骨皮质表面及横断点呈点状渗血(“Paprika”征),并且确保周围软组织呈正常状态。对于Cierny-MaderⅢ型的病灶,虽然骨皮质清创至创面渗血,但是残存的骨皮质因长时间浸泡在脓液中,受到一定的污染,关于这部分骨皮质的清除与保留问题尚未统一,若是一味行扩大清除将会增加骨缺损的范围,二期植骨时将面临骨量不足的难题。李杭教授团队[12]的经验是,早期感染的Cierny-MaderⅢ型的病灶清创至“红辣椒征”即可,而晚期感染的病灶行节段性切除。早期感染形成的生物膜为“未成熟”阶段,该阶段的生物膜可以被抗生素所杀灭,而晚期的生物膜发展成为“成熟”阶段,只能依靠彻底的清创和更换植入物来清除。对于移植物感染失效的患者,螺钉孔的清创及原植入物的清除、更换至关重要,螺钉孔内残存的细菌会在72 h内形成“成熟”的生物膜,导致清创的失败[13]。关于清创后去除及更换植入物的问题,要根据病灶处骨的稳定性及机体的生理功能等方面综合考虑[14]。骨髓炎的有效清创范围并未达到共识,但是依据骨髓炎分型及患者生理功能指导清创,感染骨边缘清创至“红辣椒”征的基本原则已被大多数骨科医生所接受。 2.1.2 清创频次 虽然清创是降低骨髓炎术后感染复发的关键点,但是由于各种因素的影响,有时一次清创术不能达到感染灶的完全清除,临床上常出现2次或多次的清创手术。行清创术后若出现以下情况,则提示感染复发,可能需再次清创,即:局部出现红、肿、热、痛等典型感染症状,窦道提示感染进入慢性期;白细胞计数、红细胞沉降率、C-反应蛋白、血小板计数/血小板平均体积比升高,出现异常升高的指标越多,提示感染复发可能性越大;血培养发现致病菌;MRI检查病灶内出现炎性水肿和脓肿;局部分层穿刺液涂片发现细菌或脓细胞[15]。多次反复清创后术中多点取材细菌培养阴性,红细胞沉降率、C-反应蛋白、白细胞计数恢复正常,是感染完全控制的指标。在一项国外的流行病学调查中发现,经过反复多次清创手术的患者,1/4的患者病灶处细菌谱发生明显变化,甚至在有的病灶处出现2/3的新细菌[16]。这项研究是在全程抗生素治疗下进行的,不能证明新感染的细菌是多次清创的后果还是细菌耐药性产生的结果。李杭[12]认为清创频次需要根据术前骨髓炎的宿主分型作为参考,对于C类的患者,机体生理功能严重受损,多次的清创带来负面效果可能更甚;对于A类宿主患者,如果感染不太严重,依靠其自身正常的免疫系统可能并不需要反复的清创。多次的清创术会增加骨缺损的范围,为二期植骨带来难题,增加患者痛苦,延长住院时间,且该技术的临床疗效尚未获得普遍认可,因此多次的清创术似乎是临床的无奈之举。 2.1.3 新型清创方式 针对复杂感染灶,传统清创方式的有效性受到一定影响,新型清创术从骨和软组织两方面降低细菌负荷,提高清创效果。在一项动物实验中,实验者采用高速骨钻清创技术去除慢性骨髓炎的病灶骨,结果显示高速骨钻在减少细菌负荷方面具有巨大优势,可以极大降低术后感染复发率[17]。高速骨钻清创技术可以有效清除感染骨中的隐匿病灶、减少细菌负荷,但是高速转动的骨钻会产生升温效应,影响正常骨质活性。扩髓-灌洗-吸引器技术采用高速钻头扩髓加灌洗技术,可以有效清除髓腔内的感染灶,在预防骨髓炎术后感染复发方面有良好的前景[18]。扩髓-灌洗-吸引器技术中持续灌洗可以显著降低高速骨钻产生的升温反应,边扩髓边冲洗能高效清除髓腔内感染灶及残留的骨水泥,然而会面临大量出血及医源性骨折或穿孔的风险。改良双套管脉冲持续冲洗结合负压封闭引流技术能迅速控制病灶区的炎症反应,促进骨髓炎清创术后伤口的恢复。该技术有两个显著优点:术后仍可持续有效灌洗伤口;配合负压封闭引流技术持续负压引流能更高效地保持伤口清洁。但是该技术不但增加患者住院费用,脉冲产生的高压还会损害软组织[19]。 低频超声波清创技术是一种针对软组织的清创技术。MESSA等[20]的临床试验中发现,低频超声清创术促进了60%“不可愈合”伤口的愈合。低频超声清创术的显著优点归纳为3点:适用于任何慢性感染性伤口;有效清除生物膜;促进伤口的愈合速度。目前低频超声波清创尚未被广泛应用于骨髓炎患者,该技术清创后的治疗方案也没有标准化指南。 新型清创技术高效的清除骨髓炎感染灶周围的细菌及生物膜,提供了健康的植骨环境,有效降低了诱导膜技术治疗骨髓炎术后的感染复发率。各种新型清创技术的优缺点,见表1。"
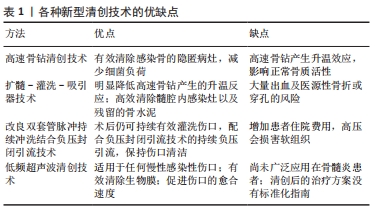
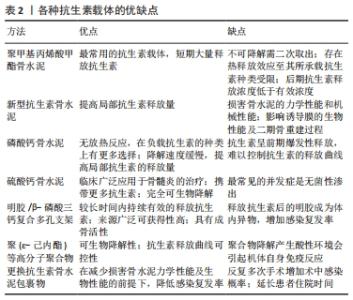
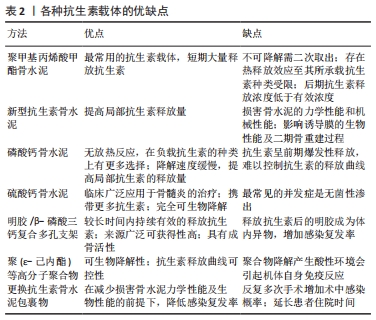
2.2 优化抗生素的应用 2.2.1 如何选用抗生素 抗生素在骨髓炎治疗方案中是不可或缺的重要环节,抗生素的选用应针对培养菌和药敏实验,采用敏感抗生素。采集标本是培养致病菌的第一步,为了避免抗生素对病灶处细菌谱的影响,采集标本前抗生素至少停用2周以上[21]。窦道处液体/脓液会受到表面污染物的影响,该处的标本培养结果不准确,手术中获得的死骨碎片是理想的培养样本。为了进一步提高培养结果的精确性,王剑[22]认为致病菌的确定需要遵循533原则,即5处标本(死骨、骨髓腔远端及近端、髓腔内脓液、死骨周围软组织)至少 3处培养发现感染菌,同一感染菌在同一取材部位发现3次以上,才可以认为该感染菌为致病菌。需要注意是并非所有患者的细菌培养都能培养出致病菌。国内学者在对124例创伤性骨髓炎患者的细菌培养结果进行分析,结果显示致病菌的阳性率75.81%,阴性率高达18.55%[23]。传统的细菌培养方法致病菌检出率并不理想;核酸扩增实验(PCR)可以提高致病菌的检出率,但是具有一定的假阳性率;对术前应用抗生素的样本,超声液体培养比组织培养更敏感,但不推荐做常规检测手段;适当延长标本培养时间至10-14 d,可以提高检出率[24]。骨标本应该分别进行需氧和厌氧菌培养,针对有症状的患者,需要进行分枝杆菌及真菌病原体的培养,值得一提的是创伤性骨髓炎很少见到厌氧菌感染[25]。针对培养结果阴性的患者,允许医生经验性应用广谱抗生素,广谱类抗生素的选择需要针对革兰阳性菌和革兰阴性菌,必要时联合用药[23]。除了致病菌的阴性结果,致病菌的感染时机也需要警惕,即创伤后骨髓炎的致病菌可能发生在手术干预之前、术间或术后医院获得的皮肤菌群。陈培生等[26]认为术前及术后不需要常规采取样本,仅需在明确感染存在后进行标本采集。正确的涂片准备及由经验丰富的实验室技术人员操作对于获得可靠结果至关重要。尽管现今医学检验技术获得长足发展,但是由于致病菌的多样性,如何在不同时间点识别不同区域细菌仍需要继续探索。 2.2.2 抗生素如何使用 (1)全身应用抗生素:全身应用抗生素包括治疗性和抑菌性两个目的,抑菌性应用抗生素,推荐清创术后立即静脉注射2周,而后改为口服用药;治疗性应用抗生素,则要求取出内固定物后系统应用6周(2周静脉注射,4周口服)[27]。 长期全身应用抗生素将会导致肝、肾功能损害,相比短期抗生素疗程,后者感染复发率并未升高。有研究对902例采用诱导膜技术治疗骨髓炎的患者进行不同疗程的抗生素治疗,结果表明短期抗生素治疗方案(仅静脉注射2周)在感染根除率方面并不弱于长期静脉注射[28]。短期全身应用抗生素是近年提出来的新理念,至少2周的静脉应用抗生素已被越来越多人的认可。 全身应用抗生素的疗效取决于靶点血药浓度,有研究发现头孢唑啉的血药浓度在四肢不同的靶点部位有很大差异,头孢唑啉的局部血药浓度与靶点的位置有关,而且随着用药剂量的增加,局部靶点位置的血药浓度也随之增加[29]。由于存在天花板效应,这种剂量-浓度关系并非一直维持,更高浓度的头孢唑林不仅不会产生更少的外科伤口感染,还会增加病灶区细菌的耐药性。全身应用抗生素时,抗生素的剂量需要根据靶点的位置进行调整,不同部位的病灶所需要的抗生素的剂量可能存在差异。不同种类抗生素及不同靶点部位所需的有效抗生素剂量尚需要更多临床试验验证。 (2)抗生素的局部应用:临床证实全身应用抗生素治疗骨髓炎效果有限,这主要因为病灶区的血液供应受到限制,不能携带足量抗生素作用于病灶处,而且细菌生物膜会阻止感染区获得有效浓度的抗生素。为了使感染区获得足够的抗生素,局部应用抗生素成为降低诱导膜技术治疗骨髓炎术后感染复发的重要举措。 ①固定方式的改良: 诱导膜技术第一阶段采用何种固定方式对感染复发有很大影响,病灶骨的稳定性在预防骨髓炎感染复发的过程中至关重要[14]。外固定架作为传统的骨髓炎固定方式可极大减少细菌生物膜的形成,然而在面临骨髓炎清创后导致的大段骨缺损时,外固定的稳定性较差,再发骨折的风险显著提高,而且还面临针道感染的风险。近年抗生素骨水泥的应用使得以内固定的方式维持骨端的稳定性成为可能。抗生素骨水泥是在聚甲基丙烯酸甲酯骨水泥中掺入抗生素,在感染区缓慢、持续释放抗生素。MASQUELET的理念是不要在聚甲基丙烯酸甲酯水泥中添加抗生素,他认为抗生素可能会掩盖局部感染迹象,延误抗感染治疗的时机[4]。经过多项试验后,研究者发现在适当的药物负荷量下(总抗生素与骨水泥的比例小于1∶5),抗生素对骨水泥产生的不良反应是可以接受的[30]。 有研究对183例感染性骨缺损的患者使用抗生素骨水泥涂层锁定板作为临时固定方式,经历第一次清创术后感染的控制率达到91.3%[31]。采用钢板作为临时固定方式应将钢板完全包裹在骨水泥中,避免残留在钢板上的细菌形成生物膜。国外一项采用抗生素骨水泥涂层带锁髓内钉治疗下肢骨髓炎的研究,结果显示感染的控制率达80%[32]。根据数据显示,涂层钢板的抗菌效果优于涂层髓内钉,但是2020年专家意见认为抗生素涂层髓内钉仍是长骨骨感染良好的固定方式[33]。细菌更容易黏附在金属物表面形成牢固的生物膜,因此使用内固定时需要满足彻底清创和抗生素骨水泥完全包裹两个基本条件。 ②抗生素载体:载体材料负载靶向抗生素传递至骨,在较长时间内局部持续释放抗生素,提高局部抗生素的抗菌性[34],因其具有消灭死腔和控制感染的作用,成为降低骨髓炎感染复发方面的研究热点。 聚甲基丙烯酸甲酯骨水泥:作为最常用的抗生素载体,聚甲基丙烯酸甲酯骨水泥在短期大量释放抗生素,但是聚甲基丙烯酸甲酯骨水泥属于不可降解材料需二次取出,热释放效应致其承载抗生素种类受限,后期抗生素释放浓度低于有效浓度[35]。 新型抗生素骨水泥:将硼酸盐生物活性玻璃掺入到聚甲基丙烯酸甲酯抗生素骨水泥,促进抗生素从骨水泥中释放,混合骨水泥的机械强度保持在较高水平[36]。添加聚醚F68(亲水添加剂)后混合抗生素骨水泥的万古霉素释放量达100%,持续释放时间长达11周,机械性能保持良好[37]。加入二氧化钛纳米管后,混合骨水泥抗生素的总释放量可达50%,持续释放时间长达2个月,力学性能保持良好,药物释放后的机械强度也得到保障[38]。新型抗生素骨水泥的理念尚未达成共识,高药物负荷量的抗生素不但会损害骨水泥的力学性能和机械性能,同时还可能会影响诱导膜的生物性能及二期骨重建过程。 磷酸钙骨水泥:作为抗生素载体具有两个优点,其一,磷酸钙骨水泥凝固时没有放热反应,在负载抗生素的种类上有更多选择;其二,缓慢的降解速度更有助于抗生素在局部发挥作用。但是抗生素呈前期爆发性释放,难以控制抗生素的释放曲线[39]。 硫酸钙骨水泥:临床被广泛应用于骨髓炎的治疗,携带更多抗生素,完全可生物降解,最常见的并发症是无菌性渗出[40]。 明胶/β-磷酸三钙复合多孔支架:较长时间内持续有效地释放抗生素,来源广泛可获得性高,具有成骨活性。但释放抗生素后的明胶成为体内异物,增加感染复发率[41]。 聚(ε-己内酯)等高分子聚合物:具有2个显著优点,第一,具有可生物降解性;第二,抗生素释放曲线具有可控性。但是聚合物降解产生的酸性环境会引起机体自身免疫反应[34]。 LAM等[42]采用更换抗生素骨水泥包裹物的方式来控制感染,每次清创外层的骨水泥都会被移除,再包裹一层新的抗生素骨水泥,临床试验实现了接近100%的感染控制率。每次更新抗生素骨水泥,也是在间接延长骨水泥中抗生素的释放量,但是这一方式需要反复多次手术,增加术中感染概率,延长了患者住院时间。 抗生素载体分为不可生物降解的抗生素载体和可生物降解的抗生素载体两大类,可显著提高局部抗生素浓度,提高抗菌疗效,降低药物毒性,提高生物利用度。但目前抗生素载体难以根据局部所需的有效抗生素浓度进行精准调控抗生素的释放曲线,如何精准调控抗生素释放曲线以应对不同时机的细菌负荷是未来学者研究方向。各种抗生素载体的优缺点,见表2。"

③移植骨中混合抗生素:在诱导膜技术植骨过程中,移植骨暴露在空气中可能会受到微生物的污染而增加感染复发率。在移植骨中混和抗生素,既能防止移植物感染,也能在局部释放抗生素预防骨髓炎术后感染复发[43]。MOHAJERANI等[44]将移植骨浸泡克林霉素溶液3 min,发现局部应用小剂量克林霉素(20 mg/L)冲洗或浸泡3 min可有效去除颗粒状植骨的污染。临床上自体移植骨的种类包括皮质骨、松质骨及混合骨,对于不同种类的移植骨,体外实验结果证明其释放万古霉素的能力没有显著差异[45]。但是这项实验是一个体外实验,生物体内存在生物反应和抗生素局部扩散反应,体内的骨移植可能会产生不同的结果,这需要大样本量的生物实验来进一步证实。 2.2.3 针对耐药菌 越来越多的研究者在骨髓炎病灶处发现耐药菌株,这些耐药菌株难以被寻常抗生素杀灭,成为骨髓炎感染复发的重要原因之一。金黄色葡萄球菌是慢性骨髓炎病灶处常见的致病菌,其中耐甲氧西林金黄色葡萄球菌感染的骨髓炎病例逐年增多。据报道,利福平联合喹诺酮类抗生素/夫西地酸在抑制耐甲氧西林葡萄球菌效果显著[46]。生物膜是传统抗生素难以彻底消灭细菌的重要原因,达托霉素可穿透生物膜、快速杀菌活性,打破了抗生素难以“杀灭”生物膜的禁锢,成为治疗球菌性骨髓炎的一线药物[47]。达托霉素可以治疗甲氧西林敏感金黄色葡萄球菌、耐甲氧西林金黄色葡萄球菌感染的骨髓炎,但是抗菌药物的应用必须建立在彻底清创的基础上。抗菌肽作为抗生素的替代品,在治疗耐药菌感染的骨髓炎时具有多个优点:对多药耐药菌、广泛耐药菌具有良好的抗性和高度特异性;影响机体免疫系统,从而降低平均C-反应蛋白和白细胞计数;没有抗生素的交叉耐药性[48]。在一项动物实验中,实验者对耐甲氧西林金黄色葡萄球菌感染的骨髓炎小鼠施以抗菌肽疗法,以硫酸钙作为载体在局部释放抗菌肽,结果显示抗菌肽对该致病菌感染的骨髓炎有较好的局部治疗效果[49]。 噬菌体疗法是一种针对耐药菌的新型抗菌方式,但缺乏明确的临床指南,准确鉴定宿主细菌的噬菌体特异性是针对性应用噬菌体的前提,然而目前关于噬菌体特异性的研究报道甚少。 2.2.4 非抗生素抗菌剂 骨髓中含有的粒细胞前体-粒细胞巨噬细胞具有预防感染的作用。HERNIGOU等[50]的试验证实,接受粒细胞前体松质骨移植的骨髓炎患者感染复发率明显降低。骨髓粒细胞前体松质骨移植可以保护骨感染部位,防止感染复发和移植骨吸收,有效降低术后的感染复发率。生物活性玻璃通常由二氧化硅和其他氧化物(例如钙、磷和钠的氧化物)组合制成,生物活性玻璃植入生物体内后会改变局部pH值和渗透压,使其具有一定的抗菌性[51]。掺入铜的生物活性玻璃在杀灭金黄色葡萄球菌方面有杰出的表现,再与3D胶原蛋白支架结合成复合物,具有良好的生物相容性,促进骨的生长和血管生成的能力也得到加强[52]。该复合物作为一种新的组织工程产物,同时满足限制感染和促进骨骼愈合2个条件,在治疗骨髓炎方面显示出的巨大潜力。银作为最有潜质的金属纳米颗粒会诱导自身氧自由基和活性氧的增加,从而在蛋白质、DNA和包括膜在内的细胞不同结构中发生氧化应激损伤,基于这些机制,银纳米粒可以显著降低细菌活性[53]。非抗生素的抗菌剂在降低细菌感染方面具有出色的表现,而且无抗生素对诱导膜生物性能的影响,如何将非抗生素抗菌剂与诱导膜技术联合应用值得未来学者进一步探究。 2.3 局部软组织重建方法的改进 2.3.1 皮瓣移植 软组织覆盖是诱导膜技术形成优良诱导膜的基础。游离皮瓣在骨髓炎所形成感染和低血供的恶劣环境中难以存活,带蒂皮瓣移植成为软组织重建相对安全的方式。刘军等[54]通过对13例创伤性胫骨骨髓炎伴软组织缺损患者进行分期治疗,即二期行皮瓣移植,在确保软组织健康的前提下行三期更换内固定物、植骨,成功控制感染,未发生感染复发的病例。石健等[55]对骨髓炎伴软组织损伤的患者行诱导膜技术+带蒂皮瓣移植治疗,获得良好的临床效果,他认为带蒂皮瓣减少了瘢痕形成,改善了局部血供,增加了软组织的抗感染能力。穿支动脉皮瓣成为继带蒂皮瓣后疗效更佳的移植物,腓肠内侧动脉穿支皮瓣伴有长达10 cm穿支动脉可以更加灵活地修复创面,抗感染能力强,成为骨髓炎伴软组织缺损患者行软组织修复的新方向。行穿支动脉皮瓣移植术前,应用微泡增强超声技术和血管三维重建技术对血管造影的血管数据进行重建,可以提高手术的准确性和安全性[56]。血管化的软组织覆盖物成活率较高,在骨骼与微生物组之间提供了物理和微生物屏障,防止裸露的骨中建立新的感染,此外软组织填充死腔,有利于抗生素在病灶区的传递。 2.3.2 Rigenera微移植技术 应用显微外科技术行带蒂皮瓣移植手术对术者技术要求高,在面临骨髓炎窦道这样面积较小的软组织缺损,可操作性及移植物存活性显著降低。近来有一项被称为Rigenera技术的微移植技术被提出,UEHARA等[57]采用该技术为1例左足拇指慢性骨髓炎伴皮肤溃疡患者进行了溃疡皮肤清创、微移植技术,术后该患者足拇指皮肤获得愈合。采用Rigenera微移植技术获得的移植物富含祖细胞,并能够将移植物的细胞活力和再生潜力维持在较高水平;此外,培养皿中培养的微植物是无菌的移植物[58]。微移植物富含间充质干细胞及高活力细胞,可提高局部组织的愈合效果,对面积较小的骨髓炎窦道进行微移植技术,在提高软组织愈合率的基础上可降低手术困难度。 2.4 创面负压治疗技术的改进 2.4.1 负压伤口疗法 负压伤口疗法作为感染伤口的临时处理措施在临床上得到广泛应用,主要的优势是:可以稳定伤口环境,减少细菌负荷,作为反复清创和分阶段闭合的辅助手段,可以一直应用到伤口不再受到感染,再行软组织覆盖,从而增加移植物存活率[59]。与传统纱布敷料处理感染伤口相比,负压伤口疗法能更有效地控制需氧细菌[60]。该文提到骨髓炎致病菌培养结果显示,几乎所有创伤性骨髓炎都是需氧菌感染,这让负压伤口疗法对骨髓炎致病菌的控制更加高效。据报道该技术也有疼痛和感染等并发症,KWA等[61]的一项研究中发现,负压伤口疗法结束时细菌的负荷略高于开始时,在负压伤口疗法过程中总感染率保持不变的情况下,金黄色葡萄球菌的数量和细菌的总量增加。KWA等的研究并未提及细菌数量及负荷的增加是否对感染的其他指标(例如红细胞沉降率、C-反应蛋白、白细胞计数)产生影响。有研究认为,虽然一定负压环境可能会刺激某些细菌的生长,但负压伤口疗法并不会增加感染概率[62]。 负压伤口疗法所创造的负压环境促进局部血液循环,减少伤口渗液,不利于细菌的存活,而且密闭的环境能有效阻止细菌入侵,减少病灶处细菌负荷。作为感染伤口的临时处理措施,负压伤口疗法自问世以来,创面填充材料及负压的选择取得长足发展,在临床得到广泛应用,然而其作用机制仍缺乏统一共识,负压环境刺激某些细菌生长的问题也需要进一步解决。 2.4.2 负压伤口滴注疗法 为了提高负压伤口疗法的临床效果、减少并发症的发生率,一种兼具负压疗法与间歇性地将溶液滴入创面以持续降低细菌负荷的新技术被提出,即负压伤口滴注疗法,该技术改变了生物膜的结构,减少了生物膜的厚度和细菌的数量,更高效地控制感染[63]。KIM等[64]对分别接受负压伤口疗法和负压伤口滴注疗法治疗的感染伤口进行分析,结果显示采用后者治疗感染伤口可以更有效控制感染灶,获得更好的伤口愈合效果。为了明确这种疗效,KAMAPATHY等[65]做了一项Meta分析,结果显示负压伤口滴注疗法的确可提供更高的伤口愈合率,改善各种复杂伤口的愈合情况;与负压伤口疗法技术相比较,负压伤口滴注疗法促进肉芽组织生长的能力明显提高。 目前已有几种溶液作为负压伤口滴注疗法的滴注液,包括生理盐水、次氯酸盐溶液 (Dakin’s)、防腐剂、次氯酸和抗生素灌注液。次氯酸溶液无细胞毒性,对伤口中常见的细菌有广谱覆盖范围;此外,次氯酸溶液还可破坏生物膜,更适骨髓炎等感染伤口[19]。FAUST团队[66]认为对有生物污染、反复感染的创面,首选次氯酸溶液作为负压伤口滴注疗法的滴注液,此外还需配合敏感抗生素和彻底清创等治疗方法。该文提到清创后处于休眠期的细菌会在72 h形成“成熟”生物膜,作者认为应首先对骨髓炎病灶进行彻底清创,然后配合负压伤口滴注疗法的滴注冲洗和负压环境减少伤口渗液,降低细菌活性,从而抑制生物膜的再形成。对于负压伤口滴注疗法的理想滴注溶液和停留时间尚需要大量的随机临床研究,以便针对不同致病菌感染的骨髓炎病灶选择相应的负压伤口滴注疗法。"

|
[1] 王钊,闫石.应用Masquelet技术治疗大段骨缺损减少自体骨用量的可能性[J].中国组织工程研究,2020,24(24):3862-3869. [2] ZAYZAN KR, YUSOF NM, SULONG AF, et al. Functional outcome and quality of life following treatment for post-traumatic osteomyelitis of long bones. Singapore Med J. 2020. doi: 10.11622/smedj.2020164. [3] 买吾拉尼江·加马力,艾合买提江·玉素甫. Masquelet技术治疗大段骨缺损的最新进展[J].实用骨科杂志,2020,26(2):136-139. [4] MASQUELET AC. Induced membrane technique: pearls and pitfalls. J Orthop Trauma. 2017;31:S36-38. [5] O’CONNOR CM, PERLOFF E, DRINANE J, et al. An Analysis of Complications and Bone Defect Length With the Use of Induced Membrane Technique in the Upper Limb: A Systematic Review. .Hand (N Y), 2020: 1558944720918368. doi: 10.1177/1558944720918368. [6] WANG XH, WANG SL, FU JS, et al. Risk factors associated with recurrence of extremity osteomyelitis treated with the induced membrane technique. Injury. 2020;51:307-311. [7] CHOUFANI C, DEMOURES T, DE L’ESCALOPIER N, et al. Application of the Masquelet technique in austere environments: experience from a French forward surgical unit deployed in Chad. Eur J Trauma Emerg Surg. 2020. doi: 10.1007/s00068-020-01471-5. [8] CHAN JKK, FERGUSON JY, SCARBOROUGH M, et al. Management of Post-Traumatic Osteomyelitis in the Lower Limb: Current State of the Art. Indian J Plast Surg. 2019;52: 62-72. [9] 谢肇.对骨感染控制瓶颈问题的思考[J].中华骨科杂志,2018,38(9): 519-522. [10] 杨聪林,陈元标,马绍华,等.Masquelet技术治疗感染性骨缺损的疗效分析[J].临床医药文献电子杂志,2019,6(27):65-66. [11] 刘兵,马翔宇,杨超,等.抗生素骨水泥涂层髓内钉结合Masquelet 技术治疗胫骨干感染性骨缺损[J].局解手术学杂志,2020,29(10): 791-795. [12] 李杭.胫骨感染性骨不连的规范化治疗现状和难点[J].中华创伤杂志,2019,35(2):97-100. [13] 谢肇,喻胜鹏.膜诱导技术治疗感染性骨不连、骨缺损[J].中华骨科杂志,2018,38(9):570-576. [14] METSEMAKERS WJ, MORGENSTERN M, SENNEVILLE E, et al. General treatment principles for fracture-related infection: recommendations from an international expert group. Arch Orthop Trauma Surg. 2020; 140:1013-1027. [15] VEMU L, SUDHAHARAN S, MAMIDI N, et al. Need for appropriate specimen for microbiology diagnosis of chronic osteomyelitis. J Lab Physicians. 2018;10:21-25. [16] WUARIN L, ABBAS M, HARBARTH S, et al. Changing perioperative prophylaxis during antibiotic therapy and iterative debridement for orthopedic infections? PLoS One. 2019;14: e0226674. [17] SU DTR, HENRY RH. Debridement with high speed burr reduce more colonies of Staphylococcus aureus in chronic osteomyelitis of rabbit’s tibia compare to debridement with curettage. Int J Res Med Sci. 2016;4(10):4370-4375. [18] 李海峰,顾三军,殷渠东.扩髓-灌洗-吸引器的研究现状与应用特点[J].中国组织工程研究,2018,22(14):2284-2289. [19] 张斌,杨志刚,杨晓斐,等.应用改良双套管脉冲持续冲洗结合负压封闭引流技术治疗骨髓炎[J].骨科,2017,8(6):433-438. [20] MESSA CA, CHATMAN BC, RHEMTULLA IA, et al. Ultrasonic debridement management of lower extremity wounds: retrospective analysis of clinical outcomes and cost. J Wound Care. 2019; 28: S30-S40. [21] RUPP M, ERNK S, WEBER T, et al. Polymicrobial infections and microbial patterns in infected nonunions - a descriptive analysis of 42 cases. BMC Infect Dis. 2020;20: 667. [22] 王剑.骨髓炎的诊治原则[J].中华肩肘外科电子杂志,2019,7(4):383-384. [23] 魏丽艳,刘畅,卞婧,等.北京积水潭医院创伤性骨髓炎患者病原 菌分布及抗菌药物应用情况分析[J].临床药物治疗杂志,2019,17 (10):42-45,81. [24] GOVAERT GAM, KUEHL R, ATKINS BL,et al. Diagnosing Fracture-Related Infection: Current Concepts and Recommendations. J Orthop Trauma. 2020;34: 8-17. [25] VEMU L, SUDHAHARAN S, MAMIDI N, et al. Need for appropriate specimen for microbiology diagnosis of chronic osteomyelitis. J Lab Physicians. 2018;10:21-25. [26] 陈培生,林凤飞,陈宾,等.骨折相关感染细菌培养规范取材的研究进展[J].中华创伤骨科杂志,2020,22(4):365-368. [27] 中华医学会骨科学分会创伤骨科学组,中华医学会骨科学分会外固定与肢体重建学组,中国医师协会创伤外科医师分会创伤感染专家委员会.中国骨折内固定术后感染诊断与治疗专家共识(2018版)[J].中华创伤骨科杂志,2018,20(11):929-936. [28] WANG XH, FANG L, WANG SL, et al. Antibiotic treatment regimens for bone infection after debridement: a study of 902 cases. BMC Musculoskelet Disord. 2020;21:215. [29] SANDERS FRK, GOSLINGS JC, MATHOT RAA, et al. Target site antibiotic concentrations in orthopedic/trauma extremity surgery: is prophylactic cefazolin adequately dosed? A systematic review and meta-analysis. Acta Orthop. 2019;90:97-104. [30] 李海峰,顾三军,芮永军,等.诱导膜技术修复骨缺损研究现状及应用方法的改进[J].中国组织工程研究,2019,23(30):4855-4860. [31] JIA C, WANG XH, YU SP, et al. An antibiotic cement-coated locking plate as a temporary fixation for treatment of infected bone defects: a new method of stabilization. J Orthop Surg Res. 2020;15:44. [32] MAKHDOM AM, BUKSBAUM J, ROZBRUCH SR, et al. Antibiotic Cement-Coated interlocking Intramedullary Nails in the Treatment of Septic Complex Lower Extremity Reconstruction; A Retrospective Analysis with Two year Minimum Follow up. J Bone Jt Infect. 2020;5:176-183. [33] METSEMAKERS WJ, FRAGOMEN AT, MORGENSTERN M. Fracture-Related Infection consensus g.Evidence-Based Recommendations for Local Antimicrobial Strategies and Dead Space Management in Fracture-Related Infection. J Orthop trauma. 2020;34(1):18-29. [34] ZHOU CH, REN Y, ALI A, et al. Single-stage treatment of chronic localized tibial osteomyelitis with local debridement and antibiotic-loaded calcium sulfate implantation: a retrospective study of 42 patients. J Orthop Surg Res. 2020;15:201. [35] SOARES D, LEITE P, BARREIRA P, et al. Antibiotic-loaded bone cement in total joint arthroplasty. Acta Orthop Belg. 2015;81:184-190. [36] GRAHMN AF, JONATHAN CB, KIMBERLY AC. Antibiotic Elution and Mechanical Strength of PMMA Bone Cement Loaded With Borate Bioactive Glass. J Bone Jt Infect. 2018;3(4):187-196. [37] OH EJ, OH SH, LEE IS, et al. Antibiotic-eluting hydrophilized PMMA bone cement with prolonged bactericidal effect for the treatment of osteomyelitis. J Biomater Appl. 2016;30:1534-1544. [38] SHEN SC, ETCHMANAN K, CHOW PS, et al. Antibiotic elution and mechanical property of TiO nanotubes functionalized PMMA-based bone cements. J Mech Behav Biomed Mater. 2019;91:91-98. [39] CHEN G, LIU B, LIU H, et al. Calcium Phosphate Cement loaded with 10% vancomycin delivering high early and late local antibiotic concentration in vitro. Orthop Traumatol Surg Res. 2018;104:1271-1275. [40] JIANG N, ZHAO XQ, WANG L, et al. Single-stage debridement with implantation of antibiotic-loaded calcium sulphate in 34 cases of localized calcaneal osteomyelitis. Acta Orthop. 2020;91:353-359. [41] ROTMAN SG, THOMPSON K, GRIJPMA DW, et al. Development of bone seeker-functionalised microspheres as a targeted local antibiotic delivery system for bone infections. J Orthop Translat. 2020;21:136-145. [42] LAM YL, YAU R, HO KW, et al. Antibiotic-laden cement wrap: A simple but effective way of treating patients with megaprosthesis infection. J Orthop Surg (Hong Kong). 2019;27:2309499019825587. [43] KAMRA P, LAMBA AK, FARAZ F. Effect of antibiotic impregnation time on the release of gentamicin from cryopreserved allograft bone chips: an in vitro study. Cell Tissue Banking. 2019;20(2):267-273. [44] MOHAJERANI H, IRAJIAN G, LATIFI F, et al. Efficacy of low-dose local clindamycin in different times for microbial decontamination of autogenous particulate bone graft. Int J Implant Dent. 2020;6:70. [45] ERIVAN R, LOPEZ-CHICON P, FARINAS O, et al. Which type of bone releases the most vancomycin? Comparison of spongious bone, cortical powder and cortico-spongious bone. Cell Tissue Bank. 2020;21: 131-137. [46] 徐一宏,徐卫东.急性假体周围感染清创方法及抗生素策略[J].中华骨与关节外科杂志,2018,11(6):475-480. [47] 达托霉素临床应用专家意见编写专家组,中国研究型医院学会感染性疾病循证与转化专业委员会.达托霉素临床应用专家意见[J].中国感染控制杂志,2019,18(11):989-1003. [48] TAATI MM, AMIRMOZAFARI N, SHARIATI A, et al. How Phages Overcome the Challenges of Drug Resistant Bacteria in Clinical Infections. Infect Drug Resist. 2020;13:45-61. [49] MELICHERCIK P, ČEROVSKY V, NESUTA O, et al. Testing the efficacy of antimicrobial peptides in the topical treatment of induced osteomyelitis in rats. Folia Microbiol (Praha). 2018;63:97-104. [50] HERNIGOU P, DUBORY A, HOMMA Y, et al. Single-stage treatment of infected tibial non-unions and osteomyelitis with bone marrow granulocytes precursors protecting bone graft. Int Orthop. 2018;42: 2443-2450. [51] LINDFORS N,GEURTS J, DRAGO L, et al. Antibacterial Bioactive Glass, S53P4, for Chronic Bone Infections - A Multinational Study. Adv Exp Med Biol. 2017;971:81-92. [52] RYAN EJ, RYAN AJ, GONZALEZ VA, et al. Collagen scaffolds functionalised with copper-eluting bioactive glass reduce infection and enhance osteogenesis and angiogenesis both in vitro and in vivo. Biomaterials. 2019;197:405-416. [53] VALLET-REGI M, LOZANO D, GONZALEZ B, et al. Biomaterials against Bone Infection. Adv Healthc Mater. 2020;9:e2000310. [54] 刘军,芮永军,吴永伟,等.创伤性胫骨骨髓炎并软组织及骨缺损的分期治疗[J].中国矫形外科杂志,2018,26(4):378-381. [55] 石健,吕乾,陈星宇. Masquelet技术结合小腿皮瓣治疗胫骨感染性骨缺损伴广泛软组织缺损的疗效分析[J].中华创伤骨科杂志, 2021,23(1):62-67. [56] 林光豪,陈芝武,郑钧水,等.游离腓肠内侧动脉穿支肌皮瓣修复骨髓炎创面[J].中华整形外科杂志,2019,35(12):1234-1239. [57] UEHARA M, SHIMIZU F. Progress report for intractable ulcer and osteomyelitis cases using autologous micrografts. SAGE Open Med Case Rep. 2019;7:2050313X19848301. [58] MARCARELLI M, TROVATO L, NOVARESE E, et al. Rigenera protocol in the treatment of surgical wound dehiscence. Int Wound J. 2017;14: 277-281. [59] ELDENBURG E, PFAFFENBERGER M, GABRIEL A. Closure of a Complex Lower Extremity Wound With the Use of Multiple Negative Pressure Therapy Modalities. Cureus. 2020;12:e9247. [60] DHAWAN R, ASIF M. Effect of negative pressure wound therapy on the bacterial flora of wounds: A prospective randomized study. Int J Res Med Sci. 2019;2(8):13-15. [61] KWA KAA, KRIJINEN P, BERNARDS AT, et al. Bacterial Species and Load Increase During Negative Pressure Wound Therapy: A Prospective Cohort Study. Wounds. 2020;32(3):74-80. [62] 余泮熹,杨晓楠,靳小雷,等.负压创面治疗技术的研究进展[J].医学研究杂志,2018,47(3):172-174,78. [63] ORGILL DP, BAYER LR. Negative pressure wound therapy: past,present and future. Int Wound J. 2013;10(Suppl 1):15-19. [64] KIM PJ, SILVERMAN R, ATTINGER CE, et al. Comparison of Negative Pressure Wound Therapy With and Without Instillation of Saline in the Management of Infected Wounds. Cureus. 2020;12:e9047. [65] KAMAPATHY M, MANTELAKIS A, KHAN N, et al. Clinical application and efficacy of negative pressure wound therapy with instillation and dwell time (NPWTi-d): A systematic review and meta-analysis. Int Wound J. 2020;17:1948-1959. [66] FAUST E, OPOKU-AGYEMAN JL, BEHNAM AB. Use of Negative-Pressure Wound Therapy With Instillation and Dwell Time: An Overview. Plast Reconstr Surg. 2021;147:16S-26S. |
| [1] | Feng Jianbo, Li Chencheng, Liu Jinyue, Wang Xiaomin, Peng Jiachen. Implantation of Kirschner wire with Staphylococcus aureus biofilm establishes a traumatic osteomyelitis model in rats [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 700-705. |
| [2] | Le Guoping, Xi Licheng. Preparation and performance evaluation of composite tissue-engineered material hydrogel with sustained-release antibacterial microspheres [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(21): 3298-3305. |
| [3] | Li Yufan, Lin Mingyue, Wang Chenxin, Zhang Rui, Li Yubao, Chen Li, Zou Qin. Application of micro-CT in rabbit tibial osteomyelitis modeling [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(18): 2874-2880. |
| [4] | Hua Haotian, Zhao Wenyu, Zhang Lei, Bai Wenbo, Wang Xinwei. Meta-analysis of clinical efficacy and safety of antibiotic artificial bone in the treatment of chronic osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(6): 970-976. |
| [5] | Li Xingping, Xiao Dongqin, Zhao Qiao, Chen Shuo, Bai Yiguang, Liu Kang, Feng Gang, Duan Ke. Preparation and properties of copper-loaded antibacterial functional film on titanium surface [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 553-557. |
| [6] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [7] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [8] | Gao Tianhao, Qian Huifang, Yang Shangliang, Xin Chaofei, Lu Shitao, Xu Jianzhong. Calcium sulfate antibiotic carrier in the treatment of periprosthetic infection after arthroplasty and its effect on serum calcium [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(30): 4823-4827. |
| [9] | Ma Rui, Wang Jialin, Wu Mengjun, Ge Ying, Wang Wei, Wang Kunzheng. Relationship of pathogenic bacteria distribution with drug resistance and treatment cycle for periprosthetic joint infection after total joint arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 380-385. |
| [10] | Tian Lin, Shi Xiaoqing, Mao Jun, Zhang Nongshan, Zhang Li, Xing Runlin, Wang Peimin. Meta-analysis of vacuum-sealing drainage combined with antibiotic bone cement in the treatment of chronic osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(16): 2618-2624. |
| [11] | Xu Canhong, Meng Lin, Dong Panfeng, Zhan Huasong, Song Shilei. Masquelet technique in treatment of infectious nonunion: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(15): 2445-2452. |
| [12] | Ma Jinchao, Liu Tiansheng, Liu Aipeng, Wang Hao, Wang Qi, Liang Yongjian, Wang Lin, Di Haiwei. Photodynamic antimicrobial chemotherapy for repairing a rabbit model of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(8): 1254-1259. |
| [13] | Zhou Zihong, Wu Yongwei, Feng Dehong, Zhao Jijun, Gu Sanjun, Xu Yajun, Rui Yongjun, Yin Xiaogen, Yin Qudong. Bone healing effects of early-stage versus late-stage bone grafting within induced membrane [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(4): 493-498. |
| [14] | Guo Juan, Zheng Shan, Xie Hui, Hu Yahui. An analysis of pathogenic bacteria infection in 422 kidney transplant recipients [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(32): 5198-5202. |
| [15] | Yang Feng, Chang Lipu, Huang Changshan, Gong Xiaoguang, Chang Shunwu. Macrolide antibiotics protects against ischemia-reperfusion injury after liver transplantation in rats [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(26): 4176-4182. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||