其他干细胞
-
图 1|胚龄10 d的Cx43+/+小鼠横切面免疫组织化学和免疫荧光双染色形态
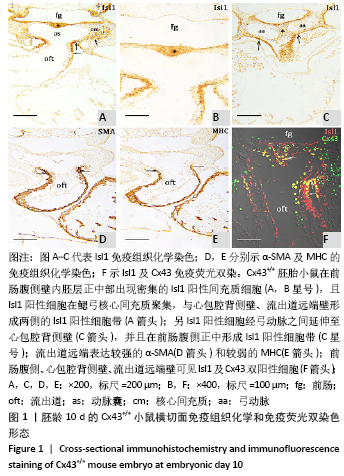
结果:小鼠胚龄10 d,心管向右弯曲成襻,可分辨心室、心房和流出道。流出道壁由心肌、内皮及二者之间的心胶质构成。流出道远端与动脉囊相连,动脉囊背侧与前肠腹侧内胚层相邻,两侧与弓动脉相通。Cx43+/+小鼠胚胎前肠腹侧壁内胚层的正中部与两侧相比,表达较强的Isl1,且内胚层正中部的腹侧出现密集的间充质细胞,同样为Isl1强阳性,见图1A,B,连续切片观察这些Isl1阳性间充质细胞经弓动脉之间延伸至心包腔背侧壁,在前肠腹侧正中形成Isl1阳性细胞带,见图1C。鳃弓核心间充质Isl1阳性细胞聚集,并与心包腔背侧壁、流出道远端壁形成两侧的Isl1阳性细胞带,见图1A。相邻切片染色显示流出道远端壁的Isl1阳性区表达较强的α-SMA和较弱的MHC,见图1D,E,提示Isl1阳性细胞正在向心肌细胞分化。前肠腹侧、心包腔背侧壁及流出道远端壁部分Isl1阳性细胞同时表达Cx43,见图1F。
图 2|胚龄10 d的Cx43-/-小鼠横切面免疫组织化学染色形态

结果:Cx43-/-小鼠未见Cx43表达,进一步确认基因敲除成功,见图2A。与野生型小鼠相比,Cx43基因敲除小鼠胚龄10 d,前肠腹侧内胚层的正中部仍表达Isl1,相邻间充质内也可见Isl1阳性细胞密集分布,见图2B,C;但鳃弓核心间充质的Isl1阳性表达少于野生型小鼠胚胎,见图1A,2D。相邻切片染色显示流出道远端仍表达较强的α-SMA和较弱的MHC,见图2E,F,说明Isl1阳性细胞仍可向心肌细胞分化。
图 3|胚龄11 d的Cx43+/+小鼠横切面免疫组织化学和免疫荧光双染色形态
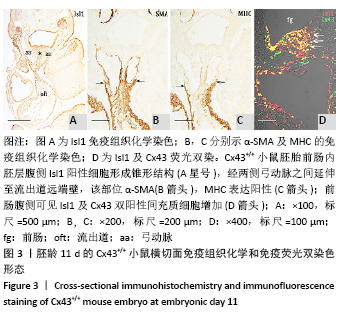
结果:小鼠胚龄11 d,前肠内胚层腹侧Isl1阳性间充质细胞显著增多,形成锥形结构,经两侧弓动脉之间延伸至流出道远端壁,见图3A,该部位为α-SMA和MHC阳性,见图3B,C,即心肌性流出道远端直接与心包腔背侧壁相连续,鳃弓核心间充质的Isl1阳性细胞明显减少,且失去了与心包腔背侧壁的连续性(数据未显示),即与胚龄10 d不同,至胚龄11 d,第二生心区Isl1阳性细胞主要分布于前肠腹侧间充质与心包腔背侧壁。免疫荧光双染结果显示前肠腹侧Isl1和Cx43双阳性间充质细胞较胚龄10 d增多,见图3D。
图 4|胚龄11 d的Cx43-/-小鼠横切面免疫组织化学染色形态
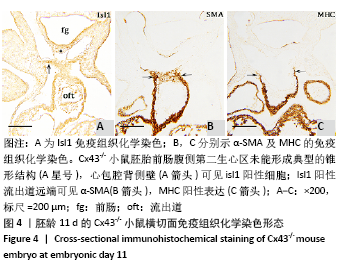
结果:Cx43-/-小鼠胚胎11 d,前肠腹侧内胚层正中部仍表达Isl1,由动脉端向静脉端移行,前肠内胚层腹侧的间充质、心包腔背侧壁,见图4A,均可见Isl1阳性细胞,但数量明显少于野生型小鼠胚胎,未能形成典型的锥形结构,见图3A,4A。相邻切片染色显示Isl1阳性的流出道远端可见α-SMA,MHC的表达,见图4B,C,提示流出道远端依然有心肌细胞分化,促使流出道继续增长。
图 5|胚龄11.5 d的Cx43+/+小鼠横切面免疫组织化学染色形态
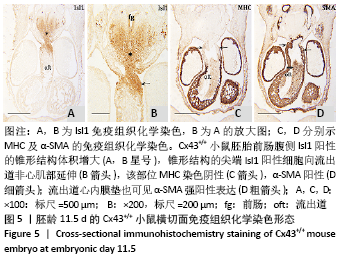
结果:至胚龄11.5 d,前肠腹侧Isl1阳性的锥形结构体积增大,见图5A,B。动脉囊进入心包腔,MHC染色阴性,见图5C,因此成为流出道的非心肌部。锥形结构的尖端Isl1阳性细胞向流出道非心肌部延伸,见图5B,该部位α-SMA阳性,见图5D,MHC阴性说明此处迁入的Isl1阳性细胞不再向心肌细胞分化。
图 6|胚龄13 d的Cx43+/+小鼠三维重建以及横切面免疫组织化学染色形态
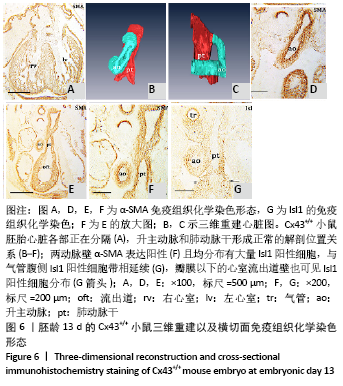
图 7|胚龄13 d的Cx43-/-小鼠三维重建以及横切面免疫组织化学染色形态
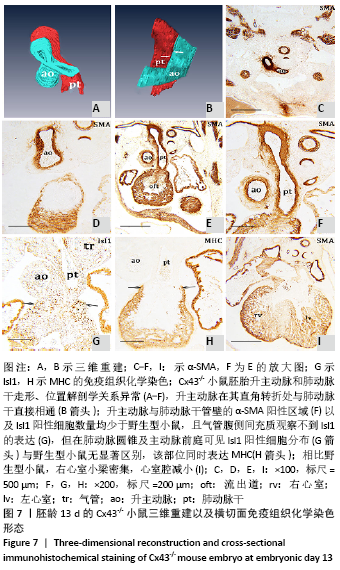
结果:胚龄13 d,心脏各部正在分隔,见图6A。流出道缩短,在Cx43+/+和Cx43-/-小鼠胚胎均可观察到流出道的非心肌部已分隔为升主动脉和肺动脉干。瓣膜以下的流出道心内膜垫正在融合形成流出道隔,将流出道分隔为左右两部分,即主动脉前庭和肺动脉圆锥。野生型小鼠胚胎升主动脉由肺动脉干右侧经腹侧斜上走行到达其左侧,形成成体心脏升主动脉、肺动脉干正常的解剖位置关系,见图6B-F。两动脉壁均分布有大量Isl1阳性细胞,与气管腹侧Isl1阳性细胞带相延续,见图6G,相邻切片显示α-SMA的强阳性表达,见图6F。瓣膜以下的心室流出道壁也可见Isl1阳性细胞分布,见图6G。而在Cx43-/-小鼠胚胎,连续切片与三维重建显示升主动脉由肺动脉干右侧首先直行离开心包腔,再横向左行形成主动脉弓,见图7A-F,而升主动脉在其直角转折处与肺动脉干直接相通,见图7B,升主动脉与肺动脉干管壁内Isl1阳性细胞数量明显少于野生型小鼠,气管腹侧间充质观察不到Isl1的表达,见图6G,7G,两动脉管壁近内皮侧为α-SMA强阳性,但α-SMA阳性区域少于野生型小鼠,见图6F,7F。在肺动脉圆锥、主动脉前庭Isl1阳性细胞分布与野生型小鼠无显著区别,见图6G,7G,该部位同时表达MHC,见图7H。与野生型小鼠胚胎相比,Cx43基因敲除小鼠胚胎右心室小梁密集,心室腔减小,见图6A,7I。
图 8|胚龄10-11.5 d的Cx43+/+小鼠和Cx43-/-小鼠横切面免疫组织化学和免疫荧光双染色形态

结果:小鼠胚龄10 d,野生型小鼠胚胎Ap2α阳性神经嵴细胞呈鞘状包裹弓动脉壁,一侧延伸至动脉囊腹侧及其与之相连的流出道远端的心胶质内,提示流出道心内膜垫开始形成。另一侧延伸至动脉囊背侧壁开始形成间充质隔,具体可见图8A,B。Cx43-/-小鼠动脉囊腹侧与背侧壁Ap2α阳性细胞明显少于野生型小鼠胚胎,流出道远端心胶质内未观察到Ap2α阳性细胞,见图8C。胚龄11 d,Ap2α阳性神经嵴细胞继续沿弓动脉壁向流出道的心内膜垫迁移,弓动脉壁周围可见Cx43与Ap2α双阳性细胞,见图8D。Cx43-/-小鼠胚胎神经管两侧Ap2α阳性的间充质细胞迁移至弓动脉壁周围,呈散在分布。在动脉囊背侧、腹侧以及与之相连的流出道心内膜垫远端仅可观察到少量Ap2α阳性细胞,见图8E。至胚龄11.5 d,大量Ap2α阳性分布于弓动脉周围、前肠腹侧Isl1阳性的锥形结构的两侧,见图5B,8F。此期动脉囊成为流出道的非心肌部,该部分并无心内膜垫,因此弓动脉壁周围的Ap2α不再向此处迁移,见图8F。流出道心内膜垫内间充质细胞数量达高峰,这些细胞不表达Ap2α,而是α-SMA强阳性,见图5D,8F。
引用本文:李 行, 景 雅, 李云华, 李海荣, 杨艳萍. Cx43敲除小鼠胚胎心脏流出道内第二生心区和心脏神经嵴来源间充质细胞减少[J]. 中国组织工程研究, 2021, 25(13): 2018-2024.
点击此处查看全文