中国组织工程研究 ›› 2013, Vol. 17 ›› Issue (29): 5364-5370.doi: 10.3969/j.issn.2095-4344.2013.29.016
• 复合支架材料 composite scaffold materials • 上一篇 下一篇
三维打印制备钛/羟基磷灰石复合体及功能梯度材料
钱 超,樊英姿,孙 健
- 上海交通大学医学院附属第九人民医院口腔修复科,上海市口腔医学重点实验室,上海市 200011
-
收稿日期:2012-11-10修回日期:2012-12-19出版日期:2013-07-22发布日期:2013-07-22 -
通讯作者:孙健,副主任医师,上海交通大学医学院附属第九人民医院口腔修复科,上海市口腔医学重点实验室,上海市 200011 -
作者简介:钱超★,男,1987年生,江苏省无锡市人,汉族,2012年上海交通大学医学院毕业,硕士,医师,主要从事数字化设计与制作应用于口腔修复方面的研究。 qianch1987@yahoo.com.cn -
基金资助:上海市重点学科(特色学科)建设基金资助项目(T0202,S30206);上海市自然科学基金资助项目(09ZR1416600)
Three-dimensional printing of titanium/hydroxyapatite composite and functionally graded materials
Qian Chao, Fan Ying-zi, Sun Jian
- Department of Prosthodontics, the Ninth People’s Hospital, School of Medicine, Shanghai Jiao Tong University, Shanghai Key Laboratory of Stomatology, Shanghai 200011, China
-
Received:2012-11-10Revised:2012-12-19Online:2013-07-22Published:2013-07-22 -
Contact:Sun Jian, Associate chief physician, Department of Prosthodontics, the Ninth People’s Hospital, School of Medicine, Shanghai Jiao Tong University, Shanghai Key Laboratory of Stomatology, Shanghai 200011, China -
About author:Qian Chao★, Master, Physician, Department of Prosthodontics, the Ninth People’s Hospital, School of Medicine, Shanghai Jiao Tong University, Shanghai Key Laboratory of Stomatology, Shanghai 200011, China qianch1987@yahoo.com.cn -
Supported by:the Leading Academic Discipline (Featured Ddisciplines) Construction Fund Project of Shanghai City, No. T0202*, S30206*; the Natural Science Foundation of Shanghai City, No. 09ZR1416600*
摘要:
背景:传统压模成形法制备的钛/羟基磷灰石复合材料结构简单,自动化程度较低,难以控制材料的孔隙率及孔径,不能满足多样化需求。 目的:评价三维打印成型技术制备钛/羟基磷灰石复合体及功能梯度材料的可行性。 方法:设计钛/羟基磷灰石复合体为直径25 mm、高度15 mm的圆柱体,功能梯度材料为直径25 mm,上层5 mm的钛粉末层,下层5 mm钛/羟基磷灰石粉末层的圆柱体CAD模型。利用三维打印技术制备钛/羟基磷灰石复合体及功能梯度材料并进行烧结。观察烧结完成后钛/羟基磷灰石复合体和钛/羟基磷灰石功能梯度材料的显微结构,并行X射线衍射分析和抗压强度检测。 结果与结论:烧结后的钛/羟基磷灰石复合体及功能梯度材料试件均匀无收缩和变形。钛/羟基磷灰石复合体形成紧密结晶体,孔径为50-150 μm。钛和羟基磷灰石在烧结中发生了化学反应,生成物包含Ca3(PO4)2、CaTiO3、TiO2和CaO,其抗压强度为(184.3±27.1) MPa。烧结后钛/羟基磷灰石功能梯度材料在微观结构下可见不同材料间较为清晰的分界线,具有梯度结构。表明三维打印技术制备钛/羟基磷灰石复合体及功能梯度材料的微观结构和力学性能可满足医用生物植入材料的要求。
中图分类号:
引用本文
钱 超,樊英姿,孙 健. 三维打印制备钛/羟基磷灰石复合体及功能梯度材料[J]. 中国组织工程研究, 2013, 17(29): 5364-5370.
Qian Chao, Fan Ying-zi, Sun Jian . Three-dimensional printing of titanium/hydroxyapatite composite and functionally graded materials[J]. Chinese Journal of Tissue Engineering Research, 2013, 17(29): 5364-5370.

图3为三维打印成形后的钛/羟基磷灰石功能梯度初胚,可见结构清晰两层不同材料的结合,两者间有明显的分界,两种材料结合部位无断裂,无裂纹缺损。

图4为烧结后的钛/羟基磷灰石功能梯度样品,肉眼可见样品明显分成了两层色泽不同的结构:上部为100%钛功能梯度层,表面呈现银灰色,其结构较为致密;下部为80%钛/20%羟基磷灰石复合功能梯度层,其颜色较上层较为暗淡,表面呈现黑灰色,结构较为疏松,可见散在的细小孔隙。

2.2 80%钛/20%羟基磷灰石复合体及钛/羟基磷灰石功能梯度材料的显微结构 图5为80%钛/20%羟基磷灰石复合体初胚成型后在场发射电子显微镜下放大 10 000倍的表面显微结构,其表面为钛和羟基磷灰石复合粉末散在分布,结构较为疏松,存在着不规则的孔隙,无明显的晶体化规则结构。

图6为80%钛/20%羟基磷灰石复合体烧结后的表面显微结构,与烧结前相比,烧结后复合材料的晶化程度很高,可见明显结晶体,拥有一定的层次结构,结构变得致密,晶体间的孔隙减小。

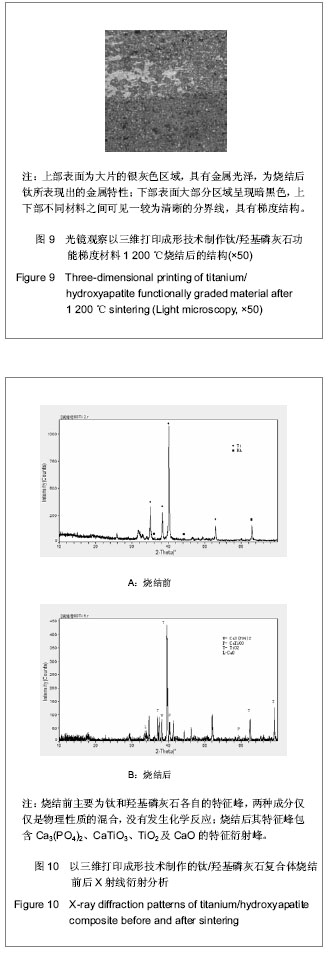
图7,8为烧结前后的80%钛/20%羟基磷灰石复合体放大100倍后的电镜图,烧结前其表面的结构排列疏松,存在大小不等的孔隙和裂隙,各个不同层次间连接不紧密,孔径为100-200 μm;烧结后仍存在不同大小的孔隙,其大小较烧结前有所减小,各个层次间结合加强,烧结后的孔径为50-150 μm。 图9为烧结后钛/羟基磷灰石功能梯度材料在50倍光学显微镜放大后的微观结构,其上部为100%钛功能梯度层,表面为大片的银灰色区域,具有金属光泽,为烧结后钛所表现出的金属特性;下部为80%钛/20%羟基磷灰石复合功能梯度层,表面大部分区域呈现暗黑色,两层不同材料之间可见一较为清晰的分界线,具有梯度结构。

2.3 80%钛/20%羟基磷灰石复合体X射线衍射分析 图10A显示烧结前80%钛/20%羟基磷灰石复合体X射线衍射主要为钛和羟基磷灰石各自的特征峰,两种成分仅仅是物理性质的混合,没有发生化学反应。图10B显示烧结后钛/羟基磷灰石复合材料X射线衍射,其特征峰包含Ca3(PO4)2,CaTiO3,TiO2,CaO的特征衍射峰,说明在钛/羟基磷灰石复合材料烧结过程中钛和羟基磷灰石发生了化学反应,从而产生了Ca3(PO4)2,CaTiO3,TiO2,CaO等新的化合物。
2.4 80%钛/20%羟基磷灰石的抗压强度 80%钛/ 20%羟基磷灰石的抗压强度为(184.3±27.1) MPa。

| [1] Gibson LJ. The mechanical behaviour of cancellous bone. J Biomech.1985; 18(5): 317-328.[2] Liu QB,Leu MC,Schmitt SM. Rapid prototyping in dentistry: technology and application.Int J Adv Manuf Technol.2006; 29(3): 317-335.[3] Wen CE,Mabuchi M,Yamada Y,et al. Processing of biocompatible porous Ti and Mg. Script Material.2001;45(10): 1147-1153.[4] Chen YJ,Feng B,Zhu YP,et al.Fabrication of porous titanium implants with biomechanical compatibility.Mater Lett.2009; (63): 2659-2661.[5] Szilvia E,Dermot B,Stefan L,et al.Selective laser sintering of hydroxyapatite/poly-ε-caprolactone scaffolds.Acta Biomater. 2010;6: 2511-2517.[6] Li LH,Kommareddy KP,Pilz C,et al.In vitro bioactivity of bioresorbable porous polymeric scaffolds incorporating hydroxyapatite microspheres. Acta Biomater.2010;6(7): 2525-2531.[7] Ning CQ,Zhou Y.On the microstructure of biocomposites sintered from Ti, HA and bioactive glass.Biomaterial.2004; 25(17):3379-3387.[8] Salman S,Gunduz O,Yilmaz S,et al. Sintering effect on mechanical properties of composites of natural hydroxyapatites and titanium.Ceram Int. 2009;35(7): 2965-2971.[9] Pompe W,Worch H,Epple M,et al. Functionally graded materials for biomedical applications. Mater Sci Eng A.2003;362(1-2):40-60. [10] Hedia HS,Mahmoud NA.Design optimization of functionally graded dental implant. Biomed Mater Eng.2004;14(2): 133-143.[11] Lin D,Li Q,Li W,et al.Functionally Graded Dental Implant and Its Effect on Bone Remodeling.Advanced Mater Res. 2008; 47-50:1035-1038.[12] Azari A,Nikzad S. The evolution of rapid prototyping in dentistry:A review. Rapid Prototyping J.2009;15(3):216-225.[13] Lam CXF,Mo XM,Teoh SH,Scaffold development using 3D printing with a starch-based polymer. Mater Sci Eng C.2002; 20(1-2):49-56.[14] Kieback B,Neubrand A,Riedel H.Processing techniques for functionally graded materials. Mater Sci Eng A.2003;362(1): 81-105.[15] Chu C,Zhu J,Yin Z,et al.Structure optimization and properties of hydroxyapatits-Ti symmetrical functionally graded biomaterial. Mater Sci Eng A.2001;A316:205-210.[16] Watari F,Yokoyama A,Saso F,et al.Fabrication and properties of functionally graded dental implant.Comp Part B Eng. 1997;28(1):5-11.[17] Ning CQ,Zhou Y. Correlations between the in vitro and in vivo bioactivity of the Ti/HA composites fabricated by a powder metallurgy method.Acta Biomater.2008;4(6): 1944-1952.[18] 宁聪琴,周玉,孟庆昌.50Ti/HA生物材料的组织结构与体外生物活性[J].无机材料学报,2001,16(2): 263-268.[19] Hench L.Bioceramics.J Am Ceram Soc.1998;81(7): 1705-1728. [20] Tampieri A,Gelotti G,Szontagh F,et al.Sintering and characterization of HA and TCP bioceramics with control of their strength and phase purity. J Mater Sci Mater Med. 1997;8(1): 29-37.[21] 阮建明,邹俭鹏. HA-Ti和HA-BG-Ti复合生物材料的力学性能和微观结构[J].中国有色金属学报,2003,13(8): 1361-1367.[22] Kieback B,Neubrand A,Riedel H.Processing techniques for functionally graded materials. Mater Sci Eng A.2003; 362(1): 81-105.[23] Wang J,Shaw L.Fabrication of Functionally Graded Materials Via Inkjet Color Printing.J Am Ceram Soc.2006;89(10): 3285-3289. |
| [1] | 陈子扬, 蒲 锐, 邓 爽, 袁凌燕. 外泌体对运动介导胰岛素抵抗类疾病的调控作用[J]. 中国组织工程研究, 2021, 25(25): 4089-4094. |
| [2] | 江小燕, 朱海飞, 蔺海旗, 林文弢. 冷疗干预延迟性肌肉酸痛的自限性恢复[J]. 中国组织工程研究, 2021, 25(23): 3609-3613. |
| [3] | 解景舒, 张祥林, 刘金磊, 文 静. High Resolution精密断层重建在中、内耳CT扫描成像中的应用[J]. 中国组织工程研究, 2021, 25(23): 3614-3618. |
| [4] | 刘金伟, 陈允震, 万春友. 应力作用下骨不连断端组织中成骨因子的变化[J]. 中国组织工程研究, 2021, 25(23): 3619-3624. |
| [5] | 罗安玉, 刘瀚霖, 谢小飞, 黄 琛. 抗氧化合剂对膝骨关节炎模型大鼠结构性退变的作用[J]. 中国组织工程研究, 2021, 25(23): 3625-3629. |
| [6] | 周 武, 王彬娉, 王雅雯, 程亚楠, 黄谢山. 转化生长因子β和骨形成蛋白2联合诱导小鼠成骨细胞系MC3T3-E1细胞的增殖与分化[J]. 中国组织工程研究, 2021, 25(23): 3630-3635. |
| [7] | 高 坤, 陈大宇, 张 勇, 刘伟东, 孙淑芬, 赖文强, 马笃军, 吴益宏, 林展鹏, 蒋鹰鹭, 余伟吉. 牛膝醇提物调控滑膜成纤维细胞外泌体抑制软骨细胞外基质降解[J]. 中国组织工程研究, 2021, 25(23): 3636-3640. |
| [8] | 梁美富, 曲淑华. 依据反向传播神经网络建模预测骨骼肌的最佳功率负荷[J]. 中国组织工程研究, 2021, 25(23): 3641-3647. |
| [9] | 白胜超, 高 扬, 王 博, 李俊平, 王瑞元. 针刺干预大负荷运动损伤模型大鼠骨骼肌线粒体功能的动态变化[J]. 中国组织工程研究, 2021, 25(23): 3648-3653. |
| [10] | 杨彩会, 刘启成, 董 明, 王丽娜, 左美娜, 陆 颖, 牛卫东. 丝氨酸/苏氨酸蛋白激酶促进慢性根尖周炎模型小鼠的骨破坏[J]. 中国组织工程研究, 2021, 25(23): 3654-3659. |
| [11] | 范军朝, 陈 勇, 宋俊杰. 七氟醚联合氙气预处理对脊髓缺血再灌注损伤模型大鼠的保护作用[J]. 中国组织工程研究, 2021, 25(23): 3660-3665. |
| [12] | 左振魁, 韩佳瑞, 计树灵, 贺璐璐. 银杏酮酯预处理减轻辐射所致模型小鼠的急性肠损伤[J]. 中国组织工程研究, 2021, 25(23): 3666-3671. |
| [13] | 张 亮, 马晓燕, 王佳虹. 肾衰饮调控慢性肾功能衰竭大鼠肾脏细胞凋亡的机制[J]. 中国组织工程研究, 2021, 25(23): 3672-3677. |
| [14] | 程亚楠, 吴毓聪, 毛秋华, 陈 灵, 陆丽英, 徐 普. 渗透树脂联合生物活性玻璃修复脱矿牙釉质的效果及稳定性[J]. 中国组织工程研究, 2021, 25(22): 3522-3526. |
| [15] | 毕庆伟, 刘承璞, 李 岩, 赵雯雯, 韩 梅. 两种离心程序制备的富血小板纤维蛋白结构分析[J]. 中国组织工程研究, 2021, 25(22): 3534-3539. |
设计:样本计算机辅助设计、快速成形技术制作。
三维打印制备钛/羟基磷灰石复合体及功能梯度材料实验的材料:
.jpg)
主要观察指标:烧结前后钛/羟基磷灰石复合体和钛/羟基磷灰石功能梯度材料的显微结构,X射线衍射分析和抗压强度检测结果。
1传统压模成形法制备的钛/羟基磷灰石复合材料结构简单,自动化程度较低,难以控制材料的孔隙率及孔径,不能满足多样化需求。实验拟运用三维打印成形技术制备钛/羟基磷灰石复合体和钛/羟基磷灰石功能梯度材料,并进行初步的力学性能与微观组织结构检测,为进一步的研究提供理论依据。 2为避免钛由于温度过低而无法与羟基磷灰石相结合,羟基磷灰石由于温度过高而产生分解,导致钛和羟基磷灰石的结合程度下降,影响烧结后强度的问题,实验选择1 200 ℃作为烧结温度。 3运用传统的方法无法制备出符合要求的功能梯度复合体,实验将数字化的三维打印技术创新应用于钛/羟基磷灰石复合体及功能梯度材料的制作中,评价其可行性,获得的复合体及功能梯度材料的微观结构和力学性能满足医用生物植入材料的要求。
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||