Chinese Journal of Tissue Engineering Research ›› 2026, Vol. 30 ›› Issue (19): 5007-5014.doi: 10.12307/2026.218
Previous Articles Next Articles
Stem cell-derived exosomes modulate the inflammatory microenvironment and enhance regenerative capacity of oligodendrocytes
Zhang Xixian
- College of Basic Medicine and Forensic Medicine, Henan University of Science and Technology, Luoyang 471000, Henan Province, China
-
Received:2025-08-25Accepted:2025-11-09Online:2026-07-08Published:2026-02-24 -
About author:College of Basic Medicine and Forensic Medicine, Henan University of Science and Technology, Luoyang 471000, Henan Province, China -
Supported by:Key Scientific Research Project of Henan Province Higher Education (Basic Research Project), No. 24A360016 (to ZXX)
CLC Number:
Cite this article
Zhang Xixian. Stem cell-derived exosomes modulate the inflammatory microenvironment and enhance regenerative capacity of oligodendrocytes[J]. Chinese Journal of Tissue Engineering Research, 2026, 30(19): 5007-5014.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
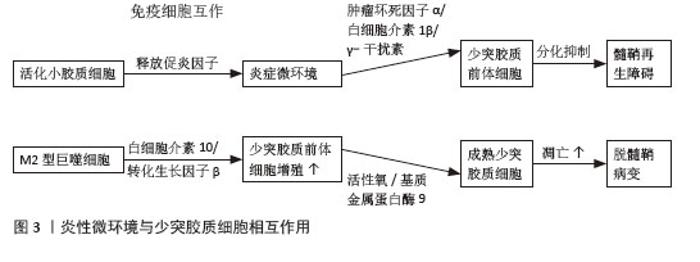
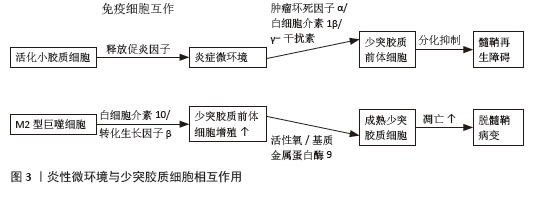
2.1 炎性微环境对少突胶质细胞修复的调控作用 2.1.1 少突胶质细胞在神经修复再生中的作用 少突胶质细胞通过生成髓磷脂以确保神经信号的高效传导,在维持轴突代谢和结构完整性中扮演着关键角色。少突胶质细胞通过轴突-髓鞘“突触”相互作用释放各种因子来给予神经元营养支持以及控制轴突生长信号。少突胶质细胞主要来源于少突胶质前体细胞和脑室下区衍生的神经干细胞,其中少突胶质前体细胞驱动的髓鞘再生过程分为3个步骤[6-8]:少突胶质前体细胞激活、增殖迁移和分化;首先脱髓鞘发生后激活为有丝分裂活跃状态并上调单羧酸转运蛋白1、性别决定区盒基因、少突细胞转录因子1/2、同源结构域蛋白NK2同源盒2等促进增殖、分化、成熟的正向基因表达以启动再生程序;其次损伤微环境中的活化神经胶质细胞感知损伤时,通过释放血小板衍生生长因子等有丝分裂原刺激少突胶质前体细胞增殖,同时通过清除髓鞘碎片分泌趋化因子引导少突胶质前体细胞向病灶定向迁移;随后在轴突电活动及表面分子的引导下,以及在脑源性神经营养因子等促分化因子、转录因子及Wnt/β-catenin信号通路、磷脂酰肌醇-3-激酶/蛋白激酶B/哺乳动物雷帕霉素靶蛋白等多信号通路调控下分化为成熟少突胶质细胞,完成髓鞘膜层状螺旋包裹与致密结构重塑,最终形成多层髓鞘结构。该过程每个阶段均受微环境信号分子与细胞内在基因程序的精密调控。 2.1.2 炎性微环境对少突胶质细胞修复的作用 炎性微环境既可以促进神经组织修复,也可以阻碍神经细胞再生。从细胞组成来看,炎性微环境主要包含促炎的M1型小胶质细胞/巨噬细胞和辅助性T细胞17(Thelper cell 17,Th17),以及抗炎的M2型小胶质细胞/巨噬细胞、淋巴细胞。在炎性微环境损伤早期,M1型细胞通过分泌肿瘤坏死因子α、白细胞介素1β和活性氧簇等递质清除细胞碎片;而在修复期,M2型细胞则通过分泌白细胞介素10、转化生长因子β等因子促进组织修复。从分子层面分析,促炎因子如肿瘤坏死因子α和白细胞介素1β可通过激活核因子κB信号通路抑制少突胶质前体细胞的分化;而γ-干扰素则通过上调MHCⅡ类分子表达增强免疫反应;抗炎因子如白细胞介素10、转化生长因子β不仅能抑制过度炎症,还能直接促进少突胶质前体细胞的成熟和髓鞘形成[9-12]。研究表明,炎性微环境与少突胶质细胞修复能力的动态平衡是决定神经损伤修复的关键因素。适度的炎症反应可以促进少突胶质前体细胞的增殖和迁移,而过度或持续的炎症反应则抑制少突胶质前体细胞分化和髓鞘形成能力[13-14]。例如,肿瘤坏死因子α可通过核因子κB信号通路抑制少突胶质前体细胞向成熟少突胶质细胞的分化。同时,炎性微环境中活性氧簇的积累也会对少突胶质细胞造成氧化损伤,进一步阻碍髓鞘修复,导致神经缺损功能难以恢复。值得注意的是,炎性微环境中的免疫细胞如M1型小胶质细胞和Th1细胞主要发挥促炎作用,而M2型小胶质细胞和调节性T细胞则具有抗炎和促修复功能[15-16]。因此,通过调节炎性微环境可以有效影响少突胶质细胞的修复活性,见图3。"
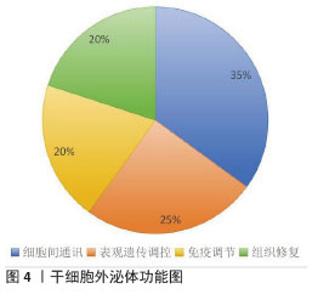
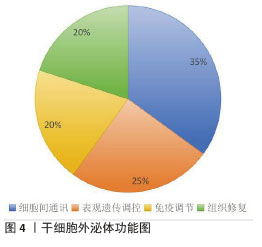
研究显示,虽然脑梗死区的损伤是不可逆的,但是脑梗死后异常微环境带来的继发性损伤是可以控制的。脑缺血后局部炎症微环境迅速形成,这是由激活的小胶质细胞、星形胶质细胞以及浸润的外周免疫细胞共同作用的结果。小胶质细胞首先被激活,释放出炎症因子,从而触发炎症反应。它们能够通过细胞因子信号进一步激活星形胶质细胞,导致炎症反应放大。早期转录组研究揭示了星形胶质细胞的两种基因表达模式:A1神经毒性表型和A2神经保护性表型。急性脑卒中激发了2条免疫级联瀑布:一条是为对抗缺血性脑损伤后释放的中枢神经系统自身抗原所发生的自身免疫反应,其结局是产生脑组织炎症,导致缺血区脑组织破坏;另一条是迅速、严重而且持久的外周免疫抑制即“脑卒中诱导的免疫抑制”。激活的小胶质细胞/巨噬细胞对神经发生也有损伤和促进的双重作用,促进脑损伤后小胶质细胞/巨噬细胞从M1型向M2型转化为脑损伤的治疗提供了一个新思路。恶化的脑梗死区微环境不仅导致迁移到梗死部位的干细胞数量和质量降低,也使组织细胞的再生和修复能力下降。通过调节干细胞源性外泌体的分泌可干预脑梗死后的细胞或组织周围微环境,抑制核因子κB的活化,降低炎症因子表达水平,进而抑制炎性和促纤维化途径的激活,通过激活核因子κB/NOD样受体热蛋白结构域相关蛋白3(NOD-like receptor thermal protein domain associated protein 3,NLRP3)炎症小体信号通路可影响干细胞源性外泌体中携带蛋白质、DNA、mRNAs、miRNAs、长链非编码RNA和环状RNA等成分变化[17-18],促使新生神经元与周围环境中的神经细胞建立有生物功能的突触联系,实现正常突触连接、释放神经递质及发挥正常神经元的功能。 2.2 干细胞源性外泌体的生物学特性 干细胞源性外泌体是由干细胞分泌的直径30-150 nm的细胞外囊泡,从分子构成来看,干细胞源性外泌体携带的活性成分主要包括3大类:核酸(miRNA和长链非编码RNA等)、蛋白质(生长因子、细胞因子和功能酶等)以及脂质(胆固醇、鞘磷脂和磷脂酰丝氨酸等);在递送机制方面,干细胞源性外泌体主要通过内吞作用、膜融合和配体-受体相互作用3种方式被靶细胞摄取;在生物标志物方面,主要有四跨膜蛋白家族成员(CD9、CD63、CD81)、热休克蛋白(热休克蛋白70、热休克蛋白90)以及参与膜运输的蛋白TSG101。研究显示:干细胞源性外泌体不仅保留了干细胞的治疗特性,如抗炎和组织修复能力,而且避免了直接使用干细胞可能带来的风险,如免疫排斥和肿瘤形成等,见图4。值得注意的是,与其他细胞来源外泌体相比,间充质干细胞源性外泌体具有独特的治疗优势:①保留干细胞的多种生物活性;②表面分子可延长体内循环时间;③纳米级尺寸利于穿越血脑屏障;④内容物可经工程化改造增强靶向性。动物实验证实,静脉注射的外泌体能够穿过血脑屏障,优先聚集在损伤部位,同时外泌体介导的信号传递可协调不同细胞类型的反应,这些特性使干细胞源性外泌体表现出更丰富的内容物组成和更强的组织修复能力,参与细胞间通讯、免疫调节、组织修复等多种生理和病理过程。 "
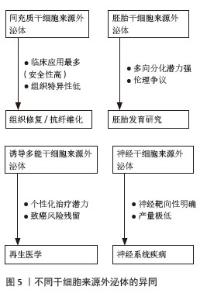
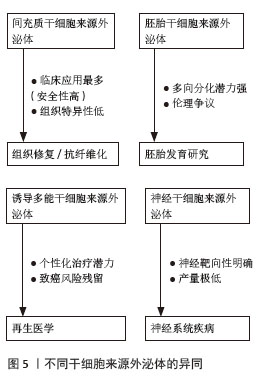
2.3 不同干细胞来源外泌体生物学特性的异同 不同干细胞来源外泌体在生物学特性、功能作用和应用潜力上存在显著差异,它们都携带来源细胞的特定蛋白质、核酸和脂质,均可以通过介导细胞间通讯,发挥免疫调节、组织修复、抗纤维化、抗凋亡、促血管生成等多种生物学效应。 间充质干细胞来源外泌体主要特点:①强大的免疫调节能力,这是间充质干细胞源外泌体最突出的特性;②显著的组织修复与再生能力,通过传递促血管生成因子促进血管新生;通过传递抗凋亡因子保护受损细胞;通过传递调节因子促进成骨、成软骨、成神经分化等;③抗纤维化:能抑制肝、肺、肾等器官的纤维化进程;④抗凋亡,保护多种组织细胞免受损伤诱导的凋亡;⑤低免疫原性与高安全性,且无细胞移植带来的潜在致瘤性和栓塞风险,临床应用安全性相对较高。间充质干细胞来源外泌体来源广泛、安全性高,是目前研究和应用最广泛、最接近临床转化的干细胞外泌体类型。 胚胎干细胞来源外泌体作用特点:①强大的促增殖与再生潜力,携带大量维持干细胞多能性和促进快速增殖的因子[19-20];②潜在的分化能力,可能携带引导特定分化的信号;③心肌保护与修复能力,在心肌梗死模型中显示出促进心肌细胞存活、减少瘢痕、改善心功能的作用;④对神经细胞有保护作用,促进神经再生。胚胎干细胞来源外泌体涉及人类胚胎,具有潜在的致瘤性风险。 诱导多能干细胞来源外泌体作用特点:携带多能性因子,具有促进细胞增殖、组织修复和再生的能力。在心肌修复、神经保护、皮肤再生等方面有报道。诱导多能干细胞外泌体来源于患者自身细胞,理论上无免疫排斥,但有致瘤性风险[21-22]。 其他组织特异性干细胞/祖细胞来源外泌体:神经干细胞来源外泌体富含神经相关因子,在促进神经突触生长、神经保护(如抗氧化、抗凋亡)、调节神经炎症方面有独特优势,应用于脑卒中、脊髓损伤、神经退行性疾病(如阿尔茨海默病、帕金森病)的研究较多。心脏祖细胞来源外泌体富含心脏发育和修复相关因子,在促进心肌细胞存活、增殖、血管新生、改善心脏功能方面有针对性效果,是心肌修复研究的热点。造血干细胞来源外泌体参与造血微环境的调节,影响造血干细胞的自我更新和分化[23-25]。见图5。 "
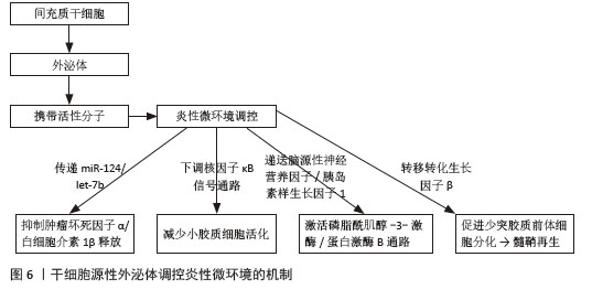
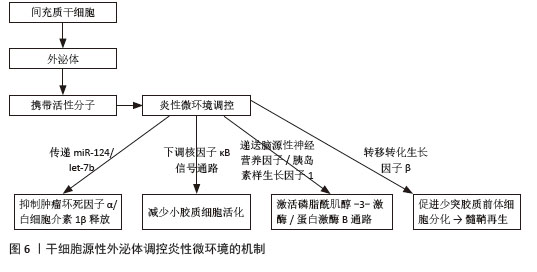
2.4 干细胞源性外泌体调控炎性微环境的机制 干细胞源性外泌体内含的miRNA、mRNA、长链非编码RNA、脂质及代谢产物等多元活性分子,共同构建了髓鞘生成原料的“双向调控枢纽”[26-27]。研究表明,在正常微环境状态下,干细胞源性外泌体通过与相邻细胞、细胞基质及多种细胞因子和激素相互作用,维持正常的自我更新能力,参与脑组织的再生和修复。异常的微环境会导致神经细胞凋亡因子、髓鞘轴突再生抑制因子的过度分泌,使细胞信号转导紊乱加速,导致细胞凋亡、衰老。干细胞源性外泌体作为一种潜在的无细胞治疗方式具有强大的免疫调节特性及旁分泌能力,可通过膜表面整合素等蛋白靶向少突胶质前体细胞实现特异性结合;或直接穿过血脑屏障作用于少突胶质前体细胞和损伤区域;亦能递送miRNA介导基因表达改善炎症微环境将炎症控制在“适度”水平,这种结构-功能偶联的双向调控特性,对减轻炎症反应及促进髓鞘再生具有重要意义[28-29]。 干细胞源性外泌体通过多种分子途径精确调控炎性微环境,其中miRNA递送是最重要的机制之一。研究表明,间充质干细胞外泌体富含的miR-124可通过靶向Toll样受体4信号通路抑制小胶质细胞活化;而miR-17-92簇则通过调控磷酸酶和张力蛋白同源物/蛋白激酶B通路促进M2型巨噬细胞极化。间充质干细胞来源外泌体中的miR-146a可通过靶向肿瘤坏死因子受体相关因子6/核因子κB信号通路抑制炎症反应;miR-21则通过调节程序性细胞死亡因子4/激活蛋白1通路减少促炎因子的产生。这些miRNA能在转录后水平调节数百种炎症相关基因的表达,形成广泛的调控网络。干细胞源性外泌体可以直接中和促炎因子或激活抗炎信号通路,有研究表明,神经干细胞来源外泌体含有转化生长因子β、白细胞介素10等抗炎因子,能够抑制小胶质细胞的过度激活并促进其向M2型极化。干细胞源性外泌体对免疫细胞功能的调控是调节炎性微环境的另一重要机制。外泌体通过传递特定信号分子影响T细胞亚群的分化和功能,如促进Treg细胞的增殖和抑制Th17细胞的活化,神经干细胞来源外泌体携带的转化生长因子β可直接抑制T淋巴细胞活化,Galectin-1则通过诱导T细胞凋亡减轻炎症反应。同时,外泌体还能调节巨噬细胞/小胶质细胞的极化状态,增加M2型细胞的比例,从而减轻炎症反应并促进组织修复。见图6。 "
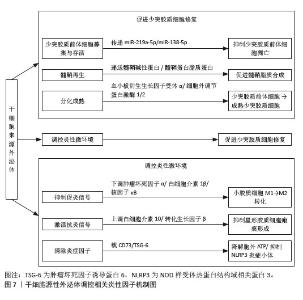
2.5 干细胞源性外泌体调控少突胶质细胞修复的机制 干细胞源性外泌体作为一种新型的细胞间通讯媒介,通过调控炎性微环境为少突胶质细胞修复创造了有利条件,作用机制涉及多种分子途径,包括miRNA介导的信号通路调节、抗炎因子分泌和免疫细胞功能调控等。这些机制共同促进了少突胶质前体细胞的增殖、分化和髓鞘形成。 2.5.1 干细胞源性外泌体调节炎性因子对少突胶质细胞修复活性的影响 在正常微环境状态下,干细胞源性外泌体通过与相邻细胞、细胞基质及多种细胞因子和激素相互作用,维持正常的自我更新能力,参与脑组织的再生和修复。异常的微环境会导致神经细胞凋亡因子、髓鞘轴突再生抑制因子的过度分泌。异常微环境不仅参与炎症介导的病理性损伤,而且参与“保护性自身免疫”。免疫微环境一方面促进少突胶质细胞再生,另一方面又抑制炎症反应减轻继发性病理损伤,为髓鞘修复提供适宜的修复环境。M1型巨噬细胞/小胶质细胞和T细胞均可分泌促炎细胞因子并相互活化,形成的炎症级联反应是导致少突胶质前体细胞分化受阻的核心机制之一。首先小胶质细胞经Toll样受体识别有害刺激后通过核因子κB核转位驱动M1型极化,分泌主导性炎症因子肿瘤坏死因子α和γ-干扰素并分别激活Caspase级联反应、FasR表达和内质网应激直接损伤少突胶质细胞;而M1型小胶质细胞可有效将高表达的组织相容性复合体分子和共刺激分子递呈给CD4?T细胞并大量增殖分化为Th1细胞、Th17细胞,经细胞间接触分泌γ-干扰素、白细胞介素17等促炎因子反向激活巨噬细胞、小胶质细胞释放毒性物质,迅速形成持续性正反馈炎症环路,加剧少突胶质细胞损伤及抗原释放,最终导致抗原扩散-脱髓鞘恶性循环[30-32]。而M2型小胶质细胞可分泌白细胞介素4、白细胞介素10及转化生长因子β等并介导信号转导和转录活化因子6磷酸化释放抗炎因子,抑制M1型活化并促进Th2、Treg细胞应答从而减少炎症对髓鞘的攻击。LI等[33]研究发现干细胞源性外泌体通过调控免疫细胞表型极化来减轻炎症反应和脱髓鞘损伤:一方面下调M1型巨噬细胞/小胶质细胞等炎症因子释放及标志物表达;另一方面上调M2型巨噬细胞/小胶质细胞表达来调控表型转换,从而减弱M1型细胞复杂的级联反应,最终构建炎症抑制性微环境,促进轴突再生和髓鞘保留实现了神经功能的保护性修复。ZHANG等[34]研究发现干细胞源性外泌体通过双重机制改善神经炎症和促进神经修复:既通过阻断Toll样受体2/ 丝氨酸/苏氨酸蛋白激酶1/核因子κB信号通路抑制M1型极化,减少下游炎症因子释放,又能增加抗炎修复M2型小胶质细胞转化,进而促进髓鞘再生,恢复神经信号的正常传导功能。另有研究发现人脂肪间充质干细胞来源外泌体对T细胞亚群分化具有显著的免疫靶向调节作用,能够快速下调致病性Th1和Th17细胞比例,并同步减少γ-干扰素、白细胞介素17A炎症因子含量,抑制炎症正反馈通路,继而调控髓鞘修复微环境促进髓鞘再生[35-37],见图7。 "
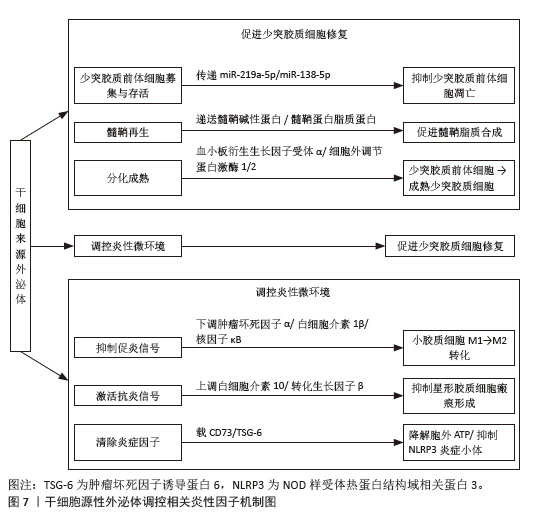
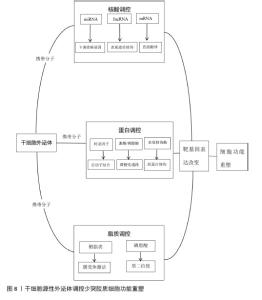
最新研究发现:当过量的髓鞘碎片因延迟清除而异常积累时,其作为炎症刺激物不仅会触发持续性炎症反应干扰少突胶质前体细胞功能,还会加剧二次免疫应答;此时M2型小胶质细胞通过主动吞噬清除这些病理产物来维持微环境稳态,而在小胶质细胞吞噬功能耗竭的情况下,巨噬细胞则会启动代偿性吞噬机制以处理残余的髓鞘碎片,为髓鞘再生提供空间。研究显示,在实验性变态反应性脑脊髓炎小鼠模型中敲除miR-223表现出髓鞘碎片清除障碍和再生功能受损[38-39];反之外源性补充miR-223可通过特异性激活M2型巨噬细胞/小胶质细胞及吞噬碎片功能,进而促进神经系统髓鞘再生。此外,通过分选神经系统驻留细胞群体发现miR-146a在小胶质细胞中特异性高表达,敲除实验发现miR-146a缺失会显著抑制小胶质细胞的吞噬碎片功能,加剧脱髓鞘发生,潜在机制可能是与Toll样受体4/核因子κB信号通路的激活有关。MECHA等[40]研究发现干细胞源性外泌体可以促进具有胶原结构的巨噬细胞受体表达,通过增强巨噬细胞对髓鞘碎片的识别吞噬能力,显著提升损伤部位碎片清除效率,从而为髓鞘再生创造有利的微环境。 值得注意的是,缺血条件下的小胶质细胞和星形胶质细胞展现出双重作用。M1型小胶质细胞加剧缺血引起的炎症反应,而M2型小胶质细胞促进少突胶质细胞的分化与髓鞘形成。同样,C3阳性(神经毒性)星形胶质细胞通过释放促炎细胞因子抑制少突胶质前体细胞的分化,而PTX3免疫蛋白阳性(神经保护)星形胶质细胞则通过释放营养因子和抗炎因子促进少突胶质细胞的成熟。随着脑内微环境信号的变化,小胶质细胞的表型可动态转化。例如,在髓鞘期间小胶质细胞可以从一氧化氮合酶/白细胞介素1β阳性(神经毒性)亚型转变为巨噬细胞CD206/精氨酸酶1阳性(神经保护)亚型,这种转变能有效促进少突胶质细胞的分化。总结来说,抑制过度炎症反应并促进神经保护型胶质细胞极化是支持脑缺血后少突胶质细胞形成的重要策略。 综上,外泌体通过双重协同机制调控少突胶质细胞活性参与神经修复:在分子层面,外泌体作为多功能信号载体通过递送miRNA、功能蛋白及相关基因或靶向调控Wnt/β-catenin、磷脂酰肌醇-3-激酶/蛋白激酶B/哺乳动物雷帕霉素靶蛋白和髓鞘碱性蛋白等关键信号通路的动态平衡,从而调节少突胶质前体细胞的定向迁移、增殖及终末分化;在微环境层面,外泌体通过抑制神经炎症、促进损伤碎片清除及重塑免疫细胞表型,构建出有利于髓鞘再生的微环境稳态,从而缓解炎症浸润及脱髓鞘等病理现象。 2.5.2 干细胞源性外泌体调控关键基因表达 神经修复与再生过程受正负调控基因的动态平衡控制,每个基因有不同的作用途径。正向调控方面:单羧酸转运蛋白1主要在少突胶质细胞中表达,通过运输乳酸和丙酮酸为轴突提供腺苷三磷酸和脂质合成所需的能量与物质基础。性别决定区盒基因10与少突细胞转录因子处于调控少突胶质前体细胞终末分化和髓鞘形成的前馈循环层级上游[41-43],通过调控少突胶质前体细胞增殖和少突胶质细胞分化,进而构建促分化的转录微环境增强髓鞘生成。而少突细胞转录因子2可靶向干扰Smad信号通路,抑制基因表达,直接驱动髓鞘碱性蛋白、髓磷脂相关糖蛋白等相关基因的表达和少突胶质细胞分化。负向调控方面,性别决定区盒基因6和Hes5通过竞争结合位点抑制分化激活因子性别决定区盒基因10的功能,协同阻滞细胞过早向成熟阶段分化并抑制髓鞘相关基因表达,形成双重负向调控机制以维持细胞前体的稳态。 不同来源外泌体可直接或间接靶向促进相关基因表达,协同驱动少突胶质前体细胞分化和成熟:在铜酮诱导的动物模型中发现,人脂肪间充质干细胞来源外泌体治疗后胼胝体出现髓鞘再生现象,显著改善了中毒后小鼠的运动功能障碍,分子机制是表达更高水平的少突胶质细胞谱系相关基因(少突细胞转录因子2、髓鞘碱性蛋白和髓磷脂相关糖蛋白等),使少突胶质细胞开始增殖,进一步增加髓鞘厚度和促进损伤区域修复。miR-23a和miR-23b均能够以剂量依赖方式负向调控核纤层蛋白B1的表达,进而明显提高髓鞘碱性蛋白和髓鞘少突胶质细胞糖蛋白的合成量,解除对髓鞘形成的阻碍作用,加快少突胶质细胞发育,最终促进神经系统髓鞘形成。 2.5.3 调控多种信号通路 缺血后形成的炎症微环境在一定条件下可以抑制或促进少突胶质细胞的分化与成熟。多种信号通路如磷脂酰肌醇-3-激酶/蛋白激酶B/哺乳动物雷帕霉素靶蛋白、Wnt/β-catenin等在脑缺血后少突胶质细胞生成过程中发挥了关键作用。 Wnt信号通路:髓鞘生成调控经典通路(糖原合成酶激酶3/β-catenin和Wnt7/β-catenin)可促进干细胞分化并正向调控髓鞘形成;非经典通路(Wnt5a-Ca2?/RhoA)通过调控细胞运动与极性抑制髓鞘生成,其中T-box转录因子1作为一种转录因子桥接2条Wnt通路的功能,并通过3′非翻译区与miRNA互作形成双向调控枢纽,负向关联髓鞘蛋白表达;而Wnt7/β-catenin信号通路能够有效逆转Tbr1诱导的轴突缺陷。QIN等[44]研究发现,人脂肪间充质干细胞来源外泌体以剂量依赖性促进少突胶质前体细胞分化标志物表达,且外泌体递送的miR-23a-3p不仅能够抑制Wnt5a表达,亦可直接靶向抑制Tbr1,进而提高Wnt7a/b基因和髓鞘少突胶质细胞糖蛋白、髓鞘碱性蛋白等髓磷脂相关蛋白表达,促进髓鞘再生,增加髓鞘密度,有利于神经功能恢复。相反,研究发现miR-27a通过下游靶标APC或糖原合成酶激酶3β调控髓鞘形成和再生过程,亦可明显增加下游NKD1水平,抑制β-catenin核定位,阻碍其正常进入细胞核,形成了一种负反馈机制,导致Wnt/β-catenin信号通路对少突胶质细胞分化成熟的积极影响被抑制,降低髓鞘再生效率。 髓鞘碱性蛋白信号通路:纤维蛋白原介导的骨形态发生蛋白4是少突胶质前体细胞分化的重要负调节因子,与Ⅰ型和Ⅱ型受体结合后形成异四聚体复合物获得活性后促进SMAD1/5/8磷酸化,并与SMAD4形成复合物转移至细胞核内,直接上调Id1/2蛋白表达与少突细胞转录因子1/2 结合,从而抑制少突胶质前体细胞向少突胶质细胞分化,可见该通路激活是髓鞘再生的关键阻碍。HOU等[45]研究发现外泌体miR-128-3p既能上调髓鞘碱性蛋白表达促进少突胶质前体细胞分化为少突胶质细胞,又可通过特异性抑制髓鞘碱性蛋白信号通路拮抗纤维蛋白原对髓鞘的破坏作用,形成“抑制分化阻碍+激活成熟驱动”的双向分化正性调控机制,从而促进髓鞘再生,减少梗死面积。 磷脂酰肌醇-3-激酶/蛋白激酶B/哺乳动物雷帕霉素靶蛋白信号通路:介导胆固醇形成正性依赖性互作机制支持髓鞘基因表达和轴突鞘构建。胆固醇形成膜微结构域作为信号分子平台富集酪氨酸激酶受体后激活哺乳动物雷帕霉素靶蛋白和蛋白激酶B信号通路,前者促进髓鞘碱性蛋白生物合成,后者则驱动轴突鞘组装;上述通路激活后可活化甾醇调节元件结合蛋白转录因子,特异性结合胆固醇生物合成相关基因启动子区域,显著上调转录水平进而持续补充微结构域所需的胆固醇储备,维持髓鞘形成所需的胆固醇稳态和信号传导基础[46-47]。研究发现,miR-23a和间充质干细胞来源外泌体miR-17-92均可通过靶向抑制磷酸酶和张力蛋白同源物激活磷脂酰肌醇-3-激酶/蛋白激酶B/哺乳动物雷帕霉素靶蛋白信号通路,特异性增强髓鞘碱性蛋白等髓鞘结构蛋白水平,并促进胆固醇合成及相关基因表达,可见这种双重作用模式同步增强了髓鞘膜结构成分合成与胆固醇供给,有效保障了髓鞘膜的稳定生成[48-50],见图8。 综上可知,干细胞源性外泌体不仅提供髓鞘形成所需的脂质和蛋白质成分,还调节髓鞘相关基因的表达。一方面,它们提供髓鞘形成所需的脂质前体如胆固醇和鞘磷脂;另一方面,外泌体携带的髓鞘蛋白可作为模板促进新生髓鞘组装。外泌体激活相关通路能上调脂质合成相关基因表达,而哺乳动物雷帕霉素靶蛋白信号通路的激活则促进髓鞘蛋白的翻译,这种双重作用显著提高了髓鞘再生效率。 "
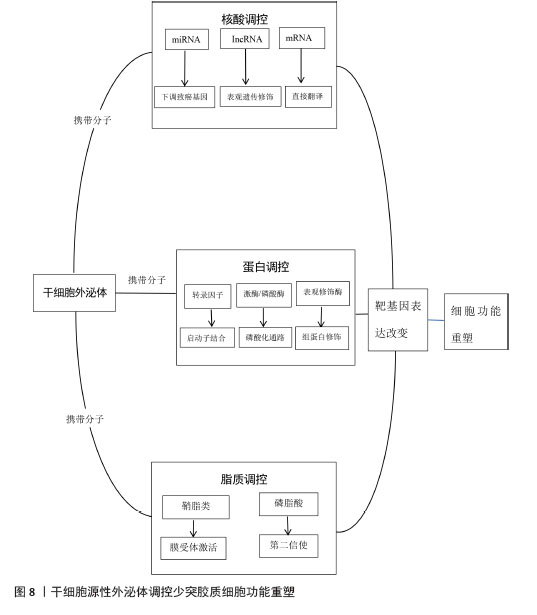
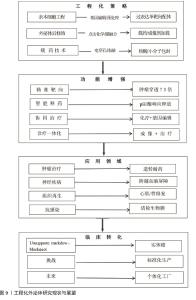
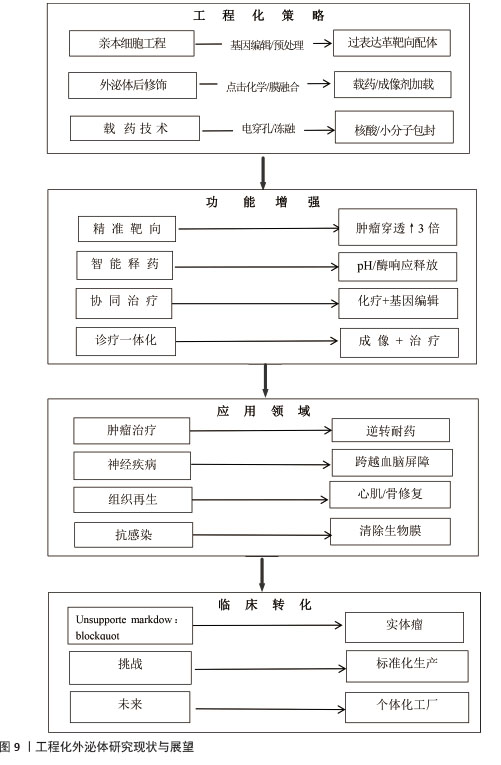
2.6 工程化外泌体:功能强化与精准治疗的新前沿 工程化外泌体通过主动修饰外泌体生物学特性(如靶向性、载药能力、稳定性),突破天然外泌体的局限性,在疾病治疗、药物递送和诊断领域展现出革命性潜力[51-52]。天然外泌体存在循环半衰期短、非特异性分布、载药效率低等缺陷,严重制约临床转化应用。针对这一瓶颈,目前通过采用靶向配体修饰技术对膜表面进行重构,提升循环稳定性和病灶靶向富集能力;功能化载药技术对外泌体内容物进行定向设计,突破递送精度壁垒、增强药物摄取效率构建多元化精准治疗模式。最新研究发现:通过外泌体功能化修饰技术能解决中药及活性成分治疗脑卒中的递送难题(如血脑屏障穿透、靶向病灶、全身不良反应),可以将大分子和治疗药物直接输送到损伤组织靶细胞,大幅提高缺血病灶部位的药物有效浓度[53-54],这为提高药物活性成分高效、精准递送,促进损伤组织再生和修复提供新的治疗策略。目前,构建功能化外泌体主要通过外泌体的表面修饰完成。外泌体的靶向修饰可以增强外泌体跨过生理屏障,实现外泌体载药对特定组织或器官的特异性递送,提高药物的递送效率和治疗效果[55]。 研究显示,c(RGDyK)肽是由精氨酸-甘氨酸-天门冬氨酸-D-酪氨酸-赖氨酸(cyclo rginine-glycineaspartate-D-tyrosine-lysine peptide)序列组成的短肽,是整合素与配体蛋白相互识别的位点,将cRGDyK修饰到骨髓间充质干细胞衍生外泌体表面,形成环(Arg-Gly-Asp-D-Tyr-Lys)肽c(RGDyK),可以提高外泌体的靶向性,可突破生理屏障实现靶向调控及髓鞘再生修复,为神经疾病治疗提供创新策略[56-57]。TIAN等[58]使用点击化学技术将c(RGDyK)肽接枝于间充质干细胞外泌体表面,发现间充质干细胞外泌体在静脉给药后可靶向至缺血性脑损伤部位;HE等[59]通过内源性负载技术对人胚肾细胞293进行工程化改造,成功制备高表达性别决定区盒基因的功能性外泌体,实验显示在脱髓鞘小鼠模型中,性别决定区盒基因高表达的功能性外泌体较未修饰外泌体不仅能特异性上调髓鞘碱性蛋白表达、增加髓鞘厚度,还可通过改善脱髓鞘微环境促进少突胶质细胞向成熟髓鞘分化,显著减轻胼胝体区域病理损伤。研究人员通过将神经生长因子及具有抗炎特性的姜黄素装载至M2型巨噬细胞外泌体之中,发现功能化外泌体具有出色的炎症调控能力与神经保护功能。HUANG等[60]装载沉默结缔组织生长因子基因小干扰RNA的间充质干细胞外泌体,并将这种外泌体尾静脉注射至脊髓损伤大鼠体内,发现间充质干细胞外泌体抑制了脊髓损伤区域神经元凋亡,促进了脊髓损伤大鼠运动功能恢复。 工程化外泌体与中药成分的整合研究仍处于探索阶段,为精准调控-协同增效-多点微调治疗提供新路径。中医药可以通过调控干细胞源性外泌体分泌、改善炎性微环境、促进损伤区抗炎-促炎平衡状态,促进少突胶质细胞参与神经修复与再生的全过程。六味地黄丸改良方补肾益髓方可通过调控外泌体多途径作用于靶点,展现促进髓鞘再生的独特药理机制:①促进miR-124并降低miR-155表达以调节靶基因水平,推动M1型小胶质细胞向M2型转化减轻神经炎症和脱髓鞘;②促进miR-15b-5p表达使其特异性结合Wnt3a mRNA阻碍翻译过程,降低Wnt3a、糖原合成酶激酶3、β-catenin表达以阶段依赖性抑制Wnt通路,促进少突胶质前体细胞分化和成熟并显著影响髓鞘形成;③促进miR-219、miR-338表达使得抑制性因子表达受阻,髓鞘碱性蛋白表达上调,从而加速少突胶质前体细胞分化并提升包裹轴突的能力[61-64],结果表明补肾益髓方通过整合微环境调控、前体细胞激活及髓鞘结构重建3个层面的治疗优势,系统促进髓鞘再生。GE等[65]基于点击化学技术将c(RKDyK)靶向肽偶联至外泌体表面构建靶向递送系统,成功实现姜黄素的药物负载,实验证实该复合体系较游离姜黄素或单纯外泌体治疗能更显著抑制脑损伤区域的炎症反应并降低细胞凋亡水平,展现出协同调控的治疗优势,见图9。 "
| [1] BUSCHAM TJ, EICHEL-VOGEL MA, STEYER AM, et al. Progressive axonopathy when oligodendrocytes lack the myelin protein CMTM5. Elife. 2022;11: e75523. [2] YIN X, KIDD GJ, OHNO N, et al. Proteolipid protein-deficient myelin promotes axonal mitochondrial dysfunction via altered metabolic coupling. J Cell Biol. 2016;215(4):531-542. [3] OSORIO-QUEREJETA I, SÁENZ-CUESTA M, MUÑOZ-CULLA M, et al. Models for Studying Myelination, Demyelination and Remyelination. Neuromolecular Med. 2017;19(2-3):181-192. [4] 皮桐昊,刘瑞琦,贾佳佳,等.外泌体在药物递送系统中的研究进展[J].中国药剂学杂志,2023, 21(5):250-262. [5] 居怡,SERAGAMANI HAMOOD ALI,施戈韬,等.外泌体作为药物递送载体的研究进展[J].药学进展,2023,47(11):804-816. [6] KALAFATAKIS I, KARAGOGEOS D. Oligodendrocytes and Microglia: Key Players in Myelin Development, Damage and Repair. Biomolecules. 2021;11(7):1058. [7] GARBERN JC, LEE RT. Heart regeneration: 20 years of progress and renewed optimism. Dev Cell. 2022;57(4):424-439. [8] MITREČIĆ D, HRIBLJAN V, JAGEČIĆ D, et al. Regenerative Neurology and Regenerative Cardiology: Shared Hurdles and Achievements. Int J Mol Sci. 2022;23(2):855. [9] DULAMEA AO. Role of Oligodendrocyte Dysfunction in Demyelination, Remyelination and Neurodegeneration in Multiple Sclerosis. Adv Exp Med Biol. 2017;958:91-127. [10] 黄春满,李丽薇,黄勇彬,等.外泌体靶向修饰的研究进展[J].科学通报,2023,68(33):4532-4543. [11] XIE F, HUANG Y, ZHAN Y, et al. Exosomes as drug delivery system in gastrointestinal cancer. Front Oncol. 2023;12:1101823. [12] XIE S, SUN W, FU T, et al. Aptamer-Based Targeted Delivery of Functional Nucleic Acids. J Am Chem Soc. 2023;145(14):7677-7691. [13] MILLÁN COTTO HA, PATHRIKAR TV, HAKIM B, et al. Cationic-motif-modified exosomes for mRNA delivery to retinal photoreceptors. J Mater Chem B. 2024;12(30):7384-7400. [14] LI X, QU S, OUYANG Q, et al. A multifunctional composite nanoparticle with antibacterial activities, anti-inflammatory, and angiogenesis for diabetic wound healing. Int J Biol Macromol. 2024;260(Pt 2):129531. [15] LI YJ, HE J, ZHANG QH, et al. Olig2-enriched exosomes: A novel therapeutic approach for cuprizone-induced demyelination. Neuroscience. 2024;555:41-51. [16] JIA Z, LIU J, LI B, et al. Exosomes with FOXP3 from gene-modified dendritic cells ameliorate the development of EAE by regulating the balance of Th/Treg. Int J Med Sci. 2022;19(8): 1265-1274. [17] TIMOFEEVA AM, PARAMONIK AP, SEDYKH SS, et al. Milk Exosomes: Next-Generation Agents for Delivery of Anticancer Drugs and Therapeutic Nucleic Acids. Int J Mol Sci. 2023;24(12):10194. [18] 曾文,尹贝立,谭文松,等.体外诱导间充质干细胞向成纤维细胞分化的研究[J].华东理工大学学报(自然科学版),2024,50(3):383-390. [19] 罗文彬,李若云,潘超凡,等.工程化外泌体修复组织损伤:应用潜力及优异的生物稳定性和靶向特异性[J].中国组织工程研究,2026, 30(1):204-217. [20] SADEGHI S, TEHRANI FR, TAHMASEBI S, et al. Exosome engineering in cell therapy and drug delivery. Inflammopharmacology. 2023; 31(1):145-169. [21] RAJPUT A, VARSHNEY A, BAJAJ R, et al. Exosomes as New Generation Vehicles for Drug Delivery: Biomedical Applications and Future Perspectives. Molecules. 2022;27(21):7289. [22] 徐煌.神经干细胞来源囊泡联合姜黄素治疗缺血性脑卒中的安全性评估[D].大连:大连医科大学,2023. [23] 高爽,任雪雷,韩翔宇,等.间充质干细胞来源的外泌体在心血管疾病中的研究现状[J].中国动脉硬化杂志,2022,30(11):1006-1012. [24] 王建辉,吴东颖,郭小刚.干细胞外泌体在衰老和衰老相关疾病中的作用[J].中国生物化学与分子生物学报,2023,39(2):189-195. [25] GURUNG S, PEROCHEAU D, TOURAMANIDOU L, et al. The exosome journey: from biogenesis to uptake and intracellular signalling. Cell Commun Signal. 2021;19(1):47. [26] 范星宇,廖晓倩,王梓仪,等.NLRP3炎症小体介导的细胞焦亡在慢性心力衰竭中的机制及中医药研究进展[J].中国中药杂志,2024, 49(8):2106-2116. [27] ZHANG S, SHANG D, SHI H, et al. Function of Astrocytes in Neuroprotection and Repair after Ischemic Stroke. Eur Neurol. 2021;84(6):426-434. [28] 刘丽,李琦,杜欣珂,等.M2型小胶质细胞极化促进少突胶质祖细胞的分化:促进多发性硬化症髓鞘再生的有效途径[J].中国比较医学杂志,2022,32(2):126-132. [29] KRYLOVA SV, FENG D. The Machinery of Exosomes: Biogenesis, Release, and Uptake. Int J Mol Sci. 2023;24(2):1337. [30] 原平利,刘刚,马兰香,等.毛兰素通过抑制NLRP3炎症体介导的细胞焦亡减轻心肌缺血再灌注损伤[J].山西医科大学学报,2023, 54(9):1200-1207. [31] ZHANG J, BULLER BA, ZHANG ZG, et al. Exosomes derived from bone marrow mesenchymal stromal cells promote remyelination and reduce neuroinflammation in the demyelinating central nervous system. Exp Neurol. 2022;347:113895. [32] 傅馨莹,孙天松,朱丛旭,等.基于NLRP3/caspase-1/GSDMD通路研究黄精改善糖尿病大血管焦亡损伤的作用机制[J].中国中药杂志, 2023,48(24):6702-6710. [33] LI C, QIN T, ZHAO J, et al. Bone Marrow Mesenchymal Stem Cell-Derived Exosome-Educated Macrophages Promote Functional Healing After Spinal Cord Injury. Front Cell Neurosci. 2021;15:725573. [34] ZHANG C, PATHRIKAR TV, BABY HM, et al. Charge-Reversed Exosomes for Targeted Gene Delivery to Cartilage for Osteoarthritis Treatment. Small Methods. 2024;8(9):e2301443. [35] GAO R, SONG SJ, TIAN MY, et al. Myelin debris phagocytosis in demyelinating disease. Glia. 2024;72(11):1934-1954. [36] MARTIN NA, HYRLOV KH, ELKJAER ML, et al. Absence of miRNA-146a Differentially Alters Microglia Function and Proteome. Front Immunol. 2020;11:1110. [37] SHENG X, ZHAO J, LI M, et al. Bone Marrow Mesenchymal Stem Cell-Derived Exosomes Accelerate Functional Recovery After Spinal Cord Injury by Promoting the Phagocytosis of Macrophages to Clean Myelin Debris. Front Cell Dev Biol. 2021;9:772205. [38] SOCK E, WEGNER M. Using the lineage determinants Olig2 and Sox10 to explore transcriptional regulation of oligodendrocyte development. Dev Neurobiol. 2021;81(7):892-901. [39] SCHMIDT AL, KREMP M, ARATAKE T, et al. The myelination-associated G protein-coupled receptor 37 is regulated by Zfp488, Nkx2.2, and Sox10 during oligodendrocyte differentiation. Glia. 2024;72(7):1304-1318. [40] MECHA M, YANGUAS-CASÁS N, FELIÚ A, et al. Involvement of Wnt7a in the role of M2c microglia in neural stem cell oligodendrogenesis. J Neuroinflammation. 2020;17(1):88. [41] FEDDER-SEMMES KN, APPEL B. The Akt-mTOR Pathway Drives Myelin Sheath Growth by Regulating Cap-Dependent Translation. J Neurosci. 2021;41(41):8532-8544. [42] XIN H, LIU Z, BULLER B, et al. MiR-17-92 enriched exosomes derived from multipotent mesenchymal stromal cells enhance axon-myelin remodeling and motor electrophysiological recovery after stroke. J Cereb Blood Flow Metab. 2021;41(5):1131-1144. [43] DAHL KD, ALMEIDA AR, HATHAWAY HA, et al. mTORC2 Loss in Oligodendrocyte Progenitor Cells Results in Regional Hypomyelination in the Central Nervous System. J Neurosci. 2023;43(4):540-558. [44] QIN D, WANG C, LI D, et al. Exosomal miR-23a-3p derived from human umbilical cord mesenchymal stem cells promotes remyelination in central nervous system demyelinating diseases by targeting Tbr1/Wnt pathway. J Biol Chem. 2024;300(1):105487. [45] HOU H, WANG Y, YANG L, et al. Exosomal miR-128-3p reversed fibrinogen-mediated inhibition of oligodendrocyte progenitor cell differentiation and remyelination after cerebral ischemia. CNS Neurosci Ther. 2023;29(5):1405-1422. [46] WELSH JA, GOBERDHAN DCI, O’DRISCOLL L, et al. Minimal information for studies of extracellular vesicles (MISEV2023): From basic to advanced approaches. J Extracell Vesicles. 2024;13(2):e12404. [47] 李佳林,张耀东,娄艳茹,等.间充质干细胞分泌组发挥作用的分子机制[J].中国组织工程研究,2025,29(7):1512-1522. [48] 杨丽娜,杜欣珂,刘丽,等.基于“炎症-组织”稳态偶联实现多发性硬化症髓鞘修复的研究现状及展望[J].中国中药杂志,2023,48(1):5-12. [49] ZHA Z, GAO YF, JI J, et al. Bu Shen Yi Sui Capsule Alleviates Neuroinflammation and Demyelination by Promoting Microglia toward M2 Polarization, Which Correlates with Changes in miR-124 and miR-155 in Experimental Autoimmune Encephalomyelitis. Oxid Med Cell Longev. 2021; 2021:5521503. [50] LIU SS, ZHA Z, LI C, et al. The mechanism of exosomes of BMSCs modified with Bu Shen Yi Sui capsule in promoting remyelination via regulating miR-15b/Wnt signaling pathway-mediated differentiation of oligodendrocytes. J Ethnopharmacol. 2025;340:119283. [51] JI J, SUN YQ, ZHA ZZ, et al. Bu Shen Yi Sui Capsules Promote Remyelination by Regulating MicroRNA-219 and MicroRNA-338 in Exosomes to Promote Oligodendrocyte Precursor Cell Differentiation. Evid Based Complement Alternat Med. 2022;2022:3341481. [52] 刘念,董听明,王落芫,等.干细胞外泌体和生物材料辅助外泌体修复骨缺损[J].中国组织工程研究,2026,30(1):175-183. [53] AUGUSTINE R, GEZEK M, NIKOLOPOULOS VK, et al. Stem Cells in Bone Tissue Engineering: Progress, Promises and Challenges. Stem Cell Rev Rep. 2024;20(7):1692-1731. [54] 乔树雅,田田.干细胞外泌体用于缺血性疾病治疗的研究进展[J].药学进展,2023,47(11): 817-828. [55] 孙庆,王海龙,米庆,等.外泌体在心力衰竭发生发展中的作用及临床价值[J].临床荟萃, 2024,39(3):259-263. [56] 孙姝婷.干细胞外泌体的生物学机制与应用[J].张江科技评论,2024(4):108-110. [57] LOZANO-VELASCO E, INÁCIO JM, SOUSA I, et al. miRNAs in Heart Development and Disease. Int J Mol Sci. 2024;25(3):1673. [58] TIAN T, ZHANG HX, HE CP, et al. Surface functionalized exosomes as targeted drug delivery vehicles for cerebral ischemia therapy. Biomaterials. 2018;150:137-149. [59] HE J, WANG Y, ZHAO ZH, et al. Exosome-specific loading Sox10 for the treatment of Cuprizone-induced demyelinating model. Biomed Pharmacother. 2024;171:116128. [60] HUANG L, WU E, LIAO J, et al. Research Advances of Engineered Exosomes as Drug Delivery Carrier. ACS Omega. 2023;8(46):43374-43387. [61] 李旻俊,彭泽琳,张良清.外泌体药物递送载体构建及治疗心血管疾病的研究进展[J].中华实用诊断与治疗杂志,2021,35(7):746-749. [62] ROSZKOWSKI S. Therapeutic potential of mesenchymal stem cell-derived exosomes for regenerative medicine applications. Clin Exp Med. 2024;24(1):46. [63] 王双敏,汪显耀,何志旭.工程化间充质干细胞来源外泌体在靶向递送抗肿瘤药物中的应用与问题[J].中国组织工程研究,2025,29(23): 4975-4983. [64] SHAMS F, POURJABBAR B, HASHEMI N, et al. Current progress in engineered and nano-engineered mesenchymal stem cells for cancer: From mechanisms to therapy. Biomed Pharmacother. 2023;167:115505. [65] GE L, WANG K, LIN H, et al. Engineered exosomes derived from miR-132-overexpresssing adipose stem cells promoted diabetic wound healing and skin reconstruction. Front Bioeng Biotechnol. 2023;11:1129538. |
| [1] | Jiang Xinghai, Song Yulin, Li Dejin, Shao Jianmin, Xu Junzhi, Liu Huakai, Wu Yingguo, Shen Yuehui, Feng Sicheng. Vascular endothelial growth factor 165 genes transfected into bone marrow mesenchymal stem cells to construct a vascularized amphiphilic peptide gel module [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(8): 1903-1911. |
| [2] | Chen Haojie, Wang Dai, Shen Shan. Immune inflammatory microenvironment mechanisms in peri-implantitis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(8): 2054-2062. |
| [3] | Wu Yanting, Li Yu, Liao Jinfeng. Magnesium oxide nanoparticles regulate osteogenesis- and angiogenesis-related gene expressions to promote bone defect healing [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(8): 1885-1895. |
| [4] | Hu Xiongke, Liu Shaohua, Tan Qian, Liu Kun, Zhu Guanghui. Shikonin intervention with bone marrow mesenchymal stem cells improves microstructure of femur in aged mice [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(7): 1609-1615. |
| [5] | Song Puzhen, Ma Hebin, Chen Hongguang, Zhang Yadong. Effect of bone marrow mesenchymal stem cell-derived exosomes combined with transforming growth factor beta 1 on macrophages [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(7): 1616-1623. |
| [6] | Cai Ziming, Yu Qinghe, Ma Pengfei, Zhang Xin, Zhou Longqian, Zhang Chongyang, Lin Wenping. Heme oxygenase-1 alleviates lipopolysaccharide-induced inflammatory response in nucleus pulposus mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(7): 1624-1631. |
| [7] | Yuan Xiaoshuang, Yang Xu, Yang Bo, Chen Xiaoxu, Tian Ting, Wang Feiqing, Li Yanju, Liu Yang, Yang Wenxiu. Effect of conditioned medium of diffuse large B-cell lymphoma cells on proliferation and apoptosis of human bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(7): 1632-1640. |
| [8] | Li Zhenyu, Zhang Siming, Bai Jiaxiang, Zhu Chen. Osthole improves osteogenic differentiation function of bone marrow mesenchymal stem cells under high-glucose conditions [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(7): 1641-1648. |
| [9] | Han Nianrong, Huang Yifei, Akram · Osman, Liu Yanlu, Hu Wei . Programmed cell death receptor-1 suppresses osteogenic differentiation of rat bone marrow mesenchymal stem cells in a high-glucose microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(7): 1649-1657. |
| [10] | Jin Dongsheng, Zhao Zhanghong, Zhu Ziyin, Zhang Sen, Sun Zuyan, Deng Jiang. Effects of icariin-loaded microsphere-three-dimensional scaffold on osteogenic differentiation of rabbit bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(7): 1658-1668. |
| [11] | Zou Yulian, Chen Chaopei, Huang Haixia, Lan Yuyan, Liu Min, Huang Ting. Resveratrol promotes osteogenic differentiation of bone marrow mesenchymal stem cells in an inflammatory microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(7): 1669-1678. |
| [12] | Ding Yifan, Yin Wenjie, Zhang Li, Yuan Shuya, Sun Guoju, Zhang Naili, Zhao Dongmei, Ma Lina. Repair of segmental bone defect of rabbit radius by decalcified bone matrix loaded with adipose-derived stem cells [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(7): 1679-1686. |
| [13] | Wang Qiuhua, Du Ziwei, Wang Wenshuang, Zhao Dongmei, Zhang Xiaoqing. Differences in metabolism, proliferation, differentiation of adipose-derived mesenchymal stem cells, and differentiation into vascular smooth muscle cells between male and female rats [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(7): 1687-1698. |
| [14] | He Jiale, Huang Xi, Dong Hongfei, Chen Lang, Zhong Fangyu, Li Xianhui. Acellular dermal matrix combined with adipose-derived stem cell exosomes promotes burn wound healing [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(7): 1699-1710. |
| [15] | Xia Linfeng, Wang Lu, Long Qianfa, Tang Rongwu, Luo Haodong, Tang Yi, Zhong Jun, Liu Yang. Human umbilical cord mesenchymal stem cell-derived exosomes alleviate blood-brain barrier damage in mice with septic encephalopathy [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(7): 1711-1719. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||