Chinese Journal of Tissue Engineering Research ›› 2026, Vol. 30 ›› Issue (15): 3960-3970.doi: 10.12307/2026.338
Previous Articles Next Articles
Biomechanical function and clinical significance of the lateral wall integrity in intertrochanteric fractures of the femur
Feng Tao, Yin Zhaoyang
- Lianyungang Clinical Medical College of Nanjing Medical University, Lianyungang 222000, Jiangsu Province, China
-
Accepted:2025-07-19Online:2026-05-28Published:2025-11-10 -
Contact:Yin Zhaoyang, MD, Professor, Chief physician, Master’s supervisor, Lianyungang Clinical Medical College of Nanjing Medical University, Lianyungang 222000, Jiangsu Province, China -
About author:Feng Tao, Master candidate, Lianyungang Clinical Medical College of Nanjing Medical University, Lianyungang 222000, Jiangsu Province, China -
Supported by:Jiangsu Provincial Health Commission Project, No. 2022-208 (to YZY); Lianyungang Municipal Health Commission Surface Project, No. 202212 (to YZY)
CLC Number:
Cite this article
Feng Tao, Yin Zhaoyang. Biomechanical function and clinical significance of the lateral wall integrity in intertrochanteric fractures of the femur[J]. Chinese Journal of Tissue Engineering Research, 2026, 30(15): 3960-3970.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
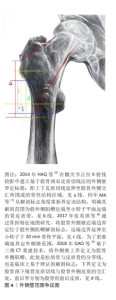
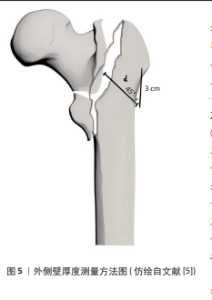
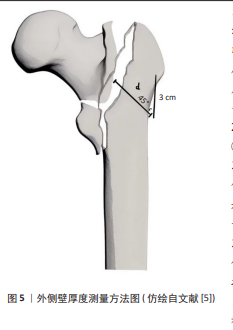
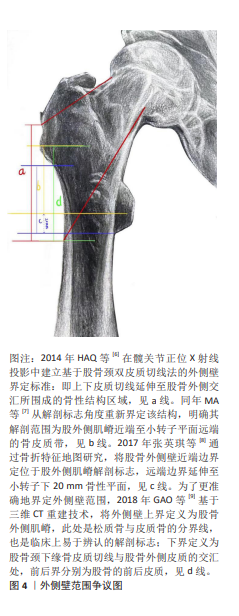
2.1 外侧壁概念由来及范围 2.1.1 外侧壁概念由来 关于“外侧壁”这一概念的理论雏形最早可溯源至1949年[2]。2004年GOTFRIED[1]首次正式提出了股骨外侧壁的概念,他认为外侧壁就是插入头颈螺钉的股骨外侧皮质,是股骨干近端的延续部分,该部分可为头颈骨折块提供外侧支撑,防止向外滑动。但他并未描述其远近端的确切范围。 2.1.2 外侧壁范围 后续IM等[3]及PALM等[4]再次明确了外侧壁就是插入头颈螺钉的位置,并指出股骨外侧肌嵴为其近端,但其远端部位未明确提及。2013年HSU等[5]首次提出外侧壁的解剖范围是从无名结节向下3 cm以内的区域,并创新性提出了外侧壁厚度的测量方法。随后2014年HAQ等[6]在髋关节正位X射线投影中建立基于股骨颈双皮质切线法的外侧壁界定标准:即上下皮质切线延伸至股骨外侧交汇所围成的骨性结构区域,如图4所示a线。同年MA等[7]从解剖标志角度重新界定该结构,明确其解剖范围为股外侧肌嵴近端至小转子平面远端的骨皮质带。其依据在于外侧肌嵴作为松质骨与皮质骨分界区,而大转子外侧松质骨区域缺乏有效内固定支撑效能,如图4所示b线。2017年张英琪等[8]通过骨折特征地图研究,将股骨外侧壁近端边界定位于股外侧肌嵴解剖标志,远端边界延伸至小转子下20 mm骨性平面,如图4所示c线。以上外侧壁范围影像学界定均基于常规X射线片。为了更准确地界定外侧壁范围,2018年GAO等[9]基于三维CT重建技术,将外侧壁上界定义为股骨外侧肌嵴,此处是松质骨与皮质骨的分界线,也是临床上易于辨认的解剖标志;下界定义为股骨颈下缘骨皮质切线与股骨外侧皮质的交汇处,前后界分别为股骨的前后皮质,如图4所示d线。此定义将外侧壁范围从二维平面拓展到了三维立体结构。武建超等[10]认为GAO等所提出的外侧壁范围更加全面且有助于指导手术方式选择。 关于外侧壁解剖学研究,目前还存在很多争议。武英楷等[11]、张世民等[12]众多学者将外侧壁定位区间确立为股外侧肌嵴至小转子中段冠状面投影区,即图4b线所示,其本质为连接上述解剖标志的皮质骨结构区域,上述观点表明目前对外侧壁的理解还是基于其功能,外侧壁是一个外科学概念。2022年张殿英[13]提出的杠杆-支点平衡理论(髋关节类似人体天然的力学杠杆,支点位于股骨头中央。当股骨转子间发生骨折时,原本支撑骨结构的网状组织全部断裂,使原本的支点无法维持,整个杠杆受力失衡)彻底否定了外侧壁学说,他强调尽管股骨近端“外侧壁”学说已获得多数学者的支持,但这一概念是基于临床诊疗过程提出的,目前仍是一个外科学概念,并未被纳入解剖学研究范畴。 2.2 外侧壁厚度 2013年,HSU等[5]基于髋关节X射线正位片首次提出了外侧壁厚度测量方法,以大转子无名结节下方30 mm骨性标记为基准,沿135°方向跨骨折线测量前后骨皮质间距,取其均值作为外侧壁厚度,并确立20.5 mm为临界阈值,低于此值提示术后外侧壁骨折风险增高,如图5所示。2018年AO/OTA分型将其纳入A1与A2亚型分类的核心影像学标准[14]。与初代版本相比,2018版AO/OTA分型强调了外侧壁的重要性,使外侧壁状态被更优先考虑。与HSU等[5]的观点截然不同的是,2016年SUN等[15]认为真正的外侧壁厚度不是外侧皮质至前后骨皮质间距均值,而是指该外侧皮质的厚度,老年患者外侧皮质实际厚度仅为2-4 mm(CT断层扫描均值),伴随骨密度降低导致其抗压强度显著下降。"
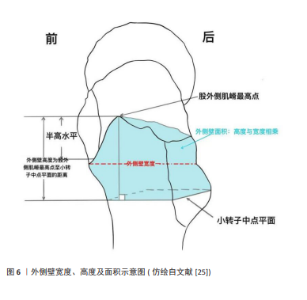
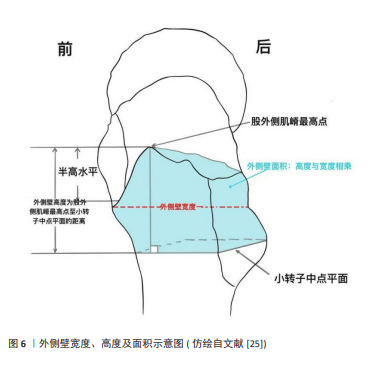
尽管外侧壁状态得到了更多重视,但目前股骨外侧壁厚度测量方式仍存在争议:①因为患者个体差异性,所收集的骨折病例数据不同,因而提出的外侧壁厚度阈值也不一致。2017年SREEJITH等[16]回顾分析66例接受动力髋螺钉治疗的股骨转子间骨折病例,提出了术中外侧壁破裂临界值为20.55 mm。2018年PRADEEP等[17]进行一项涉及135例患者的研究,提出了术前外侧壁厚度阈值为21 mm。2021年SELIM等[18]基于一项前瞻性队列研究,提出外侧壁厚度阈值是19.6 mm。2023年VAN KNEGSEL等[19]开发双侧对比评估体系,通过定义健侧转子间总厚度为从健侧外侧皮质到沿头颈轴线的粗隆间线的距离,在骨盆标准正位X射线片上测量相对外侧壁厚度,即患侧外侧壁厚度与健侧转子间总厚度百分比比值,以此预测围术期外侧壁骨折风险,发现与外侧壁厚度相比,相对外侧壁厚度是预测围术期外侧壁骨折更准确、更个性化的因素,当相对外侧壁厚度低于50.5%时,预示着围术期会发生更多外侧壁骨折。②股骨大转子无名结节具体位置难以定位。国内学者陶金等[20]认为将无名结节标记为大转子偏外侧适合外侧壁厚度的测量。国外学者SHARMA等[21]则建议以股外侧肌嵴下方20 mm处的股骨外侧皮质代替大转子无名结节下方30 mm处作为测量点。2018年张世民等[22]指出,以上两种不同测量点所测得的外侧壁厚度实际就是骨折后前方皮质及后方皮质的残留长度和均值,不论以哪个测量点进行测量,当外侧壁厚度>20.5 mm时,外侧壁被认为是完整的。③髋部正位X射线片所测图像不一定准确。常规正位X射线摄片存在影像清晰度不足及骨折端重叠干扰的问题,同时股骨旋转体位偏差易产生测量误差。YIN等[23]提出的牵引内旋标准化摄片技术可有效提升测量精度,但受限于患者疼痛耐受度,实际临床操作中难以规范实施。HECHT等[24]系统对比X射线片与三维CT重建两种影像学方式对外侧壁形态的测量效果,发现CT对外侧壁形态测量更准确,可更好地评估术中外侧壁破裂风险,因此推荐术前使用CT评估外侧壁状态。 2.3 外侧壁宽度、高度及面积 在外侧壁这一解剖区域,不光具有厚度,还具有宽度、高度及面积。2016年张世民等[25]提出,外侧壁高度为股外侧肌嵴最高点至小转子中点平面的距离,外侧壁宽度为其高度的中点平面的股骨前后径,外侧壁面积即高度与宽度相乘,面积的大小真正反映了矢状面的高度和冠状面的宽度,可能比单独的外侧壁厚度更有指导价值,见图6。张世民团队[25]通过16具尸体标本测量外侧壁高度均值为(24.4±2.4) mm,宽度均值为(23.3±2.0) mm,面积均值为(567.0±82.8) mm2。此区域为大小转子间外侧骨皮质,是内固定物的主要进钉区域,其完整性直接影响术后稳定性。"
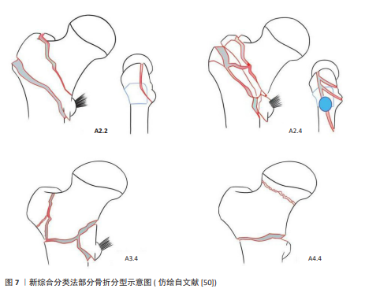
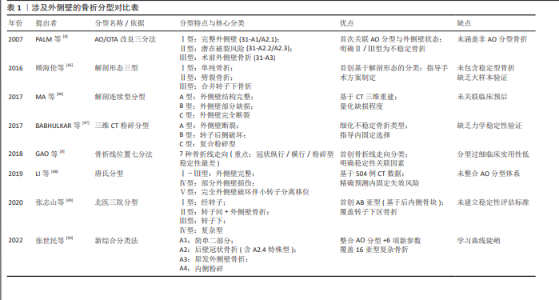
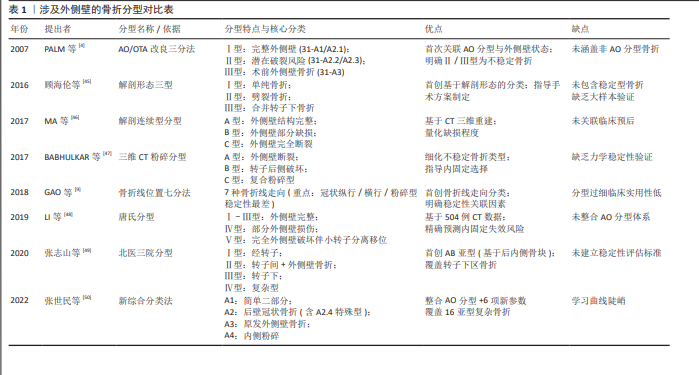
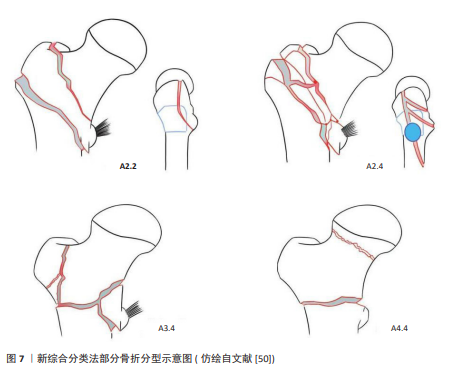
2024年张雅淳等[26]在研究外侧壁薄弱状态时认为外侧壁宽度指的是股骨干前后皮质在头颈螺钉等内固定物打入点的水平距离,冠状面骨折线会对其造成主要影响。2017年张英琪等[8]采用三维CT影像学分析,探讨股骨外侧壁骨折线分布特征,发现若后方冠状面骨折线延伸至头颈螺钉置入点水平的股骨外侧皮质,则该部位后侧皮质骨将完全缺失。这预示着残留外侧壁宽度变小,能支撑头颈骨折块的只剩下前皮质,此时术后并发症率显著升高。2023年LI等[27]通过研究55例采用股骨近端防旋髓内钉治疗合并后壁冠状面外侧壁骨折的股骨转子间骨折患者,利用三维CT影像分析系统对小转子中点平面残余外侧壁进行量化评估,发现残余外侧壁宽度小于18.55 mm可作为预测入钉点破裂的可靠指标,提示临床医生在手术前需关注残余外侧壁宽度。 目前尚无对外侧壁高度的直接研究,2020年DAI等[28]通过研究X射线片上50例股骨转子间骨折患者骨折块高度,即股骨外侧肌嵴至股骨外侧皮质骨折线之间的距离,发现当骨折块高度低于20.45 mm时,围术期外侧壁骨折风险显著增高。多数骨折线沿转子间线方向延伸,呈现大转子至小转子的斜行走向。受头颈骨块后倾(后方常伴粉碎)影响,股骨干残端保留的股骨颈皮质长度始终呈现前侧大于后侧的特征。由于前、后侧皮质均与外侧壁保持解剖连续性,当二者残留量较大时,外侧壁往往能维持较完整的面积(包括高度与宽度),这表明皮质残留长度与外侧壁高度存在正相关性。为简化评估流程,仅通过前侧皮质残留长度亦可推断外侧壁高度,二者同样呈现正相关关系。相较于单纯依据宽度或高度参数,在外侧壁发生部分骨折时,外侧壁面积(高×宽)能更准确评估残余皮质状态,表明该指标可能成为判断外侧壁薄弱程度的有效参数,此时真正发挥生物力学支撑功能的是与股骨干保持连接的残留外侧壁结构。因此,评估残余外侧壁的完整性可预测其术后维持稳定的能力。鉴于外侧壁本质是三维解剖结构,仅依赖二维影像评估存在局限性,需综合厚度、宽度、高度及面积等多维参数。残余体积作为整合二维数据的衍生指标,或能更真实地反映外侧壁的生物力学特性。ZHANG等[29]通过有限元建模技术,构建了不同残余外侧壁体积的股骨转子间骨折股骨近端防旋髓内钉固定生物力学模型。研究证实残余体积与术后稳定性存在显著关联,提出70%残余体积可能是维持生物力学支撑功能的临界阈值,该结论需进一步开展临床研究予以证实。 2.4 外侧壁的临床意义 随着对股骨外侧壁研究的持续深入,越来越多的研究者逐渐形成共识,认为外侧壁的完整性是决定股骨转子间骨折预后的核心要素。2013年ABRAM等[30]提出了股骨近端骨折髓内固定的三点稳定理论,即主钉进针点骨质连续性、外侧壁完整性以及尖顶距是内固定成功的关键三大因素,其中外侧壁完整性是最主要因素。2018年GAO等[9]开展的回顾性研究显示,位于股骨外侧壁与大转子结合区域的游离性骨组织碎块以及呈现横向走行的骨折线贯穿外侧壁结构,是构成股骨转子间骨折合并外侧壁骨折术后内固定失效的主要风险指标。股骨外侧壁的完整性通过侧向力学支撑作用,促使骨折断端实现接触嵌插,抑制骨块旋转移位及股骨干向内移位。该结构特征不仅能优化生物力学载荷分布,降低螺钉切出位移风险,更通过力学传导维持内固定系统的稳定性,显著减少内固定失效发生率。得益于良好的血运重建优势,外侧壁在愈合进程中逐步形成动态抗张力体系,通过持续性骨性支撑作用,可有效转移后内侧骨折区域的机械应力。从而加速骨痂形成进程,最终实现髋关节运动功能恢复[31]。PRADEEP等[17]学者的研究表明,股骨外侧壁完整性缺失将引发远端骨块的内向位移。若此位移量超过解剖阈值的三分之一,将改变髋部生物力学,临床表现为髋关节内翻畸形、外展肌群功能减弱及步态调节异常等,严重者可因内固定失效而丧失自主行动能力。总之,外侧壁是否完整对如何选择内固定物、股骨与内固定物上应力分配以及判断手术失败风险至关重要。所有内固定装置均需完整的外侧壁提供生物力学依托,维持稳定,此现象在髓外固定系统中尤为突出。术前要充分借助三维CT影像学资料评估外侧壁状态,从而在术前选择合适的内固定方式,避免医源性二次骨折[32]。 2.5 外侧壁与内侧壁 股骨近端内侧皮质(含小转子及股骨距)作为髋部核心承重单元,承担压力传导、抗屈曲及抗内翻畸形的生物力学功能,对转子间稳定性具有重要作用。绝大多数转子间骨折均破坏内侧壁完整性,因此内侧皮质复位质量作为力学稳定重建的基础,其接触砥柱关系的影像学评估(如X射线片、CT)日益受到重视[33]。卫禛等[34]提出的“内侧皮质支撑复位”理念中,正位影像的“正性支撑”(即近端骨块内侧皮质位于远端骨块内上4.0-5.0 mm范围内,约1个皮质厚度)尤为关键。此对位模式通过前内侧皮质接触砥柱实现骨性支撑,有效限制骨折块滑动,重建自身力学稳定性以分担内固定负荷,从而保障术后稳定性[35]。近年多项研究均证实该复位方式的临床优势[36-38]。股骨转子间骨折稳定性评估中,内外侧壁的生物力学重要性仍存争议。传统理论强调后内侧壁的核心作用,认为重建内侧支撑是治疗不稳定性骨折的关键,亦可为无法解剖复位时提供可行替代方案[39]。同时近年研究表明,外侧壁完整性同样影响术后稳定性,其缺损状态甚至可预测翻修手术需求[40]。NIE等[41]通过尸体生物力学实验发现:相比外侧壁,内侧壁缺损显著增加股骨近端防旋髓内钉固定后的应变异常,主张优先复位内侧骨块。与之呼应,MU等[42]的有限元分析证实内侧缺损较外侧缺损主钉承受的应力更大,但外侧缺损时髓内钉系统仍能满足高强度康复需求,这提示内侧支撑对初始稳定性更具决定性,而外侧壁缺损可通过髓内固定代偿。股骨转子间骨折的治疗决策需系统评估近端内、外侧壁的生物力学完整性。针对合并内侧壁破损的病例,条件允许时应通过坚强固定重建其连续性与稳定性;若内侧壁无法修复,则需重点保障外侧壁结构完整[43-44]。需特别强调的是,维持或恢复内外侧壁的解剖完整性始终是治疗成功的核心要素,选择何种内固定装置以及具体手术方式需依据具体情况而定,临床医师应将其列为关键考量。 2.6 涉及外侧壁的骨折分型 目前涉及外侧壁的骨折分型众多,尚无统一标准作为指导。2007年PALM等[4]基于AO/OTA骨折分型系统(1990版),依据外侧壁完整性提出新型三分法:Ⅰ型(31-A1/A2.1)具备完整外侧壁,术中破裂风险较低且功能恢复良好;Ⅱ型(31-A2.2/A2.3)存在潜在破裂风险,术后并发症发生率相对较高;Ⅲ型(31-A3)表现为术前外侧壁骨折。后两型属于不稳定型股骨转子间骨折。2016年顾海伦等[45]基于解剖形态学特征提出外侧壁骨折三型分类体系:Ⅰ型(单纯型骨折)、Ⅱ型(劈裂型骨折)及Ⅲ型(合并转子下骨折)。但该体系未涵盖稳定型转子间骨折亚型,存在分类学维度缺失。尽管部分临床研究显示该分型系统对制定手术方案具有指导价值,但受限于样本量不足及中期随访缺失,其临床应用尚未得到广泛认可。 2017年MA等[46]通过三维重建CT图像,基于外侧壁的解剖连续性,将股骨外侧壁视为关节面,提出新型骨折分型:A型(完整型)保留外侧壁结构,可合并大转子冠状面劈裂;B型(部分缺损型)存在外侧壁不完全断裂;C型(完全断裂型)显示外侧壁解剖结构完全中断。其中B型和C型骨折不稳定。同年BABHULKAR等[47]基于三维CT重建图像对不稳定型股骨转子间骨折进行细分,主要分为3型:A型表现为外侧壁断裂;B型表现为转子后侧骨性结构破坏;C型为(复合粉碎型)具有外侧壁粉碎、后壁多段骨折及内侧支柱(含小转子)分离等复合损伤模式。以上两种分型可较为准确描述骨折类型,为临床选择内固定物提供指导,但仍需进一步的临床证据和验证。2018年GAO等[9]根据外侧壁骨折线位置不同对股骨外侧壁骨折进行分型,主要分为7型:1型,骨折线穿过外侧壁上界;2型,骨折线穿过外侧壁下界;3型,骨折线穿过外侧壁前界;4型,外侧壁冠状面纵行骨折线;5型,外侧壁斜行骨折线;6型,外侧壁横行骨折线;7型,外侧壁粉碎骨折形成游离骨块。其中冠状面纵行骨折、横行骨折以及粉碎骨折形成游离骨块是稳定性最差的3种外侧壁骨折类型。2019年LI等[48]基于504例患者三维重建CT影像学资料,将股骨转子间骨折分为5种类型,即唐氏分型(前3型外侧壁完整):Ⅰ型,单纯转子间骨折,不伴有大转子骨折;Ⅱ型,伴小转子骨折型;Ⅲ型,大/小转子复合损伤型,转子间嵴分离移位;Ⅳ型,部分外侧壁损伤型,转子间嵴大面积分离移位同时内侧皮质支持减少;Ⅴ型,完全外侧壁破坏型伴小转子分离移位,属于极不稳定型骨折。与以X射线影像学资料为基础的AO/OTA分型相比,唐氏分型可清晰显示外侧壁厚度、骨折线走向及骨块空间关系,对粉碎性骨折的细节描述精度显著提升,可精确预测内固定失效风险,为临床决策及改善预后提供更具针对性的指导依据。2020年张志山等[49]基于外侧壁完整性及后内侧蝶形骨块存在状态,构建四型分类体系,即北医三院分型;Ⅰ型为经转子骨折;Ⅱ型为转子间骨折,存在外侧壁骨折;Ⅲ型为转子下骨折,骨折线走形于小转子远端至小转子以远7.5 cm两处所对应的股骨外侧皮质之间;Ⅳ型为复杂型骨折,合并大转子或外侧壁骨折,骨折线主要走形于转子下区。同时每型又根据后内侧是否有蝶形骨折块分为A、B亚型,A亚型股骨距完整,B亚型存在蝶形骨折块。 2022年张世民等[50]以2018年版AO/OTA分型为基础,纳入骨折分类多重指标,包括骨折线走行、骨折粉碎程度、小转子骨块情况、后冠状面骨块情况、外侧壁骨折情况、前内下角皮质粉碎情况等,提出了新的综合分类法,共将股骨转子间骨折分为4型,每型又分为4个亚型:①A1型为简单二部分骨折,无小转子和外侧壁骨折;②A2型为含有小转子骨块的顺转子间线骨折或进一步含有其他结构的后壁冠状面骨折,可伴冠状面骨折导致的外侧壁部分损伤;A2.2特点是后壁“香蕉样”骨块;A2.4特点是后壁冠状面骨折向小转子下延伸超过2 cm、向前在外侧皮质累及头颈内植物入钉通道;③A3型为原发性外侧壁反斜、横断骨折,其中A3.4是原发性全转子区骨折;④A4型为内侧壁粉碎骨折,其中A4.4是同时累及同侧股骨颈与转子间的节段性股骨颈骨折。部分骨折分型如图7所示,以上骨折分型对比见表1。2023年崔路宽等[51]研究了上述新综合分类法与1996/2007版及2018版AO/OTA分型在股骨转子间骨折患者CT影像分型中的一致性,研究结果表明新综合分类法在观察者内及观察者间的一致性良好,显示出较高的有效性。至此新综合分类法得到了有效性验证,表明了其在临床应用中的潜力。总之新综合分类法更细致描述骨折形态学特点,包含了更多罕见、复杂类型,可满足日益增长的临床需求,能更有效地指导医生进行术前评估与方案制定。 2.7 关于外侧壁的生物力学研究 基于回顾性临床观察数据的归因性分析,若未建立完整的生物力学理论框架,将外侧壁功能价值归咎于术后并发症的单一诱因,其论证效度存在显著局限。亟需通过生物力学建模与动态载荷分析,系统阐释该解剖结构在应力传导与稳定性维持中的基础作用。因此对外侧壁的生物力学研究至关重要。有限元分析是骨科生物力学验证研究中常用的工具。2018年任德新[52]利用有限元分析股骨近端防旋髓内钉治疗伴有外侧壁骨折的股骨转子间骨折生物力学稳定性,发现当外侧壁骨折时,股骨近端防旋髓内钉于股骨头、股骨颈、骨折断端处的应力较外侧壁完整时成倍增加,尤其以主钉与螺旋刀片结合部位受力增加最为明显,容易出现内固定疲劳断裂、失效。此项研究通过生物力学建模验证了外侧壁的应力调控功能:既可优化内固定物载荷分布模式,又能增强内固定系统的整体稳定性。基于上述发现,任德新团队提出术中需实施外侧壁重建,从而恢复其应力调控与力学稳定功能。2020年戴寿旺等[53]利用9具成人尸体股骨标本造模,分析股骨近端防旋髓内钉治疗股骨转子间骨折中外侧壁的生物力学作用,发现采用股骨近端防旋髓内钉治疗转子间骨折且外侧壁完整的股骨标本其最大承载力最大,滑动位移最小;合并外侧壁损伤的骨折模型滑动位移明显大于外侧壁完整的骨折模型,因此认为外侧壁的完整有利于提高股骨近端防旋髓内钉承载力及稳定性。 2022年FAN等[54]通过建立3种不同外侧壁厚度(分别为10,20.5,30 mm)的股骨转子间骨折三维有限元模型,探讨动力髋螺钉治疗不同外侧壁厚度的股骨转子间骨折的生物力学性能,发现30 mm模型最大位移远小于10 mm模型和20.5 mm模型。因此FAN等[54]认为较厚的外侧壁可以增加转子间骨折术后稳定性,而较薄的外侧壁往往会增加动力髋螺钉内固定术后失败的风险。2022年ZHENG等[55]通过建立5种不同外侧壁厚度的股骨转子间骨折三维有限元模型,分析股骨外侧壁厚度对股骨近端防旋髓内钉内固定失败风险的影响,发现当外侧壁厚度小于21.4 mm时,内固定物应力和位移明显增加,应积极采取预防措施。2023年LI等[56]通过构建4种不同股骨外侧壁厚度的有限元模型,评估股骨外侧壁厚度对动力髋螺钉、股骨近端防旋髓内钉和股骨近端锁定加压板治疗股骨转子间骨折稳定性的生物力学影响,生物力学研究证实,应用动力髋螺钉与股骨近端防旋髓内钉固定系统时,外侧壁对股骨头颈部形成有效侧向力学支撑,其力学效能与外侧壁厚度呈显著线性相关。以上3种关于外侧壁厚度的有限元分析证实外侧壁在生物力学传导中的关键作用,为股骨转子间骨折内固定物的临床选择建立了科学参考体系。 2022年林志诚[57]通过创建内外侧壁缺损的股骨转子间骨折有限元模型,发现有外侧壁缺损的A3.1型骨折模型较单纯A3.1型骨折模型股骨近端防旋髓内钉上最大应力有所增加,股骨及股骨近端防旋髓内钉整体位移增大。当使用股骨外侧钢板重建外侧壁后,股骨近端防旋髓内钉上最大应力明显降低,且股骨及股骨近端防旋髓内钉整体位移也减少,这表明当股骨外侧壁缺损时,股骨及股骨近端防旋髓内钉整体稳定性下降。而重建外侧壁有利于增强股骨力学稳定性。2023年周龙等[58]通过创建3种不同外侧壁分型(外侧壁稳定型、外侧壁危险型、外侧壁破裂型)股骨转子间骨折有限元模型,比较在站立及行走2种状态下股骨近端防旋髓内钉治疗不同外侧壁分型转子间骨折的生物力学特点,发现股骨近端防旋髓内钉固定后的外侧壁破裂型骨折在下地负重行走时其稳定性明显降低,容易造成内固定失败。因此认为外侧壁完整可降低内固定应力,使应力及位移分布更为均衡,有利于提高股骨近端防旋髓内钉术后稳定性。2024年刘玉斌等[59]通过构建3组不同(外侧壁重建组、外侧壁完整组、外侧壁缺损组)股骨转子间骨折有限元模型,对股骨近端防旋髓内钉治疗转子间骨折术后股骨近端和股骨近端防旋髓内钉内固定物从应力、应变、位移等方面进行有限元分析,发现在不同应力加载下重建组模型平均最大应力较完整组模型和缺损组模型有显著降低的趋势,最大主应变从大到小依次为重建组、完整组、缺损组,其中完整组和缺损组较重建组的位移稍大,结果表明随着外侧壁重建,股骨-股骨近端防旋髓内钉系统的部分最大应力可被外侧壁钢板分担,从而减少内固定物应力集中,增加股骨近端应变分布,提高内固定物整体稳定性。 此次综述通过整合有限元分析与尸体生物力学实验(如戴寿旺团队[53]采用9具尸体标本验证),系统阐明了外侧壁的核心力学机制:其一,有限元模型成功解析了静态尸体实验无法实现的动态过程——包括步态周期中外侧壁应力演变、钢板重建后的应力分流效应,以及厚度参数化敏感度分析;其二,研究证实有限元与尸体实验具有结论一致性:外侧壁完整性能显著降低股骨近端防旋髓内钉应力峰值并提升承载力,其厚度与稳定性呈明确正相关;其三,有限元生成的量化阈值(如ZHENG等[55]提出厚度< 21.4 mm时失效风险骤增)为临床决策提供了尸体研究难以企及的普适性指导。未来可构建多模态验证体系:以尸体实验校准有限元边界条件,结合3D打印骨质疏松仿生模型测试重建技术耐久性,并开发AI算法优化个性化固定方案。 2.8 外侧壁骨折处理方式 A3型骨折(原发外侧壁骨折)作为不稳定型骨折的典型代表,目前临床研究表明,外侧壁骨折应避免单独使用动力髋螺钉[1],机制在于动力髋螺钉拉力螺钉的滑动轴与骨折线方向一致,导致近端股骨头颈骨块因失去外侧壁阻挡会沿滑动轴过度位移引发外侧塌陷,远端股骨干相对内移造成复位丢失,最终导致内固定失败。大转子稳定钢板作为动力髋螺钉的生物力学增强装置,可有效重建外侧壁,防止外侧壁移位,提高骨折断端的生物力学稳定性。SELIM等[60]通过荟萃分析比较髓内钉与动力髋螺钉联合大转子稳定钢板治疗不稳定转子间骨折的疗效,结果表明动力髋螺钉+大转子稳定钢板治疗不稳定转子间骨折疗效可靠。但需指出的是,放置大转子稳定钢板需将外侧壁附着的肌肉等软组织广泛剥离,这会破坏外侧壁血供,影响骨折愈合。股骨近端锁定钢板、经皮加压钢板以及倒置微创内固定系统等其他髓外固定系统均是基于微创生物学固定理论设计[61],可同时稳固多个外侧壁骨块,在稳定外侧壁方面具有一定的优势;从而最大程度减少周围软组织损伤保留骨膜血运,提供利于骨痂生长的环境。 当前临床实践中,针对合并外侧壁骨折的股骨转子间骨折患者,髓内固定技术已被广泛视为首选治疗方案[62]。然而,关于术中是否需对外侧壁进行主动重建以及重建方式的选择,学界仍存在显著分歧。单纯髓内钉固定方案具有三重解剖与力学优势:首先,完整的大转子顶部骨性结构为髓内主钉通道建立提供理想入口;其次,小直径头颈螺钉设计可最大限度减少对外侧壁骨质的医源性破坏;再者,近端粗大主钉体部可形成刚性支撑结构,发挥“金属外侧壁”的生物力学功能,有效承载股骨头颈骨折块载荷并抑制其向外侧塌陷移位[63]。李祖涛团队[64]的回顾性对照研究进一步证实,应用加压交锁髓内钉系统、股骨近端防旋髓内钉及第3代Gamma钉3种髓内固定器械治疗不稳定型转子间骨折时,核心疗效指标(包括Harris髋关节功能评分、骨折临床愈合时间、并发症发生率等)组间比较均无统计学差异,提示3类髓内钉器械均可实现满意的临床预后。并且部分学者通过临床观察发现,采用单纯髓内钉固定治疗此类损伤时,未行额外复位固定的破裂外侧壁在术后康复阶段可呈现自发性复位与骨愈合现象[65]。其机制可能与局部解剖特性及生物力学环境相关:股骨大转子区域作为臀中肌、臀小肌及股外侧肌腱的关键附着点,发生骨折的外侧壁骨块在功能上类似于二腹肌截骨形成的游离片段,随着术后肢体轴向负荷恢复及股外侧肌肌力逐步增强,该骨块可依托股外侧肌嵴的锚定作用,产生类似“生物力学合页”的效应,在肌肉动力性牵拉下逐渐实现解剖复位。基于上述证据,部分学者主张对于髓内钉固定的外侧壁破裂型骨折,术中实施针对性重建并非必要干预措施。 尽管单纯髓内钉在治疗股骨转子间骨折时可获得不错临床疗效,但面对外侧壁破裂型骨折仍面临复位困难、置钉受阻及外侧骨块固定失效等多个难题,因此有学者主张术中主动重建外侧壁。DíAZ等[66]研究证实,术中实施外侧壁重建可同步实现以下目标:显著降低固定强度不足所致术后疼痛发生率,同时重建髋关节生物力学稳定系统与影像解剖对位关系。外侧壁重建策略具体表现为:①单纯性外侧壁骨折伴内侧壁支撑存在时,优先选用长螺钉实施外侧壁重建;②外侧壁劈裂性骨折,推荐应用钢丝环扎技术进行骨块复位固定;③严重粉碎性外侧壁损伤,需采用干骺端小钢板完成结构重建[67]。黄复铭等[68]通过Meta分析证实A3型股骨转子间骨折应用髓内钉固定结合外侧壁重建技术,可显著促进骨愈合进程、降低内固定失效及感染风险并显著改善术后髋关节Harris评分。吴钟汉等[69]在A3型股骨转子间骨折外侧壁重建技术的系统性综述中,对比评估了动力髋螺钉+大转子稳定钢板、经皮加压钢板、股骨近端防旋髓内钉+钢板以及股骨近端防旋髓内钉+钢丝/钛缆4种不同重建方式的临床特性,发现髓内联合髓外固定在生物力学稳定性及功能恢复方面呈现更优的临床效果。具体而言:①股骨近端防旋髓内钉+钢板被推荐为优先重建方案,其优势主要表现在优化力学传导性能、缩短术后保护性负重周期及改善髋关节功能评估指标;②股骨近端防旋髓内钉+环形捆扎技术因操作便捷可作为替代选择,尽管在关节功能恢复方面与股骨近端防旋髓内钉+钢板效果相当,但存在解剖复位精度受限、负重训练时间延迟及金属植入物相关不良反应风险;③经皮加压钢板固定系统作为次级治疗选项,其外侧壁解剖重建能力及抗旋转生物力学特性显著优于动力髋螺钉联合大转子稳定钢板方案,但与髓内外联合固定技术相比仍存在明显差距。上述方案还需结合多中心临床实践进一步验证。 股骨近端仿生髓内钉是张殿英[13]基于杠杆-支点平衡理论设计而来。杨冬松等[70]通过临床研究证实股骨近端仿生髓内钉治疗外侧壁破裂型老年股骨转子间骨折近期临床疗效好,其临床应用可改善股骨转子间骨折对外侧壁的依赖,可作为原发外侧壁骨折有效内固定方式选择之一。但由于股骨近端仿生髓内钉作为新一代髓内固定系统,临床应用尚不广泛,未来还需要进一步随访观察临床远期疗效并通过生物力学及有限元分析验证股骨近端仿生髓内钉的指导作用。人工关节置换术在股骨转子间骨折治疗中具有明确疗效,但并非外侧壁骨折的首选治疗方案。由于外侧壁骨折多合并股骨距结构损伤,实施人工关节置换时需进行股骨距重建,这不仅显著延长手术时长,还会增加操作复杂性和术后并发症风险[65]。"
| [1] GOTFRIED Y. The lateral trochanteric wall: a key element in the reconstruction of unstable pertrochanteric hip fractures. Clin Orthop Relat Res. 2004;(425):82-86. [2] 吴克俭, 汤俊君. 准确理解股骨转子间骨折“外侧壁”[J]. 中国修复重建外科杂志, 2019,33(10):1210-1215. [3] IM GI, SHIN YW, SONG YJ. Potentially unstable intertrochanteric fractures. J Orthop Trauma. 2005;19(1):5-9. [4] PALM H, JACOBSEN S, SONNE-HOLM S, et al. Integrity of the lateral femoral wall in intertrochanteric hip fractures: an important predictor of a reoperation. J Bone Joint Surg Am. 2007;89(3):470-475. [5] HSU CE, SHIH CM, WANG CC, et al. Lateral femoral wall thickness. A reliable predictor of post-operative lateral wall fracture in intertrochanteric fractures. Bone Joint J. 2013;95-B(8):1134-1138. [6] HAQ RU, MANHAS V, PANKAJ A, et al. Proximal femoral nails compared with reverse distal femoral locking plates in intertrochanteric fractures with a compromised lateral wall; a randomised controlled trial . Int Orthop. 2014;38(7): 1443-1449. [7] MA Z, CHANG SM. Letter to the editor: where is the lateral femoral wall? Int Orthop. 2014;38(12):2645-2646. [8] 张英琪, 张世民, 熊文峰, 等. 股骨近端外侧壁的骨折特征地图研究[J]. 中国临床解剖学杂志,2017,35(2):121-125. [9] GAO Z, LV Y, ZHOU F, et al. Risk factors for implant failure after fixation of proximal femoral fractures with fracture of the lateral femoral wall. Injury. 2018;49(2):315-322. [10] 武建超, 师政伟, 李吉鹏, 等. 股骨粗隆间骨折外侧壁损伤的研究进展[J]. 中国修复重建外科杂志,2018,32(12):1605-1610. [11] 武英楷, 宁尚攀, 孙国华, 等. 股骨近端外侧壁厚度及其临床意义[J]. 中国矫形外科杂志,2021,29(18):1680-1682. [12] 张世民,马卓,杜守超,等.股骨近端外侧壁的解剖学研究及其对转子间骨折内固定的意义[J].中国临床解剖学杂志, 2016,34(1):39-42. [13] 张殿英. 基于杠杆-支点平衡理论重新认识股骨近端外侧壁的作用[J]. 中华创伤杂志,2022,38(6):481-486. [14] MEINBERG EG, AGEL J, ROBERTS CS, et al. Fracture and Dislocation Classification Compendium-2018. J Orthop Trauma. 2018; 32 Suppl 1:S1-S170. [15] SUN LL, LI Q, CHANG SM. The thickness of proximal lateral femoral wall. Injury. 2016;47(3):784-785. [16] SREEJITH KP, JYOTHIPRASANTH M, SUNKU N. A comparative study to assess the preoperative thickness of lateral trochanteric wall as a predictor of postoperative lateral wall fracture in intertrochanteric fracture treated by dynamic hip screw . J Bone Rep Recomm. 2017;3:1-9. [17] PRADEEP AR, KIRANKUMAR A, DHEENADHAYALAN J, et al. Intraoperative lateral wall fractures during Dynamic Hip Screw fixation for intertrochanteric fractures-Incidence, causative factors and clinical outcome. Injury. 2018;49(2):334-338. [18] SELIM A, SEOUDI N, ALGEADY I, et al. Reliability of lateral femoral wall thickness for detecting the potential for treatment failure and implant choice in patients with trochanteric hip fractures: a prospective cohort study. Curr Orthop Pract. 2022;33: 363-368. [19] VAN KNEGSEL KP, HSU CE, HUANG KC, et al. Relative lateral wall thickness is an improved predictor for postoperative lateral wall fracture after trochanteric femoral fracture osteosynthesis. Sci Rep. 2023;13(1):17750. [20] 陶金, 熊贵润, 刘蓬然, 等. 股骨转子间骨折外侧壁的临床意义及其损伤的内固定治疗[J]. 中国组织工程研究,2020, 24(30):4854-4859. [21] SHARMA G, SINGH R, GN KK, et al. Which AO/OTA 31-A2 pertrochanteric fractures can be treated with a dynamic hip screw without developing a lateral wall fracture? A CT-based study. Int Orthop. 2016;40(5): 1009-1017. [22] 张世民, 余斌. AO/OTA-2018版股骨转子间骨折分类的解读与讨论[J]. 中华创伤骨科杂志,2018,20(7):583-587. [23] YIN J, MARCANTONIO A J, KOH J, et al. Traction Internal Rotation Radiographs Aid in the Assessment of Lateral Femoral Wall Integrity in Intertrochanteric Hip Fractures. J Surg Orthop Adv. 2025;34(1):20-22. [24] HECHT G, SAIZ AM, SHELTON TJ, et al. CT scans better assess lateral wall morphology of “stable appearing” intertrochanteric (IT) femur fractures and predict early failure of sliding hip screw (SHS) fixation. OTA Int. 2021;4(3):e140. [25] 张世民, 马卓, 杜守超, 等. 股骨近端外侧壁的解剖学研究及其对转子间骨折内固定的意义[J]. 中国临床解剖学杂志, 2016(1):39-42. [26] 张雅淳, 付宇捷, 吴斗. 股骨转子间骨折外侧壁薄弱状态研究进展[J]. 中国修复重建外科杂志,2024,38(3):363-367. [27] LI SJ, CHANG SM, LIU H, et al. Residual lateral wall width predicts a high risk of mechanical complications in cephalomedullary nail fixation of intertrochanteric fractures: a retrospective cohort study with propensity score matching. Int Orthop. 2023;47(7): 1827-1836. [28] DAI J Q, JIN D, ZHANG C, et al. Radiologic predictor of intraoperative lateral wall fractures in treatment of pertrochanteric fractures with cephalomedullary nailing. J Int Med Res. 2020;48(4):300060520920066. [29] ZHANG Y, ZHAO E, ZHU J, et al. Finite element analysis of the effect of residual lateral wall volume on postoperative stability in intertrochanteric fractures. J Orthop Surg Res. 2024;19(1):82. [30] ABRAM SGF, POLLARD TCB, ANDRADE AJMD. Inadequate “three-point” proximal fixation predicts failure of the Gamma nail. Bone Joint J. 2013;95-B(6):825-830. [31] 冯俊超, 高明暄, 骆文远. 股骨转子间骨折外侧壁与内侧壁的意义[J]. 中国矫形外科杂志,2023,31(5):436-440. [32] 卫禛, 张凯, 张世民. 股骨近端外侧壁厚度的概念及研究进展[J]. 中国临床解剖学杂志,2020,38(6):739-742. [33] CHANG SM, WANG ZH, TIAN KW, et al. A sophisticated fracture classification system of the proximal femur trochanteric region (AO/OTA-31A) based on 3D-CT images. Front Surg. 2022;9:919225. [34] 卫禛, 陈时益, 张世民. 股骨转子间骨折治疗中前内侧皮质正性支撑复位的研究进展[J]. 中国修复重建外科杂志,2019, 33(10):1216-1222. [35] 李双, 张世民, 张立智, 等. 不同组合前内侧皮质支撑复位对股骨转子间骨折髓内钉术后稳定性影响的生物力学研究[J]. 中华创伤骨科杂志,2019,21(1):57-64. [36] 刘恒山, 寿康全, 朱长谋. 内侧皮质不同复位支撑在老年股骨转子间骨折的临床应用研究[J]. 实用骨科杂志,2023,29(9): 782-786. [37] 陈文龙, 曾祥鸿, 罗景胜. 老年股骨转子间骨折髓内钉固定中不同复位质量对临床预后的影响: 基于影像学特征分析[J]. 创伤外科杂志,2025,27(4):265-271. [38] 王虎虎, 闫淑芳, 付婷. 股骨转子间骨折InterTan内固定术中内侧皮质不同支撑复位方式的临床效果对比[J]. 中国临床医生杂志,2025,53(4):485-489. [39] AHMAD A, EGELAND EH, DYBVIK EH, et al. Equivalent mortality after operation with sliding hip screw or intramedullary nail for trochanteric AO/OTA A1 and A2 fractures reported in the Norwegian Hip Fracture Register 2008 to 2020. Bone Joint J. 2024;106-B(6):603-612. [40] SHI Z, QIANG M, JIA X, et al. Association of the lateral wall integrity with clinical outcomes in older patients with intertrochanteric hip fractures treated with the proximal femoral nail anti-rotation-Asia. Int Orthop. 2021;45(12):3233-3242. [41] NIE B, CHEN X, LI J, et al. The medial femoral wall can play a more important role in unstable intertrochanteric fractures compared with lateral femoral wall: a biomechanical study. J Orthop Surg Res. 2017;12(1):197. [42] MU JX, XIANG SY, MA QY, et al. Selection of internal fixation method for femoral intertrochanteric fractures using a finite element method. World J Clin Cases. 2021; 9(22):6343-6356. [43] GREVE K, EK S, BARTHA E, et al. Sliding hip screw versus intramedullary nail for trochanteric hip fracture regarding death within 120 days and ability to return to independent living. Bone Jt Open. 2024; 5(10):843-850. [44] VALEN AK, VIBERG B, GUNDTOFT PH, et al. Mortality in patients with trochanteric hip fractures (AO/OTA 31-A) treated with sliding hip screw versus intramedullary nail: a retrospective national registry study of 9547 patients from the Danish Fracture Database. Injury. 2023:S0020-1383(23)00249-8. [45] 顾海伦, 杨军, 王维, 等. 不稳定型股骨转子间外侧壁骨折的治疗策略[J]. 中华创伤骨科杂志,2016,18(8):679-684. [46] MA Z, YAO XZ, CHANG SM. The classification of intertrochanteric fractures based on the integrity of lateral femoral wall: Letter to the editor, Fracture morphology of AO/OTA 31-A trochanteric fractures: A 3D CT study with an emphasis on coronal fragments. Injury. 2017;48(10):2367-2368. [47] BABHULKAR S. Unstable trochanteric fractures: Issues and avoiding pitfalls. Injury. 2017;48(4):803-818. [48] LI J, TANG S, ZHANG H, et al. Clustering of morphological fracture lines for identifying intertrochanteric fracture classification with Hausdorff distance-based K-means approach. Injury. 2019;50(4):939-949. [49] 张志山, 张铁超, 周方, 等. 基于股骨近端外侧壁完整性的股骨近端骨折分型方法:附888例病例分析[J]. 中华骨与关节外科杂志,2020,13(3):196-204. [50] 张世民, 胡孙君, 杜守超, 等. 股骨转子间骨折一种新的综合分类法[J]. 中国修复重建外科杂志,2022,36(9):1056-1063. [51] 崔路宽, 刘浩, 王江静, 等. 股骨转子间骨折新综合分类法有效性验证[J]. 中国修复重建外科杂志,2023,37(4):417-422. [52] 任德新. 股骨近端防旋髓内钉固定治疗累及外侧壁的股骨转子间骨折有限元分析[D]. 沈阳: 中国医科大学, 2018. [53] 戴寿旺, 许兵, 余作取, 等. 髓内固定治疗股骨粗隆间骨折中外侧壁的生物力学意义[J]. 浙江临床医学,2020,22(6): 796-798. [54] FAN J, XU X, ZHOU F. The lateral femoral wall thickness on the risk of post-operative lateral wall fracture in intertrochanteric fracture after DHS fixation: A finite element analysis. Injury. 2022;53(2):346-352. [55] ZHENG L, WONG DWC, CHEN X, et al. Risk of proximal femoral nail antirotation (PFNA) implant failure upon different lateral femoral wall thickness in intertrochanteric fracture: a finite element analysis. Comput Methods Biomech Biomed Eng. 2022;25(5): 512-520. [56] LI S, SU ZH, ZHU JM, et al. The importance of the thickness of femoral lateral wall for treating intertrochanteric fractures: a finite elements analysis. Sci Rep. 2023;13(1): 12679. [57] 林志诚. 内外侧壁缺损对A3.1型股骨转子间骨折PFNA术后力学影响的有限元分析[D]. 广州:南方医科大学,2022. [58] 周龙, 王亮, 徐锐, 等. 股骨转子间骨折不同外侧壁分型髓内钉治疗的有限元分析[J]. 中国组织工程研究,2023,27(29): 4652-4657. [59] 刘玉斌, 林志诚, 李松建. 股骨转子间骨折外侧壁重建PFNA固定的有限元分析[J]. 中国矫形外科杂志,2024,32(20): 1882-1887+1892. [60] SELIM A, PONUGOTI N, NAQVI AZ, et al. Cephalo-medullary nailing versus dynamic hip screw with trochanteric stabilisation plate for the treatment of unstable per-trochanteric hip fractures: a meta-analysis. J Orthop Surg Res. 2021;16(1): 47. [61] 曹源, 吕扬, 周方. 股骨转子间骨折内、外侧壁的理念及研究进展[J]. 中国微创外科杂志,2025,25(1):27-34. [62] ŞENSÖZ E, ERGUN S, KAYAALP ME, et al. The Comparison of Dynamic Condylar Screw Plate to Proximal Femoral Nail in Reverse Oblique and Transverse Intertrochanteric Fractures: A Retrospective Study on 61 Patients. Cureus. 2023;15(3):e36397. [63] 郭天庆, 薛飞, 冯卫. 股骨转子间骨折不同外侧壁分型的内固定治疗策略[J]. 中国组织工程研究,2020,24(6):917-923. [64] 李祖涛, 周文正, 缪晓刚, 等. InterTan、PFNA、Gamma3型髓内钉内固定治疗老年不稳定股骨粗隆间骨折的疗效比较[J]. 中国骨与关节损伤杂志,2018,33(10):1017-1020. [65] 林炳剑, 黄复铭. 累及外侧壁的股骨粗隆间骨折治疗进展[J]. 中国骨与关节损伤杂志,2024,39(8):837-841. [66] DÍAZ VJ, CAÑIZARES ACP, MARTÍN IA, et al. Predictive variables of open reduction in intertrochanteric fracture nailing: a report of 210 cases. Injury. 2016;47 Suppl 3:S51-S55. [67] KULKARNI SG, BABHULKAR SS, KULKARNI SM, et al. Augmentation of intramedullary nailing in unstable intertrochanteric fractures using cerclage wire and lag screws: a comparative study. Injury. 2017;48 Suppl 2:S18-S22. [68] 黄复铭, 谭哲伦, 张京, 等. 外侧壁重建对髓内钉治疗A3型股骨转子间骨折疗效影响的meta分析[J]. 中华骨与关节外科杂志,2024,17(4):361-370. [69] 吴钟汉, 许新忠, 张积森, 等. 粉碎性股骨逆转子间骨折一期重建外侧壁:如何提高修复后骨生物力学稳定性[J]. 中国组织工程研究, 2021, 25(36): 5838-5843. [70] 杨冬松, 王琼, 陈许冬, 等. 股骨近端仿生髓内钉治疗外侧壁破裂型老年股骨转子间骨折的近期疗效观察[J]. 创伤外科杂志,2025,27(1):34-37,42. |
| [1] | Liu Wenlong, Dong Lei, Xiao Zhengzheng, Nie Yu. Finite element analysis of tibial prosthesis loosening after fixed-bearing unicompartmental knee arthroplasty for osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2191-2198. |
| [2] | Zheng Wangyang, Fei Ji, Yang Di, Zhao Lang, Wang Lingli, Liu Peng, Li Haiyang. Finite element analysis of the force changes of the supraspinatus tendon and glenohumeral joint during the abduction and flexion of the humerus [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2199-2207. |
| [3] | Cai Qirui, Dai Xiaowei, Zheng Xiaobin, Jian Sili, Lu Shaoping, Liu Texi, Liu Guoke, Lin Yuanfang. Mechanical effects of Long’s traction orthopedic method on cervical functional units: quantitative analysis of biomechanical model of head and neck [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2208-2216. |
| [4] | Rao Jingcheng, Li Yuwan, Zheng Hongbing, Xu Zhi, Zhu Aixiang, Shi Ce, Wang Bing, Yang Chun, Kong Xiangru, Zhu Dawei. Biomechanical differences between the new proximal femoral stable intramedullary nail and traditional intramedullary nail#br# [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2217-2225. |
| [5] | Chen Long, Wang Xiaozhen, Xi Jintao, Lu Qilin. Biomechanical performance of short-segment screw fixation combined with expandable polyetheretherketone vertebral body replacement in osteoporotic vertebrae [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2226-2235. |
| [6] | Yan Xiangning, Chen Lei, Chen Yonghuan, Wang Chao, Li Xiaosheng. Influence of different depths and loads on knee joint mechanics and peripheral muscle force characteristics during squatting [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2236-2247. |
| [7] | Zhang Zizheng, Luo Wang, Liu Changlu. Application value of finite element analysis on unicompartmental knee arthroplasty for medial knee compartmental osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2313-2322. |
| [8] | Zhang Xianxu, Ma Zhong, Liu Xin, Huang Lei, Shen Wenxiang, Luo Zhiqiang . Lumbar fusion combined with unilateral fixation for lumbar degenerative diseases: biomechanics, technical evolution, and clinical applications [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2334-2342. |
| [9] | Chen Huiting, Zeng Weiquan, Zhou Jianhong, Wang Jie, Zhuang Congying, Chen Peiyou, Liang Zeqian, Deng Weiming. Tail anchoring technique of vertebroplasty in treatment of osteoporotic vertebral compression fractures with intravertebral cleft: a finite element analysis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2145-2152. |
| [10] | Zeng Xuan, Weng Rui, Ye Shicheng, Tang Jiadong, Mo Ling, Li Wenchao. Two lumbar rotary manipulation techniques in treating lumbar disc herniation: a finite element analysis of biomechanical differences [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2153-2161. |
| [11] | Cheng Qisheng, Julaiti·Maitirouzi, Xiao Yang, Zhang Chenwei, Paerhati·Rexiti. Finite element analysis of novel variable-diameter screws in modified cortical bone trajectory of lumbar vertebrae [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2162-2171. |
| [12] | Wu Hongxu, Liu Xuanyu, Wang Taoyu, Wang Shiyao, Cheng Jingyi, Zhang Mingwen, Zhang Yinxia, Liu Zhihua, Wang Xiaojie. Finite element simulation of scoliosis with muscle unit introduction: verification of correction effect under bidirectional load [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2172-2181. |
| [13] | Liu Jiafu, Ren Ruxia, Liao Zhouwei, Zhou Xiali, Wu Yihong, Zhang Shaoqun. Three-dimensional finite element analysis of cervical spine biomechanical characteristics in a rat model of cervical vertigo [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2182-2190. |
| [14] | Zhou Daobin, Wang Kehao, Xie Yang, Ning Rende. Biomechanical characteristics of volar locking plate only versus combined dorsal mini-plate fixation of distal radius fractures with dorsal ulnar fragment [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2255-2261. |
| [15] | Zhang Nan, Meng Qinghua, Bao Chunyu. Characteristics and clinical application of ankle joint finite element models [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2343-2349. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||