Chinese Journal of Tissue Engineering Research ›› 2022, Vol. 26 ›› Issue (34): 5543-5552.doi: 10.12307/2022.467
Previous Articles Next Articles
Effect of crown restoration and crown prosthesis on periodontal tissue and periodontal biomarkers
Zhang Jing, Zhang Zhao
- Department of Prosthodontics, Hebei Key Laboratory of Stomatology, Hebei Clinical Research Center for Oral Diseases, School and Hospital of Stomatology, Hebei Medical University, Shijiazhuang 050017, Hebei Province, China
-
Received:2021-07-19Accepted:2021-08-21Online:2022-12-08Published:2022-04-16 -
Contact:Zhang Zhao, MD, Associate chief physician, Department of Prosthodontics, Hebei Key Laboratory of Stomatology, Hebei Clinical Research Center for Oral Diseases, School and Hospital of Stomatology, Hebei Medical University, Shijiazhuang 050017, Hebei Province, China -
About author:Zhang Jing, Master candidate, Physician, Department of Prosthodontics, Hebei Key Laboratory of Stomatology, Hebei Clinical Research Center for Oral Diseases, School and Hospital of Stomatology, Hebei Medical University, Shijiazhuang 050017, Hebei Province, China -
Supported by:Leader of the 2020 Government-Funded Clinical Medicine Excellent Talents Training Project of Hebei Provincial Finance Department, No. 2020048149-2 (to ZZ); Medical Science Research Project of Hebei Provincial Health Commission, No. 20190098 (to ZZ)
CLC Number:
Cite this article
Zhang Jing, Zhang Zhao. Effect of crown restoration and crown prosthesis on periodontal tissue and periodontal biomarkers[J]. Chinese Journal of Tissue Engineering Research, 2022, 26(34): 5543-5552.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

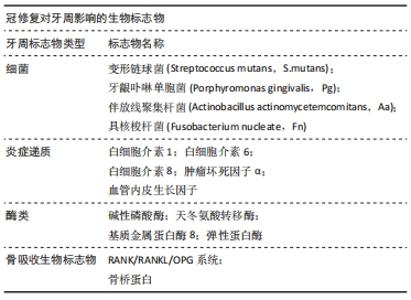
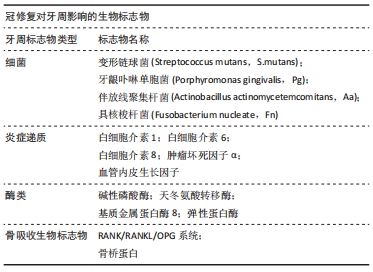
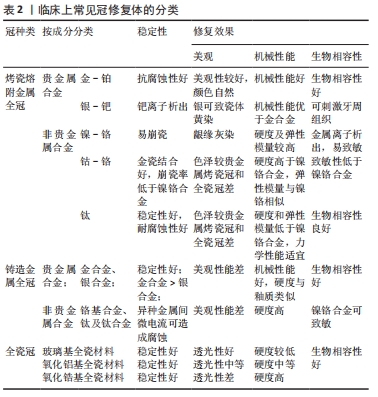
2.2.1 冠材料 不同的冠修复材料对牙周的影响不同。由于烤瓷冠和金属冠中使用的合金与牙龈和口腔黏膜密切且长期接触,当有离子在电解质液体下游离时,可能会对牙周尤其是牙龈产生刺激,修复学研究必须涉及细胞和分子生物学方法,以评估宿主的免疫状态和与材料接触的口腔组织的慢性炎症反应[9]。张彬等[10]在修复前及修复后6、12个月测量临床牙周指数和龈沟液中炎症递质白细胞介素17、白细胞介素35水平,并探讨3种不同材料的冠修复体(钴铬烤瓷冠、纯钛烤瓷冠、全瓷冠)对基牙牙周的影响,研究结果显示钴铬烤瓷冠修复后所有指标与修复前及另2组均有显著差异,全瓷、纯钛较钴铬合金对牙周组织影响较小。冠修复体种类包括烤瓷冠、金属冠和全瓷冠,其材料组成及理化性能,见表2。"

2.2.2 冠边缘的密合度及预备形式 冠边缘与预备体边缘相接处的密合度不佳时,易导致该处菌斑附着,且黏接剂会暴露于口腔中溶解,增加微渗漏,从而使牙周组织因刺激产生炎症[11]。冠边缘的多种预备形式均会对其产生影响。据研究,铸造金属全冠的牙体预备常为带浅凹形的肩台;全瓷冠常见的牙体预备边缘是有角肩台和浅凹形肩台;而对烤瓷冠来说,斜面型、斜面肩台和浅凹型可形成良好边缘密合性,斜面型和肩台型磨切牙体多,但肩台型可形成瓷颈缘,美观性好。 众多学者对烤瓷冠边缘形式进行了更详细的研究。孙培音等[12]将钴铬烤瓷冠颈部边缘预备形式分为刃状、90°肩台和135°肩台,于修复前和修复6个月测量龈沟液量,发现刃状组在修复后龈沟液量变化最多且有显著性意义,对牙周的刺激最高,其次为90°肩台,最后是135°肩台,并认为135°肩台斜面搭接边缘密合性更优。NEMANE等[13]认为凹形边缘及90°肩台的边缘密合性相似,优于45°肩台和刃状边缘。目前关于烤瓷冠哪种边缘更优尚无完全统一的意见,但多数均认为135°肩台优于凹形和90°肩台,45°和刃状肩台较差,密合度及预备形式的不同均会对牙周造成影响。 2.2.3 冠边缘的位置 通常分为龈上、齐龈和龈下边缘,出于美学考虑,在临床中选择齐龈和龈下较多。天冬氨酸转移酶、碱性磷酸酶为牙周组织细胞胞浆酶,牙周炎症时细胞发生破坏,被释放到龈沟液中,代表着牙周炎症的发生,杨乐[14]将全瓷冠分为龈上和齐龈2组,发现两组修复后3,6个月均比修复前龈沟液内天冬氨酸转移酶、碱性磷酸酶水平高,但变化差值两组之间无显著差异,说明龈上与齐龈两种冠边缘位置均对牙周组织影响较小且无显著差异。同样测量齐龈和龈下0.5 mm烤瓷冠修复前后的各项指标,杨静[15]发现修复前两组之间无明显区别,修复后各个时间段龈下组的龈沟液量、天冬氨酸转移酶、碱性磷酸酶均要明显高于齐龈组,提示烤瓷冠修复后龈下更容易造成牙周炎症,齐龈更有利于牙周组织的健康。 2.2.4 冠轴面形态 良好的轴面形态有利于修复体的自我清洁,软组织的健康和菌斑的控制。如果轴面突度过大,牙龈边缘失去生理按摩作用,容易留下食物及菌斑。反之,食物无阻挡直接撞击到牙颈部,超出生理性按摩的范围和力度,会促进牙龈组织根向退缩。 2.2.5 其他因素 在冠修复过程中许多临床操作可能会对牙周产生损伤,比如牙体预备时车针对牙龈的创伤;排龈过程中压力和方向不当所造成的损伤;树脂临时冠中残余单体对牙龈的刺激;临时冠边缘的临时黏接材料的刺激等,均会不同程度地影响牙周组织。 2.3 冠修复与冠修复体影响牙周生物标志物的应用研究 龈沟液作为牙周生物标志物的最灵敏和有效的指标,当其中相关标志物(微生物、局部递质、酶、组织分解产物和免疫球蛋白)的水平波动时,可将其标记为未来的非侵入性分析的诊断工具[16-18]。当龈沟局部受到炎症损害时,牙周结缔组织中血管通透性增加,液体渗出增多,因此龈沟液的含量可作为深层局部炎症反应的可靠表现[19]。有研究观察了修复前后龈沟液量的变化,发现钴铬合金组的龈沟液量变化大于氧化锆组。弓飞[20]和陈珂等[21]均将患者分为钴铬合金烤瓷冠修复组和氧化锆冠修复组,检测修复前的龈沟液量,并分别检测修复后6个月和1年的龈沟液量,比较结果显示2组修复后6个月或1年的龈沟液量均较修复前升高,但钴铬合金烤瓷冠组均明显高于氧化锆冠组,说明患者行全冠修复后均损伤了牙周组织,导致炎症反应,其中氧化锆全瓷冠对患者牙周组织损伤相对较小。冠修复对牙周的影响除了宏观角度的龈沟液量的变化,同时还体现在微观上龈沟液内各种生物标志物各个时期的不同指征,宏观与微观相结合,能更准确探究影响的机制。 目前已发现超过90种以上龈沟液成分与牙周炎症相关[22]。牙菌斑被认为是牙周疾病的始动因子。当人体免疫力下降、细菌毒素增强或受到冠修复等局部促进因素时,机体与牙菌斑之间相互作用失衡,牙周组织产生炎症反应,而宿主的过度防御机制进一步参与了牙周的继发性损伤。首先,细菌毒素侵害炎症细胞,释放炎症递质,贯穿整个炎症过程;然后在炎症递质的作用下,中性粒细胞或其他细胞会产生与组织水解有关的酶类[22];当炎症反应较为剧烈时,会引起牙周骨组织实质性破坏与吸收。冠修复影响牙周生物标志物的相关代表性研究汇总表[1,6,8,20,23-26],见表3。"


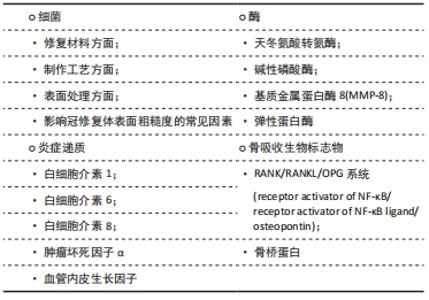
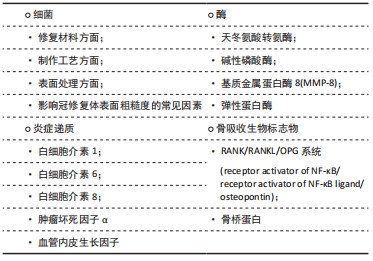
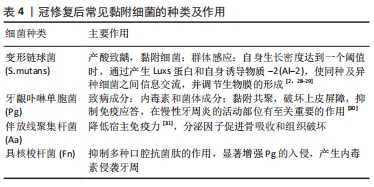
生物膜中的定植菌和宿主免疫反应在牙周病的开始及其后续进展中起着重要作用。这一系列的损害始于口腔正常菌群的改变,尤其是多微生物以生物膜的形式在牙齿及修复体表面定植和牙龈下菌群的紊乱[32-34]。牙周环境中龈沟液内细菌的种类和数量极多并相互作用,提取分离仍有难度,因此关于冠修复后龈沟液内某种细菌具体变化的研究仍较少,大多数均通过体外实验来模拟某种条件下不同冠修复体表面对细菌的黏附性,以此来推测临床中冠修复后龈沟液中细菌的变化。体外研究中最多见的为变形链球菌,国内外学者针对冠修复如何影响细菌黏附,尤其是变形链球菌做出了以下几个方面的研究: 修复材料方面:高表面能及粗糙表面创造了一个有利的环境供细菌定植,影响生物膜的形成。不同种类的微生物在口腔材料上形成生物膜的程度也不同[35]。邢成岗等[2]将烤瓷中的瓷材料和钴铬合金逐级打磨抛光后,与釉质一同比较表面变形链球菌的黏附及生长情况,发现经厌氧培养后,钴铬合金表面变形链球菌黏附量明显多于其他两组,可见同等程度抛光后钴铬合金对牙周影响较明显。郭斌等[6]在实验中发现,钴铬合金烤瓷冠修复组基牙牙周组织呈炎症状态,氧化锆冠组基牙龈下菌斑标本中Aa、Pg和Fn的检出率均较小且有显著性意义,氧化锆冠较钴铬合金烤瓷冠修复更有利于维护基牙牙周健康。然而,最理想的材料特性和制备方法仍未得到充分的研究[36]。 制作工艺方面:高茜[37]探究钴铬合金和钛经不同工艺(选择性激光熔覆、切削、铸造)制作时表面的变形链球菌黏附情况,6组中切削和铸造制作钛合金表面粗糙度最高,变形链球菌黏附量最多。CAD/CAM制作的钴铬合金烤瓷冠比传统方法制作的钴铬合金烤瓷冠边缘密合性更佳,多种菌种包括牙龈卟啉单胞菌黏附量更少,对基牙牙周组织的侵袭性小,临床恢复趋势更明显[38-39]。 表面处理方面:修复体表面单位面积内的细菌数量与表面粗糙度之间呈显著正相关。林晓丽[23]将氧化锆试件分为烧结组、调合后抛光和上釉组,并观测其表面粗糙度和变形链球菌黏附,发现调合会明显升高氧化锆表面粗糙度和变形链球菌黏附量,与烧结组无异,而抛光组、抛光膏组、上釉组均能使表面光滑,细菌黏附量减少,说明抛光和上釉的氧化锆表面最光滑,其次为烧结和调合。王美艳等[40]将臻瓷、爱迪特氧化锆陶瓷分别用不同的抛光套件(PN0301,HP321,Occlubrush)抛光或上釉处理,发现两种陶瓷材料经PN0301,HP321抛光或上釉处理比Occlubrush抛光处理和不处理表面更光滑,附着变形链球菌更少。 冠修复体有一定的粗糙度,通过体外研究可检测不同冠修复体表面4种细菌的黏附量,根据其各自的侵袭作用来预测冠修复对牙周的影响,见表5。"

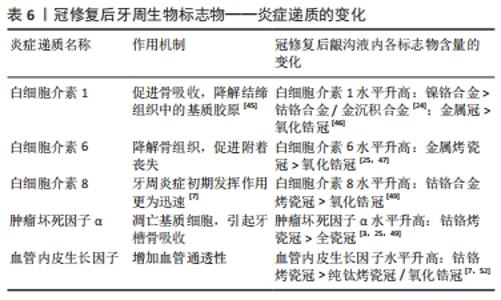
影响冠修复体表面粗糙度的常见因素:材料方面,烤瓷和氧化锆表面常见细菌黏附量明显小于钴铬合金。制作工艺上,CAD/CAM数字化切削较传统制作方法对牙周影响较小。对于不同的表面处理方法,修复体调磨后应抛光或上釉,可更好的降低氧化锆表面和龈下的S.mutans黏附。因此,冠修复体表面细菌黏附量的变化提示,抛光或上釉的CAD/CAM氧化锆冠对牙周组织的影响最小,修复效果最佳。同时,有学者认为,针对变形链球菌的群体感应途径靶向给药,抑制生物膜的形成和细菌附着,可有效降低检出率[29、41-42],向研究者提供了新的研究思路。 2.3.2 炎症递质 当机体被侵袭,炎症因子由免疫及相关细胞分泌,并调节其他细胞发挥功能。CALDEIRA等[43]的Meta分析中认为牙周病变个体的龈沟液中的调节因子(即白细胞介素1α、白细胞介素1β、白细胞介素6等)显著高于牙龈健康者。也有学者检测牙周病中各种炎症递质,并将其按照与牙周炎症相关联的程度由大到小排列,具有重大意义的前几位分别为白细胞介素1、白细胞介素6、白细胞介素8和肿瘤坏死因子α[44]。目前国内外众多学者在探索冠修复对牙周组织的影响时结合了以下几种炎症递质,下面来分别进行阐述: 白细胞介素1:在牙周炎的龈沟中可检出较高水平的白细胞介素1,诱导中性粒细胞释放各种炎症递质,促进骨吸收,同时介导金属蛋白酶降解结缔组织中的基质胶原[45]。李龙飞[24]比较钴铬合金、镍铬合金和金沉积烤瓷冠修复前和6个月后炎症指标,显示3种烤瓷材料均使牙周中白细胞介素1β含量升高,但镍铬合金组差异有显著性意义(P < 0.05),并建议使用钴铬合金和金沉积合金作为临床中烤瓷冠材料。SARAVANAKUMAR等[46]通过测定并比较冠修复后第1,45,90天的龈边缘的白细胞介素1β含量的变化来比较不同冠材料对龈沟液的影响,发现3个月分析结束时,相比于金属冠和陶瓷冠,氧化锆冠的牙龈边缘炎症最少。 白细胞介素6:可调节多种细胞生长分化和免疫应答。在牙周组织中,成骨细胞分泌白细胞介素6,刺激破骨细胞成熟,过量则会导致成骨破骨不平衡,降解骨组织。白细胞介素6也可抑制牙周膜中主要构成细胞(成纤维细胞)的生长,瓦解其附着能力,促进牙周的炎症向深部发展。许辛夷等[47]和杜花娇等[25]将患牙修复方式随机分为金属烤瓷冠和氧化锆全瓷冠2组,经检测氧化锆全瓷冠组修复后龈沟中白细胞介素6明显低于金属烤瓷冠组,可见全瓷冠对牙周组织的影响较小。 白细胞介素8:主要由单核巨噬细胞分泌,在炎症过程中,趋化中性粒细胞至病灶部位,并与其结合激活,表达表面黏附分子,释放超氧物,引起局部组织的病理学损伤。在炎症初期,其发挥作用相比于其他炎症递质(白细胞介素1b、白细胞介素6、白细胞介素10和肿瘤坏死因子α)来说更为迅速[48]。陈广庶[49]在冠修复后6个月发现治疗后全瓷冠组患者的龈沟液中白细胞介素8水平显著低于钴铬合金烤瓷冠组患者,差异有显著性意义,可见全瓷冠对于牙周组织的长期影响要小于钴铬合金烤瓷冠。目前关于冠修复后初期白细胞介素8如何变化未有大量研究,可根据其初期敏感性考虑其作为冠修复对牙周影响的早期指标进一步进行具体研究。 肿瘤坏死因子α:主要来自巨噬细胞和单核细胞,刺激黏附因子和趋化因子的表达,产生炎症递质,使基质细胞凋亡,在牙周组织中则会引起牙槽骨吸收[50-51]。一些研究均发现,患牙经钴铬合金烤瓷冠修复后,龈沟液中肿瘤坏死因子α含量显著升高,对牙周的影响大于全瓷冠[3,25,49]。 血管内皮生长因子:牙龈的血管内皮细胞在炎症状态下会分泌较多的血管内皮生长因子,增加血管通透性,使组织液渗出,龈沟液量增多,龈沟液内血管内皮生长因子含量可一定程度上反映牙周炎症程度。研究发现,比较钴铬合金烤瓷冠、纯钛烤瓷和二氧化锆各组修复前后龈沟液中血管内皮生长因子的含量,钴铬合金组修复后1,3个月明显高于修复前及其他两组,安全性较低,另外两组之间无显著差异[7]。李桐军[52]的试验呈现类似结果,修复后6个月钴铬合金组比纯钛烤瓷组龈沟液中血管内皮生长因子的含量明显增多,可见钴铬合金烤瓷冠相比于纯钛烤瓷冠和全瓷冠会刺激牙周并使血管内皮生长因子含量上调。 冠修复后引起龈沟液内炎症递质发生变化,可在炎症早期和整个炎症过程均能检测到炎症递质的升高。氧化锆冠修复后白细胞介素1、白细胞介素5、白细胞介素6、肿瘤坏死因子α和血管内皮生长因子的升高值小于金属冠和金属烤瓷冠,对牙周的影响最小,见表6。"
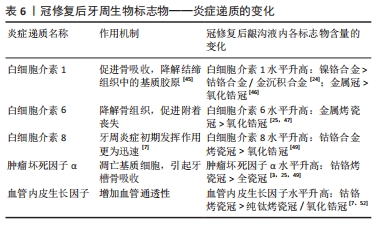
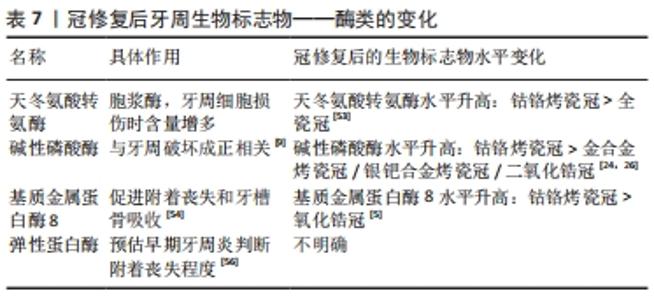
由此可推测,氧化锆全冠材料对牙周适应性最好。不同炎症递质在冠修复对牙周产生的炎症中有不同的预测价值,尤其是白细胞介素1和白细胞介素6在牙周组织炎症中起着核心作用,白细胞介素1有一定的灵敏度及持久性,白细胞介素6在深部的牙周炎症中作用更大,白细胞介素8在炎症发展初期比其他因子变化更迅速,肿瘤坏死因子α和血管内皮生长因子可作为辅助诊断因子。 2.3.3 酶 相比于其他的指示因子,酶更具有稳定性,且目前研究广泛,证据较为充足,不受性别和年龄的影响,有极大的应用前途[53]。针对冠修复引起龈沟液内酶类变化的研究中,最有价值的酶类如下: 天冬氨酸转氨酶:是一种胞浆酶,若在龈沟液中检测到较大量说明细胞壁破坏,细胞损伤或坏死,其水平与牙周组织破坏有显著的正相关。弓飞[20]和郭斌等[6]的试验表明钴铬合金烤瓷冠对牙周的刺激及长期影响高于全瓷冠,表现为修复后6个月龈沟液中各种炎症递质,细菌及天冬氨酸转移酶的增加。 碱性磷酸酶:牙周膜细胞中含有大量碱性磷酸酶,牙周炎症使细胞通透性增加,碱性磷酸酶可随之释放至龈沟。它是目前免疫诊断试剂产品最常用的标记酶之一,临床价值高,稳定性和灵敏度高,缺点是成本高、标记困难。当患牙经钴铬烤瓷冠、钯银烤瓷冠、二氧化锆全瓷冠修复后比较发现,1个月后3组与修复前,且组间均无显著差异,3个月和6个月之后,钴铬烤瓷冠组碱性磷酸酶水平比修复前明显升高且与钯银烤瓷冠组和二氧化锆全瓷冠组的差异较大[24]。贾浩等[26]和王亚玲等[4]的研究呈现相似的结论,钴铬烤瓷冠修复后龈沟液内碱性磷酸酶含量较金合金烤瓷冠更多。 基质金属蛋白酶8(matrix metalloproteinase,MMP-8):MMP-8是一种Ⅱ型胶原酶。由中性粒细胞合成分泌,可促进牙周附着丧失、牙槽骨吸收和牙周组织炎症[54]。马玉龙等[5]发现钴铬烤瓷冠可导致龈沟液量和龈沟液中MMP-8水平的增加,而全瓷冠的作用相对较小,长期疗效较好。ARIAANS等[55]将患者依照修复方式分为二硅酸锂冠组,氧化锆冠组和健康牙未修复组,并用ELISA试验分别对3组修复后3个月龈沟液内MMP-8的浓度进行定量,发现3组间无显著差异,说明全瓷修复与未修复相比没有更高的炎症反应,其中二硅酸锂陶瓷和氧化锆陶瓷修复体处理之间的牙龈反应也没有发现差异。 弹性蛋白酶:龈沟液中弹性蛋白酶是来源于中性粒细胞的一种蛋白水解酶,能广泛破坏牙周骨组织和软组织,与牙周炎关系密切。弹性蛋白酶对牙龈炎不够灵敏,但可预估早期牙周炎。关键在于与IgA的结合,可以判断附着丧失的程度,特异性敏感性在99%以上[56]。近年来关于冠修复后弹性蛋白酶的变化的研究较少,由于其对附着丧失敏感性较高,临床上可进一步研究。 冠修复后的牙周组织受损时,细胞通透性增加,释放天冬氨酸转移酶及碱性磷酸酶;中性粒细胞释放MMP-8和弹性蛋白酶于龈沟中促进附着丧失和牙槽骨吸收,龈沟液内酶类的检出量升高代表炎症的进展。不同冠材料中,氧化锆冠修复后基牙中天冬氨酸转移酶、碱性磷酸酶及MMP-8含量明显小于钴铬合金烤瓷冠,除此之外,贵金属烤瓷冠(金合金、银钯合金)修复后天冬氨酸转移酶水平也分别小于钴铬合金烤瓷冠,见表7。"
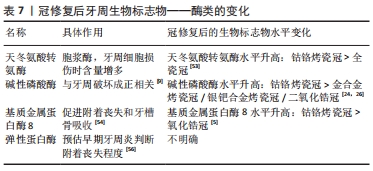
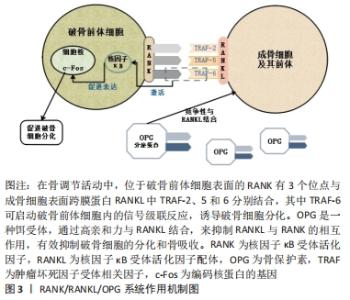
因此,文章可推测氧化锆冠修复后对龈沟液中酶类影响最小,对牙周组织适应性最好,金合金烤瓷冠和银钯合金烤瓷冠适应性也较好,钴铬合金烤瓷冠最差。 2.3.4 骨吸收生物标志物 RANK为核因子κB受体活化因子/核因子κB受体活化因子配体/骨保护素(receptor activator of NF-κB/receptor activator of NF-κB ligand/ osteopontin,RANK/RANKL/OPG)系统:RANK即核因子κB受体活化因子,属于肿瘤坏死因子受体家族,可表达于许多细胞表面,如破骨细胞及其前体,树突状细胞等[57]。RANKL即核因子κB受体活化因子配体,可表达于成骨细胞及其前体,淋巴细胞和牙周组织细胞等,在直接或间接的调控作用中发挥着重要作用。成骨细胞表达RANKL,与破骨细胞表面RANK结合,以促进破骨细胞分化成熟。而OPG是RANKL的诱导受体,两者结合以阻断RANK与RANKL结合,从而减少破骨细胞分化成熟,见图3。"
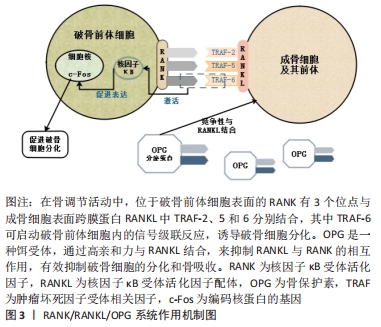
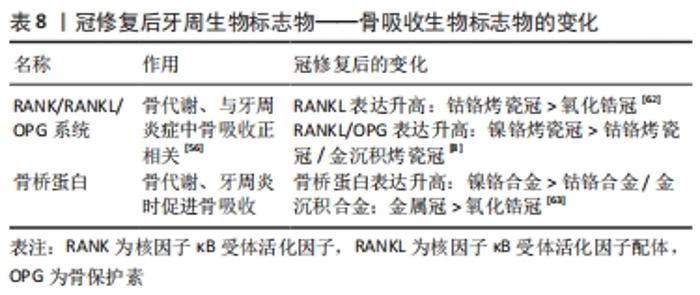
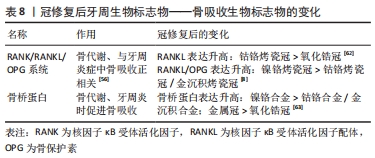
国内外学者在该系统调控全身骨代谢方面已做出大量研究。近年来逐步聚焦于探索其在牙周组织中的作用[58]。龈沟液中可以检测到OPG和RANKL,其中RANKL的表达涉及到许多因素,如白细胞介素1和肿瘤坏死因子α可以上调牙周细胞中的RANKL,并增加破骨细胞的形成;RANKL水平的升高与Pg的数量有关[59]。RANKL的增加会加快牙槽骨的吸收,而OPG表达升高则会抑制这一反应,但哪一种变化更明显,不同学者有不同观点[60-61]。邹林洪等[61]认为单独监测RANKL或OPG可能无法获得关于疾病状态的充分信息,需结合RANKL/OPG比值,更有说服力,但仍需大量实验来证实这一观点。 近年来国外学者集中于RANK/RANKL/OPG系统中各组分之间或与其他细胞因子间相互作用机制的基础研究,与口腔修复临床结合较少。中国学者将该系统与冠修复相结合,林志明等[62]分别用钴铬合金烤瓷冠和氧化锆冠修复患牙,并检测修复前和修复后6个月龈沟液内RANKL的含量,发现两种方法冠修复6个月后均明显高于修复前(P < 0.05),且钴铬合金烤瓷冠组变化更明显,说明相比钴铬合金,氧化锆修复材料对牙周组织刺激较小。赵恒越等[8]研究发现,镍铬合金、钴铬合金和金沉积烤瓷冠在修复后6个月龈沟液内的RANKL、OPG和RANKL/OPG均比修复前明显升高,且镍铬合金组的变化明显大于另外两组,证实了钴铬合金及金沉积烤瓷冠对牙周组织刺激性较镍铬合金烤瓷冠小。目前中国关于研究冠修复后龈沟液中RANKL/OPG变化及其具体作用机制仍不明确,需要进一步探索。 骨桥蛋白:一种非胶原性骨基质糖蛋白,正常状态下可存在于血清中,可由多种细胞表达分泌,包括骨细胞、成骨细胞、破骨细胞和活化的T细胞等,在骨基质的矿化和吸收过程中有重要作用。 在龈沟液中可检出骨桥蛋白,也能够将其作为检测牙周炎症的指标。章洁等[63]认为,骨桥蛋白可作为牙周组织中判断骨破坏程度的判定指标。在冠修复对龈沟液中骨桥蛋白的影响方面,也有学者进行了研究,夏冬景[1]探讨镍铬合金烤瓷冠不同边缘肩台设计(直角肩台组、带斜面的浅凹形肩台组、刃状边缘组)对龈沟液内骨桥蛋白的影响发现,修复前和修复后1个月时3组间无显著差异,3,6个月时各组骨桥蛋白均上升,刃状边缘组最明显,带斜面浅凹形肩台变化最小。此研究结果显示3种肩台设计均会对牙周组织产生刺激,其中带斜面浅凹形肩台最优,但此实验中采用的为镍铬合金烤瓷冠和龈下边缘设计,未控制镍铬合金材料和龈下对牙周组织影响,非单一变量,因此仍需严格控制变量并可进行不同牙冠材料及制作工艺,表面处理对龈沟液内骨桥蛋白的影响。 在生理状态下,牙槽骨中成骨破骨相互协调,保持平衡,而在牙周炎症侵及骨组织时,骨吸收生物标志物的含量发生明显改变,其相比于炎症发生发展过程中其他生物指标更能指示牙周炎症的深入进展程度。部分学者研究了冠修复后龈沟液内骨吸收生物标志物(RANK/RANKL/OPG系统及骨桥蛋白等)的变化,见表8。"
| [1] 夏冬景.3种冠边缘肩台设计对龈沟液中IL-1β、AST及其OPN水平的影响[J].口腔医学研究,2013,29(12):1161-1164. [2] 邢成岗,朱岩凤,李冠颖.不同口腔修复材料表面细菌黏附和生长情况的对比分析[J].全科口腔医学电子杂志,2015,2(8):59-60. [3] 刘镇凡,梁晓.全瓷冠修复体对基牙龈沟液影响的临床研究[J].广西医科大学学报,2015,32(4):611-613. [4] 王亚玲,曹直,占时霞.钴铬合金和金合金烤瓷全冠修复对龈沟液中AST、ALP、TNF-α和IL-8、GP-x、MDA水平的影响[J].海南医学院学报,2016,22(17):2069-2072. [5] 马玉龙,王海山,那日苏.钴铬合金烤瓷冠和全瓷冠修复对患牙牙周组织及龈沟液中炎症因子水平的影响研究[J].中国实用口腔科杂志,2016,9(12):747-750. [6] 郭斌,孙雷,翟晓红.氧化锆全瓷全冠修复对龈沟液患者的临床疗效观察[J].河北医学,2017,23(10):1632-1636. [7] 王一立.不同烤瓷冠修复对牙周组织龈沟出血情况及血管内皮生长因子和肿瘤坏死因子α水平变化分析[J].中国临床医生杂志, 2017,45(9):89-91. [8] 赵恒越,何文娟.三种修复金属材料对口腔修复患者牙周组织龈沟液中炎症因子水平的影响[J].河北医学,2019,25(6):894-898. [9] LIU Y, ZHAO R, REDA B, et al. Profiling of cytokines, chemokines and growth factors in saliva and gingival crevicular fluid. Cytokine. 2021; 142:155504. [10] 张彬,刘琨,李克义,等.3种全冠修复对患者焦虑抑郁心理状况及龈沟液中IL-17、IL-35水平的影响[A].中华口腔医学会全科口腔医学专业委员会、中国科学技术协会国际科技交流中心.中华口腔医学会全科口腔医学专业委员会第八次学术会议论文集[C].中华口腔医学会全科口腔医学专业委员会、中国科学技术协会国际科技交流中心:中华口腔医学会,2017:1. [11] 李学盛,李鸿波.固定修复体适应性评价方法的研究进展[J].国际口腔医学杂志,2017,44(6):726-730. [12] 孙培音,李会云,谭为聪,等.不同种类烤瓷肩台对基牙牙周组织的影响[J].全科口腔医学电子杂志,2015,2(2):84-85. [13] NEMANE V, AKULWAR RS, MESHRAM S. The effect of various finish line configurations on the marginal seal and occlusal discrepancy of cast full crowns after cementation-an in-vitro study. J Clin Diagn Res. 2015; 9(8):ZC18-ZC21. [14] 杨乐.全瓷冠龈上与平龈边缘位置的选择对牙龈的影响差异[J].医学美学美容,2018,27(19):65. [15] 杨静.烤瓷熔附金属冠颈缘位置对牙周组织的影响[D].昆明:昆明医科大学,2016. [16] KHURSHID Z, MALI M, NASEEM M, et al. Human gingival crevicular fluids (GCF) proteomics: an overview. dent J (Basel). 2017;5(1):12. [17] KHURSHID Z, WARSI I, MOIN SF, et al. Biochemical analysis of oral fluids for disease detection. Adv Clin Chem. 2021;100:205-253. [18] COSTANTINI E, SINJARI B, PISCOPO F, et al. Evaluation of salivary cytokines and vitamin d levels in periodontopathic patients. Int J Mol Sci. 2020;21(8):2669. [19] 陈崇崇,钟良军.龈沟液生物标志物在慢性牙周炎诊疗中的研究进展[J].口腔医学,2019,39(11):1047-1052. [20] 弓飞.氧化锆全瓷与钴铬合金全冠修复牙列、牙体缺损临床效果对比[J].实用中西医结合临床,2020,20(1):57-58. [21] 陈珂,舒成军,陈梦铮.二氧化锆全瓷冠对前牙牙体缺损的临床疗效及对周围组织的影响[J].现代实用医学,2020,32(4):509-511. [22] 胡竹林,赵诣,李茵.口腔龈沟液生物标志物的检测分析现状及临床应用前景展望[J].国际口腔医学杂志,2019,46(3):308-315. [23] 林晓丽.不同表面处理对氧化锆表面粗糙度和细菌黏附影响的研究[D].福州:福建医科大学,2017. [24] 李龙飞.不同修复材料对口腔修复患者炎性指标的影响比较[J].当代医学,2020,26(31):125-126. [25] 杜花娇,刘族志,吴小芳.二氧化锆全瓷冠修复前牙缺损效果研究[J].创伤与急危重病医学,2020,8(1):56-57. [26] 贾浩,宁静,王培,等.全瓷冠与金属烤瓷冠在前牙缺损修复中的疗效比较[J].河北医药,2018,40(12):1880-1883. [27] HEBOYAN A, SYED AUY, ROKAYA D, et al. Cytomorphometric analysis of inflammation dynamics in the periodontium following the use of fixed dental prostheses. Molecules. 2020;25(20):4650. [28] TU Y, LING X, CHEN Y, et al. Effect of S. Mutans and S. Sanguinis on Growth and Adhesion of P. Gingivalis and Their Ability to Adhere to Different Dental Materials. Med Sci Monit. 2017;23:4539-5445. [29] 夏丽,储冰峰.变形链球菌LuxS蛋白与LuxS/AI-2群体感应系统的研究进展[J].中华老年口腔医学杂志,2011,9(5):303-306. [30] 杜留熠,吕慧欣,王鹞,等.牙龈卟啉单胞菌fimA分型与相关疾病的研究[J].口腔医学研究,2018,34(12):1281-1283. [31] BALASHOVA N, DHINGRA A, BOESZE-BATTAGLIA K, et al. Aggregatibacter actinomycetemcomitans leukotoxin induces cytosol acidification in LFA-1 expressing immune cells. Mol Oral Microbiol. 2016;31(1):106-114. [32] FATIMA T, KHURSHID Z, REHMAN A, et al. Gingival Crevicular Fluid (GCF): A Diagnostic Tool for the Detection of Periodontal Health and Diseases. Molecules. 2021;26(5):1208. [33] SHOJI M, TAKESHITA T, MARUYAMA F, et al. Recent advances in the field of oral bacteriology. Nihon Saikingaku Zasshi. 2015;70(2):333-338. [34] MATHEW MG, SAMUEL SR, SONI AJ, et al. Evaluation of adhesion of Streptococcus mutans, plaque accumulation on zirconia and stainless steel crowns, and surrounding gingival inflammation in primary molars: randomized controlled trial. Clin Oral Investig. 2020;24(9):3275-3280. [35] DOBRZYNSKI M, PAJACZKOWSKA M, NOWICKA J, et al. Study of Surface Structure Changes for Selected Ceramics Used in the CAD/CAM System on the Degree of Microbial Colonization, In Vitro Tests. Biomed Res Int. 2019;2019:9130806. [36] HAO Y, HUANG X, ZHOU X, et al. Influence of Dental Prosthesis and Restorative Materials Interface on Oral Biofilms. Int J Mol Sci. 2018; 19(10):3157. [37] 高茜.不同工艺制作的钴铬合金和钛的细菌黏附及耐腐蚀性研究[D].济南:山东大学,2020. [38] HEBOYAN A, MANRIKYAN M, ZAFAR MS, et al. Bacteriological evaluation of gingival crevicular fluid in teeth restored using fixed dental prostheses: an In vivo study. Int J Mol Sci. 2021;22(11):5463. [39] AVETISYAN A, MARKARYAN M, ROKAYA D, et al. Characteristics of periodontal tissues in prosthetic treatment with fixed dental prostheses. Molecules. 2021;26(5):1331. [40] 王美艳,赵婵媛,王杨洋,等.不同抛光处理对两种氧化锆陶瓷表面粗糙度和细菌黏附性能的影响[J].口腔医学研究,2020,36(3): 239-242. [41] STONE VN, XU P. Targeted antimicrobial therapy in the microbiome era. Mol Oral Microbiol. 2017;32(6):446-454. [42] 胡桐楠,储冰峰.变形链球菌环境应激反应研究[J].口腔颌面修复学杂志,2017,18(2):113-116. [43] CALDEIRA FID, HIDALGO MAR, DE CARLI DIAS ML, et al. Systematic review of ratios between disease /health periodontitis modulators and meta-analysis of their levels in gingival tissue and biological fluids. Arch Oral Biol. 2021;127:105147. [44] 李显峰,陈倩,王晓静,等.龈沟液成分在牙周病和冠修复中的临床意义[J].中华老年口腔医学杂志,2010,8(2):124-127. [45] STADLER AF, ANGST PD, ARCE RM, et al. Gingival crevicular fluid levels of cytokines/chemokines in chronic periodontitis: a meta-analysis. J Clin Periodontol. 2016;43(9):727-745. [46] SARAVANAKUMAR P, THALLAM VEERAVALLI P, KUMAR VA, et al. Effect of different crown materials on the interleukin-one beta content of gingival crevicular fluid in endodontically treated molars: an original research. Cureus. 2017;9(6):e1361. [47] 许辛夷,张银莲,耿芳惠.CAD/CAM氧化锆全瓷冠和金属烤瓷冠的临床应用及对牙周组织影响[J].上海口腔医学,2017,26(3):331-335. [48] FUJITA Y, ITO H, SEKINO S, et al. Correlations between pentraxin 3 or cytokine levels in gingival crevicular fluid and clinical parameters of chronic periodontitis. Odontology. 2012;100(2):215-217. [49] 陈广庶.全瓷冠修复牙体缺损的效果分析[J].四川医学,2020,41(5): 493-496. [50] AFACAN B, ÖZTÜRK VÖ, PAŞALI Ç, et al. Gingival crevicular fluid and salivary HIF-1α, VEGF, and TNF-α levels in periodontal health and disease. J Periodontol. 2019;90(7):788-797. [51] 刘晨,毕良佳.肿瘤坏死因子-α在慢性牙周炎中的研究进展[J].中华老年口腔医学杂志,2019,17(5):308-313. [52] 李桐军.不同烤瓷冠修复对牙周组织和龈沟周围细胞因子的影响分析[J].中国社区医师,2019,35(26):36-39. [53] 梅冰馨,杨杨.龈沟液中酶类与牙周健康相关性的研究进展[J].临床口腔医学杂志,2015,31(10):635-637. [54] MAURAMO M, RAMSEIER AM, MAURAMO E, et al. Associations of oral fluid MMP-8 with periodontitis in Swiss adult subjects. Oral Dis. 2018;24(3):449-455. [55] ARIAANS K, HEUSSEN N, SCHIFFER H, et al. Use of molecular indicators of inflammation to assess the biocompatibility of all-ceramic restorations. J Clin Periodontol. 2016;43(2):173-179. [56] HANIOKA T, MATSUSE R, SHIGEMOTO Y, et al. Relationship between periodontal disease status and combination of biochemical assays of gingival crevicular fluid. J Periodontal Res. 2005;40(4):331-338. [57] CHEN B, WU W, SUN W, et al. RANKL expression in periodontal disease: where does RANKL come from? Biomed Res Int. 2014;2014:731039. [58] BARBATO L, FRANCIONI E, BIANCHI M, et al. Periodontitis and bone metabolism. Clin Cases Miner Bone Metab. 2015;12(2):174-177. [59] 李小娜.OPG/RANK/RANKL信号通路研究进展[J].河南医学研究, 2018,27(10):1802-1804. [60] Sojod B, Chateau D, Mueller CG, et al. RANK/RANKL/OPG signalization implication in periodontitis: new evidence from a RANK transgenic mouse model. Front Physiol. 2017;8:338. [61] 邹林洪,胡丹,张琳林,等.OPG/RANKL/RANK调节系统与大鼠慢性牙周炎发展的相关性分析[J].重庆医学,2016,45(31):4334-4336. [62] 林志明,陈宏柏,彭秀燕.两种冠修复材料对牙周状况及龈沟液中TWEAK、RANKL水平的影响[J].临床口腔医学杂志,2019,35(8): 467-470. [63] 章洁,徐国超.骨桥蛋白在牙周炎防治中的影响研究[J].中国卫生检验杂志,2017,27(4):511-512,515. |
| [1] | LIU Danni, SUN Guanghua, ZHOU Guijuan, LIU Hongya, ZHOU Jun, TAN Jinqu, HUANG Xiarong, PENG Ting, FENG Wei-bin, LUO Fu. Effect of electroacupuncture on apoptosis of neurons in cerebral cortex of rats with cerebral ischemia-reperfusion injury at "Shuigou" and "Baihui" points [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(在线): 1-6. |
| [2] | Xiang Xinjian, Liu Fang, Wu Liangliang, Jia Daping, Tao Yue, Zhao Zhengnan, Zhao Yu. High-dose vitamin C promotes the survival of autologous fat transplantation in rats [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1242-1246. |
| [3] | Tang Wenjing, Wu Siyuan, Yang Chen, Tao Xi. Inflammatory responses in post-stroke depression [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1278-1285. |
| [4] | Liu Yiyi, Qiu Junqiang, Yi Longyan, Zhou Cailiang. Effect of resistance training on interleukin-6 and C-reactive protein in middle-age and elderly people: a Meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 804-812. |
| [5] | He Junjun, Huang Zeling, Hong Zhenqiang. Interventional effect of Yanghe Decoction on synovial inflammation in a rabbit model of early knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 694-699. |
| [6] | Feng Jianbo, Li Chencheng, Liu Jinyue, Wang Xiaomin, Peng Jiachen. Implantation of Kirschner wire with Staphylococcus aureus biofilm establishes a traumatic osteomyelitis model in rats [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 700-705. |
| [7] | Wei Zhoudan, Li Wenjin, Zhu Li, Wang Yu, Zhao Jiaoyang, Chen Yanan, Guo Dong, Hao Min. Platelet-rich fibrin as a material for alveolar ridge preservation significantly reduces the resorption of alveolar bone height and width after tooth extraction: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 643-648. |
| [8] | Qiu Peng, Fu Qilin, Liu Min, Lan Yuyan, Wang Pin. Comparison of oral micro-adhesion on polyetheretherketone, zirconium dioxide, and pure titanium abutment [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 540-545. |
| [9] | Cao Fei, Hui Min, Dong Xiling, Wang Le, Wang Zuxu, Zhang Min, Zhang Xiaoming, Liu Tongbin. Preparation of silver-loaded nanohydroxyapatite/polycaprolactone composite nanofiber scaffold and its osteogenic and antibacterial properties [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(34): 5461-5467. |
| [10] | Li Maoxue, Ding Yi, Guo Shujuan. Understanding of periodontal biomaterials based on the concept of bone homeostasis control and the effects on bone formation [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(34): 5562-5568. |
| [11] | Fu Yu, Shang Huayu, Li Shunchang. Aerobic and resistance exercises can alleviate liver inflammation in type 2 diabetic rats [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(29): 4666-4671. |
| [12] | Yang Wei, Han Qingmin. Exploring peripheral blood biomarkers and therapeutic drugs for osteoarthritis based on bioinformatics [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(29): 4672-4679. |
| [13] | Dong Xiling, Hui Min, Cao Fei, Lin Peng, Zhou Han, Wang Le, Zhang Xiaoming, Liu Tongbin. Preparation of copper loaded coating on polydopamine-modified polycaprolactone electrospun membrane and antibacterial and cellular properties evaluation [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(27): 4272-4278. |
| [14] | Wu Haineng, Geng Kang, Wang Jing, Xiong Aibing. Platelet-rich fibrin combined with curcumin nanoparticle hydrogel promotes wound healing in diabetic mice [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(27): 4300-4307. |
| [15] | Xu Ran, Chen Xingyu, Li Zhiqiang. Antibacterial agents loaded on hydroxyapatite scaffolds: action mechanism between the drug and the scaffold [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(27): 4411-4416. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||