Chinese Journal of Tissue Engineering Research ›› 2022, Vol. 26 ›› Issue (11): 1788-1792.doi: 10.12307/2022.367
Previous Articles Next Articles
Cervical spondylotic amyotrophy: problems about classification, diagnosis, treatment, and prognosis
Lü Shuaiyao, Guan Haishan, Hao Chen, Ding Zhuangzhi
- Department of Orthopedics, Second Hospital of Shanxi Medical University, Taiyuan 030001, Shanxi Province, China
-
Received:2021-03-12Revised:2021-03-17Accepted:2021-04-17Online:2022-04-18Published:2021-12-13 -
Contact:Guan Haishan, MD, Chief physician, Department of Orthopedics, Second Hospital of Shanxi Medical University, Taiyuan 030001, Shanxi Province, China -
About author:Lü Shuaiyao, Master candidate, Department of Orthopedics, Second Hospital of Shanxi Medical University, Taiyuan 030001, Shanxi Province, China
CLC Number:
Cite this article
Lü Shuaiyao, Guan Haishan, Hao Chen, Ding Zhuangzhi. Cervical spondylotic amyotrophy: problems about classification, diagnosis, treatment, and prognosis[J]. Chinese Journal of Tissue Engineering Research, 2022, 26(11): 1788-1792.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
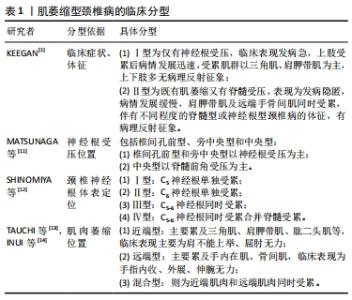
2.1 肌萎缩型颈椎病疾病发展史 肌萎缩型颈椎病首次由BRAIN等[2]于1952年提出,报道了以运动无力、上肢萎缩为特征的罕见颈椎病,无明显的感觉障碍。有研究报道脊髓颈椎病患者运动症状和感觉轻微丧失的发生率略低于7%[3],并将这种情况描述为“运动系统型脊髓病”,KEEGAN[1]于1965年提出的一种引起上肢肌萎缩、不伴或轻度伴有感觉障碍及脊髓病变的颈椎病,SOBUE等[4]证实节段性颈椎病是这种选择性肌肉萎缩的根本原因,并在1975年推荐使用“cervical spondylotic amyotrophy”,即“肌萎缩型颈椎病”一词。 2.2 肌萎缩型颈椎病的临床表现及分型 肌萎缩型颈椎病患者与脊髓型或者神经根型颈椎病患者的临床症状不同,其特点是运动无力伴有明显的上肢肌肉萎缩,而下肢没有明显的感觉障碍或痉挛性麻痹,表现为患侧肌力下降,如肩不能上举,臂下垂及手腕下垂等[1]。肌萎缩型颈椎病患者起病隐匿,出现神经系统症状的平均年龄为50-60岁,男性比女性更易出现神经系统症状。肌萎缩型颈椎病通常是单侧发病,有时是双侧发病[5-8],Li等[9]提出肌萎缩型颈椎病患者的特征是双侧受累,他们指出虽然大多数患者主诉症状出现在1个上肢,但仔细的神经系统检查发现25%的患者在另一个上肢肌肉力量轻微恶化,因此认为肌萎缩型颈椎病与亚临床性脊髓型颈椎病或脊髓型颈椎病的非典型表现密切相关。然而,临床上只有少数肌萎缩型颈椎病患者仅表现为肌萎缩而不伴有其他症状,大部分患者同时伴有明显的上肢根性疼痛或肢体感觉障碍[8]。超过1/3的患者表现出下肢反射亢进而无明显的步态障碍[9],SONOO等[7]报告称,近端和远端肌萎缩型颈椎病患者分别有79%和84%的症状在1个月内进展。在近端型肌萎缩型颈椎病患者中,常因C5或C6节段性障碍而发现肩外展和肘关节屈曲损伤。三角肌萎缩表明C5受累是主要原因,而当C6受累时,手部关节伸展和旋前圆肌功能经常受损。在远端型肌萎缩型颈椎病患者中,存在C7-T1病变的手部内外肌肉萎缩和无力。在这些症状中,手指屈曲障碍是最常见的残疾,发病率约为60%,推测主要累及C8节段。肱三头肌萎缩也经常出现。远端型肌萎缩型颈椎病的特点是发病率低,发展较慢,椎管狭窄数目多,T2W1高信号率高[8-10]。 肌萎缩型颈椎病的临床分型包括很多种方法[1,11-14],见表1,目前临床中最常用的3种类型是近端型、远端型和混合型[13-14]。"

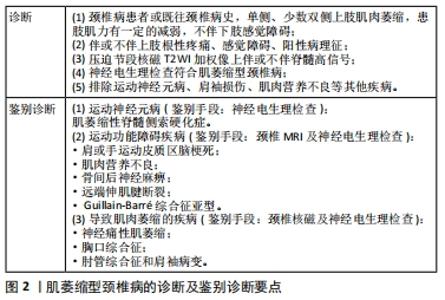
2.3 肌萎缩型颈椎病的病因和病理生理学概述 目前关于肌萎缩型颈椎病的病理生理机制尚不明确,目前已阐述了3种机制。 2.3.1 椎体后外侧增生的骨赘对腹侧神经根选择性压迫 IMAJO等[15]将21例行保守治疗的近端型肌萎缩型颈椎病患者分为不完全恢复组和完全恢复组,在三角肌和二头肌记录复合肌肉动作电位。复合肌肉动作电位的测量包括从基线到峰值的负峰值幅度,结果显示正常侧复合肌肉动作电位振幅超过10 mV的患者没有脊髓前角的撞击;正常侧复合肌肉动作电位振幅超过10 mV,患侧复合肌肉动作电位振幅超过50%正常侧显示轻度腹侧神经根损伤。 2.3.2 脊髓前角细胞损伤 脊髓前角位于脊髓沟动脉的末端支配区,易受循环血流不足的影响,随着脊髓前角血液灌注不足,导致其损伤,进而引起颈椎椎管狭窄,或者随着颈椎的过屈过伸,对脊髓内或髓外血管产生压迫,导致脊髓前角缺血损伤或者死亡。TOFUKU等[16]报道了10例使用高压氧治疗肌萎缩型颈椎病的临床结果良好或极好,这支持脊髓前角循环功能不全是肌萎缩型颈椎病的可能原因的假设。其次,临床中部分肌萎缩型颈椎病患者颈椎MRI T2W1上脊髓前角区域存在高信号,为脊髓前角缺血性损伤提供影像学依据[10,17]。TAKEBAYASHI等[18]证实了脊髓前角与远端型肌萎缩型颈椎病之间的关系。 2.3.3 腹侧神经根及脊髓前角均受累引起 FUJIWARA等[19]报道至少53%肌萎缩型颈椎病患者合并腹侧神经根和脊髓前角的损伤。 肌萎缩型颈椎病的发病率低,然而近端型肌萎缩型颈椎病较远端型肌萎缩型颈椎病发病率高的原因有2点:①解剖的特殊性原因,近端型肌萎缩型颈椎病以三角肌受损最常见,三角肌一般由C5神经支配。在颈段脊髓中,C5水平脊髓最粗,发出的神经根最细,行走的距离最短,行走后出现的角度最大,因为颈椎的前屈,C5位于前屈最大的位置,所以C5神经根张力较大,代偿空间较小,发生损伤的概率最大;②生物学特性原因,颈椎以C5-6的活动度最大,出现退变的概率最大,在颈椎退变的基础上,颈部运动可加重颈神经根和脊髓的刺激和压迫;脊髓在颈部屈曲时伸展,可被骨赘骨刺和突出椎管的椎间盘压迫;过伸可使椎体前缘与后椎板或黄韧带之间的脊髓受到挤压。反复的颈部运动和外伤也会加速颈椎病的发生;而一项动物实验研究将兔暴露于反复强迫的颈部伸展和屈曲运动中,结果显示出骨赘的早期发展[20-21]。 2.4 肌萎缩型颈椎病的辅助检查 2.4.1 影像学检查 颈椎X射线片(包括正侧位及过屈过伸位)可发现颈椎退行性改变、颈椎骨质增生及是否合并颈椎不稳定;颈椎CT可发现颈椎后方是否合并钙化,明确颈椎后纵韧带骨化;磁共振成像是肌萎缩型颈椎病患者的诊断重要检查之一,颈椎核磁共振成像表现为多节段脊髓受压,脊髓变细,脊髓内可见高信号,部分典型病例可见对称高信号(蛇眼症)。部分研究报道肌萎缩型颈椎病患者存在不同部位的压迫,椎间孔前区以腹侧神经根受压为主、旁正中区以脊髓前角受压为主、椎管内侧区域以相互混合存在。然而,对于年龄较大或者退变严重的肌萎缩型颈椎病患者来说,很难区别压迫的来源,椎间孔区的压迫也不能仅仅通过核磁来判断。当病变发生在脊髓时,脊髓节段与椎间节段之间存在差异,因此,在这种情况下,近端型肌萎缩型颈椎病患者在C4-5椎间盘水平出现脊髓病变(提示C5-6脊髓水平的前角),远端型肌萎缩型颈椎病患者在C5-6和C6-7椎间盘水平出现脊髓病变(提示C7-T1脊髓病变)[14,21]。 2.4.2 电生理检查 电生理检查在肌萎缩型颈椎病患者的诊断中具有重要的作用,神经传导速度、肌电图、运动和感觉诱发电位有助于肌萎缩型颈椎病的明确诊断和与其他类似疾病的鉴别,其中一些检查也被证明可以预测肌萎缩型颈椎病患者经过保守治疗和手术治疗后的预后。肌萎缩型颈椎病患者的标准肌电图显示萎缩肌肉的去神经支配电位和运动电位下降[8,17],而其他肌肉未见异常。这些病理表现可在相应节段的颈椎椎旁肌中观察到,而在胸段则无异常表现[7]。肌电图的纤颤和正尖波显示萎缩肌的前根或神经根损伤,而肌束和同步显示前角的下运动神经元损伤[22]。 2.5 肌萎缩型颈椎病的诊断及鉴别诊断 见图2。"


运动神经元病是与肌萎缩型颈椎病鉴别的最关键疾病,前者以肌萎缩性脊髓侧索硬化症最常见,临床常表现为上、下运动神经元合并受损的混合性瘫痪。肌萎缩性脊髓侧索硬化症的诊断目前主要依赖临床表现及家族史,起病隐袭,进展缓慢,以40岁以上人群多见;以肌肉无力、肌肉挛缩、肌束颤动以及萎缩为主要临床表现,影响咽喉部肌肉可使患者出现言语和吞咽困难;累及呼吸肌时可导致患者呼吸困难而死亡。肌萎缩性脊髓侧索硬化症通常以手肌无力、萎缩为首发症状,一般从一侧开始以后再波及对侧,随病程发展出现上、下运动神经元混合损害症状,称肌萎缩侧索硬化症[23]。神经电生理检查在两者的鉴别诊断中至关重要,重复神经刺激主要用于评估神经肌肉接头功能的电生理测试,在肌萎缩性脊髓侧索硬化症患者的检测中具有更明显的变化[23]。但据文献报道,既往有肌萎缩性脊髓侧索硬化症合并肌萎缩型颈椎病的患者鉴别诊断具有一定的困难性。 运动功能障碍疾病的鉴别诊断包括肩或手运动皮质区脑梗死、肌肉营养不良、骨间后神经麻痹、远端伸肌腱断裂、Guillain-Barré综合征亚型,如急性运动轴索神经病变和平山病。平山病也称青年上肢远端肌萎缩,发生于青春期,男性为主,临床特征包括主要的单侧肌肉无力以及手和前臂的萎缩,起病隐匿,进展缓慢,常于几年内自愈[24]。颈椎磁共振成像及神经电生理检查有助于与肌萎缩型颈椎病鉴别,且发病年龄也是二者的区别之一[25-26]。 感觉缺陷或伴有轻微疼痛需与其他可导致肌肉萎缩的疾病鉴别,如神经痛性肌萎缩、胸出口综合征、肘管综合征和肩袖病变。肩袖病变主要以肩袖损伤最常见,主要表现为肩部疼痛,夜间为重,肩部活动受限,进一步发展可致远端肌肉失用性萎缩。肩关节核磁是诊断肩袖损伤的关键检查,其可明确损伤类型及损伤程度[27],故二者可通过颈椎核磁及肩关节核磁加以鉴别。肘管综合征临床中比较多见,主要表现为手部骨间肌萎缩,手部肌肉肌力下降及手部尺侧麻木等不适[28],颈椎核磁及神经电生理检查有助于与肌萎缩型颈椎病鉴别。 2.6 肌萎缩型颈椎病的治疗 2.6.1 保守治疗 保守治疗对于肌萎缩型颈椎病患者来说,一般可以稳定或者改善症状,无法治愈。既往研究表明,保守治疗包括颈椎牵引、颈托固定、物理治疗及神经营养治疗(维生素B12或E)等对近端型颈椎病患者有效。还有文献报道高压氧、中医理疗等保守治疗方式,TOFUKU等[16]报道了10例使用高压氧治疗肌萎缩型颈椎病的临床结果良好或极好。 2.6.2 手术治疗 对于进展性或严重的神经功能恶化的肌萎缩型颈椎病患者来说通常需要手术治疗。关于手术方式的选择,一直都是临床工作中的困惑,大部分临床医师根据自己的临床经验选择手术方式,依据患者的压迫的来源、病变节段数和颈椎曲度等,予以脊髓和神经根减压,重建颈椎生理曲度。分为颈椎前路和后路2种手术,前路减压融合的优势是直接去除致压物,解除脊髓压迫,重建颈椎序列和稳定性。包括椎间盘切除减压或者椎体次全切切除减压融合固定;以单开门椎管扩大成形术为代表的后路手术,通过打开椎板扩大椎管有效容积,利用“弓弦效应”达到间接减压目的。颈椎的生理前凸是单开门椎管扩大成形术脊髓减压的保障[30-31]。其他的后路手术方式包括椎管成形植骨融合固定、椎管成形术联合椎间孔切开、椎板切除联合侧块螺钉固定[32]。中国学者的研究结果表明,<4个节段的肌萎缩型颈椎病患者可首先考虑前方入路;≥4个节段、合并有颈椎后纵韧带骨化的患者可行颈椎后路手术治疗;前路手术是首选,对于多节段颈椎后纵韧带骨化、前路不可能减压或者减压风险太大的患者选择后路手术[33]。国外有研究报道行颈椎前路手术可取得满意效果[34]。2018年,BAXTER等[35]提出神经移植技术,并成功应用于1例肌萎缩型颈椎病患者,文章报道了在涉及C5和C5的单侧颈椎病性肌萎缩症的情况下,使用神经移植(将副神经远端移位到肩胛上神经,将尺神经移位到肱二头肌运动分支,将桡神经分支移到肱三头肌至腋窝)恢复肩和肘功能。肌电图以及术后5个月的临床观察到再生的证据;术后3年,肘关节屈曲和肩外展的恢复达到医学研究理事会的4/5级,外旋得到改善,患者的手臂、肩膀和手部残疾评分得到明显改善。 2.7 肌萎缩型颈椎病治疗的预后 既往文献报道对于肌萎缩型颈椎病患者可以采取颈托固定、牵引治疗等保守治疗,但大多数临床效果并不满意[8]。大多数学者建议对于临床诊断明确的肌萎缩型颈椎病患者尽早行手术干预[21,36]。 关于手术治疗肌萎缩型颈椎病的效果,临床通过2方面来判断术后疗效:第一,主要通过徒手肌力实验及改善率评估,根据相应肌肉肌力的变化[9],分为4个等级:①极好,肌力完全恢复或者恢复较前提升2级;②好,肌力较前提升1级;③肌力无变化;④肌力较前下降。极好和好的等级称为术后疗效佳。第二,根据日本骨科协会评估治疗分数(JOA评分)于术前和术后的变化评估手术疗效。根据肌肉萎缩位置的不同分为近端型、远端型和混合型。既往国外一些作者报道了肌萎缩型颈椎病患者手术后的效果,包括所有类型肌萎缩型颈椎病患者,手术效果良好的发生率为70%-96%;其中近端型手术效果良好的发生率为58%-100%,远端型为38%-86%,混合型未见报道;有研究认为不同类型肌萎缩型颈椎病患者之间行手术治疗后中期效果无显著性差异[21]。 关于不同分型的肌萎缩型颈椎病术后疗效,目前中国报道极少,有研究认为患者术后肌力均能得到一定改善[37],而且上肢近端肌萎缩患者术后肌力恢复优于远端肌萎缩患者;有研究认为混合型较近端型和远端型效果较差,近端型与远端型之间无显著差异[38],84.21%肌萎缩型颈椎病患者(近端型100%,远端型71.43%,混合型75%)行手术治疗后取得满意的效果。 术后中期效果近端型较远端型肌力恢复较好,混合型肌力恢复较差;各类型肌萎缩型颈椎病患者术后疗效存在差异的原因,国内外报道较少,可能的原因目前存在争议:第一,远端型肌萎缩型颈椎病主要涉及对脊髓前角的损害,前角的再生能力较腹侧神经根小;第二,远端型脊髓到肌肉的距离较近端型更长[9,11,39]。至于手术方式的选择,大部分学者认为前路手术是首选,对于多阶段颈椎后纵韧带骨化、前路不可能减压或者减压风险太大的患者选择后路手术[9,34,38-43]。 关于不同手术方式术后效果,国外有研究报道行颈椎前路手术可取得满意效果,目前国内外报道很少。中国学者研究表明,导致肌萎缩型颈椎病的病变来自脊神经前根或(和)脊髓前角细胞的腹侧受损[31],且部分患者伴有颈椎曲度不良,这是前路手术较后路手术效果佳的原因之一,另外一个可能因素行颈椎后路手术的患者通常合并后纵韧带骨化等其他因素,这些本身就是影响预后的因素[9,42-43]。关于肌萎缩型颈椎病患者预后不良的影响因素,主要包括:疾病的持续时间、肌萎缩型颈椎病的类型、是否合并后纵韧带骨化症以及核磁T2W1上是否合并高信号[9,41-44]。有文献报道,疾病的持续时间与患者术后肌力的恢复有直接的关系[11,39],症状持续时间超过12个月的患者预后较差,因此认为长时间的脊髓压迫会对脊髓产生不可逆转的损害。因此,UCHIDA等[36]建议对肌萎缩型颈椎病进行外科治疗需要采取紧急措施。另外,合并颈椎后纵韧带骨化及核磁T2W1高信号是预后不良的因素。颈椎后纵韧带骨化在亚洲,尤其是中国及日本,发病率较高,患者后纵韧带骨化,前方压迫明显,压迫坚硬,无弹性,发现后一般有很长的病史,并且对脊髓的破坏更重。T2W1高信号提示脊髓损伤明显,一般合并疾病持续时间长等特点。国外有研究报道的另外一个影响预后的因素是复合肌肉动作电位平均比值(CMAP-r),该文献中报道了54例近端肌萎缩型颈椎病患者接受颈椎手术治疗,记录了三角肌和肱二头肌复合肌肉动作电位,并计算了两块肌肉(三角肌和肱二头肌)受影响侧复合肌肉动作电位振幅与正常侧复合肌肉动作电位振幅的比值,并将CMAP-r作为神经受累的严重程度,结果提示预后差的患者CMAP-r低于预后良好的患者[42]。"

| [1] KEEGAN JJ. The cause of dissociated motor loss in the upper extremity with cervical spondylosis. J Neurosurg. 1965;23(5):528-536. [2] BRAIN WR, NORTHFIELD D, WILKINSON M. The neurological manifestations of cervical spondylosis. Brain. 1952;75(2):187-225. [3] CRANDALL PH, BATZDORF U. Cervical spondylotic myelopathy. J Neurosurg. 1966;25(1):57-66. [4] SOBUE I, KATO H, YANAGI T. Clinical characteristics and classification of cervical spondylotic myelopathy. Rinsho Seikei-gaku.1975;10:999-1006 (in Japanese). [5] 王洪立,吕飞舟,马晓生,等.颈椎病伴上肢近端肌萎缩的临床诊断与手术治疗[J].中华骨科杂志,2017,37(4):210-216. [6] GEBERE-MICHAEL SG, JOHNSTON JC, METAFERIA GZ, et al. Bilaterally symmetric cervical spondylotic amyotrophy: a novel presentation and review of the literature. J Neurol Sci. 2010;290(1-2):142-145. [7] SONOO M. Cervical Spondylotic Amyotrophy. Brain Nerve. 2016;68(5):509-519. [8] JIANG SD, JIANG LS, DAI LY. Cervical spondylotic amyotrophy. Eur Spine J. 2011;20(3):351-357. [9] LI T, SHI G, SHI L, et al. Clinical features and long-term surgical outcomes of patients with cervical spondylotic amyotrophy. World Neurosurg. 2019; 121:e172-e180. [10] KAMEYAMA T, ANDO T, YANAGI T, et al. Cervical spondylotic amyotrophy. Magnetic resonance imaging demonstration of intrinsic cord pathology. Spine (Phila Pa 1976). 1998;23(4):448-452. [11] MATSUNAGA S, SAKOU T, IMAMURA T, et al. Dissociated motor loss in the upper extremities. Clinical features and pathophysiology. Spine (Phila Pa 1976). 1993;18(14):1964-1967. [12] SHINOMIYA K, KOMORI H, MATSUOKA T, et al. Neuroradiologic and electrophysiologic assessment of cervical spondylotic amyotrophy. Spine (Phila Pa 1976). 1994;19(1):21-25. [13] TAUCHI R, IMAGAMA S, INOH H, et al. Risk factors for a poor outcome following surgical treatment of cervical spondylotic amyotrophy: a multicenter study. Eur Spine J. 2013;22(1):156-161. [14] INUI Y, MIYAMOTO H, SUMI M, et al. Clinical outcomes and predictive factors relating to prognosis of conservative and surgical treatments for cervical spondylotic amyotrophy. Spine (Phila Pa 1976). 2011;36(10):794-799. [15] IMAJO Y, KATO Y, KANCHIKU T, et al. Pathology and prognosis of proximal-type cervical spondylotic amyotrophy: new assessment using compound muscle action potentials of deltoid and biceps brachii muscles. Spine (Phila Pa 1976). 2011;36(7):E476-E481. [16] TOFUKU K, KOGA H, YONE K, et al. Conservative treatment with hyperbaric oxygen therapy for cervical spondylotic amyotrophy. Spinal Cord. 2011;49(6):749-753. [17] WANG HL, LI HC, JIANG JY, et al. Evaluation of characteristics and surgical outcomes in cervical spondylotic amyotrophy. Indian J Orthop. 2014;48(5):511-517. [18] TAKEBAYASHI T, YOSHIMOTO M, IDA K, et al. Minimum invasive posterior decompression for cervical spondylotic amyotrophy. J Orthop Sci. 2013; 18(2):205-207. [19] FUJIWARA Y, TANAKA N, FUJIMOTO Y, et al. Surgical outcome of posterior decompression for cervical spondylosis with unilateral upper extremity amyotrophy. Spine (Phila Pa 1976). 2006;31(20):E728-E732. [20] TOLEDANO M, BARTLESON JD. Cervical spondylotic myelopathy. Neurol Clin. 2013;31(1):287‑305. [21] TAKAHASHI T, HANAKITA J, MINAMI M, et al. Cervical spondylotic amyotrophy: case series and review of the literature. Neurospine. 2019;16(3):579-588. [22] STĘPIEŃ A, MAZURKIEWICZ Ł, MAŚLANKO K, et al. Cervical rotation, chest deformity and pelvic obliquity in patients with spinal muscular atrophy. BMC Musculoskelet Disord. 2020;21(1):726. [23] ZHENG C, JIN X, ZHU Y, et al. Repetitive nerve stimulation as a diagnostic aid for distinguishing cervical spondylotic amyotrophy from amyotrophic lateral sclerosis. Eur Spine J. 2017;26(7):1929-1936. [24] 冯小宁,叶霞,马迅,等.平山病临床相关研究的进展[J].中华骨科杂志, 2019,39(8):518-524. [25] 复旦大学附属华山医院骨科,北京大学第三医院骨科,《中华骨科杂志》编辑部,等.平山病临床诊疗规范国际指南[J].中华骨科杂志, 2019,39(8):452-457. [26] HIRAYAMA K. Juvenile muscular atrophy of unilateral upper extremity (Hirayama disease) half-century progress and establishment since its discovery. Brain Nerve. 2008;60(1):17-29. [27] 王洪光.3.0T磁共振多平面成像对肩峰下撞击综合征的临床诊断影响分析[J].中国医疗器械信息,2021,27(4):137-138. [28] GERVASIO O, GAMBARDELLA G, ZACCONE C, et al. Simple decompression versus anterior submuscular transposition of the ulnar nerve in severe cubital tunnel syndrome: a prospective randomized study. Neurosurgery. 2005;56(1):108-117. [29] 孟亚轲,张健,杨勇,等.肌萎缩型颈椎病13例的诊治观察[J].中华医学杂志, 2017,97(17):1320-1323. [30] LIU T, XU W, CHENG T, et al. Anterior versus posterior surgery for multilevel cervical myelopathy, which one is better? A systematic review. Eur Spine J. 2011;20(2):224-235. [31] YE X, SUN Y. Advances in research of cervical spondylotic amyotrophy. Zhonghua Wai Ke Za Zhi. 2019;57(9):717-720. [32] YAMADA T, YOSHII T, USHIO S, et al. Surgical outcomes for distal-type cervical spondylotic amyotrophy: a multicenter retrospective analysis of 43 cases. Eur Spine J. 2019;28(10):2333-2341. [33] 关海山,李承罡,史洁,等.前路减压融合术与后路单开门椎管扩大成形术治疗多节段脊髓型颈椎病的中期随访研究[J].中华骨科杂志, 2019,39(17):1044-1052. [34] SRINIVASA RAO NV, RAJSHEKHAR V. Distal-type cervical spondylotic amyotrophy: incidence and outcome after central corpectomy. J Neurosurg Spine. 2009;10(4):374-379. [35] BAXTER C, MILLER TA, ROSS DC, et al. Treatment of cervical spondylotic amyotrophy with nerve transfers. J Hand Surg Am. 2018;43(7):684.e1-684.e4. [36] UCHIDA K, NAKAJIMA H, SATO R, et al. Multivariate analysis of the neurological outcome of surgery for cervical compressive myelopathy. J Orthop Sci. 2005;10(6):564-573. [37] 孟亚轲,张健,杨勇,等.肌萎缩型颈椎病13例的诊治观察[J].中华医学杂志, 2017,97(17):1320-1323. [38] 钟卓霖,胡建华,翟吉良,等.伴肌萎缩颈椎病的手术治疗效果[J].中华骨与关节外科杂志,2015,8(3):209-213. [39] UCHIDA K, NAKAJIMA H, YAYAMA T, et al. Anterior and posterior decompressive surgery for progressive amyotrophy associated with cervical spondylosis: a retrospective study of 51 patients. J Neurosurg Spine. 2009;11(3):330-337. [40] LIU X, MIN S, ZHANG H, et al. Anterior corpectomy versus posterior laminoplasty for multilevel cervical myelopathy: a systematic review and meta-analysis. Eur Spine J. 2014;23(2):362-372. [41] LU CB, MA ZS, HU JB, et al. Evaluation of anterior decompression surgical outcomes of proximal-type cervical spondylotic amyotrophy: a retrospective study. Orthop Surg. 2020;12(3):734-740. [42] IMAJO Y, NISHIDA N, FUNABA M, et al. Preoperative factors that predict fair outcomes following surgery in patients with proximal cervical spondylotic amyotrophy. A retrospective study. Spinal Cord. 2020;58(3):348-355. [43] ZHANG JT, YANG DL, SHEN Y, et al. Anterior decompression in the management of unilateral cervical spondylotic amyotrophy. Orthopedics. 2012;35(12):e1792-e1797. [44] ZHANG J, CUI C, LIU Z, et al. Predisposing factors for poor outcome of surgery for cervical spondylotic amyotrophy: a multivariate analysis. Sci Rep. 2016;6:39512. |
| [1] | Wang Jianping, Zhang Xiaohui, Yu Jinwei, Wei Shaoliang, Zhang Xinmin, Xu Xingxin, Qu Haijun. Application of knee joint motion analysis in machanism based on three-dimensional image registration and coordinate transformation [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(在线): 1-5. |
| [2] | Yu Chengxiang, Liu Lehong, Li Wenbo, Chen Jinshi, Ran Chunlei, Wang Zhongping. Correlation between spine-pelvic sagittal parameters and prognosis of vertebroplasty in the treatment of thoracolumbar osteoporotic vertebral compression fractures [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1412-1417. |
| [3] | Zhu Chan, Han Xuke, Yao Chengjiao, Zhang Qiang, Liu Jing, Shao Ming. Acupuncture for Parkinson’s disease: an insight into the action mechanism in animal experiments [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1272-1277. |
| [4] | Tang Wenjing, Wu Siyuan, Yang Chen, Tao Xi. Inflammatory responses in post-stroke depression [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1278-1285. |
| [5] | Xuan Juanjuan, Bai Hongtai, Zhang Jixiang, Wang Yaoquan, Chen Guoyong, Wei Sidong. Role of regulatory T cell subsets in liver transplantation and progress in clinical application [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1143-1148. |
| [6] | Zhang Yujie, Yang Jiandong, Cai Jun, Zhu Shoulei, Tian Yuan. Mechanism by which allicin inhibits proliferation and promotes apoptosis of rat vascular endothelial cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1080-1084. |
| [7] | He Junjun, Huang Zeling, Hong Zhenqiang. Interventional effect of Yanghe Decoction on synovial inflammation in a rabbit model of early knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 694-699. |
| [8] | Liu Yubo, Zhang Huizeng, Zhang Tongrun, Sui Gengyi, Ma Nan, Cheng Xu, Gao Xupeng, Xu Jing, Wang Chaoliang. Correlation analysis between the morphological changes of ankle acupoints and the ankle function after ankle fracture surgery [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(3): 440-445. |
| [9] | Zhang Xiaoyun, Li Huanan, Chen Feng, Chai Yuan, Gan Bin, Li Song, Chen Dingpeng. Potential molecular mechanism of Guizhi Shaoyao Zhimu Decoction in the treatment of gouty arthritis based on network pharmacology and molecular docking [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(2): 245-252. |
| [10] | Liu Xiaopeng, Zhang Sisen. Predictive value of blood biomarkers for brain injury after cardiac arrest [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(2): 302-307. |
| [11] | Chen Jincheng, Zhu Guotao, Qin Xiaofei, Chen Yancheng, Luo Jun, Liu Hongwen, Wu Yijing, Xu Jie. Guilu Erxian Gum medicated serum mediated osteogenic differentiation of rat bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(13): 2020-2026. |
| [12] | Gong Chao, Zhang Yuqiang, Wang Wei. Role and mechanism of cell therapy in repair of peripheral nerve injury [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(13): 2114-2119. |
| [13] | Wang Jianping, Zhang Xiaohui, Yu Jinwei, Wei Shaoliang, Zhang Xinmin, Xu Xingxin, Qu Haijun. Application of knee joint motion analysis in machanism based on three-dimensional image registration and coordinate transformation [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(12): 1922-1926. |
| [14] | Xu Renjie, Zhong Qiao, Liu Yubo, Yu Xiao, Yan Yongqing, Saijilafu, Yang Huilin, Chen Guangxiang. Quantitative analysis of transcriptome and proteome of knee joint synovial cells with osteopontin knockdown [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(11): 1680-1685. |
| [15] | Li Zhongkang, Zheng Jiahua, Tian Yanpeng, Huang Xianghua. Latest progress and mechanisms of mesenchymal stem cells on premature ovarian failure [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(1): 141-147. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||