Chinese Journal of Tissue Engineering Research ›› 2020, Vol. 24 ›› Issue (14): 2235-2242.doi: 10.3969/j.issn.2095-4344.2484
Previous Articles Next Articles
Role of osteogenic signaling pathway in non-traumatic femoral head necrosis
Xu Canhong1, Chen Yueping2, Zhang Xiaoyun2
- 1Guangxi University of Chinese Medicine, Nanning 530001, Guangxi Zhuang Autonomous Region, China; 2Department of Traumatic Orthopedics and Hand Surgery, Ruikang Hospital Affiliated to Guangxi University of Chinese Medicine, Nanning 530011, Guangxi Zhuang Autonomous Region, China
-
Received:2019-05-15Revised:2019-05-25Accepted:2019-07-15Online:2020-05-18Published:2020-03-16 -
Contact:Chen Yueping, MD, Doctoral supervisor, Chief physician, Department of Traumatic Orthopedics and Hand Surgery, Ruikang Hospital Affiliated to Guangxi University of Chinese Medicine, Nanning 530011, Guangxi Zhuang Autonomous Region, China Zhang Xiaoyun, Master, Attending physician, Department of Traumatic Orthopedics and Hand Surgery, Ruikang Hospital Affiliated to Guangxi University of Chinese Medicine, Nanning 530011, Guangxi Zhuang Autonomous Region, China -
About author:Xu Canhong, Master candidate, Guangxi University of Chinese Medicine, Nanning 530001, Guangxi Zhuang Autonomous Region, China -
Supported by:the National Natural Science Foundation of China, No. 81760796; the Natural Science Foundation of Guangxi Zhuang Autonomous Region, No. 2015GXNSFAA139136; the Key Project of Health Department of Guangxi Zhuang Autonomous Region, No. S201419-05; the Basic Ability Enhancement Project of Young Teachers in Guangxi Colleges and Universities, No. 2019KY0352 and KY2016YB204; the Ten Programs of Traditional Chinese Medicine Development, No. (2018)1; the Qihuang Engineering Breeding Project of Guangxi University of Chinese Medicine, No. 030030001-04131804804-500101; the Graduate Education Innovation Program of Guangxi University of Chinese Medicine in 2019, No. YCSY201900106
CLC Number:
Cite this article
Xu Canhong, Chen Yueping, Zhang Xiaoyun. Role of osteogenic signaling pathway in non-traumatic femoral head necrosis[J]. Chinese Journal of Tissue Engineering Research, 2020, 24(14): 2235-2242.
share this article
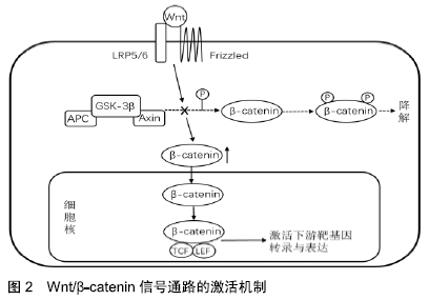
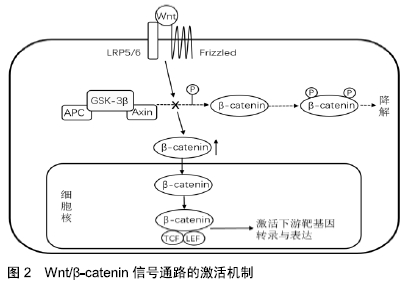
2.1 Wnt/β-catenin信号通路 Wnt/β-catenin信号通路广泛存在于多细胞动物中,是一条在物种进化中高度保守的信号通路[3],因为有β-catenin参与信号转导故又被称为经典Wnt通路。其构成主要包括:Wnt、卷曲蛋白、β-catenin、低密度脂蛋白受体相关蛋白5/6、GSK-3β、T细胞因子/淋巴增强因子等[4]。Wnt/β-catenin信号通路的激活通过活化的Wnt与细胞膜表面的卷曲蛋白受体、低密度脂蛋白受体相关蛋白5/6受体结合作为起始信号,Wnt信号进入到细胞内阻碍GSK-3β复合体对β-catenin的降解,β-catenin在细胞内蓄积并转移至细胞核内与T细胞因子/淋巴增强因子结合形成β-catenin-T细胞因子/淋巴增强因子复合体,激活下游靶基因(如Runx2、c-myc、cylinD1、Osterix等)转录并调节其表达,能够调控骨髓间充质干细胞成骨-成脂分化并促进成骨细胞的增殖分化[5-6],见图2。 "
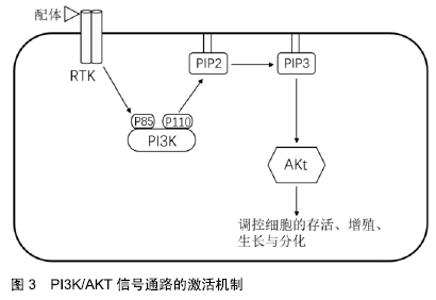
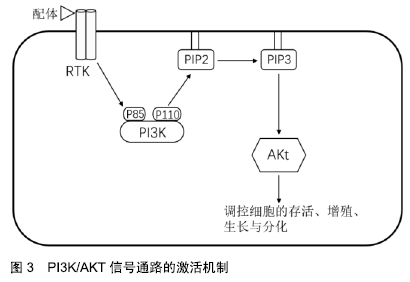
股骨头坏死的早期病理变化是骨细胞坏死凋亡、脂肪细胞增多、造血组织减少,这可能与骨髓间充质干细胞的成骨-成脂分化失衡密切相关。而Wnt/β-catenin信号通路在调节骨髓间充质干细胞的成骨成脂分化中发挥重要作用,故在股骨头坏死的相关信号通路中Wnt/β-catenin信号通路是研究热点之一。最近的一项研究对患者股骨头坏死区与骨盆中正常区骨髓间充质干细胞进行对比,发现2种细胞群的细胞增殖和表面标志物表达均存在显著差异:股骨头坏死区骨髓间充质干细胞比骨盆中正常区中的成骨分化显著降低,Runx2和β-catenin显著下降,GSK-3β表达显著升高,结果提示股骨头坏死区的骨髓间充质干细胞中存在Wnt信号通路受损[7]。然而通过GSK-3β抑制剂氯化锂干预股骨头坏死区的骨髓间充质干细胞则能抑制GSK-3β的表达,激活Wnt/β-catenin信号通路转导而增加成骨分化改善股骨头坏死,由此得出GSK-3β可能是干预股骨头坏死的重要治疗靶点。NIE等[8]通过糖皮质激素诱导的股骨头坏死大鼠模型发现,经氯化锂治疗后的股骨头坏死大鼠股骨头的空隙率和骨细胞凋亡百分比明显降低,原因是氯化锂处理后明显抑制GSK-3β及相关凋亡蛋白的表达,降低了糖皮质激素诱导的成骨细胞凋亡和骨坏死。LI等[9]研究发现局部应用掺锂的磷酸钙骨水泥治疗骨质疏松性骨折,可通过生物活性物质释放的锂激活Wnt/β-catenin信号通路来加速骨再生,实验得出锂/磷酸钙骨水泥提取物的锂离子(Li+)释放后能刺激成骨细胞的增殖和分化,有利于成骨细胞分化的最佳锂浓度为50-100 mmol/L。在骨质疏松大鼠模型中,锂/磷酸钙骨水泥较传统磷酸钙骨水泥显著增强成骨分化并引起更有效的骨形成,并且锂/磷酸钙骨水泥保持了磷酸钙骨水泥的生物活性和生物相容性,同时也显示出比磷酸钙骨水泥更好的骨传导性和骨整合度。因此,将锂/磷酸钙骨水泥作为新型生物医学填充材料应用于骨质疏松型股骨头坏死具有一定的前景,但目前国内外相关的研究较少,需要进一步探索。 分泌型卷曲相关蛋白是Wnt/β-catenin信号通路的一种胞外拮抗分子,由分泌型卷曲相关蛋白1-分泌型卷曲相关蛋白5组成,能与受体竞争结合Wnt蛋白,从而阻断Wnt/β-catenin信号通路转导[10]。张晨等[11]研究表明,使用分泌型卷曲相关蛋白1通过抑制Wnt/β-catenin信号通路可以加速骨坏死及骨细胞凋亡,加剧股骨头坏死的发生,研究结果证明Wnt/β-catenin信号通路的异常参与了股骨头坏死早期病变。Dkks也是Wnt/β-catenin信号通路的一种抑制因子,可以与细胞膜共受体低密度脂蛋白受体相关蛋白5/6结合,从而抑制Wnt信号转导,影响成骨细胞分化、增殖。ZHUN等[12]将Dkk-1 RNAi的同种异体骨髓间充质干细胞植入糖皮质激素诱导的股骨头坏死大鼠模型中,发现通过下调Dkk-1的表达可以防止大鼠股骨头坏死的进展。因此通过抑制拮抗分子表达激活Wnt/β-catenin信号通路可缓解股骨头坏死进展,但能否找到Wnt/β-catenin信号通路的促进剂或靶向启动剂将是今后的研究重点。 2.2 PPARγ信号通路 PPARγ是一种广泛表达的核转录因子,在骨髓间充质干细胞的分化中发挥重要作用,以抑制成骨分化为代价促进成脂分化[13],是近些年的研究热点之一。骨髓间充质干细胞向脂肪细胞或成骨细胞分化主要受2个关键转录因子PPARγ2和Runx2的转录调控,PPARγ2在脂肪细胞分化过程中高度表达,并调节脂肪生成相关基因的表达;Runx2是最重要的成骨转录因子之一,能诱导成骨基因表达,增加成骨细胞分化[14]。虽然PPARγ2和Runx2的转录调节已被广泛研究,但调控骨髓间充质干细胞成骨成脂分化平衡的潜在分子机制仍不清楚。 有研究报道糖皮质激素导致股骨头坏死的主要原因是骨髓间充质干细胞的成脂成骨分化异常,表现为脂肪细胞分化增加,成骨细胞分化抑制[15]。糖皮质激素诱导的人和动物中的骨髓间充质干细胞中均存在PPARγ基因的高表达,Runx2、β-catenin基因的低表达,Wnt/β-catenin信号通路被抑制,而PPARγ在骨髓基质细胞中表达水平的增加促进脂肪细胞的形成,进一步加剧股骨头坏死的发生[16]。由此可见PPARγ在调节骨髓基质细胞向脂肪细胞的分化中发挥关键作用,靶向抑制PPARγ基因表达,调控骨髓间充质干细胞的成骨成脂分化平衡,可能是阻止股骨头坏死进展的一个新方法。 LI等[17]通过地塞米松诱导的大兔模型证实,地塞米松会使兔的股骨头骨髓坏死、脂肪细胞肥大增殖、造血功能减退、小梁变薄稀疏、骨细胞腔隙增大,最终导致股骨头骨坏死,而携带靶向PPARγ基因siRNA的重组腺病毒穿梭载体则能防止这种现象的发生,研究表明靶向PPARγ基因的siRNA可通过抑制骨髓间充质干细胞的成脂分化和伴随的成骨增强,防止类固醇诱导的兔骨坏死。基因治疗作为一种快速发展的技术具有广阔的应用前景,使用腺病毒载体将siRNA递送到靶组织中以干扰疾病特异性基因的表达,或许能为预防股骨头坏死提供新的途径。王耀清等[18]研究双酚A二缩水甘油醚单独或与锂盐结合治疗家兔激素性股骨头坏死的效果,体外实验发现双酚A二缩水甘油醚抑制了兔的骨髓间充质干细胞成脂分化,脂肪分化主要调节因子PPARγ和C/EBPα的表达也受到抑制,并且与锂盐结合后这些生物活性得到进一步增强;体内研究结果显示,双酚A二缩水甘油醚单独治疗或与锂盐结合增加了β-catenin和RUNX2的表达,抑制了PPARγ和C/EBPα的表达,降低了坏死组织中血清总胆固醇和游离脂肪酸水平,降低了骨坏死发生率,减少脂肪细胞分化,并且改善了骨密度及骨质量。但该实验仅局限于使用单一剂量的双酚A二缩水甘油醚和氯化锂进行研究,未进一步对不同剂量下的实验结果进行探讨,也未能确定预防股骨头坏死发展的最佳剂量,这值得进一步研究。 2.3 TGF-β/Smad信号通路 TGF-β信号的转导参与绝大多数细胞过程,特别是在骨细胞的早期增殖、分化、成熟及凋亡过程中发挥着重要作用,是目前成骨相关信号通路的研究热点之一。TGF-β超家族系由40多种具有多功能生物学活性的细胞因子所构成,包括转化生长因子、骨形态发生蛋白、激活素和抑制素。TGF-β信号转导通过与受体丝氨酸/苏氨酸激酶结合形成异聚复合物,磷酸化后作用于底物Smad蛋白,活化的Smad蛋白充当信使将信号从细胞膜传递到细胞核内,由此协同核内的其他因子激活或抑制靶基因的转录与表达[19]。TGF-β和BMP都属于TGF-β超家族。TGF-β包括TGF-β1至 TGF-β5多种亚型,其中TGF-β1、TGF-β2、TGF-β3为哺乳动物所仅有,TGF-β是参与骨细胞功能和代谢的重要细胞因子,它不仅对骨细胞发挥促有丝分裂作用,还能减少骨胶原的丢失,增加骨沉积速率,促进成骨细胞分化[20]。BMP是TGF-β超家族中最大的家族,是广泛分布在细胞外基质上的酸性糖蛋白[21],包括BMP2至BMP16多种亚型,在调节骨形成、骨发育中发挥重要作用,其中BMP2是所有亚型中作用最强的成骨诱导因子,可明显增促进骨髓间充质干细胞向成骨细胞分化,增加骨形成量,提高骨折愈合强度和速度,因此也是骨再生领域的研究热点[22]。Smad作为TGF-β受体信号转导的直接作用底物,负责在成骨和软骨形成分化过程中转导BMP和TGF-β信号,是参与调节骨细胞增殖分化的关键环节之一[23]。 大量实验研究证实了TGF-β/Smads信号通路与股骨头坏死间存在密切的联系,促进TGF-β/Smad信号通路转导,能够有效抑制成骨细胞凋亡,同时可提高碱性磷酸酶水平,加速成骨分化,促进股骨头坏死的骨修复和再生。TAO等[24]研究发现,成人非创伤性股骨头坏死患者股骨头标本中存在TGF-β1表达明显降低,证明了TGF-β/Smad通路异常参与了股骨头坏死的病变过程,并提出通过直接内注射或靶向过表达外源性引入TGF-β1可能是非创伤性股骨头坏死某些阶段骨损伤和骨修复的有效治疗方法。BAI等[25]研究发现,股骨头坏死模型大鼠血清中TGF-β和Smad7水平较正常对照组降低,使用microRNA(miR)-27a模拟物能显著提高TGF-β和Smad7蛋白表达,有效增加碱性磷酸酶、BMP2、Runx2和骨粘连蛋白mRNA的表达,具有促进成骨分化和细胞增殖的作用,并且能降低细胞中caspase-3/9和Bax等凋亡蛋白的表达以抑制骨细胞凋亡,结果表明成骨细胞中TGF-β/Smad7信号通路的激活可能是miR-27a调节激素诱导股骨头坏死的潜在机制。 YANG等[26]在动物实验中发现淫羊藿和女贞子的活性成分能上调转TGF-β1、Smad2-4的表达,刺激TGF-β1/Smad信号通路的激活,提高骨形成标志物碱性磷酸酶、骨钙素的血清水平,降低骨吸收标志物抗酒石酸酸性磷酸酶的血清水平,促进成骨分化,逆转地塞米松诱导的成骨细胞抑制和骨吸收,增加骨强度和骨密度,改善骨组织结构,维持骨的代谢稳态。另一项关于淫羊藿苷的研究同样发现,淫羊藿苷可防止糖皮质激素相关股骨头坏死大鼠模型中的骨丢失,通过介导促进BMP2/Runx2信号通路中的成骨,并通过抑制PPARγ介导的糖皮质激素诱导途径抑制脂肪形成,促进骨修复和预防或延缓糖皮质激素相关股骨头坏死的进展[27]。因此通过促进TGF-β或BMP在股骨头坏死部位的表达,激活TGF-β/Smad信号通路转导或许是治疗股骨头坏死的可行办法,目前研究发现多种中药活性成分如淫羊藿苷、女贞苷等对TGF-β/Smad信号通路具有促进作用,但其中具体的作用机制仍未阐明,需要更深入的探究和思考。 2.4 PI3K/AKT信号通路 PI3K/AKT信号通路由PI3K和下游效应器AKT构成,其中PI3K包括调控亚基p85和催化亚基p110,当配体与酪氨酸激酶(RTK)类受体结合使胞质结构域中酪氨酸残基自磷酸化,重新聚集对接蛋白的磷酸化酪氨酸残基与调控亚基p85结合时,催化亚基p110被激活,细胞膜内层的底物磷脂酰肌醇-4,5二磷酸(PIP2)被p110亚基磷酸化,形成磷脂酰肌醇-3,4,5三磷酸(PIP3),PIP3充当膜内的第二信使激活下游的AKT信号,从而参与调控细胞存活、增殖、生长、分化等生理过程[28],见图3。 "

PI3K/AKT信号通路的激活在成骨细胞增殖和分化过程中是必需的。最近的一项研究表明,适当浓度的镁离子(6-10 mmol/L)可引起成骨细胞黏附能力、细胞活力、碱性磷酸酶活性、细胞外基质矿化水平和成骨细胞分化相关基因表达水平的增强,其机制是该浓度下的镁离子能激活PI3K/AKT信号通路促进成骨细胞的分化成熟[29]。在成骨细胞的抗凋亡中,PI3K/AKT信号通路同样起重要作用。有研究发现miR-28-3p激活PI3K/AKT信号通路导致促凋亡蛋白Bax表达量的下调和抗凋亡蛋白Bc1-2的上调,这可以导致Bax/Bc1-2比例下降进而抑制凋亡的进行,从而促进成骨细胞增殖,加速骨折的愈合[30]。 PI3K/AKT信号通路的异常表达与股骨头坏死的发生发展有着密切关系。CHEN等[31]研究发现乙醇抑制了成骨基因Runx2和骨钙蛋白的表达,下调成骨分化,损害AKT向质膜的募集,并抑制PI3K/AKT信号通路的表达,导致股骨头坏死的发生;而一种新型的AKT激活剂SC-79注射液也许可以作为预防酒精诱导的股骨头坏死的治疗方法,SC-79能够逆转乙醇对PI3K/AKT信号通路的抑制作用,进而抑制酒精引起的骨坏死,在对照实验中,SC-79与乙醇联合组比对照组(乙醇组)的股骨头坏死发生率显著降低。另一项激素性股骨头坏死的大鼠模型实验研究发现,红景天能激活PI3K/AKT信号通路并下调成骨细胞中caspase-3表达来减轻地塞米松诱导的成骨细胞凋亡,防止大鼠股骨头坏死的发生[32]。DENG等[33]研究发现糖皮质激素通过抑制PI3K/AKT信号通路的激活,上调成骨细胞和MC3T3-E1细胞中GSK-3β的表达,从而激活caspase3,caspase8和caspase9等凋亡途径诱导骨细胞和成骨细胞的凋亡。有趣的是,有研究发现磷酸化的GSK-3β是PI3K/AKT信号通路与Wnt/ β-catenin信号通路相互连接的关键点[34],通过抑制或剔除GSK-3β的表达,激活PI3K/AKT信号通路与Wnt/ β-catenin信号通路的促成骨分化作用可能是防止糖皮质激素诱导的成骨细胞凋亡的一个治疗或预防靶点。 2.5 MAPK信号通路 MAPK是普遍存在于各种哺乳动物细胞中的一组丝氨酸/苏氨酸蛋白激酶,能被多种外环境所激活,通过三级酶促级联反应进行信号转导,参与细胞生长、分化、凋亡等多种生理过程。MAPK信号通路的信号转导通过3种激酶的依次激活而完成,首先MAPKKK磷酸化并激活MAPKK,接着MAPK也被磷酸化,活化的MAPK磷酸化激活下游多种靶基因的表达[35]。目前发现的MAPK家族信号通路主要有3条,分别是ERK信号通路、p38信号通路和JNK信号通路。ERK是最早被发现的一条MAPK信号通路,具有ERK1和ERK2两种亚型,两者在成骨细胞中均有表达,均由MEK1(MAP2K1)和MEK2(MAP2K2)激活[36]。p38是由Brewster在1993年首次发现,有p38α、p38β、p38γ和p38δ四种亚型,主要由上游MAPK激酶MKK3和MKK6激活,其中MKK6能磷酸化所有的p38亚型,MKK3只能磷酸化p38α、p38γ和p38δ[37]。JNK信号通路共有JNK1、JNK2、JNK3三种亚型,其中JNK1和JNK2普遍表达,而JNK3的表达较局限,主要存在于神经元中。 ERK信号通路是骨骼发育及维持骨代谢动态平衡的必要条件,参与调控成骨细胞的增殖、分化、凋亡,并且在骨代谢、炎症反应中也发挥重要作用[38]。一项成人成骨细胞的体外培养研究发现,葛根素可以促进体外培养的成骨细胞的增殖与分化,加快骨形成。主要机制是葛根素通过激活ERK1/2信号通路刺激成骨细胞的细胞周期,激活碱性磷酸酶的表达,促进钙的沉积,最终成骨细胞成熟分化致使骨[39]。股骨头坏死是一种炎症相关性疾病,骨坏死早期存在软骨和软骨下骨的降解和破坏。一项体外实验研究从股骨头坏死患者中分离原代软骨细胞,分别在存在或不存在200 μg/L颗粒体蛋白前体的情况下培养24,48 h,然后收集总核糖核酸并进行实时聚合酶链反应分析,结果表明颗粒体蛋白前体能够诱导ERK1/2信号通路的快速激活,促进聚集蛋白聚糖和胶原蛋白Ⅱ的产生,改善股骨头坏死区域退化软骨的合成代谢,对股骨头坏死有一定的治疗作用[40]。另一项激素性股骨头坏死兔模型研究发现,股骨头缺血坏死后ERK1、ERK2表达显著下降,JNK和p38表达显著上升,经过羟基红花黄色素A治疗后ERK1、ERK2水平有明显升高,JNK和p38水平均有不同程度的降低,这说明羟基红花黄色素A能通过调控ERK、p38和JNK的磷酸化水平,激活或抑制MAPK的相关通路进而抑制股骨头髓腔内的骨坏死并促进成骨细胞增殖、分化加快坏死区的骨修复,对股骨头坏死起一定的治疗作用[41]。由此可见MAPK信号通路的表达与抑制在股骨头坏死的进展中存在一定的关联。 最近的一项大鼠骨髓间充质干细胞细胞体外培养研究报道显示,通过无定形碳薄膜涂层的纯钛金属植入物表面显示出增强的细胞黏附、增殖和成骨分化能力,成骨基因表达、碱性磷酸酶活性、胶原分泌和钙结节形成明显增强。深入研究后发现碳涂层以时间依赖性方式提高表达谱ILK的表达,并显著促进p38的磷酸化,有利于骨髓间充质干细胞的黏附、增殖和成骨分化。但在使用p38抑制剂后,骨髓间充质干细胞对金属植入物表面的成骨分化显著减弱,进一步的揭示ILK/p38信号传导在骨髓间充质干细胞对金属植入物表面的成骨调节中起重要作用[42]。这些发现为无定形碳涂层种植体的未来临床应用提供了依据,也有助于钛种植体的设计和优化,或许能在未来为股骨头坏死的保髋治疗提供新的思路。 2.6 Notch信号通路 Notch信号通路是一条存在于脊椎动物和非脊椎动物中的高度保守通路,通过相邻细胞间的信号转导参与调节细胞的分化、增殖、凋亡等过程,在多细胞生物的细胞分化中起重要作用。Notch基因最早于1917年由Morgan及其同事在突变的果蝇体内发现,缺少该基因的果蝇会出现翅膀边缘缺损,故被命名为Notch基因。该基因在人体的多个系统中均有表达,其信号通路在骨骼系统、心血管系统、中枢神经系统中均发挥重要作用[43]。 Notch信号通路由Notch受体、配体、转录因子及下游靶基因(Hes1、5和Hey等)组成。在哺乳动物中共有4种Notch受体,即Notch1、Notch2、Notch3、Notch4;5种Notch配体,分别为DLL1、DLL3、DLL4、Jagged1和Jagged2[44]。Notch信号通路的激活是不需要胞内第二信使参与的简单信号转导过程,当Notch受体与相邻细胞的Notch配体结合时,经过水解酶的三步切割裂解,Notch受体最终经γ-分泌酶切割后释放胞内域NICD而被活化,NICD进入细胞核内与转录因子特异性结合后激活Hes、Hey等下游靶基因的表达[45]。 Notch信号是调控骨髓间充质干细胞成骨分化和维持骨代谢动态平衡的重要通路之一。有学者在体外实验发现,淫羊藿苷能通过上调Hesl、Runx2 mRNA的表达并增加Noth1、CBF1、Jagged-1蛋白表达,以激活Notch通路的信号转导促进骨髓间充质干细胞向成骨细胞分化[46]。也有研究发现,Notch信号通路可能在协调骨形态发生蛋白诱导骨髓间充质干细胞向成骨细胞分化中对骨代谢和骨重建起重要的调节作用,通过激活BMP/Smad信号通路促进BMP诱导的骨髓间充质干细胞成骨分化[47]。柚皮苷是从中草药骨碎补中提取的一种活性化合物,能够减少骨吸收并促进成骨,已被证明是体外骨髓间充质干细胞成骨分化的有效刺激因子[48]。YU等[49]发现柚皮苷增强大鼠骨髓间充质干细胞的成骨分化,可能是通过激活Notch信号通路实现的,表现为Notch1表达水平增高,碱性磷酸酶活性增加、矿化增强、成骨基因mRNA上调和PPARγ2基因转录水平下调。相反,在应用Notch抑制剂DAPT治疗后引起柚皮苷诱导的Notch1表达水平的部分降低,同样,柚皮苷介导的碱性磷酸酶活性、钙沉积和成骨基因转录水平的上调及PPARγ2基因的下调也被DAPT阻断。 另外,许多研究结论的差异显示着Notch信号通路在成骨细胞的分化中有促进作用的同时又存在抑制作用,这种双向调节作用可能与成骨细胞的不同分化阶段有关。有研究表明,Notch信号通路的转导活化在早期成骨分化中可能起促进成骨作用,而在后期则抑制成骨细胞的分化与成熟,以此维持骨髓间充质干细胞的活性,促进骨髓间充质干细胞增殖,提高成骨分化潜能[50]。有学者通过对激素性股骨头坏死家兔Notch信号通路关键成员进行基因检测发现,股骨头坏死发病是Notch1、Notch2、Notch3、Notch4综合作用结果,其中Notch1和Notch3与股骨头坏死呈负相关,当Notch1与Notch3的活性被抑制时骨髓间充质干细胞的增殖和成骨分化也被抑制,进而造成股骨头坏死的发生。有学者通过动物实验发现中药制剂活血通络汤能缓解家兔的激素性股骨头坏死,机制可能与Notch1的通路的激活有关,通过增加胞内NICD的表达,促进坏死区域的成骨分化或降低破骨分化而参与对细胞增殖分化以及凋亡的调控起到治疗股骨头坏死的作用[51]。总之,Notch信号通路作为调控成骨细胞分化维持骨代谢平衡的关键通路在股骨头坏死的发生发展中有着重要作用,但目前国内外的相关研究仍较少,且许多学者对Notch信号通路的作用众说纷纭,而探索其中的具体作用机制是继续深入研究的目标。 "

| [1] LIU F, WANG W, YANG L, et al.An epidemiological study of etiology and clinical characteristics in patients with nontraumatic osteonecrosis of the femoral head.J Res Med Sci.2017;22(1):15. [2] GOU WL, LU Q, WANG X, et al.Key pathway to prevent the collapse of femoral head in osteonecrosis.Eur Rev Med Pharmacol Sci.201;19(15):2766-2474. [3] MOHAMMED MK, SHAO C, WANG J, et al.Wnt/β-catenin signaling plays an ever-expanding role in stem cell self-renewal, tumorigenesis and cancer chemoresistance.Genes Dis.2016; 3(1):11-40. [4] BURGERS TA, WILLIAMS BO.Regulation of Wnt/β-catenin Signaling within and from Osteocytes.Bone.2013;54(2): 244-249. [5] YAO Q, YU C, ZHANG X, et al.Wnt/β-catenin signaling in osteoblasts regulates global energy metabolism.Bone.2017;97: 175. [6] CHEN Z, ZOU Y, MA J, et al.Apoptosis associated with Wnt/β-catenin pathway leads to steroid-induced avascular necrosis of femoral head.BMC Musculoskelet Disord. 2015; 16(1):132. [7] HUANG L, WANG Y, JIANG Y, et al.High levels of GSK-3β signalling reduce osteogenic differentiation of stem cells in osteonecrosis of femoral head.J Biochem.2018;163:243-251. [8] NIE Z, CHEN S, PENG H.Glucocorticoid induces osteonecrosis of the femoral head in rats through GSK3β-mediated osteoblast apoptosis.Biochem Biophys Res Commun.2019;511:693-699. [9] LI L, PENG X, QIN Y, et al.Acceleration of bone regeneration by activating Wnt/β-catenin signalling pathway via lithium released from lithium chloride/calcium phosphate cement in osteoporosis. Sci Rep.2017;7:45204. [10] ELZI DJ, SONG M, HAKALA K, et al.Wnt antagonist SFRP1 functions as a secreted mediator of senescence.Mol CellBiol. 2012;32(21):4388. [11] 张晨,李苗,马骏,等.Wnt/β-catenin信号通路在大鼠早期激素性股骨头缺血性坏死中的作用机制研究[J].中国修复重建外科杂志, 2016,30(6):661-668. [12] ZHUN W, DONGHAI L, ZHOUYUAN Y, et al.Efficiency of Cell Therapy to GC-Induced ONFH: BMSCs with Dkk-1 Interference Is Not Superior to Unmodified BMSCs.Stem Cells Int. 2018;2018:1340252. [13] YUAN N, LI J, LI M, et al.BADGE, a synthetic antago-nist for PPARgamma, prevents steroid - related osteone-crosis in a rabbit model.BMC Musculoskelet Disord.2018;19(1):129. [14] KIM J, KO J.A novel PPARγ2 modulator sLZIP controls the balance between adipogenesis and osteogenesis during mesenchymal stem cell differentiation.Cell Death Differ. 2014; 21(10):1642-1655. [15] WANG T, TENG S, ZHANG Y, et al.Role of mesenchymal stem cells on differentiation in steroid-induced avascular necrosis of the femoral head.Exp Ther Med.2017;13(2): 669-675. [16] YU Z, FAN L, LI J, et al.Lithium prevents rat steroid-related osteonecrosis of the femoral head by β-catenin activation. Endocrine.2016;52:380-390. [17] LI J, LI Y, WANG Y, et al.Preventive effects of siRNA targeting PPARγ gene on steroid-induced osteonecrosis in rabbits. Connect Tissue Res.2014;55(5-6):322-330. [18] 王耀清,潘振宇,陈帆.BADGE联合锂盐通过抑制PPARγ预防家兔激素性股骨头坏死[J].武汉大学学报(医学版), 2019,40(4): 517-523. [19] CHEN G, DENG C, LI YP.TGF-β and BMP Signaling in Osteoblast Differentiation and Bone Formation.Int J Biol Sci. 2012;8(2):272-288. [20] WU M, CHEN G, LI YP.TGF-β and BMP signaling in osteoblast, skeletal development, and bone formation, homeostasis and disease.Bone Res.2016;4:16009. [21] LI R, LIU J, LI Q, et al.miR-29a suppresses growth and metastasis in papillary thyroid carcinoma by targeting AKT3.Tumor Biol. 2016;37:3987-3996. [22] MD SR, NAZNIN A, HOSSEN MJ.TGF-β/BMP signaling and other molecular events: regulation of osteoblastogenesis and bone formation. Bone Res.2015;3(1):11-30. [23] ZHANG YE.Mechanistic insight into contextual TGF-β signaling. Curr Opin Cell Biol.2018;51:1-7. [24] TAO J, DONG B, YANG LX, et al.TGF-β1 expression in adults with non‑traumatic osteonecrosis of the femoral head.Mol Med Rep. 2017;16:9539-9544. [25] BAI Y, LIU Y, JIN S, et al.Expression of microRNA-27a in a rat model of osteonecrosis of the femoral head and its association with TGF-β/Smad7 signalling in osteoblasts.Int J Mol Med. 2019;43(2):850-860. [26] YANG Y, NIAN H, TANG X, et al.Effects of the combined Herba Epimedii and Fructus Ligustri Lucidi on bone turnover and TGF-β1/Smads pathway in GIOP rats.J Ethnopharmacol. 2017; 201(Complete):91-99. [27] HUANG Z, CHENG C, CAO B, et al.Icariin Protects against Glucocorticoid-Induced Osteonecrosis of the Femoral Head in Rats.Cell Physiol Biochem.2018;47:694-706. [28] MANNING BD, TOKER A. AKT/PKB Signaling: Navigating the Network.Cell.2017;169(3):381-405. [29] WANG J, MA XY, FENG YF, et al.Magnesium Ions Promote the Biological Behaviour of Rat Calvarial Osteoblasts by Activating the PI3K/Akt Signalling Pathway.Biol Trace Elem Res. 2017;179:284-293. [30] 徐栋.microRNA-28-3p通过抑制Sox6并激活PI3K/AKT通路促进骨折愈合的研究[D].青岛:山东大学,2017. [31] CHEN YX, TAO SC, XU ZL, et al.Novel Akt activator SC-79 is a potential treatment for alcohol-induced osteonecrosis of the femoral head.Oncotarget.2017;8(19):31065-31078. [32] XUE XH, FENG ZH, LI ZX, et al.Salidroside inhibits steroid-induced avascular necrosis of the femoral head via the PI3K/Akt signaling pathway:In vitroandin vivostudies.Mol Med Rep. 2018;17(3):3751-3757. [33] DENG S, DAI G, CHEN S, et al.Dexamethasone induces osteoblast apoptosis through ROS-PI3K/AKT/GSK3β signaling pathway.Biomed Pharmacother.2019;110:602-608. [34] HU J, MAO Z, HE S, et al.Icariin protects against glucocorticoid induced osteoporosis, increases the expression of the bone enhancer DEC1 and modulates the PI3K/Akt/GSK3β/β-catenin integrated signaling pathway. Biochem. Pharmacol. 2017;136:109-121. [35] ARTHUR SC, LEY SC.Mitogen-activated protein kinases in innate immunity[J].Nat Rev Immunol.2013;13(9):679-692. [36] GREENBLATT MB, SHIM JH, GLIMCHER LH. Mitogen-Activated Protein Kinase Pathways in Osteoblasts. Ann Rev Cell DevBiol. 2013;29(1):63-79. [37] THOUVEREY C, CAVERZASIO J.The p38α MAPK positively regulates osteoblast function and postnatal bone acquisition. Cell Mol Life Sci.2012;69(18):3115-3125. [38] KIM JM, YANG YS, PARK KH, et al.The ERK MAPK Pathway Is Essential for Skeletal Development and Homeostasis.Int J Mol Sci.2019;20(8):1803-1817. [39] 钟海波,郭祥,黄琳惠.葛根素通过ERK1/2和p38 MAPK信号通路刺激成骨分化和骨形成的机制[J].中国比较医学杂志,2019, 29(2):78-83. [40] HAN Y, SI M, ZHAO Y, et al. Progranulin Protects Against Osteonecrosis of the Femoral Head by Activating ERK1/2 Pathway.Inflammation.2017;40:946-955. [41] 齐振熙,万甜,吴敏瑞,等.羟基红花黄色素A不同给药方式对激素性股骨头缺血坏死模兔ERK1/2、JNK和p38蛋白表达的影响[J].中华中医药杂志,2014,29(9):2927-2930. [42] YUE G, SONG W, XU S, et al.Role of ILK/p38 pathway in mediating the enhanced osteogenic differentiation of bone marrow mesenchymal stem cells on amorphous carbon coating. Biomater Sci.2019;7:975-984. [43] PENTON AL, LEONARD LD, SPINNER NB.NOTCH signaling in human development and disease.Semin Cell Devl Biol. 2012;23(4):450-457. [44] CANALIS E.Notch in skeletal physiology and disease. Osteoporos Int.2018;29:2611-2621. [45] GURUHARSHA KG, KANKEL MW, ARTAVANIS-TSAKONAS S.The Notch signalling system: recent insights into the complexity of a conserved pathway.Nat Rev Genet.2012; 13(9):654-666. [46] 邓宇,陈廖斌.淫羊藿苷通过激活Notch信号通路促进骨髓间充质干细胞向成骨细胞分化的实验研究[J].中医学报, 2017,32(12): 2393-2398. [47] VIALE-BOURONCLE S, GOSAU M, MORSCZECK C.OTCH1 signaling regulates the BMP2/DLX-3 directed osteogenic differentiation of dental follicle cells.Biochem Biophys Res Commun.2014; 443(2):500-504. [48] LI N, JIANG Y, WOOLEY PH, et al.Naringin promotes osteoblast differentiation and effectively reverses ovariectomy-associated osteoporosis.J Orthop Sci.2013;18: 478-485. [49] YU GY, ZHENG GZ, CHANG B, et al.Naringin Stimulates Osteogenic Differentiation of Rat Bone Marrow Stromal Cells via Activation of the Notch Signaling Pathway.Stem Cells Int. 2016;2016: 7130653. [50] ZANOTTI S, CANALIS E.Notch Signaling and the Skeleton. Endocr Rev.2016;37(3):223-253. [51] 蔡万翔.活血通络汤在SANFH家兔造模过程中干预Notch1、HERP1及bFGF的实验研究[D].成都:成都中医药大学,2018. |
| [1] | Hou Jingying, Yu Menglei, Guo Tianzhu, Long Huibao, Wu Hao. Hypoxia preconditioning promotes bone marrow mesenchymal stem cells survival and vascularization through the activation of HIF-1α/MALAT1/VEGFA pathway [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 985-990. |
| [2] | Liang Xueqi, Guo Lijiao, Chen Hejie, Wu Jie, Sun Yaqi, Xing Zhikun, Zou Hailiang, Chen Xueling, Wu Xiangwei. Alveolar echinococcosis protoscolices inhibits the differentiation of bone marrow mesenchymal stem cells into fibroblasts [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 996-1001. |
| [3] | Geng Yao, Yin Zhiliang, Li Xingping, Xiao Dongqin, Hou Weiguang. Role of hsa-miRNA-223-3p in regulating osteogenic differentiation of human bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1008-1013. |
| [4] | Lun Zhigang, Jin Jing, Wang Tianyan, Li Aimin. Effect of peroxiredoxin 6 on proliferation and differentiation of bone marrow mesenchymal stem cells into neural lineage in vitro [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1014-1018. |
| [5] | Zhu Xuefen, Huang Cheng, Ding Jian, Dai Yongping, Liu Yuanbing, Le Lixiang, Wang Liangliang, Yang Jiandong. Mechanism of bone marrow mesenchymal stem cells differentiation into functional neurons induced by glial cell line derived neurotrophic factor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1019-1025. |
| [6] | Pei Lili, Sun Guicai, Wang Di. Salvianolic acid B inhibits oxidative damage of bone marrow mesenchymal stem cells and promotes differentiation into cardiomyocytes [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1032-1036. |
| [7] | Wang Shiqi, Zhang Jinsheng. Effects of Chinese medicine on proliferation, differentiation and aging of bone marrow mesenchymal stem cells regulating ischemia-hypoxia microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1129-1134. |
| [8] | Chen Junyi, Wang Ning, Peng Chengfei, Zhu Lunjing, Duan Jiangtao, Wang Ye, Bei Chaoyong. Decalcified bone matrix and lentivirus-mediated silencing of P75 neurotrophin receptor transfected bone marrow mesenchymal stem cells to construct tissue-engineered bone [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 510-515. |
| [9] | Ma Zhijie, Li Jingyu, Cao Fang, Liu Rong, Zhao Dewei. Influencing factors and biological property of novel biomedical materials: porous silicon carbide coated with bioactive tantalum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 558-563. |
| [10] | Shi Xiaoxiu, Mao Shilong, Liu Yang, Ma Xingshuang, Luo Yanfeng. Comparison of tantalum and titanium (alloy) as orthopedic materials: physical and chemical indexes, antibacterial and osteogenic ability [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 593-599. |
| [11] | Yang Junhui, Luo Jinli, Yuan Xiaoping. Effects of human growth hormone on proliferation and osteogenic differentiation of human periodontal ligament stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(25): 3956-3961. |
| [12] | Sun Jianwei, Yang Xinming, Zhang Ying. Effect of montelukast combined with bone marrow mesenchymal stem cell transplantation on spinal cord injury in rat models [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(25): 3962-3969. |
| [13] | Zhang Lishu, Liu Anqi, He Xiaoning, Jin Yan, Li Bei, Jin Fang. Alpl gene affects the therapeutic effect of bone marrow mesenchymal stem cells on ulcerative colitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(25): 3970-3975. |
| [14] | Hao Xiaona, Zhang Yingjie, Li Yuyun, Xu Tao. Bone marrow mesenchymal stem cells overexpressing prolyl oligopeptidase on the repair of liver fibrosis in rat models [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(25): 3988-3993. |
| [15] | Jiang Tao, Ma Lei, Li Zhiqiang, Shou Xi, Duan Mingjun, Wu Shuo, Ma Chuang, Wei Qin. Platelet-derived growth factor BB induces bone marrow mesenchymal stem cells to differentiate into vascular endothelial cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(25): 3937-3942. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||