Chinese Journal of Tissue Engineering Research ›› 2017, Vol. 21 ›› Issue (15): 2418-2423.doi: 10.3969/j.issn.2095-4344.2017.15.022
Previous Articles Next Articles
Characters and progress of three-dimensional printing technology in bone tissue engineering
Wu Cheng-cong1, Wang Fang2, Rong Shu1, Wu Zheng1, Liu Tao1, Liu Ke-ting1, Zhu Bo1, Huang He-fei1
- 1First Department of Orthopedics, the First People’s Hospital of Qujing, Qujing 655000, Yunnan Province, China; 2Department of Pathology, the Second People’s Hospital of Qujing, Qujing 655000, Yunnan Province, China
-
Online:2017-05-28Published:2017-06-07 -
Contact:Rong Shu, Master, Associate chief physician, First Department of Orthopedics, the First People’s Hospital of Qujing, Qujing 655000, Yunnan Province, China -
About author:Wu Cheng-cong, Master, Physician, First Department of Orthopedics, the First People’s Hospital of Qujing, Qujing 655000, Yunnan Province, China -
Supported by:the Research Foundation of the Department of Education of Yunnan Province, No. 2016ZDX074
CLC Number:
Cite this article
Wu Cheng-cong, Wang Fang, Rong Shu, Wu Zheng, Liu Tao, Liu Ke-ting, Zhu Bo, Huang He-fei. Characters and progress of three-dimensional printing technology in bone tissue engineering[J]. Chinese Journal of Tissue Engineering Research, 2017, 21(15): 2418-2423.
share this article

2.1 3D打印技术原理及分类 3D打印技术又称为快速成型技术,其利用计算机辅助设计技术(computer aided design,CAD)的数据,通过快速成型机,通过迭加成型的技术逐层增加材料来形成3D实体[3](见图2)。3D打印技术利用3D打印机喷头在水平方向和垂直方式将粉末金属、高分子材料等可粘合材料进行三维打印。而针对于组织工程器官打印:首先通过CT/MRI获取病变部位成像数据,利用CAD建立数据模型,根据相关数据输入3D打印机,打印机根据数据将生物材料逐层打印并堆积,形成与目标组织一致的三维生物材料结构[4]。其优势体现在能够快速精准的构建复杂外观与内部微观结构的一体化生物材料,实现支架与缺失、病变部位完美匹配,实现个性化生产[5]。 3D打印技术包括光固化立体印刷(SLA),熔融沉积成型(FDM)、选择性激光烧结(SLS)和材料-细胞同时打印的3D生物打印等[7-8]。"

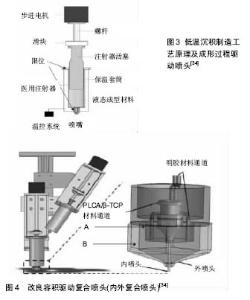
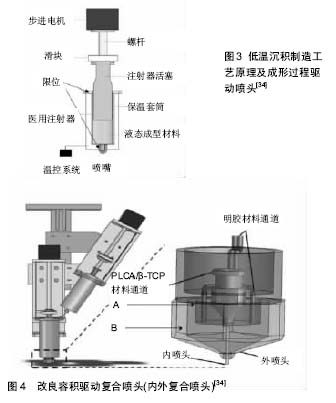
2.1.1 固化立体印刷 是实用最早、目前运用最广泛的3D打印技术[8],其具有高精密度、高稳定性及支架力学强度高,但其成型后需要清洗以去除杂质。该技术原料为光敏性树脂,包括具有高光敏性的高分子材料如:聚乳酸(PLA)、聚己内酯(PCL)以及蛋白质和多糖或者其他复合材料等[9-10]。 2.1.2 熔融沉积成型 该技术将融化状的材料按计算机控制路径挤出,逐层沉积凝固,其成型精度、支架强度高,无需添加溶剂故成型后无需去除杂质[11]。但成型过程中高温容易造成高分子材料降解、生物大分子活性丧失,目前主要运用于热塑性高分子如聚酰胺、聚酯、聚乙烯等材料打印。 2.1.3 选择性激光烧结 通过激光束将原料表面熔融实现粘结固化,新粉末再次熔融粘合,逐层烧结形成所需支架。该技术可创造出精细结构[12],但其打印成品表面较粗糙,高温容易造成高分子材料降解。近年出现微波烧结3D打印技术烧结三磷酸钙支架材料,相对传统3D打印技术,其在材料的力学性能、生物学性能及促进人成骨细胞分化方面具有明显的优越性[13]。 2.1.4 3D生物打印技术 传统组织工程技术由人体组织中分离培养干细胞,实验室中增殖培养后复合支架材料,利用不同生长因子诱导干细胞向不同组织、不同功能的细胞分化,以期最终构建出具有特定功能的组织或器官。目前该方法是解决供体器官/组织短缺的潜在途径,但传统组织工程仍存在干细胞分布不均、无法完全仿生正常组织等弊端。3D生物打印技术,其以活体细胞、营养物质和液态生物材料的共混物直接打印材料-细胞一体化支架,能够使种子生物材料内部、表面分布均匀[8]。不过,种子细胞能否正常存活并实现生理功能,成为一个待攻克的难题。生物打印通常将细胞与生物材料同时打印,理想的生物材料除具备良好的生物相容性和可降解性外,还需要在打印过程中及成型后能够维持适宜的力学强度和生物活性等要求。同时,3D生物打印技术需对打印速度、分辨率、细胞浓度、液滴体积及种子细胞直径进行高度控制,故3D生物打印技术对生物材料选择其十分严格,其需满足种子细胞的生存条件,目前能够满足生物打印的材料较少,水凝胶被认为是最有潜力的软组织制作材料[14]。为评价3D打印材料特性,Yao等[15]通过扫描新西兰大白兔股骨、脊椎的三维CT数据并通过CAD制图打印聚己酸内酯-羟基磷灰石模型,通过测量孔隙率、纤维支架直径、总体形状、载荷力、形变、最大负荷等,发现通过三维CT数据及CAD软件制作的生物支架材料完全能满足复杂制作工程材料的制作要求。 2.2 3D打印组织工程骨支架材料要求 骨组织是一种由无机纳米羟基磷灰石颗粒与胶原及少量非胶原蛋白等基质自主装形成的多孔复合材料。理想的骨支架材料具有良好的骨传导性、骨诱导性、生物相容性、生物降解性、力学性能、三维多孔结构为种子细胞生长提供空间。支架材料的设计需要尽量模仿天然骨的复杂的多孔微观结构,以诱导成骨的方式实现骨的修复和再生。针对3D打印组织工程骨的设计要求,研究者Scott提出了4F准则[16]:形状诉求(Form),即支架材料其形状必须完全填充三维缺损,并且可以诱导相应组织再生;性能诉求(Function),即支架的力学强度及性能等,可以在缺失组织修复前暂时起到缺失组织的替代作用;功能诉求(Formation),即材料需具有相应的生物活性,能够为种子细胞提供适宜的环境以促进组织再生,能为种子细胞提供黏附、分化、增殖或迁移的的条件;可植入性(Fixation),即支架材料可通过手术操作植入人体,要求支架材料可以固定于骨缺损中,并提供合适的表面以满足固定需要,并起到预期功效。 然而,传统的支架构建方法(包括溶液浇筑/离子洗出法、静电纺锤法、相分离/冻干法、原位成型法、气体成孔纤维编织法、纤维粘接法、熔化造型法和气压造孔法等)因缺乏稳定的结构[17-19]、力学性能差、残留有害化学溶剂、难以实现复杂非均质材料支架的成形制造和对孔隙结构的准确控制、难以实现个性化的植入物制造等局限性不能满足组织工程制备需要[20]。3D打印技术出现后,对于传统方法中不能实现对支架材料形状、孔隙率及细胞分布不均问题开辟了新的途径,Gómez等[21]利用泰森多边形构图原理(Voronoi tessellation method)构建3D组织工程骨,其具有精确的骨形态参数(骨小梁厚度、间隔,骨小梁数量、密度,表面积),具有良好力学性能及流体力学性能。利用3D电子光束溶解打印不同孔隙率和直径的钛合金支架材料,发现较小孔径(2 mm)的支架材料相对较大孔孔径(3 mm、4 mm)支架材料更易获得干细胞增殖及黏附[22]。 通过3D打印技术构建骨组织工程支架,材料需具有:一定流动性、稳定性和可湿性。①材料的流动性决定了打印产品的分辨率,即3D打印的高精度,其取决于微粒大小和形状,微粒大小与流动性成反比,但不代表流动性越大精度越高,在运用过程中需寻找最适微粒大小[23];②微粒的横向剪切力和重力可影响最终成品的准确度和完整性,提高材料的黏合度可提高稳定性;Farzadi A发现在相同空隙直径参数下,向X轴向打印的硫酸钙支架材料具有更接近于CAD软件设计图,具有更好的强度韧性及杨氏模量[24];③粉末的可湿性直接影响打印的精确度和三维结构的原始强度。其决定于粉末与黏合剂的接触角、黏合剂喷射速度、粉末表面形势以及粉末与粘合剂间的化学作用;④粉末与黏合剂的反应性直接影响打印层与层之间的黏合,最终影响打印的精确度[25];⑤良好的组织工程材料表面需具备亲水基团以附着生长因子为细胞分化提供基础,3D打印材料表面改性显得尤为重要,Lee等[26]通过3D打印聚已酸内酯支架,利用聚多巴胺附着材料表面并结合重组人形态发生蛋白2成功获得了具有良好水通透性、长期缓释生长因子并促进种子细胞分化的复合组织工程材料。 2.3 骨组织工程3D打印材料分类 可聚合的水凝胶材料如海藻酸钠-氯化钠体系形成的水凝胶结构稳定,含水量高,适合作为制作组织工程支架材料。近年,在生物材料中添加生长因子为组织工程生物材料生物性能、力学性能提供了新途径。利用明胶基质基于磷酸钙3D打印支架材料缓释骨形态发生蛋白2,体内外验证缓释骨形态发生蛋白2对山羊基质干细胞成骨分化能力影响,研究发现缓释生长因子能够促进山羊基质细胞在小鼠/大鼠皮下成骨分化,并发现骨形态发生蛋白2促进骨分化并不受缓释时间的影响。 人工合成多聚体:属于热塑材料,如聚乳酸,聚羟基乙酸及其共聚物。其降解产物无毒及良好的生物相容性,聚乳酸和聚羟基乙酸已经通过美国FDA的批准,可作为植入物。良好的组织工程材料表面需具备亲水基团以附着生长因子为细胞分化提供基础,而人工合成多聚体一般水溶性差,常利用有机溶剂氯仿增加材料亲水性。但氯仿残留可能导致支架残留毒性风险[27],因此3D打印材料表面改性显得尤为重要[26]。Cavo等[28]利用3D打印技术构建聚乳酸支架并将胶原蛋白涂布与支架表面,通过计算机流体动力学评估,成功获得构建组织工程骨相关理论模型。国内学者运用磷脂将纳米金刚石进行表面改造,发现纳米金刚石与磷脂混合比例为质量比10∶50时混合物分散效果最佳,将改性后具备疏水结构的纳米金刚石与聚乳酸-羟基乙酸共聚物(PLGA)制备的纳米金刚石/聚乳酸-羟基乙酸共聚物膜具有良好的生物力学强度及生物相容性[29]。 天然高分子聚合物:包括胶原、纤维蛋白、甲壳素及其衍生物和藻酸盐等,天然聚合物具有良好的生物相容性、水溶性、细胞识别信号,利于细胞黏附、增殖和分化。大量的天然高分子聚合物用于医学支架材料的打印,但它们难以大量获取、降解时难以控制、缺乏一定的机械强度,难以单独用作成骨细胞培养基质材料,很难单独作为组织工程中成骨性细胞种植的载体,不过可作为良好的材料包埋和添加剂。近年,深海高分子聚合物、生物多磷酸盐、生物型二氧化硅被证实可促进破骨细胞和成骨细胞活性、增加骨盐沉积,通过3D打印生物制陶后具有良好的机械性能,有望广泛应用于组织工程中[30]。 生物陶瓷:磷酸钙盐陶(磷酸三钙)、羟基磷灰石都具有优异的骨传导性能,可不同程度地整合入宿主骨。但单纯打印的支架材料其由于脆性大、不易吸收、降解速率与新骨形成不匹配而受到限制。从3D打印技术改进方面,通过微波烧结3D打印技术烧结三磷酸钙支架材料相对传统3D打印技术在材料的力学性能、生物学性能及促进人成骨细胞分化方面具有明显的优越性[13]。利用3D打印技术,将质量比为为3∶1和4∶1的珊瑚羟基磷灰石与左旋-聚乳酸为原料,打印制备数字化珊瑚羟基磷灰石骨组织支架材料,相对传统珊瑚羟基磷灰石其孔隙率升高、孔径增大,支架具有良好的降解性能[31],一定程度扩展了羟基磷灰石的应用范围。 2.4 骨组织工程3D打印支架材料特点 组织工程支架要求具有高隙率及架自身降解能力,同时还需支架具有一定的力学强度,为细胞提供支撑作用及保持结构的稳定性。生物制陶共同存在的问题是机械强度低,为增加机械强度,常在烧结前期加入有机黏合剂,但可能导致打印产品毒性增加,常用酸来做黏结剂如磷酸和柠檬酸。利用生物3D打印聚乳酸-羟基磷灰石(PLA-HA)复合材料上,骨髓基质细胞能够健康生长,材料具有较好的组织相容性,能在体内生物反应器内促进新骨生长[32]。 由于单一材料常因机械强度不足、降解产物不利于骨细胞成长分化,复合材料常作为种子细胞支架材料。针对于机械强度,利用新型低温3D打印技术制备的镁有机复合入聚(乙交酯-丙交酯共聚物-β-磷酸三钙-Mg)多孔支架具有良好的相互连接的多孔结构及适宜骨重建的机械强度[33]。但随之而来,复合材料结构上缺乏功能性基团与细胞、组织亲和性低,例如高分子聚合物表面亲水性较低(缺乏细胞识别信号),导致复合支架不利于细胞黏附、增殖、分化,需对原始材料进行表面处理,提高支架材料的亲水性以提高复合支架的生物相容性、组织再生能力。邓伟等[34]利用CAD设计支架内部三维微结构及支架表面改性,在低温沉积制造工艺单喷头(见图3)平台基础上改进喷头设计成内外复合喷头(见图4),形成复合喷射低温沉积快速成形工艺对支架结构内部表面进行改性,即在主体材料喷头喷射制备主体支架结构的同时对主体结构(聚乳酸/羟基乙酸共聚物/磷酸三钙)亲水活性材料(明胶)同步喷涂,可制备出具有三级多孔结构的包芯组织工程骨仿生支架,从而提高种子细胞在生物材料表面的黏附、增殖和分化能力。"
| [1] Ku KC, Lee MW, Kuo SM, et al. Preparation and evaluation of collagen I/ gellan gum/beta-TCP microspheres as bone graft substitute materials. Conf Proc IEEE Eng Med Biol Soc. 2013; 2013:6667-6770.[2] Temple JP, Hutton DL, Hung BP,et al. Engineering anatomically shaped vascularized bone grafts with hASCs and 3D-printed PCL scaffolds. J Biomed Mater Res A.2014; 102(12):4317-4325.[3] 王雪莹. 3D打印技术与产业的发展及前景分析[J].中国高新技术企业,2012,26:3-5.[4] Leong KF, Cheah CM, Chua CK. Solid freeform fabrication of three-dimensional scaffolds for engineering replacement tissues and organs. Biomaterials.2003;24(13):2363-2378.[5] 王镓垠.人体器官3D打印的最新进展[J]. 机械工程学报,2014, 50(23):119-127.[6] Cox SC, Thornby JA, Gibbons GJ, et al. 3D printing of porous hydroxyapatite scaffolds intended for use in bone tissue engineering applications. Mater Sci Eng:C,2015;47: 237-247.[7] Seol YJ, Kang TY, Cho DW.Solid freeform fabrication technology applied to tissue engineering with various biomaterials. Soft Matter.2012;8(6):1730-1735.[8] 田冶,曾庆慧,胡相华,等. 3D打印技术及在组织工程领域的研究进展[J].中国医疗器械信息,2015,21(8):7-12.[9] Jansen J, Melchels FP, Grijpma DW, et al. Fumaric acid monoethyl ester-functionalized poly(D,L-lactide)/N-vinyl-2 -pyrrolidone resins for the preparation of tissue engineering scaffolds by stereolithography. Biomacromolecules.2009;10(2):214-220.[10] Matsuo A,Chiba H,Takahashi H,et al.Clinical application of a custom-made bioresorbable raw particulate hydroxyapatite/poly-L-lactide mesh tray for mandibular reconstruction. Odontology. 2010;98(1):85-88.[11] 王宁,李杰,王晓龙,等. 应用3D打印熔融沉积技术制作个性化种植修复体的精确度研究[J]. 华西口腔医学杂志, 2015,33(5): 509-512.[12] Hoy MB. 3D printing: making things at the library.Med Ref Serv Q.2013,32(1): 94-99.[13] Tarafder S, Balla VK, Davies NM, et al. Microwave-sintered 3D printed tricalcium phosphate scaffolds for bone tissue engineering.J Tissue Eng Regen Med.2013;7(8):631-641.[14] Cui X, Boland T, D'Lima DD, et al. Thermal inkjet printing in tissue engineering and regenerative medicine.Recent Pat Drug Deliv Formul.2012;6(2):149-155.[15] Yao Q, Wei B, Guo Y, et al.Design, construction and mechanical testing of digital 3D anatomical data-based PCL-HA bone tissue engineering scaffold. J Mater Sci Mater Med.2015;26(1):5360.[16] Hollister SJ.Scaffold Design and Manufacturing: From Concept to Clinic.Adv Mater.2009;21(32-33):3330-3342.[17] Yang S, Leong KF, Du Z, et al.The design of scaffolds for use in tissue engineering. Part I. Traditional factors.Tissue Eng. 2001;7(6):679-689. [18] Guarino V, Ambrosio L.Temperature-driven processing techniques for manufacturing fully interconnected porous scaffolds in bone tissue engineering. Proc Inst Mech Eng H. 2010;224(12):1389-1400.[19] Jang JH, Castano O, Kim HW. Electrospun materials as potential platforms for bone tissue engineering. Adv Drug Deliv Rev.2009;61(12):1065-1083.[20] 廖南,邓金杨,陈殷曹.复合喷射低温沉积快速成形工艺制备包芯骨组织工程仿生复合支架[J].新疆医科大学学报,2012,35(6):755-761.[21] Gomez S, Vlad MD, Lopez J, et al. Design and properties of 3D scaffolds for bone tissue engineering. Acta Biomaterialia. 2016;42:341-350.[22] Luo Y, Zhai D, Huan Z, et al.Three-Dimensional Printing of Hollow-Struts-Packed Bioceramic Scaffolds for Bone Regeneration. ACS Appl Mater Interfaces. 2015;7(43): 24377-24383.[23] Butscher A, Bohner M, Hofmann S, et al.Structural and material approaches to bone tissue engineering in powder-based three-dimensional printing. Acta biomateri. 2011;7(3):907-920.[24] Farzadi A, Solati-Hashjin M, Asadi-Eydivand M, et al. Effect of layer thickness and printing orientation on mechanical properties and dimensional accuracy of 3D printed porous samples for bone tissue engineering. PloS one.2014;9(9): e108252.[25] Khalyfa A, Vogt S, Weisser J, et al. Development of a new calcium phosphate powder-binder system for the 3D printing of patient specific implants. J Mater Sci Mater Med. 2007; 18(5):909-916.[26] Lee SJ, Lee D, Yoon TR, et al. Surface modification of 3D-printed porous scaffolds via mussel-inspired polydopamine and effective immobilization of rhBMP-2 to promote osteogenic differentiation for bone tissue engineering.Acta biomater. 2016;40:182-191.[27] Kim SS, Sun Park M, Jeon O, et al. Poly(lactide-co-glycolide)/ hydroxyapatite composite scaffolds for bone tissue engineering. Biomaterials.2006;27(8):1399-409.[28] Cavo M, Scaglione S. Scaffold microstructure effects on functional and mechanical performance: Integration of theoretical and experimental approaches for bone tissue engineering applications. Mater Sci Eng C Mater Biol Appl. 2016;68:872-879.[29] 张帆. 新型纳米金刚石-PLGA可吸收复合材料3D打印制备颈椎间融合器的研究[D]. 第二军医大学,2015.[30] Wang X, Schroder HC, Feng Q, et al. The deep-sea natural products, biogenic polyphosphate (Bio-PolyP) and biogenic silica (Bio-Silica), as biomimetic scaffolds for bone tissue engineering: fabrication of a morphogenetically-active polymer. Marine drugs.2013;11(3):718-46.[31] 林山,黄晓梅,芮钢,等.数字化珊瑚羟基磷灰石人工骨支架的体外降解性能[J].中国组织工程研究,2016,20(3):330-5.[32] 张海峰,杜子婧,毛曦媛,等. 3D打印PLA-HA复合材料构建组织工程骨的实验研究[J].国际骨科学杂志,2016,37(1):57-63.[33] 赖毓霄,李龙,李烨,等.基于新型3D打印技术的复合活性多孔骨修复支架的研发[C]. 2015年全国高分子学术论文报告会,苏州: 2015.[34] 邓伟,金格勒,杨毅,等.复合喷射低温沉积快速成形工艺制备包芯骨组织工程仿生复合支架[J].新疆医科大学学报,2012,35(6): 755-761.[35] Barabaschi GD, Manoharan V, Li Q, et al. Engineering Pre-vascularized Scaffolds for Bone Regeneration.Adv Exp Med Biol.2015;881:79-94.[36] Bose S, Tarafder S, Bandyopadhyay A. Effect of Chemistry on Osteogenesis and Angiogenesis Towards Bone Tissue Engineering Using 3D Printed Scaffolds. Ann Biomed Eng. 2017;45(1):261-272. |
| [1] | Yao Xiaoling, Peng Jiancheng, Xu Yuerong, Yang Zhidong, Zhang Shuncong. Variable-angle zero-notch anterior interbody fusion system in the treatment of cervical spondylotic myelopathy: 30-month follow-up [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1377-1382. |
| [2] | An Weizheng, He Xiao, Ren Shuai, Liu Jianyu. Potential of muscle-derived stem cells in peripheral nerve regeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1130-1136. |
| [3] | Zhang Jinglin, Leng Min, Zhu Boheng, Wang Hong. Mechanism and application of stem cell-derived exosomes in promoting diabetic wound healing [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1113-1118. |
| [4] | He Yunying, Li Lingjie, Zhang Shuqi, Li Yuzhou, Yang Sheng, Ji Ping. Method of constructing cell spheroids based on agarose and polyacrylic molds [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 553-559. |
| [5] | He Guanyu, Xu Baoshan, Du Lilong, Zhang Tongxing, Huo Zhenxin, Shen Li. Biomimetic orientated microchannel annulus fibrosus scaffold constructed by silk fibroin [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 560-566. |
| [6] | Yang Feng, Zhao Qian, Zhang Shixuan, Zhao Tienan, Feng Bo. Effectiveness and safety of rapamycin combined with CD133 antibody stent in preventing vascular restenosis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 579-584. |
| [7] | Chen Xiaoxu, Luo Yaxin, Bi Haoran, Yang Kun. Preparation and application of acellular scaffold in tissue engineering and regenerative medicine [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 591-596. |
| [8] | Kang Kunlong, Wang Xintao. Research hotspot of biological scaffold materials promoting osteogenic differentiation of bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 597-603. |
| [9] | Shen Jiahua, Fu Yong. Application of graphene-based nanomaterials in stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 604-609. |
| [10] | Zhang Tong, Cai Jinchi, Yuan Zhifa, Zhao Haiyan, Han Xingwen, Wang Wenji. Hyaluronic acid-based composite hydrogel in cartilage injury caused by osteoarthritis: application and mechanism [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 617-625. |
| [11] | Li Hui, Chen Lianglong. Application and characteristics of bone graft materials in the treatment of spinal tuberculosis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 626-630. |
| [12] | Gao Cangjian, Yang Zhen, Liu Shuyun, Li Hao, Fu Liwei, Zhao Tianyuan, Chen Wei, Liao Zhiyao, Li Pinxue, Sui Xiang, Guo Quanyi. Electrospinning for rotator cuff repair [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 637-642. |
| [13] | Guan Jian, Jia Yanfei, Zhang Baoxin , Zhao Guozhong. Application of 4D bioprinting in tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(3): 446-455. |
| [14] | Liu Jiali, Suo Hairui, Yang Han, Wang Ling, Xu Mingen. Influence of lay-down angles on mechanical properties of three-dimensional printed polycaprolactone scaffolds [J]. Chinese Journal of Tissue Engineering Research, 2022, 10(16): 2612-2617. |
| [15] | Huang Bo, Chen Mingxue, Peng Liqing, Luo Xujiang, Li Huo, Wang Hao, Tian Qinyu, Lu Xiaobo, Liu Shuyun, Guo Quanyi . Fabrication and biocompatibility of injectable gelatin-methacryloyl/cartilage-derived matrix particles composite hydrogel scaffold [J]. Chinese Journal of Tissue Engineering Research, 2022, 10(16): 2600-2606. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||

