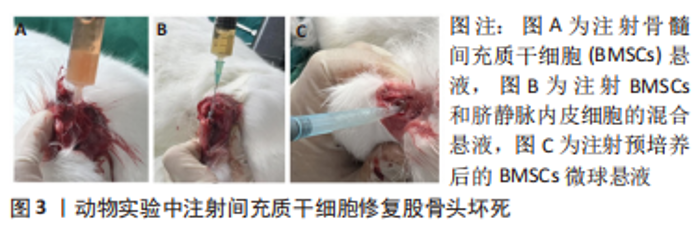
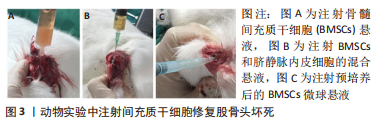
Chinese Journal of Tissue Engineering Research ›› 2024, Vol. 28 ›› Issue (9): 1450-1456.doi: 10.12307/2024.041
Previous Articles Next Articles
Application and prospect of tissue engineering in treatment of osteonecrosis of the femoral head
Chen Kaijia1, Liu Jingyun1, Cao Ning2, Sun Jianbo2, Zhou Yan3, Mei Jianguo4, Ren Qiang1, 2
- 1Department of Bone Joint, Binzhou Medical University Hospital, Binzhou 256600, Shandong Province, China; 2School of Materials and Engineering, China University of Petroleum (East China), Qingdao 266580, Shandong Province, China; 3East China University of Science and Technology, Shanghai 200237, China; 4Shandong Binzhou Animal Science & Veterinary Medicine Academy, Binzhou 256600, Shandong Province, China
-
Received:2023-03-10Accepted:2023-04-22Online:2024-03-28Published:2023-07-26 -
Contact:Ren Qiang, MD, Associate chief physician, Department of Bone Joint, Binzhou Medical University Hospital, Binzhou 256600, Shandong Province, China; School of Materials and Engineering, China University of Petroleum (East China), Qingdao 266580, Shandong Province, China -
About author:Chen Kaijia, Master candidate, Department of Bone Joint, Binzhou Medical University Hospital, Binzhou 256600, Shandong Province, China -
Supported by:Shandong Province Medical and Health Technology Development Plan Project, No. 2017WS040 (to RQ); 2020 Industry-University Collaborative Education Project, No. 202002204024 (to RQ); Xu Rongxiang Regenerative Medicine Development Plan Project of Binzhou Medical University, No. BY2019XRX04 (to RQ)
CLC Number:
Cite this article
Chen Kaijia, Liu Jingyun, Cao Ning, Sun Jianbo, Zhou Yan, Mei Jianguo, Ren Qiang. Application and prospect of tissue engineering in treatment of osteonecrosis of the femoral head[J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1450-1456.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
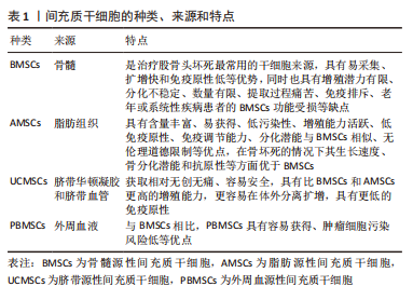
2.1 MSCs 2.1.1 MSCs的概念 MSCs参与坏死骨组织区域的骨修复和血管化,是治疗股骨头坏死的主要细胞来源,是组织工程技术治疗股骨头坏死的基础[7]。 MSCs属于多能干细胞,具有自我更新和分化成多种细胞类型的能力,不仅可以分化为成骨细胞、成软骨细胞和内皮细胞直接参与骨组织重建和血管生成,还可以通过分泌骨形态发生蛋白、骨保护素、血管内皮生长因子、血小板源性生长因子,转化生长因子β、碱性成纤维细胞生长因子等多种生长因子来调节骨形成和血管化的过程[8]。MSCs已被证明对股骨头坏死有积极影响,例如促进干细胞的成骨分化、抑制成脂分化进而促进骨坏死区的新骨和新血管形成[9]。MSCs的移植主要采用微创方法,直接注射到坏死股骨头中是移植MSCs的主要方式,此外,MSCs还可通过动脉灌注的方式改善股骨头的坏死[10]。股骨头缺血坏死后,股骨头血液供应减少,坏死股骨头中的MSCs在此缺氧微环境中发生大量应力诱导的细胞、凋亡和衰老,发生成骨和成脂分化失衡,细胞数量及活性降低,是股骨头坏死进行性进展的重要原因[11]。因此,及时补充具有优质活性的MSCs可以从发病机制层面上治疗股骨头坏死。然而,MSCs移植仍存在一定的难题,例如:①股骨头坏死部位需要的MSCs的数量没有量化标准,并且行血管灌注法移植MSCs时如何保证干细胞不随血液流失;②移植的自体MSCs如何保证富有活性且存活;③移植的MSCs的污染性、致癌性如何判定。 2.1.2 MSCs的种类 MSCs分布广泛,骨髓、脂肪、脐带、外周血等组织中均可提取,根据组织来源的不同,MSCs可分为BMSCs、脂肪源性间充质干细胞(adipose-derived mesenchymal stem cells,AMSCs)、脐带源性间充质干细胞(umbilical cord-derived mesenchymal stem cells,UCMSCs)和外周血源性间充质干细胞(peripheral blood-derived mesenchymal stem cells,PBMSCs)[12-13]。不同种类的MSCs的特点不同,具体见表1,近年来,MSCs已广泛应用于股骨头坏死治疗的基础研究,见图3。"
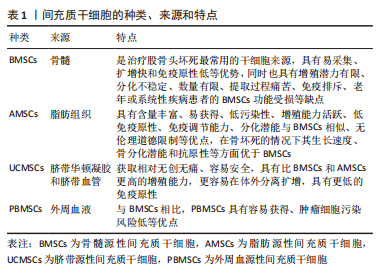

BMSCs是骨再生重塑的主要前体细胞,是治疗股骨头坏死最常用的干细胞来源。BMSCs具有容易采集、快速扩增和低免疫原性等优势,但同时也具有增殖潜力有限、分化不稳定、数量有限、提取过程痛苦、免疫排斥、老年或系统性疾病患者的BMSCs功能受损等缺点[14-16]。BMSCs在体外实验中可从兔或者鼠的股骨或胫骨骨髓中分离培养,临床上则可通过髂骨翼抽取。将BMSCs移植到坏死股骨头区域后,可以发现成骨细胞和内皮细胞具有明显的增殖和分化,并且股骨头骨密度和骨小梁体积显著增加,证明BMSCs对坏死股骨头具有成骨和成血管的修复效果。WANG等[17]在坏死股骨头髓芯减压后移植自体BMSCs,与单纯髓芯减压组比较,联合应用髓芯减压术和自体BMSCs的股骨头骨组织得到了更明显的修复,疼痛缓解和功能康复效果明显,显著提高了股骨头坏死单纯髓芯减压的治疗效果,降低了远期髋关节置换的手术率。ZHANG等[18]对股骨头坏死患者采用髓芯减压联合BMSCs移植的治疗方法,结果表明该方法具有术后股骨头的塌陷率低、临床成功率高的优点。这证明髓芯减压联合BMSCs移植的联合治疗方法不仅具有髓芯减压的优势,而且提供的种子细胞可以促进骨坏死区域的修复和重塑。AMSCs具有数量多、容易获得、增殖能力活跃、低免疫原性、免疫调节能力、分化潜能与BMSCs相似等优点,是治疗股骨头坏死另一种可靠的干细胞来源。最近的研究表明AMSCs同样具有成骨和血管生成分化的能力。在骨坏死的情况下,AMSCs在生长速度和骨分化潜能方面优于BMSCs,提示AMSCs可能是一种更有效的再生细胞来源。ZHANG等[19]提取晚期骨坏死行髋关节置换患者的关节周围脂肪组织和骨髓标本,从两种组织来源分离MSCs进行体外细胞培养,比较AMSCs和BMSCs的增殖和成骨分化潜力,实验结果显示在骨坏死的情况下,AMSCs在增殖速度和骨分化效率方面优于BMSCs,提示对于股骨头坏死患者,AMSCs可能提供更有效的骨重建能力。SCHUBERT等[20]从人的脂肪组织中分离自体吸脂细胞,发现吸脂细胞具有更强大的血管生成潜力,对坏死股骨头区域的血管化效果优于BMSCs,并且认为吸脂细胞的促血管生成能力与其分泌的血管生成因子有关,实验表明吸脂细胞组的血管内皮生长因子、碱性成纤维细胞生长因子和转化生长因子β的水平明显高于BMSCs组。此外,相较于其他研究者应用髓芯减压联合MSCs移植,SCHUBERT等[20]选择动脉灌注法植入种子细胞,将自体吸脂细胞灌注到旋内侧动脉中,发现血管内皮生长因子表达增加和微血管密度增加,吸脂细胞表现出较好的血管化。然而该实验缺少血管灌注与髓芯减压区域移植2种细胞植入方法的对照,二者的修复效果有待进一步研究。UCMSCs是用婴儿脐带制备的华顿凝胶中提取的,相较于BMSCs的提取方式,UCMSCs的获取相对无创无痛、容易安全。此外,UCMSCs具有比BMSCs和AMSCs更高的增殖能力,更容易在体外分离和扩增以及更低的免疫原性。WANG等[21]采用外植体培养法从华顿胶中分离人UCMSCs,研究人UCMCs对激素诱导的股骨头坏死的治疗作用,结果发现相较于对照组,人UCMCs组的人微血管内皮细胞的增殖和成血管能力提高,空骨陷窝率明显降低,骨密度增加,股骨头骨小梁致密,证明人UCMSCs能够通过促进血管生成和骨愈合防止激素引起股骨头坏死。人UCMCs促进骨愈合的机制可能是通过促进Runt相关转录因子2和Ⅰ型胶原的表达,抑制过氧化物酶体增殖物激活受体γ的表达,提高血清中碱性磷酸活性和降低三酰甘油含量,进而调节成骨与成脂平衡实现的。PBMSCs从外周血中提取,与BMSCs相比,PBMSCs有许多优点,如容易获得、肿瘤细胞污染风险低等优点。WANG等[22]构建兔股骨头坏死模型后,向股骨头坏死区域移植PBMSCs,实验发现移植PBMSCs的股骨头修复效果明显,其坏死部位的骨密度增大,骨小梁粗大整齐,这可能与上调骨形态发生蛋白2表达和下调过氧化物酶体增殖物激活受体γ表达有关。 2.1.3 基因转染的MSCs 随着基因工程技术的迅速发展,人们利用基因重组干细胞来调节机体生理功能,治疗相关疾病。BMSCs在股骨头坏死的缺氧条件下会发生活性降低及凋亡等变化,这限制了移植细胞对股骨头坏死的疗效。基因修饰的BMSCs稳定表达多种生长因子(如骨形态发生蛋白、血管内皮生长因子和转化生长因子β),并且增强了MSCs的存活能力,是股骨头坏死的一种新的治疗和研究方向。YANG等[23]制备了Foxc2转基因重组BMSCs,观察其对股骨头坏死的治疗作用,实验证明高表达Foxc2的转基因BMSCs对骨坏死区域成骨和成血管效果更显著,免疫组化染色发现高表达Foxc2的BMSCs的骨形态发生蛋白和血管内皮生长因子的表达增加,过氧化酶体增殖剂激活受体γ2表达减小,生物力学测定显示股骨头骨质平均弹性模量和最大压缩强度增大,证明Foxc2转基因BMSCs延缓了股骨头坏死。YANG等[23]认为Foxc2可促进BMSCs成骨分化,抑制成脂分化,机制可能与阻碍过氧化酶体增殖剂激活受体γ2活性有关。同时,该实验将基因工程和微囊化技术相结合,采用高压静电法制备海藻酸钠-多聚赖氨酸-海藻酸钠微囊化高表达Foxc2转基因BMSCs,微囊化细胞的免疫阻隔作用可避免移植后的免疫排斥,且微囊有利于BMSCs的增殖分化,高表达Foxc2联合微囊化的BMSCs的存活和增殖得到改善。但微囊化细胞体内移植仍面临微囊内细胞存活时间短、炎症细胞浸润和纤维化包裹的缺点。MicroRNAs是一种短链非编码RNA,对血管生成和成骨非常重要,并参与股骨头坏死的发病机制和治疗。MicroRNAs-378(miR-378)已被报道与细胞增殖、血管生成密切相关,转染miR-378的MSCs在缺氧缺血条件下表现出更高的成骨分化活力和血管生成。NAN等[24]研究miR-378过表达的AMSCs是否具有增强的成血管和成骨潜力,促进激素诱导的股骨头坏死的血管化和成骨。研究结果表明,miR-378-AMSCs组中的成骨相关因子骨形态发生蛋白2、RUNT相关转录因子2表达增加,证明miR-378-AMSCs逆转了激素对AMSCs的成骨分化下调,AMSCs的成骨潜力增加。同时, miR-378-AMSCs组中的相关血管生成因子例如血管内皮生长因子的表达明显改善,证明miR-378-AMSCs提高了人血管内皮细胞的增殖迁移能力。负调控融合抑制因子能够抑成骨作用,下调人血管内皮细胞的血管生成能力,实验发现坏死股骨头中AMSCs的负调控融合抑制因子表达增加,miR-378-AMSCs组中负调控融合抑制因子表达下调,因此NAN等[24]认为miR-378可能通过下调负调控融合抑制因子的表达,以增强血管生成和成骨作用。ZHOU等[25]利用细胞重编程技术,探索由自体诱导多能干细胞分化的BMSCs在增殖能力、促进骨修复等方面与正常BMSCs的等效性。ZHOU等[25]从股骨头坏死患者骨髓标本中分离得到BMSCs,用反转录病毒重编程BMSCs生成诱导多能干细胞,然后诱导分化为BMSCs,通过检测谱系特异性标记基因发现诱导多能干细胞-MSCs具有与正常BMSCs相似的免疫表型和形态,同时具有更高的增殖率、更稳定的免疫调节功能和低免疫原性,并且无致瘤倾向。老年患者、系统性疾病患者和激素依赖性患者的BMSCs分化能力下降,重编程的诱导多能干细胞-MSCs可逆转股骨头坏死中BMSCs的异常增殖和分化,为坏死区域提供具有良好生物学性能的优质BMSCs。此外,研究发现诱导多能干细胞-MSCs植入能有效促进股骨头坏死区的血管生成,其促进血管化作用与促进血管内皮生长因子和CD31的表达有关。ZHOU等[25]选择BMSCs作为重编程的供体细胞,其解释为诱导多能干细胞具有供体特异性的表观遗传记忆,BMSCs衍生的诱导多能干细胞可能倾向于分化为BMSCs。BMSCs移植到股骨头坏死区域后,常发生细胞凋亡而限制了其移植的疗效。研究发现BMSCs应激性细胞凋亡主要由氧化应激介导,BMSCs的活性氧水平升高会触发多种凋亡信号通路进而诱导细胞凋亡。帕金森病蛋白7具有在抗氧化的防御作用,通过清除过多的活性氧抵抗BMSCs的凋亡。ZHANG等[26]将帕金森病蛋白7基因编码序列区插入病毒载体中,随后将病毒载体转染到BMSCs中,使帕金森病蛋白7在BMSCs中过表达,探讨帕金森病蛋白7介导的抗应激诱导凋亡能否改善BMSCs在移植部位的存活。实验结果表明,帕金森病蛋白7增强了BMSCs对氧化应激的抗性,抑制了应激诱导的细胞凋亡,降低了BMSCs凋亡率,促进了BMSCs的存活和骨坏死区的骨再生,提高了BMSCs在早期股骨头坏死的移植效果,是保护移植区域BMSCs存活的可行方法。DUAN等[27]通过实验探索激素性股骨头坏死的分子机制,实验结果表明激素可以激活转录因子CCAAT/增强结合蛋白α,通过过氧化物酶体增殖物激活受体γ信号通路增强成脂基因的表达,进而上调BMSCs的成脂分化能力并同时抑制成骨分化,导致股骨头坏死区域进行性脂肪堆积和骨坏死。因此从基因层面敲除BMSCs的转录因子CCAAT/增强结合蛋白α基因可能会上调BMSCs的成骨能力,促进骨重建。 2.1.4 MSCs与其他细胞或生物活性因子的联合作用 移植细胞的再生和增殖能力受到股骨头坏死骨组织的损害,限制了其临床疗效。MSCs在骨坏死区域的存活和活性是能否发挥移植效果的关键,通过联合其他细胞或生物活性因子,改善MSCs的存活和增殖分化,进而提高其修复坏死骨组织的能力。XU等[28]探究了BMSCs和内皮祖细胞联合移植是否可以有效治疗激素诱导的股骨头坏死,发现BMSCs和内皮祖细胞的共培养显示出了增强的成骨和成血管能力,同时成骨标志物骨形态发生蛋白2在BMSCs与内皮祖细胞比例为5∶1时达到峰值;在坏死股骨头修复骨缺损方面,BMSCs-内皮祖细胞共移植优于单细胞移植,这证明BMSCs与内皮祖细胞在分化能力上相互促进,有利于骨和血管的再生。内皮细胞通过促进BMSCs增殖和成骨分化来调节BMSCs活性,实验结果发现BMSCs-内皮祖细胞组的成骨因子骨形态发生蛋白、骨保护素、血管内皮生长因子、血小板源性生长因子的表达高于其他各组。此外,BMSCs-内皮祖细胞组的成脂相关标记过氧化物酶体增殖物激活受体γ、CCAAT/增强结合蛋白α的表达低于MSCs组,证明BMSCs-内皮祖细胞共培养具有成骨分化倾向,因此共移植有利于股骨头修复,治疗效果是通过平衡成骨成脂分化、促进成骨和血管生成、减少脂肪生成来诱导的。由于股骨头坏死组织的极端缺氧不利于血管生成,联合内皮祖细胞移植能够促进坏死股骨头的血管化,这有利于骨修复。WANG等[29]探索联合应用富血小板血浆凝块释放物和异体UCMSCs对股骨头骨坏死的治疗作用,发现可逆转大剂量甲基强的松龙诱导的BMSCs和人脐静脉内皮细胞的增殖能力损伤,抑制细胞凋亡,促进人脐静脉内皮细胞的成血管能力,并且效果优于单独应用富血小板血浆凝块释放物或异体UCMSCs。进一步实验显示该组中的转化生长因子β、胰岛素样生长因子和血小板源性生长因子等生长因子浓度增加,表明富血小板血浆凝块释放物可以通过释放生长因子促进UCMSCs的增殖。 2.2 生物支架 2.2.1 生物支架的概念 生物支架可提供塌陷股骨头稳定的机械支持,为成骨和血管生成提供适宜场所,同时刺激MSCs的增殖和成骨分化,促进骨再生重塑并诱导血管化。为了更好地促进坏死骨组织再生,支架的构建和选择需要考虑生物相容性、降解性、孔隙度、机械性能、细胞毒性、细胞黏附性、与细胞和生长因子组合的影响等。目前动物实验研究及临床应用较为广泛的支架包括生物陶瓷如羟基磷灰石和磷酸三钙,金属植入物如钛和钽棒,同时聚乳酸-乙醇酸等聚合物常以凝胶形式制备移植到坏死股骨头区域[30-31]。 2.2.2 生物支架可联合细胞移植促进骨重建 单纯支架移植虽然能为塌陷股骨头提供有力的力学支撑,但是缺乏诱导成骨修复作用,导致股骨头重建缓慢甚至失败,联合细胞尤其是MSCs是常用的支架移植方式。SONG等[32]进行了BMSCs与纳米羟基磷灰石/Ⅰ型胶原/聚左旋乳酸支架联合植入治疗兔股骨头坏死的实验研究,将BMSCs与纳米羟基磷灰石/Ⅰ型胶原/聚左旋乳酸支架结合,移植到髓芯减压后的骨隧道中,实验结果发现相较于纳米羟基磷灰石/Ⅰ型胶原/聚左旋乳酸组,BMSCs-纳米羟基磷灰石/Ⅰ型胶原/聚左旋乳酸组坏死区域的血管生成和骨形成面积和效率更大,可以观察到更多的毛细血管和新骨组织,同时纳米羟基磷灰石/Ⅰ型胶原/聚左旋乳酸支架的降解程度和速度增加,这说明BMSCs-纳米羟基磷灰石/Ⅰ型胶原/聚左旋乳酸支架可能提高髓芯减压治疗股骨头坏死的疗效,并且联合应用BMSCs后,促进了纳米羟基磷灰石/Ⅰ型胶原/聚左旋乳酸支架的生物降解性。LI等[33]将自体MSCs与β-磷酸三钙陶瓷共培养后移植到激素性股骨头坏死患者的坏死股骨头中,随访34个月后,发现患者股骨头骨坏死未进一步进展,观察到早期骨再生,证明MSCs与生物支架材料联合应用可促进股骨头骨修复。LING等[34]将BMSCs吸附在β-磷酸三钙支架上,然后在成骨分化培养基培养下观察生物支架对BMSCs的增殖和成骨分化的影响,结果表明相较于直接将BMSCs置于成骨分化培养基上培养,预先与β-磷酸三钙支架接触的BMSCs的骨钙素、Ⅰ型胶原和碱性磷酸酶的表达增加,形成了更多的钙沉积和钙结节。植入小鼠股骨头坏死模型中可观察到新形成的骨质,新骨面积百分比更大,证明β-磷酸三钙生物支架可促进BMSCs的生长和成骨分化,并且促进BMSCs分泌生长因子,促进股骨头坏死的修复。 2.2.3 生物支架与生物活性分子的结合 在生物活性因子-支架复合物中,支架起到“蓄水池”作用,能够持续释放生物活性分子到坏死股骨头处,诱导MSCs成骨分化和血管生成,促进骨再生和骨缺损修复。LI等[35]采用低温3D打印法制备了β-磷酸三钙/聚乳酸/乙醇酸复合多孔支架,同时掺入双过氧钒[bpV (pic)] ,形成bpV (pic)/TCP/PLGA支架(以下统称为bPTCP支架),评估了bPTCP支架对股骨头坏死的治疗作用,结果表明移植bPTCP支架后,成骨细胞分化基因碱性磷酸酶、Ⅰ型胶原、骨钙素、转录因子Sp7、RUNT相关转录因子2的mRNA表达水平显著上调,这表明bPTCP支架促进BMSCs的成骨分化;同时,脂肪细胞分化基因脂肪酸结合蛋白2、CCAAT/增强子结合蛋白α、过氧化物酶体增殖物激活受体γ和脂联素的mRNA表达降低,表明bPTCP支架抑制了BMSCs的成脂分化。此外,实验发现bPTCP组的骨形成相关基因的表达上调,凋亡相关蛋白表达减少,进而改善成骨细胞活性,促进成骨和血管生成。CD31是血管生成的重要标志,其在bPTCP组中的表达明显高于TCP/PLGA组,说明bpV (pic)不仅具有成骨作用,而且具有促进血管生成的潜力。然而作者对bpV (pic)促进血管生成的机制没有明确阐述。HUANG等[36]合成了热敏聚乳酸-乙醇酸-氯化锶-羟基磷灰石水凝胶,将富含能促进骨组织再生和血管重塑的生物活性因子的超活化血小板裂解液负载的热敏水凝胶移植到髓芯减压的大鼠坏死股骨头模型,发现聚合物热敏水凝胶在30 d内稳定释放转化生长因子β和血管内皮生长因子,成骨因子骨形态发生蛋白、Ⅰ型胶原和成血管因子血小板内皮细胞黏附因子1的阳性染色程度呈超活化血小板裂解液的时间和浓度依赖性增加,聚合物热敏水凝胶显著加速了骨修复和再生,坏死区域形成广泛新骨。该实验证明该热敏水凝胶能够良好包封生长因子,使血小板裂解液可以从水凝胶中缓慢持续释放,实现了生长因子的控释,因此解决了由于生长因子半衰期较短而在坏死区域达不到有效浓度的难题。因此,将血小板裂解液包裹在水凝胶支架中可能是治疗股骨头坏死的有效策略。ZHANG等[37]通过实验研究富血小板血浆联合磷酸三钙在股骨颈骨折后股骨头坏死修复中的作用,结果发现磷酸三钙组的新生骨面积显著小于富血小板血浆+磷酸三钙组,与对照组比较,磷酸三钙组和富血小板血浆+磷酸三钙组中的骨形态发生蛋白7、转化生长因子β和碱性成纤维细胞生长因子水平均显著升高,且富血小板血浆+磷酸三钙组高于磷酸三钙组;该实验证明富血小板血浆联合磷酸三钙可促进新骨形成,显著增加新骨面积,比单独应用磷酸三钙的疗效更大。富血小板血浆含有多种能够刺激新骨和血管组织形成的生长因子,上调骨形成相关因子的表达,同时磷酸三钙人工骨植入也能诱导软骨组织和新生血管样组织的生长,二者联合应用起到相辅相成的作用,可以加速股骨头骨坏死的修复。 2.2.4 生物支架可通过修饰或改性增强其修复能力 将生物活性物质如短肽、生长因子等修饰到支架表面,对生物支架材料进行表面改性,进而提高其组织相容性、生物活性和对MSCs的招募效率和诱导能力。DPIYALSWSGMA(DPI)肽是一种对BMSCs具有特异性亲和力的线性多肽,可以帮助β-磷酸三钙招募、吸附BMSCs,促进支架与种子细胞的紧密结合,弥补了β-磷酸三钙成骨诱导性弱的缺点。MARUYAMA等[38]从增加支架对BMSCs吸附能力的角度,对β-磷酸三钙进行表面改性,用DPI肽修饰β-磷酸三钙表面,采用吸附与冷冻干燥法成功制备了具有招募BMSCs功能DPI肽修饰的功能性β-磷酸三钙支架,提高β-磷酸三钙的组织相容性和生物活性。体外实验结果显示,β-磷酸三钙-DPI组荧光信号最强且黏附细胞数量最多,表明BMSCs对DPI肽修饰的β-磷酸三钙支架具有较高的亲和力和良好的黏附能力。此外,与单纯髓芯减压和与髓芯减压后植入未修饰的β-磷酸三钙支架相比,发现DPI肽修饰的β-磷酸三钙支架中股骨头空骨陷窝率最低,改善早期股骨头坏死的效果最好。与线性多肽相比,环多肽具有高亲和力、高特异性、高稳定性和良好生物相容性等优点。MASTROGIACOMO等[39]应用噬菌体显示技术筛选出了BMSCs的特异性亲和环肽CTTNPFSLC(C7),同样应用吸附与冷冻干燥法将C7修饰在β-磷酸三钙支架上,观察BMSCs的黏附、增殖情况及坏死骨组织的修复情况,并与纯β-磷酸三钙支架进行比较;结果表明,β-磷酸三钙支架表面被C7均匀覆盖,C7对β-磷酸三钙支架上的BMSCs具有较高的亲和力,其提高了BMSCs黏附性。然而该实验也存在缺点:首先,利用环肽构建生物活性支架仍停留在动物实验,环肽对人BMSCs的亲和力不得而知,且环肽与BMSCs相互作用的确切机制尚不清楚,环肽如何通过BMSCs靶受体激活胞内信号通路的过程是下一步的研究方向;此外,没有将线性肽和环肽设置对照实验,二者用于构建生物活性支架的优势劣势对比不清楚。 2.3 生物活性分子 2.3.1 生物活性分子的概念 细胞因子可以帮助MSCs分化并增殖为成骨细胞和成软骨细胞,也可促进内皮血管成血管,与MSCs或支架移植联合使用,共同促进坏死股骨头的骨愈合和血管生成[40-41]。骨组织工程中常用的细胞因子包括骨形态发生蛋白、骨保护素、血管内皮生长因子、肝细胞生长因子(hepatocyte growth factor,HGF)、血小板源性生长因子、粒细胞集落刺激因子、干细胞因子、转化生长因子β、碱性成纤维细胞生长因子、重组人成纤维细胞生长因子等。近年来,外泌体(Exosomes)和基因重组细胞因子是研究热点。 2.3.2 外泌体 外泌体是富含各种生物活性蛋白、核酸、脂类和其他小分子的直径30-150 nm的细胞外脂质结构囊泡,经MSCs分泌后,囊泡内的生物活性分子释放出来并诱导靶细胞的生长分化,在移植区域起到与类似直接干细胞移植的治疗效果,促进骨修复和血管再生,对股骨头坏死起到治疗作用[42-44]。研究表明,外泌体在MSCs的成骨成血管效应中起到重要作用,同时与干细胞相比,外泌体的免疫原性较低、无致瘤性且通透性好[45-47]。NAN等[48]探究了诱导多能干细胞来源的MSCs分泌的外泌体在股骨头坏死血管生成中的治疗作用,将外泌体静脉注射到激素诱导的大鼠骨坏死模型中,实验结果显示与对照组相比,注射外泌体后的骨坏死部位纤维骨痂形成良好,新生骨小梁结构明显,股骨头微血管密度增加,证明外泌体移植可通过促进局部血管生成和防止骨丢失来预防股骨头坏死。进一步研究发现外泌体的促进作用可能与激活内皮细胞PI3K/Akt信号通路有关,阻断PI3K/Akt信号通路后,外泌体对内皮细胞的促进作用消失。GUO等[49]认为外泌体的作用机制可能与增加股骨头组织中的骨形态发生蛋白2和血管内皮生长因子表达有关。其他研究发现,缺氧条件下的BMSCs可以改善外泌体的促血管生成能力,可能与产生更高水平的促血管生成因子有关[50]。 2.3.3 细胞因子与基因重组技术的结合 通过手术治疗直接注射或动脉灌注细胞因子曾是应用细胞因子治疗股骨头坏死的主要方式,但存在细胞因子达不到有效浓度而降低其修复坏死股骨头效率的缺点,目前,随着基因重组技术的发展,将细胞因子的目的基因转染到MSCs中,使MSCs持续有效稳定的分泌细胞因子,是促进骨重建和血管化的有效方法[51]。LEE等[52]探索了血管内皮生长因子和骨形态发生蛋白2基因联合BMSCs治疗股骨头坏死的潜力,评估了血管内皮生长因子与骨形态发生蛋白2的联合作用在体外和体内对成骨和成血管的效应,构建共表达血管内皮生长因子和骨形态发生蛋白2的腺相关病毒载体,然后将腺相关病毒载体转染到BMSCs中。实验结果表明,相比于仅表达其中一种生长因子,转染共表达载体的细胞能产生更多的骨形态发生蛋白2和血管内皮生长因子,毛细血管和骨形成明显高于其他各组,证明同时表达血管内皮生长因子和骨形态发生蛋白2的BMSCs对诱导血管和骨形成呈相互促进作用。SHU等[53]构建重组质粒pcDNA3.1-hVEGF165,将其装填到生物骨移植材料脱蛋白骨中,检测植入坏死股骨头中的血管新生情况,结果显示重组质粒pcDNA3.1-hVEGF165转染的BMSCs表达hVEGF165 mRNA数目增多,VEGF165和Ⅰ型胶原蛋白明显表达,形成了更多的毛细血管,证明血管内皮生长因子基因转移移植是治疗骨坏死一种潜在的方法。TU等[54]将携带HGF基因的重组腺病毒(rAd-HGF)转染到BMSCs中,探究rAd-HGF对BMSCs增殖及成骨分化的影响,发现高表达HGF的BMSCs骨修复效果得到增强,对BMSCs的成骨分化和增殖具有促进作用,同时发现抑制WNT通路可以显著促进细胞成骨,因此联合应用rAd-HGF与WNT通路抑制剂是利用HGF基因修饰BMSCs治疗股骨头坏死的可行方式。CAO等[55]通过实验研究了股骨头坏死患者miR-1207-5p的表达水平及其与血管内皮生长因子的相关性,发现股骨头坏死组坏死股骨头组织和血清中miR-1207-5p的表达水平显著上调,并且miR-1207-5p表达水平越高,血管内皮生长因子表达水平越低。因此,CAO等[55]认为miR-1207-5p导致股骨头坏死可能与miR-1207-5p对血管内皮生长因子的靶向抑制有关,miR-1207-5p通过介导血管内皮生长因子调节股骨头坏死,有望成为临床预防和治疗股骨头坏死的新靶点。然而,CAO等[55]虽然发现了miR-1207-5p对激素性股骨头坏死的调控作用与其对血管内皮生长因子的抑制有关,但未探索到miR-1207-5p的直接靶点。"

| [1] HINES JT, JO WL, CUI Q, et al. Osteonecrosis of the Femoral Head: an Updated Review of ARCO on Pathogenesis, Staging and Treatment. J Korean Med Sci. 2021;36(24):e177. [2] 孙懿,赵海燕,成杰,等.激素性股骨头坏死发生机制的研究进展[J].中国矫形外科杂志,2023,31(1):58-62. [3] 韩杰,林智宇,徐志为,等.miRNA通过骨代谢机制干预股骨头坏死[J].中国组织工程研究,2023,27(32):5238-5248. [4] MONT MA, SALEM HS, PIUZZI NS, et al. Nontraumatic Osteonecrosis of the Femoral Head: Where Do We Stand Today? A 5-Year Update. J Bone Joint Surg Am. 2020;102(12):1084-1099. [5] MURAB S, HAWK T, SNYDER A, et al. Tissue Engineering Strategies for Treating Avascular Necrosis of the Femoral Head. Bioengineering (Basel). 2021;8(12):200. [6] 林苗远,杨继滨,闫文强,等.组织工程技术促进股骨头坏死骨组织再血管化的研究进展[J].中国修复重建外科杂志,2021,35(11):1479-1485. [7] ZHOU W, QU M, LV Y, et al. New Advances in Stem Cell Therapy for Osteonecrosis of the Femoral Head. Curr Stem Cell Res Ther. 2019;14(3): 226-229. [8] XU Y, JIANG Y, XIA C, et al. Stem cell therapy for osteonecrosis of femoral head: Opportunities and challenges. Regen Ther. 2020;15:295-304. [9] ZHANG F, YAN Y, PENG W, et al. PARK7 promotes repair in early steroid-induced osteonecrosis of the femoral head by enhancing resistance to stress-induced apoptosis in bone marrow mesenchymal stem cells via regulation of the Nrf2 signaling pathway. Cell Death Dis. 2021;12(10):940. [10] JIN H, XU T, CHEN Q, et al. The Fate and Distribution of Autologous Bone Marrow Mesenchymal Stem Cells with Intra-Arterial Infusion in Osteonecrosis of the Femoral Head in Dogs. Stem Cells Int. 2016;2016: 8616143. [11] ZHANG F, PENG W, ZHANG J, et al. P53 and Parkin co-regulate mitophagy in bone marrow mesenchymal stem cells to promote the repair of early steroid-induced osteonecrosis of the femoral head. Cell Death Dis. 2020; 11(1):42. [12] LAN T, LUO M, WEI X. Mesenchymal stem/stromal cells in cancer therapy. J Hematol Oncol. 2021;14(1):195. [13] 谢志鸿,彭吾训.骨髓间充质干细胞治疗股骨头坏死的研究进展[J].实用医学杂志,2021,37(1):20-24. [14] LI R, LIN QX, LIANG XZ, et al. Stem cell therapy for treating osteonecrosis of the femoral head: From clinical applications to related basic research. Stem Cell Res Ther. 2018;9(1):291. [15] 刘江锋.髓芯减压联合自体骨髓间充质干细胞移植治疗股骨头坏死[J].中国组织工程研究,2019,23(29):4599-4604. [16] 杨武,杨韵霏,郭民康,等.miR-100-5p通过抑制大鼠骨髓间充质干细胞的迁移和成骨分化参与非创伤性股骨头坏死[J].细胞与分子免疫学杂志,2022,38(2):159-164. [17] WANG Z, SUN QM, ZHANG FQ, et al. Core decompression combined with autologous bone marrow stem cells versus core decompression alone for patients with osteonecrosis of the femoral head: A meta-analysis. Int J Surg. 2019;69:23-31. [18] ZHANG C, FANG X, HUANG Z, et al. Addition of Bone Marrow Stem Cells Therapy Achieves Better Clinical Outcomes and Lower Rates of Disease Progression Compared With Core Decompression Alone for Early Stage Osteonecrosis of the Femoral Head: A Systematic Review and Meta-Analysis. J Am Acad Orthop Surg. 2020;28(23):973-979. [19] ZHANG W, ZHENG C, YU T, et al. The therapeutic effect of adipose-derived lipoaspirate cells in femoral head necrosis by improving angiogenesis. Front Cell Dev Biol. 2022;10:1014789. [20] SCHUBERT T, LAFONT S, BEAURIN G, et al. Critical size bone defect reconstruction by an autologous 3D osteogenic-like tissue derived from differentiated adipose MSCs. Biomaterials. 2013;34(18):4428-4438. [21] WANG Y, LUAN S, YUAN Z, et al. The Combined Use of Platelet-Rich Plasma Clot Releasate and Allogeneic Human Umbilical Cord Mesenchymal Stem Cells Rescue Glucocorticoid-Induced Osteonecrosis of the Femoral Head. Stem Cells Int. 2022;2022:7432665. [22] WANG H, LI X, LAI S, et al. Construction of Vascularized Tissue Engineered Bone with nHA-Coated BCP Bioceramics Loaded with Peripheral Blood-Derived MSC and EPC to Repair Large Segmental Femoral Bone Defect. ACS Appl Mater Interfaces. 2023 ;15(1):249-264. [23] YANG N, SUN H, XUE Y, et al. Inhibition of MAGL activates the Keap1/Nrf2 pathway to attenuate glucocorticoid-induced osteonecrosis of the femoral head. Clin Transl Med. 2021;11(6):e447. [24] NAN K, ZHANG Y, ZHANG X, et al. Exosomes from miRNA-378-modified adipose-derived stem cells prevent glucocorticoid-induced osteonecrosis of the femoral head by enhancing angiogenesis and osteogenesis via targeting miR-378 negatively regulated suppressor of fused (Sufu). Stem Cell Res Ther. 2021;12(1):331. [25] ZHOU M, XI J, CHENG Y, et al. Reprogrammed mesenchymal stem cells derived from iPSCs promote bone repair in steroid-associated osteonecrosis of the femoral head. Stem Cell Res Ther. 2021;12(1):175. [26] ZHANG F, YAN Y, PENG W, et al. PARK7 promotes repair in early steroid-induced osteonecrosis of the femoral head by enhancing resistance to stress-induced apoptosis in bone marrow mesenchymal stem cells via regulation of the Nrf2 signaling pathway. Cell Death Dis. 2021;12(10):940. [27] DUAN P, WANG H, YI X, et al. C/EBPα regulates the fate of bone marrow mesenchymal stem cells and steroid-induced avascular necrosis of the femoral head by targeting the PPARγ signalling pathway. Stem Cell Res Ther. 2022;13(1):342. [28] XU H, WANG C, LIU C, et al. Cotransplantation of mesenchymal stem cells and endothelial progenitor cells for treating steroid-induced osteonecrosis of the femoral head. Stem Cells Transl Med. 2021;10(5):781-796. [29] WANG Y, LUAN S, YUAN Z, et al. The Combined Use of Platelet-Rich Plasma Clot Releasate and Allogeneic Human Umbilical Cord Mesenchymal Stem Cells Rescue Glucocorticoid-Induced Osteonecrosis of the Femoral Head. Stem Cells Int. 2022;2022:7432665. [30] WEI W, DAI H. Articular cartilage and osteochondral tissue engineering techniques: Recent advances and challenges. Bioact Mater. 2021;6(12): 4830-4855. [31] 彭晨健,杜斌,孙光权,等.3D打印β-磷酸三钙支架复合淫羊藿苷微粒修复兔股骨头坏死[J].中国组织工程研究,2019,23(14):2162-2168. [32] SONG Y, WU H, GAO Y, et al. Zinc Silicate/Nano-Hydroxyapatite/Collagen Scaffolds Promote Angiogenesis and Bone Regeneration via the p38 MAPK Pathway in Activated Monocytes. ACS Appl Mater Interfaces. 2020; 12(14):16058-16075. [33] LI B, LIU Z, YANG J, et al. Preparation of bioactive β-tricalcium phosphate microspheres as bone graft substitute materials. Mater Sci Eng C Mater Biol Appl. 2017;70(Pt 2):1200-1205. [34] LING LE, FENG L, LIU HC, et al. The effect of calcium phosphate composite scaffolds on the osteogenic differentiation of rabbit dental pulp stem cells. J Biomed Mater Res A. 2015;103(5):1732-1745. [35] LI F, CAO Z, LI K, et al. Cryogenic 3D Printing of ß-TCP/PLGA Composite Scaffolds Incorporated With BpV (Pic) for Treating Early Avascular Necrosis of Femoral Head. Front Bioeng Biotechnol. 2022;9:748151. [36] HUANG Z, ZHAO Z, LANG J, et al. Therapeutic Study of Thermosensitive Hydrogel Loaded with Super-Activated Platelet Lysate Combined with Core Decompression Technology for the Treatment of Femoral Head Necrosis. Stem Cells Int. 2021;2021:7951616. [37] ZHANG XL, WANG YM, CHU K, et al. The application of PRP combined with TCP in repairing avascular necrosis of the femoral head after femoral neck fracture in rabbit. Eur Rev Med Pharmacol Sci. 2018;22(4):903-909. [38] MARUYAMA M, NABESHIMA A, PAN CC, et al. The effects of a functionally-graded scaffold and bone marrow-derived mononuclear cells on steroid-induced femoral head osteonecrosis. Biomaterials. 2018;187:39-46. [39] MASTROGIACOMO M, PAPADIMITROPOULOS A, CEDOLA A, et al. Engineering of bone using bone marrow stromal cells and a silicon-stabilized tricalcium phosphate bioceramic: evidence for a coupling between bone formation and scaffold resorption. Biomaterials. 2007;28(7):1376-1384. [40] CHE Z, SONG Y, ZHU L, et al. Emerging roles of growth factors in osteonecrosis of the femoral head. Front Genet. 2022;13:1037190. [41] 张景义,海国栋,杨昊飞,等.富集自体骨髓干细胞移植与髓芯减压治疗缺血性股骨头坏死患者血清成纤维细胞生长因子2、缺氧诱导因子1α、血管内皮生长因子的变化[J].中国组织工程研究,2020,24(1):14-19. [42] BEI HP, HUNG PM, YEUNG HL, et al. Bone-a-Petite: Engineering Exosomes towards Bone, Osteochondral, and Cartilage Repair. Small. 2021;17(50): e2101741. [43] TAO SC, YUAN T, RUI BY, et al. Exosomes derived from human platelet-rich plasma prevent apoptosis induced by glucocorticoid-associated endoplasmic reticulum stress in rat osteonecrosis of the femoral head via the Akt/Bad/Bcl-2 signal pathway. Theranostics. 2017;7(3):733-750. [44] 毕煦昆,郭成龙,赵建栋,等.骨髓间充质干细胞来源外泌体及其相关信号通路在激素性股骨头坏死中作用的研究进展[J].中国生物工程杂志,2022,42(10):70-79. [45] LIU X, LI Q, NIU X, et al. Exosomes Secreted from Human-Induced Pluripotent Stem Cell-Derived Mesenchymal Stem Cells Prevent Osteonecrosis of the Femoral Head by Promoting Angiogenesis. Int J Biol Sci. 2017;13(2):232-244. [46] KALLURI R, LEBLEU VS. The biology, function, and biomedical applications of exosomes. Science. 2020;367(6478):eaau6977. [47] 龚东亮,付文芹.BMSC-Exo通过Wnt/β-catenin途径参与股骨头坏死大鼠软骨细胞增殖、迁移和凋亡的机制研究[J].中国免疫学杂志,2022, 38(15):1819-1823. [48] NAN K, ZHANG Y, ZHANG X, et al. Exosomes from miRNA-378-modified adipose-derived stem cells prevent glucocorticoid-induced osteonecrosis of the femoral head by enhancing angiogenesis and osteogenesis via targeting miR-378 negatively regulated suppressor of fused (Sufu). Stem Cell Res Ther. 2021;12(1):331. [49] GUO SC, TAO SC, YIN WJ, et al. Exosomes from Human Synovial-Derived Mesenchymal Stem Cells Prevent Glucocorticoid-Induced Osteonecrosis of the Femoral Head in the Rat. Int J Biol Sci. 2016;12(10):1262-1272. [50] LI W, LIU Y, ZHANG P, et al. Tissue-Engineered Bone Immobilized with Human Adipose Stem Cells-Derived Exosomes Promotes Bone Regeneration. ACS Appl Mater Interfaces. 2018;10(6):5240-5254. [51] YIN S, ZHANG W, ZHANG Z, et al. Recent Advances in Scaffold Design and Material for Vascularized Tissue-Engineered Bone Regeneration. Adv Healthc Mater. 2019;8(10):e1801433. [52] LEE E, KO JY, KIM J, et al. Osteogenesis and angiogenesis are simultaneously enhanced in BMP2-/VEGF-transfected adipose stem cells through activation of the YAP/TAZ signaling pathway. Biomater Sci. 2019;7(11):4588-4602. [53] SHU P, SUN DL, SHU ZX, et al. Therapeutic Applications of Genes and Gene-Engineered Mesenchymal Stem Cells for Femoral Head Necrosis. Hum Gene Ther. 2020;31(5-6):286-296. [54] TU YJ, YE AF, PAN ZM, et al. Regulation of expression of HGF in BM-MSCs by baculovirus-mediated transduction. Cell Biol Int. 2013;37(7):659-668. [55] CAO HJ, ZHENG LZ, WANG N, et al. Src blockage by siRNA inhibits VEGF-induced vascular hyperpemeability and osteoclast activity - an in vitro mechanism study for preventing destructive repair of osteonecrosis. Bone. 2015;74:58-68. |
| [1] | Lai Pengyu, Liang Ran, Shen Shan. Tissue engineering technology for repairing temporomandibular joint: problems and challenges [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(在线): 1-9. |
| [2] | Chen Shuai, Jin Jie, Han Huawei, Tian Ningsheng, Li Zhiwei . Causal relationship between circulating inflammatory cytokines and bone mineral density based on two-sample Mendelian randomization [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(8): 1556-1564. |
| [3] | Cai Yaohao, Lang Lyu, Li Hong. Assessing the bone mass of the residual alveolar ridge in the first molar for implant placement by cone-beam computed tomography [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(8): 1572-1577. |
| [4] | Cao Yue, Ye Xinjian, Li Biyao, Zhang Yining, Feng Jianying. Effect of extracellular vesicles for diagnosis and therapy of oral squamous cell carcinoma [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(7): 1523-1530. |
| [5] | Sun Yuting, Wu Jiayuan, Zhang Jian. Physical factors and action mechanisms affecting osteogenic/odontogenic differentiation of dental pulp stem cells [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(7): 1531-1540. |
| [6] | Yang Zhihang, Sun Zuyan, Huang Wenliang, Wan Yu, Chen Shida, Deng Jiang. Nerve growth factor promotes chondrogenic differentiation and inhibits hypertrophic differentiation of rabbit bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(7): 1336-1342. |
| [7] | Hu Taotao, Liu Bing, Chen Cheng, Yin Zongyin, Kan Daohong, Ni Jie, Ye Lingxiao, Zheng Xiangbing, Yan Min, Zou Yong. Human amniotic mesenchymal stem cells overexpressing neuregulin-1 promote skin wound healing in mice [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(7): 1343-1349. |
| [8] | Jin Kai, Tang Ting, Li Meile, Xie Yuan. Effects of conditioned medium and exosomes of human umbilical cord mesenchymal stem cells on proliferation, migration, invasion, and apoptosis of hepatocellular carcinoma cells [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(7): 1350-1355. |
| [9] | Li Dijun, Jiu Jingwei, Liu Haifeng, Yan Lei, Li Songyan, Wang Bin. Three-dimensional gelatin microspheres loaded human umbilical cord mesenchymal stem cells for chronic tendinopathy repair [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(7): 1356-1362. |
| [10] | Liu Qi, Li Linzhen, Li Yusheng, Jiao Hongzhuo, Yang Cheng, Zhang Juntao. Icariin-containing serum promotes chondrocyte proliferation and chondrogenic differentiation of stem cells in the co-culture system of three kinds of cells [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(7): 1371-1379. |
| [11] | Zhang Zhenyu, Liang Qiujian, Yang Jun, Wei Xiangyu, Jiang Jie, Huang Linke, Tan Zhen. Target of neohesperidin in treatment of osteoporosis and its effect on osteogenic differentiation of bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(7): 1437-1447. |
| [12] | Li Jialin, Zhang Yaodong, Lou Yanru, Yu Yang, Yang Rui. Molecular mechanisms underlying role of mesenchymal stem cell secretome [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(7): 1512-1522. |
| [13] | He Bo, Chen Wen, Ma Suilu, He Zhijun, Song Yuan, Li Jinpeng, Liu Tao, Wei Xiaotao, Wang Weiwei, Xie Jing . Pathogenesis and treatment progress of flap ischemia-reperfusion injury [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(6): 1230-1238. |
| [14] | Li Shuai, Liu Hua, Shang Yonghui, Liu Yicong, Zhao Qihang, Liu Wen. Stress distribution on the maxilla when wearing the Twin-block appliance for Class II malocclusion [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(5): 881-887. |
| [15] | Ding Zhili, Huang Jie, Jiang Qiang, Li Tusheng, Liu Jiang, Ding Yu. Constructing rabbit intervertebral disc degeneration models by different methods under X-ray guidance: a comparative study [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(5): 995-1002. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||