Chinese Journal of Tissue Engineering Research ›› 2020, Vol. 24 ›› Issue (5): 766-772.doi: 10.3969/j.issn.2095-4344.2436
Previous Articles Next Articles
Basic science related to tendinopathy: microbiomechanics and stress shielding
Liu Chunyu1, 2, Han Xiaoyan2, Wang Lin1
- 1Beijing Sport University, Beijing 100084, China; 2School of Physical Health, Yulin Normal University, Yulin 537000, Guangxi Zhuang Autonomous Region, China
-
Received:2019-04-13Revised:2019-04-29Accepted:2019-06-22Online:2020-02-18Published:2020-01-10 -
Contact:Wang Lin, Professor, Doctoral supervisor, Beijing Sport University, Beijing 100084, China -
About author:Liu Chunyu, Doctoral candidate, Associate professor, Beijing Sport University, Beijing 100084, China; School of Physical Health, Yulin Normal University, Yulin 537000, Guangxi Zhuang Autonomous Region, China
CLC Number:
Cite this article
Liu Chunyu, Han Xiaoyan, Wang Lin. Basic science related to tendinopathy: microbiomechanics and stress shielding[J]. Chinese Journal of Tissue Engineering Research, 2020, 24(5): 766-772.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
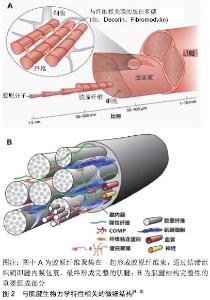
2.1 与肌腱生物力学特性相关的微细结构 2.1.1 肌腱的微细结构 肌腱微细结构组成决定了其形态和生物力学性质。具体来说,肌腱的生物力学性质主要来源于其特殊的细胞外基质结构,总体而言,低血管和低细胞性及丰富的细胞外基质是肌腱独特的组织学特征。肌腱细胞外基质主要由蛋白聚糖、结构蛋白如胶原及糖蛋白3种主要成分组成[1]。 胶原蛋白是肌腱的主要成分,其中Ⅰ型胶原占肌腱干质量的65%-80%,甚至占到正常肌腱中总胶原的近95%[2],主要以纵向方式排列,赋予肌腱很高的拉伸强度。肌腱具有严密的逐层分级的结构,肌腱纤维的基本单位从胶原分子开始。胶原分子由3条呈螺旋状排列的多肽链组成,胶原分子聚集成微纤维,进而聚集成胶原纤维,胶原纤维被认为是肌腱的基本力学传递单位。胶原纤维聚集在一起形成胶原纤维束,通过结缔组织鞘即腱内膜包裹,最终形成完整的肌腱[3],见图2A[4]。Ⅲ型胶原是肌腱细胞外基质中第二常见的胶原类型[5],主要存在腱内膜与腱外膜中,组织不太整齐、提供的强度较低,它是肌腱和韧带愈合早期合成的主要胶原类型[6]。Ⅴ型胶原位于Ⅰ型胶原原纤维的中心,可能有助于原纤维的形成。除此之外,还存在少量其他类型(Ⅱ、Ⅵ、Ⅸ、Ⅹ和Ⅺ)的胶原。上述逐层分级的结构方向上与骨骼肌轴向平行,密集排列在其他细胞外基质成分之中[7]。 在胶原蛋白上还附着一些蛋白聚糖。其中与肌腱相关的最主要的蛋白聚糖是核心蛋白聚糖,占肌腱蛋白聚糖干质量的80%,其有助于肌腱的发育,主要分布在拉伸区,可以使肌腱适应拉伸载荷[8]。其他如双糖链蛋白聚糖、纤维调节素等蛋白聚糖也少量存在,与Ⅰ型胶原结合,有利于形成大的成熟的胶原原纤维,调节肌腱的强度[9]。这些蛋白聚糖携带高度负电荷,吸引并结合水分子,能够形成水性的胶状物并影响组织的黏弹性,帮助组织抵抗压缩力[10]。蛋白聚糖可以影响肌腱中许多重要的生理过程,包括离子转运、水潴留、营养物质的扩散、介导细胞-基质间相互作用及生长因子和酶在基质中的螯合[4]。除蛋白聚糖外,促使肌腱细胞同基质结合的其他糖蛋白成分,也是保证肌腱结构完整性的重要组成部分,其中弹性蛋白比较常见,它通常与Ⅰ型胶原纤维结合形成弹性纤维并可以协助储存弹性势能[6];另外还包括纤连蛋白、腱生蛋白C及软骨寡聚体基质蛋白质等,通过与胶原和其他结构成分的相互作用促进损伤后的细胞外基质修复和机械稳定性,此外,腱生蛋白C一般在肌腱病变中表达上调[1],见图2B[8]。肌腱细胞外基质对肌腱抵抗机械力和修复损伤反应的能力具有重要影响,一些作者认为细胞外基质合成和降解的不平衡是导致肌腱结构退化的关键原因[11]。在肌腱的细胞外基质中还存在几种不同类型的肌腱细胞,多数属于成纤维细胞,它们负责合成和维持肌腱的细胞外基质成分[6]。 "
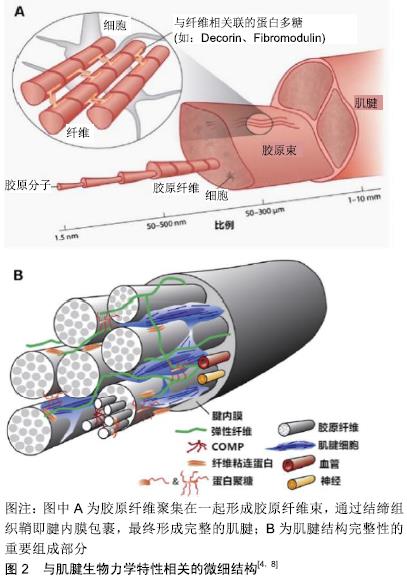
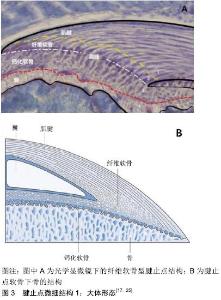
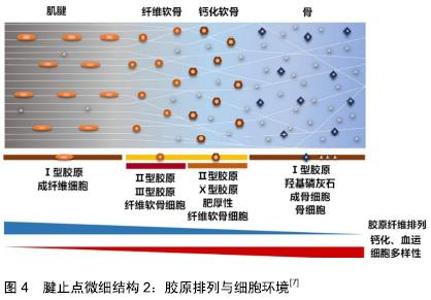
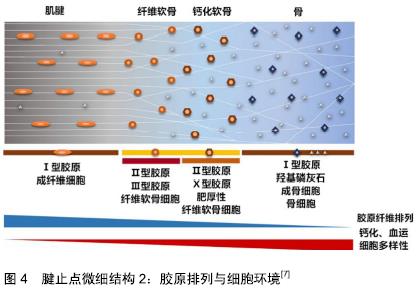
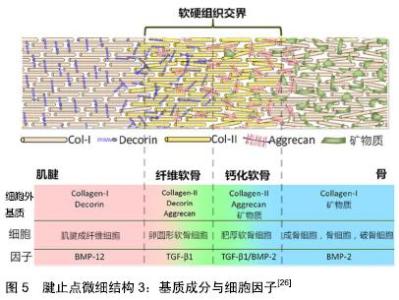
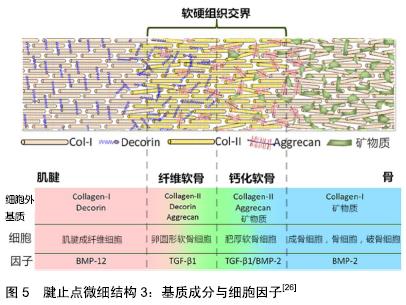
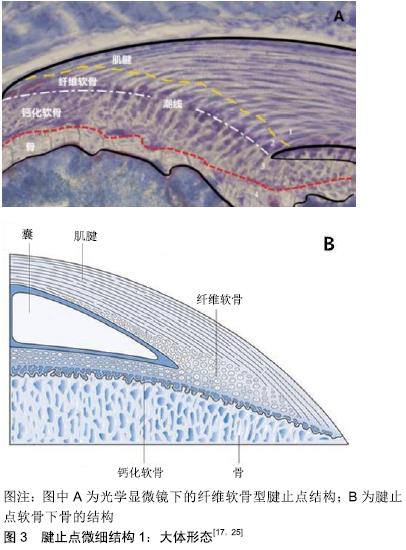
2.1.2 腱止点微细结构 腱止点是一种高度组织化的结构,有时也被称为腱止点复合体,主要包括2种类型,纤维型和纤维软骨型。纤维型腱止点也被称为间接插入,其特点是在发育过程中与骨膜结合,最终与长骨的干骺端或骨干相结合。而纤维软骨型腱止点更为常见,又称为直接插入,其特征是肌腱通过复杂的过渡组织直接与骨骺或骨突结合,肌腱的致密胶原纤维逐渐与纤维软骨相互啮合,纤维软骨逐渐钙化并继续进入邻近的皮质骨,见图3A所示。如此将2个不同的组织连接在一起,允许肌肉产生的力量传递到骨骼,并导致运动,腱止点结构不仅能使肌腱或韧带稳定地锚固到骨表面中,而且还能够平稳地传导机械力,起到“拉伸制动”的作用,即防止肌腱进入应力集中区域时变窄,腱止点是肌腱与骨之间进行力学传递的核心。因此,肌腱常常在它们的腱止点部位向外张开,以适应骨骼锚固和抵抗插入角度变化对其的影响[12]。这些功能与其逐渐过渡的分层微细结构关系密切。 纤维软骨型腱止点在光学显微镜下可以分为肌腱本身、纤维软骨、钙化软骨和骨4个过渡区域[13],如图2A所示。第一个区域由肌腱本身组成,并且具有类似于在肌腱中部类似的性质,该区域由排列良好的Ⅰ型胶原、少量Ⅲ型胶原和少量蛋白聚糖组成。第二个区域由纤维软骨组成,标志着向骨性材料过渡的开始,该区域主要由Ⅱ型和Ⅲ型胶原蛋白组成。为了消散应力,胶原纤维排列不如肌腱区域的Ⅰ型胶原那样排列整齐,并被少量的异染性细胞外基质包围[14]。与肌腱区域一样也散布着少量蛋白聚糖,不同之处在于,肌腱区域的蛋白聚糖以小分子富含亮氨酸的蛋白为主,如核心蛋白聚糖,而纤维软骨区的则以与透明质酸一起结合的大分子蛋白聚糖为主,如可聚蛋白多糖。富含亮氨酸的蛋白已被证明可在调节纤维滑动方面发挥重要作用[8,15],从而影响肌腱黏弹性和拉伸强度[8],而大分子蛋白聚糖则可以使组织具有更强大的抵抗压缩和牵伸负荷的能力[16]。第三个区域由钙化纤维软骨组成,矿物质含量逐渐增加,主要的胶原蛋白类型是Ⅱ型,并且有大量的Ⅹ型胶原蛋白以及可聚蛋白多糖存在,胶原Ⅹ可能与软骨钙化作用有关[17]。在未钙化和钙化的纤维软骨之间有一个狭窄的嗜碱性无血管区域,被称为“潮线”,一般认为其代表了机械上软硬组织之间的界限[18]。健康腱止点的潮线相对平直光滑,这种结构对于减少软骨损伤风险有重要意义,虽然潮线区分开了钙化软骨与非钙化(纤维)软骨2个区域,但这2个区域的胶原纤维仍然是连续的[19]。最后,第四个区域由骨组成,Ⅰ型胶原蛋白占主导地位,并具有非常密集的矿物质含量,为腱止点提供附着部位[20]。腱止点软骨下骨显著的特征之一是致密骨的缺乏[21],而这可能有助于在腱止点上加载应力时骨骼轻微变形,使得应力通过小梁网在骨本身内部继续传递[22]。与正常潮线的平直光滑相反,钙化软骨与骨之间的界限高度不规则,见图3B,这是肌腱和骨骼之间的真正的原子边界,是组织结合的真实部位[21]。这种不规则的形状增加了2种组织之间的接触面积,因此可以更好地促进锚固[23]。综上,腱止点在胶原结构、细胞外基质组成、矿物质含量及黏弹性等方面沿上述4层结构逐渐持续变化,见图4,5,这种性质的渐变对于减少应力集中和帮助肌腱和骨之间有效的负荷传递都是必要的[24],但具体机制尚需进一步研究。 "
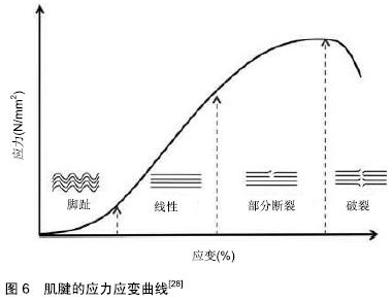
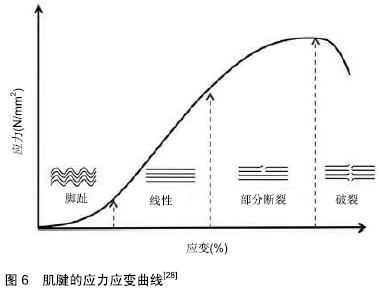
2.1.3 肌腱的生物力学特性 肌腱作为一个整体结构在承受载荷时,可以表现出其各向异性、非线性、黏弹性等特殊的力学性能特点[27],这些特点均与其微细结构密切相关。肌腱的纵向排列的纤维状结构导致各向异性和非线性特性。各向异性是指肌腱属于具有方向依赖性的材料,这导致其在沿纵向轴和横向轴的力学性能相差巨大[28]。除了各向异性特性之外,肌腱还在承受负荷时显示出非线性特征,这种特征的典型表现可以用肌腱应力-应变曲线(图6)中的不同区域来表示,在静止状态下肌腱中的腱纤维呈现出一个卷曲的结构,当承受负荷时这种卷曲的结构会慢慢变直[29]。随着应力的增加,进入区域Ⅰ,也就是是曲线的初始凹陷部分,肌腱的刚度逐渐增加,这一区域被称为“脚趾”区域,肌腱通过减小静息时胶原纤维的卷曲程度来拉长肌腱,但它们不会引起进一步的纤维拉伸,此时的负荷不会超过肌腱的弹性极限,应力去除后肌腱将恢复到其初始长度。应力继续增加,使肌腱进入“线性”区域Ⅱ,在该区域中,应力施加在已经拉直的纤维中使其进一步拉伸。在该区域的终点部分纤维开始破裂,肌腱硬度开始下降,从这一点开始去除应力肌腱也不会恢复其初始长度。随后进入区域Ⅲ,这时的纤维破裂以不可预测的方式发生。应力继续增加,进入区域Ⅳ,肌腱发生完全破裂。肌腱的非线性行为不仅依赖于胶原蛋白与胶原纤维束的机械强度,还依赖于纤维间的相互作用,如胶原的重新排列、卷曲,纤维-蛋白聚糖间的相互作以及胶原交联作用等[30]。研究表明,机械加载过程中的关键变形是通过拉直胶原蛋白的三螺旋结构,然后进行轴向拉伸和最终的分子展开来实现的[31]。黏弹性是材料显示出弹性和黏性行为的能力,一般用于描述流体。黏性是指材料抵抗变形性的特性,而弹性是指材料在导致变形的力被移除后恢复其原始形状的能力。实际上,肌腱的黏弹性行为还可以使整个肌腱表现出蠕变、应力松弛和机械滞后等特性。通常认为机械滞后是由于水通过组织运动和多层纤维复合结构的重新排序而发生的[8]。关于肌腱的黏弹性特征,有学者认为弹性是胶原三螺旋结构被拉伸的结果,而黏度是水合基质和其他纤维分子间相互作用的结果[32-33]。当肌腱承受负荷时,胶原纤维将沿其负载轴方向移动,这种机制称为胶原纤维重新排列,目的是增加肌腱的强度[28]。胶原卷曲是胶原纤维内可见的周期性波形活动,与胶原的机械行为有关[34]。尽管卷曲可以随着张力而变平或恢复,但有研究发现即使在完全拉直纤维束时,分子的卷曲也没有完全消失。这一发现提示该机制可能就是肌腱吸收冲击的形态学基础[35]。蛋白聚糖在肌腱负荷反应中的作用在过去10年中备受争议[36-37]。据推测,蛋白聚糖可以机械地连接相邻的胶原蛋白纤维,如核心蛋白聚糖就可以在很大程度上调节黏弹性参数的变化[38]。胶原蛋白的分子交联在肌腱对负荷的反应中也起着重要作用。交联为胶原蛋白纤维提供了结构完整性,也有助于在纤维内和纤维之间传递负荷[39]。但关于胶原交联和机械性能之间的结构-功能关系仍缺乏确凿的证据。 "
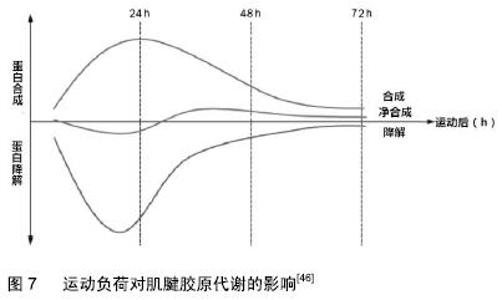
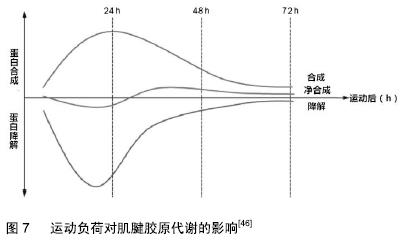
2.2 肌腱急性损伤带来的相关生物力学改变 在肌腱接受急性损伤或手术修复后的愈合过程,通常可分为炎症、增殖与重塑3个可相互重叠的阶段。修复后的肌腱组织在本质上变得更具纤维性,而肌腱细胞和胶原纤维与应力方向一致。胶原Ⅲ的生成速度减慢,并逐渐被胶原Ⅰ合成所取代。组织在本质上变得更像瘢痕,特征为肌腱细胞代谢和血管显著减少[40],进而导致强度降低和硬度增加。肌腱愈合的并发症除了包括瘢痕的形成以外,还包括影响肌腱组织滑动的粘连形成等[41]。肌腱纤维在愈合过程中早期就失去平行排列,而瘢痕主要由紊乱的胶原组成[42]。研究显示瘢痕愈合组织比天然肌腱弱得多,即使在损伤后40周生物力学性能仍显示显著降低。即使肌腱的胶原蛋白含量恢复到正常水平,胶原交联密度也会降低且不会最终恢复。修复后的肌腱其机械性能永远不会恢复到未受伤的水平,并且修复也不会重建腱止点部位的复杂的过渡组织特征。与天然肌腱和韧带相比,愈合形成的瘢痕组织与正常肌腱相比有许多生物学特点上的不同。瘢痕组织胶原Ⅰ水平较低,而胶原Ⅲ和Ⅴ的水平增加[43]。此外,蛋白聚糖的水平在愈合中跟腱中也发生着变化,损伤后双糖链蛋白多糖和核心蛋白聚糖水平增加[42]。基质金属蛋白酶及其抑制剂之间的平衡也在损伤后被破坏,导致过度降解和随后细胞外基质的减弱[44]。 2.3 慢性腱病相关的生物力学因素 腱止点处的代谢率通常较低,这种特点使其能够长期承受拉伸负荷,但同样也会导致其在损伤后愈合缓慢[45],这可以部分解释为什么腱止点正是慢性腱病的好发部位。常见的慢性腱病包括髌腱末端病、投掷肘、网球肘、跟腱止点损伤和肩袖肌腱病等,多见于涉及快速重复加减速运动与离心性收缩运动及剪切性运动之后,属于典型的过度使用性损伤,腱病的发生与腱止点所承受的负荷强度、负荷间歇及负荷类型关系密切,其修复过程缓慢,临床治疗比较困难。 2.3.1 慢性腱病与负荷间歇之间的关系 人体肌腱在承受运动负荷后肌腱胶原合成与降解情况如图7所示,肌腱组织受到负荷后会导致胶原的合成代谢上调,运动后 24 h胶原合成达到高峰,并保持高达70-80 h;然而运动也会导致胶原蛋白的降解。由于这种分解高峰的发生时间早于合成代谢高峰,这会导致训练后第一个24-36 h内的胶原蛋白出现净损失,36 h之后才真正迎来胶原蛋白的净合成增加[46]。因此,锻炼的间隔时间对组织适应至关重要,没有足够休息时间的重复训练可能导致基质降解,最终导致腱病的发生。 "

2.3.2 慢性腱病与负荷类型之间的关系 研究表明,拉伸破坏可能并不是肌腱端病的一个关键特征[47];体外研究也表明,肌腱成纤维细胞对拉伸应变反应良好[48]。即使是通常能损害整个肌腱组织结构完整性的大型拉伸应力,也能被单个成纤维细胞很好地耐受。虽然肌腱通常承受到是拉伸应力,但在某些特殊区域如腱止点和肌腱绕过滑车等部位也会受到压缩力的影响[49]。有学者提出:在腱止点,腱纤维与纤维软骨交错排列,肌腱承受压缩负荷增加,从而刺激软骨化生,间接导致腱病的发生;这可能是大多数临床腱病好发在腱止点的重要原因[50]。ALMEKINDERS等[47,51]在尸体上的研究也表明与肌腱其他部分相比,最常发生腱病的区域往往受到较低的拉伸应变。临床上可识别的腱病通常更容易发生在腱止点深部,这与腱止点内部纤维软骨的区域性差异相对应—纤维软骨在腱止点的最深处通常更为明显。有学者认为这是由于骨腱止点的深部被浅层部分压缩。纤维软骨增多正是对压缩和/或剪切负荷发生了适应性改变[52],这些压缩力可能与腱止点病变密切相关。 2.3.3 慢性腱病与应力不均之间的关系 锚固和分散应力显然是腱止点的基本功能。因此,肌腱和韧带常常在它们的腱止点部向外张开,以适应骨骼锚固和抵抗插入角度变化对其的影响,腱止点这种特殊的结构在解剖学上和生物力学上相对复杂,因为它提供了弹性肌腱与刚性骨之间的过渡界面[27]。肌腱和骨虽然具有相似的抗拉强度,但骨的弹性模量约为肌腱的10倍。因此,腱止点需要平衡它们之间如此大不相同的弹性模量[21]。关于腱止点特性相关的生物力学方面的内容较少,这主要是因为在如此小体积的组织内记录应变水平及该区域的过渡性质存在很多实际的困难,此外腱止点区域也没有特别明确的边界划分。当不同弹性模量的成分并联承担载荷时,较高弹性模量的成分承担较多的载荷,即对低弹性模量成分起到应力、应变遮挡作用,这种现象被称为应力屏蔽或应力遮挡[53]。MAGANARIS等[54]研究认为作用于腱止点上的载荷是不均匀的,腱病相关的病理改变一般都发生在应变水平最低的区域,因此他们提出腱止点上最容易受到损伤的区域最初是应力屏蔽的。对髌腱应变模式的研究也表明,应力屏蔽而非过度拉伸负荷可能是髌腱病变的关键致病因素[51]。这与分别引起肌腱和骨腱结合部退行性变化的压缩载荷的描述密切相关[55],但其中的具体机制仍不明确。 "

| [1] 刘春雨,韩小燕,王琳.末端病与细胞外基质:骨腱结合部重要蛋白及酶类的关系尚需深入研究[J].中国组织工程研究,2016,20(15): 2265-2272. [2] KANNUS P.Structure of the tendon connective tissue.Scand J Med Sci Sports.2000;10(6): 312-320. [3] KILLIAN ML, AVINATTO L, GALATZ LM, et al.The role of mechanobiology in tendon healing.J Shoulder Elbow Surg. 2012;21(2):228-237. [4] YOON JH, HALPER J.Tendon proteoglycans: biochemistry and function.J Musculoskelet Neuronal Interact. 2005;5(1): 22-34. [5] THORPE CT, SCREEN HR.Tendon Structure and Composition. Adv Exp Med Biol.2016;920:3-10. [6] HAMMOUDI TM, TEMENOFF JS.Biomaterials for Regeneration of Tendons and Ligaments. Biomaterials for Tissue Engineering Applications.Springer Vienna, 2011: 307-341. [7] NOURISSAT G, BERENBAUM F, DUPREZ D.Tendon injury: from biology to tendon repair.Nat Rev Rheumatol. 2015;11(4): 223-233. [8] THORPE CT, BIRCH HL, LEGG PD, et al.The role of the non-collagenous matrix in tendon function. Int J Exp Pathol. 2013;94(4):248-259. [9] DERWIN KA, SOSLOWSKY LJ, KIMURA JH, et al. Proteoglycans and glycosaminoglycan fine structure in the mouse tail tendon fascicle.J Orthop Res. 2001;19(2):269-277. [10] YANAGISHITA M.Function of proteoglycans in the extracellular matrix.Acta Pathol Jpn.1993;43(6):283-293. [11] ARNOCZKYS P, LAVAGNINO M, EGERBACHER M, et al. Matrix metalloproteinase inhibitors prevent a decrease in the mechanical properties of stress-deprived tendons: an in vitro experimental study.Am J Sports Med. 2007;35(5):763-769. [12] BENJAMIN M, MORIGGL B, BRENNER E, et al.The "enthesis organ" concept: why enthesopathies may not present as focal insertional disorders.Arthritis Rheum.2004; 50(10):3306-3313. [13] SCHETT G, ORIES RJ, D'AGOSTINO MA, et al.Enthesitis: from pathophysiology to treatment. Nat Rev Rheumatol. 2017; 13(12):731-741. [14] ROSSETTI L, KUNTZ LA, UNOLD E, et al.The microstructure and micromechanics of the tendon-bone insertion.Nat Mater. 2017;16(6):664-670. [15] RIGOZZI S, MULLER R, STEMMER A, et al.Tendon glycosaminoglycan proteoglycan sidechains promote collagen fibril sliding-AFM observations at the nanoscale.J Biomech.2013;46(4):813-818. [16] ANDLEY C, PARKINSON J, SAMIRIC T, et al.Overuse tendinopathy is characterised by changes in the metabolism of proteoglycans present in the extracellular matrix of tendons.J Sci Med Sport.2010;13(supp-S1):e21-22. [17] Apostolakos J, Durant TJ, Dwyer CR, et al.The enthesis: a review of the tendon-to-bone insertion.Muscles Ligaments Tendons J.2014;4(3):333-342. [18] BENJAMIN M, KUMAI T, MILZ S, et al.The skeletal attachment of tendons—tendon ‘entheses’. Comp Biochem Physiol A Mol Integr Physiol.2002;133(4):931-945. [19] LYONS TJ, STODDART RW, MCCLURE SF, et al.The tidemark of the chondro-osseous junction of the normal human knee joint.J Mol Histol.2005;36(3):207-215. [20] THOMOPOULOS S, GENIN GM, GALATZ LM.The development and morphogenesis of the tendon-to-bone insertion - what development can teach us about healing. J Musculoskelet Neuronal Interact.2010; 10(1):35-45. [21] HEMS T, TILLMANN B.Tendon entheses of the human masticatory muscles.Anat Embryol (Berl). 2000;202(3): 201-208. [22] BENJAMIN M, TOUMI H, SUZUKI D, et al.Microdamage and altered vascularity at the enthesis-bone interface provides an anatomic explanation for bone involvement in the HLA-B27- associated spondylarthritides and allied disorders. Arthritis Rheum.2007;56(1):224-233. [23] MILZ S, RUFAI A, UETTNER A, et al.Three-dimensional reconstructions of the Achilles tendon insertion in man.J Anat. 2002;200(Pt 2):145-152. [24] THOMOPOULOS S, ILLIAMS GR, GIMBEL JA, et al.Variation of biomechanical, structural, and compositional properties along the tendon to bone insertion site.J Orthop Res. 2003; 21(3): 413-419. [25] KOLT G, SNYDER-MACKLER L(Eds.).Physical Therapies in Sport and Exercise.2nd Edition.Churchill Livingstone, 2007: 30. [26] WOPENKA B, KENT A, PASTERIS JD, et al.The tendon-to-bone transition of the rotator cuff: a preliminary Raman spectroscopic study documenting the gradual mineralization across the insertion in rat tissue samples.Appl Spectrosc.2008;62(12):1285-1294. [27] CONNIZZO BK, YANNASCOLI SM, SOSLOWSKY LJ. Structure-function relationships of postnatal tendon development: a parallel to healing.Matrix Biol. 2013;32(2): 106-116. [28] LAKE SP, MILLER KS, ELLIOTT DM, et al.Tensile properties and fiber alignment of human supraspinatus tendon in the transverse direction demonstrate inhomogeneity, nonlinearity, and regional isotropy.J Biomech.2010;43(4):727-732. [29] SHARMA P, MAFFULLI N.Biology of tendon injury: healing, modeling and remodeling.J Musculoskelet Neuronal Interact. 2006;6(2):181-190. [30] VERES SP, LEE JM.Designed to fail: a novel mode of collagen fibril disruption and its relevance to tissue toughness.Biophys J.2012;102(12):2876-2884. [31] GAUTIERI A, VESENTINIS, REDAELLI A, et al.Hierarchical structure and nanomechanics of collagen microfibrils from the atomistic scale up.Nano Lett.2011;11(2):757-766. [32] VAN DER RIJT JA, VAN DER WERF KO, BENNINK ML, et al. Micromechanical testing of individual collagen fibrils. Macromol Biosci.2006;6(9):697-702. [33] GAUTIERI A, VESENTINI S, REDAELLI A, et al.Viscoelastic properties of model segments of collagen molecules.Matrix Biol.2012;31(2):141-149. [34] WOO SL, DEBSKI RE, ZEMINSKI J, et al.Injury and repair of ligaments and tendons.Annu Rev Biomed Eng. 2000;2: 83-118. [35] FRANCHI M, FINI M, QUARANTA M, et al.Crimp morphology in relaxed and stretched rat Achilles tendon.J Anat. 2007; 210(1):1-7. [36] LUJAN TJ, UNDERWOOD CJ, JACOBS NT, et al. Contribution of glycosaminoglycans to viscoelastic tensile behavior of human ligament.J Appl Physiol(1985).2009; 106(2):423-431. [37] FESSEL G, GERBER C, SNEDEKER JG.Potential of collagen cross-linking therapies to mediate tendon mechanical properties.J Shoulder Elbow Surg.2012;21(2):209-217. [38] ELLIOTT DM, ROBINSON PS, GIMBEL JA, et al. Effect of altered matrix proteins on quasilinear viscoelastic properties in transgenic mouse tail tendons.Ann Biomed Eng. 2003; 31(5):599-605. [39] UZEL SG, BUEHLER MJ.Molecular structure, mechanical behavior and failure mechanism of the C-terminal cross-link domain in type I collagen.J Mech Behav Biomed Mater. 2011; 4(2):153-161. [40] JAMES R, KESTURU G, BALIAN G, et al.Tendon: biology, biomechanics, repair, growth factors, and evolving treatment options.J Hand Surg Am.2008;33(1):102-112. [41] VOLETI PB, BUCKLEY MR, SOSLOWSKY LJ.Tendon healing: repair and regeneration.Annu Rev Biomed Eng. 2012;14:47-71. [42] ANSORGE HL, ADAMS S, BIRK DE, et al.Mechanical, compositional, and structural properties of the post-natal mouse Achilles tendon.Ann Biomed Eng. 2011;39(7): 1904-1913. [43] NAKAMURA N, HART DA, OORMAN RS, et al.Decorin antisense gene therapy improves functional healing of early rabbit ligament scar with enhanced collagen fibrillogenesis in vivo.J Orthop Res.2000;18(4):517-523. [44] GAROFALO R, CESARI E, VINCI E, et al.Role of metalloproteinases in rotator cuff tear. Sports Med Arthrosc Rev.2011;19(3):207-212. [45] SHARMA P, MAFFULLI N.Tendon injury and tendinopathy: healing and repair.J Bone Joint Surg Am.2005;87(1):187-202. [46] MAGNUSSON SP, LANGBERG H, KJAER M.The pathogenesis of tendinopathy: balancing the response to loading.Nat Rev Rheumatol.2010;6(5):262-268. [47] LYMAN J, WEINHOLD PS, ALMEKINDERS LC.Strain behavior of the distal achilles tendon: implications for insertional achilles tendinopathy.Am J Sports Med. 2004; 32(2):457-461. [48] ALMEKINDERS LC, BAYNES AJ, BRACEY LW.An in vitro investigation into the effects of repetitive motion and nonsteroidal antiinflammatory medication on human tendon fibroblasts. Am J Sports Med.1995;23(1):119-123. [49] COOK JL, PURDAM C.Is compressive load a factor in the development of tendinopathy?Br J Sports Med. 2012;46(3): 163-168. [50] SOSLOWSKY LJ, THOMOPOULOS S, ESMAIL A, et al. Rotator cuff tendinosis in an animal model: role of extrinsic and overuse factors.Ann Biomed Eng.2002;30(8):1057-1063. [51] ALMEKINDERS LC, VELLEMA JH, WEINHOLD PS.Strain patterns in the patellar tendon and the implications for patellar tendinopathy.Knee Surg Sports Traumatol Arthrosc. 2002; 10(1):2-5. [52] BENJAMIN M, RALPHS JR.Biology of fibrocartilage cells.Int Rev Cytol.2004;233:1-45. [53] 刘振东.骨折愈合原理[M].北京:人民军医出版社,2012:116. [54] MAGANARIS CN, ARICI MV, ALMEKINDERS LC, et al. Biomechanics and pathophysiology of overuse tendon injuries: ideas on insertional tendinopathy.Sports Med. 2004; 34(14):1005-1017. [55] BENJAMIN M, RALPHS JR.Fibrocartilage in tendons and ligaments-an adaptation to compressive load.J Anat. 1998; 193(Pt 4):481-494. |
| [1] | Min Youjiang, Yao Haihua, Sun Jie, Zhou Xuan, Yu Hang, Sun Qianpu, Hong Ensi. Effect of “three-tong acupuncture” on brain function of patients with spinal cord injury based on magnetic resonance technology [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-8. |
| [2] | Xu Feng, Kang Hui, Wei Tanjun, Xi Jintao. Biomechanical analysis of different fixation methods of pedicle screws for thoracolumbar fracture [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1313-1317. |
| [3] | Chen Xinmin, Li Wenbiao, Xiong Kaikai, Xiong Xiaoyan, Zheng Liqin, Li Musheng, Zheng Yongze, Lin Ziling. Type A3.3 femoral intertrochanteric fracture with augmented proximal femoral nail anti-rotation in the elderly: finite element analysis of the optimal amount of bone cement [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1404-1409. |
| [4] | Zhou Jihui, Li Xinzhi, Zhou You, Huang Wei, Chen Wenyao. Multiple problems in the selection of implants for patellar fracture [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1440-1445. |
| [5] | Jiang Hongying, Zhu Liang, Yu Xi, Huang Jing, Xiang Xiaona, Lan Zhengyan, He Hongchen. Effect of platelet-rich plasma on pressure ulcers after spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1149-1153. |
| [6] | Zeng Zhen, Hu Jingwei, Li Xuan, Tang Linmei, Huang Zhiqiang, Li Mingxing. Quantitative analysis of renal blood flow perfusion using contrast-enhanced ultrasound in rats with hemorrhagic shock during resuscitation [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1201-1206. |
| [7] | Chai Le, Lü Jianlan, Hu Jintao, Hu Huahui, Xu Qingjun, Yu Jinwei, Quan Renfu. Signal pathway variation after induction of inflammatory response in rats with acute spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1218-1223. |
| [8] | Chen Jiming, Wu Xiaojing, Liu Tianfeng, Chen Haicong, Huang Chengshuo. Effects of silymarin on liver injury and bone metabolism induced by carbon tetrachloride in mice [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1224-1228. |
| [9] | Wan Ran, Shi Xu, Liu Jingsong, Wang Yansong. Research progress in the treatment of spinal cord injury with mesenchymal stem cell secretome [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1088-1095. |
| [10] | Xie Wenjia, Xia Tianjiao, Zhou Qingyun, Liu Yujia, Gu Xiaoping. Role of microglia-mediated neuronal injury in neurodegenerative diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1109-1115. |
| [11] | Kong Desheng, He Jingjing, Feng Baofeng, Guo Ruiyun, Asiamah Ernest Amponsah, Lü Fei, Zhang Shuhan, Zhang Xiaolin, Ma Jun, Cui Huixian. Efficacy of mesenchymal stem cells in the spinal cord injury of large animal models: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1142-1148. |
| [12] | Song Chengjie, Chang Hengrui, Shi Mingxin, Meng Xianzhong. Research progress in biomechanical stability of lateral lumbar interbody fusion [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(6): 923-928. |
| [13] | Xu Yulin, Shen Shi, Zhuo Naiqiang, Yang Huilin, Yang Chao, Li Yang, Zhao Heng, Zhao Lu. Biomechanical comparison of three different plate fixation methods for acetabular posterior column fractures in standing and sitting positions [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(6): 826-830. |
| [14] | Cai Qunbin, Zou Xia, Hu Jiantao, Chen Xinmin, Zheng Liqin, Huang Peizhen, Lin Ziling, Jiang Ziwei. Relationship between tip-apex distance and stability of intertrochanteric femoral fractures with proximal femoral anti-rotation nail: a finite element analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(6): 831-836. |
| [15] | Ma Binxiang, He Wanqing, Zhou Guangchao, Guan Yonglin. Triptolide improves motor dysfunction in rats following spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 701-706. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||