Chinese Journal of Tissue Engineering Research ›› 2020, Vol. 24 ›› Issue (22): 3579-3586.doi: 10.3969/j.issn.2095-4344.2265
Previous Articles Next Articles
Small-caliber tissue-engineered vascular stent: how to produce a material with physiological remodeling activity
Yang Lei1, 2, Li Xiafei3, Dong Yuzhen2, Ma Xianfen1, Zhang Qiqing1, Zhao Liang1
- 1School of Life Sciences and Biotechnology, 3School of Medical Engineering, Xinxiang Medical University, Xinxiang 453003, Henan Province, China; 2First Affiliated Hospital of Xinxiang Medical University, Xinxiang 453003, Henan Province, China
-
Received:2019-09-28Revised:2019-10-08Accepted:2019-11-19Online:2020-08-08Published:2020-04-26 -
Contact:Dong Yuzhen, MD, Chief physician, Master’s supervisor, First Affiliated Hospital of Xinxiang Medical University, Xinxiang 453003, Henan Province, China Zhao Liang, MD, Master’s supervisor, School of Life Sciences and Biotechnology, Xinxiang Medical University, Xinxiang 453003, Henan Province, China -
About author:Yang Lei, Master candidate, School of Life Sciences and Biotechnology, Xinxiang Medical University, Xinxiang 453003, Henan Province, China; First Affiliated Hospital of Xinxiang Medical University, Xinxiang 453003, Henan Province, China -
Supported by:the College Student Innovation and Entrepreneurship Project of Henan Province, No. 141039, 110411, 201910472019; the 3rd National College Student Life Science Project, No. 30252; the Open Project of Henan Provincial Key Laboratory of Nerve Repair of Highland Discipline (Surgery), First Clinical Medicine School of Xinxiang Medical University, No. HNSJXF-2016-011; the Open Project of Central Laboratory of the 7th People’s Hospital of Zhengzhou; the Innovation Support Program for the Postgraduate of Xinxiang Medical University in 2019, No. YJSCX201905Z
CLC Number:
Cite this article
Yang Lei, Li Xiafei, Dong Yuzhen, Ma Xianfen, Zhang Qiqing, Zhao Liang. Small-caliber tissue-engineered vascular stent: how to produce a material with physiological remodeling activity[J]. Chinese Journal of Tissue Engineering Research, 2020, 24(22): 3579-3586.
share this article
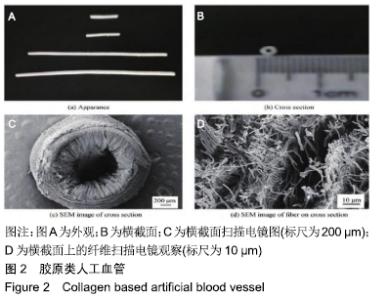
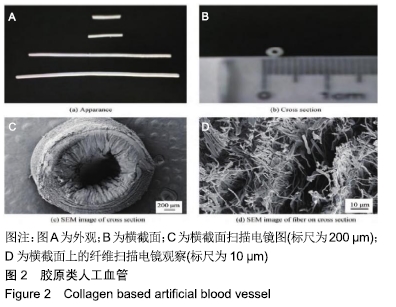
2.1 生物衍生支架材料 生物衍生支架材料主要包括胶原、壳聚糖、纤维蛋白、丝素蛋白、蛛丝蛋白、脱细胞血管基质等,是一种具有良好的生物相容性、可降解、可促进细胞重组的材料。因这些优点存在,使其在再生医学领域中应用有着悠久的历史,已经由简单的细胞微载体发展至高度、复杂生物衍生材料的器官,因而在作为组织工程血管支架材料具有广泛的前景。 2.1.1 胶原 胶原是哺乳动物体内含量最高且广泛存在的一种蛋白质,在维持细胞外基质生物及结构完整性方面中起到重要作用,同时具有良好的生物相容性、无细胞毒性、高可降解性、低免疫原性及抗爆破能力较强等优点。胶原还可以加工成网状、纤维状、海绵状等,并在生物假体心脏瓣膜、血管移植神经再生中应用[7]。为了去研究胶原类生物材料的力学性能,ZHOU等[8]以胶原类为原材料运用交联技术,制备一种双层血管导管,结果发现在干燥情况下交联后的导管最大的拉伸强度可达0.49 MPa,最大断裂伸长率为84.88%;同时,在湿态下,拉伸强度为0.37MPa、断裂伸长比是72.05%,表明该血管支架具有良好的机械性能,有可能成为一种合适的人工血管支架材料。WANG等[9]以聚乳酸和胶原为基础材料,通过静电纺丝技术制备出胶原类的小口径人工血管(d=3.0 mm)(见图2)。在研究中发现随着胶原质量比的增大,其该胶原类的人工血管的拉伸强度和爆裂强度均有所增强;此外,当胶原的质量比是70∶30和90∶10时,可以较好的满足于人造血管力学性能的要求。然而,研究者发现当胶原支架材料迅速退化后,极易引起动脉血管疾病。与此同时,胶原支架最大问题是血栓形成,因而在进行体外研究实验时,常需要进行有效的表面涂层或者预先植入一种具有活性的细胞,进而可很大程度上减少在体内小直径动脉中失败。因此,未来的研究重点是对胶原支架材料如何修饰及预防血栓等问题。 "
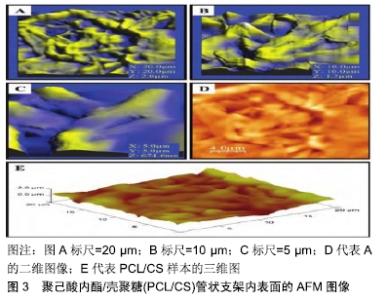
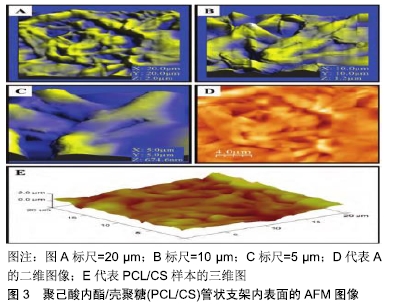
2.1.2 壳聚糖 壳聚糖是由自然界中的几丁质经脱乙酰而生成的,于1859年由Rouget首次发现,由于拥有生物相容性、无毒性、抗菌性和可降解性等优点,因此被广泛应用于生物医学工程、化工和食品等领域中。近期,BADHE等[10]采用溶剂浇铸-共颗粒浸出法制备具有双层管状结构的壳聚糖类水凝胶复合支架,结果表明,该支架的拉伸强度为(95.81±11.00) kPa,断裂伸长率为(112.5±13.0)%,气孔率为82%,16 d体外生物降解率为50%以及20 d内成纤维细胞增殖均是增强的,证实壳聚糖类支架材料可成为一种理想的血管组织工程支架。此外,REZ等[11]利用静电纺丝技术制备出壳聚糖类支架,在显微镜镜下可见其支架中内表面和外表面的形貌呈现出清晰的山脊、山谷结构(图3);另外,相对于内表面,其外表面结构比较粗糙,正是由于该支架内外表面分布着均匀的粗糙结构,使其细胞有利于黏附、增殖。实验结果表明壳聚糖类支架具有良好的生物相容性,可作为一种替代血管应用的材料。尽管研究者们对壳聚糖的研究已经取得满意的结果,但是仍存在诸多需要解决的问题,如生物降解率过快及断裂伸长度、抗冲击强度较差等,因此壳聚糖存在这些不足之处,仍然需要我们进一步去探讨解决。 "

2.1.3 纤维蛋白 纤维蛋白主要来源于人体自身血液中,通过凝血酶作用于纤维蛋白原而形成的,因其具有无免疫反应、良好的生物相容性和无毒性副作用等特性,因此被应用于不同领域的组织工程支架材料制备。为了探讨纤维蛋白类材料是否可成为理想的组织工程血管支架,PANKAJAKSHAN等[12]采用溶剂浇铸方法,制备出一种新型的纤维蛋白类血管支架,接着,将内皮细胞与支架材料进行复合培养,在电子显微镜下观察到复合培养2 h后有黏附行为,同时在培养24 h后可见内皮细胞明显的扩散,直至15 d后,支架表面上还可见连续的内皮细胞单层,该实验结果证实内皮细胞种植的纤维蛋白类支架材料在小口径组织工程血管制备中具有一定应用潜力。此外,GUNDY等[13]运用经编织技术制备出一种纤维蛋白类支架材料,为了研究该材料在冠状动脉平滑肌细胞上细胞活率,进行活死细胞染色实验。分别进行复合培养1周和3周后,结果中可见2个时间点中任何时期都很少见红色的细胞,其红细胞代表着活细胞,该实验表明纤维蛋白类材料具有良好的生物安全性,有潜能成为小口组织工程血管支架材料。但是纤维蛋白常表现出较差的机械性能及稳定性不足,因而纤维蛋白的应用受到一定程度限制。 2.1.4 丝素蛋白 丝素蛋白存在于产丝节肢动物的腺体中,通过蜕变过程纺成纤维,是一种天然的生物衍生材料,其具有良好的机械性能、生物相容性、稳定化学性能等优点,因此丝素蛋白在血管组织工程领域中应用比较广泛[14]。SUZUKI等[15]采用脱胶法从家蚕和野生柞蚕的茧中分离出丝素蛋白,去评价其拉伸性能,通过测量其应力、模量和伸长,可见丝素蛋白类材料具有较强的机械力学特性,实验表明丝素蛋白可作为理想的组织工程血管支架材料。此外,MARCOLIN等[16]运用静电纺丝技术成功制备出丝素类复合管状材料,实验结果表明该材料具有良好的稳定性、较强力学性能,可成为一种小口径血管支架材料。然而丝素蛋白支架材料在体内降解缓慢,且容易导致宿主反应等,这一缺点存在严重阻碍了该材料在小口径组织工程领域的进一步发展。 2.1.5 蛛丝蛋白 蛛丝蛋白属于一种特殊的纤维蛋白,具有热稳定性好、化学稳定性好、弹性强度高、韧性大、伸长度好、耐疲劳性强、生物可降解性高和良好的生物相容性等优点。该蛋白应用于人工合成的肌腱材料、人造皮肤、生物传感器和军事防护材料等领域。为了去探索蛛丝蛋白类血管材料在体内中反应,XIANG等[17]采用静电纺丝技术制备出蛛丝蛋白类复合血管材料,组织学结果可见,相对于聚己内酯(Polycaprolactone,PCL)类支架的周围有明显的宿主组织反应和炎症反应,而蛛丝蛋白类支架却并无明显炎症反应,反而促进宿主细胞的生长,表明该材料可作为组织工程血管支架。赵亮 等[18]将骨髓间充质干细胞种植到蛛丝蛋白血管支架内腔,应用动态培养的方法构建小口径组织工程血管,复合培养7 d后,见细胞在血管支架表面迁移,且迁移到纤维内部增殖,表明该血管支架具有良好的生物相容性,结果表明间充质干细胞与该支架复合培养可成功构建一种小口径组织工程血管(图4)。然而,研究者发现蛛丝蛋白表现出生物力学性能不足,因而如何去克服这一缺陷,仍需要做出深入研究。 "

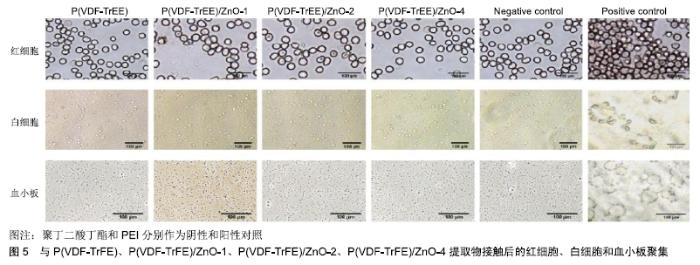
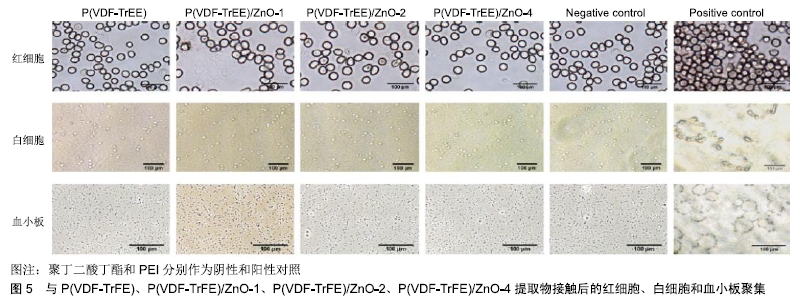
2.1.6 脱细胞血管基质 脱细胞血管基质属于常见的生物衍生支架材料之一。该材料成为目前研究的热点,是因为其具有良好的相容性、低排斥反应性和无毒性等优点[19]。为制备出一种理想的小口径组织工程化血管去构建的天然脱细胞支架,PU等[20]采用不同浓度的十二烷基硫酸钠(sodium dodecyl sulfate,SDS)、脱氧胆酸钠(sodium deoxycholate,SDC)和TritonX-100 (Triton X)联合脱细胞猪颈动脉。从结果发现只有0.5%(SDS+SDC)和1%(SDS+SDC)可完全去除细胞内的细胞内容物,并保留原有的细胞外基质结构。综上所述,基于1%(SDS+ SDC)的方法可获得较好的猪颈动脉支架,并用于构建小口径组织工程血管支架,因此,该材料是一种合适的组织工程血管移植物。此外,赵亮等[21]采用TritonX-100-丹参酚酸B联合处理制备脱细胞血管支架,与Tx组(P < 0.05)相比,在Tx-sal组中脱细胞血管支架保留着较完好血管壁的胶原纤维和弹性纤维,抗拉强度、最大变形量、断裂伸长比、爆裂压力及缝合强度均明显增强。实验表明TritonX-100联合丹参酚酸B处理可成功制备脱细胞效果良好、生物力学性能优良的脱细胞血管支架。然而,脱细胞血管极易携带病原体,体内植入后易发生感染。此外,因该材料的生物力学性能、样本的物种和年龄等因素差异,会导致结果异常。因此,该材料成为小口径组织工程血管支架的路程还很漫长。 2.2 人工合成高分子材料 人工合成高分子材料是由高分子化合物材料构成的,主要包括聚氨酯、聚乳酸、聚己内酯、聚乙烯醇等。与天然衍生支架材料相比,该材料的结构可根据特定的力学性能、降解速率、孔隙率以及微观结构进行精确的制备,其更具有可控性、降解慢、相容性好和机械完整性持久等特点,因而被广泛运用于组织工程材料制备中,同时也成为组织工程血管支架材料领域中热门的研究材料。 2.2.1 聚氨酯 聚氨酯是一种新型有机高分子材料,享有“五大塑料”之一的称号,其具有物理、生物、化学和机械性能良好等优点,因此该生物材料在血管移植物、起搏器、人工瓣膜等领域中得到广泛的应用[22]。NAFISEH等[23]采用共电纺方法制备出聚氨酯类小直径血管支架,为了评估该支架材料在体内生物相容性情况,将支架材料植入到大鼠皮下,植入45 d后,在病理切片中观察到,与对照组相比,其聚氨酯类组中只出现轻度水肿、中度纤维化和无异物肉芽肿,其表明该材料具有良好的相容性,实验表明该血管支架有潜能可作为一种小直径血管移植物。但是聚氨酯表现出疲劳性能较弱以及长期氧化降解不足,因而这一问题急迫需要研究者去解决。 2.2.2 聚乳酸 聚乳酸是以乳酸为原料构成的聚酯,该材料是无刺激、无害的合成高分子材料,拥有良好的生物相容性、可降解性和吸收性等优点[24]。ABUDULA等[25]利用电纺制备出不同比率的聚乳酸/聚丁二酸丁酯纤维支架,支架材料与成纤维细胞复合培养7 d后,在扫描电镜下观察到,与单独的聚乳酸和聚丁二酸丁酯支架相比,聚乳酸/聚丁二酸丁酯支架具有更好的细胞附着性能以及可促进附着的成纤维细胞沿纤维方向扩展,实验表明该复合支架材料血管组织工程应用中具有巨大的潜力。此外,BUSCEMI等[26]采用静电纺丝技术制备出管状聚乳酸类材料,为了研究该材料与体内相关反应,研究者对该组织切片学进行分析,结果可见慢性炎症存在,同时可见明显的新生血管形成。实验表明聚乳酸类材料适合于血管替代的一种材料,同时也适合于替代天然血管。由于聚乳酸存在一些缺点,即脆性太大、韧性不足和易碎,所以不能单独用于血管支架移植中。 2.2.3 聚己内酯 聚己内酯是以ε-己内酯单体聚合而成的高分子有机聚合物,其属于一种无毒、不溶水的聚合型聚酯。该材料的优点主要包括力学性能强和生物相容性好等,因此应用于医用缝合材料和组织工程等领 域[27-28]。近期,LI等[29]采用聚己内酯类材料建立复合血管移植物模型,去探讨不同复合血管移植的结构与力学性能之间的关系。实验结果表明,与单一材料相比,该材料的力学性能显著提高,复合血管移植具有较强的拉伸强度、断裂强度和缝合强度,可做为一种组织工程血管支架材料。然而聚己内酯作为一种体内血管移植物的材料时,其降解性能要比其他材料缓慢,且属于一种疏水性及生物惰性强的生物材料,因此如何制备出生物相容性好的材料以及如何去修饰表面生物活性等问题,还有待需要研究并解决。 2.2.4 聚乙烯醇[Poly(vinyl alcohol),PVA] 聚乙烯醇是通过醋酸乙烯酯单体聚合成聚醋酸乙烯酯,由乙酰基水解而形成的,是一种白色、无味、溶于水,在自然界中广泛存在的高分子聚合物,其具有亲水性好、生物相容性好、无毒性、力学性能强、生物可降解性高和易于细胞增殖等优点,因而用于粘合剂、乳化稳定剂、纤维加工和组织工程血管等领域[30]。TANG等[31]为提高细菌纳米纤维素管的性能,在细菌纳米纤维素管中引入聚乙烯醇制备出复合材料,采用在2个生物反应器中制备2种不同内部结构的细菌纳米纤维素管,并通过热诱导相分离法对聚乙烯醇管和聚乙烯醇-细菌纳米纤维素管状复合材料进行比较。结果发现聚乙烯醇浸润在细菌纳米纤维素管中机械性能和透水性显著提高,该材料可作为一种新型的血管移植生物材料。但是单一的聚乙烯醇缺乏促进细胞黏附能力,且其性能易受分子量和水解程度的影响。接下来,研究者应对聚乙烯醇进行化学改性,以便制备出更加理想的小口径组织工程血管支架。 2.3 复合材料 天然生物材料包括胶原、脱细胞血管基质、纤维蛋白等,其具有天然的组织结构,良好的生物相容性,可提供细胞所需的信号,促进细胞黏附及保留分化功能等优点。高分子合成材料具有可调控性降解速率、机械性能强等优点。然而,合成材料常缺乏天然组织所具有的力学性能等。理想的血管移植支架应具备与天然动脉的力学性能相一致,还应具有可降解性能等特点。研究发现单一材料不能同时满足这些要求,为了克服这一问题,研究者们将天然生物和高分子合成材料混合构建复合支架,以改善每种材料中各自具有的特性,从而充分发挥不同材料的优良性能,因此复合材料成为目前比较热门的发展趋势。 2.3.1 两组分复合材料 与合成单一的材料相比,2组分复合材料具有良好的物理、化学性质,生物相容性好,能为组织再生提供适宜的微环境,因此在中国现代化发展过程中起到举足轻重的作用,其应用十分广泛[32]。近期,JUNDZI等[33]运用静电纺丝技术制备内径为3 mm,厚度为200 μm的聚乳酸-己内酰纤维支架,组织学分析表明,与单一支架材料相比,该材料未见明显的炎症反应,并且与宿主组织可更好地结合。实验表明聚乳酸-己内酰材料具有良好的血管化能力,可应用于血管组织工程领域中。同样,TAO等[34]利用电纺技术成功制备出壳聚糖/聚乳酸-己内酰复合支架,在细胞增殖实验中可见,与单纯的聚乳酸-己内酰支架相比,该支架表面细胞生长数量明显要多,这是由于聚乳酸-己内酰支架是疏水性,加入亲水性的壳聚糖可提高其对细胞黏附作用,实验结果表明该支架有希望作用于小直径血管移植物中。此外,GAO等[35]以聚己内酯和聚乳酸-乙醇酸(poly lactic-co-glycolic acid,PLGA)为原材料,通过电纺技术制备出不同比率的PCL/PLGA复合血管支架。在皮下植入4周后,组织学结果可见PCL/PLGA(60/40)和PCL/PLGA(80/20)膜内细胞数量较多,PCL/PLGA (90/10)和PCL/PLGA(95/5)膜外表面细胞数量较少,这表明含量较高PLGA材料中,其细胞浸润也增强。实验证实该复合支架可作为血管移植物组织工程材料。 AUGUSTINE等[36]采用电纺技术制备一种新型电纺聚偏氟乙烯[Polyvinylidenefluoride-trifluoroethylene, P(VDF-TrFE)]/氧化锌(ZnO)纳米复合支架,结果发现与单纯P(VDF-TrFE)支架上培养的细胞相比,该复合材料上培养的间充质干细胞和人脐静脉内皮细胞更有较高的细胞活力、黏附性和增殖能力,其材料可促进血管生成(图5)。研究结果证实新型P(VDF-TrFE)/ZnO纳米复合材料在组织工程中的应用潜力,其具有生物相容性和促进细胞黏附和血管生成的能力。同样,JOY等[37]基于明胶和聚己内酯为原材料,并采用静电纺丝技术成功制备出明胶-聚己内酯复合血管支架材料,通过测量其孔径大小,发现该复合支架孔径为50-100 μm,这表明这一孔径有利于细胞浸润和增殖,因此该复合材料可用于血管组织工程支架材料。然而,研究者发现复合材料在临床研究中的应用极少见,复合材料构建的组织工程血管最大挑战是如何去修饰或改善其制备的技术手段,才来研发出更接近于天然血管性能,期待这一挑战能最终被广大的研究者攻破。 "

2.3.2 多组分复合材料 近年来,小口径组织工程血管支架材料的发展迅速。复合材料的研究不仅局限于2种材料共混,其还可通过3种以上的生物材料构建出多组分复合材料,该材料也是目前的研究趋势。ZHU等[38]采用室温常压共电纺制备出新型丝类人胶原/壳聚糖和聚乳酸制备血管组织工程支架。结果示胶原/壳聚糖/聚乳酸(7∶2∶1)和胶原/壳聚糖/聚乳酸(10.5∶1.8∶1)样品的血液相容性较差,约为0.3%,而胶原/壳聚糖/聚乳酸(0∶2.5∶1.2)和胶原/壳聚糖/聚乳酸(0∶2∶1.5)的血液相容性较高,支架纤维的直径接近于细胞外基质的尺寸,其仿生结构比聚乳酸更接近细胞外基质,血液相容性较好。研究表明该材料可运用于组织工程血管支架领域中。同样,WANG等[39]以Ⅰ型胶原与丝素蛋白和聚(癸二酸甘油酯)(poly glycerol-sebacate,PGS)不同比例混合,制备出一种适合于血管内支架的多功能电纺材料,实验结果发现,与水凝胶的胶原和电纺的胶原相比,该材料血小板黏附率分别降低220%-290%,该生物材料具有较强的机械性能、低降解性和降低血栓形成潜能。 此外,WANG等[40]以聚L-乳酸/聚乳酸-己内酰微孔内层与聚L-乳酸/聚己内酯的外层利用双相分离技术制备出双层管状纳米纤维支架材料,将该材料分别与内皮细胞和平滑肌细胞复合培养,结果表明该材料表面促进内皮细胞内皮化以及平滑肌细胞的浸润,该材料在小直径血管应用具有潜在应用前景。同样,WAN等[41]先采用电纺技术制备聚己内酯/角蛋白(keratin)生物材料,后将金纳米颗粒(Au)负载于该材料上,成功构建出PCL/keratin/AuNPs复合材料。为了检测该材料在内皮上增殖、黏附性,结果中可见在PCL/keratin和PCL/ keratin/AuNPs材料上细胞增殖、黏附性明显要强于单一聚己内酯材料,实验表明该复合材料在血管组织领域中具有潜在的应用前景。WAN等[42]运用共电纺制备出,后与肝素(heparin)和血管内皮生长因子(vascular endothelial growth factor,VEGF)结合,组合成PCL/ keratin/heparin/VEGF复合材料。通过测定细胞生存率性发现,相对于PCL/keratin材料对比PCL/keratin/ heparin/VEGF对脐静脉内皮细胞具有明显的促进增殖作用,而对脐动脉平滑肌细胞的生长有抑制作用,实验表明,该复合材料一种理想的组织工程血管支架材料。 2.4 3D打印技术在血管支架材料制备中的应用 在以往的研究中多采用是静电纺丝、冷冻干燥、溶剂浇铸法、相分离和颗粒沥滤等方式。然而,随着科技进步的发展,3D打印技术成为了新时代下研究者追寻的新方法。3D是一种新的技术,该技术是一种以数字模型为基础,运用塑料、粉末状金属等材料逐层打印而形成的生物材料[43]。其快速、高效成型技术和可调整构建体灵活性等优点成为近年来研究的热点,同时在卫生医疗、食品、航空建筑等领域应用广泛[44-46]。NQ等[47]利用3D打印对电纺聚己内酯纤维支架表面进行重新排列,实验中发现该支架与血管平滑肌细胞培养7 d后,其细胞数量显著增加,从而说明3D定向支架具有较高的细胞增殖能力,表明该技术可应用于组织工程血管领域中。同时,KAPPINGS等[48]研制出一种具有周围微流室的半圆形微流控血管支架(vasQchip),用于带血管蒂的三维细胞培养。实验表明vasQchip可作为一种应用于新型带血管蒂人工血管支架。此外,PINNOCK等[49]利用3D打印成类似自然动脉的管状,实验表明3D打印技术在血管组织工程是可行的。刘翀等[50]通过在3D打印构建出模拟的三维血管通路, 生成三维生物支架模型,如图6A所示为常用的3D打印支架模型,图6B,C为在图5A的基础上重新生成的包含血管网络的支架模型,为方便展示其血管结构,模型外框已隐藏。实验表明利用3D打印技术成功建立模拟生物血管网络的三维立体模型,并将其与现有的支架模型相融合,从而生成含血管通路的新生物支架。然而理想组织工程血管应该如何通过3D打印制造理想血管,这一棘手难题仍需研究者研究。 "

| [1] LEVIT RD. Engineering Vessels as Good as New?.Jacc Basic to Translational Science.2018;3(1):119-121. [2] WU J, HU C, TANG Z, et al. Tissue-engineered Vascular Grafts: Balance of the Four Major Requirements. Colloid and Interface Science Communications.2018;(23):34-44. [3] CARRABBA M, MADEDDU P. Current Strategies for the Manufacture of Small Size Tissue Engineering Vascular Grafts.Front Bioeng Biotechnol. 2018;6:41. [4] GOINS A, WEBB AR. Multi-layer approaches to scaffold-based small diameter vessel engineering: A review.Mater Sci Eng C Mater Biol Appl.2019;97:896-912. [5] KOENS MJ, KRASZNAI AG, HANSSEN AE, et al.Vascular replacement using a layered elastin-collagen vascular graft in a porcine model: one week patency versus one month occlusion. Organogenesis.2015;11(3):105-121. [6] KABIRIAN F, DITKOWSKI B, ZAMANIAN A, et al. Controlled NO-Release from 3D-Printed Small-Diameter Vascular Grafts Prevents Platelet Activation and Bacterial Infectivity.ACS Biomaterials Science & Engineering.2019;5(5):2284-2296. [7] KANG L, JIA W, LI M, et al.Hyaluronic acid oligosaccharide- modified collagen nanofibers as vascular tissue-engineered scaffold for promoting endothelial cell proliferation.Carbohydr Polym.2019;2(23):106-115. [8] ZHOU J, YING H, WANG M, et al. Dual layer collagen-GAG conduit that mimic vascular scaffold and promote blood vessel cells adhesion, proliferation and elongation.Mater Sci Eng C Mater Biol Appl. 2018;92:447-452. [9] WANG X, LIU Y, WANG C, et al. Preparation of small-diameter collagen-polylactic acid artificial blood vessel by electrospinning.AMCS.2017;(11) :2550-2555. [10] BADHE RV, BIJUKUMAR D, CHEJARA DR, et al. A composite chitosan-gelatin bi-layered, biomimetic macroporous scaffold for blood vessel tissue engineering. Carbohydr Polym. 2017;157:1215-1225. [11] REZ MFA, BINOBAID A, ALGHOSEN A, et al. Tubular Poly(ε-caprolactone)/Chitosan Nanofibrous Scaffold Prepared by Electrospinning for Vascular Tissue Engineering Applications.J Bioma Tissue Eng. 2017;7(6):427-436. [12] PANKAJAKSHAN D, PHILIPOSE LP, PALAKKAL M, et al. Development of a fibrin composite-coated poly (epsilon-caprolactone) scaffold for potential vascular tissue engineering applications.J Biomed Mater Res B Appl Biomater. 2010;87B(2):570-579. [13] GUNDY S, MANNING G, ENDA O’CONNELL E, et al. Human coronary artery smooth muscle cell response to a novel PLA textile/fibrin gel composite scaffold.Acta Biomater. 2008;4(6): 1734-1744. [14] WANG D, LIU H, FAN Y. Silk fibroin for vascular regeneration. Microsc Res Tech. 2017;80(3):280-290. [15] SUZUKI S, CHIRILA TV, EDWARDS GA. Characterization of Bombyx mori and Antheraea pernyi silk fibroins and their blends as potential biomaterials.Prog Biomater. 2016; 5(3-4): 193-198. [16] MARCOLIN C, DRAGHI L, TANZI M, et al. Electrospun silk fibroin–gelatin composite tubular matrices as scaffolds for small diameter blood vessel regeneration.J Mater Sci Mater Med. 2017;28(5):80. [17] XIANG P, WANG SS, HE M, et al. The in vitro and in vivo biocompatibility evaluation of electrospun recombinant spider silk protein/PCL/gelatin for small caliber vascular tissue engineering scaffolds. Colloids Surf B Biointerfaces. 2018; 163:19-28. [18] 赵亮,徐艳丽,何孟,等,骨髓间充质干细胞复合蛛丝蛋白血管支架构建小口径组织工程血管的研究[J].中国生物医学工程学报, 2015,34(1):70-76. [19] 何孟,赵亮,徐艳丽,等,酶法制备天然脱细胞血管支架[J].福建师大学报(自然科学版),2014,30(6):62-68. [20] PU L, WU J, PAN X, et al.Determining the optimal protocol for preparing an acellular scaffold of tissue engineered small-diameter blood vessels.J Biomed Mater Res B Appl Biomater.2018;106(2):619-631. [21] 赵亮,李霞飞,周坤,等, Triton-x100与丹参酚酸B制备脱细胞血管支架及其生物力学性能[J].中国组织工程研究, 2019,23(6):951-956. [22] 朱同贺,可降解聚氨酯弹性体的合成、改性及其用于血管组织再生[D]. 上海:东华大学, 2018. [23] NAFISEH J, DAVOD MK, ABDOLREZA S, et al. Small- diameter vascular graft using co-electrospun of composite PCL/PU nanofibers.Biomedical Materials.2018;13(5);055014 [24] 姜凯迪,王春仁,刘丽,等.基于聚乳酸及其共聚物的生物可吸收支架研究进展[J].中国医疗器械信息,2019,25(1):47-50. [25] ABUDULA T, SAEED U, MEMIC A, et al. Electrospun cellulose Nano fibril reinforced PLA/PBS composite scaffold for vascular tissue engineering.Journal of Polymer Research. 2019;26(5);110. [26] BUSCEMI S, PALUMBO VD, MAFFONGELLI A, et al. Electrospun PHEA-PLA/PCL Scaffold for Vascular Regeneration: A Preliminary inVivo Evaluation, Transplantation Proceedings 2017;49(4):716-721 . [27] CHEN Q, JIANG X, FENG L. Experimental studies on preparation of the porous and small-diameter poly(ε-caprolactone) external vascular scaffold and its degradability and biocompatibility.Regen Med Res. 2018;6:2. [28] 孙天舒,范传杰,常瑶,等.静电纺丝制备聚己内酯血管支架及其性能[J].工程塑料应用, 2019,47(6):14-19 [29] LI C, WANG F, DOUGLAS G, et al.Comprehensive mechanical characterization of PLA fabric combined with PCL to form a composite structure vascular graft.J Mech Behav Biomed Mater.2017;69:39-49. [30] COVELO A, GÓMEZ KK, CORONA-LIRA P, et al. Electrochemical characterization of PVA/SA nanofibers obtained by electrospinning processing. Surface & Interface Analysis.2018;50(6). [31] TANG J, BAO L, XUE L, et al.Potential of PVA-doped bacterial nano-cellulose tubular composites for artificial blood vessels.Journal of Materials Chemistry B.2015;3(43):1039. [32] WEI K, LIU F, YANG J, et al.Engineered-Macrophage Induced Endothelialization and Neutralization via Graphene Quantum Dot-Mediated MicroRNA Delivery to Construct Small-Diameter Tissue-Engineered Vascular Grafts.J Biomed Nanotechnol.2019;15(7):1492-1505. [33] JUNDZIŁŁ A, POKRYWCZYŃSKA M, ADAMOWICZ J, et al. Vascularization Potential of Electrospun Poly (L-Lactide-co-Caprolactone) Scaffold: The Impact for Tissue Engineering.Med Sci Monit.2017;23:1540-1551. [34] TAO L, WANG W, LIU D, et al. Electrospun Chitosan(CS)/ Poly(L-lactic-co-ε-caprolactone)(PLCL)Nanofibers and Their Potential as Small-Diameter Vascular Scaffold. Journal of Donghua University(English Edition. 2018;6(1):32-37. [35] GAO J, CHEN S, TANG D, et al. Mechanical Properties and Degradability of Electrospun PCL/PLGA Blended Scaffolds as Vascular Grafts.Transactions of Tianjin University. 2019;25(2); 152-160. [36] AUGUSTINE R, DAN P, SOSNIK A, et al. Electrospun poly(vinylidene fluoride-trifluoroethylene)/zinc oxide nanocomposite tissue engineering scaffolds with enhanced cell adhesion and blood vessel formation. Nano Research. 2017;10(10):3358-3376. [37] JOY J, PEREIRA J, AID-LAUNAIS RACHIDA, et al. Electrospun Microporous Gelatin-Polycaprolactone Blend based Tubular Scaffold as a Potential Vascular Biomaterial. Polymer International. 2019;7(68);1367-1377 [38] ZHU C, MA X, XIAN L, et al.Characterization of a co-electrospun scaffold of HLC/CS/PLA for vascular tissue engineering,Biomed Mater Eng. 2014;24(6):1999-2005. [39] WANG R, LEVI-POLYANCHENKO N, MORYKWAS M, et al. Novel nanofiber-based material for endovascular scaffolds,J Biomed Mater Res A. 2015;103(3):1150-1158. [40] WANG W, NIE W, ZHOU X, et al.Fabrication of heterogeneous porous bilayered nanofibrous vascular grafts by two-step phase separation technique.Acta Biomater.2018; 79:168-181. [41] WAN X, LIU P, JIN X, et al. Electrospun PCL/keratin/AuNPs mats with the catalytic generation of nitric oxide for potential of vascular tissue engineering.J Biomed Mater Res A. 2018; 106:3239-3247. [42] WAN X, LI P, JIN X, et al. Poly (ε-caprolactone)/ keratin/heparin/VEGF biocomposite mats for vascular tissue engineering.J Biomed Mater Res A. 2019 Oct 13. [43] RABIONET M, GUERRA AJ, PUIG T, et al. 3D-printed Tubular Scaffolds for Vascular Tissue Engineering. Procedia Cirp.2018;68:352-357. [44] SARKER MD, NAGHIEH S, SHARMA NK, et al.3D biofabrication of vascular networks for tissue regeneration:A report on recent advances.J Pharm Anal. 2018;8(5):277-296. [45] JIN G, HE R, SHA B, et al.Electrospun three-dimensional aligned nanofibrous scaffolds for tissue engineering.Materials Science and Engineering: C, 2018;92:995-1005. [46] GALBRAITH T, ROY V, BOURGET JM, et al. Cell Seeding on UV-C-Treated 3D Polymeric Templates Allows for Cost-Effective Production of Small-Caliber Tissue-Engineered Blood Vessels.Biotechnol J. 2019;14(1):e1800306. [47] NG FL, ONG YO, CHEN HZ, et al. A facile method for fabricating a three-dimensional aligned fibrous scaffold for vascular application.RSC Advances. 2019;9(23): 13054-13064. [48] KAPPINGS V, GRÜN C, IVANNIKOV D, et al.vasQchip: A Novel Microfluidic, Artificial Blood Vessel Scaffold for Vascularized 3D Tissues, Advanced Materials Technologies. 2018;3(4):246. [49] PINNOCK CB, MEIER EM, JOSHI NN, et al.Customizable engineered blood vessels using 3D printed inserts.Methods. 2016;99:20-27. [50] 刘翀,徐铭恩,王玲,等.基于3D打印细胞培养支架内部血管通道的模拟与构建[J].中国生物医学工程学报,2017,36(1):67-74. [51] LI ZK, WU ZS, LU T, et al.Materials and surface modification for tissue engineered vascular scaffolds.J Biomater Sci Polym Ed. 2016;27(15):1534-1552. [52] SHOJAEE M, BASHUR CA.Compositions Including Synthetic and Natural Blends for Integration and Structural Integrity: Engineered for Different Vascular Graft Applications.Adv Healthc Mater.2017;6(12). doi: 10.1002/adhm.201700001. |
| [1] | Yao Xiaoling, Peng Jiancheng, Xu Yuerong, Yang Zhidong, Zhang Shuncong. Variable-angle zero-notch anterior interbody fusion system in the treatment of cervical spondylotic myelopathy: 30-month follow-up [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1377-1382. |
| [2] | Zhang Jinglin, Leng Min, Zhu Boheng, Wang Hong. Mechanism and application of stem cell-derived exosomes in promoting diabetic wound healing [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1113-1118. |
| [3] | An Weizheng, He Xiao, Ren Shuai, Liu Jianyu. Potential of muscle-derived stem cells in peripheral nerve regeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1130-1136. |
| [4] | He Yunying, Li Lingjie, Zhang Shuqi, Li Yuzhou, Yang Sheng, Ji Ping. Method of constructing cell spheroids based on agarose and polyacrylic molds [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 553-559. |
| [5] | He Guanyu, Xu Baoshan, Du Lilong, Zhang Tongxing, Huo Zhenxin, Shen Li. Biomimetic orientated microchannel annulus fibrosus scaffold constructed by silk fibroin [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 560-566. |
| [6] | Chen Xiaoxu, Luo Yaxin, Bi Haoran, Yang Kun. Preparation and application of acellular scaffold in tissue engineering and regenerative medicine [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 591-596. |
| [7] | Kang Kunlong, Wang Xintao. Research hotspot of biological scaffold materials promoting osteogenic differentiation of bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 597-603. |
| [8] | Shen Jiahua, Fu Yong. Application of graphene-based nanomaterials in stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 604-609. |
| [9] | Zhang Tong, Cai Jinchi, Yuan Zhifa, Zhao Haiyan, Han Xingwen, Wang Wenji. Hyaluronic acid-based composite hydrogel in cartilage injury caused by osteoarthritis: application and mechanism [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 617-625. |
| [10] | Li Hui, Chen Lianglong. Application and characteristics of bone graft materials in the treatment of spinal tuberculosis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 626-630. |
| [11] | Gao Cangjian, Yang Zhen, Liu Shuyun, Li Hao, Fu Liwei, Zhao Tianyuan, Chen Wei, Liao Zhiyao, Li Pinxue, Sui Xiang, Guo Quanyi. Electrospinning for rotator cuff repair [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 637-642. |
| [12] | Guan Jian, Jia Yanfei, Zhang Baoxin , Zhao Guozhong. Application of 4D bioprinting in tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(3): 446-455. |
| [13] | Yun Xiao, Ding Tong, Yang Weiqiang, Guo Xinjun. Nano hydroxyapatite/chitosan scaffold loaded with Akebia saponin D in bone defect repair [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(27): 4293-4299. |
| [14] | Hu Qiuyu, Yang Long, Yang Yong, Song Shenchao. Aligned poly(butylene adipate-co-terephthalate)/type I collagen fibers promote tendon-bone healing after anterior cruciate ligament rupture [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(27): 4314-4319. |
| [15] | Shen Zhen, Guo Ying, Jiang Ziwei, Zhang Yan, Li Zige, Chen Zehua, Ye Xiangling, Chen Guoqian. Comparison of the effects between two routes of total flavones of Rhizoma Drynariae administration on large segmental bone defects in rats based on bone tissue engineering technique [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(27): 4346-4352. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||