Chinese Journal of Tissue Engineering Research ›› 2024, Vol. 28 ›› Issue (35): 5723-5731.doi: 10.12307/2024.597
Previous Articles Next Articles
Exercise intervention methods for senile sarcopenia
Lu Donglei1, Feng Zhanpeng2, Cao Liquan2, Tang Yi3, Tan Sijie2, Yu Zhongtao4
- 1School of Sports Training, 2School of Sports and Health, 3School of Physical Education, Tianjin University of Sport, Tianjin 301617, China; 4Tianjin Sports Comprehensive Support Center, Tianjin 300193, China
-
Received:2023-12-04Accepted:2024-01-08Online:2024-12-18Published:2024-03-15 -
Contact:Tan Sijie, Professor, School of Sports and Health, Tianjin University of Sport, Tianjin 301617, China -
About author:Lu Donglei, Master candidate, School of Sports Training, Tianjin University of Sport, Tianjin 301617, China -
Supported by:National Key Research and Development Program of the Ministry of Science and Technology, No. 2020YFC2006704 (to TSJ [project participant]); General Project of Social Science of Tianjin Sports Science Society, No. 22SK12 (to YZT)
CLC Number:
Cite this article
Lu Donglei, Feng Zhanpeng, Cao Liquan, Tang Yi, Tan Sijie, Yu Zhongtao. Exercise intervention methods for senile sarcopenia[J]. Chinese Journal of Tissue Engineering Research, 2024, 28(35): 5723-5731.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

2.1 肌少症的演进历程 自1989年,美国塔芙茨大学教授ROSENBERG[26]根据1988年在新墨西哥州阿布奎基召开的关于老龄人群健康和营养评估的会议精神,结合近10年相关研究的测量结果,正式定义了“骨骼肌减少症”(简称肌少症)。经过30余年的科研探索,肌少症的定义描述、内涵解读、诊断方法、诊断指标、诊断阈值以及诊断流程等逐步完善,形成了较为系统的评估体系[27-29]。国内对于肌少症的研究起步较晚。1997年,国内学者王福彭在《世界科学》期刊发表了一篇科普性译文;一直到2007年,学者李海鹏[30]、刘宇等[31]研究团队在《体育科学》杂志发表的2篇论文才揭开国内肌少症学术研究的序幕。 SGRò等[32]提出,运动、营养和药物是预防、延缓和治疗肌少症的“三架马车”。然而目前,仍未有针对肌少症有效的治疗药物,非药物干预成为治疗肌少症的主要干预策略,而运动干预更是以其独特的性价优势成为非药物干预的最佳方式[33]。现已公认,抗阻运动是治疗肌少症最有效的运动干预手段[14],但鉴于身体状况条件限制或担心不良反应及损伤发生以至于不能参与抗阻运动治疗的肌少症人群,可结合个人情况及特点推荐一些可替代的运动干预手段如有氧运动、全身振动训练、多组分运动等[34-41],见表1。"

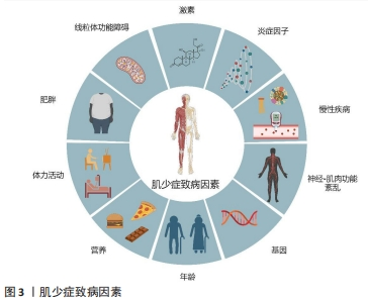
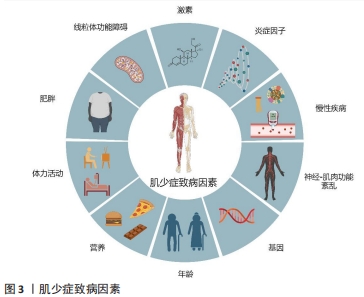
2.2 肌少症的致病因素 肌少症是由众多因素重叠混杂导致,目前影响肌少症的主要发病因素是身体活动量的减少、营养状况、慢性炎症、激素水平的变化。 2.2.1 身体活动量较低的老年人罹患肌少症的风险会明显增加[42] 随着年龄的增加,机体功能的不断衰退,老年人肌肉质量、肌肉力量等指标明显下降,其身体活动能力受限,长此以往将造成健康的恶化以及功能的受损。MEIER等[43]调查了304名老年人,探讨身体活动与肌少症的关系,发现身体活动水平与肌少症患病风险呈显著负相关(r=-0.61,P < 0.001),这是由于随着老年人身体活动量的减少,增龄相关的肌肉失用性萎缩加速肌肉退化,从而引起肌肉力量迅速下降[44]。张浩等[45]利用中国健康与养老追踪调查2015年数据,采用logistic回归分析可能发生肌少症的影响因素,结果表明除年龄(OR=2.72,P < 0.001)外,低身体活动(OR=1.65,P < 0.001)可能为肌少症发生的第二大危险因素。HAMER等[46]调查了英国6 228名老年人,探讨两种注视屏幕久坐类型与握力之间的关系,结果显示,在调整了年龄、体力活动、吸烟、饮酒、慢性疾病等混杂因素后,每天观看电视时长大于6 h的人与较低的握力相关(男性,B=-1.20 kg,95%CI:-2.26,-0.14;女性,B=-0.75 kg,95%CI:-1.48,-0.03),提示长时间久坐可能会导致老年肌肉力量的下降。王坤等[47]认为,较低的体力活动水平会导致肌肉力量降低及肌肉萎缩,从而使得基础代谢率和运动代谢率降低,进而加重久坐的习惯,使体质量恶性循环地增加。低体力活动水平会损伤肌细胞代谢功能,导致肌肉质量及力量下降,而高体力活动水平则可通过促进蛋白质合成、改善机体低水平慢性炎症状态以及增加抗氧化作用来保持中老年人肌肉力量[45]。 2.2.2 不良的营养状况是导致肌少症的重要危险因素[48] 老年人身体活动量的减少通常伴随着高脂肪的不均衡饮食[49],这使肌肉和肝脏中的脂肪沉积,高脂肪会影响骨骼肌和卫星细胞的组成和结构,从而影响运动后的肌肉修复和再生过程[50]。老年人生活习惯、饮食习惯的改变可能会导致蛋白质摄入不足,再加上肌肉纤维逐渐纤维化被脂肪组织代替,从而导致肌少症的发病率明显增加[51],同时,老年人体内泛素-蛋白酶系统平衡会随着年龄的增大被打破,泛素-蛋白酶系统是调节蛋白质平衡、保持蛋白质稳态的重要途径,随着年龄的增加,泛素-蛋白酶系统中的肌萎缩素和肌环指蛋白1表达水平显著增加,进而促进蛋白质的降解[52]。蛋白质的合成代谢与分解代谢平衡决定了肌肉量的多少,当老年人摄入蛋白质不足时会导致体内蛋白质的分解代谢速率超过合成代谢速率[53],从而使得肌肉质量下降。老年人由于室外活动较少、营养摄入及吸收降低和体内维生素D羟化酶活性降低等因素,往往存在维生素D缺乏的现象[16]。维生素D的摄入不足会导致线粒体活性氧产生过多从而加剧肌肉萎缩、氧化损伤和ATP降低,使老年人肌力下降增大患肌少症的风险[54-55]。研究表明,严重缺乏维生素D可导致肌肉萎缩现象,且补充维生素D可逆转这一现象[56]。此外,蛋白质的合成和调节钙转运这一过程也会受到维生素D的调节,包括细胞增殖分化[57]、肌肉收缩功能[58]、改善肌力及肌肉生理功能[59]。因此,蛋白质和维生素D也是影响肌肉合成代谢的关键因素。 2.2.3 慢性炎症几乎是所有已知疾病的潜在致病因素 随着年龄的增加,老年人机体衰老过程中通常伴随炎性标志物及其相关因子的增加,与骨骼肌代谢相关的促炎细胞因子如白细胞介素6、肿瘤坏死因子α及C-反应蛋白等水平的升高会导致肌细胞减少,导致肌少症患病风险增加[60]。生长激素(growth hormone,GH)/胰岛素样生长因子1(insulinike growthfactors 1,IGF-1)轴是骨骼肌生长和适应的关键介质,自分泌/旁分泌IGF-1已被证明可调节骨骼肌的代偿性适应以及肌肉的生长和发育,已经有研究表明,白细胞介素6过表达可以干扰GH/IGF-1轴从而导致骨骼肌萎缩[61]。BIAN等[62]探讨了老年肌少症与炎症因子白细胞介素6和肿瘤坏死因子α之间的关系,指出肌少症患者血清中白细胞介素6和肿瘤坏死因子α的水平显著高于健康人。同时,VISSER等[63]的研究表明,血清中肿瘤坏死因子α值的标准差每增加一个,握力则会降低1.2-1.3 kg。此外,老年人由于功能衰退、免疫力下降,机体更容易处于慢性炎症状态,尤其是血清中C-反应蛋白含量大量积聚时,则会导致肌肉蛋白质合成减少、分解代谢增加,从而使肌肉质量下降,增加罹患肌少症的风险[64]。 2.2.4 激素水平与肌少症的发生密切相关[65] 激素水平(生长激素、性激素、胰岛素等)对人体维持肌肉的合成与降解平衡非常重要[66]。BRIOCHE等[67]发现生长激素替代疗法可以增加骨骼肌蛋白质合成和线粒体生物的发生途径,促进骨骼肌蛋白质的合成,降低与年龄相关的氧化损伤,从而促进骨骼肌肌肉质量增加及肌肉肥大。一项荟萃分析表明,雌激素治疗可以改善绝经后女性的肌肉力量[68](相比对照组约增加5%);而雌激素作为一种抗氧化剂和肌纤维膜稳定剂,还可以维持骨骼肌收缩性及防治肌肉损伤[69]。与雌激素类似,雄激素(如睾酮)在骨骼肌生理学中起着至关重要的作用,主要是促进蛋白质的合成和抑制肌肉蛋白的水解,此外可以通过激活肌肉卫星细胞和增加IGF-1水平促进肌肉纤维的再生和修复[70]。胰岛素也与肌肉合成与功能相关,其通过增加氨基酸转运、蛋白质合成[磷脂酰肌醇-3-激酶(phosphatidylinositol 3-kinase,PI3K)、蛋白激酶B(protein kinase B,Akt/PKB)途径][71]、抑制蛋白质水解等,在蛋白质代谢中发挥着重要作用。 除上述因素外,肌少症还与肌肉线粒体功能障碍、慢性疾病、神经-肌肉功能紊乱、基因、肥胖等众多因素有关,见图3。"

2.3 抗阻运动与老年肌少症 2.3.1 抗阻运动对老年肌少症患者的影响 抗阻运动目前是干预老年肌少症最有效的运动形式。有研究认为抗阻运动可降低血清IGF-1水平,还发现在进行抗阻运动后血清中IGF-1浓度与骨骼肌质量呈负相关,提示抗阻运动可以促进IGF-1在体内循环系统和骨骼肌组织之间的重新分布,从而增加人体骨骼肌的合成代谢[72]。当前对于抗阻运动促进骨骼肌合成代谢机制的主要观点为:抗阻运动主要通过激活IGF-1下游蛋白mTORC1,进而磷酸化eEF2、S6K1、4EBP1等蛋白,最后启动蛋白质翻译与肽链延长过程,从而促进骨骼肌的合成代谢[73]。多项研究证明,抗阻运动可以对抗和改善肌无力和身体虚弱,减轻与年龄相关的肌内脂肪浸润[74],提高身体运动表现,增加肌纤维横断面面积及肌肉质量,提高胰岛素敏感性[75],降低老年人跌倒和骨折的风险[76]。此外,抗阻运动可以通过改善体内葡萄糖稳态、防止肌内脂质积聚、增加氧化和糖酵解酶能力、增强氨基酸摄取和蛋白质合成以及通过将合成代谢/分解代谢环境转向合成代谢来提高骨骼肌的合成代谢能力[77],从而改善肌肉质量。 抗阻运动的形式主要包括自重训练、抗阻训练器械、弹力带、抗阻训练结合营养干预等。CEBRIà IRANZO等[78]研究表明,为期12周、每周训练3次、单次干预时长40 min的中等强度抗阻训练提高了老年肌少症患者呼吸肌和骨骼肌的肌肉力量。此外,VIKBERG等[79]针对老年肌少症前期患者,采用为期12周、每周干预3次、每次训练45 min、中等运动强度的简易家庭抗阻训练进行干预,结果显示,抗阻训练干预组的瘦体质量平均增加了(1 147±282) g,身体总脂肪量减少了(553±225) g;身体功能表现方面,椅站测试时间减少了(0.9±0.6) s。LICHTENBERG等[80]对22例老年肌少症患者进行了为期36周、每周2次、每次60 min的高强度抗阻训练运动干预,结果显示,受试者骨骼肌质量指数、握习惯性步态速度均得到较好改善。FLOR-RUFINO等[81]探讨了为期24周、每周干预2次、每次干预65 min的高强度(70% 1RM,RM为最大力量,1 repetition maximum)抗阻训练对肌少症患者身体成分、身体功能表现及MRI生物标志物的影响,结果显示高强度抗阻训练运动干预降低了身体脂肪含量,并增强了上肢和下肢的肌肉力量,此外生物标志物影像学显示干预后肌肉水和作用水平保持不变,微观脂肪量减少。提示中高强度的抗阻训练可以有效提高肌肉质量并防止功能性力量的丧失。 弹力带抗阻训练也是一种干预老年肌少症的常用运动手段。LIAO等[82]发现,借助弹力带进行为期12周渐进式抗阻训练对患有肌肉减少性肥胖症的女性老年人的身体成分(无脂肪质量和肌肉质量指数增加;绝对总脂肪质量降低)和身体功能表现方面(步速、椅站测试、握力等)有显著改善。SEO等[83]基于自重和弹力带,采用渐进式抗阻训练对12例老年女性肌少症患者进行为期16周运动干预,结果表明,渐进式抗阻训练改善了受试者的功能适应性、步速及等长肌肉力量,此外肌肉生长因子如卵泡抑素水平在干预后得到增加。上述研究提示,弹力带抗阻训练可有效改善老年肌少症患者的功能表现。 抗阻训练联合营养干预对老年肌少症的影响也十分重要。CHANG等[84]、MALTAIS等[85]和LICHTENBERG等[80]证实了抗阻训练联合蛋白质营养补充对老年肌少症患者的影响,结果表明抗阻训练联合蛋白质营养干预有助于提高老年人骨骼肌肌肉质量及功能表现。CHANG等[84]还发现在设计肌少症患者康复计划时可以先进行有营养支持的抗阻训练以快速增大肌肉体积,随后进行系统、结构性的家庭锻炼来保持之前的康复效果。提示抗阻运动的同时补充足量的膳食蛋白质被视为建立和维持极少正老年人肌肉质量、力量以及功能的有效方案。 血流限制联合低强度抗阻运动作为一种新兴的运动干预方法,近来备受关注。该训练方法是在肢体近心端使用弹性绑带施加压力阻止静脉回流,通过限制血流量,刺激肌肉对于低强度运动的适应性反应,从而提高肌肉质量和力量[86]。LETIERI等[87]针对11例60岁以上女性老年肌少症患者进行为期16周的血流限制联合低强度抗阻运动干预,结果表明,实验组肌肉质量、握力、椅站测试、6 min步行测试、上肢柔韧性等指标均有显著改善,且并未出现不良反应,这提示血流限制联合低强度抗阻训练可以应用于老年肌少症患者,具有较高的安全性,可更有效地提高肌肉质量、肌肉力量及身体功能表现的训练效果。但目前关于血流限制联合低强度抗阻运动的相关文献较少,针对现有各项肌少症诊断标准确定的肌少症患者的血流限制联合低强度抗阻运动的治疗效果相关研究仅有一篇,未来应扩大血流限制联合低强度抗阻运动治疗老年肌少症的相关研究,以评估其适用性及安全性。 综上,不同形式的抗阻运动对于改善老年肌少症患者的肌肉质量、肌肉力量及身体功能等具有重要作用,且高等强度的抗阻运动效果最佳,但需要注意的是老年肌少症患者因体质状况下降,骨质较弱,易发生骨折,因此干预运动强度需循序渐进,避免干预起始阶段采用大负荷高强度训练而产生不必要的运动损伤,见表2。"


2.3.2 抗阻运动干预老年肌少症患者的方案建议 抗阻运动干预老年肌少症的效果受多方面因素的影响,主要包括:运动强度、运动频率和组间休息时间、运动形式。对此,此次研究基于已有证据提出了抗阻运动干预老年肌少症效果的影响因素及建议方案。 (1)运动强度:抗阻运动中,常用相对1RM的百分比或绝对值来表示训练负荷,1RM是指一个人在某个特定动作上在完整执行一次的情况下所能负荷的最大力量。多项研究证实中等到高等强度的抗阻运动可以改善老年肌少症患者的肌肉状况和功能表现[74,76];美国国家体能协会建议老年人进行抗阻运动锻炼时以70%-85% 1RM的运动强度肌肉状况改善效果较好[88]。然而有研究指出老年人体质因增龄性退化并不推荐干预初期采用大强度抗阻训练,推荐训练负荷由低到高渐进式逐步递增至中高训练负荷强度[80]。此外,不同老年肌少症患者之间身体情况差异较大,在设定训练强度时应做到因人而异,必要时可采用Berg疲劳感知表等量表严密监控训练负荷。 (2)运动频率和组间间隔:运动频率是指每周运动次数,此文纳入多数研究建议为每周至少2次,每次训练时间30 min以上,且均未发生不良事件;同时,世界卫生组织提出,老年人应每周进行2次以上的中高强度活动[89]。此外美国国家体能协会针对老年人抗阻训练计划中指出,每周宜进行2次左右的多关节训练,单次训练时间30-60 min[90]。上述提示,抗阻训练干预老年肌少症患者时采用每周两三次,单次干预时长为40-60 min较为合适。 组间间隔:组间间隔是指运动中的组间恢复时间,在一定程度上取决于干预方案中其他变量如运动强度、运动方式、运动量等变量的相互作用。在涉及老年人的抗阻运动中,组间休息时间通常为60-180 s,但在训练早期阶段,组间休息时间应取决于老年人对运动刺激的耐受性,并由专业人员制订他们的休息时间,而且该研究提示,组间休息需至少2 min才能最大限度地提高个体肌肉力量增益[16]。关于组间休息时间长短对抗阻训练肌肉的影响研究仍有待大样本的随机对照试验研究加以验证。 (3)运动形式:抗阻运动干预老年肌少症的运动方式分为自重和借助健身训练器械进行训练。常规的自重抗阻训练方式包括深蹲、仰卧起坐、俯卧撑、站姿提踵等;而借助健身训练器械的抗阻训练的常用设备包括各种康复力量训练器械如划船机、史密斯训练仪、腿举器、血流限制加压绑带等,此外最近新兴的带有负荷数值的弹力带也因其直观性、便捷性、低成本性逐步步入大众的视野。 综上,建议针对老年肌少症患者进行抗阻训练遵循干预频次为每周两三次,单次干预时长为40-60 min,组间间隔60-180 s,运动强度为中高强度,运动形式为自重训练、抗阻训练器械、弹力带、抗阻训练结合营养干预以及血流限制联合低强度抗阻运动的干预方案。 2.4 有氧运动与老年肌少症 2.4.1 有氧运动对老年肌少症患者的影响 有氧运动是指在氧供充足时全身大肌群参与的持续性、有一定节奏性、较低强度的运动[91]。长期规律的有氧运动可以防治多种代谢疾病,其机制是通过对骨骼肌细胞不同代谢通路进行调控,从而改善代谢紊乱,而代谢紊乱可加速骨骼肌的衰老、凋亡,因此有氧运动的增肌效果可能没有抗阻运动效果好,但可能是改善老年肌少症的有效方法[92]。研究表明,随着年龄的增加,老年人骨骼肌细胞会出现胰岛素抵抗病理状态[93],可能与衰老骨骼肌细胞蛋白质合成代谢功能下降有关。BACURAU等[94]研究表明,有氧运动可通过增强胰岛素信号通路(Akt/mTORC1)敏感性、增加小鼠骨骼肌细胞蛋白合成从而发挥康肌肉萎缩作用。由于线粒体在调控骨骼肌细胞能量代谢、信号通路及凋亡中发挥关键作用,因此线粒体功能失调与骨骼肌衰老密切相关[95],而有氧运动可以抑制细胞凋亡因子的表达,上调过氧化物酶体增殖物受体γ共激活因子1α的表达,从而提高细胞线粒体质量和健康线粒体的合成,增强代谢酶活性,从而改善骨骼肌功能并提高衰老骨骼肌的有氧能力[96]。针对干预老年肌少症,有氧运动方式主要包括健步走、有氧操、游泳等。 健步走是干预老年肌少症常见的运动形式。OSSOWSKI等[97]采用为期12周、每周干预3次、每次训练时间57-63 min、以最大心率50%-70%运动强度的北欧式健步走对23例63-79岁老年肌少症患者进行干预,结果显示,受试者的骨骼肌质量指数、膝关节等长肌肉力量、身体功能表现得到显著改善,体质量、体质量指数、体脂百分比显著下降。BRIGHTWELL等[98]对12例65岁以上健康老年人进行为期24周、每周干预3次、单次干预时长45 min、以70%强度储备心率的健走有氧运动方式进行干预,结果显示,运动干预后受试者身体成分并无显著变化,最大摄氧量提升了15.95%,肌纤维蛋白合成率从干预前每小时0.039 6%提升到每小时0.059 7%、毛细血管密度显著增加、骨骼肌质量和股四头肌肌肉力量也得到改善。 有氧操是由专业教练严格按照有氧代谢心率制定的一种全身性锻炼的运动方式,该运动方式简单易学、趣味性较好,对患肌少症人群要求不高,可随时跟练。CHEN[99]对15例65-75岁老年肌少症患者进行为期8周、每周干预2次、每次训练时间55-65 min、中等强度的有氧舞蹈干预,结果表明,与空白对照组相比,短期中等强度的有氧运动可以提高老年肌少症患者的肌肉质量、并会减少总脂肪量和挥发性脂肪酸,同时有氧训练可使得老年肌少症患者的血清IGF-1水平提高。MASON等[100] 指出,为期12个月的有氧运动干预可小幅提高女性老年肌少症患者的肌肉质量,并指出通过有氧运动干预使女性老年肌少症患者的体质量适当减少5%-10%,并且可以降低多种慢性病的患病风险,这是有氧运动干预相对于阻力运动干预的优势所在。 多种组合有氧运动是指多种不同方式有氧运动相互组合的运动方式。多种组合有氧运动可根据患者具体需求进行个性化制定,患者亦可选择感兴趣的一种或多种有氧运动方式同时进行训练,增加了其依从性。魏渼淇等[101]针对60-75岁肌少症患者进行为期20周、每周干预四五次、单次干预40-60 min的快走、慢跑、游泳、健身操、广场舞等多种形式相结合的有氧运动干预,结果表明,有氧运动和抗阻运动均有助于预防老年人与年龄相关的肌间脂肪积累,但无法实现肌间脂肪积累的逆转,且在预防肌少症发生发展中,抗阻运动的效果优于有氧运动。见表3。"

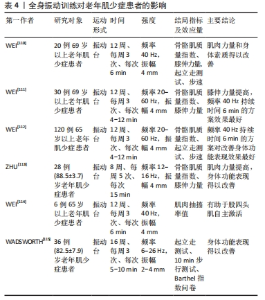
基于相关表型的研究提示,有氧运动可通过刺激线粒体生物合成来提高骨骼肌的质量、增加成骨相关基因表达以及通过Wnt/β-catenin和PI3K/Akt信号通路改善骨骼及肌肉的质量和力量,有效防治肌肉骨骼减少症的发生。Wnt/β-catenin和PI3K/Akt信号通路在调控骨骼肌生成和骨组织代谢中发挥重要作用。研究表明,长期低强度有氧运动可以增加AMP依赖的蛋白酶的活性,从而刺激健康线粒体的合成以改善骨骼肌细胞的代谢能力[102]。王兵等[103]对年老大鼠进行12周有氧运动干预,结果显示年老大鼠股骨中Wntl、Wnt3a、Lrp5、Axin2和Ctnnbl的mRNA水平明显增加,因此长期有氧运动可以增强老年大鼠骨组织中 Wnt/β-catenin 通路的活性,从而延缓老年大鼠的骨质流失。此外有研究报道,对去卵巢大鼠进行有氧运动干预可以通过调控PI3K/Akt信号通路来调整线粒体稳态以增加肌肉质量[104]。但目前仍缺乏针对老年肌少症人群或动物模型的研究[105]。因此,需做进一步相关研究探索有氧运动在老年肌少症患者中的作用效果及其生物学机制。 2.4.2 有氧运动干预老年肌少症患者的方案建议 运动强度、运动频率、运动形式主要制约有氧运动干预老年肌少症的效果。对此,此次研究基于已有证据提出了抗阻运动干预老年肌少症效果的影响因素及建议方案。 (1)运动强度:纳入多数研究表明,中等强度或高强度的有氧运动在老年肌少症患者的应用是安全有效的。但需要注意的是,高强度的有氧运动可以损伤年老小鼠骨骼肌细胞线粒体并增加活性氧簇炎症与炎症因子堆积,从而使小鼠衰老加快[106]。此外其中高强度有氧运动对老年肌少症患者的体质要求较高,更适用于肌少症诊断初期和康复期病情平稳的患者。此文纳入研究多数为以直接心率法确定运动强度,综合所纳入研究,建议运动强度为50%-70%最大心率。 (2)运动频率:此文纳入多数研究建议为每周至少2次,每次训练时间15 min以上,且均未发生不良事件;美国运动医学会针对老年肌少症患者运动频率为每周干预3-5次,单次干预时长75-150 min(根据运动强的大小调节)的中等强度或高强度的有氧运动[90];上述提示,有氧运动干预老年肌少症患者时采用每周2-5次、单次干预时长为15-65 min的运动频率较为合适。 (3)运动形式:有氧运动干预老年肌少症的运动方式分为自重和借助健身训练器械进行训练。常规的自重有氧训练方式包括健走、慢跑、跑步、游泳等。而借助健身训练器械的有氧训练的常用设备包括各种有氧训练器械如功率自行车、跑步机等。 综上,建议针对老年肌少症患者进行有氧训练遵循干预频次为2-5次每周,单次干预时长为15-65 min,运动强度为中等强度或高强度,运动形式为健走、慢跑、跑步、游泳、骑行等的干预方案。 2.5 全身振动训练与老年肌少症 2.5.1 全身振动训练对老年肌少症患者的影响 全身振动训练是通过特定振动台,利用其产生的冲击性振动刺激肌群,提高主动肌的激活程度并增加高阈值运动单位的活性,从而引起参与运动单位高频率放电,达到神经肌肉系统兴奋性提高的训练方法[105]。全身振动训练运动提高肌肉质量、力量及身体功能表现的根本生物学效应之一是训练过程中能够通过表面肌电监测到横纹肌活动的增加[107],通过直接刺激肌肉引起肌肉反射性的收缩及调节肌肉的神经兴奋性来改善肌肉状况[108]。此外有研究表明,全身振动训练还可以提高血清中的睾酮和生长激素水平,降低皮质醇水平,促进骨骼肌蛋白质合成代谢,改善肌肉萎缩情况[109]。 多项研究已证实全身振动训练运动在肌少症中的临床效果,见表4。WEI等[110-112]针对老年肌少症患者进行不同频率全身振动训练的多项研究证实,进行全身振动训练运动干预时,40 Hz的全身振动频率与每次360 s的持续时间相结合对于肌肉力量和运动表现的改善效果最好。ZHU等[113]的研究表明持续8周频率为12-16 Hz、振幅为4 mm的全身振动训练会改善老年肌少症患者的髂腰肌、股四头肌和胫骨前肌的肌力以及握力,且5次坐立时间和起立-行走测试时间明显缩短,但对肌肉质量并无明显改善。表明全身振动训练可以通过改善肌肉力量来防治老年肌少症。WEI等[114]针对65岁以上老年肌少症患者进行全身振动训练,对于股四头肌的自主激活效果研究发现,持续12周频率为40 Hz、振幅为4 mm、每次6 min的全身振动训练有助于老年肌少症患者的股四头肌的自主激活。WADSWORTH等[115]指出,便携、高效、低强度的全身振动训练可以提高体弱老年人的身体功能表现,但在停训一段时间后,干预效果会减少或消失。"
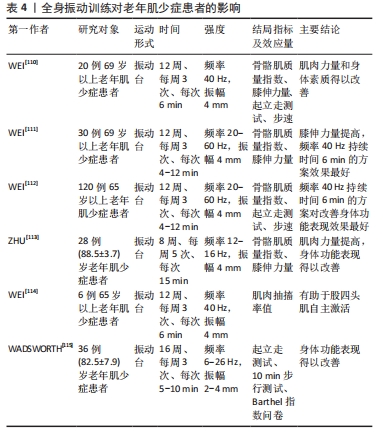

当前全身振动训练应用于老年肌少症的相关研究较少,并且部分研究人员对于全身振动训练防治老年肌少症持不同观点,这可能与振动台设置的强度和训练时长有关。因此,未来需有进一步研究验证全身振动训练在改善老年肌少症方面的效果。 2.5.2 全身振动训练运动干预老年肌少症患者的方案建议 振动台频率、振幅及运动频率主要制约全身振动训练干预老年肌少症的效果。对此,此次研究基于已有证据提出了全身振动训练干预老年肌少症效果的影响因素及建议方案。 (1)振动台频率、振幅:人体是一个弹性体,每个器官都有其固定的振动频率,因此在应用全身振动训练干预方案时应谨慎设计其频率及振幅。MESTER等[116]的研究表明,人体对振幅0.5 mm、频率20-25 Hz的全身振动具有不良反应。此外,研究表明如果振动加速较大,也易发生不良反应,甚至对脏器产生伤害[117]。结合此文纳入文献,建议振动台频率50 Hz左右、振幅为4 mm。 (2)运动频率:此文纳入全身振动训练干预老年肌少症研究的运动频率多为每周3次,单次干预时长4-15 min,且均未产生不良反应。此外,有研究报道过长的振动时间会对人体产生不良反应[118]。因此,建议运动频率每周训练3次、单次干预时长5-10 min。 综上,建议针对老年肌少症患者进行全身振动训练遵循运动频率每周训练3次、单次干预时长5-10 min、振动台频率50 Hz左右、振幅为4 mm的干预方案。 2.6 多组分运动与老年肌少症 2.6.1 多组分运动对老年肌少症患者的影响 多组分运动是指肌少症运动干预过程中不局限于某一种运动手段,而是将多种运动干预手段互相组合,如抗阻运动、有氧运动、柔韧性训练及功能性训练融合使用[119]。每种运动干预手段对肌肉质量和身体功能都有其独特的特征和预期效应,且会对其他系统器官产生相对应的预期效用。多组分运动结合了不同的运动方式,可以最大程度发挥单个运动手段各自的优势,并根据肌少症老年人不同的年龄、体质量、身体情况等提供更适合他们的个性化运动干预。持续、系统、规律的多组分运动能够降低患者的体脂肪含量、促进脂肪因子的变化以及改善老年人的身体成分、肌肉力量和功能表现。 KIM等[120]、PARK等[121]、ZHU等[122]指出,包含抗阻训练、有氧训练及平衡训练在内的多组分运动可以提高老年肌少症患者的肌肉质量、肌肉力量,并改善其身体成分及运动表现。MAKIZAKO等[123]研究表明,为期12周包含抗阻训练、有氧训练、平衡训练、柔韧性训练的多组分运动不仅提高了老年肌少症患者的握力,而且椅站测试时间减少、步速增快,但右侧大腿骨骼肌质量指数并无显著改善。BAGHERI等[124]证实了为期12周包含抗阻训练和有氧训练在内的多组分运动干预不仅提高了老年肌少症患者的体脂率和下肢肌肉力量,而且最大摄氧量水平也有所提升。以上说明,多组分运动可以改善老年肌少症患者的肌肉力量、身体功能表现以及心肺功能。MARUYA等[125]的研究表明,24周包含抗阻训练和有氧训练在内的多组分运动训练有效改善了老年肌少症患者的最大步行速度和肌肉力量,但对改善肌肉质量的效果微乎其微。MONTI等[126]指出,为期2年包含抗阻训练、平衡训练和有氧训练在内的多组分运动提高了老年肌少症患者的握力,提高了简易体能状况量表所测得分,改善了其身体成分。多组分运动干预可以刺激和促进机体众多生理系统(神经肌肉系统、心血管系统等)产生良性适应,进而改善老年肌少症。见表5。"

| [1] TOURNADRE A, VIAL G, CAPEL F, et al. Sarcopenia. Joint Bone Spine. 2019;86(3): 309-314. [2] KELLER K. Sarcopenia. Wien Med Wochenschr. 2019;169(7-8):157-172. [3] XU W, CHEN T, CAI Y, et al. Sarcopenia in Community-Dwelling Oldest Old is Associated with Disability and Poor Physical Function. J Nutr Health Aging. 2020; 24(3):339-345. [4] 吴琳瑾, 李静欣. 中国社区老年人肌少症患病率的Meta分析[J]. 现代预防医学,2019,46(22):4109-4112+4140. [5] 胡世莲, 王静, 程翠, 等. 中国居民慢性病的流行病学趋势分析[J]. 中国临床保健杂志,2020,23(3):289-294. [6] YEUNG SSY, REIJNIERSE EM, PHAM VK, et al. Sarcopenia and its association with falls and fractures in older adults: A systematic review and meta-analysis. J Cachexia Sarcopenia Muscle. 2019;10(3):485-500. [7] OHARA DG, PEGORARI MS, OLIVEIRA DOS SANTOS NL, et al. Cross-Sectional Study on the Association between Pulmonary Function and Sarcopenia in Brazilian Community-Dwelling Elderly from the Amazon Region. J Nutr Health Aging. 2020; 24(2):181-187. [8] IDA S, KANEKO R, NAGATA H, et al. Association between sarcopenia and sleep disorder in older patients with diabetes. Geriatr Gerontol Int. 2019;19(5):399-403. [9] PENG TC, CHEN WL, WU LW, et al. Sarcopenia and cognitive impairment: A systematic review and meta-analysis. Clin Nutr. 2020;39(9):2695-2701. [10] HARRIS R, CHANG Y, BEAVERS K, et al. Risk of Fracture in Women with Sarcopenia, Low Bone Mass, or Both. J Am Geriatr Soc. 2017;65(12):2673-2678. [11] YIN J, QIAN Z, CHEN Y, et al. MicroRNA regulatory networks in the pathogenesis of sarcopenia. J Cell Mol Med. 2020;24(9):4900-4912. [12] MORLEY EJ. Hormones and Sarcopenia. Curr Pharm Des. 2017;23(30):4484-4492. [13] 沈睿, 王茜茜, 徐霓影, 等. 老年肌少症患者运动干预的最佳证据总结[J]. 中华护理杂志,2021,56(10):1560-1566. [14] 闵文珺, 陈亚梅, 卢群, 等. 老年肌少症患者运动干预的最佳证据总结[J]. 解放军护理杂志,2022,39(3):75-78. [15] DENT E, MORLEY JE, CRUZ-JENTOFT AJ, et al. International Clinical Practice Guidelines for Sarcopenia (ICFSR): Screening, Diagnosis and Management. J Nutr Health Aging. 2018;22(1):1148-1161. [16] 孙建琴, 张坚, 常翠青, 等. 肌肉衰减综合征营养与运动干预中国专家共识(节录)[J]. 营养学报,2015,37(4):320-324. [17] DE MELLO RGB, DALLA CORTE RR, GIOSCIA J, et al. Effects of Physical Exercise Programs on Sarcopenia Management, Dynapenia, and Physical Performance in the Elderly: A Systematic Review of Randomized Clinical Trials. J Aging Res. 2019; 1959486-1959486. [18] HASSAN BH, HEWITT J, KEOGH JWL, et al. Impact of resistance training on sarcopenia in nursing care facilities: A pilot study. Geriatr Nurs. 2016;37(2):116-121. [19] RODRIGUES F, DOMINGOS C, MONTEIRO D, et al. A Review on Aging, Sarcopenia, Falls, and Resistance Training in Community-Dwelling Older Adults. Int J Environ Res Public Health. 2022;19(2):874. [20] YOO SZ, NO MH, HEO JW, et al. Role of exercise in age-related sarcopenia. J Exerc Rehabil. 2018;14(4):551-558. [21] LU LQ, HE XF, MA L, et al. Effects of vibration training vs. conventional resistance training among community-dwelling older people with sarcopenia: three-arm randomized controlled trial protocol. Front Aging Neurosci. 2022;14:905460. [22] 李静雅, 程亮. 不同频率全身振动训练对老年女性平衡能力、下肢肌力和位置觉的影响[J]. 体育学刊,2018,25(2):128-134. [23] 朱晓凤. 不同频率全身振动训练对老年人平衡和核心稳定性的影响[J]. 中国康复理论与实践,2020,26(3):291-294. [24] DISTEFANO G, GOODPASTER BH. Effects of Exercise and Aging on Skeletal Muscle. Life Sci Alliance. 2018;8(3):a029785. [25] 王丽丽, 田丽雅, 牛琪, 等. 11种运动对老年肌少症患者身体功能改善效果的网状Meta分析[J]. 中华护理杂志,2022,57(21):2652-2660. [26] ROSENBERG IH. Sarcopenia: origins and clinical relevance. J Nutr. 1997;127(5): 990S-991S. [27] DA SILVA MZC, VOGT BP, REIS NSDC, et al. Update of the European consensus on sarcopenia: what has changed in diagnosis and prevalence in peritoneal dialysis? Eur J Clin Nutr. 2019;73(8):1209-1211. [28] CRUZ-JENTOFT AJ, BAHAT G, BAUER J, et al. Sarcopenia: revised European consensus on definition and diagnosis. Age Ageing. 2019;48(1):16-31. [29] YAKABE M, HOSOI T, AKISHITA M, et al. Updated concept of sarcopenia based on muscle-bone relationship. J Bone Miner Metab. 2020;38:7-13. [30] 李海鹏, 卢健, 陈彩珍. Sarcopenia机制研究进展[J]. 体育科学,2007,27(11): 66-69,82. [31] 刘宇, 彭千华, 田石榴. 老年人肌力流失与肌肉疲劳的肌动图研究[J]. 体育科学,2007,27(5):57-64. [32] SGRO P, SANSONE M, SANSONE A, et al. Physical exercise, nutrition and hormones: three pillars to fight sarcopenia. Aging Male. 2018;22(2):75-88. [33] 李海鹏, 刘宇. 肌肉衰减症的动态识解及对我国运动科学研究的启示[J]. 体育科学,2020,40(9):61-73. [34] FIATARONE MA, O’NEILL EF, RYAN ND, et al. Exercise training and nutritional supplementation for physical frailty in very elderly people. N Engl J Med. 1994; 330(25):1769-1775. [35] BAUMGARTNER RN, KOEHLER KM, GALLAGHER D, et al. Epidemiology of sarcopenia among the elderly in New Mexico. Am J Epidemiol. 1998;147(8):755-763. [36] CRUZ-JENTOFT AJ, BAEYENS JP, BAUER JM, et al. Sarcopenia: European consensus on definition and diagnosis: Report of the European Working Group on Sarcopenia in Older People. Age Ageing. 2010;39(4):412-423. [37] CHEN LK, LIU LK, WOO J, et al. Sarcopenia in Asia: consensus report of the Asian Working Group for Sarcopenia. J Am Med Dir Assoc. 2014;15(2):95-101. [38] HASSAN BH, HEWITT J, KEOGH JW, et al. Impact of resistance training on sarcopenia in nursing care facilities: A pilot study. Geriatr Nurs. 2016;37(2):116-121. [39] BECKWéE D, DELAERE A, AELBRECHT S, et al. Exercise interventions for the prevention and treatment of sarcopenia. A systematic umbrella review. J Nutr Health Aging. 2019;23:494-502. [40] CHEN LK, WOO J, ASSANTACHAI P, et al. Asian Working Group for Sarcopenia: 2019 consensus update on sarcopenia diagnosis and treatment. J Am Med Dir Assoc. 2020;21(3):300-307. e2. [41] IZQUIERDO M, MERCHANT R, MORLEY J, et al. International exercise recommendations in older adults (ICFSR): expert consensus guidelines. J Nutr Health Aging. 2021;25(7):824-853. [42] WALL BT, DIRKS ML, SNIJDERS T, et al. Substantial skeletal muscle loss occurs during only 5days of disuse. Acta Physiol. 2014;210(3):600-611. [43] MEIER NF, LEE DC. Physical activity and sarcopenia in older adults. Aging Clin Exp Res. 2020;32(9):1675-1687. [44] 杨玲, 杜娟, 刘荣雁, 等. 肌肉减少症病因学研究现状与展望 [J]. 中国骨质疏松杂志,2020,26(11):1689-1693. [45] 张浩, 胡建伟, 赵晓慧, 等. 我国中老年人可能肌肉减少症患病情况及其影响因素 [J]. 医学与社会,2023,36(8):44-48. [46] HAMER M, STAMATAKIS E. Screen-based sedentary behavior, physical activity, and muscle strength in the English longitudinal study of ageing. PloS one. 2013;8(6): e66222. [47] 王坤, 罗炯, 刘立, 等. 老年人肌少症的成因、评估及应对[J]. 中国组织工程研究,2019,23(11):1767-1773. [48] 张文婧, 王佳贺. 老年肌少症与营养干预的研究进展[J]. 国际老年医学杂志, 2020,41(2):125-128. [49] RAHI B, MORAIS JA, DIONNE IJ, et al. The combined effects of diet quality and physical activity on maintenance of muscle strength among diabetic older adults from the NuAge cohort. Exp Gerontol. 2014;49:40-46. [50] ZAMBONI M, MAZZALI G, FANTIN F, et al. Sarcopenic obesity: A new category of obesity in the elderly. Nutr Metab Cardiovasc Dis. 2008;18(5):388-395. [51] 裴泽华, 蔡轶男, 王乐兵, 等. 肌少症现状及蛋白质对其预防作用的研究进展[J]. 食品工业科技,2022,43(24):469-477. [52] CLAVEL S, COLDEFY AS, KURKDJIAN E, et al. Atrophy-related ubiquitin ligases, atrogin-1 and MuRF1 are up-regulated in aged rat Tibialis Anterior muscle. Mech Ageing Dev. 2006;127(10):794-801. [53] RONG S, WANG L, PENG Z, et al. The mechanisms and treatments for sarcopenia: could exosomes be a perspective research strategy in the future?. J Cachexia Sarcopenia Muscle. 2020;11(2):348-365. [54] ABIRI B, VAFA M. Vitamin D and sarcopenia. Adv Obes Weight Manag Control. 2017;6(3):00155. [55] REMELLI F, VITALI A, ZURLO A, et al. Vitamin D deficiency and sarcopenia in older persons. Nutrients. 2019;11(12):2861. [56] SISHI B, LOOS B, ELLIS B, et al. Diet‐induced obesity alters signalling pathways and induces atrophy and apoptosis in skeletal muscle in a prediabetic rat model. Exp Physiol. 2011;96(2):179-193. [57] BUITRAGO CG, ARANGO NS, BOLAND RL. 1α, 25 (OH) 2D3‐dependent modulation of Akt in proliferating and differentiating C2C12 skeletal muscle cells. J Cell Biochem. 2012;113(4):1170-1181. [58] POLLY P, TAN TC. The role of vitamin D in skeletal and cardiac muscle function. Front Physiol. 2014;5:145. [59] WAGATSUMA A, SAKUMA K. Vitamin D signaling in myogenesis: potential for treatment of sarcopenia. Biomed Res Int. 2014;2014:121254. [60] 杨玲, 杜娟, 刘荣雁, 等. 肌肉减少症病因学研究现状与展望[J]. 中国骨质疏松杂志,2020,26(11):1689-1693. [61] LIESKOVSKA J, GUO D, DERMAN E. IL-6-overexpression brings about growth impairment potentially through a GH receptor defect. Growth Horm IGF Res, 2002;12(6):388-398. [62] BIAN AL, HU HY, RONG YD, et al. A study on relationship between elderly sarcopenia and inflammatory factors IL-6 and TNF-α. Eur J Med Res. 2017;22(1): 1-8. [63] VISSER M, PAHOR M, TAAFFE DR, et al. Relationship of interleukin-6 and tumor necrosis factor-α with muscle mass and muscle strength in elderly men and women: the Health ABC Study. J Gerontol A Biol Sci Med Sci. 2002;57(5): M326-M332. [64] BANO G, TREVISAN C, CARRARO S, et al. Inflammation and sarcopenia: a systematic review and meta-analysis. Maturitas. 2017;96:10-15. [65] PRIEGO T, MARTÍN A, GONZÁLEZ-HEDSTRÖM D, et al. Role of hormones in sarcopenia. Vitam Horm. 2021;115:535-570. [66] MORLEY JE. Hormones and sarcopenia. Curr Pharm Des. 2017;23(30):4484-4492. [67] BRIOCHE T, KIREEV R, CUESTA S, et al. Growth Hormone Replacement Therapy Prevents Sarcopenia by a Dual Mechanism: Improvement of Protein Balance and of Antioxidant Defenses. J Gerontol A Biol Sci Med Sci. 2014;69(10):1186-1198. [68] GREISING SM, BALTGALVIS KA, LOWE DA, et al. Hormone Therapy and Skeletal Muscle Strength: A Meta-Analysis. J Gerontol. 2009;64(10):1071-1081. [69] 王焕如, 于翰, 邵晋康. 肌肉减少症研究进展[J]. 中国骨质疏松杂志,2022, 28(2):304-307. [70] TIAN X, LOU S, SHI R. From mitochondria to sarcopenia: role of 17β-estradiol and testosterone. Front Endocrinol. 2023;14:1156583. [71] CLEASBY ME, JAMIESON PM, ATHERTON PJ. Insulin resistance and sarcopenia: mechanistic links between common co-morbidities. J Endocrinol. 2016;229(2): R67-R81. [72] BROOK MS, WILKINSON DJ, SMITH K, et al. The metabolic and temporal basis of muscle hypertrophy in response to resistance exercise. Eur J Sport Sci. 2016; 16(6):633-644. [73] ARNARSON A, GEIRSDOTTIR OG, RAMEL A, et al. Insulin-like growth factor-1 and resistance exercise in community dwelling old adults. J Nutr Health Aging. 2015; 19:856-860. [74] GOODPASTER BH, CHOMENTOWSKI P, WARD BK, et al. Effects of physical activity on strength and skeletal muscle fat infiltration in older adults: a randomized controlled trial. J Appl Physiol. 2008;105(5):1498. [75] BARRY VW, CHURCH T, BLAIR SN. Effects of exercise modality on insulin resistance and functional limitation in older adults: a randomized controlled trial. Curr Cardiovasc Risk Rep. 2009;3(4):235-236. [76] SILVA RB, ESLICK GD, DUQUE G. Exercise for Falls and Fracture Prevention in Long Term Care Facilities: A Systematic Review and Meta-Analysis. J Am Med Dir Assoc. 2013;14(9):685-689.e2. [77] LEBRASSEUR NK, WALSH K, ARANY Z. Metabolic benefits of resistance training and fast glycolytic skeletal muscle. Am J Physiol. 2011;300(1):E3-E10. [78] CEBRIÀ I IRANZO MÀ, I BERNAT MB, TORTOSA-CHULIÁ MÁ, et al. Effects of Resistance Training of Peripheral Muscles versus Respiratory Muscles in Institutionalized Older Adults with Sarcopenia: A Randomized Controlled Trial. J Aging Phys Act. 2018;26(4):637-646. [79] VIKBERG S, SÖRLÉN N, BRANDÉN L, et al. Effects of Resistance Training on Functional Strength and Muscle Mass in 70-Year-Old Individuals With Pre-sarcopenia: A Randomized Controlled Trial. J Am Med Dir Assoc. 2019;20(1):28-34. [80] LICHTENBERG T, STENGEL SV, SIEBER C, et al. The Favorable Effects of a High-Intensity Resistance Training on Sarcopenia in Older Community-Dwelling Men with Osteosarcopenia: The Randomized Controlled FrOST Study. Clin Interv Aging. 2019;14:2173-2186. [81] FLOR-RUFINO C, BARRACHINA-IGUAL J, PéREZ-ROS P, et al. Fat infiltration and muscle hydration improve after high-intensity resistance training in women with sarcopenia. A randomized clinical trial. Maturitas. 2023;168:29-36. [82] LIAO CD, TSAUO JY, LIN LF, et al. Effects of elastic resistance exercise on body composition and physical capacity in older women with sarcopenic obesity: A CONSORT-compliant prospective randomized controlled trial. Med. 2017;96(23): e7115. [83] SEO MW, JUNG SW, KIM SW, et al. Effects of 16 weeks of resistance training on muscle quality and muscle growth factors in older adult women with sarcopenia: A randomized controlled trial. MDPI. 2021;18(13):6762. [84] CHANG DS. Effectiveness of early versus delayed exercise and nutritional intervention on segmental body composition of sarcopenic elders-A randomized controlled trial. Clin Nutr. 2021;40(3):1052-1059. [85] MALTAIS ML, LADOUCEUR JP, DIONNE IJ. The Effect of Resistance Training and Different Sources of Postexercise Protein Supplementation on Muscle Mass and Physical Capacity in Sarcopenic Elderly Men. J Strength Cond Res. 2016;30(6): 1680. [86] SATO Y. The history and future of KAATSU training. Int J KAATSU Tra Res. 2005; 1(1):1-5. [87] LETIERI RV, FURTADO GE, BARROS PMN, et al. Effect of 16-week blood flow restriction exercise on functional fitness in sarcopenic women: A randomized controlled trial. Int J Morphol. 2019;37(1):59-64. [88] FRAGALA MS, CADORE EL, DORGO S, et al. Resistance Training for Older Adults: Position Statement From the National Strength and Conditioning Association.J Strength Cond Res. 2019;33(8):2019-2052. [89] WOO J. Combating frailty and sarcopenia in aging populations: Switching to a more positive paradigm. Aging Med. 2019;2(1):7-10. [90] WESTCOTT WL, WINETT RA, ANNESI JJ, et al. Prescribing Physical Activity: Applying the ACSM Protocols for Exercise Type, Intensity, and Duration Across 3 Training Frequencies. Phys Sports Med. 2009;37(2):51-58. [91] 朱园园, 陶月仙. 有氧运动结合抗阻运动对肥胖青少年健康体适能的影响研究进展[J]. 全科护理,2020,18(33):4571-4574. [92] 谢凌坚, 傅力. 运动与饮食干预改善原发性肌肉衰减症研究进展[J]. 中国运动医学杂志,2017,36(1):76-79. [93] PETERSEN MC, SHULMAN GI. Mechanisms of insulin action and insulin resistance. Physiol Rev. 2018;98(4):2133-2223. [94] BACURAU AV, JANNIG PR, DE MORAES WM, et al. Akt/mTOR pathway contributes to skeletal muscle anti-atrophic effect of aerobic exercise training in heart failure mice. Int J Cardiol. 2016;214:137-147. [95] LEE S, KIM M, LIM W, et al. Strenuous exercise induces mitochondrial damage in skeletal muscle of old mice. Biochem Biophys Res Commun. 2015;461(2):354-360. [96] 蒲锐, 陈子扬, 袁凌燕. 外泌体:运动防治肌少症的新靶点[J]. 生理科学进展, 2021,52(5):347-351. [97] OSSOWSKI ZM, SKROBOT W, ASCHENBRENNER P, et al. Effects of short-term Nordic walking training on sarcopenia-related parameters in women with low bone mass: a preliminary study. Clin Interv Aging. 2016;11:1763-1771. [98] BRIGHTWELL CR, MARKOFSKI MM, MORO T, et al. Moderate-intensity aerobic exercise improves skeletal muscle quality in older adults. Transl Sports Med. 2019;2(3):109-119. [99] CHEN HJ. Effects of Different Types of Exercise on Body Composition, Muscle Strength, and IGF-1 in the Elderly with Sarcopenic Obesity. J Am Geriatr Soc. 2017;65(4):827-832. [100] MASON C, XIAO L, IMAYAMA I, et al. Influence of diet, exercise, and serum vitamin d on sarcopenia in postmenopausal women. Med Sci Sports Exerc. 2013; 45(4):607-614. [101] 魏渼淇, 杨光, 魏茂泉, 等. 不同运动干预下老年肌少症患者的CT影像特征变化[J]. 陕西师范大学学报(自然科学版),2022,50(6):95-103. [102] ZIAALDINI MM, MARZETTI E, PICCA A, et al. Biochemical pathways of sarcopenia and their modulation by physical exercise: a narrative review. Front Med. 2017; 4:167. [103] 王兵, 段富贵. 长期有氧运动上调老年大鼠骨组织中Wnt/β-catenin通路[J]. 西南师范大学学报 (自然科学版),2017,42(4):132-136. [104] GAO L, LI Y, YANG YJ, et al. The Effect of Moderate-Intensity Treadmill Exercise on Bone Mass and the Transcription of Peripheral Blood Mononuclear Cells in Ovariectomized Rats. Front Physiol. 2021;12:729910. [105] 靳丹, 代新宇, 刘淼, 等. 肌肉骨骼减少症作用机制及其运动防治效果[J/OL]. 生物化学与生物物理进展,1-16[2024-01-09]https://doi.org/10.16476/j.pibb.2023.0327. [106] LEE S, KIM M, LIM W, et al. Strenuous exercise induces mitochondrial damage in skeletal muscle of old mice. Biochem Biophys Res Commun. 2015;461(2):354-360. [107] RITZMANN R, GOLLHOFER A, KRAMER A. The influence of vibration type, frequency, body position and additional load on the neuromuscular activity during whole body vibration. Eur J Appl Physiol. 2013;113(1):1-11. [108] 陈如洋, 杨占宇, 马小迪, 等. 全身振动治疗在康复领域的研究进展[J]. 中华脑科疾病与康复杂志(电子版),2020,10(6):374-377. [109] FRICKE O, SEMLER O, LAND C, et al. Hormonal and Metabolic Responses to Whole Body Vibration in Healthy Adults. Endocrinologist. 2009;19(1):24-30. [110] WEI N, NG SMS, NG G, et al. Whole body vibration training improves muscle and physical performance in community dwelling with sarcopenia: A randomized controlled trial. Int J Sports Phys Ther Rehabil. 2016;2:1-6. [111] WEI N, PANG MY, NG SS, et al. Optimal frequency/time combination of whole body vibration training for developing physical performance of people with sarcopenia: a randomized controlled trial. Clin Rehabil. 2017;31(10):1313-1321. [112] WEI N, PANG MY, NG SS, et al. Optimal frequency/time combination of whole-body vibration training for improving muscle size and strength of people with age-related muscle loss (sarcopenia): A randomized controlled trial. Geriatr Gerontol Int. 2017;17(10):1412-1420. [113] ZHU YQ, PENG N, ZHOU M, et al. Tai Chi and whole-body vibrating therapy in sarcopenic men in advanced old age: a clinical randomized controlled trial. Eur J Ageing. 2019;16(3):273-282. [114] WEI N, NG GYF. The effect of whole body vibration training on quadriceps voluntary activation level of people with age-related muscle loss (sarcopenia): a randomized pilot study. BMC Geriatr. 2018;18:1-6. [115] WADSWORTH D, LARK S. Effects of Whole-Body Vibration Training on the Physical Function of the Frail Elderly: An Open, Randomized Controlled Trial. Arch Phys Med Rehabil. 2020;101(7):1111-1119. [116] MESTER J, KLEINÖDER H, YUE Z. Vibration training: benefits and risks. J Biomech. 2006;39(6):1056-1065. [117] CARDINALE M, POPE M. The effects of whole body vibration on humans: dangerous or advantageous? Acta Physiol Hung. 2003;90(3):195-206. [118] SITJÀ-RABERT M, RIGAU D, FORT VANMEERGHAEGHE A, et al. Efficacy of whole body vibration exercise in older people: a systematic review. Disabil Rehabil. 2012;34(11):883-893. [119] MARZETTI E, DUQUE G. Multicomponent Strategies and Sarcopenia. J Nutr Health Aging. 2023;27(8):683-684. [120] KIM HK, SUZUKI T, SAITO K, et al. Effects of exercise and amino acid supplementation on body composition and physical function in community-dwelling elderly Japanese sarcopenic women: a randomized controlled trial. J Am Geriatr Soc. 2012;60(1):16-23. [121] PARK J, KWON Y, PARK H. Effects of 24-Week Aerobic and Resistance Training on Carotid Artery Intima-Media Thickness and Flow Velocity in Elderly Women with Sarcopenic Obesity. J Atheroscler Thromb. 2017;24(11):1117-1124. [122] ZHU LY, CHAN R, KWOK T, et al. Effects of exercise and nutrition supplementation in community-dwelling older Chinese people with sarcopenia: a randomized controlled trial. Age Ageing. 2019;48(2):220-228. [123] MAKIZAKO H, NAKAI Y, TOMIOKA K, et al. Effects of a Multicomponent Exercise Program in Physical Function and Muscle Mass in Sarcopenic/Pre-Sarcopenic Adults. J Clin Med. 2020;9(5):1386. [124] BAGHERI R, MOGHADAM BH, CHURCH DD, et al. The effects of concurrent training order on body composition and serum concentrations of follistatin, myostatin and GDF11 in sarcopenic elderly men. Exp Gerontol. 2020;133:110869. [125] MARUYA K, ASAKAWA Y, ISHIBASHI H, et al. Effect of a simple and adherent home exercise program on the physical function of community dwelling adults sixty years of age and older with pre-sarcopenia or sarcopenia. J Phys Ther Sci. 2016; 28(11):3183-3188. [126] MONTI E, TAGLIAFERRI S, ZAMPIERI S, et al. Effects of a 2-year exercise training on neuromuscular system health in older individuals with low muscle function. J Cachexia Sarcopenia Muscle. 2023;14(2):794-804. |
| [1] | Wang Ji, Zhang Min, Li Wenbo, Yang Zhongya, Zhang Long. Effect of aerobic exercise on glycolipid metabolism, skeletal muscle inflammation and autophagy in type 2 diabetic rats [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1200-1205. |
| [2] | Jiang Zihao, Wang Guanglan, Chen Peng, Sun Xianghong, Wang Ting, Jia Shaohui, Zheng Cheng. Effect of eccentric training combined with different frequency whole body vibration training on patellar tendinopathy [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 493-498. |
| [3] | Dong Hongming, Li Jianping, Liu Chao, Zhang Honghao, Li Guqiang. Relationship between muscle activation characterization and fall risk in older adults during walking up and down stairs [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(34): 5419-5424. |
| [4] | Xu Zheng, Zhao Xiaoqin, Chen Xiaodan, Wang Jiapu, Bao Fenmiao, Yu Liang, Li Junping, Wei Yan. Aerobic exercise upregulates the thioredoxin system and inhibits cardiomyocyte apoptosis in aging rats [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(34): 5508-5515. |
| [5] | Zhang Jinpu, Wang Junli, Zhang Siqi, Chen Jiahao, Yang Qiushi. Effectiveness of exercise interventions for fibromyalgia syndrome: a Meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(32): 5210-5216. |
| [6] | Xu Rui, Li Yanyan, Xu Hong. Effect and mechanism of short-chain fatty acids in aged rats with sarcopenia [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(32): 5172-5176. |
| [7] | Li Huijun, Li Chuikun, Wei Cuilan, Zhang Yeting. Notch1-mediated aerobic exercise promotes hippocampal nerve cell proliferation in Alzheimer’s disease mice [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(31): 4951-4957. |
| [8] | Chen Tianxin, Dong Tingting, Li Yan, Zhang Sheng, Zhang Lei. Causal relationship between blood metabolites and sarcopenia-related traits: a Mendelian randomization study [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(27): 4288-4292. |
| [9] | Guo Hui, Kong Jianda, Tian Chunlan. The role of mitochondrial autophagy-related receptor proteins and signaling pathways in the prevention and treatment of sarcopenia through exercise [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(27): 4397-4404. |
| [10] | Liu Xu, Chen Bo, Ning Ke, Chen Xiaohong. Mechanism and potential of vitamin C supplementation in sarcopenia prevention and treatment [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(27): 4405-4412. |
| [11] | Kong Jianda, Xie Yingao, Ma Wen, Liu Youhan, Wang Qinglu. Mitochondrial dysfunction in Parkinson’s disease and the potential ameliorative effects of exercise [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(27): 4413-4420. |
| [12] | Yang Liyuan, Zhang Yeting, Li Chuikun, Wei Cuilan. Effects of aerobic exercise on the expression of Notch1 and Caspase-3 in the hippocampus of Alzheimer’s disease mice [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(26): 4113-4120. |
| [13] | Peng Zhihua, Pan Junxi, Feng Qinghui, Tian Tianzhao, Zhang Sheng, Li An, Cai Yingfeng. The causal relationship between blood lipids and muscle atrophy based on Mendelian randomization analysis of two samples [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(23): 3699-3703. |
| [14] | Kong Jianda, Xie Yingao, Chen Shijuan, Zhu Lei. Blood flow restriction training interventions for sarcopenia in older adults: biological mechanisms and proposed application protocols [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(23): 3743-3750. |
| [15] | Wang Jingfeng, Wen Dengtai, Wang Shijie, Gao Yinghui. Atg-mediated autophagy, exercise and skeletal muscle aging [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(2): 295-301. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||