Chinese Journal of Tissue Engineering Research ›› 2024, Vol. 28 ›› Issue (35): 5695-5701.doi: 10.12307/2024.557
Previous Articles Next Articles
Regulatory role of transforming growth factor beta subfamily in osteoarthritis
Guo Lei, Qi Yansong, Niu Xiaobo
- Inner Mongolia Autonomous Region People’s Hospital, Hohhot 010017, Inner Mongolia Autonomous Region, China
-
Received:2023-10-07Accepted:2023-11-22Online:2024-12-18Published:2024-03-15 -
Contact:Qi Yansong, Associate chief physician, Associate researcher, Inner Mongolia Autonomous Region People’s Hospital, Hohhot 010017, Inner Mongolia Autonomous Region, China Niu Xiaobo, Associate chief physician, Inner Mongolia Autonomous Region People’s Hospital, Hohhot 010017, Inner Mongolia Autonomous Region, China -
About author:Guo Lei, Master candidate, Inner Mongolia Autonomous Region People’s Hospital, Hohhot 010017, Inner Mongolia Autonomous Region, China -
Supported by:Natural Science Foundation of Inner Mongolia Autonomous Region, No. 2021MS08036 (to NXB)
CLC Number:
Cite this article
Guo Lei, Qi Yansong, Niu Xiaobo. Regulatory role of transforming growth factor beta subfamily in osteoarthritis[J]. Chinese Journal of Tissue Engineering Research, 2024, 28(35): 5695-5701.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
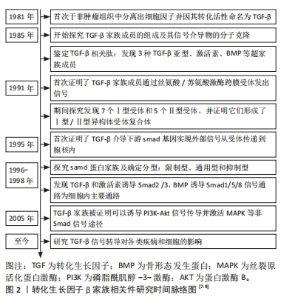
2.1 转化生长因子β亚家族及其信号通路概述 转化生长因子β超家族是由一组结构相关的细胞因子组成,共有40多个成员,包括转化生长因子β、骨形态发生蛋白、生长分化因子、激活素、抑制素和其他亚家族成员等。在1981年,ROBERTS等[7]首次从正常组织中分离纯化出转化生长因子β。在此之前,转化生长因子β一直被认为是肿瘤组织所产生的因子,像许多生长因子一样刺激细胞增殖,但随后学者们很快就发现转化生长因子β的功能不仅于此。在单层细胞培养中,转化生长因子β可以抑制依赖于表皮生长因子的细胞的增殖,而在软琼脂培养中,面对相同细胞的条件下,转化生长因子β又表现出与表皮生长因子协同促细胞生长效应[8],这也向研究者们提示了转化生长因子β可能是一种双功能调节因子。随着研究的不断深入,转化生长因子β所具有的双重调节功能和背景依赖性性质在多种细胞系统和生物反应中得到了进一步证实,并展现出涉及到多种细胞的增殖和分化、伤口愈合和免疫系统等方面的多重生理学效应[9]。目前,人们普遍认为转化生长因子β参与调节生物体内正常发育和生理学中的多种关键事件,而转化生长因子β信号传导的异常与结缔组织疾病、骨骼疾病、纤维化和癌症等疾病的发病机制密切相关,见图2。"
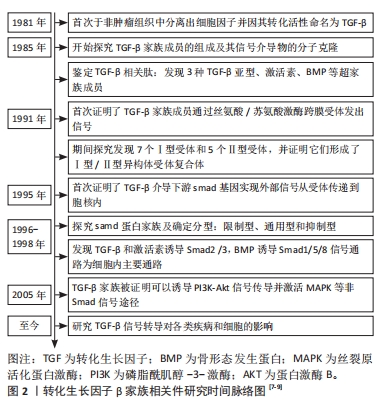
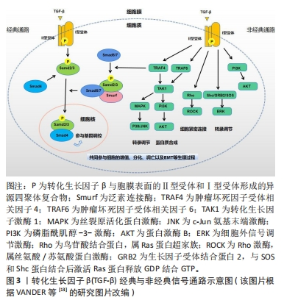
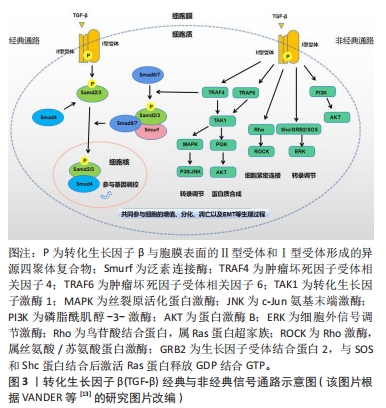
目前在转化生长因子β超家族分子的相关研究中,关于转化生长因子β亚型的研究最为广泛,因此在文章中,研究者们重点关注转化生长因子β亚家族在骨关节炎中所起到的调控作用。目前在人类体内发现的转化生长因子β主要包括转化生长因子β1、转化生长因子β2和转化生长因子β3共3种核苷酸序列高度同源的亚型,尽管三者在人体所有细胞中都有表达,但在不同组织内其表达存在差异性[10]。在健康的关节软骨基质中包含大量转化生长因子β及其亚型(高达300 ng/g),其主要亚型为转化生长因子β1(占比为60%-85%),多以非活性的潜伏复合物沉积在基质中[11]。 2.1.1 经典通路 转化生长因子β信号网络在体内通过经典以及非经典两种途径参与生物体内正常发育和平衡调节。在经典途径中转化生长因子β激活后与胞膜表面的Ⅱ型受体相结合形成二聚体,后者磷酸化Ⅰ型受体的GS序列(甘氨酸-丝氨酸富集区域)并活化Ⅰ型受体的丝氨酸/苏氨酸活性从而形成异源四聚体复合物。其中Ⅰ型受体又被称为激活素受体样激酶(activin receptor-like kinases,ALKs),ALK5作为经典途径的主要胞内效应器进而招募并活化下游受体调节的通路限制性Smads蛋白2/3,通过Smads2/3 C端的磷酸丝氨酸与公用型Smad4的MH2结构域识别并聚合移位到细胞核中,与抑制性Smads蛋白6/7共同完成调控靶基因转录与表达的过程[12],这就是经典的转化生长因子β/ALK5/Smads2/3信号通路。 2.1.2 非经典通路 在 Smads蛋白介导的典型转化生长因子β信号机制的背景下,活化的Ⅰ型受体与Smad7相互作用募集特异性泛素E3连接酶启动降解程序,降解的靶向蛋白通过泛素化修饰可刺激多种激酶激活非经典转化生长因子β信号通路[13],如磷脂酰肌醇-3-激酶、丝裂原活化蛋白激酶、细胞外信号调节激酶以及c-Jun氨基末端激酶等,见图3。这些激酶能够磷酸化Smads 2/3 N端MH1和C端MH2结构域之间的区域进行信号转导[14],并且它们既可以作为独立通路也可以与Smads蛋白一起介导信号反应调节下游细胞反应。"

2.2 转化生长因子β对关节软骨及细胞外基质的影响 关节软骨是一种覆盖在关节表面的固态结缔组织,具有黏弹性、各向异性、拉伸-压缩和非线性等特性[15],这不仅使关节软骨可承受极高的机械应力,并赋予了关节软骨分配所施加载荷的能力。这些特性依赖于关节软骨独特的生理构造,正常的关节软骨中没有神经、血管以及淋巴系统,主要由富含Ⅱ型胶原、透明质酸和蛋白多糖的细胞外基质与少量软骨细胞有序排列构成[16],这也使关节软骨的自我修复能力极低,即使是轻微的病变也可能导致进行性的损伤,最终导致骨关节炎的发生。 2.2.1 维持稳态 研究发现,通过特异性敲除小鼠模型中ALK5基因,在发育早期的小鼠关节中出现进展性的类骨关节炎表型[17]。软骨细胞中基质金属蛋白酶13和含Ⅰ型血小板结合蛋白基序的解聚蛋白样金属蛋白酶5等分解代谢因子过量产生,而负责合成的代谢因子表达减少。合成与分解代谢的失衡导致细胞外基质分解增加以及肥大软骨细胞表型增加,软骨细胞凋亡增强,并在随后观察到广泛关节软骨丢失的情况出现,这一现象表明转化生长因子β信号通路在早期软骨形成方面发挥重要作用。DU等[18]也在报道中指出,转化生长因子β3在健康的关节内通过Smad2/3信号通路诱导软骨细胞增殖并促进Ⅱ型胶原蛋白聚集和蛋白聚糖沉积,且此过程可抵消骨关节炎中的病理性软骨细胞肥大,保持软骨完整性从而维持关节稳态。以上证据均表明转化生长因子β在正常的关节软骨发育中具有积极作用。 2.2.2 促软骨修复 转化生长因子β亚家族在促软骨修复方面也拥有巨大的潜力。研究表明转化生长因子β1可引导骨髓间充质干细胞发生迁移,诱导Sox-9基因表达上调并刺激软骨细胞的分化,使蛋白多糖和Ⅱ型胶原分泌增多,增加细胞外基质的产生,在吸收部位形成新的软骨,从而显示出优秀的促软骨分化能力[19]。同时,转化生长因子β1还可通过抑制软骨细胞的肥大和终末分化,阻碍软骨基质的钙化和血管化,从而维持细胞外基质的完整性,起到软骨修复的作用[20]。在一项大型动物研究中,MRUGALA等[21]将绵羊骨髓间充质干细胞与转化生长因子β3结合壳聚糖生物支架植入绵羊髌骨软骨缺损区,在术后9周通过组织学检查发现,缺损处都填充了光滑的白色修复组织,且新生的软骨细胞样细胞完全嵌入透明软骨基质中并与自体软骨组织完全整合,而与之对应的对照组(单独应用骨髓间充质干细胞修复)在相同的区域内,纤维组织与修复组织交错重叠,修复组织中不仅新生软骨细胞密度更低,且细胞整合度明显劣于治疗组;并且在治疗组中,还观察到新生组织染色一直延伸到软骨下骨中,这表明转化生长因子β3不仅具备促进外源性骨髓间充质干细胞分化的能力,同时也能从骨髓中招募内源性细胞进行组织修复。也有报道称转化生长因子β2和转化生长因子β3诱导干细胞促软骨分化的能力可能优于转化生长因子β1[22]。尽管利用转化生长因子β诱导关节软骨再生技术仍停留在试验阶段,但是基于干细胞外泌体结合转化生长因子β进行关节腔靶向递送的治疗策略有望在为骨关节炎软骨修复上开辟一条新的可行的途径。 2.2.3 受miRNA调控 大量研究证实了miRNA通过调节相关基因表达来控制组织发育和体内生理平衡,而miRNA的失调涉及许多疾病的发病机制,包括骨关节炎。最近,一项基于微阵列的研究发现,与晚期骨关节炎患者相比,早期骨关节炎患者血清中的miR-26b-5p表达降低[23]。研究发现,miR-26b-5p通过负反馈靶向调节Asporin蛋白介导软骨的退变和衰老。作为其下游因子,Asporin是一种隶属于富含亮氨酸的小蛋白聚糖家族的细胞外基质蛋白,其表达水平随着关节软骨退变的进展而增加。LIU等[24]在内侧半月板失稳小鼠模型中发现,Asporin通过控制转化生长因子β1/Smad2轴,抑制小鼠关节中Smad2磷酸化,从而诱导软骨细胞衰老标志物p16INK4a和p21表达升高,加速软骨细胞衰老的同时加剧骨关节炎的进展;将Asporin基因沉默处理后,小鼠骨关节炎模型中软骨退变明显减弱;而此保护作用则被添加转化生长因子β1的特异性抑制剂后丧失,以上证据充分表明转化生长因子β1信号参与了骨关节炎中软骨细胞衰老的调节进程从而延缓骨关节炎的进展。 2.2.4 促分解代谢 尽管转化生长因子β在骨关节炎进展中表现出积极作用,但在骨关节炎进展中同样存在与之相反的促骨关节炎作用。PARK等[25]将正常人与骨关节炎患者的关节软骨进行对照研究后发现,在骨关节炎患者软骨中转化生长因子β1表达明显增强,上调的转化生长因子β1通过转谷氨酰胺酶2激活ERK和p38非经典通路刺激软骨细胞中基质金属蛋白酶13和Ⅹ型胶原蛋白的表达增加,加剧了骨关节炎中软骨细胞外基质分解代谢和软骨退化。而前者被公认为是导致骨关节炎关节软骨基质降解最重要水解酶之一。 与早期软骨发育阶段所起到的维持和形成作用不同,在成熟关节内,转化生长因子β1活性的增加很有可能是软骨退变的早期信号。CHEN等[26]为了探究转化生长因子β1信号对成年小鼠关节软骨退变的影响,选择性将8周龄小鼠关节软骨中Ⅱ型受体基因敲除,然后对小鼠进行了半月板失稳诱导手术,于生长12个月时对小鼠实施安乐死并采集关节标本,结果发现,实验组小鼠的关节软骨中没有观察到明显的结构特征变化,通过免疫组化也未检测到关节软骨中软骨退变相关标志物的表达。这一现象表明在成熟关节中转化生长因子β1的维持作用几乎可以忽略不计。为了验证这一结果,他们还将自然发育成熟的野生小鼠在接受手术后立即用受体抑制剂进行治疗,实验结果表明小鼠的关节同样未发生明显退变。以上的实验均证明了抑制成熟关节软骨中转化生长因子β1信号转导实际上可延缓小鼠模型所诱导的软骨退变。 2.2.5 参与炎症反应 另一方面,骨关节炎作为典型的退行性疾病之一,炎性因素对骨关节炎的发生发展起到不可忽视的作用,炎性因子的失衡引起软骨细胞合成和分解代谢的紊乱从而诱导软骨发生退化。研究发现,转化生长因子β1可诱导健康的关节软骨及滑膜表达白细胞介素18和白细胞介素6以及肿瘤坏死因子α等炎性因子[27],这些炎症因子尽管不是引起软骨退变的成因,但是其联级放大效应却加剧了软骨的破坏。 实际上,转化生长因子β信号通路在骨关节炎进展中所显示出的双重作用已经得到专家的共识,但如何控制它在不同阶段所发挥的多效性以及如何界定干预时机,依旧是导致其尚未转化为临床治疗手段的壁垒。但不可否认的是,相较于其他信号通路,转化生长因子相关的基因治疗药物是最接近临床的骨关节炎基因治疗药物。近来国外一种名为TissueGene-C的基因药物疗法在骨关节炎大鼠模型中的作用显著[28],其原理利用软骨细胞病毒转导转化生长因子β注入患膝,在注射后14周内明显缓解骨关节炎模型的疼痛并实现软骨结构的改善。尽管该药物处于试验阶段,其安全性和有效性仍需未来临床试验进一步评估,但该药物的成功研发也让研究者们看到利用转化生长因子β靶向治疗的可行性。因此阐明转化生长因子β通路和相关基因发挥其作用的分子机制至关重要。转化生长因子β信号通路调控关节软骨的研究详见表1。"


2.3 对软骨下骨重塑的调控 骨关节炎的主要病理表现不但累及关节表面被覆关节软骨的破坏和细胞外基质蛋白的逐渐丢失,另一个典型表现为软骨下骨的重塑失衡,包括骨硬化和囊性变,髓腔减小以及类骨质的形成等[29]。根据Wolff定律,当人体的关节在面对不同的机械应力时,软骨下骨通过不断调整自身的微观结构适应其机械载荷,从而与关节软骨联级实现应力传导。当软骨下骨构架的功能完整性被破坏,不仅会降低软骨下骨对关节软骨传递载荷的承载能力,还会显著改变被覆关节软骨应力峰值的分布。一项基于人类胫骨数据的计算机模拟模型中指出,即使软骨下骨仅扩张1%-2%也会显著增加关节软骨所需承载的应力,甚至在软骨下骨硬化区内,软骨应力可较正常区域提高约50%[30]。而长期异常应力的集中,又会促使软骨下骨微结构非均匀重塑致晚期力线失衡,导致继发性的软骨损伤和退行性改变。这被认为是软骨退变的主要来源之一,同时也能解释在在骨关节炎终末期力线偏移的状态下因过度负荷所引发关节功能的急剧恶化。 据最近的一项报道指出,在晚期骨关节炎患者机械应力集中的区域内发现软骨下骨中转化生长因子β1信号表达显著增高,该区域下可以明显观察到软骨下骨异常增厚、骨硬化等典型骨关节炎特征,且该区域被覆关节软骨的退变明显高于其他区域[31]。ZHEN等[32]也在小鼠前交叉韧带切除模型中早期检测到转化生长因子β1活性增加,并在随后观察到软骨下骨微结构发生变化,这充分表明了转化生长因子β1信号是骨关节炎病变的靶标之一。 2.3.1 参与骨细胞转导 骨细胞占骨骼细胞总数的90%-95%,软骨下骨的动态重塑过程有赖于骨细胞对成骨与破骨细胞的精准协调,并且作为响应机械载荷的微裂隙的基础感觉单元,骨细胞依赖于转化生长因子β1信号将机械物理信号转导为细胞分子的生化信号,招募破骨与成骨细胞来启动修复过程,通过骨腔隙-小管网络重塑,替换其周围的骨基质以维持矿物质稳态、骨小梁形态以及调节骨密度,最终实现响应机械负荷以调节软骨下骨重塑和软骨稳态,这一点已在ZHEN等[33]的研究中得到证实。为明确转化生长因子β信号传导对骨细胞维持关节稳态所产生的影响,BAILEY等[34]通过培育骨细胞Ⅱ型受体基因特异性缺失小鼠及同窝对照小鼠,于8周经内侧半月板切除+副韧带离断处理后16周采集后肢关节标本,实验发现,对照组小鼠在损伤的作用下承重区域内软骨下骨厚度较实验组明显增加,而实验组小鼠对损伤引起的软骨下骨厚度与体积变化不明显,骨关节炎进展减弱,这进一步佐证了软骨下骨对损伤的机械反应需要骨细胞转化生长因子β1信号的转导。值得一提的是,在相同条件下,雌性实验组小鼠在软骨下骨结构变化上与对照组没有显示出显著差异,且两组雌性小鼠在软骨下骨骨量上相对保持完整,这表明骨细胞转化生长因子β信号在骨关节炎进展中还具备性别特异性作用。 2.3.2 软骨下骨微结构 MURATOVIC等[35]通过采集35例接受全膝关节置换的晚期骨关节炎患者的软骨下骨样本发现[注:在术中将胫骨平台划分为存在且相对完整的软骨(CA+)区域和具有严重退化/耗尽软骨(CA-)的相邻区域],在(CA-)区域下软骨下骨内活性转化生长因子β1浓度显著高于(CA+)区域骨组织,且(CA-)区域下骨密度及微观结构参数明显不同,软骨下骨吸收凹陷增加,在空间上与活性转化生长因子β1水平增加的区域相关。且转化生长因子β1高活性区域内软骨下骨的小梁骨较正常数量升高约50%,骨量增加了38%,软骨下骨硬化程度更高且分布不均,其形态也发生改变,板/杆状骨小梁比例升高,而板状骨小梁增多是软骨下骨硬化的早期标志之一。 生理情况下小梁骨以多孔网架结构按主压应力曲线规律性排列,以适应机械载荷增加骨强度,同时有助于在关节加载和运动过程中将剪切应力转化为压缩和拉伸应力[36]。但伴随板状骨小梁数量的增加,使得局部骨骼硬度增加但连接性降低,且正常的各向异性丢失,迫使关节软骨和远端皮质骨必须接受和分散更多负荷,衰减和储存能量的能力被耗尽,从而加重关节超负荷。这些变化在骨关节炎的恶性循环中扮演着核心角色,既往的研究也表明板状骨小梁数量与骨关节炎严重程度呈显著正相关[37]。 LI等[38]的体外实验也证实了转化生长因子β1过表达不仅提高了碱性磷酸酶的活性,还促进骨钙素及RUNX-2等成骨细胞相关标志物的表达,这与既往的研究结论软骨下骨的异常重塑是骨关节炎疾病进展的典型特征相一致,并进一步表明活性转化生长因子β1可能是这些变化的起因或在此过程中发挥驱动作用。 2.3.3 骨基质成分 此外,骨的力学性能不仅由微观结构决定,另一方面则受到胶原纤维与羟基磷灰石所组成材料的影响。在软骨下骨硬化区内,通过SR-μCT观察到小梁骨基质中矿物质分布的高度异质性和胶原蛋白基质分布杂乱无章;且硬化骨中碳酸盐基磷灰石与羟基磷灰石的比值较正常骨组织升高,这提示骨基质矿化不足,且过量的转化生长因子β1还通过改变Ⅰ型胶原蛋白α1和α2链的比例(Ⅰ型胶原蛋白为软骨下骨沉积的主要胶原蛋白亚型)来影响骨基质的矿化过程[30]。尽管硬化骨的骨密度呈上升趋势,但矿物质与胶原的沉积反而减少,这一改变带来的不仅导致骨骼表观密度降低,还会使骨力学刚度显著下降[39]。同时,MURATOVIC团队[35]还观察到高转化生长因子β1信号区内骨细胞腔隙-小管网受抑制的特征,包括小管网络破坏,骨细胞腔隙密度显著增高,单个骨细胞陷窝体积减小,周围的矿化骨基质较少。而骨腔隙-小管网在骨细胞控制基质矿化和胶原组织沉积方面具有重要作用,这也为转化生长因子β信号通路干预软骨下骨重塑提供了有力的证据。 2.3.4 骨髓水肿 与此同时,软骨下骨吸收过程中释放到骨髓的活性转化生长因子β1会募集大量巢蛋白阳性骨髓间充质干细胞 /骨祖细胞在髓腔原位聚集,进行异常重塑形成类骨质岛致骨髓腔隙减小,并为随后在MRI中显示为骨髓水肿的征象做出贡献[40],这与之前在骨关节炎患者中软骨下骨样本中发现的特征相一致[41]。实际上,转化生长因子β1现被发现的所有已知作用几乎都与骨髓水肿的组织学特征相关,如低矿化骨质、骨髓灌注增加、矿化无关的类骨质形成和局部骨髓纤维化等,且该征象是目前已知与骨关节炎疼痛、功能障碍和进行性软骨损伤相关的预后因素之一[42-43]。 软骨下骨重塑作为骨细胞对异常机械负荷的反应之一,尽管在最初的尝试以代偿性增加骨密度来承载更高的机械负荷,但无序的胶原纤维排列和矿物晶体的异常沉积,导致晚期骨骼脆性显著增加,刚度下降,反而使骨骼承受变形的能力降低,进一步降低了对关节软骨在冲击载荷下的吸收和缓冲能力,使软骨下骨在机械性能上处于劣势,加重了关节软骨的额外损伤。随着研究的不断深入,高水平的活跃转化生长因子β1在破坏软骨下骨稳态和结构完整性上得到了越来越多的证据支持。但鉴于转化生长因子β1在广泛的生物过程中发挥着重要作用,例如生长分化、细胞迁移、促纤维化、上皮间质转换以及免疫调节等[44]。因此,系统性的抑制转化生长因子β1活性可能会影响其他器官(包括关节软骨)中的组织稳态。近年来,一项使用组织蛋白酶 K 抑制剂抑制软骨下骨重塑的策略正在进行二期临床试验,结果表明骨关节炎患者的骨和软骨进展显著减少[45]。因此特异性抑制软骨下骨中转化生长因子β1活性的组织导向性疗法将可能在未来延缓骨关节炎的药物开发占有一席之地。转化生长因子β信号通路对软骨下骨重塑的影响详见表2。"


2.4 参与血管生成 软骨下骨消散负荷能力的降低会改变关节软骨上的应力分布和破坏软骨细胞中维持软骨稳态的信号通路,而软骨的退变则会加重软骨下骨微结构的异常重塑,这会导致额外骨关节炎的进展。因此关节软骨与软骨下骨二者作为一个完整的的复合骨功能单元,不仅在生物力学上息息相关,细胞分子间的交流也必不可少,而血管作为中间桥梁,软骨下骨血流的变化也会干扰营养物质和氧气对被覆软骨的供应。正常情况下关节软骨 和软骨下骨通过骨软骨交界处整合在一起,骨软骨交界处由钙化软骨区和下方的软骨下骨板组成,其中软骨层与钙化层之间有一明显的组织学边界为潮线,起到连接二者的作用。 钙化软骨作为关节软骨与软骨下骨间的屏障,依靠其致密的结构限制软骨下骨的小分子扩散进入关节软骨区域,从而保证关节软骨无毛细血管神经网络覆盖,维持关节软骨生理微环境的稳定。而在人类骨关节炎标本中,观察到骨软骨交接处孔隙率升高,来自软骨下骨的新生血管侵蚀钙化软骨层,使钙化区厚度及血管密度显著升高[46]。研究表明,新生血管突破潮线侵犯到关节软骨中,不仅打破了关节微环境稳态的同时还增加关节软骨微环境中的氧气张力迫使关节软骨中需氧量增加,从而加速细胞外基质的降解和异常激活潜伏在基质中转化生长因子β配体,活化的转化生长因子β1一方面通过p44/p42 MAPKs与SAPK/JNK非经典途径轴向调节软骨细胞内血管内皮生长因子基因表达增加;另一方面,在缺氧条件下,转化生长因子β1还通过调节缺氧诱导因子1α的表达诱导巨噬细胞产生血管内皮生长因子[47-48]。过表达的血管内皮生长因子不仅能够促进血管生成和软骨内骨形成,同时使软骨细胞肥大表型及凋亡增加,促使关节软骨微环境进一步恶化,最终导致关节软骨不可逆的退变[49]。CUI等[50]在体外实验中证实了骨软骨交接处血管生成数量与骨关节炎疾病严重程度和软骨退变呈显著正相关,而抑制转化生长因子β/Smad 2/3信号通路可显著减少血管生成,延缓骨关节炎模型中关节软骨的退变。因此,软骨下骨中异常血管生成和关节软骨的血管入侵同样可作为骨关节炎早期诊断的特征之一。 可喜的是,随着生理学研究的不断进展,最新发现的一种H形血管为理解软骨下骨重塑和关节软骨退化间的联系提供了新的见解。作为高表达CD31和内皮黏蛋白的特异血管亚型,H型血管主要分布于干骺端和骨膜下,其特征是周围分布密集的Osterix阳性骨祖细胞与Ⅰ型α胶原蛋白阳性成骨细胞[51]。研究表明,H 型血管可通过刺激骨髓中骨祖细胞增殖和分化来主动指导骨形成,在减少骨骼内H型血管的数量后,局部骨骼出现骨小梁结构受损,骨皮质变薄,而骨缺损区在骨重建期间呈现明显的骨再生能力减弱[52]。不仅如此,在青少年长骨构塑期,骨骼的发育有赖于H型血管释放的基质蛋白酶,特别是基质金属蛋白酶9,以此实现生长板内软骨基质再吸收和替换,从而维持长骨的纵向生长[53]。学者们将成骨和血管生成在空间和时间上密切关联称为“血管生成-成骨偶联”。 伴随生长发育,骨骼内的H型血管的数量随着年龄的增长而不断减少[54],这也能解释在老年人骨伤后骨愈合能力弱于青壮年。但在患有骨关节炎的人类膝关节中却发现H型血管数量的异常增加。早在骨关节炎小鼠模型术后2周,SU等[55]即观察到 H 型血管在小鼠软骨下骨和骨髓中增生,甚至部分新生的H 型血管已侵入钙化软骨。结合之前ZHEN等[32]在骨关节炎进展中,发现骨重塑吸收过程中破骨细胞所产生的转化生长因子β1有助于早期软骨下骨中的血管生成的这一结论,文章可以做出大胆推论,鉴于其在促进成骨方面的基础作用,这表明增生的H型血管对骨关节炎中活跃的骨重塑做出贡献;而软骨下骨微结构的变化不仅意味着骨软骨界面完整性的丧失,同时伴随H型血管突破屏障侵入关节软骨,异常交流通道的创建增加了关节软骨与软骨下骨间的细胞分子间的串扰,使得原本关节软骨中低代谢活性的基质转换进一步落后于软骨下骨中明显增强的骨转换,进而使关节软骨的稳态调节与软骨下骨的重塑脱节,这也可能是骨关节炎进展过程中出现非耦合骨重塑的原因之一。 WANG等[56]发现抑制巢蛋白阳性骨髓间充质干细胞中的转化生长因子β活性可减弱骨重塑、异常H型血管生成和软骨损伤。这也向研究者们提示了转化生长因子β信号可能通过软骨下骨中增加的微裂隙和血管通道参与骨软骨代谢的调节来介导骨软骨的生化串扰,这种串扰可能是这些病理变化的结果,也可能是这些病理变化的促成因素。遗憾的是,目前尚未有研究探讨将过度活跃的转化生长因子β信号与软骨下骨中H型血管形成联系起来的具体机制,也没有H型血管直接沟通的关节软骨与软骨下骨的证据。只有几种药物报道称可通过抑制转化生长因子β活性和减少H型血管形成来减缓膝骨关节炎的进展[57]。 H型血管的发现也侧面向研究者们论证了一个事实,在骨关节炎的发病中软骨退变与软骨下骨的重塑不单是相互独立的状态,二者之间更是互为因果、相互依存的关系。而充分认识到其中的关联有助于研究者们完善骨关节炎的发病机制,探寻更高效的治疗方法从而极大降低晚期患者的手术率,改善大部分患者的生活质量。"

| [1] 张莹莹,李旭东,杨佳娟,等.中国40岁及以上人群骨关节炎患病率的Meta分析[J].中国循证医学杂志,2021,21(4):407-414. [2] ZHANG Z, HUANG C, JIANG Q, et al. Guidelines for the diagnosis andtreatment of osteoarthritis in China (2019 edition). Ann Transl Med. 2020;8(19):1213. [3] CHO Y, JEONG S, KIM H, et al. Disease-modifying therapeutic strategies in osteoarthritis: current status and future directions. Exp Mol Med. 2021;53(11): 1689-1696. [4] HU W, CHEN Y, DOU C, et al. Microenvironment in subchondral bone: predominant regulator for the treatment of osteoarthritis. Ann Rheum Dis. 2021; 80(4):413-422. [5] ZHANG L, WEN C. Osteocyte dysfunction in joint homeostasis and osteoarthritis. Int J Mol Sci. 2021;22(12):6522. [6] YAO Q, WU X, TAO C, et al. Osteoarthritis: pathogenic signaling pathways and therapeutic targets. Signal Transduct Target Ther. 2023;8(1):56. [7] ROBERTS AB, ANZANO MA, LAMB LC, et al. New class of transforming growth factors potentiated by epidermal growth factor: isolation from non-neoplastic tissues. Proc Natl Acad Sci USA. 1981;78(9):5339-5343. [8] ROBERTS AB, ANZANO MA, WAKEFIELD LM, et al. Type beta transforming growth factor: a bifunctional regulator of cellular growth. Proc Natl Acad Sci USA. 1985; 82(1):119-123. [9] MORIKAWA M, DERYNCK R, MIYAZONO K. TGF-β and the TGF-β family: context-dependent roles in cell and tissue physiology. Cold Spring Harb Perspect Biol. 2016;8(5):a021873. [10] REN LL, LI XJ, DUAN TT, et al. Transforming growth factor-β signaling: from tissue fibrosis to therapeutic opportunities. Chem Biol Interact. 2023;369:110289. [11] ALBRO MB, NIMS RJ, CIGAN AD, et al. Dynamic mechanical compression of devitalized articular cartilage does not activate latent TGF-β. J Biomech. 2013; 46(8):1433-1439. [12] ZI Z. Molecular engineering of the TGF-β signaling pathway. J Mol Biol. 2019; 431(15):2644-2654. [13] VANDER ARK A, CAO J, LI X. TGF-β receptors: in and beyond TGF-β signaling. Cell Signal. 2018;52:112-120. [14] ZHANG YE. Non-smad signaling pathways of the TGF-β family. Cold Spring Harb Perspect Biol. 2017;9(2):a022129. [15] LEE W, MILLER EY, ZHU H, et al. High frame rate deformation analysis of knee cartilage by spiral dualMRI and relaxation mapping. Magn Reson Med. 2023; 89(2):694-709. [16] HARDY MJ, PU X, OXFORD JT. Purification and isolation of proteins from hyaline cartilage. Methods Mol Biol. 2023;2598:217-225. [17] WANG Q, TAN QY, XU W, et al. Cartilage-specific deletion of Alk5 gene results in a progressive osteoarthritis-like phenotype in mice. Osteoarthritis Cartilage. 2017;25(11):1868-1879. [18] DU X, CAI L, XIE J, et al. The role of TGF-beta3 in cartilage development and osteoarthritis. Bone Res. 2023;11(1):2. [19] ZHAN X, CAI P, LEI D, et al. Comparative profiling of chondrogenic differentiation of mesenchymal stem cells (MSCs) driven by two different growth factors. Cell Biochem Funct. 2019;37(5):359-367. [20] VAN DER KRAAN PM, BLANEY DAVIDSON EN, BLOM A, et al. TGF-beta signaling in chondrocyte terminal differentiation and osteoarthritis: modulation and integration of signaling pathways through receptor-Smads. Osteoarthritis Cartilage. 2009;17(12):1539-1545. [21] MRUGALA D, BONY C, NEVERS N, et al. Phenotypic and functional characterisation of ovine mesenchymal stem cells: application to a cartilage defect model. Ann Rheum Dis. 2008;67(3):288-295. [22] LIU S, DENG Z, CHEN K, et al. Cartilage tissue engineering: from proinflammatory and anti inflammatory cytokines to osteoarthritis treatments (Review). Mol Med Rep. 2022;25(3):99. [23] ALI SA, GANDHI R, POTLA P, et al. Sequencing identifies a distinct signature of circulating microRNAs in early radiographic knee osteoarthritis. Osteoarthritis Cartilage. 2020;28(11):1471-1481. [24] LIU L, ZHAO C, ZHANG H, et al. Asporin regulated by miR-26b-5p mediates chondrocyte senescence and exacerbates osteoarthritis progression via TGF-β1/Smad2 pathway. Rheumatology (Oxford). 2022;61(6):2631-2643. [25] PARK JY, BAE HC, PVO SH, et al. TGFβ1-induced transglutaminase-2 triggers catabolic response in osteoarthritic chondrocytes by modulating MMP-13. Tissue Eng Regen Med. 2021;18(5):831-840. [26] CHEN R, MIAN M, FU M, et al. Attenuation of the progression of articular cartilage degeneration by inhibition of TGF-β1 signaling in a mouse model of osteoarthritis. Am J Pathol. 2015;185(11):2875-2885. [27] CARABALLO CB, COELHO TRP, DE HOLANDA AFONSO RC, et al. Osteoarthritic synovial fluid and TGF-β1 induce interleukin-18 in articular chondrocytes. Cartilage. 2020;11(3):385-394. [28] LEE H, KIM H, SEO J, et al. TissueGene-C promotes an anti-inflammatory micro-environment in a rat monoiodoacetate model of osteoarthritis via polarization of M2 macrophages leading to pain relief and structural improvement. Inflammopharmacology. 2020;28(5):1237-1252. [29] GAO J, REN P, GONG H. Morphological and mechanical alterations in articular cartilage and subchondral bone during spontaneous hip osteoarthritis in guinea pigs. Front Bioeng Biotechnol. 2023;11:1080241. [30] ZHU X, CHAN YT, YUNG PSH, et al. Subchondral bone remodeling: a therapeutic target for osteoarthritis. Front Cell Dev Biol. 2021;8:607764. [31] DAI G, XIAO H, LIAO J, et al. Osteocyte TGFβ1 Smad2/3 is positively associated with bone turnover parameters in subchondral bone of advanced osteoarthritis. Int J Mol Med. 2020;46(1):167-178. [32] ZHEN G, WEN C, JIA X, et al. Inhibition of TGF-β signaling in mesenchymal stem cells of subchondral bone attenuates osteoarthritis. Nat Med. 2013;19(6):704-712. [33] ZHEN G, GUO Q, LI Y, et al. Mechanical stress determines the configuration of TGFβ activation in articular cartilage. Nat Commun. 2021;12(1):1706. [34] BAILEY KN, NGUYEN J, YEE CS, et al. Mechanosensitive control of articular cartilage and subchondral bone homeostasis in mice requires osteocytic transforming growth factor β signaling. Arthritis Rheumatol. 2021;73(3):414-425. [35] MURATOVIC D, FINDLAY DM, QUARRINGTON RD, et al. Elevated levels of active transforming growth factor β1 in the subchondral bone relate spatially to cartilage loss and impaired bone quality in human knee osteoarthritis. Osteoarthritis Cartilage. 2022;30(6):896-907. [36] SIMKIN PA. Marrow fat may distribute the energy of impact loading throughout subchondral bone. Rheumatology (Oxford). 2018;57(3):414-418. [37] FINNILA MAJ, THEVENOT J, AHO OM, et al. Association between subchondral bone structure and osteoarthritis histopathological grade. J Orthop Res. 2017; 35(4):785-792. [38] LI J, GE L, ZHAO Y, et al. TGF-β2 and TGF-β1 differentially regulate the odontogenic and osteogenic differentiation of mesenchymal stem cells. Arch Oral Biol. 2022; 135:105357. [39] LI Y, LIEM Y, DALL’ARA E, et al. Subchondral bone microarchitecture and mineral density in human osteoarthritis and osteoporosis: a regional and compartmental analysis. J Orthop Res. 2021;39(12):2568-2580. [40] CRANE JL, CAO X. Bone marrow mesenchymal stem cells and TGF-β signaling in bone remodeling. J Clin Invest. 2014;124(2):466-472. [41] HU Y, CHEN X, WANG S, et al. Subchondral bone microenvironment in osteoarthritis and pain. Bone Res. 2021;9(1):20. [42] ZHEN G, CAO X. Targeting TGFβ signaling in subchondral bone and articular cartilage homeostasis. Trends Pharmacol Sci. 2014;35(5):227-236. [43] AKHAVAN S, MARTINKOVICH SC, KASIK C, et al. Bone marrow edema, clinical significance, and treatment options: a review. J Am Acad Orthop Surg. 2020; 28(20):e888-e899. [44] PENG D, FU M, WANG M, et al. Targeting TGF-β signal transduction for fibrosis and cancer therapy. Mol Cancer. 2022;21(1):104. [45] LINDSTROM E, RIZOSKA B, TUNBLAD K, et al. The selective cathepsin K inhibitor MIV-711 attenuates joint pathology in experimental animal models of osteoarthritis. J Transl Med. 2018;16(1):56. [46] ZHOU X, CAO H, YUAN Y, et al. Biochemical signals mediate the crosstalk between cartilage and bone in osteoarthritis. Biomed Res Int. 2020;2020:5720360. [47] KOIDE N, ODKHUU E, NAIKI Y, et al. Augmentation of LPS-induced vascular endothelial cell growth factor production in macrophages by transforming growth factor-β1. Innate Immun. 2014;20(8):816-825. [48] KUROYANAGI G, OTSUKA T, YAMAMOTO N, et al. Resveratrol suppresses TGF-β-induced VEGF synthesis in osteoblasts: Inhibition of the p44/p42 MAPKs and SAPK/JNK pathways. Exp Ther Med. 2015;9(6):2303-2310. [49] PEI YA, CHEN S, PEI M. The essential anti-angiogenic strategies in cartilage engineering and osteoarthritic cartilage repair. Cell Mol Life Sci. 2022;79(1):71. [50] CUI Z, CRANE J, XIE H, et al. Halofuginone attenuates osteoarthritis by inhibition of TGF-β activity and H-type vessel formation in subchondral bone. Ann Rheum Dis. 2016;75(9):1714-1721. [51] PENG Y, WU S, LI Y, et al. Type H blood vessels in bone modeling and remodeling. Theranostics. 2020;10(1):426-436. [52] JI G, XU R, NIU Y, et al. Vascular endothelial growth factor pathway promotes osseointegration and CD31hiEMCNhi endothelium expansion in a mouse tibial implant model: an animal study. Bone Joint J. 2019;101-B(7_Supple_C):108-114. [53] 王峰,徐佳,孔令驰,等.H型内皮细胞在成血管-成骨偶联中的作用[J].中华创伤骨科杂志,2020,22(7):641-644. [54] WANG L, ZHOU F, ZHANG P, et al. Human type H vessels are a sensitive biomarker of bone mass. Cell Death Dis. 2017;8(5):e2760. [55] SU W, LIU G, LIU X, et al. Angiogenesis stimulated by elevated PDGF-BB in subchondral bone contributes to osteoarthritis development. JCI Insight. 2020; 5(8):e135446. [56] WANG R, XU B. TGFβ1-modified MSC-derived exosome attenuates osteoarthritis by inhibiting PDGF-BB secretion and H-type vessel activity in the subchondral bone. Acta Histochem. 2022;124(7):151933. [57] LIU Y, XIE HQ, SHEN B. Type H vessels-a bridge connecting subchondral bone remodelling and articular cartilage degeneration in osteoarthritis development. Rheumatology (Oxford). 2023;62(4):1436-1444. |
| [1] | Li Yongjie, Fu Shenyu, Xia Yuan, Zhang Dakuan, Liu Hongju. Correlation of knee extensor muscle strength and spatiotemporal gait parameters with peak knee flexion/adduction moment in female patients with knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1354-1358. |
| [2] | Qi Haodong, Lu Chao, Xu Hanbo, Wang Mengfei, Hao Yangquan. Effect of diabetes mellitus on perioperative blood loss and pain after primary total knee arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1383-1387. |
| [3] | Du Changling, Shi Hui, Zhang Shoutao, Meng Tao, Liu Dong, Li Jian, Cao Heng, Xu Chuang. Efficacy and safety of different applications of tranexamic acid in high tibial osteotomy [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1409-1413. |
| [4] | Yang Yifeng, Ye Nan, Wang Lin, Guo Shuaicheng, Huang Jian. Signaling pathway of dexmedetomidine against ischemia-reperfusion injury [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1464-1469. |
| [5] | Wei Juan, Li Ting, Huan Mengting, Xie Ying, Xie Zhouyu, Wei Qingbo, Wu Yunchuan. Mechanism by which static exercise improves insulin resistance in skeletal muscle of type 2 diabetes [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1271-1276. |
| [6] | Huang Xiarong, Hu Lizhi, Sun Guanghua, Peng Xinke, Liao Ying, Liao Yuan, Liu Jing, Yin Linwei, Zhong Peirui, Peng Ting, Zhou Jun, Qu Mengjian. Effect of electroacupuncture on the expression of P53 and P21 in articular cartilage and subchondral bone of aged rats with knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1174-1179. |
| [7] | Yue Yun, Wang Peipei, Yuan Zhaohe, He Shengcun, Jia Xusheng, Liu Qian, Li Zhantao, Fu Huiling, Song Fei, Jia Menghui. Effects of croton cream on JNK/p38 MAPK signaling pathway and neuronal apoptosis in cerebral ischemia-reperfusion injury rats [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1186-1192. |
| [8] | Zhao Garida, Ren Yizhong, Han Changxu, Kong Lingyue, Jia Yanbo. Mechanism of Mongolian Medicine Erden-uril on osteoarthritis in rats [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1193-1199. |
| [9] | Liu Xin, Hu Man, Zhao Wenjie, Zhang Yu, Meng Bo, Yang Sheng, Peng Qing, Zhang Liang, Wang Jingcheng. Cadmium promotes senescence of annulus fibrosus cells via activation of PI3K/Akt signaling pathway [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1217-1222. |
| [10] | Li Rui, Zhang Guihong, Wang Tao, Fan Ping. Effect of ginseng polysaccharide on the expression of prostaglandin E2/6-keto-prostaglandin 1alpha in traumatic osteoarthritis model rats [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1235-1240. |
| [11] | Liu Jianhong, Liao Shijie, Li Boxiang, Tang Shengping, Wei Zhendi, Ding Xiaofei. Extracellular vesicles carrying non-coding RNA regulate the activation of osteoclasts [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(7): 1076-1082. |
| [12] | Liu Tao, He Zhijun, Li Jinpeng, Song Yuan, Yao Xingzhang, Chen Wen, Li Yan, Bai Bihui. Role and mechanism of noncoding RNA in diabetic peripheral neuropathy [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(7): 1124-1129. |
| [13] | Zhang Kefan, Shi Hui. Research status and application prospect of cytokine therapy for osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(6): 961-967. |
| [14] | Zhang Zeyi, Yang Yimin, Li Wenyan, Zhang Meizhen. Effect of foot progression angle on lower extremity kinetics of knee osteoarthritis patients of different ages: a systematic review and meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(6): 968-975. |
| [15] | Shen Feiyan, Yao Jixiang, Su Shanshan, Zhao Zhongmin, Tang Weidong. Knockdown of circRNA WD repeat containing protein 1 inhibits proliferation and induces apoptosis of chondrocytes in knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 499-504. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||