1.1 设计 随机对照动物实验。实验方案设计见图1。

1.2 时间及地点 实验于2023年8-12月在首都医科大学中国康复研究所实验动物中心及东区实验室开展。
1.3 材料
1.3.1 实验动物 成年雌性SD大鼠50只,SPF级,6-8周龄,体质量(220±20) g,由北京斯贝福公司提供,动物生产许可证号:SCXK(京)2024-0001。饲养于中国康复科学所实验动物中心[动物使用许可证号:SYXK(京)2021-0021],饲养环境:湿度40%-47%,温度20-25 ℃,光照12 h阴暗12 h循环。运用随机数字表法将50只SD大鼠随机分为假手术组(n=10)、脊髓损伤组(n=20)、埃博霉素B组(n=20)。
实验方案经首都医科大学动物实验伦理委员会批准(批准号:AEEI-2022-056)。实验过程遵循了国际兽医学编辑协会《关于动物伦理与福利的作者指南共识》和本地及国家法规。实验动物在异氟烷、空气混合物麻醉下进行所有手术,并尽一切努力最大限度地减少其疼痛、痛苦和死亡。
1.3.2 主要药物与试剂 埃博霉素B(Med Chem Express)的分子式为C27H41NO6S,化学名称为(1S,3S,7S,10R,11S,12S,16R)-7,11-二羟基-8,8,10,12,16-五甲基-3-[(1E)-1-甲基-2-(2-甲基-4-噻唑基)乙烯基]-4,17-二氧杂双环[14.1.0]十七烷-5,9-二酮。埃博霉素B的结构式见图2。埃博霉素B的溶解体系由二甲基亚砜、聚乙二醇300和聚山梨酯80 3种溶剂协同配制,该混合溶剂系统通过腹腔注射途径给予脊髓损伤模型大鼠。

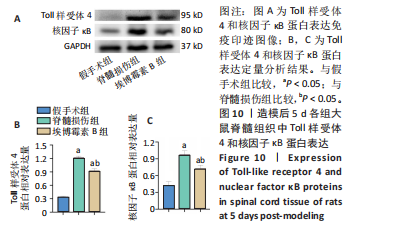
Western Blot检测使用的抗体:兔抗Toll样受体4多克隆抗体(货号:48-2300,Thermo Fisher Scientific);兔抗重组抗核因子κb p105/p50抗体(货号:ab32360,Abcam);兔抗GAPDH(货号:ab181602,Abcam);山羊抗兔IgG H&L(货号:ab205718,Abcam)。
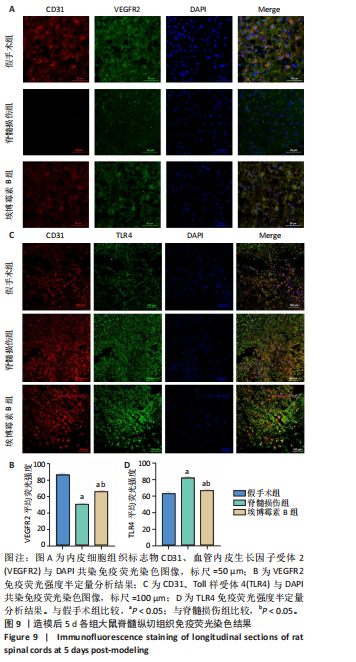
免疫荧光染色使用的抗体:兔抗CD31抗体(货号:ab222783,Abcam);兔抗磷酸化血管内皮生长因子受体2多克隆抗体(货号:PA5-105765,Thermo Fisher Scientific);兔抗Toll样受体4多克隆抗体(货号:PA5-23124,Thermo Fisher Scientific);山羊抗兔IgG (H+L) DyLight™ 650(货号:84546,Thermo Fisher Scientific);山羊抗兔IgG (H+L)FITC(货号:65-6111,Thermo Fisher Scientific)。
1.3.3 主要仪器 PSI-IH脊髓挫伤打击器(美国新泽西州立罗格斯大学);激光散斑血流成像系统(深圳市瑞沃德生命科技股份有限公司);倒置相差显微镜、激光共聚焦显微镜(日本尼康公司);微量分光光度计(中国杭州奥盛仪器有限公司);旷场(美国Clever Sys公司);冰冻切片机(德国Leica公司);-80 ℃冷冻冰箱(中国海尔股份有限公司);超速离心机、酶标仪、荧光定量 PCR检测系统、恒温摇床(美国Thermo Fisher Scientific公司);移液枪(德国Eppendorf公司);超声破碎器(中国Biosafer公司);电热恒温水浴锅(中国上海精宏设备有限公司);电热毯(中国石家庄市北极人电器有限公司);立式自动压力蒸汽灭菌锅(中国上海博迅实业有限公司);灌注仪(中国保定兰格恒流泵有限公司);超净工作台(中国北京森雷普实验室设备有限公司);制冰机(日本松下公司);超纯水净化器(中国北京费尔德科学仪器有限公司);组织研磨器(中国天根生化科技有限公司);水平摇床(中国海门市其林贝尔仪器有限公司)。
1.4 实验方法
1.4.1 大鼠脊髓损伤模型的制备与分组干预
麻醉及定位:术前禁食12 h。检查装置气密性后,将大鼠置于小动物麻醉机的诱导箱中,吸入3%异氟烷与流量为0.5 L/min的空气混合物诱导麻醉,待3-5 min成功麻醉后将异氟烷浓度调至2%,使用呼吸面罩维持麻醉状态。将大鼠从诱导箱中取出,用电动理发剪在背部约3 cm×4 cm区域备皮,备皮完成后用碘伏棉球消毒,再用医用乙醇脱碘。定位方法如下:以手指探寻处于麻醉状态且呈俯卧位的大鼠脊椎最高处(突出的一节),以此为中心,用手术刀片在背部作一纵向正中切口,切开长2.0-3.0 cm的皮肤后可见两侧白色腱膜呈V字形,其交汇处的下方即为大鼠T10椎体。
手术操作:沿着T10椎体棘突两侧粗略地用直剪剪开该处筋膜、肌肉及肌腱,再用弯剪贴近棘突分离棘突两侧附着的肌肉及肌腱,至充分暴露T9-T11节段椎板,此过程中应及时止血。以大鼠椎板咬骨钳依次咬除T10棘突和T10、T11之间的关节突,自尾侧关节突缝隙内入钳,逐步咬除T10椎板,适度去除T10椎体椎弓根,避免它对脊髓打击造成影响,注意保留硬膜囊及T9、T11棘突的完整。充分暴露T10节段脊髓后,假手术组直接逐层缝合切口,其他两组转移至打击器的适配器上,用镊子夹持T9与T11的棘突并锁死机械臂,保证大鼠身体不会存在垂直方向上的位移(图3A)。
打击过程:打开PSI-IH脊髓挫伤打击器程序,设定打击力度1.5 N,用旋钮前后左右微调调整适配器位置,在光照下确认打击锤位于脊髓正中,打击目标区域内无骨渣及渗出血液残留。打击前先将打击锤悬置于刚好接触但不压迫脊髓的高度,转动高度调节旋钮一圈,使打击锤上升一定高度,再点击电脑上的打击按钮,使用打击器打击T10节段脊髓(图3B)。观察到打击后大鼠双后肢伸直、抽搐,尾巴摆动,损伤局部脊髓迅速出现充血水肿且硬膜囊完整,表示造模成功。自适配器上取下大鼠后,在呼吸面罩麻醉下用带针缝合线逐层缝合肌肉、筋膜和皮肤,再次消毒,将大鼠置于电热毯上等待其完全苏醒,而后转移至饲养笼内。

分组干预:造模后即刻,对大鼠编号、称体质量,假手术组与脊髓损伤组腹腔注射0.75 mg/kg埃博霉素B溶液的溶剂;埃博霉素B组一次性腹腔注射0.75 mg/kg埃博霉素B溶液[25]。术后每日早晚为大鼠按摩膀胱以辅助排尿,直至大鼠能够建立完整的排尿反射。排尿时,用左手撑起大鼠腹部,右手找到膀胱,按住膀胱底部,自上而下轻柔挤压,将尿液排尽。排尿后,及时处理大鼠浸湿的肢体与会阴部,防止压疮发生。护理时注意观察大鼠的精神状态及肢体完整情况,如若有大鼠出现自我清洁行为减少、体质量急剧减轻、精神萎靡等到达仁慈终点的表现,及时处理;若出现大鼠啃咬自身后肢的现象,及时对伤口进行消毒并涂抹红霉素软膏,避免伤口恶化。

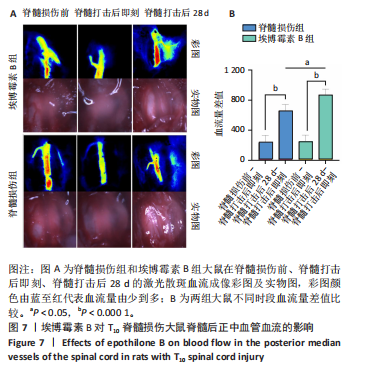
1.4.2 激光散斑血流成像 造模前后与造模后28 d,对埃博霉素B组和脊髓损伤组大鼠脊髓开展激光散斑血流检测,检测对象为脊髓背侧的正中血管。首先,利用激光散斑观测仪自带的红色激光进行定位,当电脑屏幕视野中出现手术切口后,切换至照明灯并放大画面,使用系统自带的图形工具在实物图中划定感兴趣区域,待血流平稳后记录60 s的数据。系统会自动绘制出这60 s内感兴趣区域的平均血流变化曲线。随后,从中选取最为平稳的20 s数据进行统计分析,系统将生成一个Excel表格,表格中包含该时间段内血流的最大值、最小值、均值以及方差等数据。为更直观地呈现脊髓打击前后的情况,需导出彩图及实物图(图4) 。

1.4.3 运动系统评价
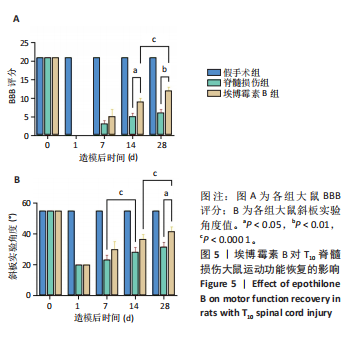
BBB评分:BBB(Basso,Beattie,Bresnahan)评分用于评价大鼠脊髓损伤后的运动功能恢复情况[15]。造模前及造模后第1,7,14,28天,每组每个时间点随机取3只大鼠,将大鼠放置于消毒巾上,由2名对实验分组完全不知情的实验人员辅助完成。BBB评分范围为0-21分,评分越高表示大鼠运动功能恢复越好。
斜板实验:由于操作简单、可重复性高且与脊髓损伤相关性较好,斜板实验常被用来作为测试大鼠脊髓损伤后后肢肌力的一种方法。造模前及造模后第1,7,14,28天,将大鼠身体纵轴与斜板长轴保持一致,从0°开始,自大鼠头侧抬高斜板,每次抬高5°。对于每个位置,大鼠若能保持5 s身体不向下滑落则记为成功。记录大鼠在斜板上保持姿势的最大角度,该角度越大说明大鼠后肢的承重能力越强。每只动物测试3次,取平均值。
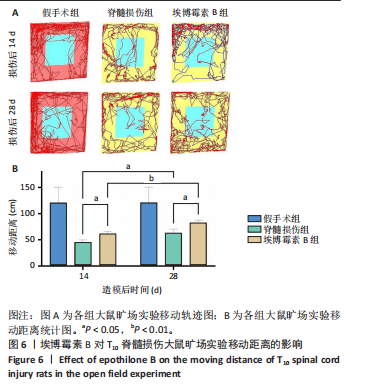
旷场实验:造模后第14,28天,将大鼠放入旷场中,用摄像头观察并记录大鼠的运动轨迹,时长为300 s,结束后导出大鼠的运动距离及运动轨迹图,作为脊髓损伤后运动功能恢复的指标。每组实验后用卫生纸擦净大鼠残留的粪便、尿液等,避免对下次实验造成影响。
1.4.4 组织学检查 造模后第28天,每组随机取3只大鼠取材,进行苏木精-伊红染色。造模后第5天,假手术组随机取3只大鼠,脊髓损伤组与埃博霉素B组各随机取6只大鼠取材,进行免疫荧光染色。造模后第5天,每组随机取3只大鼠取材,进行Western Blot检测。
大鼠灌注及取材处理:吸入异氟烷深度麻醉后,将大鼠固定于取材台上,破开腹壁,显露腹腔及膈肌,再依次剪开膈肌及两侧肋骨,暴露出心脏。去除心脏表面隔膜后,自心脏左下端心尖处入针,插入针头至主动脉处,随后夹持住针头,开始用生理盐水灌注,并用直剪剪开右心房,待大鼠肝脏完全变色、右心房开口处流出清亮液体为止。需要染色切片的大鼠继续换用甲醛溶液固定,以大鼠四肢抽动、身体僵直为停止标准,取材时小心打开大鼠背部损伤区域,以损伤核心点为中心取出长约1 cm的脊髓组织,放入15 mL离心管中以甲醛溶液固定,置于4 ℃冰箱中保存。为保证取出脊髓组织的良好形态,可用2 mL注射器的推杆作为固定基座,将取出的组织放入推杆的十字间隙中,用棉线轻轻缠绕,保证其不会脱落即可。进行蛋白检测的大鼠直接进行取材,取出的脊髓组织放入EP管中于-80 ℃冰箱内冷冻。
脊髓组织切片及组织上清液的获取:①为保证组织冰冻切片时脱水完全,需要切片的脊髓组织于4 ℃冰箱中保存1周,每隔2 d换用浓度梯度为20%,25%,30%的蔗糖甲醛溶液进行脱水处理,避免贴片时组织薄片产生空泡。将脊髓组织水平放入预制的包埋盒中,用OCT包埋剂包埋后急冻约15 min,待包埋块整体变白、内部完全冻结后,用OCT包埋剂固定于切片机基座上,设定切片厚度为12 μm,对脊髓组织进行纵切。切出的合适切片用细毛笔小心展平,并贴附于载玻片上,编号并放入冰箱保存,等待染色。②用手术剪将冻存的脊髓组织剪成小块,用组织研磨器研磨,按RIPA裂解液(含1%蛋白酶磷酸酶抑制剂)与脊髓组织400 μL:100 mg的比例于冰上对组织进行裂解,每5 min混合振荡1次。将裂解完毕的组织液放入超速离心机中,在4 ℃下12 000×g离心10 min,取组织上清液。
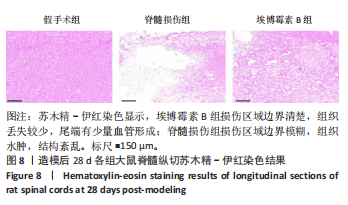
苏木精-伊红染色:取出冰冻切片室温下复温20 min,用PBS于水平摇床上(50 r/min,2 min)清洗去除包埋剂;60 ℃下烘片30 min,用PBS清洗3遍;苏木精染液染色5 min,冲洗,分化液分化,冲洗,蓝化液反蓝,伊红染色2 min,漂洗,常规脱水、透明,滴入中性树脂封固,显微镜下观察,使用Image J(Version 1.53a)软件统计脊髓空洞面积与总面积。用脊髓空洞面积与总面积的比值表示组织丢失情况。
Western Blot检测:用BCA法测定蛋白(组织上清液)浓度,按蛋白样本与蛋白上样缓冲液体积比4∶1的比例在100 ℃下煮样10 min;采用10孔的凝胶,将蛋白样品(组织上清液,每孔10 μL,每样品相同上样量)经SDS-PAGE凝胶电泳分离,转膜,用5%脱脂牛奶室温封闭1 h;分别加入Toll样受体4(1∶200)、核因子ĸB(1∶1 000)、GAPDH(1∶10 000,内参)抗体于4 ℃孵育过夜,加入山羊抗兔IgG H&L室温孵育2 h,用TBST缓冲液洗脱3次,每次10-15 min;于暗处加入ECL发光液孵育1.0-2.0 min,放入曝光机中对条带进行曝光。用Image J(Version 1.53a)软件获得条带灰度值。蛋白相对表达用目的蛋白条带灰度值与内参条带灰度值比值确定。
免疫荧光染色:取出冰冻切片于室温下复温30 min,用PBS洗涤3次,滤纸吸干后用免疫组化笔围绕脊髓组织圈画出一个大小合适的圆圈,在该区域内先加入200 μL 0.5%TritonX-100室温破膜30 min,再加入200 μL 5%牛血清白蛋白室温封闭30 min;弃血清后将切片放入避光黑盒内,分别加入兔抗CD31抗体(1∶100)、兔抗磷酸化血管内皮生长因子受体2多克隆抗体(1∶200)、兔抗Toll样受体4多克隆抗体(1∶200)于4 ℃孵育过夜,用PBS洗涤3次,每次10 min;加入山羊抗兔IgG (H+L) DyLight™ 650或山羊抗兔IgG (H+L)FITC室温孵育1.0-2.0 h,用PBS洗涤3次,每次10 min,期间注意避光;加入DAPI室温下避光染核5 min,使用激光共聚焦显微镜获取图像,使用Image J(Version 1.53a)对图片进行定量分析。
1.5 主要观察指标 各组大鼠运动功能、脊髓后正中血管血流恢复情况、脊髓组织病理观察以及脊髓组织Toll样受体4、核因子ĸB蛋白表达、血管内皮生长因子受体2表达。
1.6 统计学分析 使用SPSS (Version 25.0)进行数据分析,数据使用Prism(Version 10.4.0)作图。所有测量结果若符合正态分布,表示为x±s,多组之间比较采用双因素方差分析和Tukey post hoc test测试,方差不等时使用Dunnett-t检验,事后比较采用最小显著性差异法(LSD)。P < 0.05时差异有显著性意义。该文统计学方法已经王方永专家审核。