Chinese Journal of Tissue Engineering Research ›› 2014, Vol. 18 ›› Issue (42): 6856-6862.doi: 10.3969/j.issn.2095-4344.2014.42.025
Previous Articles Next Articles
Research front and hotspots of neuronal calcium sensor-1
Zhu Yu-zhen, Zhang Qing-wen
- College of Physical Education & Training, Shanghai University of Sport, Shanghai 200438, China
-
Revised:2014-09-11Online:2014-10-08Published:2014-10-08 -
Contact:Zhang Qing-wen, Professor, Doctoral supervisor, College of Physical Education & Training, Shanghai University of Sport, Shanghai 200438, China -
About author:Zhu Yu-zhen, Studying for doctorate, College of Physical Education & Training, Shanghai University of Sport, Shanghai 200438, China
CLC Number:
Cite this article
Zhu Yu-zhen, Zhang Qing-wen. Research front and hotspots of neuronal calcium sensor-1[J]. Chinese Journal of Tissue Engineering Research, 2014, 18(42): 6856-6862.
share this article
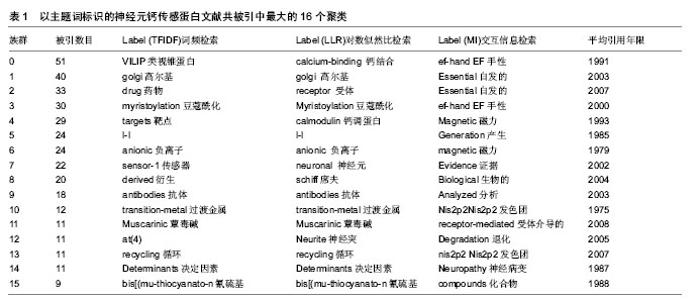
2.1 神经元钙传感蛋白研究前沿领域的代表人物与热点论文 采用CitespaceⅢ可视化分析软件,对科学文献索引数据进行分析。参数设置见研究方法①。根据参数设定的标准,进入标准的突显词是221个,有效的参考文献是 311 421,占99.950 9%,无效参考文献是153,占 0.049 1%,可能是由于检索年限的设定为1982年,而那时很多文献存在摘要、关键词等不全的情况,不符合参数设定标准,此类文献被排除,考虑到本文是对研究前沿的分析,早期文献量较少,对分析结果的影响不大,因此在本文数据分析过程中,仍使用这一数据集。节点Nodes= 417,连线 Links=1 160。 文献共被引聚类是被引文献由于共被引的关系而聚集在一起形成的网络,这是研究前沿的聚类。可视化结果显示,神经元钙传感蛋白共被引文献聚类形成了类似圆形的网络,分布在四周的各个聚类是相对独立的,以PongO为中心的聚类网络交织在一起,是紧密联系的;而且模块性Modularity Q=0.890 2,平均剪影度silhouette= 0.707 9,这一数据也表明共被引文献形成明显而又相对独立的聚类网络,同时表明各个聚类的标签描述也相对准确。这为分析数据提供可靠的依据。 神经元钙传感蛋白共被引文献形成40个文献共被引聚类,根据每个聚类网络内包含文献数目的多少分别编号,表示为0-40。文章着重分析最大的16个聚类,从上到下依次分别是0-15聚类族群(表1)。根据文献共被引聚类标注词,可以看出学者专家采用不同的技术手段对蛋白质的性质、结构、功能、作用靶点进行了研究,可以将这些知识群划分为4个主要学科群,即生物学、生物化学、生物物理学和医药学。结合高被引论文发现,对神经元钙传感蛋白的研究仍以生物学为主,而且主要对蛋白质的生理功能进行了横向和纵深的研究,体现了神经元钙传感蛋白的研究前沿。"

某一领域的研究前沿通过科学家积极引用的文章来体现,它代表了一个研究领域的思想现状。被引用次数多的文献处于核心位置,成为研究领域中的核心成果,但被引频率与文献在研究进程中的贡献没有直接的因果关系。文献在研究进程中的地位和贡献是通过突变值来体现的。科学文献的新趋势和突现的出现是由于:①文献提出一个新发现和科学重大突破。②可能启发科学家从新角度来研究问题[35]。在分析文献共被引网络图谱基础上,对高被引文献进行二次检索,重点分析,探测神经元钙传感蛋白研究的前沿领域。10篇高被引论文尤其是标出突现值的4篇文章[8,14-15],不仅是本聚类中的核心文献,也是整个共被引网络中的核心文献;这10篇文献中的每一篇都有一个新的发现,是研究的起点,代表了研究的新趋势,引领了研究的一个方向。 从表2中10篇引用率最高的文献可以看出,每篇文章都有新的发现,这些发现采用不同的技术手段,主要从神经元钙传感蛋白在不同等级生物体内的功能进了行研究。这些高被引文献的研究对象包括果蝇、酿酒酵母、哺乳动物中的牛科动物、人类,从低等生物到高等生物,逐渐拓展不同等级物种中的这一蛋白的生理生化知识;研究的内容则体现在蛋白质在不同物种、不同生理环境的功能,这些研究内容朝着纵深方向对这一蛋白进行研究,引领这一研究领域的发展方向,成为这一领域的研究前沿。10篇高被引文献中的5篇属于聚类7(表2),占高被引论文的50%。聚类7的词频检索是传感器,对数似然比检索是神经元,交互信息检索是证据,其中Pongs等[15]的这篇文章处于被共引文献聚类中最核心的位置,不仅是7号族群,也是整个网络中引用频率(109)最高的文献,其中心性(centrality)(0.18)和Sigma(2.00)均最大,这表明在对神经元钙传感蛋白的研究中,这篇文章是该研究领域中创新性最大的核心成果,代表了研究前沿和研究的转变方向。"

Pongs等[15]在文章中提出,在体外,神经元钙传感蛋白(Frequenin)是一种鸟苷酸环化酶催化剂,并指出Frequenin与恢复蛋白和视锥蛋白有关,具有对钙离子敏感并与其结合的特性,主要分布于突触中,如肌肉神经接点的运动神经末梢,认为Frequenin是果蝇神经系统内调节突触效能的一种新型的钙结合蛋白。这为神经元钙传感蛋白的研究打开了思路,指明了一个方向。突现值为4.77也进一步说明了这一点;聚类7中的这5篇文献从不同的角度对神经元钙传感蛋白的功能进行了探讨和分析,聚类2是10篇高被引论文中的第二大族群,其中的3篇高被引文献对神经元钙传感蛋白功能做了更加深入的探讨,其中Mcferran等[8](1999)的这篇文献突现值是6.98,说明其在整个蛋白质研究中的地位和贡献巨大,其不仅是本聚类中,也是整个共被引网络中的核心文献,引领了研究的一个方向。聚类1中Mcferran等[14](1998)提出了神经元钙传感蛋白在嗜铬细胞和PC12细胞内进行表达,并指出其可能的生理功能,突现值是5.17。聚类0在10篇高被引文献中虽然只有1篇,在文中提出非洲爪蟾蜍神经元钙传感蛋白的分子克隆和功能特性。但其突现值是6.72,sigma是1.67,中心值时0.08,这些数据从定量的层面上显示此篇文章的创新性,以及这篇文章在0号聚类乃至整个网络中的重要位置。这些分析也进一步证明神经元钙传感蛋白的生理功能是该领域的研究前沿。 2.2 神经元钙传感蛋白研究热点的知识图谱和分析 参数设置见研究方法②。文章中的关键词在知识图谱网络中出现频率高,可以用来确定一个研究领域的热点[36],另外从文章中提取出来的名词短语在一定程度上代表某学科的研究热点。借助CiteSpaceⅢ可视化软件,对文献题录中的关键词进行分析,确定神经元钙传感蛋白研究的热点(表3)。"
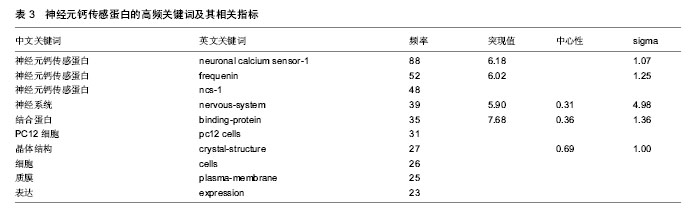

神经元钙传感蛋白(neuronal calcium sensor-1)是出现频率最高的关键词,也是这一领域研究的起点和核心。;在不同时期神经元钙传感蛋白的命名不同,frequenin是其早期的命名,此外还有neuronal calcium sensor-1、freq-1、ncs-1;出现频率较高的关键词还有神经系统、结合蛋白、PC12细胞、晶体结构、质膜和表达等。从这些高频关键词可以看出,对蛋白质的研究主要还是集中于生理功能,此为这一领域的专家学者们最为关注的课题。高中心性的关键词也再次说明了这一问题。中心性表明了关键词的重要程度与地位,中心性数值越大,此关键词在这一领域中的贡献越大,地位越重要;高中心性的关键词一般是某一段时间内研究者共同关注的问题,是研究的热点和前沿。中心性(centrality)数值最大的是晶体结构,为0.69。神经元钙传感蛋白晶体结构的解出,为蛋白质的研究提供了更为广阔的空间和前景及新的研究方向。中心性高的关键词还有磷脂酰肌醇4激酶ß、戊烷-2 (pentane-2)、钙结合蛋白、神经系统、钙调蛋白、EF手性、通道、恢复蛋白。这些关键词分为两类:一类是对蛋白质功能的描述,主要在肿瘤(磷脂酰肌醇4激酶ß)等疾病中的应用,第二类是表明蛋白质的属类,如钙结合蛋白、钙调蛋白、EF手性蛋白和恢复蛋白,主要在神经系统和某些通道发挥作用。这表明神经元钙传感蛋白功能和属类在这一领域中占有重要的地位,是一段时间内研究者共同关注的问题。 Sigma值的大小是用来衡量研究成果创新性的,Sigma值越大,表示研究成果的创新性越大,代表了本研究领域的前沿。关键词“神经系统”的Sigma值最大,为4.98,创新性的提出了神经元钙传感蛋白在体内所处的位置,并逐渐发现这一蛋白与恢复蛋白的相似性,都是结合蛋白的一种,而且还参与了胞外分泌的生理活动。创新性高的关键词还有恢复蛋白、结合蛋白、胞外分泌、分子克隆。Sigma值不同的关键词主要表明蛋白质的性质和功能。相关研究人员从不同的角度、不同的层面、不同深度对这一蛋白的功能进行了创新性研究,引领该领域的研究前沿与热点。 为了更为清楚的了解各个时间段的研究热点,采用时区视图(timezone view),对以关键词标识的研究热点进行分析,从而可以对学科或者研究主题的发展趋势从整体上加以把握。结果显示,研究热点转变的时间点主要集中在1994至1996年,2000年,2008年和2012年。每一阶段研究热点不同,表现出较大的差异性,根据关键词的引用频率及其中心性,筛选出每一阶段研究热点的高频关键词(表4)。结合关键词的引用频率和中心性,1992年至2000年研究热点主要集中于蛋白质的结构和性质,2004年至2012年主要集中于研究蛋白质的功能和作用机制。"

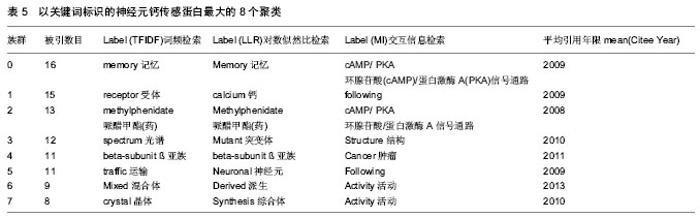
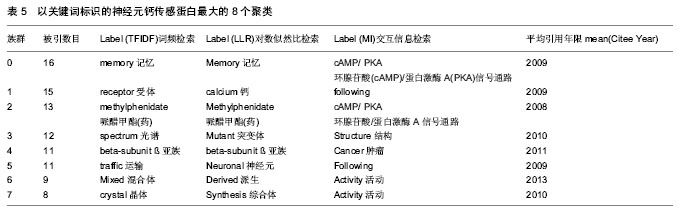
考虑到研究热点具有阶段性,而且其最近的转变点体现在2008年和2012年,因此为更清楚的探测近年来的研究热点,特对2008至2014年的关键词进行聚类分析和时间轴视图(timeline view)分析,参数设置见研究方法中③。关键词聚类排名前八的聚类中(表5),有关记忆的研究是最大的聚类,被引数量最大,是近五年来研究者最为关注的课题;蛋白质受体也是这一领域专家主要研究的重点之一。哌醋甲酯是一种精神兴奋药,能提高精神活动,可对抗抑郁症。采用光谱相关的技术手段,对蛋白质结构的研究表明,蛋白质突变体会导致精神病学相关疾病,如抑郁症、精神分裂症和自闭症等。这一点已经在相关研究中得到验证[31-32]。另外研究还显示,神经元钙传感蛋白R102Q突变影响了蛋白质与质膜间的循环,使其在细胞质和细胞膜之间的循环速度加快[32],导致蛋白质结构和功能的缺 失[27]。最新研究表明神经元钙传感蛋白缺失导致焦虑行为和抑郁样行为,但这些行为可以通过抗焦虑药物和抗抑郁药物进行治疗[22]。目前神经元钙传感蛋白和多巴胺D2受体(D2R)的相互作用被认为是抗精神病药发展的新方向和新目标[37],越来越受到研究者的关注。多巴胺D2受体是抗精神病药物的靶点,这类药物影响神经元钙传感蛋白的表达水平[38-39];另外,神经元钙传感蛋白与D2R的相互作用在中枢神经系统和成瘾行为中起到重要的作用,然而两者相互作用的机制尚不完全清楚。表5显示出,近年来的研究热点更集中在记忆、抑郁症、突变导致的神经系统相关疾病及肿瘤等方面的研究。"

由于研究热点呈现出一定的阶段性,现阶段的研究热点也是本领域中具有潜在研究价值的问题,能够为今后的研究指明方向,确立目标。引用频率会随着时间的临近而减少,此时中心性能更加清楚的表明该关键词在共引网络中的地位和贡献。根据引用频率(F:frequence)和中心性(C:centrality)选取出来的热点关键词(表6),而神经元钙传感蛋白不同时期的命名(frequenin、ncs-1、neuronal calcium sensor-1)都不列在研究热点关键词中,以此对近年来的研究热点进行探测和提取。 高频、高中心性关键词中的肾上腺嗜铬细胞和PC12细胞被广泛用于神经系统疾病研究,尤其是对神经系统中肿瘤的研究,磷脂酰肌醇4羟激酶、ADP核糖基化因子1、氧固醇结合细胞也用于对肿瘤的研究;谷氨酸释放与脑缺血等造成的神经元损伤有关。结合表5和表6可以看出,近年来神经元钙传感蛋白的研究热点是在研究蛋白质生理功能的基础上,更侧重于这一蛋白质的高级功能(如记忆)和各种疾病(如精神分裂症、肿瘤、抑郁症、老年痴呆症、神经元损伤等)的研究。"

| [1] Hui H, McHugh D, Hannan M, et al. Calcium-sensing mechanism in TRPC5 channels contributing to retardation of neurite outgrowth.J Physiol.2006;572: 165-172. [2] Nakamura TY, Jeromin A, Smith G,et al. Novel role of neuronal Ca2+ sensor-1 as a survival factor up-regulated in injured neurons. J Cell Biol. 2006;172: 1081-1091. [3] Sippy T, Cruz-Martin A, Jeromin A,et al.Acute changes in short-term plasticity at synapses with elevated levels of neuronal calcium sensor-1. Nat Neurosci. 2003;6:1031-1038. [4] Jo J, Heon S, Kim MJ, et al.Metabotropic glutamate receptor-mediated LTD involves two interacting Ca(2+) sensors, NCS-1 and PICK1. Neuron. 2008;60: 1095-1111. [5] Haynes LP, Thomas GM,Burgoyne RD. Interaction of neuronal calcium sensor-1 and ADP-ribosylation factor 1 allows bidirectional control of phosphatidylinositol 4-kinase beta and trans-Golgi network-plasma membrane traffic. J Biol Chem. 2005;280: 6047-6054. [6] Burgoyne RD,Weiss JL. The neuronal calcium sensor family of Ca2+-binding proteins. Biochem J. 2001;353: 1-12. [7] Burgoyne RD. Neuronal calcium sensor proteins: generating diversity in neuronal Ca2+ signalling. Nat Rev Neurosci. 2007; 8: 182-193. [8] McFerran BW, Weiss JL.Burgoyne RD.Neuronal Ca(2+) sensor 1. Characterization of the myristoylated protein, its cellular effects in permeabilized adrenal chromaffin cells,Ca(2+)- independent membrane association, and interaction with binding proteins, suggesting a role in rapid Ca(2+) signal transduction. J Biol Chem.1999;274: 30258-30265. [9] Weiss JL, Hui H, Burgoyne RD. Neuronal calcium sensor-1 regulation of calcium channels, secretion, and neuronal outgrowth. Cell Mol Neurobiol.2010;30: 1283-1292. [10] Amici M, Doherty A, Jo J,et al. Neuronal calcium sensors and synaptic plasticity. Biochem Soc Trans.2009;37: 1359-1363. [11] Burgoyne RD, O'Callaghan DW, Hasdemir B, et al. Neuronal Ca2+-sensor proteins: multitalented regulators of neuronal function. Trends Neurosci.2004;27: 203-209. [12] Weiss JL, Archer DA,Burgoyne RD. Neuronal Ca2+ sensor-1/frequenin functions in an autocrine pathway regulating Ca2+ channels in bovine adrenal chromaffin cells.J Biol Chem.2000;275: 40082-40087. [13] Dason JS, Romero-Pozuelo J, Marin L, et al. Frequenin/ NCS-1 and the Ca2+-channel alpha1-subunit co-regulate synaptic transmission and nerve-terminal growth. J Cell Sci.2009;122: 4109-4121. [14] McFerran BW, Graham ME, Burgoyne RD. Neuronal Ca2+ sensor 1, the mammalian homologue of frequenin, is expressed in chromaffin and PC12 cells and regulates neurosecretion from dense-core granules. J Biol Chem. 1998;273: 22768-22772. [15] Pongs O,Lindemeier J,Zhu XR,et al.Frequenin--a novel calcium-binding protein that modulates synaptic efficacy in the Drosophila nervous system. Neuron.1993;11: 15-28. [16] Tsujimoto T,Jeromin A, Saitoh N,et al.Neuronal calcium sensor 1 and activity-dependent facilitation of P/Q-type calcium currents at presynaptic nerve terminals. Science. 2002;295: 2276-2279. [17] Rivosecchi R, Pongs O, Theil T, et al.Implication of frequenin in the facilitation of transmitter release in Drosophila. J Physiol. 1994;474: 223-232. [18] Gomez M, De Castro E, Guarin E, et al. Ca2+ signaling via the neuronal calcium sensor-1 regulates associative learning and memory in C. elegans. Neuron. 2001;30: 241-248. [19] Saab BJ, Georgiou J, Nath A, et al. NCS-1 in the dentate gyrus promotes exploration, synaptic plasticity, and rapid acquisition of spatial memory. Neuron.2009;63: 643-656. [20] Hammond RS, Tull LE, Stackman RW.On the delay-dependent involvement of the hippocampus in object recognition memory. Neurobiology of Learning and Memory. 2004;82: 26-34. [21] Drumond LE, Mourão FA, Leite HR, et al.Differential effects of swimming training on neuronal calcium sensor-1 expression in rat hippocampus/cortex and in object recognition memory tasks. Brain Research Bulletin. 2012;88: 385-391. [22] de Rezende VB, Rosa D V, Comim CM, et al. NCS-1 deficiency causes anxiety and depressive-like behavior with impaired non-aversive memory in mice. Physiology & behavior. 2014;130: 91-98. [23] Comim CM, Silva NC, Mina F, et al.Evaluation of NCS-1, DARPP-32, and neurotrophins in hippocampus and prefrontal cortex in rats submitted to sepsis. Synapse. 2014;68(10): 474-479. [24] Aronica E, Boer K, Doorn KJ, et al. Expression and localization of voltage dependent potassium channel Kv4.2 in epilepsy associated focal lesions. Neurobiol Dis.2009;36: 81-95. [25] Braunewell KH. The darker side of Ca2+ signaling by neuronal Ca2+-sensor proteins: from Alzheimer's disease to cancer. Trends Pharmacol Sci. 2005;26: 345-351. [26] Torres KC, Souza BR, Miranda DM, et al. Expression of neuronal calcium sensor-1 (NCS-1) is decreased in leukocytes of schizophrenia and bipolar disorder patients. Prog Neuropsychopharmacol Biol Psychiatry.2009;33: 229-234. [27] Handley MT, Lian LY, Haynes LP, et al. Structural and functional deficits in a neuronal calcium sensor-1 mutant identified in a case of autistic spectrum disorder. PLoS One. 2010;5: e10534. [28] Burgoyne RD, Haynes LP. Neuronal calcium sensor proteins: emerging roles in membrane traffic and synaptic plasticity. F1000 Biol Rep. 2010;2. [29] Koh PO, Undie AS, Kabbani N, et al. Up-regulation of neuronal calcium sensor-1 (NCS-1) in the prefrontal cortex of schizophrenic and bipolar patients. Proc Natl Acad Sci U S A. 2003;100: 313-317. [30] Bai J, He F, Novikova SI,et al. Abnormalities in the dopamine system in schizophrenia may lie in altered levels of dopamine receptor-interacting proteins. Biol Psychiatry.2004;56: 427-440. [31] Saab BJ. The synaptic role of neuronal calcium sensor 1 in dentate gyrus plasticity, curiousity and spatial memory, In Department of Molecular Genetics, University of Toronto. 2010. [32] Piton A, Michaud JL, Peng H, et al.Mutations in the calcium-related gene IL1RAPL1 are associated with autism. Hum Mol Genet.2008;17: 3965-3974. [33] Chen C.CiteSpace II: Detecting and Visualizing Emerging Trends and Transient Patterns in Scientific Literature. Jounal of the American society for information science and technology. 2006;57: 359-377. [34] Chaomei Chen,Yuee Chen,Mark Horowitz,et al.Towards an explanatory and computational theory of scientific discovery. Journal of Informetrics. 2009;3: 191-209. [35] 刘则渊,陈悦,侯海燕.科学知识图谱方法与应用[M].北京:人民出版社, 2008. [36] 栾春娟,赵呈刚.基于SCI的基因操作技术国际前沿分析[J].技术与创新管理.2009;30:11-13. [37] Kabbani N, Woll MP, Nordman JC, et al. Dopamine receptor interacting proteins: targeting neuronal calcium sensor-1/D2 dopamine receptor interaction for antipsychotic drug development. Curr Drug Targets. 2012; 13(1):72-79. [38] Lian LY, Pandalaneni SR, Patel P, et al. Characterisation of the interaction of the C-terminus of the dopamine D2 receptor with neuronal calcium sensor-1. PLoS One. 2011; 6(11): e27779. [39] Woll MP, De Cotiis DA, Bewley MC, et al. Interaction between the D2 dopamine receptor and neuronal calcium sensor-1 analyzed by fluorescence anisotropy. Biochemistry.2011; 50(41): 8780-8791. |
| [1] | Zhu Xuefen, Huang Cheng, Ding Jian, Dai Yongping, Liu Yuanbing, Le Lixiang, Wang Liangliang, Yang Jiandong. Mechanism of bone marrow mesenchymal stem cells differentiation into functional neurons induced by glial cell line derived neurotrophic factor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1019-1025. |
| [2] | Wang Feng, Zhou Liyu, Saijilafu, Qi Shibin, Ma Yanxia, Wei Shanwen. CaMKII-Smad1 promotes axonal regeneration of peripheral nerves [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1064-1068. |
| [3] | Lu Jie, Li Xue, Wang Lu, Fan Jia, Zhang Yeting, Lu Xiaobin, Yuan Qiongjia. Effects of different-intensity swimming exercises on spatial learning and memory ability and the expression of Orexin A in the rat cerebellum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(23): 3697-3703. |
| [4] | Wang Donghui, Wu Xin, Sun Ningning, Zhang Han, Gao Jianfeng. Electroacupuncture intervention on the expression of synaptic plasticity-related proteins in the hippocampi of mice with radiation-induced brain injury [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(14): 2205-2210. |
| [5] | Wang Guoyu, Cheng Zhijian, Yang Baohui, Li Haopeng, He Xijing. Olfactory ensheathing cell transplantation promotes the ultrastructure repair at the lesion site of rat models of spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(5): 699-703. |
| [6] | Zhou Jun, Gong Yusuo, Li Shenghua, Zhu Yanguo. Biomechanical characteristics of the modified memory alloy internal fixator for separation of pubic symphysis [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(36): 5764-5767. |
| [7] | Li Ying, Guan Hantian, Zhou Yu. Semantic memory impairment and neuroregulation in patients with mild cognitive impairment [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(32): 5236-5242. |
| [8] | Du Xiaowen, Lin Dapeng, Tu Guanjun. S100A4 promotes differentiation of neural stem cells through up-regulation of brain-derived neurotrophic factor [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(19): 3029-3034. |
| [9] | Gong Jiao, Liu Ming. Human induced pluripotent stem cell transplantation for hypoxic-ischemic encephalopathy in neonatal mice [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(33): 5322-5327. |
| [10] | Zhang Xiaozhuo, Lü Tingting, Wang Zhaoqin, Weng Zhijun, Cui Yunhua, Zhang Fang, Zhao Min, Liu Huirong, Wu Huangan. Satellite glial cells in dorsal root ganglia: implication for pain regulation [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(33): 5396-5403. |
| [11] | Cui Xuewen, Yang Kaiyuan, Yang Wenjing, Lu Hao1, Shi Wentao, Chen Pingbo, Bi Shiqi, Shen Yuanhao, Zhang Zhijian. Effect of fibrin glue scaffolds embedded with sonic hedgehog-loaded chitosan microspheres on the differentiation of nasal mucosa-derived ectomesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(29): 4694-4700. |
| [12] | Shi Jiang, Gao Shilun, Liu Jinduo, Gu Tianxiang, Shi Enyi. Bone marrow mesenchymal stem cell exosomes alleviate oxygen-glucose deprivation/reperfusion injury in hippocampal neurons [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(21): 3316-3322. |
| [13] | Zhang Yeting1, 2, Fu Yan3, Li Xue1, Zhang Kang4, Yuan Qiongjia1. Effects of different loads of swimming on the expression of post-synaptic density-95 and neural cell adhesion molecule in the rat hippocampus [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(19): 3067-3073. |
| [14] | Ma Jiehua, Zhang Dan, Huo Yanli, Wei Yawei, Sun Lin, Zhao Yu. Lentiviral-mediated transplantation of olfactory ensheathing cells modified by ciliary neurotrophic factor for treatment of spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(17): 2709-2715. |
| [15] | Wang Xianbin, Li Liyan. Interaction between satellite glial cells and neurons in sensory neuropathic pain [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(11): 1788-1793. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||