Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (26): 4223-4230.doi: 10.12307/2023.535
Previous Articles Next Articles
Changes in microvascular reactivity and exercise intervention in obese patients
Xiao Zhe1, Zhou Shufeng1, Zhu Huan1, Li Feng2, Hu Jiangping3
- 1School of Physical Education, Hubei University for Nationalities, Enshi 445000, Hubei Province, China; 2School of Physical Education, Guangxi University of Science and Technology, Liuzhou 545000, Guangxi Zhuang Autonomous Region, China; 3School of Physical Education, Guangxi Normal University for Nationalities, Chongzuo 532200, Guangxi Zhuang Autonomous Region, China
-
Received:2022-08-29Accepted:2022-10-10Online:2023-09-18Published:2023-01-28 -
Contact:Hu Jiangping, PhD candidate, Associate professor, School of Physical Education, Guangxi Normal University for Nationalities, Chongzuo 532200, Guangxi Zhuang Autonomous Region, China -
About author:Xiao Zhe, Master, Lecturer, School of Physical Education, Hubei University for Nationalities, Enshi 445000, Hubei Province, China -
Supported by:Hubei Provincial Teaching Research Project of Higher Education Institutions in 2020, No. 2020550 (to ZH); Key Project of Hubei Provincial Education Department Science Research Program in 2021, No. D20211901 (to ZH); Doctoral Foundation Project of Guangxi University of Science and Technology, No. 20S07 (to LF); Hubei Engineering Research Center Open Project for Selenium Products Nutrition and Health Intelligent Technology in 2022, No. PT082208 (to ZH, XZ, and ZSF [project participants])
CLC Number:
Cite this article
Xiao Zhe, Zhou Shufeng, Zhu Huan, Li Feng, Hu Jiangping. Changes in microvascular reactivity and exercise intervention in obese patients[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(26): 4223-4230.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

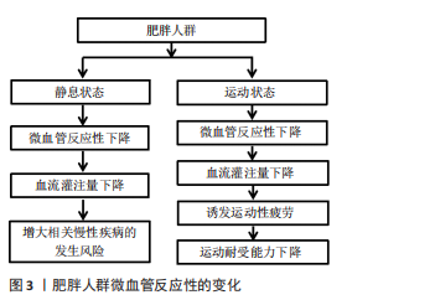
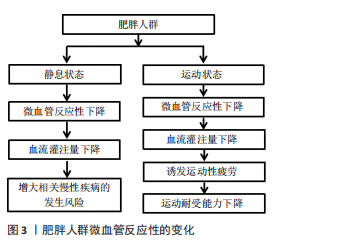
2.1.1 静息状态下肥胖人群微血管反应性的变化 对于肥胖人群,静息状态下微血管反应性出现下降,导致血流灌注不足,增大相关慢性疾病的发生风险。LA FAVOR等[14]研究表明,肥胖人群体内过氧化氢和超氧化物水平升高,股外侧肌乙酰胆碱刺激后微血管血流增加幅度降低,表明肥胖人群微血管内皮功能受损。另外,唐东辉等[11]研究表明肥胖青少年存在微血管内皮细胞功能障碍,导致微血管反应性显著下降。肥胖人群微血管功能的变化与白色脂肪增多有关。白色脂肪组织会释放游离脂肪酸,启动机体氧化应激反应,造成微血管内皮细胞损伤;同时脂肪组织扩张造成脂肪组织缺氧促进炎性细胞因子释放,降低一氧化氮(Nitric oxide,NO)利用率,进一步加重微血管功能障碍,使微血管反应性下降[15-16]。此外,微血管反应性会随着肥胖程度的加剧进一步下降。PIENAAR等[17]研究发现,肥胖人群微血管内皮依赖式舒张反应能力与BMI、体脂率、腰围、胰岛素抵抗指数及血压具有显著负相关。对于肥胖人群,随着肥胖程度的增大会进一步提高白色脂肪诱发的氧化应激和炎症反应水平,加剧微血管内皮细胞的损伤,导致微血管反应性进一步下降。此外,当肥胖人群出现胰岛素抵抗后,微血管反应性也会进一步下降。胰岛素抵抗会破坏血管内皮细胞中胰岛素介导的PI3通路,抑制内皮型一氧化氮合酶(Endothelial nitric oxide synthase,eNOS)激活,减少NO的生成,同时增强内皮素1(Endothelin-1,ET-1)的血管收缩效应,降低微血管反应性[12,18]。 肥胖人群皮肤微血流阻断后反应性充血能力也显著下降。微血管血流阻断后反应性充血是局部组织受压,引起周围软组织毛细血管缺血及低血氧(缺氧),解除压迫血流又进入组织,受压区开始充血,包括快速充血和血流持续性补偿2个阶段[19-20], 尤其是充血速度是一种新的微血管功能标记物,是一种定量、实时、迅速、无创性的评价微血管功能的手段,也是评价不良心血管事件发生的重要标志。ZHANG等[21]研究发现,肥胖青少年血液Adropin(一种调节内皮功能的分泌蛋白)水平、微血管反应性充血指数均显著低于正常体质量青少年。另外,动态甲襞毛细血管视频镜评估显示肥胖人群红细胞速度基线和微血管充血后的血流峰值均显著低于正常人[22]。肥胖人群微血管反应性充血能力的下降与感觉神经、内皮源性超极化因子以及腺苷等舒血管因子有关。由于肥胖人群上述因子与调节路径的变化,导致微血流阻断后反应性充血能力下降。 综上,肥胖人群微血管内皮细胞功能受损,导致微血管舒张反应能力下降,使血流灌注不足,增大脂肪肝、心肌缺血、高血压、2型糖尿病等疾病发生风险。但也有少数研究报道,肥胖群体微血管反应性无显著变化。LIMBERG等[23]研究发现,正常、肥胖和代谢综合征群体中微血管内皮依赖性和非内皮依赖性舒张反应均无显著差异。MONTERO等[24]得出相似结论,与正常体质量的青少年相比,肥胖青少年内皮给药乙酰胆碱、硝普钠及局部加热刺激后皮肤微血管的血流峰值无显著变化。导致不同学者间研究结果的差异可能与肥胖人群体内氧化应激、炎症反应水平有关,其中准确的原因有待于进一步研究验证。由于受试者肥胖程度不同,体内氧化应激、炎症反应等水平具有较大差异,导致微血管功能变化上的差异。 2.1.2 运动状态下肥胖人群微血管反应性的变化 运动过程中尤其在大强度运动中肥胖人群微血管反应性明显下降,导致血流灌注不足。FRANCO等[25]研究发现,一次性急性大强度运动显著增加正常体质量男性和肥胖男性前臂微血管反应性,但正常体质量男性运动后不同时段血流量增加的幅度均大于肥胖男性。此外,VINET等[26]研究发现大运动强度期间正常体质量男性和肥胖男性下肢微血管反应性均显著增大,但正常体质量男性高于肥胖男性。大强度运动中肥胖人群微血管反应性的下降对进一步诊断微血管功能的变化有着重要意义。当运动强度或运动量较小时,机体不需要动用最大的血流储备功能满足运动时能量代谢的需求,此时只需要动用部分血流储备能力便能满足运动时能量代谢的需求。虽然肥胖人群微血管反应性下降,但微血管仍具有一定血流储备功能,能满足低强度运动过程中的能量代谢需求,因此微血管并不会表现出明显的功能障碍,微血管反应性的变化与正常体质量的人可能并无显著差别。但当运动强度较大时或最大强度运动时,微血管需要动用最大血流储备能力来满足运动时的能量代谢,但由于肥胖人群微血管反应性下降,运动过程中微血管血流储备能力将低于正常体质量的人,因此血流量的增加幅度小于正常体质量的人。因此,对于肥胖人群运动时微血管反应能力的评价,应尽可能采用大强度运动方案,以准确评估肥胖人群运动时的微血管反应性的变化。但目前该方面的研究成果较少且使用的运动方案差异较大,尚无法形成统一的运动方案,未来应加强该方面的研究,建立成熟可推广的运动方案。 大强度运动过程中微血管血流灌注不足会降低血液与组织细胞间的物质交换,导致肌肉细胞无法获得充足的氧气和能源物质,并使代谢产物在细胞内堆积,诱发运动性疲劳的产生,使运动耐受能力下降。运动耐受能力不仅是评价肥胖人群体质健康的重要指标,且是影响日常体力活动的重要因素。另外,由于肥胖人群运动过程中微血管反应性下降,导致骨骼肌等器官血流灌注不足,诱发组织细胞缺氧,增大不良心血管事件的发生风险。因此,肥胖人群在进行大强度运动前应进行运动耐受能力评估,排除运动过程中可能存在的风险。此外,微血管血流量下降还会影响运动后血液与细胞间的物质交换,导致运动过程中产生的代谢废物在运动后无法及时排除以及组织细胞无法获得充足的氧气、能源物质,加重运动性疲劳的发生。多项研究表明,微血管功能下降是诱发运动性疲劳产生的重要因素,运动后采取恢复方式提高微血管功能可促进运动性疲劳的消除[27-29]。因此,肥胖人群在大强度运动后应采取积极的恢复方式提高微血管反应性,增大血流灌注水平,使运动过程中产生的代谢废物及时排除并为细胞提供充足的氧气、能量物质,进而促进疲劳的消除和身体功能的恢复。 2.2 不同形式运动对肥胖人群微血管反应性的干预效应 见图4。"
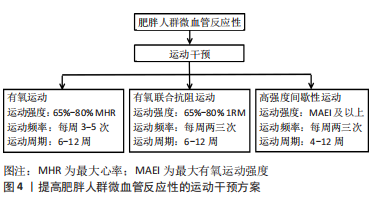

2.2.1 有氧运动对肥胖人群微血管反应性的干预效应 有氧运动是控重减脂的有效方式,并能逆转肥胖人群微血管功能障碍,因此有氧运动是改善肥胖人群微血管反应性的常用运动方式。运动强度是有氧运动干预首要考虑因素。最大心率(Maximal heart rate,MHR)百分比是有氧运动干预中常见的运动强度制定依据。TANG等[8]研究表明,6周运动强度为70%MHR的有氧运动结合饮食干预能有效改善肥胖青少年微血管反应性充血能力。PASQUALINI等[30]研究表明,8周运动强度为65%-80% MHR的有氧训练能显著改善肥胖受试者皮肤微血管反应性和血浆脂联素水平。另外,12周运动强度为60%-80%MHR的有氧运动能显著提高肥胖青少年Adropin水平和微血管反应性充血指数,且Adropin是影响微血管反应性充血指数的独立因素[21]。通过对上述学者研究结果分析,得出60%-80%MHR的有氧运动是改善肥胖人群微血管反应性的有效运动强度,但相关研究对运动强度的制定缺少个体化差异的考虑。虽然相关研究对运动强度进行了量化,但对所有的受试者施加相同的运动强度会忽略受试者之间的差异性,而应根据受试者运动能力和身体机能特点制定个体化、精准化的运动强度。个体最大脂肪氧化强度(Maximal fat oxidation,FATmax)是指单位时间内个体脂肪氧化利用最大化时所对应的运动强度,该运动强度能最大程度促进脂肪分解,达到有效减脂效果[31]。FATmax强度能根据受试者运动能力和身体功能特点制定个体化的运动强度,实现精准运动干预,是运动减肥的最佳运动强度[32]。作者前期的一项研究表明,10周基于FATmax强度的有氧运动能显著改善肥胖大学生微血管反应性,并降低体质量、体脂率、BMI及胰岛素抵抗指数[9]。因此,建议相关研究以FATmax强度的有氧运动为切入点,深入探讨FATmax强度对肥胖人群微血管反应性的干预效应,为精准化运动处方的制定提供证据支撑。对于有氧运动的频率,相关研究主要为每周3-5次[8-9,21,30]。作者团队的一项研究表明,每周3-5次、持续12周有氧运动能提高习惯久坐肥胖大学生微血管反应性,但每周一两次的有氧运动对微血管反应性无显著影响[33]。因此,建议改善肥胖人群微血管反应性的有氧运动频率不低于每周3次,当有氧运动频率低于每周3次时,可能因运动量不足难以对肥胖人群微血管带来积极影响。 对于有氧运动的运动周期,相关研究主要为6-12周[8-9,21,30],该运动周期能显著改善肥胖人群微血管反应性。此外,还有研究得出10个月家庭有氧运动干预能显著降低肥胖青少年BMI、体脂率、高敏c-反应蛋白,提高运动能力和微血管内皮细胞功能[34]。作者认为,虽然更长周期的有氧运动也能显著改善肥胖人群微血管反应性,但随着运动干预时间的延长,应根据受试者运动能力和身体功能的变化增大运动强度,进而对微血管产生新的刺激,以获得新的干预效应。此外单次有氧运动也能对肥胖人群微血管反应性产生积极效应。LAMPRECHT等[35]研究得出,30 min 70%最大摄氧量强度的跑步运动能显著增加肥胖妇女皮肤微血管血流量、血红蛋白相对浓度。另外口服高脂肪食物耐受性试验前一天进行90 min的跑步机行走运动能显著提高肥胖受试者微血管反应性,并降低三酰甘油浓度[36]。因此,当肥胖人群无法坚持长时间运动时,可通过单次有氧运动提高微血管反应性,以获得微血管反应性的短暂性变化,尤其当肥胖人群高脂高糖膳食后应进行适当的有氧运动,以减轻高脂高糖膳食对微血管内皮细胞的损伤。 综上,持续6-12周、每周3-5次、运动强度为60%-80% MHR的有氧运动能显著提高肥胖人群微血管反应性。但也有研究得出,4个月的有氧运动不能提高肥胖人群微血管反应性,需要更高剂量(延长运动周期和增大运动量)的运动干预才能引起微血管反应性的显著变化[24]。因此,未来应重点围绕有氧运动改善肥胖人群微血管反应性的“剂量-效应”关系进行研究,明确不同剂量的运动对肥胖人群微血管反应性的影响,为有氧运动处方的制定提供精准的数据支撑。 2.2.2 抗阻运动及有氧联合抗阻运动对肥胖人群微血管反应性的干预效应 抗阻运动是肌肉克服外来阻力而进行的主动肌肉收缩运动,其阻力包括外部阻力(如运动器械)和自身质量两类。 基于抗阻运动在改善骨骼肌质量、胰岛素敏感性等方面的优势,其已成为减重降脂的重要运动形式[37]。DIAS等[10]研究表明,12周运动强度为10RM的抗阻运动能显著改善肥胖青少年体脂、腰围、腰臀比以及微血管反应性,但受试者的体质量在干预前后未发生显著变化,该研究认为微血管反应能力的变化与体质量无显著关系。虽然体质量是判断肥胖发生的重要指标,但单一体质量的变化并不能客观反映出身体成分变化,骨骼肌含量的增加同样可以引起体质量的改变。因此,体质量的增加可能不是导致微血管反应性下降的关键因素,而体脂率、腰围、腰臀比等指标可能起到更重要的作用,抗阻运动能降低肥胖人群体脂率并提高骨骼肌含量,进而改善微血管功能。但BEIJER等[38]研究得出,6周全身振动训练能显著提高肥胖人群血容量和微血管反应能力,但6周运动强度为80%1RM(每周两三次)的抗阻运动后肥胖人群微血管反应性未发生显著变化。作者认为,上述两项研究结果的差异与运动干预的时间有关。虽然抗阻运动能通过改善骨骼肌质量和功能提高肥胖受试者微血管功能,但由于相同运动时间内抗阻运动中整体能量消耗偏少(较持续性有氧运动),因此需要更长时间的干预才能有效改善身体成分以及提高微血管反应性。有氧联合抗阻运动将有氧运动和抗阻运动结合起来,相同时间内较单一的抗阻运动具有更高的能量消耗,因此对身体成分和微血管功能的干预效果更佳。唐东辉等[11]研究表明,6周有氧联合抗阻运动能调节肥胖青少年微血管平滑肌细胞收缩和舒张,改善微血管内皮细胞障碍。李娟等[39]得出相似研究结论,6周有氧联合抗阻运动65%-70%1RM能显著提高肥胖青少年血管反应性充血能力,并降低体质量、BMI、体脂百分比、胰岛素抵抗指数。因此,以有氧联合抗阻运动作为改善微血管反应性的运动方式,6周可能就具有较好的干预效应,但以抗阻运动为干预方式时则需更长的干预时间。 此外,随着运动干预时间的延长,有氧联合抗阻运动的干预效应可能更佳。作者一项研究表明10周基于FATmax的有氧运动和有氧结合抗阻运动均能改善肥胖大学生微血管反应性,且有氧联合抗阻运动干预效果更佳[9]。另有研究得出,12周有氧运动和有氧联合抗阻运动(70%-85%1RM)均能改善肥胖男性血管舒张功能且有氧联合抗阻运动的效果优于单纯有氧运动[40]。作者认为,随着干预时间的延长有氧联合抗阻运动在改善肥胖人群身体成分(主要通过增加骨骼肌含量和提高骨骼肌功能)较单一的有氧运动更具有优势,因此引起微血管发生更为显著的变化。对于运动强度,65%-85%1RM的抗阻运动具有较好的干预效果[38-40],但随着肥胖人群肌肉功能的提高,应逐渐增加运动强度,以便获得持续性的干预效果。对于运动频率,相关研究主要为每周两三次[10,38-40]。作者认为,当抗阻运动部分的频率低于每周3次,应适当通过增加有氧运动的次数以保证整体的运动量。此外,抗阻运动部分应隔天进行(间隔48 h以上),使肌肉功能在下次训练时得到充分的恢复,以避免身体恢复不足导致运动疲劳甚至运动损伤[41]。 2.2.3 高强度间歇性运动对肥胖人群微血管反应性的干预效应 高强度间歇性训练是短时间高强度运动与短时间间歇性运动交替进行,并不断重复的运动[42]。相比于传统的有氧运动,高强度间歇训练能显著减少运动时间,并存在间歇性的休息期,其不仅具有较好的减重效果,且提高了锻炼者的依从性[43]。运动强度是影响高强度间歇性训练效果的重要因素。有氧运动的强度可分为3个等级,低强度为52%-63%MHR,中等强度为64%-75%MHR,高强度为76%-85%或76%-87%MHR[44]。因此当运动强度达到85%-87% MHR时,机体承受的运动强度为最大有氧运动强度(Maximum aerobic exercise intensity,MAEI)。COCKS等[12]研究表明,4周运动强度为100% MAEI的高强度间歇训练和持续性有氧训练均能显著提高肥胖人群骨骼肌微血管功能,改善胰岛素敏感性,高强度间歇训练是替代长时间持续性训练提高肥胖人群有氧能力、胰岛素敏感性、微血管功能的有效方案。另有研究得出,8周运动强度为100%-110%MAEI的高强度间歇性运动能显著提高肥胖青少年血管舒张功能,并能改善血脂代谢及胰岛素抵抗指数[45]。TJ?NNA等[46]得出类似结论,12周运动强度为90%MHR(约等于103%MAEI)高强度间歇性运动能显著提高肥胖受试者微血管血流速度,降低BMI、脂肪百分比、平均动脉血压以及增加血氧峰值。此外,基于高强度间歇性训练对肥胖人群心肺功能、传统心血管疾病危险因素、氧化应激、炎症反应等更佳的干预效应,有研究认为高强度间歇性训练在改善肥胖人群微血管功能方面可能更具优势。氧化应激损伤、炎症反应等是导致肥胖人群微血管内皮细胞损伤的重要因素,其水平的降低能改善微血管内皮细胞功能,促进内皮舒血管因子释放,进而提高微血管舒张功能。王珅等[47]研究表明,12周运动强度为100%MAEI的高强度有氧间隔训练和有氧运动均能改善肥胖青少年血管舒张功能,但高强度有氧间隔训练干预效果更好。一项Meta分析也表明,高强度间歇性运动在改善血管功能方面比中等强度连续训练更有效[48]。综上,运动强度为MAEI及以上的高强度间歇性运动能显著提高肥胖人群微血管反应性。 对于高强度间歇性训练的频率,相关研究主要为每周两三次[12,45-47]。由于高强度间歇性运动的运动强度较大加之肥胖人群运动耐受能力下降,运动后需要更长的时间才能实现身体功能恢复,因此应严格控制高强度间歇性训练的运动频率,保证下次运动时身体功能已完全恢复,防止在运动过程中因身体疲劳出现运动伤害事故。对于运动周期,COCKS等[12]得出4周的高强度间歇性运动就能显著改善肥胖人群微血管反应性,这可能与高强度间歇性运动较好的减重降脂效果有关。其他学者研究选择的运动周期多为8-12周[45-47],该运动周期能有效改善肥胖人群微血管反应性。但也有研究指出,12周中等强度持续性有氧训练和高强度间歇训练(90%-95%MHR)均能改善肥胖青少年身体成分,并能提高微血管血流量的基线值,但对微血管阻断后反应性充血能力无显著影响[49]。微血管血流量基线值主要与微血管的密度有关,而微血管阻断后反应性充血能力主要与血管舒张因子有关,说明两种运动能促进微血管新生,但不能促进血管舒张因子的释放,其中的原因有待于进一步研究明确。 综上,持续4-12周、每周两三次、运动强度为MAEI及以上的高强度间歇性运动能改善肥胖人群微血管反应性,但由于相关研究的成果仍较少,因此需进一步研究明确高强度间歇性运动对肥胖人群微血管反应性的干预效应。此外,由于肥胖人群运动能力与心血管的耐受能力已出现下降,建议进行高强度间歇性训练前应先进行一定时间的有氧运动干预以提高运动耐受能力和心血管功能,为高强度间歇性训练提供体能基础。 2.3 运动改善肥胖人群微血管反应性的主要机制 见图5。"
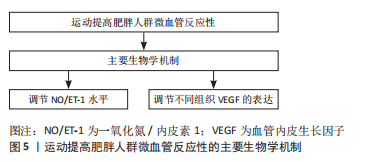

2.3.1 调节NO/ET-1的平衡 NO是一种气体血管扩张因子,能使血管产生舒张反应。ET-1是最强的血管收缩因子,能引起血管产生强烈的收缩反应。正常情况下,NO和ET-1的动态平衡是维持微血管正常舒缩功能的主要原因。肥胖人群血清NO水平下降,ET-1水平升高,导致微血管舒张功能下降。TODA等[50]研究表明,肥胖人群eNOS活性和表达能力下降,导致NO生成减少,同时超氧阴离子、二甲基精氨酸和ET-1生成增加,诱发微血管内皮舒张功能障碍。唐东辉等[11]得出相似结论,肥胖青少年循环系统中NO水平降低、ET-1水平增高,导致NO/ET-1失衡诱发微血管内皮功能障碍。肥胖人群血清NO/ET-1失衡与氧化应激、炎症反应以及胰岛素抵抗等因素有关。肥胖常伴随全身慢性低度炎症,且患者氧化应激水平上升。慢性炎症反应使大量中性粒细胞黏附于内皮细胞,阻塞微血管,同时炎症递质还导致微血管内皮细胞通透性增大以及破坏血管的基底膜,加重微血管内皮细胞功能障碍,降低内皮细胞释放NO的能力[51]。当氧化应激水平增高时,自由基抑制eNOS的表达,降低NO的生成,自由基还与NO结合,导致NO降解。此外,当肥胖人群出现胰岛素抵抗后,微血管反应性也会下降。胰岛素能刺激血管产生NO,增加骨骼肌血流灌注量,提高骨骼肌摄取葡萄糖的能力,胰岛素抵抗会抑制eNOS激活,减少NO的生成,同时增强ET-1的血管收缩效应[12,18]。 综上,肥胖人群机体NO/ET-1水平失衡是导致微血管反应性下降的重要原因,而炎症反应、氧化应激损伤、胰岛素抵抗与NO/ET-1水平失衡有着密切关系。运动能调节肥胖人群NO、ET-1水平,提高微血管反应性。唐东辉等[11]研究表明,运动能降低肥胖青少年ET-1的表达,增加血清NO水平,改善微血管功能。周术锋等[33]研究表明,运动能通过调节习惯久坐肥胖大学生血清NO、ET-1水平提高微循环功能。作者一项研究表明,运动能通过改善NO、ET-1等因子水平提高肥胖大学生微循环功能[9]。综上,运动可能通过调节肥胖人群NO、ET-1水平提高微血管反应性,因此在制定改善肥胖人群微血管反应性的运动方案中,应重点关注受试者血清NO、ET-1水平的变化。此外,炎症反应、氧化应激损伤及胰岛素抵抗是导致NO/ET-1水平失衡的重要因素,因此还应进一步关注肥胖人群炎症反应、氧化应激水平及胰岛素抵抗的变化,以便精准判断运动对微血管功能的干预效应。 2.3.2 调节血管内皮生长因子(Vascular endothelial growth factor,VEGF)的表达 VEGF是一种特异的、强烈的血管内皮细胞促分裂因子和血管生成因子,具有促进血管内皮细胞增殖、增加血管通透性、促进血管支持物的形成等作用[52-53]。肥胖人群VEGF表达异常,但不同组织中VEGF的变化特点不同。在白色脂肪组织中,VEGF表达增强。体质量增加会导致白色脂肪组织扩张以及代谢需求增大,为了满足机体代谢的需求,需要靠血管和淋巴管生成为组织提供更多的血流量,而血管生长过程依赖于VEGF及其家族成员的表达。研究发现,肥胖受试者脂肪组织中VEGF、VEGF-c、VEGF-d、可溶性VEGF受体2、血管生成素2和内皮抑素均显著升高,且与BMI呈正相关[54]。白色脂肪组织中VEGF表达上调与脂肪组织的缺氧有关,缺氧能上调缺氧诱导因子1α mRNA和蛋白表达,促进VEGF的表达。VEGF表达会促进脂肪组织微血管密度新生,为脂肪组织的扩充和生长提供氧气和能量物质,加剧肥胖的发生。运动能下调白色脂肪组织VEGF表达能力,降低白色脂肪组织微血管的增生能力,进而抑制白色脂肪组织的扩充和生长[55]。与白色脂肪组织不同,肥胖人群肌肉组织VEGF表达能力下降,导致微血管稀疏,诱发骨骼肌血流灌注障碍。刘雨佳等[56]研究表明,肥胖降低骨骼肌VEGF表达能力,诱导大鼠骨骼肌毛细血管稀疏的发生。张靓等[57]得出相似结论,肥胖使比目鱼肌VEGF表达能力下降,毛细血管生成受阻。肥胖诱导骨骼肌VEGF表达能力下降与骨骼肌代谢水平下降、胰岛素抵抗等因素有关。微血管主要功能是负责组织细胞与血液的物质能量交换,其功能与机体的物质能量代谢水平相匹配。伴随着骨骼肌代谢水平下降,微血管可能出现萎缩,导致血管稀疏的发生。 此外,当肥胖人群出现胰岛素抵抗后,微血管功能会进一步下降。胰岛素能特异性通过胰岛素受体和激活PI3K/Akt通路调控VEGF基因表达,提高心肌组织的毛细血管密度,而胰岛素抵抗能选择性抑制该通路使VEGF表达能力下降和毛细血管密度降低[58]。因此,提高骨骼肌VEGF表达能力能促进微血管新生,提高微血管血流灌注水平。运动干预能增强骨骼肌VEGF的表达能力,逆转肥胖诱导的骨骼肌微血管稀疏。刘雨佳等[56]研究表明,8周有氧运动训练能激活骨骼肌内的AMPK,促进eNOS合成,增强VEGF的表达能力,促进微血管新生,改善肥胖诱导的微血管稀疏。另有研究发现,肥胖导致骨骼肌毛细血管稀疏,运动能恢复MiRNA-126水平和VEGF信号通路,逆转微血管稀疏[59]。AHN[60]、SHIN等[61]得出相似结论。作者一项研究表明,运动干预能提高肥胖大学生NO/ET-1、VEGF等因子水平,改善微血管功能[9]。 综上,肥胖人群白色脂肪组织扩张导致脂肪中VEGF表达增加,使白色脂肪组织微血管增生,而肌肉组织VEGF表达能力降低,导致肌肉中微血管稀疏,有氧运动能降低白色脂肪中的VEGF的表达,上调肌肉组织中VEGF表达,改善微血管功能。因此,在运动干预过程中应关注肥胖人群不同组织的VEGF水平,以精准判断不同组织微血管功能的变化。"

| [1] 中国营养学会肥胖防治学组、中国营养学会临床营养学组、中国预防医学会行为健康学组等.中国居民肥胖防治专家共识[J].中国预防医学杂志,2022,23(5):321-339. [2] 王亮亮,黄瑜,郭伟,等.肥胖和中心性肥胖对高血压的交互作用分析[J].预防医学,2022,34(2):129-134. [3] 刘烨,王海宁.2021年ADA/EASD《糖尿病缓解专家共识》与《2022年ADA糖尿病指南:2型糖尿病的预防和治疗中肥胖与体重管理》解读——糖尿病缓解的定义与治疗策略[J].临床内科杂志,2022, 39(5):299-302. [4] 柯居中,刘晓琳,吴抗,等.社区居民肥胖、中心性肥胖与冠心病发病风险的前瞻性队列研究[J].现代预防医学,2020,47(7):1310-1314. [5] 陈燕子,刘莉,付晓丽,等.肥胖与癌症的关系的知识图谱分析[J].中华疾病控制杂志,2016,20(6):604-608. [6] 陈浩,龚涛,王晓霞,等.中国多学科微血管疾病诊断与治疗专家共识[J].中国循环杂志,2020,35(12):1149-1165. [7] GRAUPERA M, CLARET M. Endothelial cells: new players in obesity and related metabolic disorders. Trends Endol Metab. 2018;29(11):781-794. [8] TANG DH, BAI S, LI XL, et al. Improvement of microvascular endothelial dysfunction induced by exercise and diet is associated with microRNA-126 in obese adolescents. Microvasc Res. 2019;123:86-91. [9] 肖哲,朱欢,胡江平,等.10周有氧运动和有氧结合抗阻运动对肥胖大学生微循环功能的影响及机制研究[J].中国全科医学,2022, 25(19):2349-2355+2362. [10] DIAS I, FARINATTI P, DE SOUZA MG, et al. Effects of resistance training on obese adolescents. Med Sci Sports Exerc. 2015;47(12):2636-2644. [11] 唐东辉,侯玉洁,杨东升,等. 有氧运动结合抗阻训练对肥胖青少年微血管内皮功能的影响[C]//第四届(2016)全国运动生理与生物化学学术会议——运动·体质·健康论文摘要汇编[G].2016:56-57. [12] COCKS M, SHAW CS, SHEPHERD SO, et al. Sprint interval and moderate-intensity continuous training have equal benefits on aerobic capacity, insulin sensitivity, muscle capillarisation and endothelial eNOS/NAD(P)hoxidase protein ratio in obese men. J Physiol. 2016;594(8):2307-2321. [13] 唐元梁,李桂香,姚立平,等.皮肤微血管调节功能无创检测技术进展[J].中国医疗设备,2022,37(6):153-157. [14] LA FAVOR JD, DUBIS GS, YAN H, et al. Microvascular endothelial dysfunction in sedentary, obese Humans is mediated by NADPH oxidase: influence of exercise training. Arterioscler Thromb Vasc Biol. 2016;36(12):2412-2420. [15] KWAIFA IK, BAHARI H, YONG YK, et al. Endothelial dysfunction in obesity-induced inflammation: molecular mechanisms and clinical implications.Biomo. 2020;10(2):291-311. [16] 邓林华,温玉,张运娇,等.血管内皮功能障碍与高血压关系的研究进展[J].中华高血压杂志,2021,29(10):935-940. [17] PIENAAR PR, MICKLESFIELD LK, LEVITT NS, et al. Insulin resistance is associated with lower acetylcholine-induced microvascular reactivity in nondiabetic women. Metab Syndr Relat Disord. 2014;12(3):178-184. [18] MURIS DM, HOUBEN AJ, SCHRAM MT, et al. Microvascular dysfunction: an emerging pathway in the pathogenesis of obesity-related insulin resistance. Rev Endocr Metab Disord. 2013;14(1):29-38. [19] 沈英华,傅汉菁,赵静.糖尿病患者足部皮肤反应性充血在三种血流阻断压力下的变化[J].微循环学杂志,2009,19(2):36-37+40+ 77+80. [20] 朱欢,高炳宏.微血管反应性在耐力性运动员训练中的应用[J].中国运动医学杂志,2019,38(10):907-914. [21] ZHANG H, JIANG L, YANG YJ, et al. Aerobic exercise improves endothelial function and serum adropin levels in obese adolescents independent of body weight loss. Sci Rep. 2017;7(1):17717-17724. [22] MARANHãO PA, DE SOUZA MD, KRAEMER-AGUIAR LG, et al. Dynamic nailfold videocapillaroscopy may be used for early detection of microvascular dysfunction in obesity. Microvasc Res. 2016;106:31-35. [23] LIMBERG JK, HARRELL JW, JOHANSSON RE, et al. Microvascular function in younger adults with obesity and metabolic syndrome: role of oxidative stress. Am J Physiol Heart CircPhysiol. 2013;305(8): H1230-H1237. [24] MONTERO D, WALTHER G, PEREZ-MARTIN A, et al. Effects of a lifestyle program on vascular reactivity in macro- and microcirculation in severely obese adolescents. J Clin Endocrinol Metab. 2014;99(3):1019-1026. [25] FRANCO RL, FALLOW BA, HUANG CJ, et al. Forearm blood flow response to acute exercise in obese and non-obese males. Eur J Appl Physiol. 2013;113(8):2015-2023. [26] VINET A, KARPOFF L, WALTHER G, et al. Vascular reactivity at rest and during exercise in middle-aged obese men: effects of short-term, low-intensity, exercise training. Int J Obes (Lond). 2011;35(6):820-828. [27] 张昊楠,高炳宏,朱欢.男子赛艇运动员赛前6周训练微循环血流储备能力与相关生化指标的关系[J].中国应用生理学杂志,2017, 33(2):112-116+120. [28] 董徽徽,高炳宏,朱欢.下肢间歇负压疗法对优秀赛艇运动员股四头肌皮肤微循环血流灌注量的急性效应[J].南京体育学院学报, 2019,2(9):47-52. [29] 田广,高炳宏,朱欢.下肢间歇负压对优秀男子跆拳道运动员微循环功能的急性干预效应[C]//.第十二届全国体育科学大会论文摘要汇编——墙报交流(运动训练分会) [G].2022:74-75. [30] PASQUALINI L, SCHILLACI G, INNOCENTE S, et al. Lifestyle intervention improves microvascular reactivity and increases serum adiponectin in overweight hypertensive patients. Nutr Metab Cardiovasc Dis. 2010; 20(2):87-92. [31] 孔凡明,朱苗苗,米靖,等.运动与脂肪氧化动力学特征的应用启示[J].中国组织工程研究,2022,26(29):4709-4715. [32] 李盈盈,黄丽,彭莉.肥胖女大学生最大脂肪氧化强度研究[J].中国学校卫生,2021(9):1407-1410+1414. [33] 周术锋,肖哲,朱欢,等.12周有氧运动对习惯久坐大学生微循环功能的影响[J].中国学校卫生,2021,42(9):1332-1335+1339. [34] BRUYNDONCKX L, HOYMANS VY, DE GUCHTENAERE A, et al. Diet, exercise, and endothelial function in obese adolescents. Pediatrics. 2015;135(3):e653-e661. [35] LAMPRECHT M, OBERMAYER G, STEINBAUER K, et al. Supplementation with a juice powder concentrate and exercise decrease oxidation and inflammation, and improve the microcirculation in obese women: randomised controlled trial data. Br JNutr. 2013;110(9):1685-1695. [36] GILL JM, Al-MAMARI A, FERRELL WR, et al. Effects of prior moderate exercise on postprandial metabolism and vascular function in lean and centrally obese men. J Am Coll Cardiol. 2004;44(12):2375-2382. [37] 胥祉涵,王世强,李丹,等.2022年美国运动医学会《2型糖尿病患者的运动/身体活动指南》解读及启示[J].中国全科医学,2022, 25(25):3083-3088. [38] BEIJER Å, DEGENS H, WEBER T, et al. Microcirculation of skeletal muscle adapts differently to a resistive exercise intervention with and without superimposed whole-body vibrations. Clin Physiol Funct Imaging. 2015;35(6):425-435. [39] 李娟,唐东辉,陈巍.有氧运动结合抗阻训练对男性肥胖青少年心血管功能的改善及可能机制[J].体育科学,2013,33(8):37-42. [40] 赵军,梁晋裕.有氧运动结合抗阻训练对肥胖男性大学生身体成分、心血管功能及血清C反应蛋白水平的改善作用[J].吉林大学学报(医学版),2019,45(5):1134-1140. [41] 中国2型糖尿病防治指南(2017年版)[J].中国实用内科杂志,2018, 38(4):292-344. [42] 孙文新,秦曼,李丽丽,等.高强度间歇训练对超重肥胖女大学生减脂效果的Meta分析[J].中国学校卫生,2021,42(10):1480-1486. [43] 高靖波. HIIT对大学生自行车运动员专项运动能力影响的实验研究[D].呼和浩特:内蒙古师范大学,2022. [44] 王成浩,何辉,熊开宇.不同强度有氧运动对中高度近视女大学生眼压的影响[J].中国学校卫生,2019,40(8):1254-1257. [45] 魏胜敏,高前进,王二利.高强度间歇训练对肥胖青年血清adropin水平和血管内皮功能的影响[J].中国康复医学杂志,2019,34(9): 1058-1064. [46] TJøNNA AE, STøLEN TO, BYE A, et al. Aerobic interval training reduces cardiovascular risk factors more than a multitreatment approach in overweight adolescents. Clin Sci (Lond). 2009;116(4):317-326. [47] 王珅,廖静雯,黄俊豪,等.高强度有氧间隔训练对肥胖青少年血管内皮功能的影响及机制[J].山东医药,2018,58(20):45-47. [48] RAMOS JS, DALLECK LC, TJONNA AE, et al. The impact of high-intensity interval training versus moderate-intensity continuous training on vascular function: a systematic review and meta-analysis. Sports Med. 2015;45(5):679-692. [49] MORRISSEY C, MONTERO D, RAVERDY C, et al. Effects of exercise intensity on microvascular function in obese adolescents. Int J Sports Med. 2018;39(6):450-455. [50] TODA N, OKAMURA T. Obesity impairs vasodilatation and blood flow increase mediated by endothelial nitric oxide: an overview. J Clin Pharmacol. 2013;53(12):1228-1239. [51] 罗丽珊,孙嘉.微循环障碍相关细胞信号通路的研究进展[J].微循环学杂志,2013,23(1):67-70. [52] 朱欢,高炳宏.有氧运动对人体微血管反应性的作用及机制研究进展[J].生命科学,2020,32(8):855-863. [53] 王成科,朱欢,董徽徽,等.运动对高血压患者微血管反应性的干预效应及可能机制研究进展[J].中国预防医学杂志,2021,22(9): 726-731. [54] SILHA JV, KRSEK M, SUCHARDA P, et al. Angiogenic factors are elevated in overweight and obese individuals. Int J Obes (Lond). 2005; 29(11):1308-1314. [55] AHMADI-KANI GOLZAR F, FATHI R, MAHJOUB S. High-fat diet leads to adiposity and adipose tissue inflammation: the effect of whey protein supplementation and aerobic exercise training. Appl Physiol Nutr Metab. 2019;44(3):255-262. [56] 刘雨佳,梅婷,陈瞳. AMPK/PGC-1α/VEGF通路在运动训练调节肥胖大鼠骨骼肌毛细血管生成中的作用[C].第十二届全国体育科学大会论文摘要汇编——墙报交流(运动生理生化分会)[G]. 2022:215-216. [57] 张靓,马谨,陈雪飞,等.跑台运动对肥胖大鼠比目鱼肌毛细血管生成及apelin表达的影响[J].中国运动医学杂志,2017,36(5):383-389. [58] 李靖.跑台运动通过增加MicroRNA-126改善高脂饮食诱导的肥胖大鼠血运重建[J].井冈山大学学报(自然科学版),2018,39(1):95-101. [59] HE Z, OPLAND DM, WAY KJ, et al. Regulation of vascular endothelial growth factor expression and vascularization in the myocardium by insulin receptor and PI3K/Akt pathways in insulin resistance and ischemia. Arterioscler Thromb Vasc Biol. 2006;26(4):787-793. [60] AHN N, KIM K. Effects of Aerobic and Resistance Exercise on Myokines in High Fat Diet-Induced Middle-Aged Obese Rats. Int J Environ Res Public Health. 2020;17(8):2685-2695. [61] SHIN KO, BAE JY, WOO J, et al. The effect of exercise on expression of myokine and angiogenesis mRNA in skeletal muscle of high fat diet induced obese rat. J Exerc Nutrition Biochem. 2015;19(2):91-98. |
| [1] | Ke Weiqiang, Chen Xianghui, Chen Xiaoling, Meng Jie, Ma Yanlin. Rituximab combined with autologous peripheral blood stem cell transplantation in the treatment of diffuse large B-cell lymphoma and the expression of related factors [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(6): 915-920. |
| [2] | Wang Lijuan, Liu Guobin, Han Qiuqin, Zhao Zhihong, He Jinjing, Li Wenhui. Protective effect of ethanol extract of Zizhu on vascular endothelial cell injury induced by high glucose and high lipids [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(26): 4132-4138. |
| [3] | Wang Wenbo, Xu Jingzhi, Wu Liang, Xi Kun, Xin Tianwen, Tang Jincheng, Gu Yong, Chen Liang. In vitro experiment of composite nanofibrous periosteum to promote vascularization and osteogenic mineralization [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(25): 4028-4037. |
| [4] | Tang Juan, Yu Donglin, Liu Guoqi, Song Jiaojiao, Zuo Jinhua, Fu Honghai. Osteogenic and angiogenic differentiation of dental pulp stem cells modified by hypoxia-inducible factor-1 alpha gene in vitro [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(24): 3865-3870. |
| [5] | Li Gang, Song Yun, Liang Guoguang. Wenyang Tongluo capsule intervenes with inflammation and angiogenesis in rat osteoarthritic chondrocytes [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(23): 3682-3692. |
| [6] | Xie Pingjin, Luo Zhen, Lu Qigui, Guo Yanxing, Chen Qunqun, Li Feilong. Effect of ligustrazine and overexpression of miR-20b-5p on synovial, cartilage and subchondral bone angiogenesis in rats with early-stage knee osteoarthritis: a histological observation [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(2): 237-245. |
| [7] | Niu Zihan, Yu Yang, Ai Jiang, Bu Panpan, Li Wenbo, Suriye·Reheman, Ma Shaolin. Total flavonoids of Hippophae rhamnoides L. interfere with the regression of hypertrophic scar tissue blocks in a rabbit ear model [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(2): 258-263. |
| [8] | Wang Baojuan, Zheng Shuguang, Zhang Qi, Li Tianyang. Miao medicine fumigation can delay extracellular matrix destruction in a rabbit model of knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1180-1186. |
| [9] | Wang Qin, Shen Cheng, Liao Jing, Yang Ye. Dapagliflozin improves renal injury in diabetic nephropathy rats [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1216-1222. |
| [10] | Lyu Zichen, Tu Zhenxing, Xu Ao, Cheng Kang, Wang Hongtao, Wang Bin. Mechanism of bone healing and angiogenesis during distraction osteogenesis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(36): 5881-5888. |
| [11] | Yu Yunbao, Chen Lin, Wu Xiya, Yan Lerong, Miao Zhang, Man Yang, Jing Renyi, Lei Zhen, Chu Zhiqiang, Zhang Hongwei. Vascular endothelial growth factor-Notch signaling pathways in endothelial precursor cells in promoting the transformation of bone marrow mesenchymal stem cells into hepatocyte-like cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(31): 4946-4953. |
| [12] | Zhao Xinxin, Yang Xiaoqing, Zhang Yuquan. Umbilical cord mesenchymal stem cells improve pregnancy outcomes of spontaneous abortion mouse models by promoting vascular endothelial growth factor expression in decidua [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(30): 4793-4799. |
| [13] | Zhao Dun, Fang Bin, Yi Chunzhi, He Mincong, Zheng Jiaqian, Li Yue. Effects of total flavonoids of Rhizoma drynariae on bone remodeling and expression of bone morphogenetic protein-2, vascular endothelial growth factor and CD31 [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(29): 4638-4642. |
| [14] | Lu Qigui, Xie Pingjin, Luo Zhen, Li Feilong, Chen Qunqun, Chai Shengting. MicroRNA-20b-5p effects on cartilage and subchondral bone angiogenesis in early-stage osteoarthritis rats [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(29): 4658-4665. |
| [15] | Yu Xiaofan, Jiang Huijiao, Tan Xiaowu, Wu Xiangwei. Expression of vasohibin-1 and other factors after the co-culture of two kinds of Echinococcus granulosus protoscolex and endothelial progenitor cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(24): 3892-3896. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||