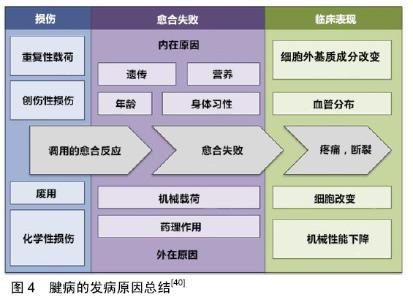
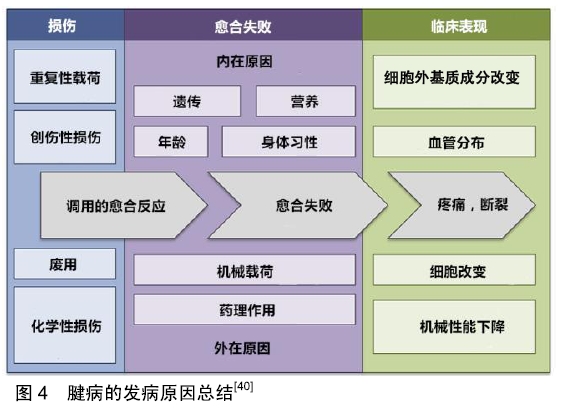
Chinese Journal of Tissue Engineering Research ›› 2020, Vol. 24 ›› Issue (2): 282-288.doi: 10.3969/j.issn.2095-4344.1917
Previous Articles Next Articles
Tendinopathy: debate on concepts and pathogenesis
Liu Chunyu1, Han Xiaoyan2, Wang Lin1
- 1Beijing Sport University, Beijing 100084, China; 2School of Physical Education and Health, Yulin 537000, Guangxi Zhuang Autonomous Region, China
-
Received:2019-04-13Revised:2019-04-29Accepted:2019-06-12Online:2020-01-18Published:2019-12-25 -
Contact:Wang Lin, Professor, Doctoral supervisor, Beijing Sport University, Beijing 100084, China -
About author:Liu Chunyu, Doctoral candidate, Associate professor, Beijing Sport University, Beijing 100084, China
CLC Number:
Cite this article
Liu Chunyu, Han Xiaoyan, Wang Lin. Tendinopathy: debate on concepts and pathogenesis[J]. Chinese Journal of Tissue Engineering Research, 2020, 24(2): 282-288.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
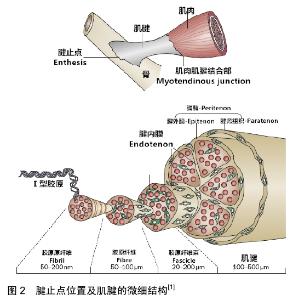
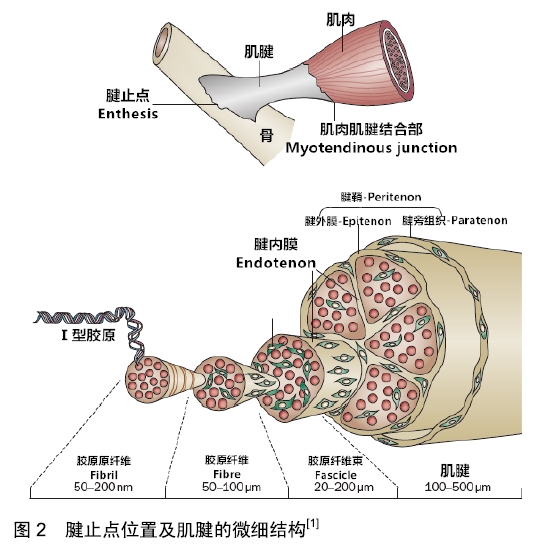
2.1 腱病概念与名词方面的争论 2.1.1 腱病的发生部位与微细结构 肌肉通过肌腱与骨骼连接起来,通过腱止点固定在骨骼上,肌腱主要由Ⅰ型胶原纤维构成,包括胶原纤维束、胶原纤维、胶原原纤维等逐层分级的组织结构。胶原纤维被认为是肌腱的基本力学传递单位,密集排列在肌腱的细胞外基质内,见图2[1]。有学者指出,用于描述上述结构的术语如胶原原纤维、胶原纤维与胶原纤维束,以及腱内膜、腱外膜与腱鞘等所指部位经常容易发生混淆[2]。肌腱插入骨骼的部位称为Enthesis,一般译作附丽区、或腱止点,与骨腱结合部所描述的部位相同。腱病可发生在肌腱中部或腱止点,发生在肌腱中部的腱病又称为非插入性腱病,一般包括腱周炎、腱鞘炎等[3],而发生在腱止点部位的腱病因为发生于肌腱插入骨骼的位置,故又称为插入性腱病,即末端病。 "

2.1.2 腱病相关概念 英文中用于描述腱病的术语包括:Tendinitis、Tendinosis、Enthesiopathy和Tendinopathy,概念较多且容易混乱。“Tendonitis”可译为肌腱炎,最早被用来描述慢性疼痛性肌腱症状,这一概念暗示存在炎症状态作为主要疾病过程[4-5],描述的是一种以肌腱炎症为特征并伴有肌腱变性和血管破裂的病症;通常也可定义为周围组织发炎,如腱周炎与腱鞘炎,特点是积液和肿胀,炎性细胞浸润,腱周组织增厚,有时与正常肌腱组织发生粘连,其病情并不一定会发展为退化或不愈合状态,并且通常可以用休息、物理治疗或非类固醇抗炎药来进行治疗[6-7]。“Tendinosis”则被定义为一种无炎症存在的退行性改变,一般译作肌腱退化,这是一种失败的愈合反应,伴随着肌腱细胞外基质的退变与合成的失衡[8],宏观上,肌腱发生黏液样变性,并且外观由白色变成灰褐色且无光泽[9];组织学上,胶原成分异常,Ⅲ型与Ⅰ型胶原的比例显著高于正常,此外还包括胶原纤维排列紊乱、长度不均、直径减小等组织学表现,新生血管形成增加并内向生长,纤维间有糖胺聚糖成分(GAGs)增加,有时还有肌腱钙化的出现[10]。 “Enthesiopathy”一般译作腱止点病或末端病,但是通常较多的用于风湿病学描述的一个专业术语。“Tendinopathy”译为肌腱病,是一个用来描述肌腱功能障碍及其病理学基础的比较宽泛的术语,事实上从现有的研究看,腱病病理过程中炎症过程是否存在仍然有很大的争议,生物退化的过程可能在其中占主导地位。因此,使用“Tendinopathy”一词似乎更为可取,它能更好地描述肌腱遭受的一系列生物和结构重排的深刻过程[4,11]。 2.2 腱病中是否存在炎症的争论 2.2.1 肌腱急性损伤愈合过程中的炎症表现 广义的肌腱病包含着急性与慢性2种类型,为了更好地理解慢性腱病的病理过程,有必要先了解一下肌腱组织在急性损伤或手术后的愈合过程。肌腱组织与骨骼肌的情况类似,愈合过程主要来自于修复过程,而在修复过程中不可避免的会伴随着炎症的出现,表现为或多或少的瘢痕区域形成,其结构和功能特性弱于原始组织。另外,与骨骼肌相比,肌腱组织的自我修复能力较低,这可能主要是由于肌腱组织血运较少而导致的[12]。肌腱修复的过程一般可以分为炎症期、增生期与重塑期3个连续的阶段,而这3个分期之间并不存在时间上的明确界限[13]。 炎症期也称为渗出期,开始于急性损伤后即刻,一般可持续到伤后第4-7天。作为对于结构损伤的生理反应,血管网损伤后,血浆和组织液在受伤区域内溢出。存在于受损区域中的血小板与通过创伤暴露的胶原相关联并释放磷脂,进而刺激凝血机制[13]。大约在伤后1 h后,可以在受伤区域观察到纤维蛋白和纤维连接蛋白,它们与受伤的胶原纤维形成交联[14],进而形成一种细小的胶状结构,它起到一种类似“软木”的作用,尽管在结构上仍然很脆弱,但这种机制对受损的肌腱纤维维持其自身的拉伸强度起到重要的支撑作用。伤后几小时后,受损区域的白细胞开始迁移,出现大量多形核细胞和单核细胞。这种细胞浸润主要发生在创伤后的前24 h,并持续二三天[13]。炎症期的主要任务之一是从受伤区域清除坏死组织和废物,只有在这些被移除后或者在受伤后5-7 d,增殖期才可能完全开始,炎症过程的消退最终由成纤维细胞活性调节[15],有研究表明,炎症期对于肌腱整个愈合过程的成败是至关重要的[16]。 增殖期从伤后1周左右开始到第4-6周结束,开始于损伤区域内成纤维细胞和内皮细胞的积累[17]。血小板和巨噬细胞产生的生长因子的存在促进了这些细胞的迁移和增殖过程[13]。新生毛细血管在此阶段开始增殖,并开始与原有的毛细血管网络发生功能上的联系。在增殖期,来源于损伤肌腱本身、或者来源于腱外膜、腱鞘或者腱周组织的成纤维细胞表现出很强的增殖与合成细胞外基质的活性。碱性成纤维生长因子在受损区域内的细胞增殖和血管分布方面起重要作用[18]。新生毛细血管成纤维细胞与肌成纤维细胞和细胞外基质之间的相互作用为肉芽组织的产生提供了条件,而在炎症阶段的早期形成的类似“软木”的胶状物质被更稳定的结构取代。同时,纤连蛋白使成纤维细胞可以更好的迁移和黏附。在增殖期的初始阶段,或者说从损伤的大约第7天开始,成纤维细胞就开始产生用于组装细胞外基质(主要是透明质酸)和Ⅲ型胶原蛋白的糖胺聚糖,即使直到损伤后第3周才能观察到胶原合成的明显增加。而且,新形成的胶原纤维既不具有一致的组织结构,也不具有清晰的解剖学取向。增殖期的最后阶段可以观察到Ⅰ型胶原蛋白的产生,这种情况一直持续到重塑期结束[19]。更坚实的Ⅰ型胶原从第12-14天开始逐渐替代相对脆弱的Ⅲ型胶原,同时肉芽组织进一步成熟,瘢痕形成并呈现其坚实结构,与此同时,血管内皮生长因子的大量释放有助于新血管和肉芽组织的形成。转化生长因子β在炎症和增殖期都很活跃,它可以促进细胞外基质的沉积及改善瘢痕组织的形成[20],增殖期持续3-6周,然后逐渐被重塑期取代。 重塑期在时间上是较长的一个,有报道称达到完全愈合甚至需要1年的时间[13]。在重塑阶段,巨噬细胞、成纤维细胞和毛细血管的数量以缓慢和渐进的方式减少,同时也伴随着合成活性的下降,从第10周开始,正常肌腱组织逐步替换瘢痕纤维组织。此外,糖胺聚糖的量缓慢减少并改变其自身的分布方式,肌腱胶原蛋白的结构致密性变得不那么致密,并且主要由Ⅰ型胶原蛋白组成,生物力学性能得到提高[21]。胶原蛋白的完全成熟和纤维的完全重新排列通常需要五六个月的时间。在重塑期结束时,成纤维细胞停止其生物合成活性,将其自身转化为纤维细胞。胶原纤维的成熟和重建有利于更好的组织形成。尽管如此,肌腱的再生并不能完全恢复到损伤之前的状况,局部组织玻璃样变、胶原直径改变、纤维丝变细等永久性改变最终造成了肌腱力量和抗拉性均降低,肌腱的拉伸强度可能会降低30%以上[22]。以上变化的机制主要是由蛋白水解过程造成的,蛋白质的活性是组织生长和维持所必需的生物成分,损伤后,蛋白水解对于去除受损基质和瘢痕区重塑都是必要的[23]。肌腱急性损伤后修复期的主要分子与基质改变规律总结如表1所示。 "

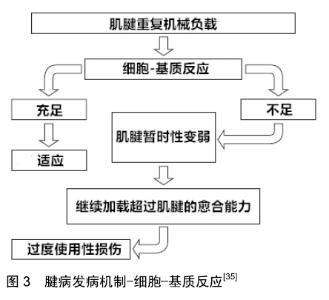
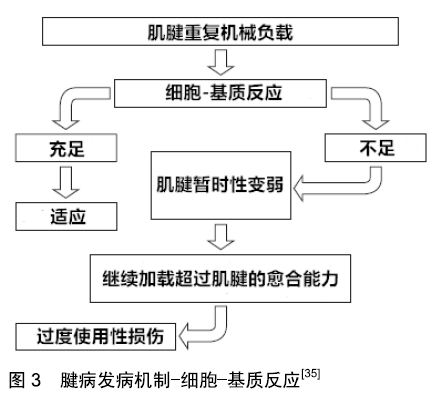
2.2.2 慢性腱病中是否存在炎症的争论 而关于慢性腱病的病理过程中是否存在着炎症,如前所述,一直以来有很多争论,大体上可以分为4个时期:①20世纪90年代之前,“肌腱炎”时期,这一时期认为炎症是其主要病理改变,这也就是为什么在其名称tendinitis中带有表示炎症的后缀“-itis”的原因。这一观点被当时的医学界广泛接受,治疗方法主要是以非类固醇抗炎药及糖皮质激素为主[6,8,25];②20世纪90年代时期,抛弃“肌腱炎”的概念,在这一时期,越来越多的研究者发现,慢性腱病的病变区域,并没有急性炎症应有的典型细胞出现,也没有炎症浸润,组织学特点更符合退行性变化的特征。因此KHAN等[6]提出了应该抛弃“肌腱炎”这一称呼,用全新的视角看待慢性腱病[26-27];③21世纪的头十年,对于非炎症退行性变这一时期,研究者通常以非炎症性或者叫做退行性改变的理论来解释腱病,在此基础上很多相关的理论模型被提出,包括积累性损伤及血管功能不全[8]、愈合反应失败等[28]。这些理论与退行性理论一样影响力巨大。这一时期主要的治疗方式包括理疗(如离心运动)和血小板富集血浆注射等;④最近这10年间,对于该病的治疗疗效并没有取得明显的突破,于是研究者们开始反思,炎症反应到底没有参与到腱病的发生过程中?越来越多的研究者认为,无论是用退行性改变或者是炎症来解释所有腱病一样都是不明智的。有部分学者提出末端病可以分为2个阶段,早期的炎症反应期及随后的退化期[29]。还有其他研究人员坚持腱病是一种退化现象而没有炎症反应[30]。这两种观点都缺乏足够的证据支持。因为在腱病的发病过程中即便没有在某一特定时间点上观察到炎症,但这并不代表炎症没有参与。 有学者指出腱病是一种活化的细胞反应,而不是炎症反应[31]。在疾病的初始阶段,服用非类固醇类和皮质类固醇等抗炎药物可能是有益的。然而,这不是因为它们本身的抗炎特性,而是因为它们在一定程度上抑制了细胞的反应性。COOK等[28]指出腱病中可能存在“某种形式的炎症”,但细节尚不清楚。同样有学者认为重复性的载荷会导致微细损伤的发生,持续下去可能会导致慢性炎症、组织退变及重建等结果[32]。到目前为止,虽尚未就炎症在腱病中的确切作用达成最终共识,但大部分作者倾向认为腱病总体上属于退行性变[4-5],但在病变早期存在着一些不典型的或者亚炎症反应过程[33],进而认为它是微细损伤和退行性变共同作用的结果。 2.3 腱病的病理机制与分期 与光泽、白色和坚硬的正常肌腱相比,腱病在组织病理学上表现为暗淡、灰色和易碎的外观,是退化过程的典型特征[34];在显微镜下,胶原纤维破坏及分型比例改变,血管分布和细胞增加,基质增加,纤维软骨化生等。虽然目前关于与腱病相关的病理学变化存在许多临床信息,但这种病症的精确发病机理仍然存在着诸多的争议。为此,研究者们做出了许多有益的尝试,提出了很多关于病理机制与病理分期的假说。 2.3.1 细胞-基质间相互作用 早在1995年ARCHAMBAULT等[35]就提出,由于肌腱细胞对过度负荷的机械生物学反应引发了一系列细胞-基质间的相互作用,在这种情况下,肌腱细胞不能维持肌腱的细胞外基质正常状态,进而导致基质的退化和组织的短暂变弱,使其更容易受到持续负荷的损害。然后这种损伤逐渐累积,直至发生腱病,如图3所示。但尚未描述细胞与基质之间相互作用的精确机制。后续的许多学者也都认同这一观点,认为肌腱细胞对过度负荷的机械生物学反应引发了导致肌腱病变的退行性事件级联[36-37]。许多研究者推测肌腱在承受过度重复负荷以后,肌腱基质内发生微创伤[35,38]。如果这种微创伤不能通过肌腱细胞的主动修复反应来平衡,则会导致累积损伤并最终导致肌腱退化[39]。 "
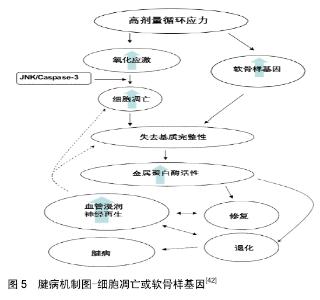
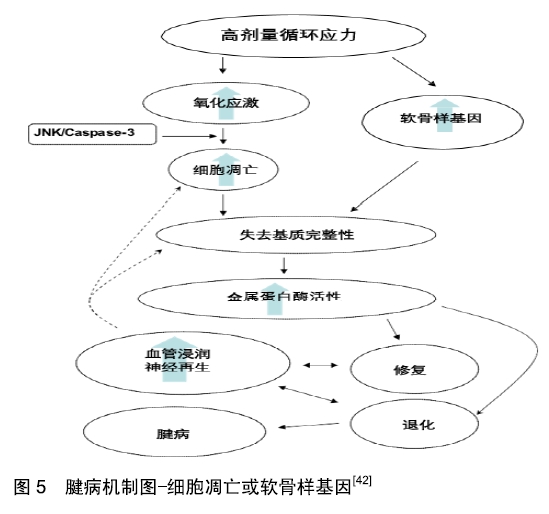
2.3.3 细胞凋亡 后来有学者在2008年对Archambault等学者提出的细胞-基质间反应的腱病机制图进行了完善[35],在精确机制上提出了进一步的假设[42],他认为高剂量的循环应力诱导相关基因遵循如下2种主要途径来影响腱病(图5):①氧化应激-细胞凋亡;②软骨样基因。这2种途径之间的相互作用尚未完全确定。一旦腱病变开始,肌腱细胞变圆,细胞凋亡开始,产生的基质中Ⅰ型胶原蛋白含量很低,因此在性质上更偏向软骨性质和“不成熟”的状态。一旦正常的细胞-基质复合物被破坏,就会诱发“相对”的应力剥夺[43-44],基质金属蛋白酶破坏开始,腱止点疼痛变得更明显,血管增生,机械性能下降,发生血管和神经浸润以尝试修复,而在修复过程中,细胞凋亡也参与了损伤修复部位成纤维细胞过度增殖的清除机制。"
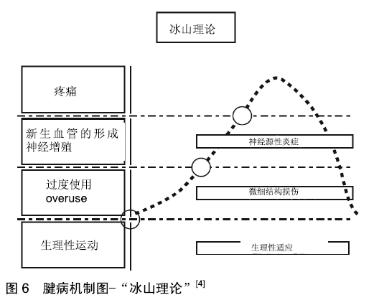
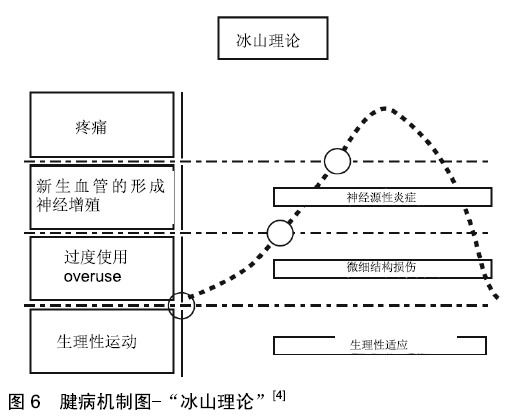
2.3.4 冰山理论 为了完善对于炎症现象与退行性疾病之间并发关系的理解,ABATE等[4]针对腱病的这一问题提出了“冰山理论”,见图6,在这其中可以看到很多顺序发生的阶段层面。冰山的底部代表肌腱处于正常生理状况之下,在腱病的初始阶段可以识别出2个阶段:无症状期和有症状期。这种划分意味着疼痛是一种报警信号,标志着腱病从第一个阶段到第二个阶段的过渡。首先要考虑的是,在第一阶段或者说在非致痛阶段患者,通常不会主动进行影像学检查,因此冰山的底层机制事实上仍然未被研究清楚。适度的体育锻炼是增加肌腱机械性能的重要手段,但是一旦超过了某一“限度”,则会激活一种“微创机制”一旦这种机制被激活,则可能会导致2种不同的可能:①对于微创伤的肌腱可以给予适当的“再生性间歇”,促使再生过程战胜创伤性过程。通过这种方式肌腱组织得以保持功能平衡;②微创损伤肌腱如果无法获得充分的“再生性间歇”时间,肌腱结构将被继续破坏,促炎细胞因子、促血管生成因子和自由基的致病级联开始产生,这将进一步引起肌腱结构的进行性退化并伴发神经增殖,而后者可能才是导致疼痛症状爆发的主要原因。该理论中可以的出2点启示:首先,腱病是在肌腱承受生理负荷时所发生的,在自我修复过程和微损伤之间的一种失衡现象;其次,保障肌腱动态平衡的生理性工作负荷和能够破坏这种微妙平衡的非生理负荷之间的界线比较模糊,难以确定。"

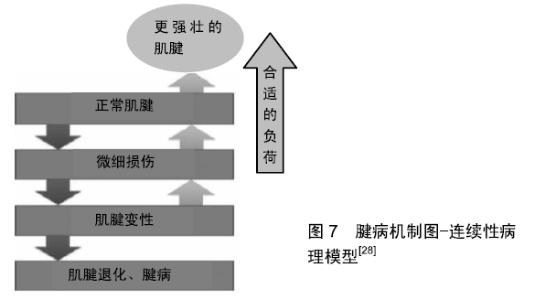
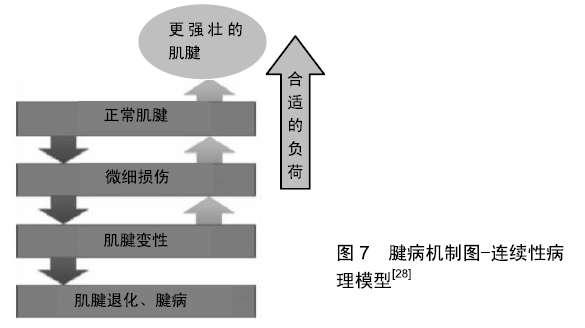
反应性肌腱病:从组织病理学角度来看,反应性肌腱病的特征在于细胞外环境中合成的大蛋白聚糖增加,以便结合更多的水[45]。临床上,这一阶段通常是由于肌腱暴露于过度的负荷而没有足够的时间恢复而导致的短期反应,此时肌腱变厚,这是一种可以在短期内减轻肌腱组织应力的正常反应。临床上,这被视为增厚的肌腱-虽然这有时被描述为由于肿胀的外观和急性疼痛而被视为“炎症”现象,但炎症细胞没有显着的增多[46]。重要的是,肌腱中胶原纤维的完整性不会改变,如果这时负荷适当减少,肌腱可以恢复到正常的阶段。此时的肌腱的细胞已经变得更具有反应性,努力修复对肌腱的损伤。由于胶原排列不变,肌腱的拉伸强度不降低。因此,尽管肌腱在此时会有不适感,但是仍能够坚持运动。 肌腱失调:是肌腱尝试愈合的阶段,在上一阶段的基础上,如果肌腱负荷没有充分降低或者没有给予足够的恢复时间,则肌腱从反应性肌腱病向肌腱失调进展,进入到第二损伤阶段。在肌腱内部,肌腱细胞的数量以及蛋白聚糖的生成增加,胶原蛋白开始变得混乱,结果使拉伸强度下降。在这个阶段,肌腱更容易发生超负荷运动,其损伤的活动阈值水平比健康肌腱要低[47]。如果此时停止所有超负荷的活动并善加处理,肌腱仍然可以恢复,尽管可能需要更长的时间。 退行性肌腱病:这一阶段如果继续对肌腱施压,损伤就会进入退化阶段,包括肌腱内的细胞的持续死亡、胶原蛋白基质降解、胶原纤维排列混乱等一系列不可逆的退行性变化,肌腱的愈合能力受到严重影响,拉伸强度显著下降,进一步的过度负荷甚至可能导致肌腱断裂。 从细胞与基质间失败的愈合反应,再到“冰山理论”与腱病的4个病理分期,可以看出对于腱病的病理机制的了解经历了一个长期而复杂的认识过程。目前可以将腱病的病理过程总结为:腱病是肌腱承受各种强度的负荷时所发生的,在自我修复过程和微损伤之间的一种失衡现象,以及由此引发的一系列退行性变化。而在这一过程中,导致失衡的负荷强度与负荷间歇时间均比较模糊,这可能预示着日后的的研究重点。 "

| [1] MIENALTOWSKI MJ, BIRK DE.Structure, physiology, and biochemistry of collagens.Adv Exp Med Biol. 2014;802:5-29. [2] BENJAMIN M, RALPHS JR. Fibrocartilage in tendons and ligaments-an adaptation to compressive load.J Anat.1998;193(Pt 4): 481-494. [3] ACKERMANN PW, Renström P.Tendinopathy in sport.Sports Health. 2012;4(3):193-201. [4] ABATE M, SILBERNAGEL KG, SILJEHOLM C, et al. Pathogenesis of tendinopathies: inflammation or degeneration?Arthritis Res Ther.2009; 11(3):235. [5] ANDRES BM, MURRELL GA.Treatment of tendinopathy: what works, what does not, and what is on the horizon.Clin Orthop Relat Res.2008; 466(7):1539-1554. [6] KHAN KM, OOK JL, KANNUS P, et al.Time to abandon the "tendinitis" myth. BMJ.2002;324(7338):626-627. [7] SCHEPSIS AA, JONES H, HAAS AL.Achilles tendon disorders in athletes.Am J Sports Med.2002;30(2):287. [8] REES JD, WILSON AM, Wolman RL.Current concepts in the management of tendon disorders.Rheumatology(Oxford).2006;45(5): 508-521. [9] BASS E.Tendinopathy: why the difference between tendinitis and tendinosis matters.Int J Ther Massage Bodywork.2012;5(1):14-17. [10] FU SC, ROLF C, CHEUK YC, et al.Deciphering the pathogenesis of tendinopathy: a three-stages process.Sports Med Arthrosc Rehabil Ther Technol.2010;2:30. [11] MAFFULLI N, KADER D.Tendinopathy of tendo achillis.J Bone Joint Surg Br.2002;84(1):1-8. [12] BLUMAN EM, LLEN SD, FADALE PD.Tendon Repair and Regeneration. Orthopedic Biology and Medicine,2006. [13] HILDEBRAND KA, GALLANT-BEHM CL, KYDD AS, et al.The Basics of Soft Tissue Healing and General Factors that Influence Such Healing. Sports Med Arthrosc Rev.2005;13(3):136-144. [14] LEHTO M, JOZSA L, KVIST M,et al. Fibronectin in the ruptured human Achilles tendon and its paratenon. An immunoperoxidase study.Ann Chir Gynaecol. 1990;79(2):72-77. [15] ANDIA I, SANCHEZ M, MAFFULLI N.Tendon healing and platelet-rich plasma therapies. Expert Opin Biol Ther. 2010; 10(10):1415-1426. [16] DOVI JV,HE LK,DI PIETRO LA.Accelerated wound closure in neutrophil-depleted mice.J Leukoc Biol.2003;73(4):448-455. [17] HARRISON R,JONES M,GROBBELAR AO,et al.Tendon Healing Intrinsic or Extrinsic? Direct Evidence for Dual Mechanisms in Early Stages of Tendon Injury.Tissue Eng.2003;9(4):852. [18] JUNEJA SC, SCHWARZ EM, O'KEEFE RJ,et al.Cellular and molecular factors in flexor tendon repair and adhesions: a histological and gene expression analysis.Connect Tissue Res.2013;54(3):218-226. [19] WU YF, CHEN CH, CAO Y, et al. Molecular Events of Cellular Apoptosis and Proliferation in the Early Tendon Healing Period.J Hand Surg Am.2010;35(1):2-10. [20] ORYAN A, MOSHIRI A.A long term study on the role of exogenous human recombinant basic fibroblast growth factor on the superficial digital flexor tendon healing in rabbits.J Musculoskelet Neuronal Interact.2011;11(2):185-195. [21] WANG JH.Mechanobiology of tendon.J Biomech. 2006;39(9): 1563-1582. [22] ZHANG LN, WAN WB, WANG YX, et al.Evaluation of Elastic Stiffness in Healing Achilles Tendon After Surgical Repair of a Tendon Rupture Using In Vivo Ultrasound Shear Wave Elastography.Med Sci Monit. 2016 ;22:1186-1191. [23] EVERTS V.Phagocytosis and intracellular digestion of collagen, its role in turnover and remodeling.Histochem J.1996:229-245. [24] PIERO V.The Lower Limb Tendinopathies.Sports Traumatol, 2016. [25] REES JD, MAFFULLI N, COOK J.Management of tendinopathy.Am J Sports Med.2009;37(9):1855-1867. [26] KHAN KM, COOK JL, BONAR F, et al. Histopathology of common tendinopathies. Update and implications for clinical management. Sports Med.1999;27(6):393-408. [27] JÓZSA L, KANNUS P.Histopathological findings in spontaneous tendon ruptures.Scand J Med Sci Sports. 1997;7(2):113-118. [28] COOK JL, PURDAM CR.Is tendon pathology a continuum? A pathology model to explain the clinical presentation of load-induced tendinopathy.Br J Sports Med. 2009;43(6):409-416. [29] MILLAR NL, MURRELL GA.Heat shock proteins in tendinopathy: novel molecular regulators.Mediators Inflamm. 2012;2012:436203. [30] THORNTON GM, HART DA.The interface of mechanical loading and biological variables as they pertain to the development of tendinosis.J Musculoskelet Neuronal Interact.2011;11(2):94-105. [31] REES JD,STRIDE M,SCOTT A.Tendons--time to revisit inflammation. Br J Sports Med. 2014 ;48(21):1553-1557. [32] GOEL VK, MOLITOR SC.Effects of rate of loading on viscoelastic supraspinous ligament inflammation and cumulative lumbar disorder.Spine J.2010;10(12):1078-1085. [33] DEL BUONO A, BATTERY L, DENARO V, et al.Tendinopathy and inflammation: some truths.Int J Immunopathol Pharmacol. 2011;24 (1 Suppl 2):45-50. [34] KRAUSHAAR BS, NIRSCHL RP. Tendinosis of the elbow (tennis elbow). Clinical features and findings of histological, immunohistochemical, and electron microscopy studies.J Bone Joint Surg Am.1999;81(2):259-278. [35] ARCHAMBAULT JM, WILEY JP,BRAY RC. Exercise loading of tendons and the development of overuse injuries.A review of current literature. Sports Med.1995;20(2):77-89. [36] ARCHAMBAULT J, TSUZAKI M, HERZOG W, et al.Stretch and interleukin-1beta induce matrix metalloproteinases in rabbit tendon cells in vitro.J Orthop Res.2002;20(1):36-39. [37] WANG JH, JIA F, YANG G, et al.Cyclic mechanical stretching of human tendon fibroblasts increases the production of prostaglandin E2 and levels of cyclooxygenase expression: a novel in vitro model study. Connect Tissue Res. 2003;44(3-4): 128-133. [38] SHARMA P, MAFFULLI N.Tendon injury and tendinopathy: healing and repair.J Bone Joint Surg Am. 2005;87(1):187-202. [39] KER RF.The implications of the adaptable fatigue quality of tendons for their construction, repair and function.Comp Biochem Physiol A Mol Integr Physiol.2002;133(4):987-1000. [40] MURRELL GA.Understanding tendinopathies. Br J Sports Med. 2002; 36(6):392-393. [41] TSUZAKI M, BYNUM D, ALMEKINDERS L, et al.ATP modulates load-inducible IL-1beta, COX 2, and MMP-3 gene expression in human tendon cells.J Cell Biochem.2003;89(3):556-562. [42] XU Y,MURRELL GAC.The Basic Science of Tendinopathy.Clin Orthop Relat Res.2008;466(7):1528-1538. [43] ARNOCZKY SP, LAVAGNINO M, EGERBACHER M.The mechanobiological aetiopathogenesis of tendinopathy: is it the over-stimulation or the under-stimulation of tendon cells? Int J Exp Pathol. 2007;88(4):217-226. [44] ARNOCZKY SP, LAVAGNINO M, EGERBACHER M, et al. Matrix metalloproteinase inhibitors prevent a decrease in the mechanical properties of stress-deprived tendons: an in vitro experimental study. Am J Sports Med.2007;35(5):763-769. [45] MAGNUSSON SP, LANGBERG H,KJAER M.The pathogenesis of tendinopathy: balancing the response to loading.Nat Rev Rheumatol. 2010;6(5):262-268. [46] SCOTT A, COOK JL, HART DA, et al.Tenocyte responses to mechanical loading in vivo: a role for local insulin-like growth factor 1 signaling in early tendinosis in rats.Arthritis Rheum.2007;56(3): 871-881. [47] KHAN KM, MAFFULLI N, COLEMAN BD, et al.Patellar tendinopathy: some aspects of basic science and clinical management.Br J Sports Med.1998;32(4):346-355. |
| [1] | Li Huo, Wang Peng, Gao Jianming, Jiang Haoran, Lu Xiaobo, Peng Jiang. Relationship between revascularization and internal microstructure changes in osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1323-1328. |
| [2] | Zhang Haobo, Zhao Yunan, Yang Xuejun. Role and therapeutic implications of pyroptosis in intervertebral disc degeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1445-1451. |
| [3] | Xiang Xinjian, Liu Fang, Wu Liangliang, Jia Daping, Tao Yue, Zhao Zhengnan, Zhao Yu. High-dose vitamin C promotes the survival of autologous fat transplantation in rats [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1242-1246. |
| [4] | Wu Bingshuang, Wang Zhi, Tang Yi, Tang Xiaoyu, Li Qi. Anterior cruciate ligament reconstruction: from enthesis to tendon-to-bone healing [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1293-1298. |
| [5] | Liu Yiyi, Qiu Junqiang, Yi Longyan, Zhou Cailiang. Effect of resistance training on interleukin-6 and C-reactive protein in middle-age and elderly people: a Meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 804-812. |
| [6] | He Junjun, Huang Zeling, Hong Zhenqiang. Interventional effect of Yanghe Decoction on synovial inflammation in a rabbit model of early knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 694-699. |
| [7] | Chen Xiaoxu, Luo Yaxin, Bi Haoran, Yang Kun. Preparation and application of acellular scaffold in tissue engineering and regenerative medicine [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 591-596. |
| [8] | Li Anan, Jiang Tao, Zhan Min, Cai Yuning, Song Min, Li Congcong, Lin Wenzheng, Zhang Jiayuan, Liu Wengang. Pharmacological mechanism of Shenling Baizhu San in the treatment of knee osteoarthritis based on network pharmacology and molecular docking [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(2): 197-204. |
| [9] | Wang Kun, He Benxiang. Asperosaponin VI therapy for Achilles tendinopathy in rabbits [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(2): 211-217. |
| [10] | Zhang Chao, Lü Xin, Liu Jinyuan, Wang Xiaohu, Xu Xiaopei, Liu Zemin. Greater trochanter pain syndrome: anatomy, pathology, differential diagnosis and treatment [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(2): 296-301. |
| [11] | Yang Xue, Wang Baoqun, Jiang Xiaowen, Zou Shengcan, Ming Jinfa, Lin Shasha. Preparation and properties of biodegradable plant polysaccharide hemostatic microspheres [J]. Chinese Journal of Tissue Engineering Research, 2022, 10(16): 2607-2611. |
| [12] | Zhao Tianyu, Jin Song, Zhang Di, Liu Xiaoxiao, Ma Jiang, Wang Ju. Baduanjin training for patellar tendinopathy in a randomized controlled trial: improving pain, muscle flexibility and lower limb balance stability [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(11): 1662-1668. |
| [13] | Xing Hongchang, Cao Jianping, Zhu Jing, Yao Kun. Mechanism by which enalapril alleviates myocardial injury in a rat model of limb ischemia-reperfusion [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(11): 1747-1751. |
| [14] | Huang Lan, Wang Qin, Ge Song. Research progress on the application of self-assembled peptides in endodontics and periodontitis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(10): 1625-1630. |
| [15] | Zhao Zixi, Xu Jun, Ding Min, Li Xiwen, Zhang Jinghang, Wang Penghua. Changes of type I and III collagen and matrix metalloproteinase 2 and 9 on the wound of diabetic foot ulcer with external application of medical collagen dressing [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(10): 1544-1550. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||