Chinese Journal of Tissue Engineering Research ›› 2026, Vol. 30 ›› Issue (29): 7673-7679.doi: 10.12307/2026.263
Previous Articles Next Articles
A new perspective on exercise for the prevention and treatment of type 2 diabetes mellitus: pyroptosis#br#
#br#
Zhao Yanan, Cao Liquan, Tan Sijie
- Tianjin Key Laboratory of Physical and Health Integration and Health Promotion, Tianjin University of Sport, Tianjin 301617, China
-
Received:2025-08-04Revised:2025-12-08Online:2026-10-18Published:2026-03-06 -
Contact:Tan Sijie, Professor, Doctoral supervisor, Tianjin Key Laboratory of Physical and Health Integration and Health Promotion, Tianjin University of Sport, Tianjin 301617, China -
About author:Zhao Yanan, MS candidate, Tianjin Key Laboratory of Physical and Health Integration and Health Promotion, Tianjin University of Sport, Tianjin 301617, China -
Supported by:the National Key Research and Development Program of China, No. 2020YFC2006704 (to TSJ [project participant]); the Tianjin Social Science Planning Youth Project, No. TJTY16-002Q (to CLQ)
CLC Number:
Cite this article
Zhao Yanan, Cao Liquan, Tan Sijie. A new perspective on exercise for the prevention and treatment of type 2 diabetes mellitus: pyroptosis#br#
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
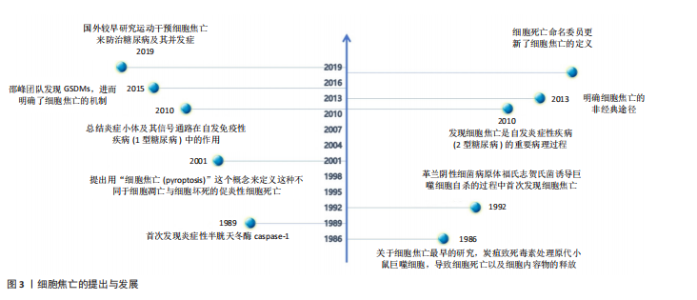
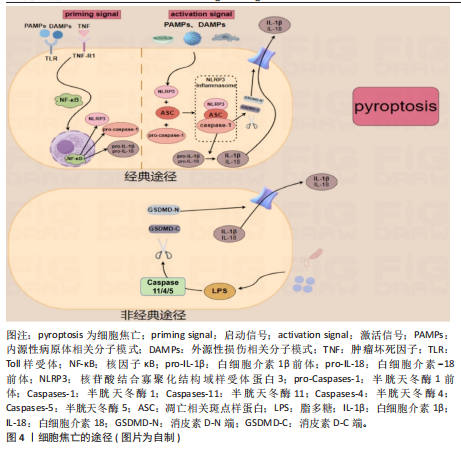
菌可诱导巨噬细胞以不同于凋亡的方式自杀。直至2001年,Cookson和Brennan首次提出“细胞焦亡”概念,指这种促炎性细胞死亡[11],pyroptosis源自希腊词汇,其中pyro指火或热,ptosis则是指下降或陨落。之后,细胞死亡命名委员会于2018年更新了细胞焦亡的定义并一直沿用至今,即是由促炎信号等干扰细胞内外环境稳态而引发的、为维持稳态的主动性、调节性、免疫性细胞消亡过程[12]。见图3。 2.1.2 细胞焦亡的途径 细胞焦亡主要依靠炎症小体的活化进而使半胱天冬酶家族蛋白激活,并引发一系列的炎症性反应[13],炎症小体是由多种成分构成的复合体,可以保护机体免受危险刺激与病原体的伤害[14]。介导消皮素D裂解与细胞焦亡的炎症小体以核苷酸结合寡聚化结构域样受体蛋白3炎性体为主[15],核苷酸结合寡聚化结构域样受体蛋白3是一种细胞内的传感器,可以感受外界环境的刺激以及内源性的危险信号,导致核苷酸结合寡聚化结构域样受体蛋白3炎症小体的形成与活化[16]。上述途径为细胞焦亡的经典途径,又称为炎症小体途径,依赖于半胱天冬酶家族中的半胱天冬酶1,同时,细胞焦亡还包括非经典途径(即非炎症小体途径),依赖于半胱天冬酶家族中的半胱天冬酶11/4/5。 (1)细胞焦亡的经典途径(炎症小体途径):炎症小体的形成开始于细胞膜模式识别受体对不同刺激的识别[5],根据识别到的不同刺激分为2种模式,即内源性病原体相关分子模式与外源性损伤相关分子模式[17]。但由于正常情况下细胞内核苷酸结合寡聚化结构域样受体蛋白3水平较低,无法形成并活化核苷酸结合寡聚化结构域样受体蛋白3炎症小体[18],因此需要经历2个信号通路方可激活核苷酸结合寡聚化结构域样受体蛋白3炎症小体,即启动信号通路与激活信号通路[19]。这一系列过程导致核苷酸结合寡聚化结构域样受体蛋白3与凋亡相关斑点样蛋白以及半胱天冬酶1前体相结合,构成完整的核苷酸结合寡聚化结构域样受体蛋白3炎症小体(核苷酸结合寡聚化结构域样受体蛋白3炎症小体是经典途径的总开关[20]);并诱导半胱天冬酶1前体活化为成熟的半胱天冬酶1[21]。成熟半胱天冬酶1可切割消皮素D使细胞膜形成膜孔导致细胞肿胀(消皮素D的N末端发挥作用),并诱导白细胞介素1β和白细胞介素18成熟[22]。随后,细胞被迫吸收细胞外的水分与电离子等物质,直至细胞破裂、溶解,使细胞内白细胞介素1β与白细胞介素18释放至细胞外并引发一系列的炎症反应并引发细胞焦亡,此为细胞焦亡的经典途径。 (2)细胞焦亡的非经典途径(非炎症小体途径):不同于经典途径,非经典途径中半胱天冬酶11/4/5的激活并不依赖上游复合物,而是通过自身半胱氨酸蛋白酶激活和招募域直接与病原体的脂多糖发生特异性结合发生快速的寡聚过程使半胱天冬酶11/4/5活化[23],成熟的半胱天冬酶11/4/5同样可以将消皮素D切割为活性N端并使细胞膜形成孔道[24],但是成熟的半胱天冬酶11/4/5无法诱导白细胞介素1β与白细胞介素18前体形成成熟的白细胞介素1β与白细胞介素18,它们可以通过核苷酸结合寡聚化结构域样受体蛋白3/半胱天冬酶1通路来介导白细胞介素1β与白细胞介素18的成熟[25],进而导致细胞焦亡的发生。见图4。 2.2 细胞焦亡与2型糖尿病 1型糖尿病又称为自身免疫性糖尿病,由于胰岛β细胞被自身免疫系统破坏导致胰岛素绝对缺乏,造成机体高血糖状态[26]。与1型糖尿病不同,2型糖尿病则表现为胰岛素抵抗与胰岛素进行性分泌不足(胰岛β细胞功能障碍)导致的胰岛素相对缺乏[27],约90%的糖尿病患者属于2型糖尿病,所以此次研究也将以2型糖尿病为主,研究它与细胞焦亡、运动三者之间的关系。近年来的许多研究表明,胰岛β细胞等焦亡中核苷酸结合寡聚化结构域样受体蛋白3炎症小体的形成与活化可能参与、并促使糖尿病及其并发症的发生与发展。因此,细胞焦亡一系列信号途径可能成为防治2型糖尿病新的靶点,但细胞焦亡在2型糖尿病中的作用及其分子机制仍需进一步梳理与总结。 糖脂代谢紊乱与肥胖是2型糖尿病发生发展的重要病理特征,这些病理特征均会导致机体长期处于慢性炎症状态[28]。有证据表明,自身免疫系统在2型糖尿病的发病机制中起着关键作用[29],并且揭示了胰岛β细胞焦亡与2型糖尿病发病机制的紧密联系,这包括氧化应激、核苷酸结合寡聚化结构域样受体蛋白3的形成与活化(2型糖尿病发生的核心步骤),以及促炎细胞因子白细胞介素1β、白细胞介素18的释放等一系列过程。在2型糖尿病的发展过程中,多种刺激因子和代谢产物,如高糖状态、脂肪酸、胰岛淀粉样多肽的异常沉积、胃肠道菌群产生的脂多糖以及活性氧的生成等,都可以激活核苷酸结合寡聚化结构域样受体蛋白3并触发胰"

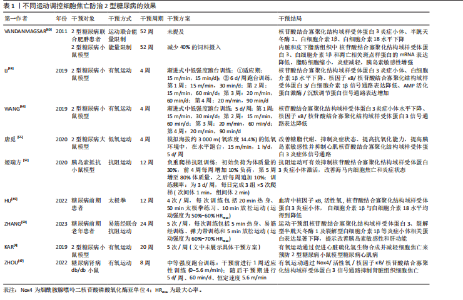
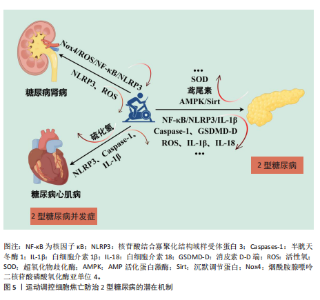
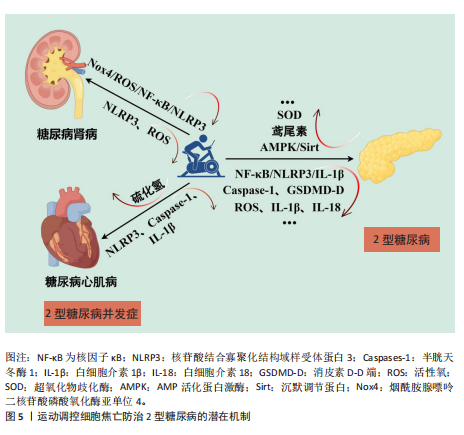
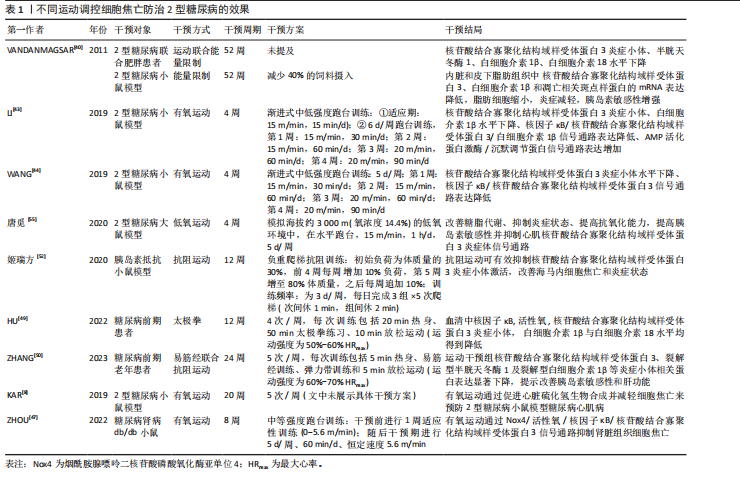
岛β细胞的焦亡[30]。2010年SCHRODER等[31] 首次提出核苷酸结合寡聚化结构域样受体蛋白3炎症小体参与2型糖尿病的病理过程,具体而言,机体长期暴露于慢性高糖的环境会诱导还原型辅酶Ⅱ磷酸-氧化酶系统产生活性氧簇,进而导致线粒体功能障碍与氧化应激;同时氧化应激亦会导致线粒体内硫氧还蛋白相互作用蛋白(与胰岛素抵抗相关的蛋白)高表达,上述活性氧产生增多与硫氧还蛋白结合蛋白水平升高(即硫氧还蛋白结合蛋白-核苷酸结合寡聚化结构域样受体蛋白3-消皮素D信号通路介导的胰岛β细胞炎症与焦亡[32-33])均会激活胰岛β细胞中核苷酸结合寡聚化结构域样受体蛋白3炎症小体,从而使胰岛处于慢性炎症状态以及被免疫细胞(如巨噬细胞)浸润,导致胰岛β细胞发生细胞焦亡及功能障碍。后续有学者也进行了相关的实验来确定血糖调节控制对核苷酸结合寡聚化结构域样受体蛋白3炎症小体的影响,结果表明高血糖激活氧化应激通路来活化胰岛β细胞中核苷酸结合寡聚化结构域样受体蛋白3炎症小体,导致白细胞介素1β、白细胞介素18等促炎细胞因子分泌,诱导胰岛素抵抗与胰岛功能障碍(如白细胞介素1β会影响骨骼肌胰岛素信号通路,使血糖调节发生紊乱[34-35]),最终导致2型糖尿病的发生。因此,近年来许多针对核苷酸结合寡聚化结构域样受体蛋白3炎症小体介导的细胞焦亡抑制剂等相关研究也逐渐涌现,如ZHANG等[36]学者以高脂饮食制作2型糖尿病小鼠模型,并予以表没食子儿茶素没食子酸酯治疗,结果发现表没食子儿茶素没食子酸酯可以作为核苷酸结合寡聚化结构域样受体蛋白3炎症小体的抑制剂并发挥抗炎、清除活性氧的作用,最终可以改善2型糖尿病小鼠的糖耐量。同样的,XU等[37]发现中药穿心莲内酯可以通过抑制硫氧还蛋白结合蛋白-核苷酸结合寡聚化结构域样受体蛋白3-消皮素D轴来缓解胰岛β细胞焦亡以及减少炎症因子的表达。此外,其他信号通路也可以实现对胰岛β细胞焦亡、2型糖尿病的调控。近期的研究显示,有丝分裂不发生基因A相关激酶家族中丝氨酸/苏氨酸蛋白激酶丝氨酸/苏氨酸蛋白激酶7在2型糖尿病患者与小鼠模型中表达升高并参与核苷酸结合寡聚化结构域样受体蛋白3炎症小体的激活,同时降低微糖核苷酸的表达水平[37],丝氨酸/苏氨酸蛋白激酶7为微糖核苷酸的靶向基因,诱导2型糖尿病患者与小鼠模型中微糖核苷酸过表达可以减少核苷酸结合寡聚化结构域样受体蛋白3炎症小体诱导的胰岛β细胞焦亡以缓解2型糖尿病及胰岛β细胞焦亡导致的肝肾损伤。同时,CHANG等[38]的研究亦系统揭示了miR-23a-3p在2型糖尿病发病机制中的关键调控作用,发现其可通过靶向下调丝氨酸/苏氨酸蛋白激酶7,从而抑制核苷酸结合寡聚化结构域样受体蛋白3炎症小体的激活,减少炎症因子释放与细胞焦亡,进而缓解肝肾组织损伤并改善胰岛素敏感性。 总之,随着研究的不断深入,越来越多的证据表明,细胞焦亡在2型糖尿病及其并发症的发生与发展中发挥着不可忽视的关键作用。现有研究不仅揭示了核苷酸结合寡聚化结构域样受体蛋白3炎症小体及其相关信号通路(如硫氧还蛋白结合蛋白-核苷酸结合寡聚化结构域样受体蛋白3-消皮素D轴、丝氨酸/苏氨酸蛋白激酶7调控通路等)在调节胰岛β细胞焦亡中的核心地位,也提示氧化应激、代谢异常及免疫失衡等多种内外源性刺激通过相互作用共同促进了2型糖尿病的慢性炎症状态。因此,深入探讨细胞焦亡介导的2型糖尿病病理生理机制,不仅有助于进一步揭示其发病机制的复杂性与多样性,还为寻找新的防治靶点、优化干预策略及推动相关研究成果向临床实践转化提供了新的思路与方向。 2.3 运动调控细胞焦亡防治2型糖尿病 目前针对2型糖尿病的临床治疗主要包括药物干预与生活方式干预,其中运动作为生活方式干预的重要组成部分,因安全性高、依从性强、干预成本低且具备长期效应,已被公认为防治和管理2型糖尿病的有效手段。近年来,随着细胞焦亡机制的不断揭示,越来越多的研究将运动与胰岛β细胞焦亡之间的关系作为研究重点,认为运动不仅能通过传统路径改善胰岛素抵抗,还可作为抑制炎症性程序性细胞死亡的新策略,更有效地延缓糖尿病的进展[39]。 如前文所述,核苷酸结合寡聚化结构域样受体蛋白3炎症小体的激活是细胞焦亡及其介导疾病的开端,其形成与活化可促使白细胞介素1β、白细胞介素18等促炎因子释放,加剧组织胰岛素抵抗并导致β细胞功能衰竭,抑制核苷酸结合寡聚化结构域样受体蛋白3炎症小体的形成与活化、减少促炎细胞因子的释放可以降低2型糖尿病患者机体炎症状态并改善组织对胰岛素的敏感性,从而减缓糖尿病进程。2011年VANDANMAGSAR团队[40]进行的研究较早地发现了运动(并未提及具体运动方案)与能量限制干预可以让2型糖尿病联合肥胖患者达到减重的目的,更重要的是能够抑制脂肪细胞的焦亡并减少脂肪组织中核苷酸结合寡聚化结构域样受体蛋白3的表达从而抑制炎症的发展、提高胰岛素的敏感性。此外,运动可以诱导骨骼肌表达、合成并分泌多种生物活性物质,如细胞因子(如鸢尾素),这些物质可以通过血液循环途径调控多种器官组织的代谢功能[41]。最近有研究发现,将2型糖尿病小鼠模型的胰岛β细胞株放置鸢尾素环境中,检测结果显示鸢尾素可以上调miR-19b-3p/细胞因子信号抑制因子3 /信号转导与转录激活子3信号通路[42],该信号通路介导的自噬可以清除受损的线粒体与核苷酸结合寡聚化结构域样受体蛋白3炎症小体,从而减轻胰岛β的焦亡发挥防治2型糖尿病的作用,此发现不仅丰富了细胞因子的功能内涵,也为探索运动调控细胞焦亡的新机制提供了分子基础。 总之,不同类型的运动方式在生理负荷、代谢调节路径、分子应答机制等方面存在较大差异,其对细胞焦亡的调控效应也呈现多样性。为更全面地理解运动干预的机制基础,提升干预精准性和个体化水平,以下将从有氧运动、抗阻运动和低氧运动3类运动方式入手,系统梳理其在调控胰岛β细胞焦亡、防治2型糖尿病中的研究进展与作用机制。 2.3.1 有氧运动调控细胞焦亡防治2型糖尿病的效果及潜在机制 对于具体的运动方式而言,有氧运动相比于其他的运动方式研究得更为深入,如LI等[43]与WANG等[44]均采用有氧运动(跑台训练)的方式对2型糖尿病小鼠模型进行为期4周的干预,两项不同的研究得出了相似的结果,即长期的有氧运动可以上调小鼠模型中活化蛋白激酶/沉默调节蛋白通路(该信号途径可以抑制核因子κB等炎症相关转录因子的活性、改善氧化应激等减轻胰岛β细胞的损伤,从而对糖尿病相关的神经退行性疾病起到防治作用)[45],同时下调核因子κB/核苷酸结合寡聚化结构域样受体蛋白3/白细胞介素1β信号通路表达来抑制核苷酸结合寡聚化结构域样受体蛋白3炎症小体的激活。 有氧运动同样是糖尿病并发症的有效治疗措施。机体高糖状态下会导致肾皮质中烟酰胺腺嘌呤二核苷酸磷酸氧化酶亚单位4增多,继而通过烟酰胺腺嘌呤二核苷酸磷酸氧化酶亚单位4/活性氧/核因子κB/核苷酸结合寡聚化结构域样受体蛋白3信号通路诱导氧化应激与肾脏核苷酸结合寡聚化结构域样受体蛋白3炎症小体的活化,导致糖尿病肾病的发生[46];一项针对db/db小鼠的运动干预实验证明,持续8周、每周5次(每次60 min)的有氧运动可以抑制烟酰胺腺嘌呤二核苷酸磷酸氧化酶亚单位4/活性氧/核因子κB/核苷酸结合寡聚化结构域样受体蛋白3信号通路的表达,并改善肾脏氧化应激、炎症以及纤维化等病理变化[47],提示有氧运动可以作为改善糖尿病导致肾损伤的潜在治疗措施。对于糖尿病心肌病而言,KAR等[8]通过高脂饮食建立糖尿病心肌病小鼠模型,并进行长期的有氧运动干预,发现有氧运动可以作为治疗糖尿病心肌病的有效手段,可以促进心肌细胞硫化氢(抗氧化物质)的生物合成并抑制心肌细胞焦亡(抑制核苷酸结合寡聚化结构域样受体蛋白3、半胱天冬酶1以及白细胞介素1β的表达),从而发挥保护心肌组织、防治糖尿病心肌病的作用。 传统健身功法作为有氧运动亦为运动防治2型糖尿病提供了新的思路,许多研究已经证实传统健身功法可以改善糖尿病患者的糖脂代谢并增加胰岛素敏感性[48],其潜在机制可能与抑制核苷酸结合寡聚化结构域样受体蛋白3及促炎细胞因子有关。HU等[49]于2022年进行的一项针对人体的试验中,以糖尿病前期患者为研究对象,以每周4次、每次80 min的太极拳运动进行共12周的干预,发现太极拳干预可有效调节糖尿病前期患者血糖与血脂水平并改善胰岛素抵抗,且患者血清中核因子κB、活性氧、核苷酸结合寡聚化结构域样受体蛋白3炎症小体、白细胞介素1β与白细胞介素18水平均得到降低,潜在机制为通过运动提高机体鸢尾素水平来抑制核苷酸结合寡聚化结构域样受体蛋白3炎症信号通路的表达,从而减轻机体炎症状态和缓解胰岛素抵抗,尽管该研究并未直接探讨细胞焦亡相关蛋白的表达变化,但其对核苷酸结合寡聚化结构域样受体蛋白3通路及其上游活性氧、核因子κB以及促炎因子等的抑制作用;同时也验证了前文中所述鸢尾素之于核苷酸结合寡聚化结构域样受体蛋白3炎症信号通路的调控作用,提示太极拳可能对细胞焦亡过程具有间接调控作用,值得进一步探索。后续的ZHANG等[50]采取易筋经联合抗阻训练的干预方式,观察到糖尿病前期人群在12周干预后核苷酸结合寡聚化结构域样受体蛋白3、核因子κB、活性氧等炎症因子水平下降,胰岛素抵抗显著缓解,血糖血脂得到改善。虽然目前相关研究尚未直接聚焦于细胞焦亡的核心标志物,但对核苷酸结合寡聚化结构域样受体蛋白3通路及其上游关键因子的干预效果,为其在调控细胞焦亡方面提供了间接支持。未来应进一步结合分子机制研究,深入探讨传统健身功法对调控细胞焦亡路径、防治2型糖尿病的潜力。 2.3.2 抗阻运动调控细胞焦亡防治2型糖尿病的效果及潜在机制 根据美国运动医学会在2022年发布的对于2型糖尿病运动指南的声明,抗阻运动(尤其是高强度抗阻运动)对2型糖尿病患者整体的血糖管理更加有益[51],但是对于抗阻运动调控细胞焦亡防治2型糖尿病的研究却十分少有,例如姬瑞方等[52]研究抗阻运动对胰岛素抵抗小鼠模型海马内细胞焦亡相关蛋白的影响,发现抗阻运动组小鼠海马内核苷酸结合寡聚化结构域样受体蛋白3炎症小体、消皮素D-D蛋白以及相关促炎细胞因子蛋白表达显著降低。这提示了抗阻运动调控细胞焦亡防治2型糖尿病的潜在机制,但未来仍需更多的动物模型实验加以证实。 2.3.3 低氧运动调控细胞焦亡防治2型糖尿病的效果及潜在机制 近年来,低氧运动抑制核苷酸结合寡聚化结构域样受体蛋白3炎症小体信号通路治疗2型糖尿病及其并发症的研究也逐渐显现。低氧运动(hypoxia training)是指在氧气浓度较低的高海拔地区或人工创建的低氧气浓度的环境中进行急性或慢性运动的方式[53],适当的低氧运动可以提高机体抗氧化能力、清除氧自由基从而缓解氧化应激对组织的损伤[54],但目前低氧运动应用于防治糖尿病的研究较少,其潜在机制亦不明确,国内学者唐觅等[55]的研究在领域做出了探索,其团队以2型糖尿病大鼠为研究对象,探究4周低氧运动对大鼠糖尿病及心肌组织核苷酸结合寡聚化结构域样受体蛋白3炎症小体的影响,干预结束后进行血清生化指标、氧化应激指标、Western blotting等检测,结果显示低氧运动组甘油三酯、总胆固醇、低密度脂蛋白胆固醇水平下降且高密度脂蛋白胆固醇水平升高,同时超氧化物歧化酶、血清白细胞介素1β以及心肌组织中核苷酸结合寡聚化结构域样受体蛋白3与半胱天冬酶1水平均降低,这提示低氧运动可以改善2型糖尿病大鼠糖脂代谢与抗氧化能力并通过抑制核苷酸结合寡聚化结构域样受体蛋白3炎症小体通路减少糖尿病心肌病的发生。 上述研究结果提示,低氧运动可能通过抑制核苷酸结合寡聚化结构域样受体蛋白3炎症小体通路,从而在一定程度上缓解糖尿病相关的慢性炎症,延缓糖尿病性心肌病的发生。然而,虽然该研究表明低氧运动可以抑制细胞焦亡的关键步骤——核苷酸结合寡聚化结构域样受体蛋白3炎症小体通路,但并未进一步探讨核苷酸结合寡聚化结构域样受体蛋白3下游分子如消皮素D的表达水平,因此其调控细胞焦亡的具体机制仍需进一步验证。此外,当前低氧运动干预在处方制定、干预强度和安全边界方面尚不完善,过度低氧可能诱发心血管或神经系统损伤[56]。鉴于现有研究大多集中于动物实验,未来应加强临床研究,系统评估低氧运动在糖尿病防治中的安全性与有效性,进一步明确其在调控血脂、炎症及细胞焦亡中的作用机制。 综上所述,不同运动调控胰岛β细胞等细胞焦亡防治2型糖尿病的效果及其潜在机制在动物实验与人体试验中逐渐显现,但不同运动所发挥的作用却不尽相同,如相比于抗阻运动,有氧运动在抑制炎症因子的表达和缓解炎症状态方面更加突出;但抗阻运动对于血糖控制却更具优势等[57],这提示在未来应当探索更多运动模式对于调控胰岛β细胞等细胞焦亡防治2型糖尿病的作用及机制。不同运动调控细胞焦亡防治2型糖尿病的效果见表1,运动调控细胞焦亡防治2型糖尿病的潜在机制见图5。"
| [1] GENUTH SM, PALMER JP, NATHAN DM. Classification and Diagnosis of Diabetes//COWIE CC, CASAGRANDE SS, MENKE A, et al. Diabetes in America. Bethesda (MD) interest.; National Institute of Diabetes and Digestive and Kidney Diseases (US). 2018. [2] KOLB H, MARTIN S. Environmental/lifestyle factors in the pathogenesis and prevention of type 2 diabetes. BMC Med. 2017;15(1):131. [3] Global, regional, and national burden of diabetes from 1990 to 2021, with projections of prevalence to 2050: a systematic analysis for the Global Burden of Disease Study 2021. Lancet. 2023; 402(10397):203-234. [4] Global burden of 369 diseases and injuries in 204 countries and territories, 1990-2019: a systematic analysis for the Global Burden of Disease Study 2019. Lancet. 2020;396(10258):1204-1222. [5] YU P, ZHANG X, LIU N, et al. Pyroptosis: mechanisms and diseases. Signal Transduct Target Ther. 2021;6(1):128. [6] VASUDEVAN SO, BEHL B, RATHINAM VA. Pyroptosis-induced inflammation and tissue damage. Semin Immunol. 2023;69:101781. [7] LU F, LAN Z, XIN Z, et al. Emerging insights into molecular mechanisms underlying pyroptosis and functions of inflammasomes in diseases. J Cell Physiol. 2020;235(4):3207-3221. [8] KAR S, SHAHSHAHAN HR, HACKFORT BT, et al. Exercise Training Promotes Cardiac Hydrogen Sulfide Biosynthesis and Mitigates Pyroptosis to Prevent High-Fat Diet-Induced Diabetic Cardiomyopathy. Antioxidants (Basel). 2019;8(12):638. [9] FRIEDLANDER AM. Macrophages are sensitive to anthrax lethal toxin through an acid-dependent process. J Biol Chem. 1986;261(16):7123-7126. [10] ZYCHLINSKY A, PREVOST MC, SANSONETTI PJ. Shigella flexneri induces apoptosis in infected macrophages. Nature. 1992;358(6382):167-169. [11] D’SOUZA CA, HEITMAN J. Dismantling the Cryptococcus coat. Trends Microbiol. 2001;9(3): 112-113. [12] GALLUZZI L, VITALE I, AARONSON SA, et al. Molecular mechanisms of cell death: recommendations of the Nomenclature Committee on Cell Death 2018. Cell Death Differ. 2018;25(3):486-541. [13] CAO Z, HUANG D, TANG C, et al. Pyroptosis in diabetes and diabetic nephropathy. Clin Chim Acta. 2022;531:188-196. [14] FANG Y, TIAN S, PAN Y, et al. Pyroptosis: A new frontier in cancer. Biomed Pharmacother. 2020; 121:109595. [15] WANG L, SHARIF H, VORA SM, et al. Structures and functions of the inflammasome engine. J Allergy Clin Immunol. 2021;147(6):2021-2029. [16] SWANSON KV, DENG M, TING JP. The NLRP3 inflammasome: molecular activation and regulation to therapeutics. Nat Rev Immunol. 2019;19(8):477-489. [17] LISTON A, MASTERS SL. Homeostasis-altering molecular processes as mechanisms of inflammasome activation. Nat Rev Immunol. 2017;17(3):208-214. [18] 陈俊,贾绍辉,薛新轩.核苷酸结合寡聚化结构域样受体蛋白3炎症小体:运动防治心血管疾病的重要靶点[J].中国生物化学与分子生物学报,2024,40(11):1493-1503. [19] SHARMA M, DE ALBA E. Structure, Activation and Regulation of NLRP3 and AIM2 Inflammasomes. Int J Mol Sci. 2021;22(2):872. [20] 田蕾,赵文景.细胞焦亡在糖尿病肾脏疾病中的作用机制及研究进展[J].重庆医科大学学报, 2024,49(8):937-941. [21] JO EK, KIM JK, SHIN DM, et al. Molecular mechanisms regulating NLRP3 inflammasome activation. Cell Mol Immunol. 2016;13(2):148-159. [22] MAN SM, KARKI R, KANNEGANTI TD. Molecular mechanisms and functions of pyroptosis, inflammatory caspases and inflammasomes in infectious diseases. Immunol Rev. 2017;277(1): 61-75. [23] SHI J, ZHAO Y, WANG Y, et al. Inflammatory caspases are innate immune receptors for intracellular LPS. Nature. 2014;514(7521):187-192. [24] AGLIETTI RA, ESTEVEZ A, GUPTA A, et al. GsdmD p30 elicited by caspase-11 during pyroptosis forms pores in membranes. Proc Natl Acad Sci U S A. 2016;113(28):7858-7863. [25] SHI J, GAO W, SHAO F. Pyroptosis: Gasdermin-Mediated Programmed Necrotic Cell Death. Trends Biochem Sci. 2017;42(4):245-254. [26] SUN X, PANG H, LI J, et al. The NLRP3 Inflammasome and Its Role in T1DM. Front Immunol. 2020;11:1595. [27] GALICIA-GARCIA U, BENITO-VICENTE A, JEBARI S, et al. Pathophysiology of Type 2 Diabetes Mellitus. Int J Mol Sci. 2020;21(17):6275. [28] ROHM TV, MEIER DT, OLEFSKY JM, et al. Inflammation in obesity, diabetes, and related disorders. Immunity. 2022;55(1):31-55. [29] MAMUN AA, WU Y, NASRIN F, et al. Role of Pyroptosis in Diabetes and Its Therapeutic Implications. J Inflamm Res. 2021;14:2187-2206. [30] LI X, XIAO GY, GUO T, et al. Potential therapeutic role of pyroptosis mediated by the NLRP3 inflammasome in type 2 diabetes and its complications. Front Endocrinol (Lausanne). 2022; 13:986565. [31] SCHRODER K, ZHOU R, TSCHOPP J. The NLRP3 inflammasome: a sensor for metabolic danger? Science. 2010;327(5963):296-300. [32] AN X, ZHANG Y, CAO Y, et al. Punicalagin Protects Diabetic Nephropathy by Inhibiting Pyroptosis Based on TXNIP/NLRP3 Pathway. Nutrients. 2020; 12(5):1516. [33] RUSSELL-GUZMÁN J, AMÉRICO-DA SILVA L, CADAGAN C, et al. Activation of the ROS/TXNIP/NLRP3 pathway disrupts insulin-dependent glucose uptake in skeletal muscle of insulin-resistant obese mice. Free Radic Biol Med. 2024; 222:187-198. [34] IANNANTUONI F, DIAZ-MORALES N, ESCRIBANO-LOPEZ I, et al. Does Glycemic Control Modulate the Impairment of NLRP3 Inflammasome Activation in Type 2 Diabetes? Antioxid Redox Signal. 2019;30(2):232-240. [35] 孙绍华, 张钰英, 余鹏, 等. 细胞焦亡与糖尿病及其并发症的关系研究进展[J]. 生命科学, 2022,34(12):1476-1484. [36] ZHANG C, LI X, HU X, et al. Epigallocatechin-3-gallate prevents inflammation and diabetes -Induced glucose tolerance through inhibition of NLRP3 inflammasome activation. Int Immunopharmacol. 2021;93:107412. [37] XU W, WANG H, SUN Q, et al. TXNIP-NLRP3-GSDMD axis-mediated inflammation and pyroptosis of islet β-cells is involved in cigarette smoke-induced hyperglycemia, which is alleviated by andrographolide. Environ Toxicol. 2024;39(3): 1415-1428. [38] CHANG H, CHANG H, CHENG T, et al. Micro-ribonucleic acid-23a-3p prevents the onset of type 2 diabetes mellitus by suppressing the activation of nucleotide-binding oligomerization-like receptor family pyrin domain containing 3 inflammatory bodies-caused pyroptosis through negatively regulating NIMA-related kinase 7. J Diabetes Investig. 2021;12(3):334-345. [39] LI N, ZHANG L, WANG X, et al. Exploring exercise-driven inhibition of pyroptosis: novel insights into treating diabetes mellitus and its complications. Front Endocrinol (Lausanne). 2023;14:1230646. [40] VANDANMAGSAR B, YOUM Y H, RAVUSSIN A, et al. The NLRP3 inflammasome instigates obesity-induced inflammation and insulin resistance. Nat Med. 2011;17(2):179-188. [41] 陈演, 邱俊强, 于涛,等. 肌肉-器官交互作用:运动诱导的肌肉因子研究进展[J]. 中国运动医学杂志,2022,41(11):887-895. [42] YANG J, TAN A, LI T, et al. Irisin alleviates the pyroptosis of β cells in T2DM by inhibiting NLRP3 inflammasome through regulating miR-19b-3p/SOCS3/STAT3 axis mediated autophagy. IUBMB Life. 2024;76(12):1264-1278. [43] LI J, LIU Y, LIU B, et al. Mechanisms of Aerobic Exercise Upregulating the Expression of Hippocampal Synaptic Plasticity-Associated Proteins in Diabetic Rats. Neural Plast. 2019;2019: 7920540. [44] WANG Q, HU J, LIU Y, et al. Aerobic Exercise Improves Synaptic-Related Proteins of Diabetic Rats by Inhibiting FOXO1/NF-κB/NLRP3 Inflammatory Signaling Pathway and Ameliorating PI3K/Akt Insulin Signaling Pathway. J Mol Neurosci. 2019;69(1):28-38. [45] ABEDIMANESH N, ASGHARI S, MOHAMMADNEJAD K, et al. The anti-diabetic effects of betanin in streptozotocin-induced diabetic rats through modulating AMPK/SIRT1/NF-κB signaling pathway. Nutr Metab (Lond). 2021;18(1):92. [46] YUAN N, CHEN Y, YAN Y, et al. Myricetin alleviates renal tubular epithelial-mesenchymal transition via NOX4/NF-κB/snail axis in diabetic nephropathy based on network pharmacology analysis. Heliyon. 2024;10(16):e35234. [47] ZHOU Z, YING C, ZHOU X, et al. Aerobic exercise training alleviates renal injury in db/db mice through inhibiting Nox4-mediated NLRP3 inflammasome activation. Exp Gerontol. 2022; 168:111934. [48] LU WA, CHEN YS, WANG CH, et al. Effect of a Single Session of Tai Chi Chuan Practice on Glucose and Lipid Metabolism and Related Hormones. Life (Basel). 2020;10(8):145. [49] HU S, HU Y, LONG P, et al. The effect of tai chi intervention on NLRP3 and its related antiviral inflammatory factors in the serum of patients with pre-diabetes. Front Immunol. 2022;13:1026509. [50] ZHANG T, TIAN J, FAN J, et al. Exercise training-attenuated insulin resistance and liver injury in elderly pre-diabetic patients correlates with NLRP3 inflammasome. Front Immunol. 2023;14:1082050. [51] KANALEY JA, COLBERG SR, CORCORAN MH, et al. Exercise/Physical Activity in Individuals with Type 2 Diabetes: A Consensus Statement from the American College of Sports Medicine. Med Sci Sports Exerc. 2022;54(2):353-368. [52] 姬瑞方, 卞学鹏, 刘蓓蓓, 等. 抗阻运动对胰岛素抵抗小鼠海马内焦亡相关蛋白的影响[J]. 中国应用生理学杂志,2020,36(5):456-461. [53] SINEX JA, CHAPMAN RF. Hypoxic training methods for improving endurance exercise performance. J Sport Health Sci. 2015;4(4):325-332. [54] ROSSETTI GMK, MACDONALD JH, WYLIE LJ, et al. Dietary nitrate supplementation increases acute mountain sickness severity and sense of effort during hypoxic exercise. J Appl Physiol (1985). 2017;123(4):983-992. [55] 唐觅, 晏晴艳, 李若愚. 低氧运动可改善2型糖尿病大鼠的血脂代谢、抗氧化能力并抑制心肌NLRP3炎症体信号通路[J]. 基因组学与应用生物学,2020,39(7):3249-3255. [56] PUTHON L, BOUZAT P, ROBACH P, et al. Effect of ageing on hypoxic exercise cardiorespiratory, muscle and cerebral oxygenation responses in healthy humans. Exp Physiol. 2017;102(4):436-447. [57] 温瑞明, 吕红艳, 常波, 等. NLRP3炎症小体在糖尿病及运动中作用的研究进展[J]. 生理学报, 2023,75(6):788-798. |
| [1] | Zhang Qingtong, Chen Leqin, Liu Chang, Chen Yuting, Guo Ruiwu. Neuromechanism of the endocannabinoid system in regulating exercise motivation [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(在线): 1-11. |
| [2] | Liu Jinlong, Abuduwupuer·Haibier, Bai Zhen, Su Danyang, Miao Xin, Li Fei, Yang Xiaopeng. Efficacy of different nonsurgical treatments for adolescent idiopathic scoliosis: a systematic review and network meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2370-2379. |
| [3] | Cao Yong, Teng Hongliang, Tai Pengfei, Li Junda, Zhu Tengqi, Li Zhaojin. Interactions between cytokines and satellite cells in muscle regeneration [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(7): 1808-1817. |
| [4] | Pan Dong, Yang Jialing, Tian Wei, Wang Dongji, Zhu Zheng, Ma Wenchao, Liu Na, Fu Changxi. Resistance exercise activates skeletal muscle satellite cells in aged rats: role of adiponectin receptor 1 pathway [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(7): 1736-1746. |
| [5] | Chen Yulin, He Yingying, Hu Kai, Chen Zhifan, Nie Sha Meng Yanhui, Li Runzhen, Zhang Xiaoduo , Li Yuxi, Tang Yaoping. Effect and mechanism of exosome-like vesicles derived from Trichosanthes kirilowii Maxim. in preventing and treating atherosclerosis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(7): 1768-1781. |
| [6] | Hou Chaowen, Li Zhaojin, Kong Jianda, Zhang Shuli. Main physiological changes in skeletal muscle aging and the multimechanism regulatory role of exercise [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(6): 1464-1475. |
| [7] | Sun Yaotian, Xu Kai, Wang Peiyun. Potential mechanisms by which exercise regulates iron metabolism in immune inflammatory diseases [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(6): 1486-1498. |
| [8] | Liu Yu, Lei Senlin, Zhou Jintao, Liu Hui, Li Xianhui. Mechanisms by which aerobic and resistance exercises improve obesity-related cognitive impairment [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(5): 1171-1183. |
| [9] | Wen Fan, Xiang Yang, Zhu Huan, Tuo Yanfang, Li Feng. Exercise improves microvascular function in patients with type 2 diabetes [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(5): 1225-1235. |
| [10] | Chen Qiang, Wu Wenjuan, Jiang Shuhua, Huang Da. Physical exercise improves physical function in burn patients: a systematic review and meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(5): 1269-1281. |
| [11] | Jiang Yang, Peng Hao, Song Yanping, Yao Na, Song Yueyu, Yin Xingxiao, Li Yanqi, Chen Qigang. Isometric exercise reduces resting blood pressure: a meta-analysis of moderating factors and dose effects [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(4): 975-986. |
| [12] | Li Hanyue, Li Yini, Xiang Linmei, Li Sen. Effects of resistance exercise therapy on pain and function in patients with cervical spondylotic radiculopathy: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(4): 987-996. |
| [13] | Sun Jiahe, Shi Jipeng, Zhu Tianrui, Quan Helong, Xu Hongqi. Effect of exercise intervention in elderly individuals with sarcopenia and its comorbidities: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(4): 997-1007. |
| [14] | Xu Jiamu, Yang Cheng, Li Weimin, Wang Chunqing. Role and pathogenesis of pyroptosis and inflammatory factors in osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(3): 691-700. |
| [15] | Zhao Ke, Zhang Ping, Xi Yongping, Zeng Fanzhi, Zhang Liru. Optimal exercise prescription for chronic low back pain in adults: a network meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(29): 7688-7695. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||