Chinese Journal of Tissue Engineering Research ›› 2026, Vol. 30 ›› Issue (28): 7323-7331.doi: 10.12307/2026.808
Previous Articles Next Articles
Synergistic imbalance in lumbar core muscles and novel targeted interventions for intervertebral disc degeneration
You Chenyang1, Jiang Chao2, Che Yanjun2
- 1School of Medical Imaging, Nanjing Medical University, Nanjing 211166, Jiangsu Province, China; 2Department of Orthopedics and Sports Medicine Center, Affiliated Suzhou Hospital of Nanjing Medical University, Suzhou 215000, Jiangsu Province, China
-
Received:2025-09-17Revised:2025-12-12Online:2026-10-08Published:2026-02-11 -
Contact:Che Yanjun, MD, Associate chief physician, Associate professor, Department of Orthopedics and Sports Medicine Center, Affiliated Suzhou Hospital of Nanjing Medical University, Suzhou 215000, Jiangsu Province, China -
About author:You Chenyang, School of Medical Imaging, Nanjing Medical University, Nanjing 211166, Jiangsu Province, China -
Supported by:Jiangsu Provincial Innovation and Entrepreneurship Talent Program Project, No. JSSCBS20211588 (to CYJ); Suzhou Gusu Health Talent Program Research Project, No. GSWS2021035 (to CYJ); Suzhou Major Disease Multicenter Clinical Research Project, No. DZXYJ202307 (to CYJ); Suzhou Science and Technology Development Plan (Medical and Health Science and Technology Innovation) Project, No. SKY2022185 (to CYJ); Suzhou Integrated Traditional Chinese and Western Medicine Research Fund Project, No. SKYD2023254 (to CYJ); Clinical Research Project of Nanjing Medical University Gusu College, No. GSKY20240208 (to CYJ); Clinical Research Project of Nanjing Medical University Gusu College, No. GSKY20230402 (to CYJ); Educational Research Project of Nanjing Medical University, No. 2023ZC081 (to CYJ); Suzhou Science and Technology Breakthrough Plan (Medical and Health Innovation) Project, No. SYWD2025002 (to CYJ)
CLC Number:
Cite this article
You Chenyang, Jiang Chao, Che Yanjun. Synergistic imbalance in lumbar core muscles and novel targeted interventions for intervertebral disc degeneration[J]. Chinese Journal of Tissue Engineering Research, 2026, 30(28): 7323-7331.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
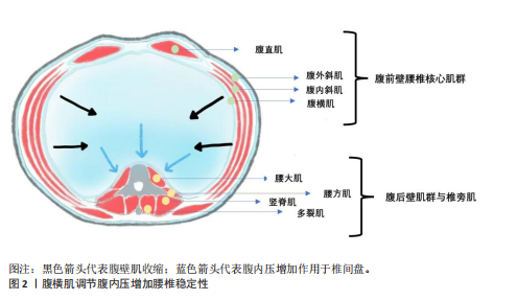
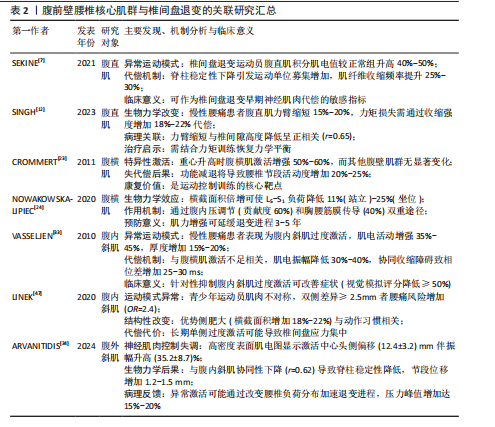
2.1 腹前壁肌群 2.1.1 腹直肌 SEKINE等[7]的肌电图研究表明,在高强度划船运动过程中,椎间盘退变运动员的腹直肌积分肌电值(integrated electromyography,IEMG)较正常运动员显著升高,提示椎间盘退变运动员的腹直肌运动单位募集数量增加[8-10],表明该肌肉的激活强度增强;TAGUCHI等[11]在棒球运动员中的研究结果与之类似,患有椎间盘退变的运动员挥棒时腹直肌、腹内斜肌、腹外斜肌的肌电活动水平均显著高于对照组。从生物力学角度分析,这种代偿性肌肉激活增强现象可能与椎间盘退变导致的脊柱稳定性下降有关。当脊柱自身的稳定功能受损时,运动系统通过增加核心肌群,包括腹直肌、腹内/外斜肌等的神经驱动强度来补偿脊柱稳定性的不足,从而维持运动过程中的力学平衡,这一代偿机制反映了神经肌肉系统对脊柱结构退变的适应性调节。 SINGH等[12]通过肌力矩研究证实,慢性腰痛患者各腰椎节段包括L3-L4、L4-L5等的腹直肌力臂值显著低于健康对照组。基于生物力学原理,力矩为肌力与力臂长度的乘积,在肌力恒定的情况下,力臂缩短将直接导致椎间盘/脊柱的稳定性与运动控制效能降低。典型表现为:当维持脊柱稳定性或执行躯干屈曲动作时,腹直肌需代偿性增强收缩强度,以弥补力臂减小造成的力矩损失,从而维持等效的生物力学效应。虽然慢性腰痛不等于椎间盘退变,但椎间盘退变作为慢性腰痛的最重要原因之一[2,13-15],其有可能是导致腹直肌激活程度增加的深层原因。 现有部分研究表明,腹直肌分离可能与腰椎间盘退变存在关联,如YUAN等[16]和WU等[17]的研究都认为产后妇女患有腹直肌分离与腰痛呈正相关,但根据SOKUNBI等[18]的系统综述报道腹直肌分离与腰痛有关的研究只是少数(38.5%),更多的研究结果认为二者无关,因此腹直肌分离与腰椎间盘退变/腰痛的关联有待进一步研究。 2.1.2 腹横肌 现有研究表明,腹横肌作为深层腹壁肌肉的核心组成部分,在腰椎生物力学活动中发挥关键作用[19],解剖学研究证实腹横肌肌纤维在腹壁前外侧形成独特的束带结构[20],它的功能机制主要体现在以下2个方面:首要通过腹内压调节系统[21],其次通过胸腰筋膜力学传导途径维持腰椎稳定性[22]。CROMMERT 等[23]的肌电研究揭示了腹横肌区别于其他腹壁肌肉(包括腹内斜肌、腹外斜肌及腹直肌)的特异性稳定功能,该肌肉在脊柱承受不同方向力矩(屈曲/伸展)时均表现出显著的激活增强现象,特别是在人体重心升高导致的稳定性需求增加时,这种特异性激活模式更为明显。NOWAKOWSKA-LIPIEC等[24]通过生物力学建模研究量化了腹横肌对腰椎负荷的影响,结果显示:当腹横肌横截面积增至生理值的2倍时,L5-S1节段负荷在直立位和坐位分别降低11%和25%,由此得出增加腹横肌强度能够减小椎间盘负荷,延缓椎间盘退变。 临床观察研究为腹横肌的功能重要性提供了进一步的证据。GILDEA 等[5]针对芭蕾舞者的对比研究发现,腰痛患者组腹横肌的收缩功能显著减弱,此结果与上述研究相互印证,进一步体现腹横肌对腰椎的保护作用。在太空的微重力环境下,宇航员的椎旁及腹壁肌肉均会萎缩,回到地球后会出现椎间盘退变与腰痛的症状,根据HIDES等[25]的研究,宇航员的腹横肌萎缩最为显著,横截面积减少幅度达33%,显著高于腹前外侧壁肌肉的平均减少水平(16%),该结果同样体现腹横肌对于维持腰椎稳定性、延缓椎间盘退变的保护意义(图2)。 病理生理机制:慢性腰痛患者的腹横肌功能减退并非孤立现象,而是涉及多层次、多系"
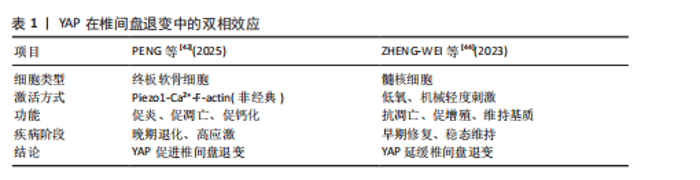
统的病理生理过程。研究发现,这一过程始于中枢神经调控的异常改变:患者初级运动皮质对腹横肌和多裂肌的神经支配信号由正常的兴奋性指令转变为抑制性输出,同时维持对竖脊肌和腹外斜肌的兴奋性控制[26-27],这种选择性抑制导致腹横肌激活不足(肌电振幅降低30%-40%)与多裂肌萎缩(横截面积减少15%-20%)[2,19],进而破坏脊柱的动态平衡,表现为异常前凸增加50%或活动度降低35%[15,28]。 腹横肌的功能障碍直接影响核心的腹内压调节机制。动物实验表明,双侧腹横肌收缩可使腰椎节段活动度显著减少13%,而这一稳定效应在肌肉附着点切断后完全消失[29]。值得注意的是,虽然通过膈肌代偿性收缩可部分恢复腹内压水平,但缺乏腹横肌特有的定向控制能力,导致脊柱在动态负荷下的稳定性下降[29]。临床观察进一步证实,腹横肌萎缩患者的腹内压波动幅度异常增大达60%,这种不稳定的力学环境可能加速椎间盘的疲劳损伤[21]。 慢性的异常神经调控还会引发伤害性反射失衡。腰痛患者的伤害性撤回反射在腹壁肌群与椎旁肌群之间呈现显著不对称性:腹壁肌肉的反应阈值升高25%,而椎旁肌群的反应阈值反而降低15%[30],这种反射性收缩的强度差异导致脊柱承受异常的瞬时扭矩(峰值力矩差异达40%),长期作用可能诱发纤维环微损伤,进一步加剧退变进程[30]。 更深入的研究揭示,腹横肌功能障碍与椎间盘退变之间存在双向促进的恶性循环。一方面,腹横肌的失用导致腰椎节段稳定性下降,活动度增加20%-30%[22],异常的生物力学负荷加速椎间盘退化;另一方面,退变椎间盘释放的炎症因子(如肿瘤坏死因子α)通过胸腰筋膜等途径进一步抑制腹横肌的神经支配[31],形成自我强化的病理循环,这一过程还伴随着肌肉组织的进行性脂肪浸润(年进展率8%-12%)和运动皮质的功能重组(功能性核磁共振成像显示功能区偏移15%)[26,32],使得病情呈现慢性化趋势。 长期的功能代偿还会引发系统性病理重构。腹外斜肌和腹内斜肌的代偿性肥大(厚度增加15%-22%)可能加剧腰椎前凸[33-34],而腰大肌-腰方肌的区域性代偿则改变了正常的负荷分布模式,致压力峰值偏移30%[35-36]。远端肌群如臀大肌也参与这一代偿网络,其活动抑制(肌电降低40%-45%)会影响整个骨盆-脊柱动力链的协调性[37-38],这种全身性的适应性改变虽然短期内可能维持基本功能,但长期来看会进一步扭曲脊柱的正常生物力学环境,为椎间盘退变创造有利条件。 运动控制训练:运动控制训练作为一种针对腰痛患者的康复干预手段,主要通过增强核心肌群(尤其是腹横肌)的神经肌肉控制能力来改善临床症状。现有循证医学证据表明,运动控制训练可显著降低慢性腰痛患者的疼痛程度(视觉模拟评分降低40%-60%)和功能障碍指数(Oswestry功能障碍指数改善35%-45%)[19]。XU等[39]的系统综述从多角度阐明了运动控制训练的作用机制:①中枢神经系统层面,通过重塑运动皮质对核心肌群的调控模式,功能性核磁共振成像显示初级运动皮质激活区域扩大15%-20%;②外周神经肌肉层面,改善腹横肌的募集时序(肌电活动起始提前50-80 ms)和收缩效率(厚度增加25%-30%);③分子生物学层面,下调促炎因子使白细胞介素6、肿瘤坏死因子α水平降低30%-50%,并促进神经营养因子分泌增加两三倍。 运动控制训练不仅通过改善肌肉控制和脊柱稳定性缓解腰痛,还可能通过调节中枢神经功能发挥治疗作用。近期一项静息态功能性核磁共振成像研究表明,6周运动控制训练干预后,腰痛患者双侧枕中回的低频振幅值显著增高,提示该区域神经元自发性活动增强[40],进一步分析发现,左侧枕中回低频振幅值的增加与疼痛灾难化量表评分改善呈负相关,表明运动控制训练可能通过调节枕中回神经活动,改善疼痛相关心理障碍。 枕中回参与视觉-情绪整合调节,其功能改变可能与慢性疼痛的情绪认知加工有关,运动控制训练通过增强该脑区活动,促进负面情绪调节,从而间接缓解疼痛。这一发现为运动控制训练的中枢机制提供了新视角,提示未来可结合神经调控技术进一步优化治疗效果。 仰卧屈髋试验:仰卧屈髋试验作为运动控制训练的关键组成部分,它的疗效机制得到CHON等[41]研究的进一步验证。该研究采用超声影像学测量发现,经过8周踝背屈肌-腹横肌协同收缩训练后,受试者腹横肌厚度显著增加[健康组:(18.2±2.1) mm→(22.5±2.3) mm;腰痛组:(15.8±1.9) mm→(20.3±2.0) mm,P < 0.01],这种训练效果可能源于:①通过远端-近端肌肉链的协同激活,增强腹横肌的神经驱动使肌电振幅提高35%-45%;②改善腰椎-骨盆节段的动力学耦合使节段间位移减少1.2-1.5 mm。基于腹横肌在维持腰椎稳定性中的核心作用(可降低L4-L5节段负荷20%-25%[2]),仰卧屈髋试验作为代表性靶向训练为椎间盘退变相关腰痛提供了具有循证依据的康复方案。 病理生理机制整合与临床启示:腹横肌功能减退通过“神经调控异常→力学稳定性下降→代偿性结构改变→炎症微环境形成”的级联反应,构建了一个复杂的椎间盘退变促进网络。最新研究强调,针对这一网络的干预需要采取多靶点策略:既要通过运动控制训练重塑中枢神经调控模式[39],也要利用仰卧屈髋试验等技术改善外周力学环境[41],同时还需要关注全身代偿性改变的整体调控,这种系统性的治疗理念,为打破椎间盘退变的恶性循环提供了新的思路。 分子机制:椎间盘退变过程中,与力学微环境密切相关的关键信号通路为 Piezo1-F-actin- YAP通路。Piezo1 是一种机械敏感性阳离子通道,广泛表达于多种组织,参与多种生理与病理过程。研究表明,Piezo1在椎间盘退变中表达上调,且Piezo1表达水平与疾病严重程度呈正相关[42]。Piezo1激活后可介导钙离子内流,进而促进F-actin细胞骨架聚合;F-actin重组进一步激活 YAP信号[43]。YAP异常激活可促使细胞外基质降解、炎症反应加剧及软骨细胞钙化,从而加速椎间盘退变进程。因此,增强腰椎核心肌群功能有助于减轻椎间盘异常负荷,从力学源头上降低对Piezo1通路的刺激,进而延缓椎间盘退变。 YAP的激活状态尤其值得关注。作为Hippo通路中的关键共转录因子,YAP经 LATS1/2激酶磷酸化后滞留于胞质并降解;而在Hippo通路抑制时,未磷酸化的YAP可入核与 TEAD等转录因子结合,启动促增殖、存活与迁移等相关基因的转录[44]。YAP在椎间盘退变中表现出复杂的双相调控作用:在晚期退变中,氧化应激和高机械应力通过Piezo1-Ca2?-F-actin非经典通路激活YAP,主要作用于软骨终板细胞,促进钙化并加剧退变[42,45];而在早期退变或修复阶段,轻度机械刺激与低氧环境可通过经典Hippo通路激活YAP作用于髓核细胞,促进细胞增殖与细胞外基质合成,从而延缓椎间盘退变进展[44]。该双相效应的机制主要源于YAP下游靶基因的差异:非经典Piezo1通路诱导病理性基因(如炎症因子)表达,而经典Hippo通路则激活保护性基因(如Sox9、Aggrecan、结缔组织生长因子)表达,细胞类型(如软骨终板细胞与髓核细胞)及微环境差异(晚期退化与早期修复环境)可能是造成该差异的重要因素。值得注意的是,YAP的转录输出不仅取决于核转位状态,还受到转录复合物组成与表观遗传环境的调控,这一发现对未来针对YAP的分子治疗具有重要启示:不仅需严格区分疾病阶段,也提示核心肌群训练与分子靶向干预联合应用时需注意时序配合。YAP在椎间盘退变中的双相效应见表1。 此外,椎间盘退变中核因子E2相关因子2/核因子κB通路亦发挥重要作用。退变微环境中活性氧过量可激活核因子E2相关因子2与核因子κB:活性氧通过修饰Keap1蛋白促进核因子E2相关因子2核转位,启动抗氧化基因(如血红素加氧酶1)转录,同时激活核因子κB介导的炎症反应。值得注意的是,YAP可与核因子E2相关因子2基因启动子区结合,增强转录活性,提升抗氧化能力,并可抑制核因子κB转录活性,降低肿瘤坏死因子α、白细胞介素6、白细胞介素1β等促炎因子表达[46]。因此,YAP在调控氧化应激与炎症反应中具有"
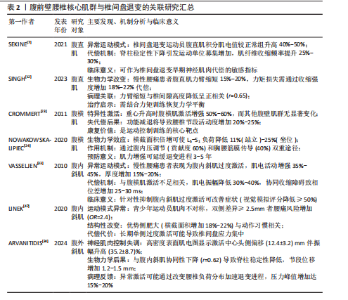
核心地位,其作为治疗靶点的潜力将在后续干预策略中进一步探讨。 2.1.3 腹内斜肌 研究表明,慢性腰痛患者的腹壁肌肉存在特征性的功能紊乱模式。VASSELJEN等[33]的肌电图研究证实,通过特异性激活腹横肌同时抑制腹内斜肌的治疗策略可显著缓解腰痛症状,使视觉模拟评分降低≥50%(P < 0.01),主要在于慢性腰痛患者普遍表现出腹内斜肌的异常运动模式:肌电活动增强35%-45%,超声测量肌肉厚度增加15%-20%,与腹横肌激活不足(肌电振幅降低30%-40%)形成鲜明对比,这种协同收缩障碍导致腹壁肌肉运动协调性下降(相位差增加25-30 ms),进而使脊柱稳定性降低[33]。 LINEK等[47]的前瞻性队列研究进一步揭示了腹内斜肌不对称性的临床意义。在青少年足球运动员中,腹内斜肌厚度差异≥2.5 mm的个体在6个月观察期内腰痛发生率显著增高(OR=2.4,95%CI:1.6-3.8);MRI影像分析显示,这种不对称性主要源于优势侧肌肉肥大,横截面积增加达18%-22%,可能机制为运动模式异常导致的单侧过度激活、生物力学代偿引起的适应性肥大及神经肌肉控制失调。 上述这些发现提示,腹内斜肌的功能异常,包括过度激活和不对称性可能是椎间盘退变的早期生物力学标志,通过改变腰椎负荷分布(压力峰值增加15%-20%)加速退变进程。未来研究需要结合动态MRI和表面肌电技术,进一步阐明这种肌肉功能紊乱与椎间盘退变间的时空关联。 2.1.4 腹外斜肌 ARVANITIDIS等[34]通过高密度表面肌电图(high-density surface electromyography,HDsEMG)对腰痛患者腹外斜肌的肌电活动特征进行了深入研究。研究结果显示,在脊柱屈曲运动过程中,腰痛患者的腹外斜肌表现出显著的神经肌肉控制异常,具体表现为肌电活动振幅较健康对照组增加(35.2±8.7)%,同时肌肉激活中心向头侧偏移达(12.4±3.2) mm,这种异常激活模式与腹内斜肌的改变具有高度相关性(r=0.62,P < 0.01),共同导致腹壁肌肉协调性显著下降,表现为肌肉收缩相位差增加15- 20 ms,脊柱节段稳定性降低。 进一步分析表明,腹外斜肌的这种特征性改变反映了腰椎间盘退变患者的神经肌肉控制功能障碍。与腹直肌和腹内斜肌类似,腹外斜肌的异常激活模式可能是由于中枢神经系统对躯干肌肉的调控策略发生改变所致,这种多块腹壁肌肉的协同功能障碍不仅降低了脊柱的动态稳定性,还可能通过改变腰椎负荷分布而加速椎间盘退变进程。研究结果提示,在临床评估和治疗腰椎退行性疾病时,应当将腹外斜肌的功能状态纳入考量,并针对异常激活模式制定相应的康复策略。未来研究可结合动态MRI和生物力学建模技术,进一步量化腹外斜肌功能改变与椎间盘力学环境变化之间的关系。 腹前壁腰椎核心肌群与椎间盘退变的关联研究汇总见表2。 2.2 椎旁肌与腹后壁肌群 2.2.1 多裂肌、竖脊肌 椎旁肌群(包括多裂肌、竖脊肌和腰大肌)的脂肪浸润与椎间盘退变之"
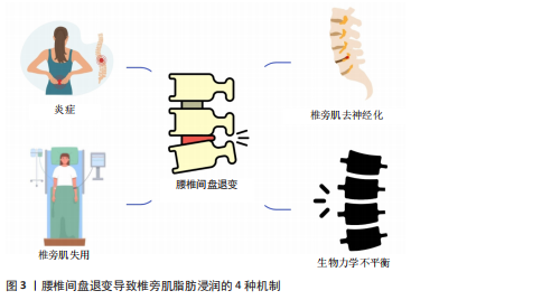
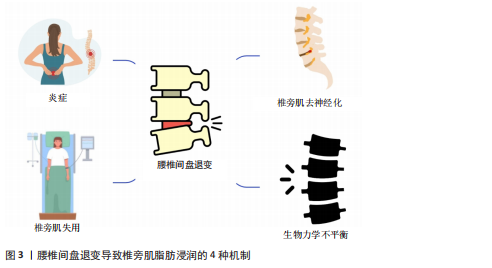
间存在明确的病理生理联系。根据JIANG等[2]的系统综述,这一关联主要通过4种相互关联的机制发挥作用。 炎症反应在疾病进程中起着关键作用。椎间盘退变过程中释放的肿瘤坏死因子α和白细胞介素1β等促炎因子可导致肌肉组织纤维化,表现为胶原沉积增加40%-60%,同时这些炎症因子还会引起椎旁肌横截面积的左右不对称性改变,研究显示这种不对称性差异可达15%-25%[31]。 神经损伤机制同样重要。椎间盘突出压迫神经根可导致支配区域肌肉的运动终板密度降低30%-50%,并引起肌纤维类型比例改变,其中Ⅰ型慢肌纤维比例可减少25%[48],这种神经源性损害直接影响肌肉的功能状态。 失用性萎缩在长期制动人群中表现尤为明显。研究数据显示,卧床患者和宇航员的椎旁肌横截面积每月递减2%-3%,而脂肪浸润比例则以每年8%-12%的速度递增[32],这种进行性改变与肌肉活动减少直接相关。 从生物力学角度看,椎间隙狭窄会导致黄韧带厚度增加35%-45%,进而引起腰椎节段稳定性下降,表现为活动度增加20%-30%,这种改变使椎旁肌承受异常负荷,导致肌纤维应力分布发生改变,最终形成继发性脂肪浸润,其年进展率约为10%[2]。 这些机制共同构成了椎旁肌退变与椎间盘退变之间的复杂病理网络。以上4种机制汇总见图3。 竖脊肌作为腰椎后方重要的稳定肌群,它"

的结构和功能状态与椎间盘退变密切相关。尽管SEYEDHOSEINPOOR等[49]的系统综述表明,腰痛患者竖脊肌的整体横截面积和脂肪浸润程度与健康人群相比无显著差异,但竖脊肌在腰椎稳定性维持及退变进程中的角色仍不容忽视。近年来基于深度学习的高精度MRI研究揭示,竖脊肌实际上可进一步分为髂肋肌与最长肌2个功能亚单位,肌肉在退变过程中可能呈现差异化改变[50]。例如,在L2-L5节段,髂肋肌的横截面积随椎间盘水平下降而逐渐减小,而脂肪浸润程度在腰痛患者中虽整体不高,但仍存在局部微结构改变。竖脊肌与多裂肌、腰大肌等核心肌群共同构成腰椎的“肌性铠甲”,肌群功能失衡可通过改变腰椎负荷传递模式,进一步加剧椎间盘机械应力分布异常[13],尤其在代偿性姿势或运动模式下,竖脊肌可能出现过度激活或抑制,影响脊柱-骨盆链的整体协调性[51]。因此,在评估与干预腰椎退行性病变时,需将竖脊肌纳入核心肌群协同网络中进行整体考量,而非孤立视之。 2.2.2 腰方肌与腰大肌 现有研究揭示了腰大肌与腰方肌在腰椎退变中的特殊作用模式。SIONS等[52]针对102例老年腰椎间盘退变患者的影像学研究显示,虽然多裂肌和竖脊肌表现出显著的形态学改变,横截面积减少(15.2±3.8)%,脂肪浸润增加(22.5±6.3)%(P < 0.01),但腰大肌和腰方肌在横截面积(变化< 5%,P=0.32)和脂肪浸润程度[增加(7.8±4.1)%,P=0.15]方面均未达到统计学差异,这一结果提示这两块肌肉可能通过功能调节而非结构改变参与病理过程。 进一步的功能学研究发现了更为复杂的代偿机制。PARK等[35]的研究表明,当患者处于坐姿脊柱后凸位时,竖脊肌激活不足的亚组表现出明显的腰方肌后部和腰大肌代偿性激活增强,这种代偿现象在未分亚组的整体比较中并不显著,说明具有特定的病理生理学背景。后续研究在脊柱功能评估中观察到更为精细的代偿模式[36]:在脊柱伸展动作中,腰痛患者的腰大肌腹外侧部活动显著降低[(25.4±6.7)%,P < 0.05],而腹内侧部与腰方肌则呈现协同激活增强[(32.1±7.9)%,P < 0.01],这种区域内(腰大肌-腰方肌)与区域间(竖脊肌-腰大肌/腰方肌)的双重代偿机制,反映了神经系统对脊柱稳定性下降的精确调节能力。 这些发现具有重要的临床启示:首先,腰大肌和腰方肌在腰椎退变中主要表现出功能性重组而非结构改变;其次,代偿模式具有动作特异性,不同体位和运动状态下呈现差异化的激活特征;最后,这种代偿机制可能成为针对性康复治疗的潜在靶点。未来研究需要采用更精细的肌群分区和动作分析方法,以深入揭示这些代偿机制的具体调控规律。 椎旁肌与腹壁后肌群与椎间盘退变的关联研究汇总见表3。 2.3 髋部核心肌群 SEBRO等[53]通过CT评估发现,在多变量分析中,臀大肌脂肪浸润(表现为密度降低)是唯一能准确预测椎间盘退变的肌肉指标。FR?CZ等[54]的MRI研究进一步显示,超过50%的椎间盘退变伴腰痛患者存在疼痛侧臀大肌、臀小肌和梨状肌横截面积减小,其中臀中肌在右侧疼痛患者中未见明显萎缩,可能机制有两点:一是优势侧代偿,对于右利手患者(约占90%),右下肢常为优势支撑侧,日常活动中右侧臀中肌持续接受更高强度的神经肌肉激活刺激,这种生理性激活模式可能抵消了椎间盘退变导致的失用性萎缩[55];二是疼痛侧保护性代偿,疼痛侧骨盆稳定性需求增加,神经系统通过增强同侧臀中肌的募集维持步态平衡,与健侧相比产生“超负荷保护”,该现象在单侧腰痛患者中表现显著[54]。AMABILE等[56]的研究证实,女性腰痛患者双侧臀大肌横截面积均显著减小。结合椎间盘退变作为腰痛主要病因的共识[2],提示臀大肌萎缩可能与椎间盘退变存在病理关联。 在功能研究方面,MOHAMED等[37]和CHOI等[57]通过肌电图均观察到腰椎不稳定患者臀大肌活动度降低,这一发现与AMABILE等[38] 的研究结果相互印证,后者表明经常进行爬楼梯等臀大肌激活活动的人群腰痛发生率较低,尤其在女性和急性腰痛患者中更为显著。COOPER等[58]则发现腰痛患者存在臀中肌肌力减弱和压痛现象。值得注意的是,OTHMAN等[59]研究提示,合并梨状肌综合征的腰椎不稳定患者表现出更显著的臀大肌功能抑制,且髋部肌肉形态学改变具有特异性。髋部核心肌群与椎间盘退变的关联研究汇总见表4。 2.4 多肌群协同机制整合及多因素分析实例 2.4.1 三类核心肌群失能模式总结 前文已系统阐述了腰椎核心肌群中三类关键肌群的失能模式,在此做出总结:①腹前壁拮抗代偿:腹横肌抑制(激活不足、横截面积减小)伴随腹内/外斜肌过度激活;②腰方肌区域双重代偿:区域内腰大肌-腰方肌功能重组,区域间竖脊肌-腰方肌/腰大肌协同异常;③臀肌失衡:臀大肌脂肪浸润与活动抑制,伴臀中肌优势侧保护性代偿。这些模式并非孤立存在,而是构成一个多肌群协同失衡网络,共同促使腰椎稳定性下降,加速椎间盘退变进程。 2.4.2 多肌群多因素分析实例 SEBRO等[53]一项CT多因素分析为此提供了直接临床证据。该研究同时评估了腹壁、椎旁及臀肌等共8组肌肉的CT密度(反映脂肪浸润程度),并在校正年龄、性别和体质量指数后进行了多变量回归分析,结果发现,在所有肌肉中,仅臀大肌密度是椎间盘退变的独立预测因子(OR=3.2,95%CI:1.8-5.6),而仅腹横肌密度与小关节退变显著相关(P=0.019)。这一结果提示,不同肌肉在退变过程中的作用具有特异性,且多肌群协同评估比单一肌群更能揭示退变的生物力学基础。 2.4.3 多肌群协同失衡与椎间盘退变关联机制分析 基于上述发现,进一步提出多肌群协同失衡与椎间盘退变之间的两条核心病理联系机制:①骨盆-脊柱动力轴破坏:臀肌(尤其是臀大肌)薄弱导致髋关节稳定性下降,腰肌(如腰大肌、腰方肌)代偿性负荷增加,引发骨盆前倾。这一姿势改变使腹直肌力臂缩短,力矩减小,需增强收缩以维持脊柱稳定[12],同时腹横肌因不在最适初长度而肌力下降,进一步促"

| [1] IWAI K, KOYAMA K, OKADA T, et al. Asymmetrical and smaller size of trunk muscles in combat sports athletes with lumbar intervertebral disc degeneration. Springerplus. 2016;5(1):1474. [2] JIANG J, HUANG Y, HE B. Advances in the interaction between lumbar intervertebral disc degeneration and fat infiltration of paraspinal muscles: critical summarization, classification, and perspectives. Front Endocrinol (Lausanne). 2024;15:1353087. [3] SUNG PS, O’SULLIVAN E, PARK MS. The reaction times and symmetry indices in the bilateral trunk and limb muscles in control subjects and subjects with low back pain that persisted two months or longer. Eur Spine J. 2021;30(10):2975-2982. [4] SPRINGER BA, MIELCAREK BJ, NESFIELD TK, et al. Relationships among lateral abdominal muscles, gender, body mass index, and hand dominance. J Orthop Sports Phys Ther. 2006;36(5):289-297. [5] GILDEA JE, HIDES JA, HODGES PW. Morphology of the abdominal muscles in ballet dancers with and without low back pain: a magnetic resonance imaging study. J Sci Med Sport. 2014;17(5):452-456. [6] HIDES J, STANTON W, FREKE M, et al. MRI study of the size, symmetry and function of the trunk muscles among elite cricketers with and without low back pain. Br J Sports Med. 2008;42(10):809-813. [7] SEKINE C, MATSUNAGA N, OKUBO Y, et al. Lumbar Intervertebral Disc Degeneration Does Not Affect Muscle Synergy for Rowing Activities. Appl Bionics Biomech. 2021;2021:6651671. [8] MERLETTI R, MUCELI S. Tutorial. Surface EMG detection in space and time: Best practices. J Electromyogr Kinesiol. 2019;49:102363. [9] CLANCY EA, MORIN EL, HAJIAN G, et al. Tutorial. Surface electromyogram (sEMG) amplitude estimation: Best practices. J Electromyogr Kinesiol. 2023;72:102807. [10] HUANG P, LU X, GUO L, et al. Study on diagnosis and treatment of lumbar disc herniation and related factors based on dynamic electromyography. Zhongguo Gu Shang. 2022; 35(10):984-989. [11] TAGUCHI N, IZUMI S, MIYAKAWA S. Analysis of trunk rotation during baseball batting with lumbar disc degeneration. Fukushima J Med Sci. 2023;69(1):1-10. [12] SINGH R, KUMAR P, WADHWANI J, et al. Do MRI-derived muscle moment-arms in patients with chronic low back pain differ from healthy individuals? A comparative study. Eur Spine J. 2023;32(4):1115-1122. [13] WANG Z, ZHAO Z, HAN S, et al. Advances in research on fat infiltration and lumbar intervertebral disc degeneration. Front Endocrinol (Lausanne). 2022;13:1067373. [14] SHI L, YAN B, JIAO Y, et al. Correlation between the fatty infiltration of paraspinal muscles and disc degeneration and the underlying mechanism. BMC Musculoskelet Disord. 2022;23(1):509. [15] PEZOLATO A, DE VASCONCELOS EE, DEFINO HL, et al. Fat infiltration in the lumbar multifidus and erector spinae muscles in subjects with sway-back posture. Eur Spine J. 2012;21(11):2158-2164. [16] YUAN S, WANG H, ZHOU J. Prevalence and risk factors of low back and pelvic pain in women with rectus abdominis diastasis: a multicenter retrospective cohort study. Korean J Pain. 2022; 35(1):86-96. [17] WU L, GU Y, GU Y, et al. Diastasis recti abdominis in adult women based on abdominal computed tomography imaging: Prevalence, risk factors and its impact on life. J Clin Nurs. 2021;30(3-4):518-527. [18] SOKUNBI G, CAMINO-WILLHUBER G, PASCHAL PK, et al. Is Diastasis Recti Abdominis Associated With Low Back Pain? A Systematic Review. World Neurosurg. 2023;174:119-125. [19] FERREIRA PH, FERREIRA ML, MAHER CG, et al. Changes in recruitment of transversus abdominis correlate with disability in people with chronic low back pain. Br J Sports Med. 2010;44(16):1166-1172. [20] UNSGAARD-TØNDEL M, LUND NILSEN TI, MAGNUSSEN J, et al. Is activation of transversus abdominis and obliquus internus abdominis associated with long-term changes in chronic low back pain? A prospective study with 1-year follow-up. Br J Sports Med. 2012;46(10):729-734. [21] CRESSWELL AG, GRUNDSTRÖM H, THORSTENSSON A. Observations on intra-abdominal pressure and patterns of abdominal intra-muscular activity in man. Acta Physiol Scand. 1992;144(4):409-418. [22] BARKER PJ, GUGGENHEIMER KT, GRKOVIC I, et al. Effects of tensioning the lumbar fasciae on segmental stiffness during flexion and extension: Young Investigator Award winner. Spine (Phila Pa 1976). 2006;31(4):397-405. [23] CROMMERT ME, EKBLOM MM, THORSTENSSON A. Activation of transversus abdominis varies with postural demand in standing. Gait Posture. 2011;33(3):473-477. [24] NOWAKOWSKA-LIPIEC K, MICHNIK R, LINEK P, et al. A numerical study to determine the effect of strengthening and weakening of the transversus abdominis muscle on lumbar spine loads. Comput Methods Biomech Biomed Engin. 2020;23(16):1287-1296. [25] HIDES JA, LAMBRECHT G, SEXTON CT, et al. The effects of exposure to microgravity and reconditioning of the lumbar multifidus and anterolateral abdominal muscles: implications for people with LBP. Spine J. 2021;21(3):477-491. [26] LI X, LIU H, GE L, et al. Cortical Representations of Transversus Abdominis and Multifidus Muscles Were Discrete in Patients with Chronic Low Back Pain: Evidence Elicited by TMS. Neural Plast. 2021; 2021:6666024. [27] TSAO H, TUCKER KJ, HODGES PW. Changes in excitability of corticomotor inputs to the trunk muscles during experimentally-induced acute low back pain. Neuroscience. 2011;181:127-133. [28] SUO M, ZHANG J, SUN T, et al. The association between morphological characteristics of paraspinal muscle and spinal disorders. Ann Med. 2023;55(2):2258922. [29] HODGES P, KAIGLE HOLM A, HOLM S, et al. Intervertebral stiffness of the spine is increased by evoked contraction of transversus abdominis and the diaphragm: in vivo porcine studies. Spine (Phila Pa 1976). 2003;28(23):2594-2601. [30] MASSÉ-ALARIE H, HAMER GV, SALOMONI SE, et al. Nociceptive withdrawal reflexes of the trunk muscles in chronic low back pain. PLoS One. 2023;18(6):e0286786. [31] JAMES G, CHEN X, DIWAN A, et al. Fat infiltration in the multifidus muscle is related to inflammatory cytokine expression in the muscle and epidural adipose tissue in individuals undergoing surgery for intervertebral disc herniation. Eur Spine J. 2021;30(4):837-845. [32] DE MARTINO E, HIDES J, ELLIOTT JM, et al. Intramuscular lipid concentration increased in localized regions of the lumbar muscles following 60 day bedrest. Spine J. 2022;22(4):616-628. [33] VASSELJEN O, FLADMARK AM. Abdominal muscle contraction thickness and function after specific and general exercises: a randomized controlled trial in chronic low back pain patients. Man Ther. 2010;15(5):482-489. [34] ARVANITIDIS M, JIMÉNEZ-GRANDE D, HAOUIDJI-JAVAUX N, et al. Low Back Pain-Induced Dynamic Trunk Muscle Control Impairments Are Associated with Altered Spatial EMG-Torque Relationships. Med Sci Sports Exerc. 2024;56(2):193-208. [35] PARK RJ, TSAO H, CLAUS A, et al. Recruitment of discrete regions of the psoas major and quadratus lumborum muscles is changed in specific sitting postures in individuals with recurrent low back pain. J Orthop Sports Phys Ther. 2013;43(11): 833-840. [36] PARK RJ, TSAO H, CRESSWELL AG, et al. Changes in direction-specific activity of psoas major and quadratus lumborum in people with recurring back pain differ between muscle regions and patient groups. J Electromyogr Kinesiol. 2013; 23(3):734-740. [37] MOHAMED RR, ABDEL-AZIEM AA, MOHAMMED HY, et al. Chronic low back pain changes the latissmus dorsi and gluteus maximus muscles activation pattern and upward scapular rotation: A cross-sectional study. J Back Musculoskelet Rehabil. 2022;35(1):119-127. [38] AMABILE AH, LARSON SL, HOGLUND LT, et al. Greater number of weekly stairs climbed is associated with lower low back pain prevalence among female but not male physical therapists. PLoS One. 2023;18(10):e0292489. [39] XU HR, ZHANG YH, ZHENG YL. The effect and mechanism of motor control exercise on low back pain: a narrative review. EFORT Open Rev. 2023;8(7):581-591. [40] 张婵娟,李悦龙,张洲,等.运动控制训练改善慢性非特异性腰痛的fMRI研究[J].中国康复医学杂志,2022,37(3):303-310. [41] CHON SC, YOU JH, SALIBA SA. Cocontraction of ankle dorsiflexors and transversus abdominis function in patients with low back pain. J Athl Train. 2012;47(4):379-389. [42] PENG F, SUN M, JING X, et al. Piezo1 promotes intervertebral disc degeneration through the Ca2+/F-actin/Yap signaling axis. Mol Med. 2025; 31(1):90. [43] ZHANG C, WANG F, XIE Z, et al. AMOT130 linking F-actin to YAP is involved in intervertebral disc degeneration. Cell Prolif. 2018;51(6):e12492. [44] ZHENG-WEI S, YUAN T, CHAO-SHUAI F, et al. Roles of Hippo-YAP/TAZ signalling in intervertebral disc degeneration. Biomed Pharmacother. 2023; 159:114099. [45] HU T, SHI Z, SUN Y, et al. SEPHS1 attenuates intervertebral disc degeneration by delaying nucleus pulposus cell senescence through the Hippo-Yap/Taz pathway. Am J Physiol Cell Physiol. 2024;326(2):C386-C399. [46] WU L, WANG Z, WU Z, et al. Therapeutic targeting of Nrf2/HO-1/NF-κB signaling axis with casticin mitigates intervertebral disc degeneration: in vitro and in vivo investigations. In Vitro Cell Dev Biol Anim. 2025. doi: 10.1007/s11626-025-01108-0. [47] LINEK P, NOORMOHAMMADPOUR P, MANSOURNIA MA, et al. Morphological changes of the lateral abdominal muscles in adolescent soccer players with low back pain: A prospective cohort study. J Sport Health Sci. 2020;9(6):614-619. [48] YALTIRIK K, GÜDÜ BO, IŞIK Y, et al. Volumetric Muscle Measurements Indicate Significant Muscle Degeneration in Single-Level Disc Herniation Patients. World Neurosurg. 2018;116:e500-e504. [49] SEYEDHOSEINPOOR T, TAGHIPOUR M, DADGOO M, et al. Alteration of lumbar muscle morphology and composition in relation to low back pain: a systematic review and meta-analysis. Spine J. 2022;22(4):660-676. [50] XU Y, ZHENG S, TIAN Q, et al. Deep learning-based structure segmentation and intramuscular fat annotation on lumbar magnetic resonance imaging. JOR Spine. 2024;7(3):e70003. [51] SMITH JA, STABBERT H, BAGWELL JJ, et al. Do people with low back pain walk differently? A systematic review and meta-analysis. J Sport Health Sci. 2022;11(4):450-465. [52] SIONS JM, ELLIOTT JM, POHLIG RT, et al. Trunk Muscle Characteristics of the Multifidi, Erector Spinae, Psoas, and Quadratus Lumborum in Older Adults With and Without Chronic Low Back Pain. J Orthop Sports Phys Ther. 2017;47(3):173-179. [53] SEBRO R, O’BRIEN L, TORRIANI M, et al. Assessment of trunk muscle density using CT and its association with degenerative disc and facet joint disease of the lumbar spine. Skeletal Radiol. 2016;45(9):1221-1226. [54] FRĄCZ W, MATUSKA J, SZYSZKA J, et al. The Cross-Sectional Area Assessment of Pelvic Muscles Using the MRI Manual Segmentation among Patients with Low Back Pain and Healthy Subjects. J Imaging. 2023;9(8):155. [55] LEE SK, LEE SY, JUNG JM. Muscle activity of the gluteus medius at different gait speeds. J Phys Ther Sci. 2014;26(12):1915-1917. [56] AMABILE AH, BOLTE JH, RICHTER SD. Atrophy of gluteus maximus among women with a history of chronic low back pain. PLoS One. 2017;12(7): e0177008. [57] CHOI WJ, KIM WD, PARK DC, et al. Comparison of compensatory lumbar movement in participants with and without non-specific chronic low back pain: A cross-sectional study. J Back Musculoskelet Rehabil. 2022;35(6):1365-1372. [58] COOPER NA, SCAVO KM, STRICKLAND KJ, et al. Prevalence of gluteus medius weakness in people with chronic low back pain compared to healthy controls. Eur Spine J. 2016;25(4):1258-1265. [59] OTHMAN IK, RAJ NB, SIEW KUAN C, et al. Association of Piriformis Thickness, Hip Muscle Strength, and Low Back Pain Patients with and without Piriformis Syndrome in Malaysia. Life (Basel). 2023;13(5):1208. [60] 黄吉成.TAZ对炎症反应中小鼠小胶质细胞的保护作用及机制[D].长春:吉林大学,2020. [61] HUANG JC, YUE ZP, YU HF, et al. TAZ ameliorates the microglia-mediated inflammatory response via the Nrf2-ROS-NF-κB pathway. Mol Ther Nucleic Acids. 2022;28:435-449. |
| [1] | Zhu Xiaolong, Zhang Wei, Yang Yang. Visualization analysis of research hotspots and cutting-edge information in the field of intervertebral disc regeneration and repair [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2391-2402. |
| [2] | Zhou Tianle, Wang Wei, Zhang Zhiwen, Liu Ximing. Application and progress of transcriptomics and proteomics techniques in the study of intervertebral disc degeneration [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(23): 5925-5933. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||

