Chinese Journal of Tissue Engineering Research ›› 2021, Vol. 25 ›› Issue (25): 4082-4088.doi: 10.12307/2021.024
Previous Articles Next Articles
Culture, research and application of patient-derived tumor organoids
Feng Ziyi, Liang Shanshan, Yu Weiting, Wang Ruoyu
- Liaoning Provincial Key Laboratory for High Throughput Screening and Targeted Drug Transformation of Molecular Markers of Breast and Digestive Tumors, Affiliated Zhongshan Hospital of Dalian University, Dalian 116001, Liaoning Province, China
-
Received:2020-07-11Revised:2020-07-14Accepted:2020-09-05Online:2021-09-08Published:2021-03-30 -
Contact:Yu Weiting, MD, Researcher, Liaoning Provincial Key Laboratory for High Throughput Screening and Targeted Drug Transformation of Molecular Markers of Breast and Digestive Tumors, Affiliated Zhongshan Hospital of Dalian University, Dalian 116001, Liaoning Province, China Wang Ruoyu, MD, Chief physician, Liaoning Provincial Key Laboratory for High Throughput Screening and Targeted Drug Transformation of Molecular Markers of Breast and Digestive Tumors, Affiliated Zhongshan Hospital of Dalian University, Dalian 116001, Liaoning Province, China -
About author:Feng Ziyi, Master candidate, Liaoning Provincial Key Laboratory for High Throughput Screening and Targeted Drug Transformation of Molecular Markers of Breast and Digestive Tumors, Affiliated Zhongshan Hospital of Dalian University, Dalian 116001, Liaoning Province, China -
Supported by:Dalian Medical Science Research Project, No. 1811113 (to YWT)
CLC Number:
Cite this article
Feng Ziyi, Liang Shanshan, Yu Weiting, Wang Ruoyu. Culture, research and application of patient-derived tumor organoids[J]. Chinese Journal of Tissue Engineering Research, 2021, 25(25): 4082-4088.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
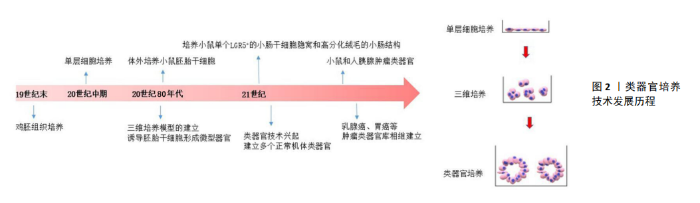
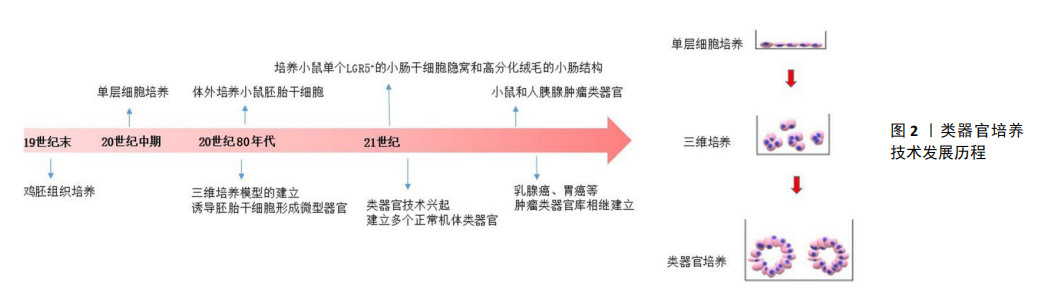
2.1 肿瘤类器官培养体系的建立 20世纪60年代至80年代,人们尝试利用胚胎干细胞在三维培养条件下诱导分化形成微型器官来研究器官的发育及功能[8],但由于操作复杂且成功率低而没有得到广泛应用。2009年,荷兰的Hans Clevers验室通过将小鼠单个LGR5+的小肠干细胞种植在含有ENR细胞因子组合(表皮生长因子、Noggin、R-spondin)的三维基质胶培养体系中,发现干细胞通过增殖分化形成了包含具有增殖功能的隐窝和高分化绒毛的小肠结构,且该结构中仍有LGR5+的干细胞,高效模拟了小肠形态结构及功能[9]。类器官培养技术由此兴起并迅速拓展,人们成功建立了包括大脑和胃等机体正常组织的类器官模型[10-11],并进一步试图将类器官技术运用到肿瘤等疾病的研究中。2014年,BOJ等[12]成功在体外培育出小鼠的胰腺肿瘤类器官,并在此基础上优化培养体系成功建立人胰腺导管癌类器官,通过对比原位肿瘤的基因测序发现包括Kras在内的基因突变都保持一致,这是肿瘤类器官的首次成功建立。随后人们又成功构建了结直肠癌[13]、胃癌[14]、前列腺癌[15]、膀胱肿瘤[16]、食道癌和子宫内膜癌等肿瘤类器官模型[17-18](见图2)。与传统肿瘤研究模型相比,肿瘤类器官可以最大程度地模拟肿瘤在体内的结构和功能,既能直观展现肿瘤生长的过程,又能反映患者个体差异,是一种直观、可靠、高效和避免伦理争议的器官水平研究体系,更加适合于体外的肿瘤生物学和治疗相关的研究。 利用肿瘤类器官进行相关研究的基础是肿瘤类器官培养体系的建立,现有报道的培养体系是基于对干细胞培养及三维培养的经验而来,即在优化三维培养的基质材料的同时,添加适当的细胞因子以维持细胞干性,促进其增殖及分化能力。由于癌种的区别和患者的个体化差异,肿瘤细胞的获得、所需细胞因子与基质材料也有所不同。 2.1.1 患者肿瘤细胞的获得 构建患者来源的肿瘤类器官,其细胞获取途径主要包括肿瘤组织来源、液体活检来源和肿瘤干细胞来源(见表1)。 (1)患者肿瘤组织来源:肿瘤组织主要是通过手术、组织活检等途径获得,通过酶消化方法进行组织处理得到肿瘤细胞来进行类器官培养。SACHS等[19]利用乳腺癌患者手术取得的肿瘤组织在剪碎、胶原酶消化及裂解红细胞等处理后得到单个悬浮的肿瘤细胞,将其种植于基底膜提取物,再加入含细胞因子的改良培养基成功培养出乳腺癌类器官。其中典型的乳腺癌类器官形态与患者原发肿瘤的组织病理学、激素受体状态和HER2表达情况相匹配。DNA拷贝数和序列变化在来源肿瘤与类器官中也是一致的,即使在传代后也可基本保持稳定;除了从患者的手术标本直接取材外,组织活检等微创途径得到的肿瘤组织也可以用于肿瘤类器官的培养。NUCIFORO等[20]将从肝癌针刺活检中得到的肿瘤组织用Ⅳ型胶原酶消化后接种到Ⅱ型基底膜提取物上,通过含不同细胞因子的培养基传代培养后得到肝癌类器官,并且发现其同样保留了原始肿瘤的组织形态和遗传学特征。这种直接通过患者肿瘤组织来源获取肿瘤细胞的方法是目前比较成熟、运用最广泛的肿瘤类器官建立方法,通过这种方法已经成功建立了胆管癌[21]、头颈鳞癌和结直肠癌等多种肿瘤类器官[22-23]。患者肿瘤组织来源建立的肿瘤类器官,具有与患者的个体特点一致性高、可以反映肿瘤体内真实的生物学特点、培养技术较成熟的优点,但不易监测患者临床动态变化,且从患者肿瘤组织中取材属于有创操作。 (2)患者液体活检来源:液体活检是利用患者血液、尿液、胸腹水等体液进行临床相关检验分析,是近年来新兴的临床诊疗手段,已有学者利用其成功建立肿瘤类器官。在恶性肿瘤患者的腹水中存在游离的肿瘤细胞,MARU等[24]利用离心收集妇科肿瘤患者癌性腹水中的细胞,裂解红细胞后得到单个肿瘤细胞,将其与慢病毒颗粒在基质胶上共同孵育过夜,第2天选择存活的细胞接种至基质胶上,并在其上层再覆盖一层基质胶形成“三明治”样结构,利用这种双层基质胶类器官培养方式提高了腹水来源的肿瘤类器官成功率。并且腹水来源的肿瘤类器官,不仅保留了原发灶肿瘤的囊性或筛状形态结构,也保留了ER、PR、p53等组织病理学特性。随着诊疗手段的进步,循环肿瘤细胞(circulating tumor cells,CTCs)被称为肿瘤远处转移的“种子”,可以代表原发灶及远处转移灶的某些表型[25]。Zhang等[26]从早期肺癌患者血样中通过CTC-芯片捕获血液样本中的CTCs,与成纤维细胞和细胞外基质共培养模拟肿瘤微环境,建立CTCs来源的肿瘤类器官,结果显示肿瘤类器官基因突变与原发肿瘤一致。随后他们利用CTCs来源的肿瘤类器官检测ALK阳性转移性肺癌患者对ALK抑制剂的治疗反应:分别在初次诊断、显示耐药及出现脑转移时进行血液采样,培养后进行分析,以ALK重排细胞个数> 15%为阳性标准,发现3次采样培养的CTCs肿瘤类器官均显示出ALK重排阳性;进行基因突变检测发现患者表现克唑替尼耐药及影像学进展时,CTCs类器官中显示L1196M突变;当脑转移发生时,肿瘤类器官中的L1196M突变消失。上述肿瘤类器官的研究结果与临床组织活检结果一致。这也表明CTCs衍生的肿瘤类器官可应用于临床药物疗效预测。通过患者液体活检来源进行肿瘤类器官的构建,具有无创、取材不受肿瘤部位限制以及可在肿瘤进展的不同阶段或用药前后随时动态观测的优点,但对微环境要求高,培养成功率低,且尚不能判断液体活检所获取的细胞是否具有肿瘤异质性。 (3)富集肿瘤干细胞来源:现有研究认为肿瘤干细胞是导致肿瘤异质性的重要原因之一,肿瘤干细胞是肿瘤组织中一类具有自我更新、增殖及分化潜能的细胞群,与肿瘤形成、转移和复发密切相关[27]。FENDLER等[28]从透明细胞肾细胞癌患者手术组织中利用流式细胞仪富集CXCR+MET+CD44+标记的肿瘤干细胞,并将其分别接种至悬浮培养基和基质胶内,1周后悬浮培养基中肿瘤干细胞形成紧密球状结构,而基质胶条件下形成空腔或管状类器官结构,苏木精-伊红染色进一步提示:基质胶条件下培养出的肿瘤类器官呈现出与原发肿瘤相似的组织结构;肿瘤类器官外侧细胞显示E-cadherin阳性,表明肿瘤类器官存在上皮分化,而悬浮培养出的肿瘤干细胞球外侧几乎不存在E-cadherin表达;标记肾脏近端小管刷状缘的LTL仅在肿瘤类器官中表达,透明细胞肾细胞癌的典型病理表现糖原沉积和脂滴,仅在肿瘤类器官中出现。不论是组织结构还是病理特征,肿瘤类器官均与实体肿瘤更相近,是更加合适的体外模型。HWANG等[29]为探究过表达c-met的干细胞在脑胶质瘤中的作用,首次从患者体内获得c-met突变的诱导性多能干细胞培育脑胶质瘤类器官模型,体外培养诱导性多能干细胞聚集体后接种至低附着培养皿内,加入E8培养基,细胞在第15天时逐渐向神经元细胞分化,最终形成神经元样脑胶质瘤类器官。该模型不仅表达高水平的胶质纤维酸性蛋白(人脑胶质瘤的典型标志),同时也表达了高水平的p-MET和p-STAT3,透射电镜显示肿瘤类器官中有中间丝生成,与原发性脑胶质瘤中表现一致。肿瘤干细胞来源的肿瘤类器官可分化形成与原发肿瘤中类似的异种细胞,实现了体外模型保留肿瘤异质性的目的,但对微环境要求高,培养成功率低。"
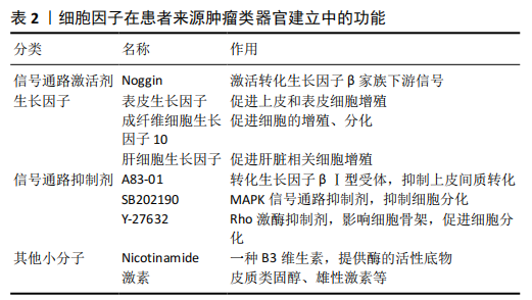
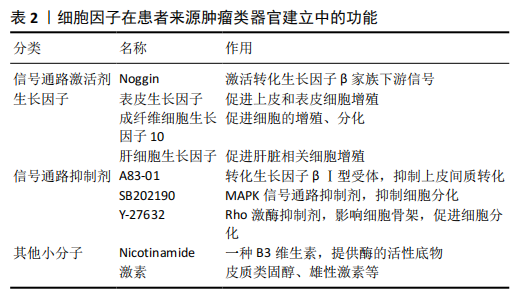
2.1.2 肿瘤类器官的培养 肿瘤微环境的体外重现是肿瘤类器官形成高度模拟体内组织的关键。主要的培养条件要素包括细胞因子和生物学材料,其中细胞因子可以促进肿瘤细胞的增殖、分化,而生物学材料模拟细胞外基质、提供生物力学等支撑。 (1)细胞因子:培养基是培养环境中最重要的组成部分,它为细胞生长提供必要的营养、生长因子和激素,还可以调节培养环境的pH值和渗透压[30]。而肿瘤类器官的培养除了基本培养基外,还需要加入包括相关通路激活剂或抑制剂和激素等不同类型的细胞因子来保障肿瘤细胞的生长,如在肝癌类器官培养中需要在正常肝类器官培养方案中去除R-Spondin1、Noggin和Wnt3a,并加入地塞米松和Rho激酶抑制剂,最终形成肝癌类器官。其中一些因子主要作用是促进肿瘤细胞的增殖,如表皮生长因子和成纤维细胞生长因子等属于所需的基本细胞因子;肿瘤干细胞的活性依赖Wnt通路和Notch通路的持续激活,而R-Spondin1作为Wnt信号通路的激动剂,不仅可以促进肿瘤细胞的增殖还可以控制分泌细胞的分化[31-32],在乳腺癌、结直肠癌等肿瘤类器官培养中是必要的细胞因子之一;为了抑制细胞发生上皮间质转化的分化,在前列腺癌等类器官中需要加入转化生长因子β信号通路的抑制剂A83-01[33]。除了这些基本因子外,不同肿瘤还需要一些关键因子:乳腺癌类器官的培养需要补充神经调节蛋白1,它是人表皮生长因子受体(Her) 3和4的配体,与乳腺癌的发生和发展密切相关,添加到肿瘤类器官培养基中可以提高乳腺癌肿瘤类器官形成率,且可以将传代次数延长至20次以上[19];肝癌类器官的培养中,需要加入肝细胞生长因子等因子特异性地促进肝癌细胞的增殖[20];恶性卵巢肿瘤主要驱动因素是P53的突变,因此在恶性卵巢癌类器官培养基中可添加Nutlin-3a[24]。此外还需要一些小分子物质,前列腺癌类器官需要加入雄激素,肝癌和胰腺肿瘤类器官中需要添加胃泌素,一些无机物质也作为营养辅助成分添加,如维生素C、烟酰胺等。这些因子的加入不仅利于培养出肿瘤类器官,且培养体系更加接近体内的肿瘤微环境,从而保证了体外培养的肿瘤类器官与原发灶肿瘤的基本特质的一致性(见表2)。 (2)患者来源肿瘤类器官基质材料:患者来源肿瘤类器官基质材料与类器官培养中所需的基质材料类似,模拟细胞外基质为细胞生长提供支持。患者来源肿瘤类器官的培养中用到生物学材料可以分为两类:一类是以基底膜提取物、基质胶为主的天然材料;另一类是人工合成材料。基质胶作为一种天然材料,目前在肿瘤类器官的培养中应用最为普遍,它是从EHS小鼠肉瘤中提取的可溶和无菌的基底膜蛋白,主要成分包括生长因子、层粘连蛋白、Ⅳ型胶原、巢蛋白及细胞因子等[34],其组成成分及其比例与人体基底膜相同。有研究表明基质胶可以促进乳腺上皮细胞生长并形成管样结构[35]、 还可以促进唾液腺细胞形成腺体[36]。正是因为基质胶可以模拟体内肿瘤生长的局部环境促进肿瘤类器官增殖和腺体分化的优点,所以被广泛用于多种肿瘤类器官培养。人工合成材料以合成高分子为主,因其孔隙结构、力学性能可控的优势也常被用于肿瘤类器官的培养,传统组织培养皿多为聚苯乙烯和玻璃,其机械刚度远高于人体软组织的刚度,导致细胞在传统培养中发生生物学行为改变。BALACHANDER等[37]将乳腺癌细胞MDA-MB-231接种到聚己内酯的多孔支架中,通过调控多孔支架的弹性模量,使其接近体内力学环境,还可以通过调控支架孔径与形态,更好地模拟乳腺组织的圆形腺泡结构,有利于形成与体内肿瘤类似组织结构的肿瘤类器官,并且发现该培养方式比二维培养的乳腺癌细胞侵袭转移能力更强。随后NAYAK等[38]将乳腺癌的癌症相关性成纤维细胞接种到多孔支架中制备细胞外基质,脱细胞处理后种植患者来源的乳腺癌细胞,培养更短的时间得到了乳腺癌肿瘤类器官,证明了癌症相关性成纤维细胞可促进乳腺癌增殖。肿瘤的分化、增殖和迁移等生物学行为是在一个三维环境下进行的,并与周围的基质存在相互作用,因此基质材料的运用可以尽可能的去模拟体内的真实环境,促进肿瘤类器官培养的成功。 "
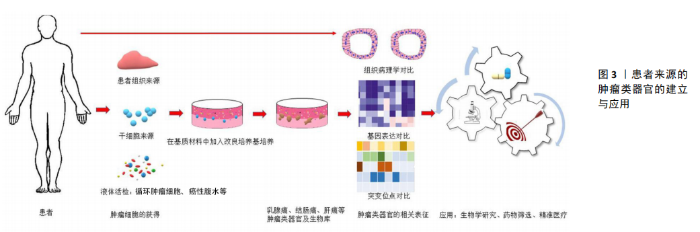
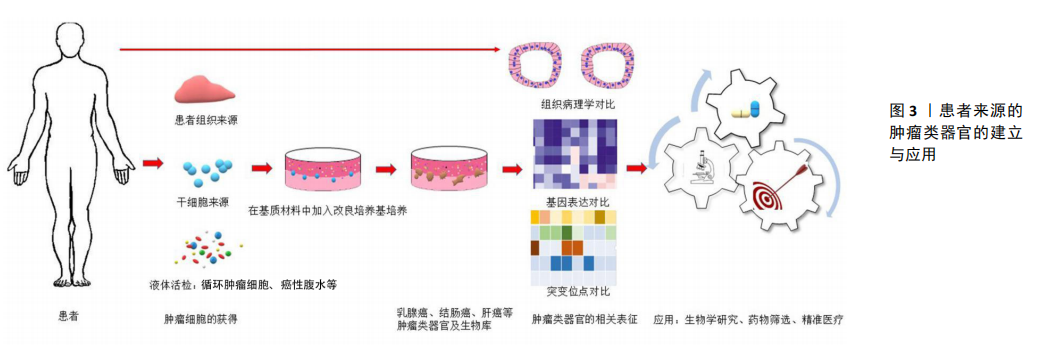
2.2 应用 随着组学研究的进展,利用蛋白组学、基因组学和代谢组学等高通量筛选技术,使得肿瘤生物学及抗肿瘤药物的研究效率显著提高,构建能够维持肿瘤体内特征的体外模型是提高转化效率的关键。肿瘤细胞系并不能良好的反映原始肿瘤的特征,而患者来源的肿瘤类器官极大的保留了肿瘤的异质性,并具有与体内高度相似的肿瘤微环境,经过长期体外培养也不会呈现明显的均一化,是肿瘤的生物学研究、新药筛选和个体化治疗等的优秀临床前模型(见图3)。 2.2.1 肿瘤的生物学研究 单层细胞的肿瘤生物学研究,研究对象以单细胞或细胞亚群为主,缺乏细胞与肿瘤微环境的联系,也无法在组织或器官等更高层次上研究肿瘤的生物学行为,这也是多种类细胞群或肿瘤微环境等肿瘤生物学研究的瓶颈。肿瘤类器官技术的开展,尤其针对患者来源的肿瘤类器官技术有望攻克上述瓶颈问题。SHIMOKAWA等[39] 对LGR5+肿瘤细胞进行标记后分析发现其在肿瘤发生过程中具有自我更新和分化能力,明确了LGR5+细胞的肿瘤干细胞特性,随后他们通过结直肠癌类器官技术进行培养,利用药物对患者来源的肿瘤类器官中LGR5+干细胞进行消耗,发现肿瘤类器官体积先变小后又增大的现象。进一步研究证实肿瘤类器官体积的恢复是因LGR5-细胞转化为具有增殖特性的细胞所致,但LGR5-的转化并不能完全代偿LGR5+消除,随后他们敲入KRT20标记分化的肿瘤细胞,发现肿瘤体积缩小之后KRT20+细胞去分化成具有自我更新和增殖能力的LGR5+细胞以维持肿瘤的继续生长。由此可见,与传统二维单层培养技术相比,肿瘤类器官技术实现了肿瘤生长过程的可视化,提供了肿瘤干细胞克隆动态和可塑性的研究方法,为寻找肿瘤治疗的潜在靶点提供了依据。细胞外囊泡是细胞间信息传递的重要载体,对早期癌症的诊断有帮助。APC基因突变激活Wnt通路,导致结直肠癌的发生,SZVICSEK等[40]在体外建立结直肠癌类器官,发现APC突变引起的Wnt激活可诱导细胞外囊泡产生,并且观察到细胞外基质分泌的蛋白也可促进细胞外囊泡的分泌,同时利用肿瘤类器官探索肿瘤与间质细胞作用发现成纤维细胞在低氧环境下可诱导结直肠癌类器官的形成。肿瘤类器官可以在体外再现肿瘤发生发展的过程,反映体内肿瘤组织与肿瘤微环境中其他类型细胞的相互作用等,这些都是原有的培养技术所无法完成的。 2.2.2 新药筛选 对于肿瘤的新药发现,无论是通过靶点结构的人工设计还是高通量筛选获得,在用于临床之前都需要一个实验模型来进行药物的测试。随着NCL-60由于低预测性被淘汰,基于患者肿瘤的异种移植体成为了新的金标准平台。虽然患者肿瘤的异种移植体可以在一定程度上保持肿瘤的异质性及相对的稳定性,但是由于移植成功率低、测试通量低、不能反映患者的免疫环境等固有缺点依然不能完美地反映药物的作用[41]。而PDO却可以克服这些短板,在药物筛选的应用上有着更佳的应用前景[42]。Hans Clevers等首次建立了一个由20个结直肠癌患者来源的肿瘤与对应正常组织的类器官组成的生物样本库,对83种药物组合包进行筛选(包括临床用药25种、化疗药物10种、正在进行临床试验的药物29种、针对不同癌症靶点的化合物29种),发现西妥昔单抗对于BRAF突变患者的类器官反应不敏感,Nutlin-3a对TP53基因突变的类器官敏感,这与之前的临床患者的回顾性研究结果相一致,同时发现了WNT分泌抑制剂对WNT负反馈调节因子RNF43突变的患者有潜在作用[23],这一发现对于指导临床治疗结直肠癌患者具有重大意义。为进一步促进药物高通量筛选,BOEHEKE等[43]在12孔板中利用患者来源的肿瘤细胞培育形成肿瘤类器官,再利用自动化平台将PDO单细胞悬液接种至384孔板中培养,4 d后形成具有空间结构的结肠癌类器官,对384孔板内形成的结肠癌类器官进行分析,检测ATP发光值比较各个孔之间PDO的生长空间均匀性,利用平板均匀性研究384孔内PDO的活性,分析测定了与药物验证相关指标,结果均显示PDO适用于自动化平台,可自动接种和给药,实现高通量及可重复的筛选研究。由于肿瘤类器官与患者体内肿瘤特性的一致,利用类器官的生物样本库进行药物敏感性的检测及新药的筛选十分具有优势,缩短了临床前试验与临床试验间的周期,减少了药物开发成本及风险。目前已经建立了包括乳腺癌、胃癌等多种癌肿的肿瘤类器官样本库,弥补了新药开发及筛选所需大规模临床前模型的短板,提供了优质平台。 2.2.3 个体化治疗 肿瘤类器官能够反映患者的个体特征,可以用来探索个体化治疗方案,降低了患者药物毒副作用和耐药风险,在避免试药过程中减缓经济消耗,为准确选择患者治疗方案赢得时间窗口。VLACHOGIANNIS等[44]在成功构建患者来源的肿瘤类器官后,为了解PDO对患者临床疗效预测并指导临床治疗,利用紫杉醇、西妥昔单抗及瑞格非尼作用于PDO,结果发现PDO与相应临床患者对药物反应一致;随后为了进一步验证PDO的临床预测效果,试验构建了PDO异种移植模型,结果显示PDO异种移植模型对药物的反应与相应临床患者一致;同时观察比较了PDO异种移植模型在治疗前后的变化,显示与临床患者表现一致。通过分析发现PDO具有100%敏感性,93%特异性以及88%阳性预测值和100%阴性预测值,由此可见,PDO不仅可以指导化疗药物的临床应用,还可以指导肿瘤的放疗。DRIEHUIS 等[22]在构建了一个31例头颈部鳞状细胞癌类器官样本库后,将其中7个患者的肿瘤类器官的放疗敏感性与患者的放疗疗效进行了比对,发现对应的肿瘤类器官放疗敏感性可预测个体放疗疗效。由于肿瘤类器官的培养及建立所需的时间为4-6周,所以目前用于二线或辅助治疗的前瞻性测试[45]。进一步改善培养条件,缩短培养周期将为患者个体化治疗提供更加精准的方案。 由此可见,患者来源肿瘤类器官弥补了传统肿瘤细胞系与患者肿瘤的异种移植体的缺点,相比与其他来源建立的类器官,PDO来源于肿瘤患者,可以更好的保留肿瘤异质性,实现患者疾病模型的个体化,使PDO技术能更有效的指导临床肿瘤患者的个体化用药。 "
| [1] LANCASTER MA, KNOBLICH JA. Organogenesis in a dish:Modeling development and disease using organoid technologies. Science. 2014; 345:1247125. [2] CHAN AS, YAN HHN, LEUNG SY. Breakthrough Moments:Organoid models of cancer. Cell Stem Cell. 2019;24:839-840. [3] DAGOGO-JACK I, SHAW AT. Tumour heterogeneity and resistance to cancer therapies. Nat Rev Clin Oncol. 2018;15:81-94. [4] FONG EL, HARRINGTON DA, FARACH-CARSON MC, et al. Heralding a new paradigm in 3D tumor modeling. Biomaterials. 2016;108:197-213. [5] FONTOURA JC, VIEZZER C, DOS SANTOS FG, et al. Comparison of 2D and 3D cell culture models for cell growth, gene expression and drug resistance. Mater Sci Eng C Mater Biol Appl. 2020;107:110264. [6] FAN H, DEMIRCI U, CHEN P. Emerging organoid models: leaping forward in cancer research. J Hematol Oncol. 2019;12:142. [7] BLEIJS M, VAN DE WETERING M, CLEVERS H, et al. Xenograft and organoid model systems in cancer research. EMBO J. 2019;38:e101654. [8] BRADLEY A, EVANS M, KAUFMAN MH, et al. Formation of germ-line chimaeras from embryo-derived teratocarcinoma cell lines. Nature. 1984;309(5965):255-256. [9] SATO T, VRIES RG, SNIPPERT HJ, et al. Single Lgr5 stem cells build crypt-villus structures in vitro without a mesenchymal niche. Nature. 2009;459:262-265. [10] CHEN HI, SONG H, MING GL. Applications of human brain organoids to clinical problems. Dev Dyn. 2019;248:53-64. [11] POMPAIAH M, BARTFELD S. Gastric Organoids:An emerging model system to study helicobacter pylori pathogenesis. Curr Top Microbiol Immunol. 2017;400:149-168. [12] BOJ SF, HWANG CI, BAKER LA, et al. Organoid models of human and mouse ductal pancreatic cancer. Cell. 2015;160:324-338. [13] SATO T, STANGE DE, FERRANTE M, et al. Long-term expansion of epithelial organoids from human colon, adenoma,adenocarcinoma,and barrett\”s epithelium. Gastroenterology. 2011;141(5):1762-1772. [14] YAN HHN, SIU HC, LAW S, et al. A comprehensive human gastric cancer organoid biobank captures tumor subtype heterogeneity and enables therapeutic screening. Cell Stem Cell. 2018;23:882-897.e11 [15] GAO D, VELA I, SBONER A, et al. Organoid cultures derived from patients with advanced prostate cancer. Cell. 2014;159:176-187. [16] LEE SH, HU W, MATULAY JT, et al. Tumor evolution and drug response in patient-derived organoid models of bladder cancer. Cell. 2018;173: 515-528.e17. [17] LI X, FRANCIES HE, SECRIER M, et al. Organoid cultures recapitulate esophageal adenocarcinoma heterogeneity providing a model for clonality studies and precision therapeutics. Nat Commun. 2018;9:2983 [18] GIRDA E, HUANG EC, LEISEROWITZ GS, et al. The use of endometrial cancer patient-derived organoid culture for drug sensitivity testing is feasible. Int J Gynecol Cancer. 2017;27:1701-1707. [19] SACHS N, DE LIGT J, KOPPER O, et al. A living biobank of breast cancer organoids captures disease heterogeneity. Cell. 2018;172:373-386.e10. [20] NUCIFORO S, FOFANA I, MATTER MS, et al. Organoid models of human liver cancers derived from tumor needle biopsies. Cell Rep. 2018;24: 1363-1376. [21] SAITO Y, MURAMATSU T, KANAI Y, et al. Establishment of patient-derived organoids and drug screening for biliary tract carcinoma. Cell Rep. 2019;27:1265-1276.e4. [22] DRIEHUIS E, KOLDERS S, SPELIER S, et al. Oral mucosal organoids as a potential platform for personalized cancer therapy. Cancer Discov. 2019;9:852-871. [23] VAN DE WETERING M, FRANCIES HE, FRANCIS JM, et al. Prospective derivation of a living organoid biobank of colorectal cancer patients.Cell. 2015;161:933-945. [24] MARU Y, TANAKA N, ITAMI M, et al. Efficient use of patient-derived organoids as a preclinical model for gynecologic tumors. Gynecol.Oncol. 2019;154:189-198. [25] KELLER L, PANTEL K. Unravelling tumour heterogeneity by single-cell profiling of circulating tumour cells. Nat Rev Cancer. 2019;19:553-567. [26] ZHANG Z, SHIRATSUCHI H, PALANISAMY N, et al. Expanded circulating tumor cells from a patient with ALK-positive lung cancer present with EML4-ALK rearrangement along with resistance mutation and enable drug sensitivity testing: a case study. Thorac Oncol. 2017;12(2):397-402. [27] VISVADER JE, LINDEMAN GJ. Cancer stem cells in solid tumours: accumulating evidence and unresolved questions. Nat Rev Cancer. 2008;8:755-768. [28] FENDLER A, BAUER D, BUSCH J, et al. Inhibiting WNT and NOTCH in renal cancer stem cells and the implications for human patients. Nat Commun. 2020;11:929. [29] HWANG JW, LOISEL-DUWATTEZ J, DESTERKE C, et al. A novel neuronal organoid model mimicking glioblastoma (GBM) features from induced pluripotent stem cells (iPSC).Biochim Biophys Acta Gen Subj. 2020;1864:129540. [30] CANTOR JR. The rise of physiologic media.Trends Cell Biol.2019;29: 854-861. [31] PINTO D, GREGORIEFF A, BEGTHEL H, et al.Canonical Wnt signals are essential for homeostasis of the intestinal epithelium. Genes Dev. 2003;17(14):1709-1713. [32] KIM KA, KAKITANI M, ZHAO J, et al. Mitogenic Influence of human R-Spondin1 on the intestinal epithelium. Science. 2005;309(5738): 1256-1259. [33] DROST J, KARTHAUS WR, GAO D, et al. Organoid culture systems for prostate epithelial and cancer tissue. Nature Protocols. 2016;11(2): 347-358. [34] BENTON G, ARNAOUTOVA I, GEORGE J, et al. Matrigel: From discovery and ECM mimicry to assays and models for cancer research. Advanced Drug Delivery Reviews. 2014;79-80:3-18. [35] LEWIS MT, LANDUA JD, ADAMS HC 3RD, et al. A mystery wrapped in an enigma: Matrigel enhancement of mammary cell growth and morphogenesis. J Mammary Gland Biol Neoplasia. 2012;17:99-101. [36] BARKA T, GRESIK ES, MIYAZAKI Y. Differentiation of a mouse submandibular gland-derived cell line (SCA) grown on matrigel. Exp Cell Res. 2005;308:394-406. [37] BALACHANDER GM, BALAJI SA, RANGARAJAN A, et al. Enhanced metastatic potential in a 3D tissue scaffold toward a comprehensive in vitro model for breast cancer metastasis. ACS Appl Mater Interfaces. 2015;7:27810-27822. [38] NAYAK B, BALACHANDER GM, MANJUNATH S, et al. Tissue mimetic 3D scaffold for breast tumor-derived organoid culture toward personalized chemotherapy. Colloids Surf B Biointerfaces. 2019;180:334-343. [39] SHIMOKAWA M, OHTA Y, NISHIKORI S, et al. Visualization and targeting of LGR5 human colon cancer stem cells. Nature. 2017;545:187-192. [40] SZVICSEK Z, OSZVALD Á, SZABÓ L, et al. Extracellular vesicle release from intestinal organoids is modulated by Apc mutation and other colorectal cancer progression factors. Cell Mol Life Sci. 2019;76: 2463-2476. [41] APARICIO S, HIDALGO M, KUNG AL. Examining the utility of patient-derived xenograft mouse models. Nat Rev Cancer. 2015;15:311-316. [42] PAULI C, HOPKINS BD, PRANDI D, et al. Personalized in vitro and in vivo cancer models to guide precision medicine. Cancer Discovery. 2017;7(5):462. [43] BOEHNKE K, IVERSEN PW, SCHUMACHER D, et al. Assay establishment and validation of a high-throughput screening platform for three-dimensional patient-derived colon cancer organoid cultures. J Biomol Screen. 2016;21:931-941. [44] VLACHOGIANNIS G, HEDAYAT S, VATSIOU A, et al. Patient-derived organoids model treatment response of metastatic gastrointestinal cancers. Science. 2018;359:920-926. [45] TUVESON D, CLEVERS H. Cancer modeling meets human organoid technology. Science. 2019;364:952-955. |
| [1] | Zhang Xiumei, Zhai Yunkai, Zhao Jie, Zhao Meng. Research hotspots of organoid models in recent 10 years: a search in domestic and foreign databases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1249-1255. |
| [2] | Xu Junma, Yu Yuechao, Liu Zhi, Liu Yu, Wang Feitong. Application of 3D-printed coplanar template combined with fixed needle technique in percutaneous accurate biopsy of small pulmonary nodules [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 761-764. |
| [3] | Pan Xuan, Zhao Meng, Zhang Xiumei, Zhao Jie, Zhai Yunkai. Research and application of biological three-dimensional printing technology in the field of precision medicine: analysis of Chinese and English literature [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(21): 3382-3389. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||