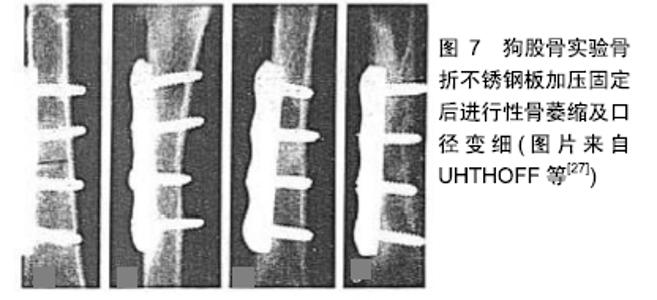
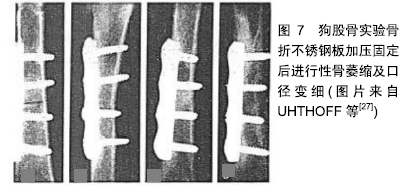
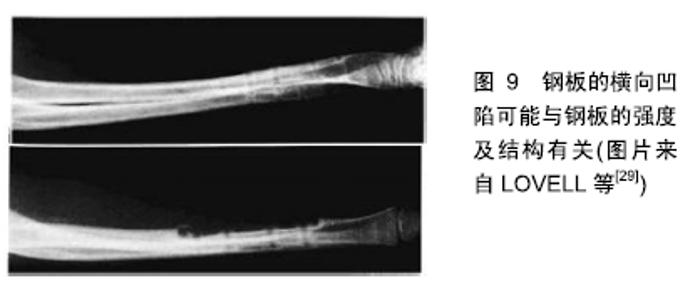
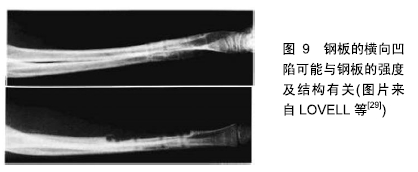
Chinese Journal of Tissue Engineering Research ›› 2020, Vol. 24 ›› Issue (6): 903-910.doi: 10.3969/j.issn.2095-4344.2452
Previous Articles Next Articles
Four-dimensional space events of fracture healing
Liu Zhendong1, Qin Sihe2
- 1Department of Orthopedics, Dandong Municipal 966 Hospital, Dandong 118000, Liaoning Province, China; 2Rehabilitation Hospital Affiliated to National Research Center for Rehabilitation Technical Aids, Beijing 100176, China
-
Received:2019-06-12Revised:2019-06-14Accepted:2019-07-15Online:2020-02-28Published:2020-01-17 -
About author:Liu Zhendong, Master, Associate chief physician, Department of Orthopedics, Dandong Municipal 966 Hospital, Dandong 118000, Liaoning Province, China -
Supported by:the Youth Fund of Medical and Health in the Army during the 10th Five-Year Plan Period, No. 01Q007
CLC Number:
Cite this article
Liu Zhendong, Qin Sihe. Four-dimensional space events of fracture healing[J]. Chinese Journal of Tissue Engineering Research, 2020, 24(6): 903-910.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
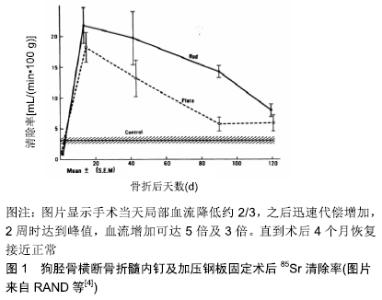
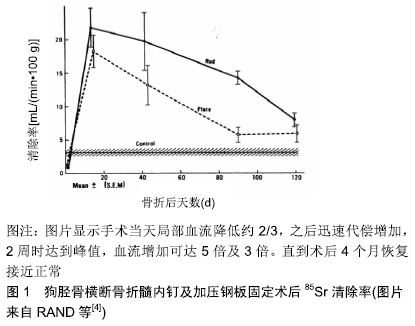
2.1 骨折及骨折内固定术后的血运潮汐 正常骨骼中的微循环具有独立于心脏的自主节律,像潮汐一样脉冲式开放,这是中国学者修瑞娟提出的第二心脏理论[1],绝大多数哈伏氏管内只走行一条毛细血管,只有间断脉冲式血流才能最有利于各种物质交换。这种生理性的微循环的血供脉冲具有短周期高频率的特点。骨骼还具有中周期和长周期的血运潮汐,骨骼在承受超负荷应力时,会诱发应力-血管生成-骨再生的偶联效应[2],因为涉及蛋白合成、组织识别、干细胞分化向特定组织再生等复杂的过程,表现为局部持续性充血,一般持续2周左右。这种中周期是人体最重要的生命周期,与初次免疫应答及子宫内膜的增殖周期高度吻合。这种中周期血运潮汐可能是骨骼塑形机制的内在基础,因为骨骼承受应力的不均匀性,中周期血运潮汐分布也不均匀,可能会导致低应力部位缺血性骨吸收,而高应力部位发生骨再生强化,这或许是Wolff定律的内在基础。当骨骼发生创伤骨折时,骨折局部的血运损失会在48 h内被代偿,在内固定2周后发生两三倍的超代偿[3-4],这种超代偿血运潮汐可以持续3个月以上(图1)。这种长周期的血运潮汐可能是创伤后多种因素共同作用的结果,包括中周期血运潮汐的持续启动和叠加;这种长周期的血运潮汐或许是胫骨横搬治疗缺血性疾病的理论基础。总之,长骨骨折后极少发生缺血现象。"

2.2 力学脉冲与生物学脉冲 在非运动状态,活体骨骼一般也承受肌肉张力、人体重力等所产生的背景应力。但这些背景应力一般强度较低,不足以刺激骨改建及骨再生[5]。但在运动状态及强化锻炼过程中,人体骨骼会受到超负荷脉冲式力学刺激,这种强力学脉冲会诱发应力-血管生成-骨再生的偶联效应,进而诱发一波2周左右的骨再生生物学脉冲。这个时间周期被McKibbin的老鼠截肢实验及Rooney的微孔弥散室体内培养异位骨化实验所证实[6-7]。由于力学脉冲可以短期内不规则地重复出现,其诱导的生物学修复脉冲可能叠加重合为一个连续的过程,因此骨再生的生物学事件具有规则的时间周期和不规则的脉冲样节律,但在临床上只能观察到一个连续的过程。骨折间隙是天然的应力集中部位,骨痂又是脆弱的组织,极小的应力就可以诱发骨折间隙的修复效应。因此,骨折早期需要稳定的固定。当骨折愈合出现问题的时候,一定是由力学脉冲向生物学脉冲的转化过程出现了问题。前面已经论述过,骨折修复的血运潮汐足够强大,几乎不可能发生缺血,但事实真是如此吗?用放射性元素测量的血运数据过于宏观,血管造影图片提供了更丰富的细节将在后面讨论。 2.3 硬组织小间隙在四维空间上的磨盘效应 骨折在合适的力学和生物学条件下会顺利愈合,那么为什么会出现骨折愈合的不良事件呢?徐莘香教授等[8]曾指出“骨断端和骨折片间的吸收,间隙增宽,周围无连续外骨痂形成是骨折固定不牢和肢体活动量过大的最早出现的征象”。国际内固定协会(AO)学者证实了在钢板固定条件下活体骨骼会发生磨损性微骨折[9],在此基础上,作者提出硬组织小间隙在四维空间上会发生磨盘效应进而发生骨吸收[10](图2),骨折间隙的磨盘效应是骨折愈合不良事件的重要原因。磨盘效应是骨折固定不稳定的表现,一方面表现为再损伤,包括微骨折和骨痂挫灭;另一方面表现为骨折周边血运超代偿,而骨折间隙血管挫灭,无法进行有效连通,即间隙内缺血。这种现象被RHINELANDER[11]的微血管造影图片很好地记录了下来(图3)。 "

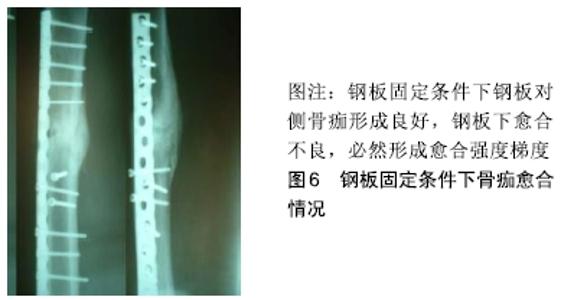
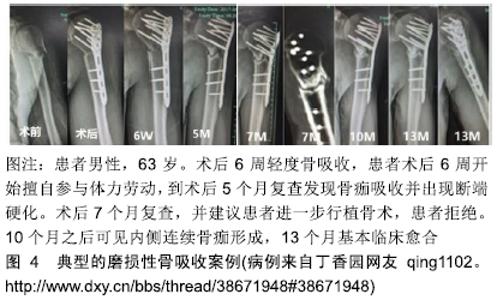
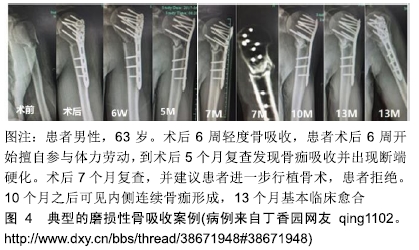
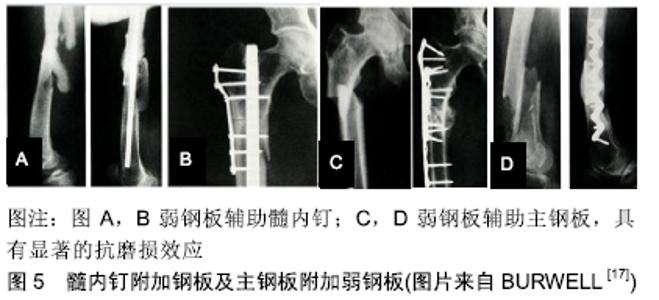
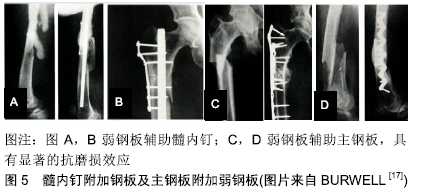
推论五:骨不连可以通过自我保护减少活动降低磨损自行愈合[15]。 推论六:截肢患者的同一肢体骨折因受力减少,磨损降低将更容易愈合,作者观察到1例小腿截肢股骨钛板内固定的成年男性患者,愈合顺利,无磨损吸收现象。 推论七:牵拉成骨早期小间隙的稳定性至关重要,早期的不稳定导致的磨盘效应会产生间隙缺血(图3),可能是牵拉成骨后期成骨不良的重要原因,而一旦牵开间隙将能耐受更大的不稳定性,因为磨损效应基本消失。 推论八:根据公式刚度=应力/应变,理想的初期固定刚度应接近所固定骨骼的刚度才不会在一般日常应力下发生显著的应变磨损。对于特定骨骼一定存在一个最佳的初始固定刚度,夏和桃教授等将之称为骨折固定的适应性刚度。随着骨折愈合,理想的适应性固定刚度应该逐步降低。 推论九:与医用不锈钢钢板相比,钛钢板因剪切强度不够,更容易发生磨损性骨吸收。 刚度是反映材料抗形变能力的概念,对于细弱的骨骼,应该采用低刚度固定,而对于粗壮的骨骼,应该采用高刚度固定。因此将适合狗和兔子的固定材料用在成年人身上在理论上并不成立。从目前的实验和临床数据分析,钛板也许更适合小动物、儿童和残疾肢体,在成人身上则看到大量的磨损延迟愈合现象(图4),提示钛板的抗剪切刚度不够,而只有通过增加厚度才能满足适应性刚度需求。可以推论医用不锈钢仍然是值得怀念的理想固定材料,一方面可以降低横截面积来满足临床需求,另一方面可以减少术后保护而更加适合日常生活。遗憾的是钛板做不到这两点。因此作者怀念钢板的徐莘香时代,他通过改变钢板的几何形状来降低不锈钢板的固定刚度,主张少量骨痂形成而没有磨损骨吸收的第3种骨折愈合方式,这种愈合形态也是那个时代理论大师的基本共识[18]。作者有理由重温充满浪漫主义情怀的AO四原则:解剖复位,坚固内固定,微创操作,早期无痛功能锻炼。只要再加上一条,可见少量骨痂形成而没有磨损吸收,骨折内固定将达到一个完美的状态。实验结果提示在合适条件下,钢板固定骨折同样可以得到100%的愈合率[19]。 推论十:当固定材料达到足够刚度后,磨盘效应将消失而不发生骨吸收,比如传统的骨折一期愈合现象。上海六院回顾研究提示股骨强弱组合的双钢板固定可以取得和带锁髓内钉相近的效果[20]。 推论十一:在不稳定状态下,多维多钉锁定髓内钉将提供更加可靠的愈合率。 2.4 骨折固定的应力遮挡效应 传递应力是活体骨骼的基本功能,应力是活体骨骼的灵魂。穿骨金属材料固定骨骼后必然改变骨骼的应力传导,分流骨骼所承受的应力,这种固定材料对骨骼的应力分流称为固定材料对骨骼的应力遮挡[21]。而固定材料正是通过应力分流起到稳定骨骼的作用,因此应力遮挡在一定限度范围内对骨折愈合起到重要的保障作用,其负面效应并不明显。传统工程力学对应力遮挡是这样定义的:当不同弹性模量的成分并联承担载荷时,较高弹性模量的成分承担较多的载荷,即对低弹性模量成分起到应力、应变遮挡作用。这个定义附加诸多的前提条件,比如材料应是完整的,形状和体积要形同,但在骨折模型根本不适用,已经被证伪[21]。问题的关键不在于材料的弹性模量,而在于固定材料究竟分担了多少骨骼的应力,因为固定材料对骨骼的力学分流还与固定材料的空间构型、横截面积、肢体的功能状态等相关[21-23]。 临床上所说的骨折固定的应力遮挡效应通常是指过于坚强的固定材料对骨折愈合所产生的不良效应。坚强固定对骨骼产生轴向和剪切方向的应力剥夺,根据应力-骨再生的偶联效应可以得出3个推论: 推论一:在钢板分担轴向应力条件下,骨折愈合达不到正常骨骼强度而停止,称为骨折的非坚固愈合状态,非坚固愈合随时间改善不明显,是取钢板后再骨折的基本原因,而且再骨折大多经原骨折线[24]。 推论二:钢板固定条件下从钢板侧到钢板对侧骨折间隙存在弹性梯度,必然导致骨折间隙的愈合存在强度梯度,钢板侧最弱,这个推论已经被远皮质锁定钢板实验所证实[24-25](图6)。 "

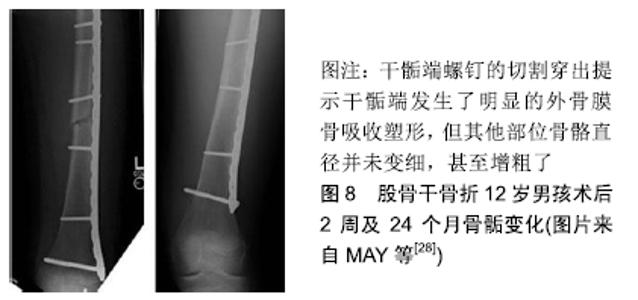
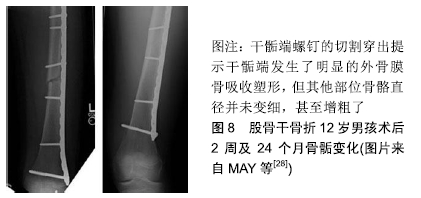
当骨折固定刚度不够时,常会发生磨损性骨吸收。而当固定刚度过强时,又会发生骨折的非坚固愈合导致拆除固定后的再骨折。近年来洛阳正骨医院的宋文超博士利用弹簧原理设计了应力可调式外固定架,随骨折愈合而降低外架的应力遮挡率,取得了良好的效果。 2.5 内固定物的四维空间漂移 骨骼依靠动力形变来维持骨骼的质量和结构[18]。当骨骼发生穿骨固定后,骨骼与固定装置共同承担应力,这会在四维空间上导致一系列形态变化,包括骨骼的形态和内固定的相对位置都会有所改变。将内固定物与骨骼的相对位置发生的缓慢变化称为内固定物的四维空间漂移。常见以下漂移现象: 2.5.1 儿童骨折的内固定物的生长漂移 由于儿童骨骺的迅速生长塑形,内固定的钢板螺钉会发生相对位置变化,钢板向骨干移位,干骺端螺钉会发生穿出现象(图8)。 "
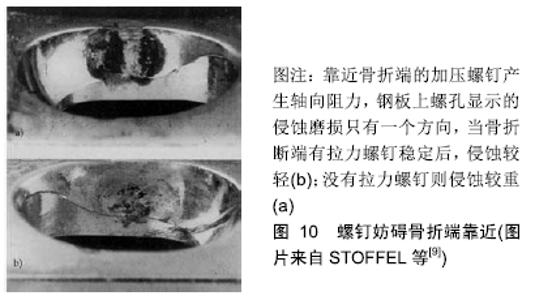
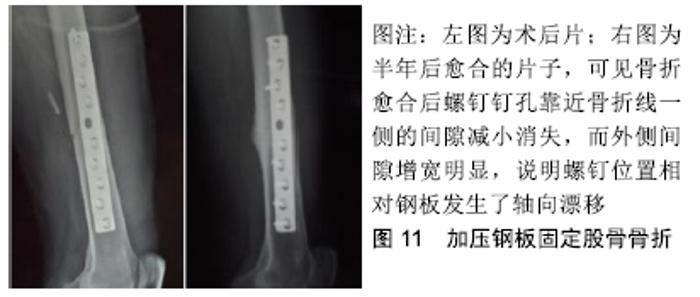
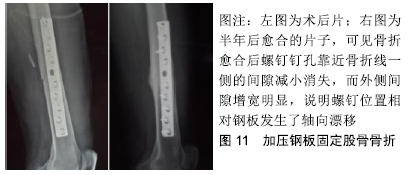
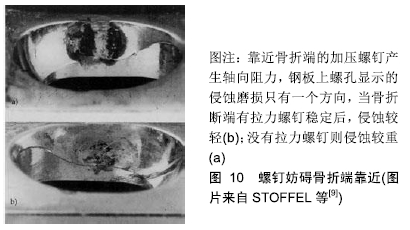
2.5.3 螺钉的轴向漂移 螺钉在股骨近端发生漂移切割以及退钉现象均很常见,但骨干骨折钢板固定后螺钉的轴向漂移现象并未引起足够重视。在20世纪中叶由于普遍采用低强度钢板而发生磨损失效,人们注意到圆形螺钉孔会妨碍骨折端相互靠近,因而设计了曾经广泛使用的Egger滑槽钢板,其后BAGBY和JANES于1958年设计了著名的动力加压钢板[30]。AO学者在实验中发现在加压钢板固定过程中,螺钉对钢板会发生定向侵蚀现象,说明螺钉和钢板之间存在力学微动[9](图10)。这种力学现象会使骨折线相互靠近产生微小短缩位移,而螺钉在反作用力作用下会产生逆向漂移切割(图11)。这种钢板固定螺钉的微小轴向漂移具有重要的理论意义,钢板分担的应力并非是固定不变的,而是随着骨折的坚固程度逐步降低[9],这种微小轴向漂移具有“智能性”轴向动力化效应[31],即恰好而自止,可以降低钢板的轴向应力遮挡。可以推论锁定钢板严重地妨碍这种轴向漂移趋势,理论上更容易发生取钢板后的再骨折,好在钛质钢板的剪切强度较弱恰好可以代偿这种趋势。"
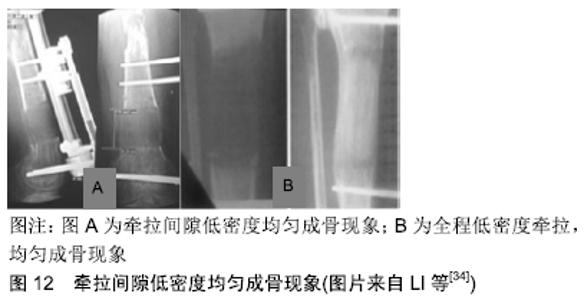
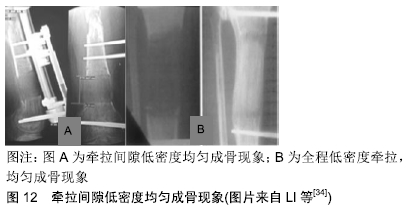
2.6 骨折间隙的四维空间调控 人类已经进入了一个对骨折愈合和骨再生的可调控时代,科学地解释骨折愈合的力学和生物机制已经露出了希望的曙光[32]。骨折术后采取保护措施本身就是对骨折间隙的力学状态进行调控,包括石膏固定、支具保护、扶拐及助行器、限制体力劳动等。循序渐进保护下负重或功能锻炼仍是骨折术后的主要康复原则。根据适应性刚度原理,逐步增加肢体负荷或适当降低固定刚度是骨折间隙四维空间调控的主要手段。 2.6.1 牵拉成骨的四维空间调控 牵拉成骨是对骨折间隙的脉冲式应力调控,牵拉成骨与牵张应力大小无关,在同等位移情况下,成骨效率与每天牵拉次数正相关[33]。延迟期在临床上具有重要的意义,延迟期骨折间隙最小,必须高度稳定以防磨损效应,此外延迟期可以修复骨膜包壳封闭骨折空间,延迟期为血管再生连通提供基本时间,延迟期内骨折间隙发生一系列细胞生物学事件,这些骨再生事件为后续牵拉再生培育了高浓度的“种子”。骨再生的基本时间周期为7-14 d,因此理想的延迟期大概也在这个范围。 有关牵拉成骨,ILIZAROV[33]曾提出中央区的生长带假说,按生长带学说推论,牵拉间隙骨痂应该出现梯度密度特征,中间弱两边高。但大量反证据临床事实包括ILIZAROV本人的实验并不支持这一推论(图12)。生长带假说并没有给出有意义的临床推论。假设牵拉间隙具有均匀的蠕变能力,可以推论牵拉间隙的每一寸空间都具备牵拉成骨能力。这个原理称为牵拉成骨的全方位成骨原理。全方位成骨原理成立的基本条件是血运重建要充分,牵拉间隙具备蠕变弹性,不发生断裂效应。由此可以得出以下基本推论: "
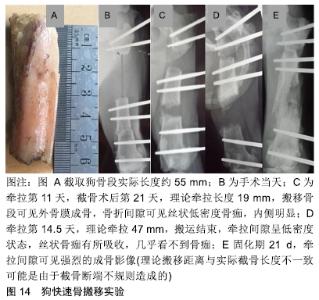
推论一:维持X射线低密度牵拉是合理的,高密度容易产生断裂效应从而产生非弹性牵拉。 推论二:单次小剂量牵拉容易达到蠕变效应,小剂量多次牵拉具有极高的成骨效率已经被Ilizarov的实验所证实[33]。 推论三:如果牵拉间隙的长度为L,每天新增加的长度为?L,?L/L简称为牵拉比值,牵拉比值反映了牵拉间隙的成骨潜力。随着牵拉间隙L的增大,每天的牵拉速度?L也可以逐步增大。根据牵拉比值推论牵拉成骨的牵拉速度可能远远超过传统的实验数据。 为了验证推论三,作者在2条成年狗股骨上设计了变加速快速骨搬移实验。分别摘除4.2 cm及5.1 cm股骨骨段造成大段骨缺损,截骨后10 d开始骨搬移,单次搬移剂量均为0.25 mm。每天牵拉2次共4 d,每天4次共2 d,然后维持牵拉比值≤0.5逐步增加牵拉次数,第1条狗最快牵拉速度达到每天6 mm(牵拉24次),持续4 d(图13)。第2条狗达到每天8 mm(牵拉32次)维持 3.5 d,均观察到完美成骨(图14)。 "
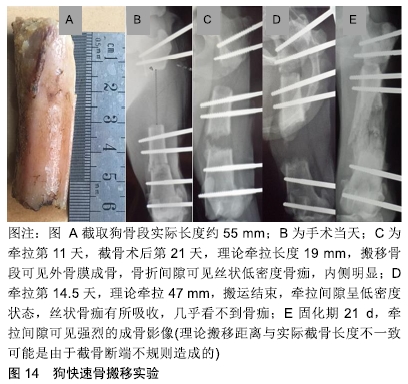
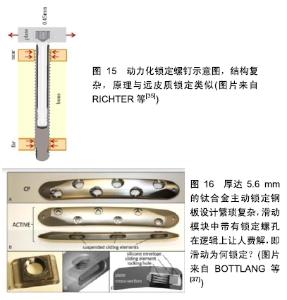
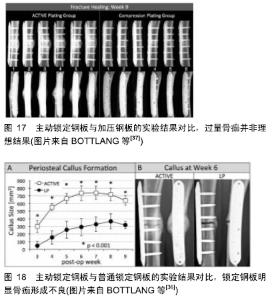
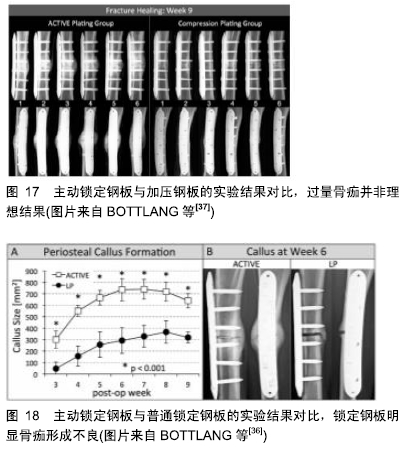
在延迟期及牵拉早期,骨折间隙较小,需要较高的稳定性防止磨盘效应[10],一旦牵开间隙,磨盘效应消失,理论上在牵拉中后期牵拉间隙可以耐受较大的不稳定,可以一次性纠正30°以内的旋转及成角畸形。在停止牵拉的固化期,可适当增加肢体负重及酌情降低外固定的剪切刚度来促进骨皮质的形成。 2.6.2 钢板内固定的四维空间调控 锁定钢板在空间构型上很难进行适应性刚度调控,改进之一是远皮质锁定钢板,近端皮质无螺纹,可以很好地促进钢板侧的骨痂形成[25]。改进之二是动力化锁定螺钉[35](图15),原理与远皮质锁定钢板类似。改进之三是主动锁定钢板,原理示意图如图16,采用可降解材料类似一个不稳定的滑槽[36-37]。从实验图片上看骨痂形成过量,且有明显的磨损吸收痕迹,唇样骨痂有断裂征象类似肥大性骨不连(图17,18),而且这种结果是在石膏固定情况下得到的,提示该种钢板具有明显的不稳定性,作者个人认为还是伴有少量连续骨痂的加压钢板结果更好,不得不反思一个问题,在骨干骨折中为什么要用锁定钢板?锁定钢板治疗简单骨折曾被权威的JBJS列为禁忌证[38],其先天缺欠是明显的。 "

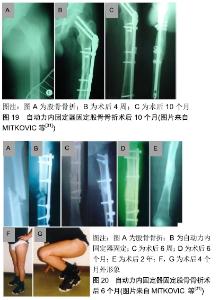
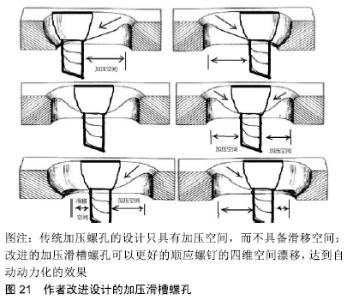
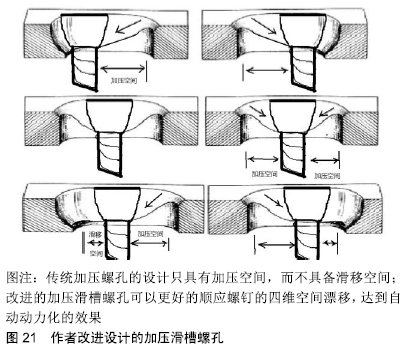
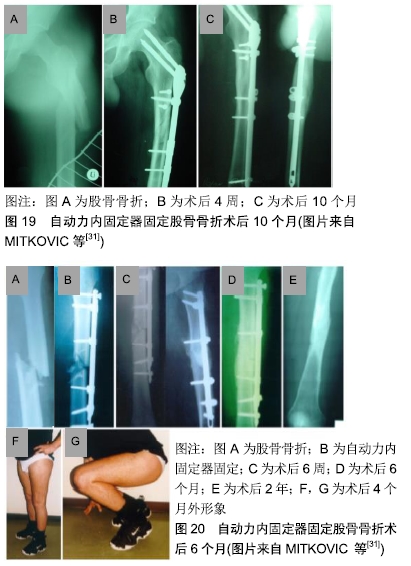
回顾历史,有些改进未免画蛇添足。从生物力学的角度分析,固定材料的剪切刚度刚好接近所固定骨骼,而轴向刚度略低于所固定骨骼的刚度则能满足骨再生的基本要求,塞尔维亚学者设计了一款自动力股骨内固定器取得了理想的临床效果,在726例得到随访的患者样本中,愈合率高达99.1%,平均愈合时间3.9个月[31]。这样的结果会让人忘记什么是股骨骨折治疗的“金标准”,毕竟骨髓腔是人体的一个重要器官,也是长骨血供的主要来源[39]。从图片分析看,该固定器得到的骨痂形态十分优美,没有骨吸收,没有肥大现象,恰到好处(图19,20)。该固定器采用医用不锈钢材料,设计简洁,利用了螺钉的轴向漂移达到自动动力化效应,而不影响固定的稳定性。Bagby设计的动力加压钢板也是简洁设计的历史杰作,椭圆孔可以在某种程度顺应螺钉的轴向漂移,作者在此基础上稍加改进设计了加压滑槽螺孔,可以更好的顺应螺钉的四维空间漂移,达到自动动力化的效果(专利号ZL 2017 2 0161734.5)(图21),并建议采用不锈钢材料来防止剪切磨损。"
| [1] 修瑞娟.微循环——微妙的生命源泉[J].微循环学杂志, 1997,7(1): 1-3. [2] 刘振东,秦泗河.骨痂的形成和分类[J].中国矫形外科杂志, 2016,24(4):332-337. [3] SMITH SR, BRONK JT, KELLY PJ. Effect of fracture fixation on cortical bone blood flow. J Orthop Res.1990; 8(4):471-478. [4] RAND JA, AN KN, CHAO EYS, et al. A comparison of the effect of open intramedullary nailing and compression-plate fixation on fracture-site blood flow and fracture union. J Bone joint Surg 1981;63-A(3);427-440. [5] TURNER CH.Three rules for bone adaptation to mechanical stimuli.Bone.1998;23(5):399-407. [6] MCKIBBIN B.The biology of fracture healing in long bones. J Bone Joint Surg.1978;60B:150-162. [7] ROONEY P, WALKER D, MCCLURE J. Cartilage and bone formation in repairing Achilles tendons within diffusion chambers: evidence for tendon-cartilage and cartilage-bone conversion in vivo.J Pathol. 1993;169:375-381. [8] 徐莘香,刘一,李长胜,等.当前骨折内固定治疗中的几个基本问题[J].中华骨科杂志,1996,16(4):204-207. [9] STOFFEL K, KLAUE K, Perren SM.Functional load of plates in fracture fixation in vivo and its correlate in bone healing.Injury.2000;31 Suppl 2:S-B37-50. [10] 刘振东,秦泗河.骨折断端磨损性骨吸收的证据分析[J].中国矫形外科杂志,2015,23(12):1147-1152. [11] RHINELANDER FW. Tibial blood supply in relation to fracture healing.Clin Orthop Relat Res. 1974;105:34-38. [12] UENG SW, CHAO EK, LEE SS, et al. Augmentative plate fixation for the management of femoral nonunion after intramedullary nailing. J Trauma.1997;43(4):640-644. [13] 刘振东,马梦然,田冠玉.骨不连的界定与分类治疗[J].中国矫形外科杂志,2007,15(20):1598-1600. [14] WU CC. The effect of dynamization on slowing the healing of femur shaft fractures after interlocking nailing.J Trauma.1997;43(2):263-267. [15] SARMIENTO A, BURKHALTER WE, Latta LL. Functional bracing in the treatment of delayed union and nonunion of the tibia.Int Orthop.2003;27(1):26-29. [16] BRINKER MR, O'CONNOR DP. Ilizarov compression over a nail for aseptic femoral nonunions that have failed exchange nailing: a report of five cases.J Orthop Trauma.2003;17(10):668-676. [17] BURWELL HN. Internal fixation in the treatment of fractures of the femoral shaft. Injury.1971; 2(3):235-244. [18] UHTHOFF HK, Bardos DI, Liskova-Kiar M. The advantages of titanium alloy over stainless steel plates for the internal fixation of fractures. An experimental study in dogs.J Bone Joint Surg.1981; 63-B(3):427-84. [19] XU H,XUE Z, DING H, et al. Callus formation and mineralization after fracture with different fixation techniques: minimally invasive plate osteosynthesis versus open reduction internal fixation. PLoS One.2015;10(10):e0140037. [20] CHENG T, XIA RG, DONG SK, et al.Interlocking intramedullary nailing versus locked dual-plating fixation for femoral shaft fractures in patients with multipleinjuries: a retrospective comparative study.J Invest Surg.2017;18:1-10. [21] 刘振东,范清宇.应力遮挡效应—寻找丢失的钥匙[J].中华创伤骨科杂志,2002,4(1):62-64. [22] 徐莘香,宁漱岩,刘建国,等.第三种骨折愈合方式的力学与生物 学基础[J].中华外科杂志,1992,30(5):308 -310. [23] 白凤德,梁铂坚,朱兴华,等.加压钢板内固定负重状态下应力遮 挡效应的生物力学实验研究[J].白求恩医科大学学报,1998,24 (3):268-270. [24] 刘振东,马梦然,田冠玉,等.对长骨干骨折钢板固定后非坚固愈合状态的探讨[J].中国矫形外科杂志,2008,16(8):639-640. [25] Bottlang M, Feist F.Biomechanics of far cortical locking.J Orthop Trauma.2011;1:21 -28. [26] 刘振东,周大鹏,秦泗河.长骨骨干的增粗机制及其临床意义[J].中国组织工程研究,2017,21(36):5868-5872. [27] UHTHOFF HK, Dubuc FL. Bone structure changes in the dog under rigid internal fixation. Clin Orthop Relat Res.1971;81:165-170. [28] MAY C, YEN YM, NASREDDINE AY, et al. Complications of plate fixation of femoral shaft fractures in children and adolescents.J Child Ortho.2013;7(3):235-243. [29] LOVELL ME, GALASKO CS, WRIGHT NB. Removal of orthopedic implants in children : morbidity and postoprerative radiologic changes. J Pediatr Orthop B.1999;8(2):144-146. [30] UHTHOFF HK, POITRAS P, BACKMAN DS. Internal plate fixation of fractures: short history and recent developments. J Orthop Sci.2006; 2:118-126. [31] MITKOVIC M, MILENKOVIC S, MICIC I,et al. Results of the femur fractures treated with the new selfdynamisable internal fixator (SIF).Eur J Trauma Emerg Surg.2012;38(2):191-200. [32] 刘振东,马梦然,张志诚.从骨折愈合论理论医学的萌芽[J].中华创伤骨科杂志,2004,6(12):1393-1395. [33] ILIZAROV GA. The tension-stress effect on the genesis and growth of tissues: Part I. The influence of stability of fixation and soft tissue preservation. Clin Orthop.1989; 238:249-281. [34] LI R,SALEH M, YANG L, et al. Radiographic classification of osteogenesis during bone distraction. J Orthop Res. 2006;24(3):339-347. [35] RICHTER H, PLECKO M, Andermatt D, et al.Dynamization at the near cortex in locking plate osteosynthesis by means of dynamic locking screws: an experimental study of transverse tibial osteotomies in sheep. J Bone Joint Surg Am.2015;97(3):208-215. [36] BOTTLANG M, TSAI S, BLIVEN EK, et al.Dynamic stabilization of simple fractures with active plates delivers stronger healing than convention compression plating. J Orthop Trauma.2017; 31(2):71-77. [37] BOTTLANG M, Tsai S, Bliven EK, et al.Dynamic stabilization with active locking plates delivers faster, stronger, and more symmetric fracture-healing. J Bone Joint Surg Am.2016;16;98(6):466-474. [38] SMITH WR, ZIRAN BH, ANGLEN JO, et al. Locking plates: tips and tricks. J Bone Joint Surg Am.2007;10:2298-2307. [39] TRIAS A, FERI A. Cortical circulation of long bones. J Bone Joint Surg.1979; 61A:1052-1059. [40] ELLIS H. The speed of healing after fracture of the tibial shaft. J Bone Joint Surg Br.1958; 40-B(1):42-46. [41] CHAO EY, ARO HT, LEWALLEN DG, et al. The effect of rigidity on fracture healing in external fixation. Clin Orthop Relat Res. 1989;241:24-35. [42] 秦泗河,曲龙.骨外固定技术的发展史与骨科自然重建理念的形成[J].中国矫形外科杂志,2009,17(16):1262-1266. |
| [1] | Yang Weiqiang, Ding Tong, Yang Weike, Jiang Zhengang. Combined variable stress plate internal fixation affects changes of bone histiocyte function and bone mineral density at the fractured end of goat femur [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(6): 890-894. |
| [2] | Cheng Shigao, , Wang Wanchun, Jiang Dong, Li Tengfei, Li Xun, Ren Lian. Comparison of the standard and long-stem bone cement prosthesis replacement in the treatment of intertrochanteric fractures in elderly patients [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 362-367. |
| [3] | Mao Guoshu, Zhou Min, Li Xiaoming, Zhou Zihong, Yin Qudong. Effect of the third fragment on the healing of femoral shaft fractures after intramedullary nailing fixation [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(15): 2405-2409. |
| [4] | Wu Yukun, Han Jie, Wen Shuaibo. Mechanism of Runx2 gene in fracture healing [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(14): 2274-2279. |
| [5] | Wu Shengxiang, Liu Yuan, Lu Shuai. Mini-locking titanium plate system fixation in the treatment of carpal scaphoid fracture [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(12): 1874-1878. |
| [6] | Xu Shaoce, Wang Shiyao, Zhou Jianwei, Pan Yixin, Wang Yuliang. Fibroblast growth factor receptor 3 regulation and mechanism in callus formation [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(7): 1083-1088. |
| [7] | Zhang Chao, Li Xingyong, Ma Guifu, Pu Xingyu, Luo Wenyuan. Hoxa9 silencing promotes tibial fracture healing by regulating osteogenic differentiation [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(35): 5600-5606. |
| [8] | Li Yanqiang, Pan Deyue, Nan Feng, Han Xin. Treatment of senile osteoporotic patella fractures with double tension band [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(33): 5338-5342. |
| [9] | Yang Shun, Chen Keyi, Cheng Yabo, Xiang Wang, Zhang Jing, Gu Hongji, Chi Haotian. Wrist arthroscopy-assisted titanium internal fixator for the treatment of complex distal radius fractures [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(3): 366-371. |
| [10] | Liu Guoming, Wang Qinfen, Lin Kefeng, Zhou Shiguo, Chen Zuxing, Lin Shishui. Whole body application of nerve growth factor promotes early healing of tibial shaft fracture and improves expression of bone morphogenetic protein-2 and vascular endothelial growth factor in rats [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(29): 4680-4685. |
| [11] | Wulan•Saitahemaiti, Ailijiang•Asila, Nuerhanati•Shayilanbieke, Nuerman•Yixijian, Asihati•Nuermaimaiti, Fang Rui. Xinjiang Sambucus sibirica Nakai bark extract promotes fracture healing [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(20): 3122-3129. |
| [12] | Qian Zhouyao, Wang Yongping. Vascular endothelial growth factor intervention: a new approach for accelerating fracture healing [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(17): 2759-2769. |
| [13] | Zhu Fuliang, Zheng Daoming, Shi Yubo, Wang Yunguo, Ni Dongkui, Li Lijun, Jiang Zhuyan, Haimiti·Abuduaini, Xue Yuan. Inverse arch roof breaking technique combined with pedicle screw and bone graft in the treatment of thoracolumbar burst fractures [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(12): 1817-1822. |
| [14] | Zhu Wanbo, Lu Jinsen, Yang Jiazhao, Fang Shiyuan. Mechanism and clinical application of stem cell-derived exosomes in promoting fracture healing [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(5): 815-820. |
| [15] | Feng Yang, Chen Yueping, Zhang Xiaoyun, Dong Panfeng, Zhuo Yinghong, Lan Jiao, Hu Qinglei, Tang Xianneng . Mechanism of bone growth factors regulating fracture healing and their application in bone regeneration and repair [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(4): 613-620. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||