Chinese Journal of Tissue Engineering Research ›› 2014, Vol. 18 ›› Issue (5): 779-784.doi: 10.3969/j.issn.2095-4344.2014.05.021
Previous Articles Next Articles
Sirolimus in kidney transplantation: theory and technology
Wang Mo, Guo Ying
- Department of Organ Transplantation, Zhujiang Hospital, Southern Medical University, Guangzhou 510282 , Guangdong Province, China
-
Revised:2013-12-07Online:2014-01-29Published:2014-01-29 -
Contact:Guo Ying, M.D., Chief physician, Professor, Master’s supervisor, Department of Organ Transplantation, Zhujiang Hospital, Southern Medical University, Guangzhou 510282 , Guangdong Province, China -
About author:Wang Mo, Studying for master’s degree, Department of Organ Transplantation, Zhujiang Hospital, Southern Medical University, Guangzhou 510282 , Guangdong Province, China
CLC Number:
Cite this article
Wang Mo, Guo Ying. Sirolimus in kidney transplantation: theory and technology[J]. Chinese Journal of Tissue Engineering Research, 2014, 18(5): 779-784.
share this article
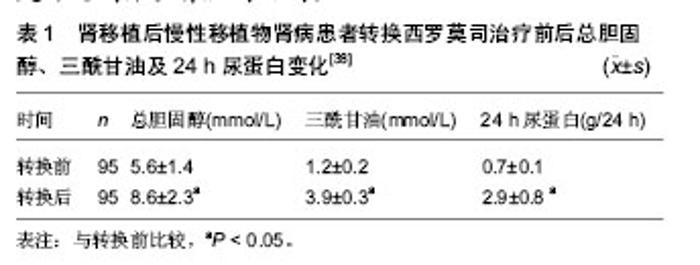
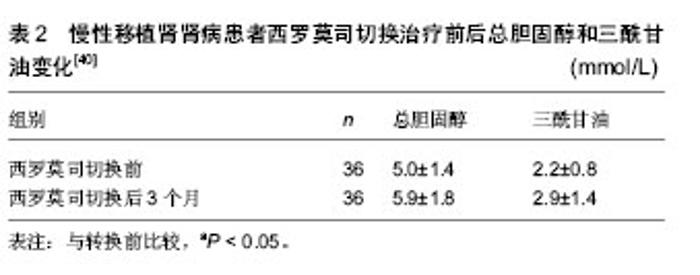
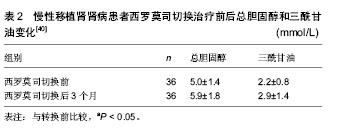
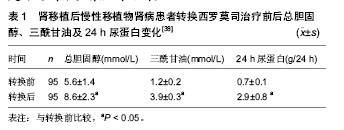
2.1 肾移植后初期使用西罗莫司 近些年来,来自美国、欧洲和中东的临床研究报告指出,肾移植后初期使用西罗莫司在术后1年急性排斥反应发生率(10%-15%)方面同钙调磷酸酶抑制剂类药物免疫抑制方案类似,且使用西罗莫司的患者肾功能(估算肾小球滤过率:65-80 mL/min)要优于使用钙调磷酸酶抑制剂类药物的患者[2-9]。肾移植后初期使用西罗莫司的临床效果同多种因素相关。 2.1.1 选择合适的患者 西罗莫司同其他免疫抑制剂相比,在肿瘤预防方面具有一定优势。在一项随访5年的随机对照试验中[4],肾移植后初期使用西罗莫司的31例患者中只有1例浅表皮肤癌复发和1例新发浅表皮肤癌,而钙调磷酸酶抑制剂组的30例患者中有3例新发浅表皮肤癌和3例新发实体器官癌症(直肠癌、乳腺癌、喉癌)。 近期发表的一项器官移植指南指出[10],使用西罗莫司可以降低巨细胞病毒感染发生率,其机制同西罗莫司可以降低巨细胞病毒细胞内p70S6K酶的活性从而抑制巨细胞病毒复制有关[11]。但并非所有的患者均适宜在肾移植后初期使用西罗莫司,选择此类免疫抑制方案前,需对患者进行严格的筛选。 Flechner[12]总结各大移植中心的相关临床经验,指出以下几类患者应尽量避免使用此类免疫抑制方案:①免疫风险较大的患者,主要包括交叉配型供者特异性抗体阳性的患者;群体反应性抗体高于20%-40%的患者;具有因免疫因素导致移植物丢失病史的二次移植患者。②术后易发生切口愈合并发症的患者,主要包括体质量指数> 30-32 kg/m2的肥胖患者;2型糖尿病患者;术前盆腔曾接受过大范围手术或放疗的患者;多年使用激素的患者(具有自身免疫性疾病病史或器官移植病史)。③肾脏原发病同大量蛋白尿相关的患者(如局灶性节段性肾小球硬化症、膜增生性肾小球肾炎等),因此类患者在术后初期使用西罗莫司更易引起蛋白尿的复发。此外,供肾质量在影响肾移植术后初期使用西罗莫司的临床疗效方面也具有重要地位。在一项扩大供肾标准的临床随机对照试验中,Durrbach等[13]使用至少符合下列条件中两项的供肾进行移植:①供者年龄≥60岁。②冷缺血时间≥30 h。③供者血肌酐≥150 μmol/L。④需要升压药维持血压。⑤死因为心肌梗死、脑血管意外或脑卒中。⑥供者具有高血压、冠心病或脑血管意外的病史。结果西罗莫司组的33例患者中有16例因肾功能延迟恢复或外科并发症而退出试验,钙调磷酸酶抑制剂组的36例患者中仅有6例因上述原因退出试验。 综上所述,在供肾质量满意的前提下,免疫风险较小,肾脏原发病同大量蛋白尿关系不大,且术后不易并发切口延迟愈合的患者可以考虑在肾移植后初期使用西罗莫司;在此基础上,若患者具有肿瘤病史、肿瘤风险或巨细胞病毒感染风险较大,选择使用西罗莫司可能会取得更好的临床效果。 2.1.2 抗体诱导方案 目前临床上主张在肾移植后初期使用西罗莫司时联合使用抗体诱导类药物,如白细胞介素2受体拮抗剂、多克隆兔抗人胸腺细胞球蛋白和达利珠单抗等;而不建议不使用抗体诱导的免疫抑制方案。Flechner等[9]的一项随机对照试验结果显示,肾移植术后初期使用西罗莫司的免疫抑制方案(西罗莫司+霉酚酸酯+泼尼松)联合白细胞介素2受体拮抗剂——巴利西单抗可以有效的预防急性排斥反应,使肾移植后1年的急性排斥反应发生率降低至10%以下,且西罗莫司组患者的肾功能优于环孢素组(血肌酐:13.2比17.8 mg/L,P=0.005)。然而,在其他两项不使用抗体诱导治疗方案的随机对照试验中[14-15],虽然西罗莫司组同环孢素组相比,取得了较好的肾功能(血肌酐:1 200比1 450 mmol/L,P=0.01),但急性排斥反应发生率却高达30%-40%。 2.1.3 血药浓度 制定合适的目标血药浓度和密切监测血药浓度对于肾移植后初期使用西罗莫司的临床效果具有非常重要的意义,大部分临床试验认为,在肾移植后最初的6个月内,西罗莫司的谷值浓度应维持在10-15 μg/L[12]。在欧洲的一项多中心研究中,西罗莫司组采用低剂量的治疗方案,目标浓度设定为4-8 μg/L的亚治疗浓度[16];结果1年急性排斥反应发生率高达37%,且肾功能同钙调磷酸酶抑制剂组相比未见优势。近期的一项多中心,随机对照前瞻性研究——ORION试验也再次强调了密切监测药物浓度的重要性[17],此试验因西罗莫司组中56%的患者在肾移植术后最初的6个月内未能达到目标浓度(10-15 μg/L)而导致1年急性排斥反应发生率高达27%,最终被迫停止试验。 2.1.4 主要不良反应 肾移植后初期使用西罗莫司的主要不良反应包括血脂异常、骨髓抑制和切口延迟愈合,其中切口延迟愈合是制约肾移植术后初期使用西罗莫司的一个非常重要的原因。最近研究显示,切口延迟愈合同西罗莫司抑制皮肤中在切口愈合方面起关键作用的γδT细胞有关[18]。 然而,近期研究报告指出可以通过以下方式有效预防切口延迟愈合[19]:①避免在体质量指数> 30- 32 kg/m2的肾移植患者中术后初期使用西罗莫司。②避免使用可吸收线缝合切口。③常规使用切口闭式负压引流两三周。④避免西罗莫司使用剂量超过5 mg/d。 2.2 肾移植后由钙调磷酸酶抑制剂类药物向西罗莫司转换 目前,临床上主要在以下几种情况发生时,考虑由钙调磷酸酶抑制剂类药物向西罗莫司转换:①程序性转换。②患者发生慢性移植肾肾病时。③患者肾移植后并发肿瘤时。 2.2.1 程序性转换 临床上在肾移植后由钙调磷酸酶抑制剂类药物向西罗莫司程序性转换时,一般选择在肾移植后的早期进行,即肾移植后6个月内;6个月后的转换一般效果不理想。 在一项多中心随机对照试验中,Schena等[20]将830例肾移植后6个月到10年(平均3年),且病情稳定的患者按照2∶1的比率随机分为由钙调磷酸酶抑制剂类药物向西罗莫司转换组和继续钙调磷酸酶抑制剂类药物组,分别在开始试验后的12个月和24个月进行意向性分析,结果显示两组患者在肾小球滤过率、移植物丢失和患者死亡率方面无明显差异。 在2012年报道的一项欧洲多中心随机对照试验中,Guba等[21]将140例肾移植后两三周的患者随机分组:继续钙调磷酸酶抑制剂类药物组患者71例,西罗莫司组69例;随访3年,结果显示西罗莫司组患者的肾小球滤过率明显高于钙调磷酸酶抑制剂组[60.88 mL/(min·1.73 m2)比53.72 mL/(min·1.73 m2),P=0.031],在排斥反应发生率、移植物存活率和患者死亡率方面无明显差异,且西罗莫司组患者的蛋白尿未见明显加重,但高脂血症发生率在西罗莫司组较高,钙调磷酸酶抑制剂组的恶性肿瘤发病率较高。同时,Guba等[21]通过多因素分析发现,以下几个因素是转换治疗后移植肾功能恢复不良[肾小球滤过率< 60 mL/(min·1.73 m2)]的预测因素,包括:①供者年龄> 60岁。②转换时血肌酐> 20 mg/L。③转换前使用的钙调磷酸酶抑制剂类药物为环孢素等。肾移植术后早期由钙调磷酸酶抑制剂类药物向西罗莫司转换可以在3年内持续改善移植肾功能,严格的患者筛选是肾移植术后早期由钙调磷酸酶抑制剂类药物向西罗莫司转换获得满意临床效果的关键。 2.2.2 在慢性移植肾肾病患者中的转换治疗 肾移植后使用钙调磷酸酶抑制剂类药物的患者出现慢性移植肾肾病时,使用西罗莫司替代钙调磷酸酶抑制剂类药物,可以在一定程度上改善肾功能。 在一项多中心临床研究中,Uslu等[22]在31例经移植肾活检诊断为慢性移植肾肾病(提示钙调磷酸酶抑制剂类药物慢性肾毒性,伴或不伴随非特异性的肾间质纤维化或肾小管萎缩)的患者中使用由钙调磷酸酶抑制剂类药物向西罗莫司转换的治疗方案,平均随访21.6个月。结果显示转换治疗1年后,患者的肾功能得到明显改善[cGFR:(40.8±2.36) mL/min比(55.7±3.6) mL/min;P < 0.000],随访期间并未观察到移植肾丢失和患者死亡。转换治疗1年后,行程序性活检发现,在肾间质纤维化/肾小管萎缩、肾小球硬化、慢性血管病变评分方面,8例(30%)患者得到改善,11例(42%)表现稳定,7例(28%)有所恶化。并且,Uslu等[22]通过单因素分析发现转换时患者的肾小球滤过率≥40.6 mL/min,血肌酐≤23.4 mg/L,病理组织损伤评分≤3分是转换治疗取得成功的预测因素。除了以上因素外,转换治疗时患者的蛋白尿程度也是一个非常重要的影响因素。Diekmann等[23-24]的研究指出,尿蛋白定量是转换治疗能否成功的独立预测因子,当患者尿蛋白< 0.8g/24 h时,约有90%的患者转换治疗有效。 2.2.3 在并发恶性肿瘤患者中的转换治疗 由于西罗莫司在免疫抑制的同时具有抗肿瘤的优势,因此,临床上在肾移植后患者并发恶性肿瘤特别是kaposi肉瘤时,考虑使用由钙调磷酸酶抑制剂药物向西罗莫司转换的治疗方案。 Stallone等[25]在15例肾移植后经病理活检诊断为kaposi肉瘤的患者中,使用由环孢素向西罗莫司转换的治疗方案;转换治疗3个月后,所有患者的kaposi肉瘤组织均消失,并且在转换治疗6个月后得到病理活检证实,所有患者的病理组织样本中均未发现kaposi肉瘤。随访期间患者肾功能稳定,且均未发生排斥反应。 中国也有相关类似的报告,韩澍等[26]报道了1例使用西罗莫司治疗肾移植后kaposi肉瘤的病例。患者73岁男性,肾移植后3个月发生皮肤kaposi肉瘤,经皮肤病理活检确诊,停用环孢素,免疫抑制方案改用西罗莫司+泼尼松。随访8个月,患者未见新生皮肤肿瘤,肾功能稳定,一般情况良好。相关研究发现,西罗莫司的抗肿瘤机制可能同以下几方面有关:①西罗莫司通过抑制哺乳动物RAPA靶蛋白(mTOR),从而阻断细胞由G1向S期转化,使肿瘤细胞停留在G1期而发生凋亡[27-31]。②通过调节凋亡信号调节酶和C-JunN端粒酶等作用诱导肿瘤细胞凋亡[28, 32]。③通过减少或者抑制血管内皮生长因子等方式抑制肿瘤血管生成,从而导致肿瘤消亡[32-33]。④通过抑制肿瘤细胞利用葡萄糖产生能量,阻止肿瘤细胞利用氨基酸形成新的蛋白质等作用抑制肿瘤生长[34]。 2.2.4 常见并发症 大量尿蛋白是肾移植后由钙调磷酸酶抑制剂类药物向西罗莫司转换治疗的常见并发症。Letavernier等[35]指出,西罗莫司可以通过诱导肾小球足细胞的血管内皮生长因子合成减少,引起足细胞损伤,导致肾小球滤过膜的完整性受损,从而引起或加重蛋白尿。Ko等[36]在近期的动物模型中,进一步证实了足细胞的血管内皮生长因子表达下降同西罗莫司所致蛋白尿之间的关系。 Ruiz等[37]在一项回顾性分析中,将94例使用肾移植后由钙调磷酸酶抑制剂类药物向西罗莫司转换治疗方案的患者按照转换治疗前蛋白尿的严重程度分为3组,即A组:< 300 mg/d,B组300-2 000 mg/d,C组:> 2 000 mg/d,试验结果显示,只有C组患者的尿蛋白加重明显,而其他两组患者的尿蛋白变化不明显。因此,Ruiz等[37]认为在转换治疗前,患者尿蛋白较严重时,则西罗莫司加重蛋白尿的风险较大;而在只有轻微蛋白尿或没有蛋白尿的患者中,此种并发症的风险较小。 田晓辉等[38]在其由钙调磷酸酶抑制剂类药物向西罗莫司转换治疗的临床试验中发现,95例患者中有32例(34%)新发或蛋白尿加重(表1),但是在加用血管紧张素转换酶抑制剂、血管紧张素受体拮抗剂、雷公藤总苷或人工冬虫夏草菌粉后,24例缓解;提示对于换用西罗莫司所引起蛋白尿,可以加用相应的抗蛋白尿药物,以更好达到保护肾脏的目的。"
| [1] Ojo AO, Held PJ, Port FK, et al. Chronic renal failure after transplantation of a nonrenal organ. N Engl J Med.2003;349 (10): 931-940.[2] Glotz D,Charpentier B,Abramovicz D,et al.Thymoglobulin induction and sirolimus versus tacrolimus in kidney transplant recipients receiving mycophenolate mofetil and steroids. Transplantation.2010;89(12):1511-1517.[3] Hamdy AF, Bakr MA, Ghoneim MA. Long-term efficacy and safety of a calcineurin inhibitor-free regimen in live-donor renal transplant recipients. J Am Soc Nephrol.2008; 19(6): 1225-1232.[4] Flechner S M, Goldfarb D, Solez K, et al. Kidney transplantation with sirolimus and mycophenolate mofetil-based immunosuppression: 5-year results of a randomized prospective trial compared to calcineurin inhibitor drugs. Transplantation.2007;83(7):883-892.[5] Larson TS, Dean PG, Stegall MD, et al.Complete avoidance of calcineurin inhibitors in renal transplantation: a randomized trial comparing sirolimus and tacrolimus. Am J Transplant. 2006; 6(3):514-522.[6] Schaefer HM, Kizilisik AT, Feurer I, et al. Short-term results under three different immunosuppressive regimens at one center.Transplant Proc.2006;38(10):3466-3467.[7] Martinez-Mier G, Mendez-Lopez MT, Budar-Fernandez LF, et al. Living related kidney transplantation without calcineurin inhibitors: initial experience in a Mexican center. Transplantation. 2006;82(11):1533-1536.[8] Flechner SM, Kurian SM, Solez K, et al. De novo kidney transplantation without use of calcineurin inhibitors preserves renal structure and function at two years. Am J Transplant. 2004; 4(11):1776-1785.[9] Flechner SM, Goldfarb D, Modlin C, et al. Kidney transplantation without calcineurin inhibitor drugs: a prospective, randomized trial of sirolimus versus cyclosporine. Transplantation.2002;74(8):1070-1076.[10] Kotton CN, Kumar D, Caliendo AM, et al. International consensus guidelines on the management of cytomegalovirus in solid organ transplantation. Transplantation.2010;89(7):779-795.[11] Johnson RA, Wang X, Ma XL, et al. Human cytomegalovirus up-regulates the phosphatidylinositol 3-kinase (PI3-K) pathway: inhibition of PI3-K activity inhibits viral replication and virus-induced signaling.J Virol.2001;75(13):6022-6032.[12] Flechner SM. Sirolimus in kidney transplantation indications and practical guidelines: de novo sirolimus-based therapy without calcineurin inhibitors. Transplantation.2009;87 (8 Suppl): S1-S6.[13] Durrbach A, Rostaing L, Tricot L, et al. Prospective comparison of the use of sirolimus and cyclosporine in recipients of a kidney from an expanded criteria donor. Transplantation.2008;85(3):486-490.[14] Kreis H,Cisterne J M, Land W, et al. Sirolimus in association with mycophenolate mofetil induction for the prevention of acute graft rejection in renal allograft recipients. Transplantation. 2000;69(7):1252-1260.[15] Groth CG, Backman L, Morales JM, et al. Sirolimus (rapamycin)-based therapy in human renal transplantation: similar efficacy and different toxicity compared with cyclosporine. Sirolimus European Renal Transplant Study Group. Transplantation.1999;67(7):1036-1042.[16] Ekberg H,Bernasconi C,Tedesco-Silva H,et al.Calcineurin inhibitor minimization in the Symphony study: observational results 3 years after transplantation. Am J Transplant.2009; 9(8):1876-1885.[17] Flechner SM, Glyda M, Cockfield S, et al.The ORION study: comparison of two sirolimus-based regimens versus tacrolimus and mycophenolate mofetil in renal allograft recipients. Am J Transplant.2011;11(8):1633-1644.[18] Mills RE, Taylor KR, Podshivalova K, et al. Defects in skin gamma delta T cell function contribute to delayed wound repair in rapamycin-treated mice.J Immunol.2008;181(6): 3974-3983.[19] Tiong HY, Flechner SM, Zhou L, et al. A systematic approach to minimizing wound problems for de novo sirolimus-treated kidney transplant recipients. Transplantation.2009; 87(2): 296-302.[20] Schena FP, Pascoe MD, Alberu J, et al. Conversion from calcineurin inhibitors to sirolimus maintenance therapy in renal allograft recipients: 24-month efficacy and safety results from the CONVERT trial. Transplantation.2009 ; 87(2): 233-242.[21] Guba M, Pratschke J, Hugo C, et al. Early conversion to a sirolimus-based, calcineurin-inhibitor-free immunosuppression in the SMART trial: observational results at 24 and 36months after transplantation. Transpl Int.2012; 25(4):416-423.[22] Uslu A, Toz H, Sen S, et al. Late conversion from calcineurin inhibitor-based to sirolimus-based immunosuppression due to chronic toxicity: a prospective study with protocol biopsy amendment. Transplant Proc.2009;41(2):756-763.[23] Diekmann F, Budde K, Oppenheimer F, et al. Predictors of success in conversion from calcineurin inhibitor to sirolimus in chronic allograft dysfunction. Am J Transplant.2004; 4(11): 1869-1875.[24] Diekmann F, Budde K, Slowinski T, et al. Conversion to sirolimus for chronic allograft dysfunction: long-term results confirm predictive value of proteinuria. Transpl Int. 2008;21(2): 152-155.[25] Stallone G,Schena A,Infante B,et al.Sirolimus for Kaposi's sarcoma in renal-transplant recipients. N Engl J Med. 2005; 352 (13):1317-1323.[26] 韩澍,王亚伟,朱有华,等.肾移植术后并发卡波西肉瘤一例报告[J].第二军医大学学报,2007,28(7):708.[27] Fingar DC, Blenis J. Target of rapamycin (TOR): an integrator of nutrient and growth factor signals and coordinator of cell growth and cell cycle progression. Oncogene.2004; 23(18): 3151-3171.[28] Fingar DC, Richardson CJ, Tee AR, et al. mTOR controls cell cycle progression through its cell growth effectors S6K1 and 4E-BP1/eukaryotic translation initiation factor 4E. Mol Cell Biol.2004;24(1):200-216.[29] Schmelzle T, Hall MN. TOR, a central controller of cell growth. Cell.2000;103(2):253-262.[30] Hashemolhosseini S, Nagamine Y, Morley SJ, et al. Rapamycin inhibition of the G1 to S transition is mediated by effects on cyclin D1 mRNA and protein stability. J Biol Chem. 1998;273(23):14424-14429.[31] Abraham RT, Wiederrecht GJ. Immunopharmacology of rapamycin. Annu Rev Immunol.1996;14:483-510.[32] Huang S, Shu L, Dilling MB, et al. Sustained activation of the JNK cascade and rapamycin-induced apoptosis are suppressed by p53/p21(Cip1). Mol Cell.2003;11(6): 1491-1501.[33] Guba M, von Breitenbuch P, Steinbauer M, et al. Rapamycin inhibits primary and metastatic tumor growth by antiangiogenesis: involvement of vascular endothelial growth factor. Nat Med.2002;8(2):128-135.[34] Ai W, Bertram PG, Tsang CK, et al. Regulation of subtelomeric silencing during stress response. Mol Cell.2002; 10(6):1295-1305.[35] Letavernier E, Bruneval P, Vandermeersch S, et al. Sirolimus interacts with pathways essential for podocyte integrity.Nephrol Dial Transplant.2009;24(2):630-638.[36] Ko HT, Yin JL, Wyburn K, et al. Sirolimus reduces vasculopathy but exacerbates proteinuria in association with inhibition of VEGF and VEGFR in a rat kidney model of chronic allograft dysfunction. Nephrol Dial Transplant.2013; 28(2):327-336.[37] Ruiz JC, Diekmann F, Campistol JM, et al. Evolution of proteinuria after conversion from calcineurin inhibitors (CNI) to sirolimus (SRL) in renal transplant patients: a multicenter study. Transplant Proc.2005;37(9):3833-3835.[38] 田晓辉,薛武军,田普训,等.钙调磷酸酶抑制剂转换为西罗莫司治疗慢性移植物肾病的疗效研究[J].器官移植,2012,3(6):320-323.[39] Morrisett JD, Abdel-Fattah G, Kahan BD. Sirolimus changes lipid concentrations and lipoprotein metabolism in kidney transplant recipients.Transplant Proc,2003,35(3 Suppl): 143S-150S.[40] 黄洪锋,吴建永,韩飞,等.慢性移植肾肾病患者西罗莫司替代钙调磷酸酶抑制剂对肾功能的影响[J].中华医学杂志,2011,91(48): 3397-3400.[41] 徐志强,万有贵,陈博,等.西罗莫司在肾移植受者中的转换治疗[J].中国组织工程研究与临床康复,2011,15(5):810-812. |
| [1] | Chen Chang-qing, Shi Bing-yi, Cai Ming, Zhao Yu-bo, Jin Bo-quan, Wang Chun-yan, Han Yong, Xiao Li, Zhou Wen-qiang, Li Zhou-li. Cytotoxic T lymphocyte-associated antigen 4 in acute rejection after renal transplantation [J]. Chinese Journal of Tissue Engineering Research, 2014, 18(5): 730-735. |
| [2] | Wei Xing, Cai Ming, Li Zhou-li, Jin Hai-long, Hong Xin, Chen Chang-qing, Shi Bing-yi. Methylprednisolone therapy for severe pulmonary infection after kidney transplantation [J]. Chinese Journal of Tissue Engineering Research, 2014, 18(5): 742-747. |
| [3] | Guo Cai-long, Mang Yuan-yi, Zhang Lei. A breakthrough in antibody-drug conjugates in anti-immune rejection [J]. Chinese Journal of Tissue Engineering Research, 2014, 18(5): 773-778. |
| [4] | Yue Jiao-xing, Huang Hai. Thoughts on constructing the donation assistance system in China [J]. Chinese Journal of Tissue Engineering Research, 2014, 18(5): 785-790. |
| [5] | Cai Qiu-cheng. T lymphocytes and immune tolerance of liver transplantation [J]. Chinese Journal of Tissue Engineering Research, 2014, 18(5): 791-796. |
| [6] | Yang Ying, Huang Hai, Qiu Hong-zhong. Influence of traditional Chinese culture and ideas on organ donation [J]. Chinese Journal of Tissue Engineering Research, 2014, 18(5): 803-808. |
| [7] | Yu Li-chong, Qian Ye-yong, Shi Bing-yi, Fan Yu, Liu Lu-peng, Yu Fei. Genomics and gene polymorphism of immunosuppressive drugs after kidney transplantation [J]. Chinese Journal of Tissue Engineering Research, 2014, 18(46): 7509-7514. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||