Chinese Journal of Tissue Engineering Research ›› 2022, Vol. 26 ›› Issue (22): 3592-3597.doi: 10.12307/2022.290
Previous Articles Next Articles
Materials of interbody fusion cage: advantages and focus of clinical application
Jin Herong1, Cui Jingbin1, Shao Cang2
- 1School of Mechanical Engineering, Yanshan University, Qinhuangdao 066004, Hebei Province, China; 2Hebei Ruihe Medical Equipment Co., Ltd., Shijiazhuang 050000, Hebei Province, China
-
Received:2020-12-29Revised:2021-02-07Accepted:2021-07-24Online:2022-08-08Published:2022-01-13 -
Contact:Jin Herong, School of Mechanical Engineering, Yanshan University, Qinhuangdao 066004, Hebei Province, China -
About author:Jin Herong, MD, Professor, School of Mechanical Engineering, Yanshan University, Qinhuangdao 066004, Hebei Province, China -
Supported by:Hebei Postgraduate Innovation Funding Project in 2021, No. CXZZSS2021049 (to CJB); Key Research and Development Project of Hebei Province in 2021, No. 21372004D (to JHR, CJB)
CLC Number:
Cite this article
Jin Herong, Cui Jingbin, Shao Cang. Materials of interbody fusion cage: advantages and focus of clinical application[J]. Chinese Journal of Tissue Engineering Research, 2022, 26(22): 3592-3597.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

2.1 金属材料 2.1.1 钛及钛合金 钛及钛合金具有良好的生物相容性、机械性能、抗疲劳性和耐腐蚀性,作为骨科内植物材料被广泛应用于临床,但钛及钛合金融合器存在一定的缺点:在X射线下不易观察骨的融合情况,弹性模量较高,术后容易出现应力遮挡造成椎体下沉等[7]。随着不断深入研究,多孔钛合金融合器作为一个新兴的发展方向引起广泛关注。多孔结构融合器有以下特点:良好的生物相容性;适合细胞黏附、增殖和分化,且有利于细胞向内生长;降低了弹性模量,有效减小或消除应力遮挡。 随着3D打印技术的发展,多孔椎间融合器的制造取得实质性进步。利用选择性激光熔融技术、电子束熔融技术可制造出多孔钛合金椎间融合器,见图2。"


多孔结构钛合金融合器降低了弹性模量,更接近人体骨组织,且内部连通的多孔结构利于骨组织长入,加上其良好的生物相容性和抗腐蚀性,使得钛合金材料应用越来越广泛。多项实验研究已证明,多孔钛合金具有良好的生物相容性且更利于细胞生长[8]。VAN BAEL等[9]采用激光熔融技术打印设计不同孔隙尺寸的多孔结构,可提高其机械性能,增强细胞的增殖和生长量。PONADER等[10]研究表明,人体成骨细胞能够在电子束熔融技术打印的多孔钛合金表面黏附、增殖和分化,且具有良好的生物相容性。2016年,北京爱康宜诚医疗器械有限公司利用电子束熔融技术打印的多孔椎间融合器,获得了国家食品药品监督管理总局认证。此后,3D打印多孔钛合金椎间融合器被逐渐应用于国内临床。杨旭等[11]对比采用聚醚醚酮融合器和3D打印融合器进行颈椎前路减压融合术的60例患者的手术过程和术后恢复情况,采用3D打印融合器不仅能减少手术时间和出血量,术后融合率、骨性结合及抗扭特性方面均优于聚醚醚酮组。刘正蓬等[12]随访63例采用减压手术治疗的脊髓型颈椎病患者,结果表明,应用3D打印椎间融合器比聚醚醚酮椎间融合器稳定性更高且并发症少。3D打印多孔钛合金椎间融合器临床表现均优于聚醚醚酮融合器,相信不久将成为临床上的主流。 2.1.2 钽 钽金属具有良好的生物相容性、无细胞毒性、高度耐腐蚀性等特点,在骨科领域应用广泛。有研究显示,多孔钽椎间融合器的孔隙率高达80%,弹性模量可低至3 GPa,结构上更接近于骨小梁,利于骨组织向内部生长,提高骨愈合率[13]。学者对多孔钽椎间融合器在临床上的应用进行了研究,贺瑞等[14]随访了22例腰椎间盘突出症术后椎间盘复发二次手术的患者,采用钽金属椎间融合器进行手术,术后患者融合情况良好,并发症少;IV-JOHN等[15]随访观察50例应用多孔钽椎间融合器进行腰椎椎间融合术的患者,术后2年融合率为100%;FERNáNDEZ-FAIREN等[16]对57例椎间前路椎间盘切除术进行融合术的患者进行11年的随访,应用多孔钽融合器患者的术后恢复良好,融合率、下沉率及稳定性方面与应用自体骨融合无明显差异;李洋[17]对3D打印多孔钽进行了研究,打印产品符合人骨致密骨的孔隙率要求,在细胞培养过程中没有毒副反应且促进骨细胞的生长和分化。随着3D打印技术及设备的更新,在节约钽材料、降低成本的情况下,多孔钽椎间融合器会进一步得到推广。 2.1.3 镍钛记忆合金 形状记忆合金以其具有超弹性、形状记忆效应等特性和良好的生物相容性,已被广泛应用于临床骨科内植物中。其中镍钛记忆合金除具有其他形状记忆合金的共性外,还具有高耐磨性和耐腐蚀性,且与人骨的弹性模量相近,是一种难得的医用骨科材料[18]。 ASSAD等[19]将镍钛记忆合金腰椎融合器植入绵羊体内,12个月后在绵羊体内展现出了良好的生物相容性,相比传统钛植入物效果更好。HONG等[20]用自体骨移植钉、螺纹圆柱钛和镍钛合金融合器进行动物实验,结果表明镍钛合金融合器的抗变形能力和稳定性均优于其他两组。记忆合金作为椎间融合器缺乏临床数据,但凭借其优良特性和3D打印技术的发展未来应用于临床有巨大潜力。 2.1.4 可降解镁及其合金 金属镁及其合金具有与人骨相近的生物力学性能,相比其他金属材料,镁及其合金的弹性模量与人体皮质骨接近,可实现骨科植入物的轻量化,减小应力遮挡,促进骨骼愈合[21]。此外,与其他可降解高分子材料相比,镁合金具有较高的韧性和力学强度,更符合骨科植入材料的要求。因此,金属镁及其合金在骨科植入物材料中一直备受关注。随着多孔镁材料的出现,在保留金属镁材料本身优势的情况下,通过模拟骨小梁结构进一步降低材料弹性模量,更接近人体骨结构,同时利于骨及软组织的长入[22]。 镁及其合金作为植入物材料也存在一定缺陷,比如降解速率过快、刚度低等。DAENTZER等[23]将镁合金椎间融合器植入羊颈椎中,实验结果显示镁合金椎间融合器溶解较快,且刚度和融合特性较差。刘辰[24]验证了不同比例的镁锶合金、镁铜合金可以降低溶解速率,为学者提供了方向。镁及其合金作为脊柱内植物材料还需克服机械强度、溶解速率等难题,作为在人体中可降解的金属材料,在未来发展中具有非常大的潜力。 2.1.5 其他金属材料 骨科领域常用的金属材料还包括锌合金、不锈钢及钴铬合金等。锌合金在机械强度、延展性和腐蚀速率方面符合结构金属植入物的要求[25]。不锈钢、钴铬合金材料的弹性模量和力学性能不满足脊柱内植物的要求,但随着3D打印设备的更新,目前激光熔融技术及电子束熔融技术3D打印设备均支持不锈钢、钴铬合金材料,可应用于椎间融合器中进行研究和性能分析,增大椎间融合器的研究方向。 2.2 高分子材料 2.2.1 聚醚醚酮 聚醚醚酮是一种具有生物稳定性的高分子材料。聚醚醚酮作为融合器材料有以下优势:首先,聚醚醚酮是一种热塑性聚合物,具有高强度、高刚度、耐腐蚀、抗水解等机械性能,且有良好的生物相容性;其次,聚醚醚酮的弹性模量介于皮质骨和松质骨之间,远低于金属材料,降低了应力遮挡造成椎体下沉的风险,提高融合率;此外,聚醚醚酮能透过X射线,术后容易观察植骨融合情况。相比于传统钛网融合器,聚醚醚酮融合器植入体内下沉量小,在临床上被广泛应用[26]。此外,聚醚醚酮材料因其在熔融加工条件下有突出的熔体流动性能,是一种理想的3D打印材料[27]。以聚醚醚酮为材料,利用3D打印技术制造骨科植入物在国内外研究热点[28-29],2020年赢创推出首个用于医用植入物的3D打印聚醚醚酮长丝[30],标志着聚醚醚酮材料在骨科植入物中重大突破。 聚醚醚酮材料同样也有不足之处,聚醚醚酮表面是疏水的,且其本身是生物惰性的,尤其是与金属内植物相比其骨整合能力不佳,导致表面成骨效能较低,研究人员将聚醚醚酮融合器的表面进行处理,在融合器表面涂层来提高它的成骨效能[31-32]。聚醚醚酮融合器在临床中占据主体地位,对其进行表面涂层和改性仍是今后探索的重要方向。 2.2.2 碳纤维 碳纤维材料轴向刚性理想,支撑效果良好,可以较好地保持椎间高度和脊柱的生理曲度。与金属材料相比,碳纤维材料的最大优势是能够穿透X射线,便于观察椎间骨的融合情况,但有传统观点认为碳纤维材料也有缺点:脆性较大,加工难度较大,产品表面产生的细微毛刺可能引起局部组织感染等。1991年,BRITIGAN等[33]成功研制出碳纤维椎间融合器应用于腰椎,而后逐渐发展成为临床上常用的椎间融合器。有研究表明,碳纤维融合器的术后下沉率和并发症较低[34-35]。王树根等[36]随访65例采用碳纤维融合器和聚醚醚酮融合器治疗腰椎滑脱的患者,结果表明两种材料融合器的临床疗效无显著差异,值得推广应用。 2.2.3 聚乳酸 聚乳酸又称聚丙交酯,是一种新型的可降解材料,包括结晶性的左旋聚乳酸、右旋聚乳酸和无定形的消旋聚乳酸(包含50%的L型单体和50%的D型单体)。 VAN DIJK等[37]将左旋聚乳酸融合器植入山羊的腰椎椎间,一段时间后其生物力学性能表现良好。VAN DIJK等[38]在山羊腰椎中植入左旋聚乳酸椎间融合器和钛金属椎间融合器进行对比,术后一段时间左旋聚乳酸融合器在体内溶解吸收,且椎体融合较好,与钛金属融合器相比有优良的特性。JIYA等[39]将左旋聚乳酸腰椎融合器与聚醚醚酮腰椎融合器进行对照研究,结果表明聚醚醚酮材料融合器在椎间融合方面和下沉率方面都优于左旋聚乳酸融合器。聚乳酸存在降解速率过快、强度低等缺点[40],不适合单独作为融合器材料。 2.2.4 其他高分子材料 医疗领域高分子材料种类繁多,研究在人体可降解生物材料成了主要趋势。聚乙醇酸又称聚羟基乙酸,是具有良好生物相容性和可降解性的高分子材料,被广泛应用于医用缝合线中。聚己内酯是一种高分子有机聚合物,具有良好的生物相容性和生物可降解性,此外还具有良好的形状记忆温控性质和力学特点,在医疗行业常作生物支架材料。但是,聚乙醇酸与聚己内酯在人体降解速率过快[41],相比金属材料、聚醚醚酮材料等其生物力学性能差,无法单独作为椎间融合器材料,研究其复合材料成为主要方向。 赢创成功开发出一种3D打印的自由流动生物可吸收粉末RESOMER? PrintPowder[42],可对其机械性能、可降解性及弹性模量等进行调控,满足椎间融合器要求,有待临床探究。 2.3 无机非金属材料 2.3.1 羟基磷灰石 羟基磷灰石具备优良的生物相容性和骨传导生物活性,其成分与人体骨骼成分相同、结构相近,是难得的骨科植入物材料,但其脆性大,不适合单独用来制造椎间融合器。目前,羟基磷灰石在融合器中常作涂层材料和复合材料,研究人员通过表面喷涂技术应用在金属植入物上用来改善其表面的骨整合性,提高融合率[43-45]。相比传统羟基磷灰石,纳米羟基磷灰石不仅使烧结温度降低,材料的强度、硬度和韧性都有显著提高[46]。已有研究通过3D打印羟基磷灰石树脂材料支架,羟基磷灰石也作为复合材料与聚醚醚酮材料、聚己内酯材料等通过3D打印制作成功[13,27]。 2.3.2 氮化硅 氮化硅(Si3N4 )是一种生物陶瓷材料,具有良好的生物相容性、耐腐蚀性和机械性能,与碳纤维、聚醚醚酮等材料相比具有良好的成骨能力,是理想的骨科植入物材料。 美国一家生物材料公司利用自动注浆成型的3D打印技术,制造出复杂的氮化硅脊柱融合器植入物,并对其性能进行了验证。近年来,对氮化硅生物陶瓷的研究逐渐增多,SUH等[47]通过体外实验研究影响椎间融合器植入椎体间后塌陷因素,结果表明相比钛合金融合器和聚醚醚酮融合器,氮化硅融合器的下降量小。KERSTEN 等[48]将氮化硅融合器和聚醚醚酮融合器植入山羊腰椎中,6个月后两组融合器表现出的生物力学稳定性无明显差异,但氮化硅组在融合率与关节固定方面优于聚醚醚酮组。MCENTIRE等[49]应用聚醚醚酮融合器和氮化硅融合器对92例腰椎疾病患者进行腰椎融合术,随访2年发现聚醚醚酮融合器和氮化硅融合器同样安全有效。氮化硅材料凭借自身优良特性在骨科内植物前景广阔。 2.4 复合材料 为了弥补单一材料椎间融合器的不足,研究提高性能的复合材料也成为了融合器发展的趋势。目前复合材料研究方向主要围绕提高聚醚醚酮材料的成骨性及强度,改变可降解材料降解速率及强度等开展。 2.4.1 聚醚醚酮复合材料 聚醚醚酮作为目前临床上最主要的椎间融合器材料,复合材料可以改变其生物活性和力学性能,从而改善临床效果。马瑞[50]将纳米羟基磷灰石和纳米硅酸钙掺入聚醚醚酮中制成的复合材料,保留聚醚醚酮优良生物力学特性的同时大幅度提高了聚醚醚酮的生物活性,促进骨源细胞的黏附、增殖和成骨分化。TSOU等[51]将纳米二氧化钛与聚醚醚酮制成复合材料,与单纯的聚醚醚酮材料相比,复合材料表现出了较好的细胞相容性和骨整合能力。TAN等[52]通过3D打印技术以聚醚醚酮和羟基磷灰石混合粉末制造出多孔复合高分子材料支架,结构表明该支架结构具有较高的稳定性,且适合细胞黏附增殖。WANG等[53]将碳纤维用来增强聚醚醚酮材料,成骨性增加,且改善了材料表面平滑度。刘学勇等[54]采用聚醚醚酮-羟基磷灰石-碳纤维复合材料与钛合金分别进行椎间盘替换,发现聚醚醚酮复合材料具有较高的融合率和较低的下沉量。 2.4.2 纳米羟基磷灰石/聚酰胺复合材料 纳米羟基磷灰石/聚酰胺复合材料也是临床研究的热点,该材料通过将纳米羟基磷灰石颗粒均匀分散在聚酰胺基质来模拟人体骨组织结构,具有与人体皮质骨相似的力学属性,其植入体内后能够与相邻骨组织中的骨磷灰石结构之间形成化学键连接,为植骨爬行生长提供“支架”结构,相较于聚醚醚酮等材料拥有更为优异的骨传导性[55]。HU等[56]7年内随访了98例进行颈椎前路减压手术的患者,应用纳米羟基磷灰石/聚酰胺66腰椎融合器的患者术后均表现出良好的融合率和低下沉率,与应用聚醚醚酮融合器的患者无明显差异。YANG等[57]对比了钛笼和纳米羟基磷灰石/聚酰胺66融合器的临床效果,纳米羟基磷灰石/聚酰胺66材料表现出更加优良的性能。 2.4.3 可降解复合材料 可降解材料是未来椎间融合器材料的理想方向,聚乳酸、聚乙醇酸与聚己内酯等都是常见的高分子可降解材料,这些材料共同特点是体内降解速率快、刚度低等,无法直接作为椎间融合器的材料。研究人员通过将多种材料混合来改变降解速率和力学特性,临床研究相对较少。聚己内酯与左旋聚乳酸的共聚物支架具有良好的生物相容性,且适于细胞黏附生长[58]。王丽等[59]利用纳米β-磷酸三钙/聚乳酸复合材料制备颈椎椎间融合器,生物力学性能良好。CAO等[60]将聚乳酸/纳米磷酸三钙复合材料融合器与聚醚醚酮融合器植入山羊颈椎中,复合材料在融合性和稳定性方面均优于聚醚醚酮组。2020年1月,空军军医大学西京医院将3D打印的可降解聚己内酯-磷酸三钙椎间融合器首次应用于临床[61],结果有待考究。目前临床常用椎间融合器材料,见表1。"
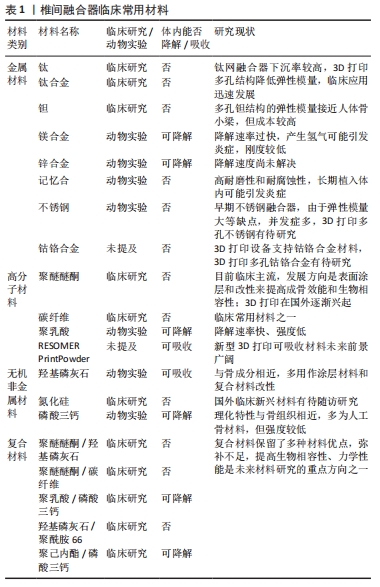

2.5 融合器中的填充物材料 临床上将椎间融合器中填充小颗粒和块状材料来提高骨的融合率和细胞黏附性,目前常用的填充材料有自体骨(如髂骨、腓骨等)、同种异体骨、人工骨和骨形态发生蛋白等。 2.5.1 自体骨 手术中将椎间减压操作时取出的自体骨中的松质骨充填于融合器内,其良好的免疫相容性和促成骨作用有利于骨融合,用自体松质骨作为填充材料是椎间融合器目前最广泛的应用形式。一些自体骨采用“就地取材”的方法,如进行腰椎手术椎板减压的同时将切下的椎板和棘突等材料加工成骨粒,颈椎前路环锯法切除的椎体骨也可以加工成骨粒填入椎间融合器中,这样可以不用取自体髂骨。为了避免产生二次损伤或疼痛并发症,取出骨量有限,开发可供替代的新材料具有重要研究意义。 2.5.2 同种异体骨 同种异体骨经过深低温冷冻去除过敏原等处理后也可用于融合器的填充体,其主要来源于尸体的骨组织,容易获得,是自体骨较好的替代品。MILLER等[62]对自体骨和同种异体骨进行分析性对比研究,随访结果表明同种异体骨在骨愈合和并发症方面与自体骨无明显差异。YUE等[63]对71例做前颈椎间盘摘除术并采用同种异体植骨融合术的患者随访2年,发现骨性融合率达92.6%。同种异体骨一定程度上可以替代自体骨,但也有研究表明采用同种异体骨少数人会出现融合不佳、疼痛等并发症,因此同种异体骨还需进一步探究,其与人工骨材料混合来减少并发症具有一定的研究前景。 2.5.3 人工骨 作为自体骨填充材料的替代品,人工骨材料发展较快,羟基磷灰石、硫酸钙、磷酸三钙是目前应用较多的人工骨材料。羟基磷灰石人工骨作为椎间融合器的效果不及自体骨,但可以提高融合率[64]。WANG等[53]将自体骨和硫酸钙人工骨作为填充材料应用到颈椎融合器中,随访结果表明融合情况无明显差异。KIM等[65]将聚醚醚酮融合器与填充磷酸三钙的聚醚醚酮融合器植入后路腰椎椎间融合的患者体内,填充磷酸三钙的一侧早期融合率明显提高。普通人工骨作为骨传导、诱导支架填充于椎间融合器中存在一定的短板:①不利于填充,需要制备成粉粒或者多孔块状;②填充后不易凝固成形;③不携带成骨细胞,它仅是一个诱导界面骨长入的支架,与人骨相比其骨诱导性能及生物活性存在差距,需要携带骨形成蛋白才能最大限度发挥骨诱导能力,促进新骨的长入和血管化。 普通的人工骨不携带成骨细胞,它仅是一个诱导界面骨长入的支架,与人骨相比的骨诱导性能及生物活性存在差距。有研究人员提出组织工程化的人工骨[66],将人工骨制成块状体或颗粒支架作为基体,将体外培养的成骨活性细胞或诱导分化的间充质干细胞在基体上培养一定时间后置入椎间融合器孔中,来促进新骨融合效能,重新建立界面骨与人工骨的融合长入。未来研究组织工程化的人工骨将是替代自体骨填充材料的重要方向。 2.5.4 骨形态发生蛋白 骨形态发生蛋白是一种功能蛋白,广泛存在于动物的骨组织和血细胞中,可促进间充质细胞定向分化成骨细胞,加快骨愈合。骨形态发生蛋白是URIST于1965年首次发现,其中以人重组骨形态发生蛋白2的诱骨活性最强,可诱导成骨细胞和软骨细胞分化,最终形成新骨,获得广泛的临床应用[67-68]。SINGH等[69]总结了10年骨形态蛋白在脊柱融合术中的应用,结果表明可以提高植骨融合率。ANNIS等[70]2年内随访61例进行椎骨融合的患者,结果表明低剂量的骨形态发生蛋白2在骨固定及融合中可获得满意的融合率。WEISBROD 等[71]回顾性研究了26例进行颈椎前路椎前盘切除和融合术的患者,研究表明人重组骨形态发生蛋白2辅助的脊柱融合,既可加速愈合又可消除自体移植患者的发病率。虽然骨形态发生蛋白在临床上已广泛应用,但其有的并发症也逐渐显现出来 [72-73],需进一步研究和实验验证。"

| [1] KOH K, YAMADA K, ENOMOTO T, et al. Sex-Specific Impact of Pain Severity, Insomnia, and Psychosocial Factors on Disability due to Spinal Degenerative Disease. Pain Res Manag. 2020;2020:1-6. [2] 汤泽瀚.新型3D打印颈椎椎间融合器的研制及动物实验初步研究[D].上海:中国人民解放军海军军医大学,2019. [3] RAO PJ, PELLETIER MH, WALSH WR, et al. Spine interbody implants: material selection and modification, functionalization and bioactivation of surfaces to improve osseointegration. Orthop Surg. 2014;6:81-89. [4] 黎庆初,闫慧博.前路椎体间融合术治疗腰椎退变性疾病[J].中国矫形外科杂志,2020,28(1):47-52. [5] OLIVARES-NAVARRETE R, HYZY SL, SLOSAR PJ, et al. Implant materials generate different peri-implant inflammatory factors: poly-ether-ether- ketone promotes fibrosis and microtextured titanium promotes osteogenic factors. Spine (Phila Pa 1976). 2015;40:399-404. [6] GUYER RD, ABITBOL JJ,O HNMEISS DD, et al.Evaluating osseointegration into a deeply porous titanium scaffold: a biomechanical comparison with PEEK and allograft. Spine (Phila Pa 1976). 2016;41:E1146-1150. [7] 赵勃然,郑修军,马金荣.椎间融合器及其材料的研究与进展[J].中国组织工程研究,2017,21(2):315-321. [8] 姜威,毛克亚.颈椎椎间融合器设计的历史沿革与研究进展[J].解放军医学院学报,2018,39(6):538-541. [9] VAN BAEL S, CHAI YC, TRUSCELLO S, et al. The effect of pore geometry on the in vitro biological behavior of human periosteum-derived cells seeded on selective laser-melted Ti6Al4V bone scaffolds. Acta Biomater. 2012;8(7):2824-2834. [10] PONADER S, VAIRAKTARIS E, HEINL P, et al. Effects of topographical surface modifications of electron beam melted Ti-6Al-4V titanium on human fetal osteoblasts. J Biomed Mater Res A. 2010;84A(4):1111-1119. [11] 杨旭,赵晓峰,齐德泰,等.3D打印ACT钛金骨小梁椎间融合器行颈椎前路减压融合后颈椎的矢状位平衡变化[J].中国组织工程研究,2020,24(36):5741-5748. [12] 刘正蓬,王雅辉,张义龙,等.3D打印椎间融合器置入治疗脊髓型颈椎病:颈椎曲度及椎间高度恢复的半年随访[J].中国组织工程研究,2021,25(6):849-853. [13] 王林楠,杨曦,宋跃明.3D打印技术在椎间融合临床应用的研究进展[J].华西医学,2018,33(9):1061-1067. [14] 贺瑞,张文志,尚希福,等.钽金属椎间融合器在腰椎间盘突出症减压术后复发融合术中的应用[J]. 颈腰痛杂志,2013(5):387-390. [15] IV-JOHN, BEUTLER W, PEPPELMAN W, et al. Clinical Outcomes with Porous Tantalum in Lumbar Interbody Fusion. Spine J. 2010;10(9-supp-S):S147-S148. [16] FERNÁNDEZ-FAIREN M, ALVARADO E, TORRES A. Eleven-year follow-up of two cohorts of patients comparing stand-alone porous tantalum cage versus autologous bone graft and plating in anterior cervical fusions. World Neurosurg. 2019;122: e156-e167. [17] 李洋.激光增材制造(3D打印)制备生物医用多孔金属工艺及组织性能研究[D].苏州:苏州大学,2015. [18] 赵维彪.镍钛形状记忆合金的材料学特征与医学应用[J].中国组织工程研究,2007,11(22):4376-4379. [19] ASSAD M, CHERNYSHOV AV, JARZEM P, et al. Porous Titanium-Nickel for Intervertebral Fusion in a Sheep Model: Part 2. Surface Analysis and Nickel Release Assessment. J Biomed Mater Res B Appl Biomater. 2003;64(2):121-129. [20] HONG X, WU XT, ZHUANG SY, et al. New Cage for Posterior Minimally Invasive Lumbar Interbody Fusion: a Study in Vitro and in Vivo. Orthop Surg. 2014;6(1):47-53. [21] ELKAIAM L, HAKIMI O, YOSAFOVICH-DOITCH G, et al. In Vivo Evaluation of Mg–5%Zn–2%Nd Alloy as an Innovative Biodegradable Implant Material. Ann Biomed Eng. 2019;48(2367):1-13. [22] 许灏铖,张帆,吕飞舟,等.金属镁及其合金植入材料在脊柱外科中的应用[J].国际骨科学杂志,2016,37(5):269-273. [23] DAENTZER D, WILLBOLD E, KALLA K, et al. Bioabsorbable interbody magnesium-polymer cage: degradation kinetics, biomechanical stiffness, and histological findings from an ovine cervical spine fusion model. Spine (Phila Pa 1976). 2014;39(20):E1220-E1227. [24] 刘辰.骨植入用新型可降解镁合金材料设计及生物医学功能研究[D].南京:南京理工大学,2016. [25] KAFRI A, OVADIA S, YOSAFOVICH-DOITCH G, et al. The Effects of 4%Fe on the Performance of Pure Zinc as Biodegradable Implant Material. Ann Biomed Eng. 2019;47(6):1400-1408. [26] SEAMAN S, KEREZOUDIS P, BYDON M, et al. Titanium vs. polyetheretherketone (PEEK) interbody fusion: meta-analysis and review of the literature. J Clin Neurosci. 2017;44:23-29. [27] 韩淑芬,陈伟伟,于洁.3D打印高分子材料研究进展[J].工程塑料应用,2017,45(10):146-150. [28] PHILIPP H, NEHA S, BRANDO O, et al. Patient-Specific Surgical Implants Made of 3D Printed PEEK: Material, Technology, and Scope of Surgical Application. Biomed Res Int. 2018;2018:4520636. [29] AHN H, PATEL RR, HOYT AJ, et al. Biological evaluation and finite-element modeling of porous poly( para -phenylene) for orthopaedic implants. Acta Biomater. 2018:S1742706118301454. [30] 钱伯章.赢创推出首个用于医用植入物的3D打印聚醚醚酮长丝[J].合成纤维,2020,49(6):59-59. [31] WILLEMS K, LAUWERYNS P, VERLEYE G, et al. Randomized controlled trial of posterior lumbar interbody fusion with Ti-and CaP-nanocoated polyetheretherketone cages: comparative study of the 1-year radiological and clinical outcome. Int J Spine Surg. 2020;13(6):575-587. [32] HASEGAWA T, USHIROZAKO H, SHIGETO E, et al. The Titanium-coated PEEK Cage Maintains Better Bone Fusion With the Endplate Than the PEEK Cage 6 Months After PLIF Surgery: A Multicenter, Prospective, Randomized Study. Spine (Phila Pa 1976). 2020;45(15):E892-E902. [33] BRANTIGAN JW, STEFFEE AD. A carbon fiber implant to aid interbody lumbar fusion. Two-year clinical results in the first 26 patients. Spine (Phila Pa 1976). 1993;18(14):2106-2107. [34] WANG YT, WU XT, CHEN H, et al. Endoscopy-assisted posterior lumbar interbody fusion in a single segment. J Clin Neurosci. 2013;21(2):287-292. [35] 宋成哲,金红旭.碳纤维椎间融合器与钛网椎间融合器修复腰椎退行性变:生物相容性比较[J].中国组织工程研究,2015,19(12): 1909-1913. [36] 王树根,孙学猛,刘瑞存,等.两种椎间融合器联合椎弓根螺钉治疗腰椎滑脱症的疗效比较[J].中国医药指南,2017,15(4):8-9. [37] VAN DIJK M, SMIT TH, BURGER EH, et al. Bioabsorbable poly-L-lactic acid cages for lumbar interbody fusion: three-year follow-up radiographic, histologic, and histomorphometric analysis in goats. Spine (Phila Pa 1976). 2002;27(23): 2706-2714. [38] VAN DIJK M, SMIT TH, SUGIHARA S, et al. The effect of cage stiffness on the rate of lumbar interbody fusion: an in vivo model using poly (L- lactic acid) and Titanium cages. Spine (Phila Pa 1976). 2002;27(2): 682-688. [39] JIYA T, SMIT T, DEDDENS J, et al. Posterior lumbar interbody fusion using nonresorbable poly-ether-ether-ketone versus resorbable poly-L-lactide-co-D,L-lactide fusion devices: a prospective, randomized study to assess fusion and clinical outcome. Spine (Phila Pa 1976). 2009;34(3):233-237. [40] REGNELL ANDERSSON S, HAKKARAINEN M, INKINEN S, et al. Customizing the Hydrolytic Degradation Rate of Stereocomplex PLA through Different PDLA Architectures. Biomacromolecules. 2012; 13(4):1212-1222. [41] 王乐,刘少喻.可吸收聚合物材料制作椎间融合器的临床应用[J].中国组织工程研究,2013,17(42):7462-7468. [42] 王哲.赢创开发出全球首款面向植入式医疗器械3D打印的自由流动生物可吸收粉末[J].现代化工,2020,40(2):12. [43] 林巧霞,殷萌,魏延,等.钛及钛合金表面羟基磷灰石涂层结合强度及稳定性[J].化学进展,2020,32(4):54-64. [44] YAN L, LENG Y, WENG LT. Characterization of chemical inhomogeneity in plasma-sprayed hydroxyapatite coatings. Biomaterials. 2003;24(15): 2585-2592. [45] CIZEK J, KHOR KA, PROCHAZKA Z. Influence of spraying conditions on thermal and velocity properties of plasma sprayed hydroxyapatite. Mater Sci Eng C. 2007;27(2):340-344. [46] SADOWSKA JM, WEI F, GUO J, et al. Effect of nano-structural properties of biomimetic hydroxyapatite on osteoimmunomodulation. Biomaterials. 2018;181:318-332. [47] SUH P B, PUTTLITZ C, LEWIS C, et al. The effect of cervical interbody cage morphology, material composition, and substrate density on cage subsidence. J Am Acad Orthop Surg. 2017;25(2):160-168. [48] KERSTEN RFMR, WU G, POURAN B, et al. Comparison of polyetheretherketone versus silicon nitride intervertebral spinal spacers in a caprine model. J Biomed Mater Res B Appl Biomater. 2019; 107(3):688-699. [49] MCENTIRE BJ, MASLIN G, BAL BS. Two-year results of a double-blind multicenter randomized controlled non-inferiority trial of polyetheretherketone (PEEK) versus silicon nitride spinal fusion cages in patients with symptomatic degenerative lumbar disc disorders. J Spine Surg. 2020;6(3): 523. [50] 马瑞.纳米生物陶瓷/聚醚醚酮复合物骨生物活性的研究[D].上海:上海交通大学,2015. [51] TSOU HK, HSIEH PY, CHI MH, et al. Improved osteoblast compatibility of medical-grade polyetheretherketone using arc ionplated rutile/anatase titanium dioxide films for spinal implants. J Biomed Mater Res A. 2012;100A(10):2787-2792. [52] TAN KH, CHUA CK, LEONG KF, et al. Fabrication and characterization of three-dimensional poly(ether- ether- ketone)/-hydroxyapatite biocomposite scaffolds using laser sintering. Proc Inst Mech Eng H. 2005;219(3):183-194. [53] WANG Z, GAO D. Friction and wear properties of stainless steel sliding against polyetheretherketone and carbon-fiber-reinforced polyetheretherketone under natural seawater lubrication. Mater Des. 2014;53:881-887. [54] 刘学勇,荆延峰,朱洪欣,等.聚醚醚酮/羟基磷灰石/碳纤维复合材料的生物力学分析[J].生物医学工程与临床,2013(3):202-207. [55] LI J, ZUO Y, CHENG X, et al. Preparation and characterization of nano-hydroxyapatite/polyamide 66 composite GBR membrane with asymmetric porous structure. J Mater Sci Mater Med. 2009;20(5):1031-1038. [56] HU B, YANG X, HU Y, et al. The n-HA/PA66 cage versus the PEEK cage in anterior cervical fusion with single-level discectomy during 7 years of follow-up. World Neurosurg. 2019;123:e678-e684. [57] YANG X, CHEN Q, LIU L, et al. Comparison of anterior cervical fusion by titanium mesh cage versus nano-hydroxyapatite/polyamide cage following single-level corpectomy. Int Orthop. 2013;37(12):2421-2427. [58] NIE W, GAO Y, MCCOUL DJ, et al. Rapid mineralization of hierarchical poly (l-lactic acid)/poly (ε-caprolactone) nanofibrous scaffolds by electrodeposition for bone regeneration. Int J Nanomedicine. 2019;14: 3929. [59] 王丽,王少俊,范仲勇,等.立构共聚聚乳酸/纳米β-磷酸三钙复合材料制备可吸收双层椎间融合器及其降解性能[J].复旦学报(自然科学版),2012,51(3):325-334. [60] CAO L, CHEN Q, JIANG LB, et al. Bioabsorbable self-retaining PLA/nano-sized β-TCP cervical spine interbody fusion cage in goat models: An in vivo study. Int J Nanomedicine. 2017;12:7197-7205. [61] 空军军医大学西京医院新型聚己内酯—磷酸三钙可降解颈椎椎间融合器首次应用临床[J].医学争鸣,2020,11(2):6. [62] MILLER LE, BLOCK JE. Safety and effectiveness of bone allografts in anterior cervical discectomy and fusion surgery. Spine (Phila Pa 1976). 2011;36(24):2045-2050. [63] YUE WM, BRODNER W, HIGHLAND TR. Long-term results after anterior cervical discectomy and fusion with allograft and plating: a 5-to 11-year radiologic and clinical follow-up study. Spine (Phila Pa 1976). 2005;30(19):2138-2144. [64] KUSHIOKA J, KAITO T, MAKINO T, et al. Difference in the fusion rate and bone formation between artificial bone and iliac autograft inside an inter-body fusion cage - A comparison between porous hydroxyapatite/type 1 collagen composite and autologous iliac bone. J Orthop Sci. 2018:S0949265818300927. [65] KIM KT, KIM KG, CHOI UY, et al. Safety and Tolerability of Stromal Vascular Fraction Combined with β-Tricalcium Phosphate in Posterior Lumbar Interbody Fusion: Phase I Clinical Trial. Cells. 2020;9(10):2250. [66] 王建华.椎间融合器内填充材料及技术[J].美中国际创伤杂志, 2005,4(4):32-33. [67] JUN SH, LEE EJ, JANG TS, et al. Bone morphogenic protein-2 (BMP-2) loaded hybrid coating on porous hydroxyapatite scaffolds for bone tissue engineering. J Mater Sci Mater Med. 2013;24(3):773-782. [68] XIE XW, JIANG H, LI N, et al. Recombinant human bone morphogenetic protein-2 induces bone repair. Chin J Tissue Eng Res. 2013;5 Suppl 7:S27-29. [69] SINGH K, NANDYALA SV, MARQUEZ-LARA A, et al. Epidemiological trends in the utilization of bone morphogenetic protein in spinal fusions from 2002 to 2011. Spine (Phila Pa 1976). 2014;39(6):491-496. [70] ANNIS P, BRODKE DS, SPIKER WR, et al. The Fate of L5-S1 with Low dose BMP-2 and Pelvic Fixation, with or without Interbody Fusion, in Adult Deformity Surgery. Spine (Phila Pa 1976). 2015;40(11):634-639. [71] WEISBROD LJ, ARNOLD PM, LEEVER JD. Radiographic and CT Evaluation of Recombinant Human Bone Morphogenetic Protein-2–assisted Cervical Spinal Interbody Fusion. Clin Spine Surg. 2019;32(2):71-79. [72] 禹名卉,赵彦涛,衷鸿宾,等.骨形态发生蛋白2在腰椎融合术中应用的效果与并发症[J].中国骨与关节杂志,2017,6(3):228-231. [73] TANNOURY CA, AN HS. Complications with the use of bone morphogenetic protein 2 (BMP-2) in spine surgery. Spine J. 2014;14(3):552-559. |
| [1] | Yao Xiaoling, Peng Jiancheng, Xu Yuerong, Yang Zhidong, Zhang Shuncong. Variable-angle zero-notch anterior interbody fusion system in the treatment of cervical spondylotic myelopathy: 30-month follow-up [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1377-1382. |
| [2] | Zhang Jinglin, Leng Min, Zhu Boheng, Wang Hong. Mechanism and application of stem cell-derived exosomes in promoting diabetic wound healing [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1113-1118. |
| [3] | An Weizheng, He Xiao, Ren Shuai, Liu Jianyu. Potential of muscle-derived stem cells in peripheral nerve regeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1130-1136. |
| [4] | Song Yuxin, Zhang Tongtong, Niu Jianxiong, Wang Zengping, Wen Jie, Zhang Qunli, Xue Wen, Liu Lin. Precise screw placement of 3D printing model and orthopedic robot in spinal deformity [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 904-907. |
| [5] | Yang Jun, Yang Qun, Zhang Rui, Jiang Chang. A novel slidable pedicle screw-rod system for lumbar tuberculosis: promoting bone graft fusion by producing stress stimulation to fused segment [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 914-918. |
| [6] | Li Jian, Bao Zhengqi, Zhou Pinghui, Zhu Ruizhi, Li Zhixiang, Wang Jinzi. Effects of posterior single open-door laminoplasty and anterior cervical corpectomy fusion on cervical sagittal balance parameters in the treatment of multilevel cervical spondylotic myelopathy [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 949-953. |
| [7] | He Yunying, Li Lingjie, Zhang Shuqi, Li Yuzhou, Yang Sheng, Ji Ping. Method of constructing cell spheroids based on agarose and polyacrylic molds [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 553-559. |
| [8] | He Guanyu, Xu Baoshan, Du Lilong, Zhang Tongxing, Huo Zhenxin, Shen Li. Biomimetic orientated microchannel annulus fibrosus scaffold constructed by silk fibroin [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 560-566. |
| [9] | Yang Feng, Zhao Qian, Zhang Shixuan, Zhao Tienan, Feng Bo. Effectiveness and safety of rapamycin combined with CD133 antibody stent in preventing vascular restenosis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 579-584. |
| [10] | Chen Xiaoxu, Luo Yaxin, Bi Haoran, Yang Kun. Preparation and application of acellular scaffold in tissue engineering and regenerative medicine [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 591-596. |
| [11] | Kang Kunlong, Wang Xintao. Research hotspot of biological scaffold materials promoting osteogenic differentiation of bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 597-603. |
| [12] | Shen Jiahua, Fu Yong. Application of graphene-based nanomaterials in stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 604-609. |
| [13] | Wang Ruanbin, Cheng Liqian, Chen Kai. Application and value of polymer materials in three-dimensional printing biological bones and scaffolds [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 610-616. |
| [14] | Zhang Tong, Cai Jinchi, Yuan Zhifa, Zhao Haiyan, Han Xingwen, Wang Wenji. Hyaluronic acid-based composite hydrogel in cartilage injury caused by osteoarthritis: application and mechanism [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 617-625. |
| [15] | Li Hui, Chen Lianglong. Application and characteristics of bone graft materials in the treatment of spinal tuberculosis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 626-630. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||