Chinese Journal of Tissue Engineering Research ›› 2021, Vol. 25 ›› Issue (20): 3226-3231.doi: 10.3969/j.issn.2095-4344.3128
Previous Articles Next Articles
Guided bone regeneration in a small animal model of critical size craniofacial bone defects
He Fan1, 2, Xiong Xiuli2, Shan Xianfeng1, Zhang Shutong1, Hu Jian2, Wang Xuejin3
- 1School of Medicine, Dalian University, Dalian 116000, Liaoning Province, China; 2Meishan Municipal People’s Hospital, Meishan 620010, Sichuan Province, China; 3Affiliated Zhongshan Hospital of Dalian University, Dalian 116000, Liaoning Province, China
-
Received:2020-06-09Revised:2020-06-11Accepted:2020-07-06Online:2021-07-18Published:2021-01-15 -
About author:Wang Xuejin, Professor, Affiliated Zhongshan Hospital of Dalian University, Dalian 116000, Liaoning Province, China
CLC Number:
Cite this article
He Fan, Xiong Xiuli, Shan Xianfeng, Zhang Shutong, Hu Jian, Wang Xuejin. Guided bone regeneration in a small animal model of critical size craniofacial bone defects[J]. Chinese Journal of Tissue Engineering Research, 2021, 25(20): 3226-3231.
share this article
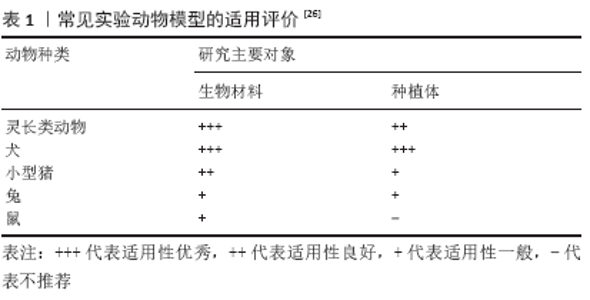
2.1 引导骨再生技术 20世纪70年代和80年代,关于牙周组织再生潜能的一系列研究逐步促成了引导组织再生原理的提出和发展。在这些实验中,研究者证明了应用屏障膜隔离上皮和结缔组织细胞,可以在牙周缺损愈合期间为牙周膜细胞重新占据牙根表面并在牙骨质层产生新的穿通纤维提供所需的空间和时间[4-5]。引导组织再生技术的临床应用包括在根部表面附近放置屏障膜,形成一个只能由牙周膜或牙槽骨来源细胞重新占据的封闭空间。同时,屏障膜阻止牙龈结缔组织成纤维细胞和口腔上皮在牙根表面生长。理论上来讲,这将导致新的结缔组织附着形成。然而,许多研究结果表明,应用屏障膜隔离出的封闭空间,为存在于骨缺损表面的骨形成细胞提供了占据该空间并进一步促进其生长的可能性[11]。因此,在将引导组织再生技术早期应用于牙周组织再生之后,许多临床前和临床研究也采用了相同的治疗原理来进行骨缺损再生或骨增量[12-13]。鉴于这种特殊的应用,以重建骨组织为目的的引导组织再生技术被正式命名为“引导骨再生技术”,其生物学原理是从骨缺损中机械地隔绝邻近的软组织,从而仅允许源自骨缺损边缘的成骨细胞重新占据骨缺损空间[14]。 2.2 临界骨缺损模型 Schmitz等[15]早在20世纪80年代就提出了临界骨缺损这一概念,即骨缺损大小达到临界值后,自然状态下缺损区域将无法形成骨性愈合,最终由纤维结缔组织填塞。这种类型的骨缺损可以在动物体内构建出适当的实验模型,从而评价不同治疗方式对骨再生效果的影响。临界骨缺损模型被广泛应用于原理验证性研究中,其优点主要表现在:①愈合是在原位骨内愈合,如在下颌骨或小腿内,这使得研究结果相比较于异位移植模型更有说服力[16];②临界骨缺损模型允许研究者以标准化和区分性的方式评估骨再生材料性能。“临界缺损尺寸”一词的现代含义中,通常不意味着可能的最小尺寸大小或者扩展愈合时间到动物的整个生命周期,相反,“临界缺损尺寸”指在特定时间内缺损无法修复的任何尺寸[17-18]。导致这种概念认知的区别是由于年龄、性别、动物品种和其他特征可能会影响愈合,例如,在CD-1小鼠颅顶骨缺陷中,直径3 mm、4 mm和5 mm对成年小鼠而言,是临界值;但对幼鼠而言,却具有较高的愈合可能[19]。因此很难准确确定最小的缺损尺寸,也由于实际的限制难以将预计观察的时间延长到动物模型的整个寿命。由于这些困难,现代骨再生领域的研究人员倾向于发展可重复的、在一段骨形成时间内缺损无法修复的实验模型。尽管目前计算机建模和体外实验技术都取得了巨大的进展,依然不存在可以模拟出复杂体内环境的离体模型[20-21]。因而,可重复并且经过验证的动物实验模型依然是新材料和新技术在临床转化前评估其安全性和有效性的最佳选择。 2.3 动物种类的选择 灵长类动物,如猴和狒狒等,由于其解剖和生理状况与人类最为接近,被认为是临床前研究的理想模型。除猴外,犬也被广泛用于构建缺损,一些研究还使用了老鼠、小型猪、绵羊和兔子[22]。按照动物体质量来进行分类的话,引导骨再生研究中使用的实验动物模型通常分为小动物模型(小鼠、大鼠和兔子)和大动物模型模型(犬、猪和猴等)。实验模型的选择很大一方面取决于研究目标和实验室的限制,如大型或非标准动物房。考虑到伦理、成本和社会问题,大型动物的使用是需要慎重考虑的,如猴和犬,应在小型动物无法模拟出临床情况时或者研究的最后验证阶段使用[23-24]。在大多数情况下,特别是探索性的研究中,像鼠和兔这样的小动物模型足以在组织学水平上评估材料生物活性成分在引导骨再生中的作用,其结果具有足够的统计学意义和医学相关性。另一方面,小型动物可以植入满足研究需求的、大小合适的生物支架材料,如兔下颌骨磨牙/前磨牙区域就足够大(长17 mm,高16 mm,深6 mm),十分利于外科手术和材料植入[25]。表1总结了口腔种植研究中常见动物种类在不同研究目的下的适用情况。 2.4 颅颌面部的临界骨缺损模型 2.4.1 颌面部临界骨缺损模型 鼠类是比较早地应用于引导骨再生研究的动物。20世纪80年代末,DAHLIN等[27]为了深入研究引导骨再生技术在临界缺损骨再生的潜力,在Sprague-Dawley大鼠双侧下颌制备了直径5 mm大小的缺损,首次在大鼠颌面部进行了引导骨再生技术的研究。实验组用聚四氟乙烯(poly tetra fluoroethylene,PTFE)膜覆盖,对照组不覆盖膜,结果发现,在实验组中,经6周愈合后,缺损区出现了完全的骨愈合;而对照组即使在22周后,显示缺损边缘部分愈合,缺损中心存在结缔组织。这项研究的结果首次表明,通过屏障膜机械性地隔离骨缺损可以使来源于缺损壁的骨形成细胞实现缺损区的骨再生;同时,屏障膜阻碍了来自周围软组织的非成骨细胞的侵入。之后,不少研究者也应用相同或类似的模型,来研究不同干预方式下引导骨再生的情况[28-29]。但在不同研究中,鼠的选择和模型建立也有差别,因而很难直接将不同研究者的研究成果进行比较直观的比较。为了将实验结果标准化,有学者提出了建立应用于引导骨再生研究的鼠颌面临界骨缺损模型的标准化程序。LIU等[30]在严格控制实验大鼠的年龄、体质量和性别等因素下,通过CT分析大鼠下颌骨解剖特征,认为下颌前牙区相比较于后牙区和升支具有更多的骨量,然后以建立临界骨缺损为目标,在下颌前牙区通过不断扩大缺损大小建模,最终认为6 mm×2 mm(长×宽)和8 mm×2 mm的缺损可以作为临界骨缺损应用于引导骨再生的研究中,并用多种生物材料来测试模型,认为这种标准化的模型能够满足生物材料研究要求,可以进一步优化材料评价体系。 兔用于实验研究有着很悠久的历史,20世纪上半叶,兔开始应用于骨科领域,用来分析新骨的新成和改建。口腔生物材料在兔体内的评价实验,较为常见的是在口腔外进行的。兔的下颌骨主要由皮质骨构,类似于人的下颌骨[25],因而许多研究是在下颌骨中进行的。在有关于兔下颌的模型中,文献报道最常见的2个部位是下颌角和下颌体。下颌角相对容易进行手术,对动物咀嚼能力的影响也最小,但是下颌角是一块较薄的骨头,骨髓较少,不含牙齿,这可能在通用性上限制了其作为引导骨再生模型的应用[31]。因此,下颌角缺损模型可能更适合于细胞和负载有限的材料在骨再生的研究。相比之下,下颌骨体建立的缺损模型可以用来研究牙列承重区几种组织类型的再生。根据研究所需的复合型组织缺损的类型,可以通过手术在下颌骨下缘或下颌骨体中部构建缺损区,并延伸到所对应的牙列。下缘缺损模型可以评估骨和神经的再生,而下颌骨体的缺损则可以用来评估骨、牙齿和口腔黏膜的修复[32]。LYE等[33]在评价聚甲基丙烯酸甲酯(PMMA)的生物相容性研究中,参考了牵张成骨的模型,通过下颌下切口入路,暴露了兔的双侧下颌骨体侧面(从颏孔到升支,高约6 mm,宽约10 mm),然后将第2前磨牙至第1磨牙的颊侧骨皮质去除,向其中充填聚甲基丙烯酸甲酯和对照材料,最后分层缝合。在这个模型中,研究者展示了在临界缺损中较为直观地评价骨再生的方法,这个下颌骨缺损模型可以按照同一标准进行重复,这在具有多个实验组的研究中至关重要。但是这个模型也是有明显的缺陷,模型中只有皮质骨被去除,因此不能反映临床中牙槽骨缺损往往是致密骨和松质骨同时缺损这一特征;此外,下颌下切口入路会完全剥离覆盖的肌肉,这会使外在肌肉的整体力量变化,从而影响模型的功能性。 2.4.2 颅顶骨临界骨缺损模型 受颅骨缺损研究的影响,许多研究者也在动物颅顶缺损中尝试进行引导骨再生的相关研究。一些研究者在大鼠颅顶制备缺损后,在颅顶缺损外部边缘和缺损内硬脑膜处分别覆盖不可吸收的PTFE膜,用以隔离软组织,而二者间的缺损区域不充填或充填自体骨,均能够在术后3周观察到大量的新骨形成[34]。而在一些应用到大鼠颅顶骨缺损研究中,研究者只覆盖外部边缘,不隔离内部硬脑膜,同样能观察到类似的结果,而那些没有覆盖膜的治疗组中,缺损被软组织充填[35]。这些研究结果证明了引导骨再生技术在颅骨缺损中的再生潜力,也为动物模型的建立提供了新的选择。总结文献报道发现,成年Sprague-Dawley大鼠的常用临界缺损尺寸为4-8 mm[36];Wistar大鼠中常用的临界尺寸为5 mm[37],也有研究中使用7 mm作为临界尺寸[38];新西兰大白兔的常用临界尺寸为5,6,8 和9 mm[39-42],最高可达12-15 mm[43]。何通文等[44]在构建兔颅顶骨临界骨缺损的研究中,通过比较不同直径缺损在 12 周观察期内的影像和组织学差别,发现直径≥5mm的兔颅顶骨缺损不能自行愈合。CHEN等[41]在研究颗粒状骨移植材料和胶原水凝胶对骨再生的影响中,建立起了一种标准化的模型。不同于较常见的直接在兔硬脑膜上充填,他们将PTFE膜不仅放置在模型顶部以覆盖缺损,而且覆盖在硬脑膜上,使二者之间创造一个孤立的空间,可以观察到愈合过程。在这个模型中,因为完全排除了包括硬脑膜在内软组织的影响,周围骨组织和骨髓成为了血管生成和成骨过程中,唯一能影响修复和愈合的自身因素。总体来看,这种颅顶骨缺损模型在手术过程上是有着明显的优势。因为切口入路相对简单,手术视野也是十分清晰,手术可控性强、重复性好,方便建立标准化的模型,从而有较强的可比性;同时,因为术区未涉及口内,术后对饮食影响较小;模型缺陷主要体现在无法模拟出在口内肌肉和复杂菌群共同作用下骨再生的情况,特别是当研究区涉及到咀嚼力时。 2.4.3 其他部位的颅颌面临界骨缺损模型 除前述常见的模型外,不少学者也在其他部位应用了临界骨缺损模型进行引导骨再生相关研究。MATZEN等[45]在大鼠腭裂周围的鼻和腭部缺损处覆盖了PTFE膜,7个月后观察到腭中缝完全的骨再生。在范围覆盖矢状缝的大鼠颅骨切除术后的引导骨再生治疗中,也观察到了类似的结果[46]。引导骨再生治疗后,不仅可以观察到大面积骨缺损的愈合,也可以在能使颅骨持续生长的矢状缝中观察到骨再生。目前的文献报道表明,通过在临界缺损模型中应用引导骨再生技术,可以在颅颌面部骨的多种类型骨缺损中实现骨再生。 2.5 临界骨缺损模型在特殊条件下的引导骨再生中的应用 2.5.1 伴有糖尿病的引导骨再生研究 一般来讲,此类研究中,首先需要建立能模拟糖尿病状态的动物模型,然后再进行骨缺损模型的建立。目前文献报道中见到的最常使用的是1型糖尿病实验动物模型,尽管2型糖尿病是人类中最常见的糖尿病类型。1型糖尿病实验动物模型是通过化学诱导动物体内产生糖尿病,多数研究人员选择此类模型主要是考虑到是其成本低,方便实施;另一方面,从结果上来看,选择1型糖尿病实验动物模型也可以大体满足研究需求,因为如果不进行干预治疗,2种类型的糖尿病都会对骨代谢和伤口愈合产生严重的负面影响。当然,由于动物之间以及动物与人之间的生物学反应各不相同,每种动物模型也仅模仿人类情况的某些特征,因此研究者必须谨慎解读实验结果。总的来说,在实验动物中诱发1型糖尿病大多是通过腹腔内注射链脲佐菌素(50-100 mg/kg)来实现的[47-48]。在研究糖尿病状况对引导骨再生影响的研究中,有研究者通过向大鼠腹腔一次性注射溶于柠檬酸盐缓冲液(0.01 mol/L,pH 4.3)的链脲佐菌素(60或65 mg/kg)来诱发糖尿病[49-50]。而在小鼠中,有研究者通过腹膜内给予低剂量链脲佐菌素(40 mg/kg,1次/d,连续5 d)成功诱发了糖尿病[51]。这种方法被认为是对大剂量链脲佐菌素诱导模型的一种改进,因为它可能模拟了与破坏胰腺细胞有关的细胞事件,从而导致了与人类1型糖尿病相似的糖尿病。也有部分研究是利用四氧嘧啶在实验动物体内诱发糖尿病。为了观察在使用胰岛素治疗糖尿病情况下,种植体骨结合过程中发生的组织学变化,研究者通过在大鼠静脉内注射四氧嘧啶(42 mg/kg)建立了1型糖尿病模型[52]。兔糖尿病模型的建立亦可以通过在耳缘静脉注射80 mg/kg四氧嘧啶,再在48 h后注射120 mg/kg来实现[53]。但是,需要注意的是,这种方法会导致持续的高血糖症,即使每天干预使用人胰岛素也常常难以控制。在一些研究中,研究者先使用链脲佐菌素诱发大鼠的糖尿病,然后在大鼠颅顶骨建立临界骨缺损模型,来评估糖尿病大鼠在进行引导骨再生后胰岛素对骨再生的影响[54],结果发现,即使在不控制胰岛素的情况下,大鼠在经引导骨再生技术处理后60 d,颅顶骨缺损区仍然实现了骨再生[36]。另外一方面,糖尿病状态与缺损区的愈合是有关的,在不控制糖尿病的情况下,引导骨再生的早期骨愈合会受到影响,通过系统使用胰岛素改善代谢控制,可以促进成骨。同时,糖尿病未控制的动物在引导骨再生愈合过程中表现出趋化因子和炎症介质基因的表达下调。 2.5.2 放射治疗后的引导骨再生研究 放射治疗会抑制骨代谢,减少血管生成,影响骨改建和细胞增殖能力。此外,术前放射治疗会完全抑制骨愈合,导致缺损区内充满结缔组织[55]。在已知的骨再生研究模型中,放射治疗方案比较多样化,各模型间差异较大。文献报道了多种离子源类型(线性加速器,钴60,铯137等),依据鼠兔模型不同,照射总剂量范围为1-55 Gy,分次剂量2.9-15 Gy,次数为1-15次;照射时机则为手术前1 d至6个月,手术后3 d至10周;疗程则为10 d至12周不等[56-58]。目前,放射治疗后对引导骨再生的确切影响尚不十分清楚,关于放射治疗后的引导骨再生研究相比其他类型仍然较少。JEGOUX等[59]在兔的左侧下颌骨行部分切除术后,在第1磨牙区建立了一个11 mm × 9 mm× 7 mm水平全层皮质骨缺损临界模型,用以羟基磷灰石和β-磷酸三钙为主要成分的骨移植材料以及胶原膜对实验组进行引导骨再生,试图增加牙槽嵴高度。术后在外部进行为期4周的分馏辐射治疗,然后再将自体骨髓注射到拟修复区内,在第16周处死对样本进行分析。组织学分析显示所有部位均出现了骨定植,片状骨与骨替代物直接接触,无纤维组织进入;而且,这项结果表明自体骨髓移植物在这些特定的缺陷条件下可能具有很强的骨诱导潜力。但是,该研究中建立的模型是处于一个比较稳定的环境中,稳定的环境有利于骨祖细胞的聚集、增殖和分化以及成骨细胞的活性表达,这与临床实际还是有一定差距,因而需要进一步的动物研究和临床前研究,以提供更多有关放射对引导骨再生影响的数据。 3 讨论 Discussion 以组织工程技术为基础的生物材料在引导骨再生技术上的应用有着巨大潜力。随着新的组织工程材料不断涌现,许多研究者尝试将其应用于引导骨再生技术的优化上,因而在许多临床前模型中进行了评估。临界骨缺损模型具有操作性和可控性强的优势,可以用来初步模拟临床实际情况并评估新材料在引导骨再生技术中的应用价值。大型灵长类动物与人类的解剖生理特性最为接近,应当是实验动物种类的最佳选择,但是考虑到经济成本,可操作性以及伦理规范等因素,这类大型动物应当谨慎使用。小型实验动物,如小鼠、大鼠和兔等,已经能够在组织学水平上评估材料生物活性成分,其结果具有足够的统计学意义,是研究初期较好的选择。考虑到解剖生理特征的相关性,应用于口腔骨再生的研究,应当选择实验动物中与人类颌骨特征相似的部位,小型动物的颅颌面部是比较适宜的选择。在研究中常见的建模部位主要集中在颌骨和颅顶骨。在颌骨模型中,除了涉及到上颌窦等特殊解剖结构的情况下,大多数研究均是在下颌骨中进行的。这可能是因为,下颌骨主要由皮质骨构成,这与人类相似,而上颌骨更适合于观察骨小梁愈合;另外一方面,下颌骨在可操作和可重复性上可能有一定优势。在颅顶骨模型中,因为建模相对简单,视野清晰,可重复性好,以及方便研究者建立起标准化的研究模型,颅顶骨临界骨缺损模型越来越受到青睐,特别是在探索性研究中。通过选择合理的建模方法,小型动物颌面部临界骨缺损模型也可以被应用到一些特殊情况的研究中,比如患有糖尿病和经放疗后的骨再生研究。此类研究中可能影响骨再生结果的因素主要是[36]:屏障膜塌陷进入缺损区,膜的生物相容性和适应性,以及使用的生物可吸收材料的类型。因而,在实验设计和结果分析时,除了动物模型本身,也需要慎重考虑生物材料本身对结果的影响。但需要注意的是,尽管可以通过这类模型直观地观察到骨再生的生理变化,小动物的骨代谢与人的骨骼有很大的不同,不应当将这些结果直接推断到人类身上。研究者应当根据自己的研究目的和实际条件选用适宜的研究模型。"

| [1] CHIAPASCO M, CASENTINI P. Horizontal bone‐augmentation procedures in implant dentistry: prosthetically guided regeneration. Periodontol 2000. 2018;77(1):213-240. [2] NAENNI N, SCHNEIDER D, JUNG RE, et al. Randomized clinical study assessing two membranes for guided bone regeneration of peri‐implant bone defects: clinical and histological outcomes at 6 months.Clin Oral Implants Res. 2017;28(10):1309-1317. [3] SØREN J, CATON JG, ALBANDAR JM, et al. Periodontal manifestations of systemic diseases and developmental and acquired conditions: Consensus report of workgroup 3 of the 2017 World Workshop on the Classification of Periodontal and Peri-Implant Diseases and Conditions. J Periodontol. 2018;89 Suppl 1:S237-S248. [4] ELGALI I, OMAR O, DAHLIN C, et al. Guided bone regeneration: materials and biological mechanisms revisited. Eur J Oral Sci. 2017;125(5):315-337. [5] 周敏月,聂敏海,陈潇,等.组织工程修复牙槽骨临界骨缺损的研究进展[J].西南军医,2020,22(1):51-54. [6] WATAHA JC. Effect of cell line on in vitro metal ion cytotoxicity. Dent Mater. 1994;10(3):156-161. [7] FREITAS NR, GUERRINI LB, ESPER LA, et al. Evaluation of photobiomodulation therapy associated with guided bone regeneration in critical size defects. In vivo study. J Appl Oral Sci. 2018;26:e20170244. [8] HELGELAND E, SHANBHAG S, PEDERSEN TO,et al. Scaffold-Based Temporomandibular Joint Tissue Regeneration in Experimental Animal Models: A Systematic Review. Tissue Eng Part B Rev. 2018;24(4):300-316. [9] 严霞,张亚楠,孟增东.构建骨缺损植入材料非人灵长类动物模型的研究与进展[J].中国组织工程研究,2018,22(31):5021-5026. [10] LIEBSCHNER MA. Biomechanical considerations of animal models used in tissue engineering of bone. Biomaterials. 2004;25(9):1697-1714. [11] GOTTLOW J, NYMAN S, KARRING T, et al. New attachment formation as the result of controlled tissue regeneration. J Clin Periodontol. 1984;11(8): 494-503. [12] AVANTIKA N, SAKSHI G, BALJEET S, et al. Bone Augmentation Materials and Membranes Used In Implant Therapies with Guided Bone Regeneration Technique. Baba Farid University Dental Journal. 2017;7(1):76-81. [13] 张璇,李云朋,张雪健,等.预成型钛网联合生物膜在美学区引导骨组织的再生[J].中国组织工程研究,2020,24(26):4112-4117. [14] KHOJASTEH A, KHEIRI L, MOTAMEDIAN SR, et al. Guided Bone Regeneration for the Reconstruction of Alveolar Bone Defects.Ann Maxillofac Surg. 2017; 7(2):263-277. [15] SCHMITZ JP, HOLLINGER JO. The Critical Size Defect as an Experimental Model for Craniomandibulofacial Nonunions. Clin Orthop Relat Res. 1986; (205):299-308. [16] WANG J, GLIMCHER MJ. Characterization of Matrix-Induced Osteogenesis in Rat Calvarial Bone Defects: I. Differences in the Cellular Response to Demineralized Bone Matrix Implanted in Calvarial Defects and in Subcutaneous Sites. Calcif Tissue Int. 1999;65(2):156-165. [17] SHAH SR, YOUNG SK, GOLDMAN JL, et al. A composite critical-size rabbit mandibular defect for evaluation of craniofacial tissue regeneration. Nature Protocols. 2016;11(10):1989-2009. [18] SUSIN C, LEE J, FIORINI T, et al. Screening of candidate biomaterials for alveolar augmentation using a critical-size rat calvaria defect model. J Clin Periodontol. 2018;45(7):884-893. [19] AALAMI O, NACAMULI RP, LENTON KA, et al. Applications of a mouse model of calvarial healing: Differences in regenerative abilities of juveniles and adults. Plast Reconstr Surg. 2004;114(3):713-720. [20] SANZHERRERA JA, REINAROMO E. Cell-Biomaterial Mechanical Interaction in the Framework of Tissue Engineering: Insights, Computational Modeling and Perspectives. Int J Mol Sci. 2011;12(11):8217-8244. [21] WILLIAMSDAVID F. A Paradigm for the Evaluation of Tissue-Engineering Biomaterials and Templates. Tissue Eng Part C Methods. 2017;23(12): 926-937. [22] BIGHAMSADEGH A, ORYAN A. Selection of animal models for pre-clinical strategies in evaluating the fracture healing, bone graft substitutes and bone tissue regeneration and engineering. Connect Tissue Res. 2015;56(3): 175-194. [23] ANDERSEN ML, WINTER LMF. Animal models in biological and biomedical research - experimental and ethical concerns. An Acad Bras Cienc. 2019; 91(suppl 1):e20170238. [24] AKAR B, TATARA A M, SUTRADHAR A, et al. Large Animal Models of an In Vivo Bioreactor for Engineering Vascularized Bone. Tissue Eng Part B Rev. 2018;24(4):317-325. [25] STUBINGER S, DARD M. The Rabbit as Experimental Model for Research in Implant Dentistry and Related Tissue Regeneration. J Invest Surg. 2013; 26(5):266-282. [26] STRUILLOU X, BOUTIGNY H, SOUEIDAN A, et al.Experimental animal models in periodontology: a review. Open Dent J. 2010;4:37-47. [27] DAHLIN C, LINDE A, GOTTLOW J, et al. Healing of bone defects by guided tissue regeneration. Plast Reconstr Surg. 1988;81(5):672-676. [28] HAN J,MA B,LIU H, et al. Hydroxyapatite nanowires modified polylactic acid membrane plays barrier/osteoinduction dual roles and promotes bone regeneration in a rat mandible defect model. J Biomed Mater Res A. 2018;106(12):3099-3110. [29] MILLER MQ, MCCOLL LF, ARUL MR, et al. Assessment of Hedgehog Signaling Pathway Activation for Craniofacial Bone Regeneration in a Critical-Sized Rat Mandibular Defect. JAMA Facial Plastic Surgery. 2019;21(2):110-117. [30] LIU G, GUO Y, ZHANG L, et al. A standardized rat burr hole defect model to study maxillofacial bone regeneration. Acta Biomater. 2019;86:450-464. [31] CAMPILLO VE, LANGONNET S, PIERREFEU A, et al. Anatomic and histological study of the rabbit mandible as an experimental model for wound healing and surgical therapies. Lab Anim. 2014;48(4):273-277. [32] SHAH SR, YOUNG SK, GOLDMAN JL, et al. A composite critical-size rabbit mandibular defect for evaluation of craniofacial tissue regeneration. Nat Protoc. 2016;11(10):1989-2009. [33] LYE KW, TIDEMAN H, WOLKE J, et al. Biocompatibility and bone formation with porous modified PMMA in normal and irradiated mandibular tissue. Clin Oral Implants Res. 2013;24 Suppl A100:100-109. [34] Dahlin C, Alberius P, Linde A, et al. Osteopromotion for cranioplasty: An experimental study in rats using a membrane technique. J Neurosurg. 1991;74(3):487-491. [35] Fadel RA, Samarani R, Chakar C, et al. Guided bone regeneration in calvarial critical size bony defect using a double-layer resorbable collagen membrane covering a xenograft: a histological and histomorphometric study in rats. Oral Maxillofac Surg. 2018;22(2):203-213. [36] Donos N, Dereka X E, Mardas N, et al. Experimental models for guided bone regeneration in healthy and medically compromised conditions. Periodontol 2000. 2015;68(1):99-121. [37] Aroni MA, De Oliveira GJ, Spolidorio LC, et al. Loading deproteinized bovine bone with strontium enhances bone regeneration in rat calvarial critical size defects. Clin Oral Investig. 2019;23(4):1605-1614. [38] RAFTERY RM, MENCIACASTANO I, SPERGER S, et al. Delivery of the improved BMP-2-Advanced plasmid DNA within a gene-activated scaffold accelerates mesenchymal stem cell osteogenesis and critical size defect repair. J Control Release. 2018;283:20-31. [39] BROGGINI N, HOFSTETTER W, HUNZIKER EB, et al.The Influence of PRP on Early Bone Formation in Membrane Protected Defects. A Histological and Histomorphometric Study in the Rabbit Calvaria.Clin Implant Dent Relat Res. 2011;13(1):1-12. [40] SALAMANCA E, HSU CC, HUANG HM, et al. Bone regeneration using a porcine bone substitute collagen composite in vitro and in vivo.Sci Rep. 2018;8(1):984. [41] CHEN C, TIEN H, CHUANG C, et al. A comparison of the bone regeneration and soft‐tissue‐formation capabilities of various injectable‐grafting materials in a rabbit calvarial defect model. J Biomed Mater Res B Appl Biomater. 2019;107(3):529-544. [42] 宫玮玉,刘绍清,董艳梅,等.纳米生物活性玻璃促进兔颅骨临界骨缺损修复[J].北京大学学报(医学版),2018,50(1):42-48. [43] PELEGRINE AA, ALOISE AC, ZIMMERMANN A, et al. Repair of critical‐size bone defects using bone marrow stromal cells: a histomorphometric study in rabbit calvaria. Part I: Use of fresh bone marrow or bone marrow mononuclear fraction. Clin Oral Implants Res. 2014;25(5):567-572. [44] 何通文,徐庚池,韩耀辉,等.构建兔颅顶骨临界骨缺损模型:确立颅顶临界骨缺损的参考值[J].中国组织工程研究,2014,18(18):2789-2794. [45] MATZEN M, KOSTOPOULOS L, KARRING T, et al. Healing of Osseous Submucous Cleft Palates with Guided Bone Regeneration.Scand J Plast Reconstr Surg Hand Surg. 1996;30(3):161-167. [46] MARDAS N, KOSTOPOULOS L, KARRING T, et al. Bone and suture regeneration in calvarial defects by e-PTFE-membranes and demineralized bone matrix and the impact on calvarial growth: An experimental study in the rat.J Craniofac Surg. 2002;13(3):453-462; discussion 462-464. [47] 王乐旬,吴惠娟,张盛昔,等.不同建模方法对链脲霉素诱导1型糖尿病成模率的影响[J].广东药科大学学报,2019,35(6):763-767. [48] MJ DB, HUYNH N, DEO M, et al. Defining the Progression of Diabetic Cardiomyopathy in a Mouse Model of Type 1 Diabetes.Front Physiol. 2020; 11:124. [49] RETZEPI M, LEWIS MP, DONOS N, et al. Effect of diabetes and metabolic control on de novo bone formation following guided bone regeneration.Clin Oral Implants Res. 2010;21(1):71-79. [50] CHENG K, LIN Z, CHENG Y, et al. Wound Healing in Streptozotocin-Induced Diabetic Rats Using Atmospheric-Pressure Argon Plasma Jet.Sci Rep. 2018; 8(1):12214. [51] XIAO L, UENO D, CATROS S, et al. Fibroblast Growth Factor-2 Isoform (Low Molecular Weight/18 kDa) Overexpression in Preosteoblast Cells Promotes Bone Regeneration in Critical Size Calvarial Defects in Male Mice. Endocrinology. 2014;155(3):965-974. [52] SIQUEIRA JT, CAVALHERMACHADO SC, ARANACHAVEZ VE, et al. Bone Formation Around Titanium Implants in the Rat Tibia: Role of Insulin.Implant Dent. 2003;12(3):242-251. [53] 林枭,李豫皖,吴向东,等.探讨糖尿病对兔膝前交叉韧带重建术后骨隧道的影响[J].重庆医科大学学报,2019,44(9):1118-1126. [54] RETZEPI M, CALCIOLARI E, WALL I, et al. The effect of experimental diabetes and glycaemic control on guided bone regeneration: histology and gene expression analyses. Clin Oral Implants Res. 2018;29(2):139-154. [55] AN H, LEE J, OH SE, et al. Adjunctive hyperbaric oxygen therapy for irradiated rat calvarial defects. J Periodontal Implant Sci. 2019;49(1):2-13. [56] JEGOUX F, MALARD O, GOYENVALLE E, et al. Radiation effects on bone healing and reconstruction: interpretation of the literature. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2010;109(2):173-184. [57] JUNG H, LEE J, LEE S, et al. Development of an experimental model for radiation-induced inhibition of cranial bone regeneration. Maxillofac Plast Reconstr Surg. 2018;40(1):34. [58] PARK K, KIM C, PARK W, et al. Bone Regeneration Effect of Hyperbaric Oxygen Therapy Duration on Calvarial Defects in Irradiated Rats.Biomed Res Int. 2019;2019:9051713. [59] JEGOUX F, AGUADO E, COGNET R, et al. Alveolar ridge augmentation in irradiated rabbit mandibles. J Biomed Mater Res A. 2010;93(4):1519-1526. |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Hu Kai, Qiao Xiaohong, Zhang Yonghong, Wang Dong, Qin Sihe. Treatment of displaced intra-articular calcaneal fractures with cannulated screws and plates: a meta-analysis of 15 randomized controlled trials [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1465-1470. |
| [3] | Huang Dengcheng, Wang Zhike, Cao Xuewei. Comparison of the short-term efficacy of extracorporeal shock wave therapy for middle-aged and elderly knee osteoarthritis: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1471-1476. |
| [4] | Xu Feng, Kang Hui, Wei Tanjun, Xi Jintao. Biomechanical analysis of different fixation methods of pedicle screws for thoracolumbar fracture [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1313-1317. |
| [5] | Jiang Yong, Luo Yi, Ding Yongli, Zhou Yong, Min Li, Tang Fan, Zhang Wenli, Duan Hong, Tu Chongqi. Von Mises stress on the influence of pelvic stability by precise sacral resection and clinical validation [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1318-1323. |
| [6] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [7] | Zhang Yu, Tian Shaoqi, Zeng Guobo, Hu Chuan. Risk factors for myocardial infarction following primary total joint arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1340-1345. |
| [8] | Wei Wei, Li Jian, Huang Linhai, Lan Mindong, Lu Xianwei, Huang Shaodong. Factors affecting fall fear in the first movement of elderly patients after total knee or hip arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1351-1355. |
| [9] | Wang Jinjun, Deng Zengfa, Liu Kang, He Zhiyong, Yu Xinping, Liang Jianji, Li Chen, Guo Zhouyang. Hemostatic effect and safety of intravenous drip of tranexamic acid combined with topical application of cocktail containing tranexamic acid in total knee arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1356-1361. |
| [10] | Xiao Guoqing, Liu Xuanze, Yan Yuhao, Zhong Xihong. Influencing factors of knee flexion limitation after total knee arthroplasty with posterior stabilized prostheses [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1362-1367. |
| [11] | Huang Zexiao, Yang Mei, Lin Shiwei, He Heyu. Correlation between the level of serum n-3 polyunsaturated fatty acids and quadriceps weakness in the early stage after total knee arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1375-1380. |
| [12] | Zhang Chong, Liu Zhiang, Yao Shuaihui, Gao Junsheng, Jiang Yan, Zhang Lu. Safety and effectiveness of topical application of tranexamic acid to reduce drainage of elderly femoral neck fractures after total hip arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1381-1386. |
| [13] | Wang Haiying, Lü Bing, Li Hui, Wang Shunyi. Posterior lumbar interbody fusion for degenerative lumbar spondylolisthesis: prediction of functional prognosis of patients based on spinopelvic parameters [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1393-1397. |
| [14] | Lü Zhen, Bai Jinzhu. A prospective study on the application of staged lumbar motion chain rehabilitation based on McKenzie’s technique after lumbar percutaneous transforaminal endoscopic discectomy [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1398-1403. |
| [15] | Chen Xinmin, Li Wenbiao, Xiong Kaikai, Xiong Xiaoyan, Zheng Liqin, Li Musheng, Zheng Yongze, Lin Ziling. Type A3.3 femoral intertrochanteric fracture with augmented proximal femoral nail anti-rotation in the elderly: finite element analysis of the optimal amount of bone cement [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1404-1409. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||