Chinese Journal of Tissue Engineering Research ›› 2019, Vol. 23 ›› Issue (20): 3248-3254.doi: 10.3969/j.issn.2095-4344.1052
Previous Articles Next Articles
Biological therapy in rotator cuff injury
Liu Yan, Yu Xi, He Hongchen, He Chengqi, He Jing
- West China Hospital, Sichuan University, Chengdu 610041, Sichuan Province, China
-
Online:2019-07-18Published:2019-07-18 -
Contact:He Jing, MD, Associate professor, West China Hospital, Sichuan University, Chengdu 610041, Sichuan Province, China -
About author:Liu Yan, Master candidate, Physician, West China Hospital, Sichuan University, Chengdu 610041, Sichuan Province, China -
Supported by:the Resident Research Foundation of West China Hospital, Sichuan University, No. YB0000005 (to LY)
CLC Number:
Cite this article
Liu Yan, Yu Xi, He Hongchen, He Chengqi, He Jing. Biological therapy in rotator cuff injury[J]. Chinese Journal of Tissue Engineering Research, 2019, 23(20): 3248-3254.
share this article
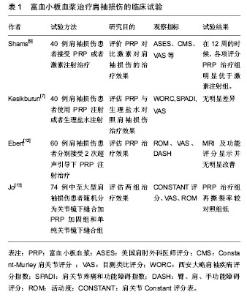
2.1 富血小板血浆制品 富含血小板的血浆是研究最多的用于肩袖撕裂和修复的佐剂之一,首先在20世纪90年代用于整形和口腔颌面部手术,富血小板血浆的吸引力在于生长因子的合并或浓缩,包括转化生长因子β、成纤维细胞生长因子、血小板衍生生长因子以及其他因子参与修复过程[5]。Boswell等[6]概述了许多部分,其中包括因富血小板血浆获益的细胞和化学信号,他们认为富血小板血浆是一系列既是分解代谢/合成代谢又是亲/抗炎的因素,作者还强调,由于这种复杂性,难以在每个患者和公司的产品中精确的复制。其中一个关键的区别就是富血小板血浆的细胞组成,因为增加的血小板浓度与合成代谢信号相关,而增加的白细胞浓度与分解代谢信号相关。 富血小板血浆在肩袖撕裂和修复的作用是刺激腱-骨界面的愈合并减轻疼痛、炎症。在非手术病例中,富血小板血浆已被用作肩峰下撞击和部分撕裂的类固醇替代治疗,特别是高水平运动员。Kesikburun等[7]进行了一项随机对照试验,对40例患有肩袖肌腱病或部分撕裂的患者进行了富血小板血浆或安慰剂注射,随后进行了康复计划,在任何时间点至1年的随访中,疼痛或功能结果评分没有差异。Filardo等[8]对各种肌腱病进行了Meta分析,并纳入了32项关于肩袖病理学的研究,研究结果再次表明富血小板血浆在肩袖肌腱病变和撕裂的非手术应用中,单次和多次注射方案治疗后效果没有差异。 在过去的3年中,已有大量有关富血小板血浆在肩袖修复中作用的文献,针对肩袖病变的富血小板血浆注射治疗正在增加。在非手术治疗方面,Shams等[9]进行了一项随机对照试验,比较皮质类固醇与富血小板血浆注射治疗症状性部分肩袖撕裂的效果。两组在所有功能评分上均有显著改善,但富血小板血浆组在12周时表现出了目测类比评分、ASES、SST和Constant-Murley评分的明显改善,尽管在6个月后无显著差异。治疗组在最终随访期间均未观察到肌腱病变程度或撕裂等级的显著变化。另外的研究还表明,含白细胞较少的富血小板血浆具有更好的合成代谢特征,刺激正常胶原基质并抑制引起炎症和基质降解的细胞因子。因此,含白细胞较少的富血小板血浆在将来的肩袖修复中可能是更优的选择,并且应该是进一步研究的焦点。Chahal等[10]将5项研究汇总到其结果中,而富血小板血浆治疗组的重复撕裂风险比为0.77 [95%CI 0.48-1.23],患者评价的结果包括CONSTANT,简单肩关节试验(SST),单一评估数字评估(SANE)和美国肩肘外科医师(ASES)评分在两组间没有差异。对11项研究更大的Meta分析发现了类似的结果。总体而言,在使用和未使用富血小板血浆的试验组之间,再撕裂率和患者结果没有差异。Warth等[11]在小组分析中发现,当撕裂大于3 cm时,富血小板血浆治疗组在双排缝合重建手术中显示再撕裂率显著降低(25.9%对比57.1%,P=0.046)。作者发现,这些研究中的大部分只是为了检测结果评分的差异,这可能导致了治疗组之间没有差异的发现。富血小板血浆可以直接注射,但通常可通过纤维蛋白、凝血酶或胶原作为基质。纤维蛋白作为基质传递系统的研究结果表明了较低的肩袖再撕裂率和有轻微的改善,另外2个随机对照试验表明加入了富血小板血浆治疗组再次撕裂的风险提高。越来越多的含较少白细胞富血小板血浆的研究表明,与多次研究中的常规富血小板血浆和其他对照相比,其再次撕裂率更低。 随机对照试验已广泛研究富血小板血浆的使用。其中一个有趣的方式是在术后即刻使用富血小板血浆,2项不同的随机对照试验分析术后7 d和14 d的富血小板血浆使用情况。这2项研究都没有设盲,也没有显示富血小板血浆对功能结果或肌腱完整性的显著影响。Ebert等[12]在调整基线分数和性别时,富血小板血浆治疗患者的外展强度有小幅增加,提高了3.3倍和0.9倍,但在3.5年后的随访结果也表明,富血小板血浆治疗似乎对功能或肌腱完整性的中期疗效没有作用。Jo等[13]是最近唯一证明富血小板血浆对重复撕裂率或功能改善有差异的试验,关键是他们的研究都集中在较大的肩袖撕裂上面。一个普遍的发现是富血小板血浆注射改善了手术后疼痛和前30 d疼痛药物的使用。这2项研究都表明,疼痛的减少可能会带来更好的康复潜力,但是鉴于一些医生在手术后6周才开始全面动员患者康复,这对患者的康复治疗会造成影响。鉴于阿片类药物的广泛使用,富血小板血浆在减轻疼痛方面的作用具有一定的价值,但必须进行成本分析和进一步研究,以评估富血小板血浆对麻醉药使用的影响。Cai等[14]在他们的分析中纳入了5项RCT的研究,虽然他们也得出结论认为富血小板血浆对临床结果没有影响,但亚组分析显示富血小板血浆降低了中小型肩袖损伤的再撕裂率,这与Warth等[11]研究结果相反。Saltzman等[15]对7项不同的Meta分析进行了系统评价,提供了3 193例患者,随访12-31个月。总体而言,他们的研究结果在最终随访期间功能评价(ASES,UCLA,Constant和SST评分)或修复完整性方面没有临床益处。有趣的是,这一广泛分析的结果显示,固体富血小板血浆与液体富血小板血浆制剂相比较有改善的结果。他们也支持Cai等[14]的发现,即富血小板血浆治疗对小至中型撕裂比大型撕裂的肩袖损伤再撕裂率较好。最后,研究组发现直接置于骨-肌腱界面的富血小板血浆比肌腱注射的富血小板血浆和双排与单排缝合修复结构的效果更好。富血小板血浆治疗肩袖损伤的临床试验见表1。"

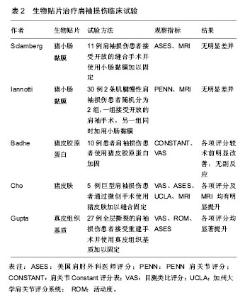
2.2 生物贴片 除富血小板血浆之外,细胞外基质或“贴片”是用于肩袖修复的主要佐剂,虽然富血小板血浆依靠细胞因子刺激肩袖撕裂的愈合,但细胞外基质提供了额外的机械强度,以增加组织中的负荷,使组织更坚硬。贴片为细胞生长提供了框架,并且最终可以证明其与自体肌腱类似的性质。最近,这类移植物已成为干预大规模肩袖撕裂(上囊重建)的焦点。此部分的重点将放在细胞外基质或补丁的使用上。 经典的细胞外基质分为两大类:异种移植和同种异体移植。异种移植物包括猪皮肤和黏膜下移植物。这些移植物在身体的其他部位已经取得了成功,但是被Sclamberg等[16]证明对于肩袖修复是不利的。在修复后仅6个月发现11个巨大肩袖损伤中的10个,功能评分没有改善(5例患者实际上评分更差)。另外2项关于猪黏膜下层移植的研究也有类似的结果,其中一项研究中15例患者中只有4例治愈了肩袖撕裂,另一项研究中10例患者中的6例得到了治愈。Iannotti等[17]报道接受移植的患者疼痛加重,Walton等[18]报道了4例需要再次手术治疗的严重副反应的患者。研究人员推测强烈的炎症反应是由于DNA仍然存在于这些移植物中。由于存在较少的DNA,猪皮肤移植物比黏膜下移植物更成功。Badhe 等[19]在大面积肩袖撕裂中使用了贴片,并且在3.5年时,10例患者中的8例具有完整的修复并且CONSTANT评分从41提高到62。类似地,Cho等[20]在最近的微型开放技术使用移植物进行缝合,在平均20.6个月的随访中,功能评分显著改善,5例患者中的4例在术后8个月完好修复。Gupta等[21]可能是使用真皮异种移植物治疗的最成功的试验,其在运动、力量和ASES评分方面显著改善(62.7至91.8;P=0.000 7),在2年的随访中,21例患者中有16例完整修复,5例(22%)有部分撕裂,只有1例患者(5%)由于跌倒再次手术。 同种异体移植物,特别是皮肤同种异体移植物,在肩袖撕裂修复方面早有成功。Bond等[22]使用GraftJacket(Wright Medical,Memphis,TN)在UCLA,Constant和SST评分上有显著改善,16例患者中有13例在平均26个月时移植物完全结合。Wong等[23]发表了类似的关于功能改善的发现,尽管他们没有在研究中完整的讨论修复。即使在大型的撕裂的中期随访中,一系列病例也证明了功能评分、力量和运动范围的改善,其中76%的病例完全修复。Barber等[24]通过修复2个肌腱的随机对照试验还提供了令人信服的证据。ASES和Constant评分在皮肤同种异体移植组中均有统计学上的增加,但评分的临床差异尚不清楚。此外,使用贴片组85%的患者完全修复,而对照组为40%。这是关于真皮异体移植物的少数LEVEL1研究之一。皮肤同种异体移植仍然是增强肩袖修复的重要工具。 近年来,研究继续试验生物贴片在增强修复中的有效性。在基础科学研究方面,Smith等[25]试图分析市售生物支架的机械性能,包括异种移植物、同种异体移植物和合成支架,所有测试的支架都不符合冈上肌肌腱的力学性能,作者指出可能是因为许多这些产品并没有考虑专门为肩袖设计。Smith等[25]建议未来的移植物应该旨在将合成移植物的宏观机械性能与生物支架的微观机械性能相结合。另一项研究通过第2次关节镜手术来活体检测使用牛胶原基质修复肩袖的部位,通过在不同时间点获得7个标本,作者能够勾勒出移植物结合的时间表。存在成纤维细胞的宿主细胞浸润在5周时在最早的样品中被看到,在3个月时注意到增加的组织,并且最终在6个月时完全并入单独的宿主组织。Beitzel等[26]试图评估移植物的类型是否影响间充质细胞在修复中的反应。虽然在结构上更强壮,但与组织较少的猪胶原支架相比,皮肤同种异体移植物的复杂结构可阻碍肌腱细胞祖细胞的浸润。该研究的后续研究观察了细胞外基质的生物化学组成在肩袖修复中的影响,他们发现Ⅰ型和Ⅲ型胶原增加的支架显著增加了骨髓间充质干细胞分化成骨和肌腱的潜力。未来的研究应该继续发现或定义理想的移植物的机械和生物诱导性质。较小的病例系列已证明在增强大型肩袖撕裂方面有良好的效果。就初级修复而言,Consigliere等[27]发现在使用皮肤细胞外基质修复大型和大面积肩袖损伤后7个月的平均随访中,Constant(53-75)和Oxford评分(30-47)显著改善,疼痛从7分降至0.6分。另外两个系列案例研究了贴片在再次修复中的作用。Petri等[28]的研究中13例患者中的12例增加了无细胞真皮异体移植物,其中只有1例患者在2个月时有再次撕裂(患者先前有4次修复),而总体ASES评分没有显示出统计学显著改善,功能评分有显著改善(P < 0.05),中位患者满意度为9/10。作者的结论是,无细胞皮肤贴片在大面积肩袖修复中是安全和有效的。在对24例再次肩袖损伤患者接受无细胞皮肤同种异体移植的平均随访50个月单独回顾中,可用于随访成像的16例患者中的10例(63%)具有修复失败的证据。总体而言,根据ASES和SANE评分,24%的患者获得了良好的结果,13%的患者获益良好,21%获得了良好的结果,42%的患者获得了良好的预后。Sears等[29]将其与没有增加修复的历史结果进行比较,发现皮肤修补物没有显著改善。最近的一项前瞻性双盲对照研究中,比较了20例肩袖损伤患者采用同种异体皮肤移植和15例未使用移植治疗患者的疗效,在24.9个月的平均随访中,增强组仅有10%的再次撕裂率,对照组为26%(P=0.048 3)。此外,与对照组相比,用同种异体皮肤移植治疗患者的ASES,SF-12和西安大略肩袖评分显著改善。 由于主要是小众人群和有限的Ⅰ级和Ⅱ级研究,通过系统评价和Meta分析试图更好地确定补片在肩袖修复中的作用。3篇回顾性文章重新强调了同种异体移植物用于大型肩袖修复的优势。Ferguson等[30]发现同种异体移植增强修复在最终随访中完好修复比为85%∶40%。作者还分析了聚丙烯贴剂的使用,发现这些优于对照和异种移植结果。Steinhaus等[31]汇集了24项至少进行了9个月的随访研究数据,他们发现平均而言,使用聚丙烯贴剂增强组的肩关节前屈度数提高了58.6°,外旋提高了16.6°和内旋提高了16.1°,ASES,UCLA,Constant,Penn和Oxford得分在统计学上显著提高。分析证实了异体移植物在功能结果方面的劣势。汇总的数据显示整体重新撕裂率为25%(增强组为34%,中间构造组为12%);重新撕裂率最高的是异种移植组(44%),以及最低的合成移植率(15%)。生物贴片治疗肩袖损伤临床试验,见表2。"


2.3 合成支架 由聚丙烯、涤纶甚至尼龙等各种材料组成的合成移植物或支架在再撕裂率方面取得了成功。合成材料通常在生物力学上有较强的强度并且不具有向量传播的理论风险。聚-L乳酸的变体在动物和人体研究中都取得了成功。一位外科医生的1个病例系列分析了在12个月和42个月时,连续18例大规模肩袖损伤患者修复的结果和修复完整性。Proctor等[32]发现18例患者中有15例在12个月时完好修复,18例中有14例在42个月时完全修复。此外,该队列的ASES评分在12个月时从25分提高到71分,在42个月时显著提高到70分。另一项利用聚碳酸酯聚氨酯贴片的研究显示,12个月时10例肩袖损伤患者完成90%的完整修复,SST,ASES和UCLA评分显著改善,无不良反应。即使在使用纯合成材料如聚酯(Dacron)的情况下,用合成支架重新强化的大面积的肩袖损伤可使疼痛减少,运动范围增加,并且患者随访的结果显著改善。这些研究缺乏对照组,但展现了合成移植物的前景。一项队列研究分析了仅用修复胶原贴片修补和用聚丙烯补片修补的治疗效果。3组共有152例患者,作者发现,所有3组患者在2个月和36个月时的目测类比评分和UCLA评分均有显著改善。在36个月时,聚丙烯组在肩关节前屈角度(140.68°比140.61°/174.71°)和强度(8.73/9.03/13.79 kg)有提高。在36个月时,聚丙烯组的再次撕裂率也明显降低(41%/51%/17%)。一些动物模型已经将这些合成支架与生物制剂如骨髓衍生的干细胞一起进行了比较,虽然胶原蛋白产生增加,但这并不转化为生物力学上更好的修复。正如Smith等[25]的生物力学研究所强调的那样。未来研究的重点应继续将合成移植物的生物力学强度与生物因素整合结合起来。 2.4 干细胞,细胞因子和生物制剂 肌腱修复是化学信号传导的复杂系统,依靠炎症和最终的组织重组,为了提高愈合率,科学家们寻找改变环境因素的办法以促进更可靠的肩袖愈合的方法。最广泛的方法之一是在修复部位应用间充质干细胞。动物研究已经支持骨髓衍生细胞可以渗入修复并增加修复强度。Gulotta等[33]在修复的机械结果方面没有发现显著的改善,但仍表明骨髓来源的细胞在修复部位具有生物活性。与单独使用支架进行修复相比,使用间充质干细胞增强生物支架已证明在加强修复方面非常有效。在人体研究方面,Hernigou等[34]进行了一项病例对照研究,比较了45例患者使用单排缝合肩袖并在修复部位使用来自骨髓穿刺的间充质干细胞,与45例单纯缝合的肩袖损伤患者相对照。干细胞组在6个月时100%完整修复,而对照组为67%,并且在10年时,该比例为87%对44%。最近的一项研究比较了35例使用脂肪间充质干细胞增殖修复患者与35例对照组患者相比较,虽然两组之间的功能结果没有差异,但对照组的重复撕裂率为28.5%,而干细胞组为14.3%。虽然干细胞在提高愈合率和改善预后方面显示出良好的前景,但需要更高水平的研究来加以证实。干细胞在愈合部位的作用是通过多种化学信号或细胞因子的复杂表达来实现的,这些因素可以在细胞外基质的各种制剂中变化,这就是为什么研究人员寻找特定细胞因子以增加肩袖修复治愈率。肌腱的合成包括肌腱、纤维软骨和骨骼,所以早期研究调查骨诱导因子作为佐剂的可能。两项使用羊的肩袖研究显示肩袖撕裂愈合率明显提高,但迄今为止,这些结果尚未在人体试验中复制。转化生长因子β是组织修复的炎症和愈合阶段中的关键信号;特别是转化生长因子β3在加速肩袖肌腱愈合方面显示出一定的应用前景,并在组织学和生物力学方面改善了修复,但在这一点上再次局限于动物模型。基质金属蛋白酶在降解胶原蛋白和其他细胞外基质蛋白中的作用一直是研究人员防止再撕裂的焦点。Gotoh等[35]发现基质金属蛋白酶3在肩袖再撕裂患者中有更高的水平表达。多西环素是一种常见的抗生素,由于其在基质金属蛋白酶抑制中的作用而被研究。在一项大鼠研究中,强力霉素已显示出预防再复发的希望。虽然基质金属蛋白酶3已被确定为与组织退化有关,但其他基质金属蛋白酶在胚胎发生中上调,并且基因修饰的干细胞具有膜型1-MMP(MT1-MMP)已经改善了纤维软骨的生产并且导致在大鼠模型中更高的负荷破坏和极限应力。还研究了特定的生长因子,如血小板衍生生长因子和成纤维细胞生长因子。已显示重组血小板衍生生长因子在与胶原基质一起使用时可改善修复的生物力学并增加骨-肌腱界面,但只能改善单独嵌入缝线时修复的组织学特征。类似地研究包括成纤维细胞生长因子2在大鼠模型中,显示出增加肌腱修复的组织学整合并改善了应用于肩袖修复时的生物力学性能。成纤维细胞生长因子2的作用是刺激导致肌腱改善骨愈合的祖细胞,甚至非细胞因子也参与了改善修复。最近的一项兔子研究表明,透明质酸可能作为肩袖修复的佐剂。尽管分析这些细胞因子和生物化合物的动物研究众多,但没有一个在人体模型中得到证实,需要进一步的研究来评估这些佐剂在肩袖修复中的安全性和有效性。"

| [1] Yamaguchi K, Ditsios K, Middleton WD. The demographic and morphological features of rotator cuff disease. A comparison of asymptomatic and symptomatic shoulders. J Bone Joint Surg Am. 2006;88(8):1699-1704. [2] Lafosse L, Brozska R, Toussaint B. The outcome and structural integrity of arthroscopic rotator cuff repair with use of the double-row suture anchor technique. J Bone Joint Surg Am. 2007;89(7):1533-1541. [3] Slabaugh MA, Nho SJ, Grumet RC, et al. Does the literature confirm superior clinical results in radiographically healed rotator cuffs after rotator cuff repair? Arthroscopy. 2010;26(3): 393-403. [4] Angeline ME, Dines JS. Factors affecting the outcome of rotator cuff surgery.//Nicholson GP, editor. Orthopaedic knowledge update: shoulder and elbow. Rosemont: American Academy of Orthopaedic Surgeons; 2013:217-228. [5] Garbis N, Romeo AA, Van Thiel G, et al. Clinical indications and techniques for the use of platelet-rich plasma in the shoulder. Oper Tech Sports Med. 2011;19(3):165–169. [6] Boswell SG, Cole BJ, Sundman EA, et al. Plateletrich plasma: a milieu of bioactive factors. Arthroscopy. 2012;28(3): 429-439. [7] Kesikburun S, Tan AK, Yilmaz B. Plateletrich plasma injections in the treatment of chronic rotator cuff tendinopathy: a randomized controlled trial with 1-year follow-up. Am J Sports Med. 2013;41(11):2609-2616. [8] Filardo G, DiMatteo B, Kon E, et al. Platelet-rich plasma in tendon-related disorders: results and indications. Knee Surg Sports Traumatol Arthrosc. 2018;26(7):1984-1999. [9] Shams A, El-SayedM, Gamal O. Subacromial injection of autologous platelet-rich plasma versus corticosteroid for the treatment of symptomatic partial rotator cuff tears. Eur J Orthop Surg Traumatol. 2016;26(8):837-842.[10] Chahal J, Van Thiel GS, Mall N, et al. The role of platelet-rich plasma in arthroscopic rotator cuff repair: a systematic review with quantitative synthesis. Arthroscopy. 2012;28(11): 1718-1727. [11] Warth RJ, Dornan GJ, James EW.Clinical and structural outcomes after arthroscopic repair of full-thickness rotator cuff tears with and without platelet-rich product supplementation: a meta-analysis and meta-regression. Arthroscopy. 2015; 31(2):306-320. 12. [12] Ebert JR Wang A, Smith A, et al. A midterm evaluation of postoperative platelet-rich plasma injections on arthroscopic supraspinatus repair: a randomized controlled trial. Am J Sports Med. 2017;45(13):2965-2974. [13] Jo CH, Shin JS, Shin WH, et al. Platelet-rich plasma for arthroscopic repair of medium to large rotator cuff tears: a randomized controlled trial. Am J Sports Med. 2015;43(9): 2102-2110. [14] Cai YZ, Zhang C, Lin XJ. Efficacy of platelet-rich plasma in arthroscopic repair of full-thickness rotator cuff tears: a meta-analysis. J Shoulder Elb Surg. 2015;24(12):1852-1859. [15] Saltzman BM, Jain A, Campbell KA, et al. Does the use of platelet-rich plasma at the time of surgery improve clinical outcomes in arthroscopic rotator cuff repair when compared with control cohorts? A systematic review of meta-analyses. Arthroscopy. 2016;32(5):906-918. [16] Sclamberg SG, Tibone JE, Itamura JM,et al. Six-month magnetic resonance imaging follow-up of large and massive rotator cuff repairs reinforced with porcine small intestinal submucosa. J Shoulder Elb Surg. 2004;13(5):538-541[17] Iannotti JP, Codsi MJ, Kwon YW, Porcine small intestine submucosa augmentation of surgical repair of chronic two-tendon rotator cuff tears. A randomized, controlled trial. J Bone Joint Surg Am. 2006;88(6):1238-1244. [18] Walton JR, Bowman NK, Khatib Y, et al. Restore orthobiologic implant: not recommended for augmentation of rotator cuff repairs. J Bone Joint Surg Am. 2007;89(4):786-791. [19] Badhe SP, Lawrence TM, Smith FD, et al. An assessment of porcine dermal xenograft as an augmentation graft in the treatment of extensive rotator cuff tears. J Shoulder Elb Surg. 2008;17(1 Suppl):35S-9S. [20] Cho CH, Lee SM, Lee YK,et al. Mini-open suture bridge repair with porcine dermal patch augmentation for massive rotator cuff tear: surgical technique and preliminary results. Clin Orthop Surg. 2014;6(3):329-335. [21] Gupta AK, Hug K, Boggess B,et al. Massive or 2-tendon rotator cuff tears in active patients with minimal glenohumeral arthritis: clinical and radiographic outcomes of reconstruction using dermal tissue matrix xenograft. Am J Sports Med. 2013; 41(4):872- 879. [22] Bond JL, DopirakRM, Higgins J, et al. Arthroscopic replacement of massive, irreparable rotator cuff tears using a GraftJacket allograft: technique and preliminary results. Arthroscopy. 2008;24(4):403-409. e1. [23] Wong I, Burns J, Snyder S. Arthroscopic GraftJacket repair of rotator cuff tears. J Shoulder Elb Surg. 2010;19(2 Suppl): 104-109. [24] Barber FA, Burns JP, Deutsch A,et al. A prospective, randomized evaluation of acellular human dermal matrix augmentation for arthroscopic rotator cuff repair. Arthroscopy. 2012;28(1):8-15.[25] Smith RDJ, Zargar N, Brown CP, et al. Characterizing the macro and micro mechanical properties of scaffolds for rotator cuff repair. J Shoulder Elbow Surg. 2017;26(11):2038-2046.[26] Beitzel K, McCarthy MB, Cote MP, et al. Properties of biologic scaffolds and their response to mesenchymal stem cells. Arthroscopy. 2014;30(3):289-298. [27] Consigliere P, Polyzois I, Sarkhel T,et al. Preliminary results of a consecutive series of large & massive rotator cuff tears treated with arthroscopic rotator cuff repairs augmented with extracellular matrix. Arch Bone Jt Surg. 2017;5(1):14-21. [28] Petri M, Warth RJ, Horan MP,et al. Outcomes after open revision repair of massive rotator cuff tears with biologic patch augmentation. Arthroscopy. 2016;32(9):1752-1760. [29] Sears BW, Choo A, Yu A, et al. Clinical outcomes in patients undergoing revision rotator cuff repair with extracellular matrix augmentation. Orthopedics. 2015;38(4):e292-296.[30] Ferguson DP, Lewington MR, Smith TD, et al. Graft utilization in the augmentation of large-to-massive rotator cuff repairs: a systematic review. Am J Sports Med. 2016;44(11): 2984-2992. [31] Steinhaus ME, Makhni EC, Cole BJ, et al. Outcomes after patch use in rotator cuff repair. Arthroscopy. 2016;32(8): 1676-1690. [32] Proctor CS. Long-term successful arthroscopic repair of large and massive rotator cuff tears with a functional and degradable reinforcement device. J Shoulder Elb Surg. 2014; 23(10):1508-1513. [33] Gulotta LV, Kovacevic D, Ehteshami JR, et al. Application of bone marrow-derived mesenchymal stem cells in a rotator cuff repair model. Am J Sports Med. 2009; 37 (11): 2126-2133. [34] Hernigou P, Flouzat Lachaniette CH, et al. Biologic augmentation of rotator cuff repair with mesenchymal stem cells during arthroscopy improves healing and prevents further tears: a case-controlled study. Int Orthop. 2014;38(9): 1811-1818. [35] Gotoh M, Mitsui Y, Shibata H,et al. Increased matrix metalloprotease-3 gene expression in ruptured rotator cuff tendons is associated with postoperative tendon retear. Knee Surg Sports Traumatol Arthrosc. 2013;21(8):1807-1812. |
| [1] | Jiang Hongying, Zhu Liang, Yu Xi, Huang Jing, Xiang Xiaona, Lan Zhengyan, He Hongchen. Effect of platelet-rich plasma on pressure ulcers after spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1149-1153. |
| [2] | He Xiangzhong, Chen Haiyun, Liu Jun, Lü Yang, Pan Jianke, Yang Wenbin, He Jingwen, Huang Junhan. Platelet-rich plasma combined with microfracture versus microfracture in the treatment of knee cartilage lesions: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(6): 964-969. |
| [3] | Jiang Lingkai, Wei Lei, Dong Zhengquan, Gu Xiaodong, Li Pengcui. Comparison of the effects of arthroscopic double-row suture fixation and suture bridge fixation for rotator cuff injury: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(21): 3431-3437. |
| [4] | Zuo Xiuqin, Yin Sasa, Xie Huimin, Jia Zishan, Zhang Lining. Applicability and specifications of platelet-rich plasma in musculoskeletal repair [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(20): 3239-3245. |
| [5] | Li Xiangze, Bu Xianmin, Li Dongmei, Chi Yulei, Su Qiang, Jin Xintong, Zhao Jian, Zhang Gaotian, Wu Bin, Meng Chunyang . Stem cells, cytokines, hormones, neuropeptides and genes in traumatic brain trauma to promote fracture healing [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(19): 3057-3063. |
| [6] | Chen Jufang, Tian Yulou, Hao Xin. Role and potential of adipose-derived stem cells in cranio-maxillofacial bone regeneration [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(13): 2087-2096. |
| [7] | Tian Yanping, Li Juan, Liu Xiaobo, Zhang Huiling, Shi Lihong, Jin Rongjiang. Knowledge network mapping of literature regarding platelet-rich plasma in recent 5 years: a visual analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(11): 1745-1752. |
| [8] | Liu Peidong, Feng Jiangfeng, Xu Wenjie, Xu Xiaodong, Yang Ziquan . Bioinformatics analysis of gene expression profile and key pathways related to fatty infiltration after rotator cuff injury [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(11): 1773-1778. |
| [9] | Yu Chenghao, Zhang Yi, Qi Chao, Chen Jinli, Gao Jiake, Yu Tengbo. Effect of cytokines and platelet-rich plasma on tendon derived stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(1): 133-140. |
| [10] | Wang Ning, Zhong Weijian. Application and function of autologous blood concentrate in tissue regeneration [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(1): 146-151. |
| [11] | Xu Guofeng, Li Xuebin, Tang Yifan, Zhao Yin, Zhou Shengyuan, Chen Xiongsheng, Jia Lianshun. The role of autophagy in ossification of the human ligamentum flavum [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(8): 1174-1181. |
| [12] | Xiu Yiping, Zhang Liyan, Qian Xueyi, Li Yan, Li Wantong. The clinical application of platelet-rich plasma to repair chronic refractory wounds: a retrospective study and literature retrieval evidence analysis [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(8): 1231-1237. |
| [13] | Qiu Guorong, He Benxiang, Wang Chun. Biological mechanism of platelet-rich plasma for tendinopathy repair: a visual study based on scientific knowledge map [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(5): 787-795. |
| [14] | Ren Jun, Zhao Yan, Xiao Bin, Ma Chao, Wang Xinke, Hao Yabin, Cheng Jie. Platelet-rich plasma promotes the healing of tibial fracture in rabbits [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(35): 5595-5599. |
| [15] | Huo Yanxu, Yang Zhi, Pei Fang, Chen Xiangyang. Clinical study on the relationship between critical shoulder joint angle and degenerative rotator cuff tear [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(35): 5644-5649. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||