Chinese Journal of Tissue Engineering Research ›› 2016, Vol. 20 ›› Issue (44): 6673-6681.doi: 10.3969/j.issn.2095-4344.2016.44.020
Previous Articles Next Articles
Research progress of bone microarchitecture and microdamage detection
Xu Can, Li Ming-qing, Wang Cheng-gong, Li Kang-hua, Liu Hua
- Department of Orthopedics, Xiangya Hospital of Central South University, Changsha 410008, Hunan Province, China
-
Revised:2016-08-10Online:2016-10-28Published:2016-10-28 -
Contact:Liu Hua, M.D., Associate chief physician, Department of Orthopedics, Xiangya Hospital of Central South University, Changsha 410008, Hunan Province, China -
About author:Xu Can, M.D., Attending physician, Department of Orthopedics, Xiangya Hospital of Central South University, Changsha 410008, Hunan Province, China -
Supported by:the National Natural Science Foundation of China, No. 81301543
CLC Number:
Cite this article
Xu Can, Li Ming-qing, Wang Cheng-gong, Li Kang-hua, Liu Hua. Research progress of bone microarchitecture and microdamage detection[J]. Chinese Journal of Tissue Engineering Research, 2016, 20(44): 6673-6681.
share this article
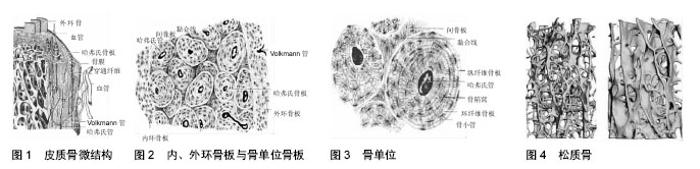
2.1 骨组织微结构 2.1.1 皮质骨(compact bone) 皮质骨由不同排列方式的骨板组成。骨板排列方式有外环骨板、内环骨板、骨单位骨板和间骨板几种类型(图1)。 外环骨板(outer circumferential lamella):环绕骨干表面且呈平行排列,约十数层或数十层,比较整齐。外环骨板的外面与骨膜紧密相接,其中可见横向穿行的管道,称穿通管,又称福克曼(Volkmann)管,外膜的小血管由此进入骨内(图2)。 内环骨板(inner circumferential lamella):居于骨干的骨髓腔面,仅由数层骨板组成,不如外环骨板平整。内环骨板中也有穿通管穿行,管中的小血管与骨髓血管相通连。 骨单位骨板(osteon lamella):又称哈弗氏骨板(Haversian lamella),位于内、外环骨板之间,是骨干皮质骨的主要组成部分。骨单位骨板呈同心圆排列,中央的管道为中央管(central canal),又称哈弗氏管。骨单位(osteon)又称哈弗氏系统(Haversian system),是皮质骨中主要起支持作用的结构和营养单位,呈长筒形,长0.6-2.5 mm,直径30-70 μm,其长轴与骨干长轴平行,由4-20层同心圆排列的骨板围成。骨单位表面有一层黏合质,它是一层含盐多、含纤维少的骨基质,在横断面的骨磨片上呈折光较强的轮廓线,称为黏合线(cement line),构成骨单位的边界(图3)。 骨单位内部各层骨板间的骨陷窝(bone lacuna)和骨小管(bone canaliculus)相互通连,最内层骨小管则开口于中央管,管内有骨膜结缔组织及血管和神经,骨细胞从中央管内的组织液获得营养并排出废物。但骨单位最外层的骨小管在黏合线以内折返,不与相邻的骨单位内的骨小管相通。相邻骨单位的中央管相互间以横行的穿通管相通连。 间骨板:为填充在骨单位之间的一些半月形或不规则的平行骨板,它是在骨生长改建中原有的骨单位或外环骨板未被吸收的残留部分。间骨板内存在骨小管但无血管通道,有时骨单位外层的骨小管会穿过黏合线,与间骨板内的骨小管相联通,形成一条骨单位中央管和间骨板之间的物质交换通道。 2.1.2 松质骨(cancellous bone) 松质骨分布在长骨的干骺端,是由棒状或者平板状骨小梁相互联通的三维立体网络结构,状如“脚手架”,承受复合力学负荷,对于皮质骨的支撑作用极为重要。松质骨内部具有大小各异的互联孔,由此形成孔隙率和密度不同的结构。棒状网络结构形成了低密度的松质骨,细胞处于较开放的环境,而板状网络结构则构成了高密度的松质骨,细胞处于较闭合的环境(图4)。松质骨的相对密度是指松质骨标本密度与完全致密的皮质骨标本密度的比值,其范围为0.05-0.7,阈值对应的孔隙率为90%-30%。 "


2.2 骨微损伤定义 早在1960年,Frost就利用不脱钙骨组织染色切片的方法发现了骨的显微损伤,然而Frost所观察到的损伤,究竟是真正的微损伤还是实验过程人为操作的破坏,一直存在争论并持续多年。直到20世纪90年代初,众多学者利用Burr等的碱性品红骨大块染色技术才最终证实了微损伤的存在。 骨微损伤是指骨因“疲劳”而导致的骨显微结构的改变。材料学上的“疲劳”现象是指材料在低于断裂强度的较小应力/应变周期性作用下,材料中会萌生微观裂纹并逐渐扩展,当损伤积累到一定程度时就会最终导致材料的整体失效。骨组织在日常的生理负荷周期性作用下会萌生两种常见的骨微损伤:“线性”和“弥散性”微损伤。当前人们对于线性微损伤的认识较为清晰,但对弥散性微损伤的认识还有所欠缺。线性微损伤和弥散性微损伤具有同等的重要性,二者在形态上有一定的相似性,但在力学和生物学特征上有着显著的差异。 线性微损伤在骨组织切片上表现为长度50- 100 μm的边界锐利的裂纹,它们是在步行和跑步等生理负荷的周期性作用下形成的。对健康人而言,生理负荷周期性作用下萌生的微损伤会随着骨重建被修复而不产生临床问题,但是当微损伤积累的速度超过了骨重建的修复能力后,微裂纹会在应力的反复作用下逐渐扩展并最终导致骨折。 线性微裂纹多发生于间质骨。间质骨是在骨重建中原有骨单位或外环骨板未被吸收的残留部分,间质骨较骨单位内的骨组织年龄较老因而经历了更多疲劳载荷的周期作用。有研究显示,间质骨中非酶胶原交联程度和矿化程度要高于新生骨单位的骨基质,这可能是线性微损伤好发于间质骨的内源性因素。骨微结构的研究显示,当沿着骨长轴观察时,微裂纹的长度显著长于横断面所观察到的长度。这是因为裂纹通常都沿着结构中的潜在间隙延伸。许多研究发现皮质骨和松质骨中的线性微损伤会随着年龄增长而显著增加;Courtney等[5]发现老龄骨和年轻骨接受相同的疲劳载荷周期作用直至屈服后,老龄骨中的线性微损伤要多于年轻骨。这些研究都说明线性微损伤与骨质量以及骨折风险相关,但是他们之间的确切关系至今仍未明确,其主要原因是现有的微损伤检测方法无法直接对临床患者进行观察。 弥散性微损伤在骨组织切片上表现为弥散性的片状红染区域,长度一般小于10 μm。人们首先在碱性品红骨大块染色的皮质骨标本中发现了弥散性微损伤,高分辨率下观察可以发现它们是由多群极小的骨细胞裂纹(1 μm以下)聚集构成的[6-9],后来人们又在松质骨中发现了弥散性微损伤[7]。在所有微损伤中,弥散性微损伤是最早且最易于萌生的。在生理负荷周期性作用的早期就会迅速出现弥散性微损伤,此外,当大小恒定的载荷持续作用于骨标本一段时间后,也会出现弥散性微损伤(材料学上称为“蠕变”)。弥散性微损伤并非线性微损伤的延伸,Boyce[10]和Diab等[11]研究发现线性和弥散性微损伤发生在相互独立的区域;弥散性微损伤常出现于张应力作用区域,而线性微损伤则常出现于压应力或剪切应力作用区域[10,12]。同时,有研究发现人体对弥散性微损伤的生理反应完全不同于线性微损伤[13]。这些都说明二者在力学和生物学特征上有着显著差异。 2.3 骨微结构以及骨微损伤的检测方法 2.3.1 破坏性方法 骨微结构和微损伤的二维检测——从骨组织形态计量学到碱性品红骨大块染色法:①骨微结构的常用检查方法——骨组织形态计量学:传统方法制作骨组织切片时需要将骨组织进行脱钙、脱水透明、石蜡包埋及切片,再染色观察。然而,在脱钙的过程中,往往原有组织的边缘形态会发生改变,不能准确地评估骨的形态。1960年美国骨整形外科医生Frost[14]提出了一种定量研究骨微结构和骨量的技术,其采用“不脱钙硬包埋法”和“活体荧光标记法”进行骨组织标本制作,更好地保留了骨组织微细结构。这就是目前检查骨微结构与评价骨转换重建最常用和有效的方法—“骨组织形态计量学”。骨组织形态计量学的测定对象是不脱钙且带有“活体”荧光标记的骨标本,其计算结果包括静态参数和动态参数。通过不脱钙硬包埋法能够较好的保持骨组织的完整性,计算所得的骨小梁体积百分数(BV/TV)、骨小梁厚度(Tb.Th)、骨小梁数量(Tb.N)、骨小梁分离度(Tb.Sp)、皮质骨厚度(Ct.Th)等静态参数值可以定量反映骨组织的微结构;同时,采用“活体”四环素、钙黄绿素双标记,可将时间因素以荧光标记在骨重建过程中,从而动态地观察骨组织的变化,得到动态参数信息,即所谓“动态骨组织形态计量学”(dynamic bone histomorphometry);②骨微损伤的常用检查方法——碱性品红骨大块染色(en bloc basic fuchsin staining):目前检测骨微损伤最常用的方法是碱性品红骨大块染色法。早在1960年Frost[14]就已经提出了碱性品红骨大块染色,但当前通用的步骤是由Burr等[15]于1990年在Frost的基础上改进后提出的。现行方法是:将含有微损伤的骨块用体积分数70%乙醇固定48 h,然后置入含1%碱性品红的乙醇(体积分数80%,90%,100%)内进行染色和逐级脱水。染色后的皮质骨可以直接切片或者用有机玻璃包埋后切片,但对松质骨需要做有机玻璃包埋后切片,切片厚度为50-100 μm。骨大块染色的优点是可以区分真正的骨微损伤和标本处理过程中的人为损伤。由于标本处理(包埋和切片)是在骨染色之后,所以标本处理所产生的微损伤并不染色。最初,人们使用常光显微镜观察碱性品红染色结果,但要将体内产生的全染色微损伤和加工过程中产生的部分染色以及未染色微损伤区分开来十分耗时费力。由于碱性品红是一种兼具强烈红光和荧光的染色剂,1998年Lee等[16]提出在荧光显微镜下进行观察骨微损伤更加简单快速并且准确;1999年Huja等[17]证实了荧光显微镜能够更敏感的检测骨微损伤,在定量评定时可以产生更精确的效果。③碱性品红骨大块染色法的发展——序贯荧光染色标记法(sequential fluorochrome labelling):碱性品红虽然能够用于微损伤染色,但存在两个缺点。首先,由于碱性品红染色的原理是它能够进入骨微结构中的空隙,所以它对微损伤染色的同时也会对骨微结构中的骨小管和血管染色,也就是说它不具备针对骨微损伤的“位点特异性”;其次,在应力作用下骨微损伤会扩展,如果要显示微损伤的扩展过程,就必须使用两种颜色不同的染色剂在微损伤扩展的前后分别染色;而碱性品红作为单一染色剂自然无法显示骨微损伤的扩展过程。为了解决这两个问题,研究者们提出了序贯荧光染色标记法。其所选择的染色剂为钙离子螯合荧光染色剂(具备针对微损伤的位点特异性),并且在加载前后使用不同荧光的螯合剂对微损伤各进行一次染色,这样就可以区分加载前已经存在的微损伤和加载后新发以及在原有基础上扩展的微损伤。2000年Lee等[18]比较了5种钙螯合荧光染色剂对骨微损伤的染色效果,发现茜素氨羧络合剂、钙黄绿素、钙黄绿素蓝、土霉素以及二甲酚橙对微损伤具有与碱性品红相同的检测能力,但缺点是不同染色剂边界欠清晰;2002年O’Brien等[19]对该法做了改进,他提出了几种荧光染色剂的理想浓度并联合使用离子色谱法(ion chromatography)以提高显像效果;2003年O’Brien等[20]应用序贯染色成功检测了疲劳试验导致的皮质骨微损伤的萌生、扩展过程。④兼顾微结构与微损伤检测的方法——保留四环素标记的荧光染色/双染色法(double labeling method):2011年Burt-Pichat等[21]在骨组织形态计量学方法和大块骨序贯染色的基础上提出了保留四环素标记的荧光染色。研究首先使用四环素(动态骨组织形态计量学常用的标记物)进行骨组织的“活体”荧光标记,取出骨标本后再使用各种不同的螯合荧光染色剂标记加工过程中产生的微损伤并比较染色效果,最终发现钙黄绿素和二甲酚橙能够较好的显示新发微损伤同时保留活体四环素荧光标记。这就使得研究者们可以在获取骨组织形态计量学参数的同时检测骨微损伤。 骨微结构和微损伤的三维成像:①连续铣削成像法(serial block face imaging):虽然有许多方法可以在无创的条件下对骨微结构进行三维成像,但这些方法在提高成像分辨率的同时往往需要减小标本体积。为了保证较高的分辨率同时兼顾标本尺寸,1997年Beck等[22]在骨大块染色法的基础上提出了连续铣削成像法(serial block face imaging)。具体方法是:对骨标本进行染色和包埋后,使用CNC数控铣床连续铣削骨标本,每次仅削除5-20 μm的薄层。进而使用高分辨率数码相机拍摄断面图像,如断面较大,则使用计算机精确控制摄像头移动后逐格拍照,后期再进行图像拼接而构成高分辨单层断面图像。接着,铣床再次削除薄层骨组织并拍摄断面,这样逐层步进,最终获取标本的连续断层图像,并使用相关软件对标本连续断层图像进行三维重建。2007年Kazakia等[23]在该技术的基础上引入了全自动铣削并使用二甲酚橙对微损伤进行荧光染色,由此极大的减小了工作强度并使连续铣削法能够检测骨微损伤,试验中标本直径8 mm,分辨率达到了3 μm×3 μm×8 μm;2008年Bigley等[24]比较了基于荧光染色的连续铣削成像法和序贯荧光染色标记法,证实二者在检测骨微损伤时具有相同的可信度;2009年Slyfield等[25]以及Tkachenko等[26]在一项针对骨小梁上破骨细胞形成的吸收陷窝的研究中,将基于荧光染色连续铣削法的分辨率进一步提高到0.7 μm;由于荧光染色连续铣削法已经能够在三维空间显示能够反映骨转换重建的吸收陷窝,2012年Slyfield等[27]正式提出了三维动态骨组织形态剂量学(Three-dimensional dynamic bone histomorphometry)的概念,之前只能通过经典的双染色二维切片获得的骨转换重建动态参数就此内能够通过荧光染色连续铣削法在三维空间内获取;2015年Goff等[28]使用钙黄绿素和二甲酚橙染色标记骨微损伤,继而使用连续铣削法构建三维模型(标本直径5.4 mm,高度4 mm),试验中分辨率进一步提高到了0.7 μm×0.7 μm×5 μm,实验清晰显示了骨微损伤的三维空间分布,充分体现了荧光染色连续铣削法对骨微损伤的检测能力。②激光扫描共聚焦显微镜:是一种利用计算机、激光和图像处理技术获得生物样品三维数据的分析仪器。激光点光源照射标本(标本预先做荧光染色)后,会在焦平面上形成一个轮廓分明的小光点,而该点被照射后所发出的荧光会被物镜收集而成像,这样以激光逐点扫描样品后,会最终聚合形成整个焦平面的共聚焦清晰图像。由于可进行荧光染色且具备较高三维空间分辨率,激光扫描共聚焦显微镜被广泛应用于各个学科。1994年Zioupos等[29]首先使用激光扫描共聚焦显微镜检测了骨微损伤;2000年O’Brien等[30]比较了激光扫描共聚焦显微镜和连续铣削成像法对碱性品红染色的骨标本中微损伤的检测能力,认为二者都可以有效的检测骨微损伤;2001年Zioupos[31]使用激光扫描共聚焦显微镜检测了皮质骨中的微损伤,分辨率达到10 μm;2007年Diab等[32]使用激光扫描共聚焦显微镜检测了碱性品红染色的皮质骨在疲劳试验中的微损伤形态;2012年Poundarik等[33]使用激光扫描共聚焦显微镜在更高分辨率下对弥散型微损伤中的亚微米级裂纹和膨胀带(dilatational bands)进行了检测。激光扫描共聚焦显微镜的优点是可以对微损伤以及微裂纹进行三维重建,具有较高的空间分辨率。其缺点是视野有限,景深较浅,只能重建标本表面以下有限深度的微损伤,无法观察到微裂纹的全貌以及骨组织的微结构,同时标本的处理(染色、切片等)也是破坏性的。 2.3.2 无创检测方法 micro-CT检测骨微结构:1972年Godfrey Hounsfield首先发明了CT技术,随后CT被迅速应用于临床;进入20世纪80年代,位于美国底特律的福特汽车公司为了探测材料中的结构和应力缺陷,不断改进CT技术,将CT的空间分辨率提高到了100 μm以上,这从侧面极大的推动了micro-CT的发展[34];到了20世纪80年代后期,底特律地区的骨科研究者们首先将micro-CT应用到了骨微结构的研究中[35-37];进入20世纪90年代以后,随着商用micro-CT的出现(分辨率10-100 μm),骨微结构的micro-CT研究也迅速增加。当前,micro-CT已成为骨微结构无创检查的常规方法。 micro-CT相对于传统的骨组织形态计量学方法有很多优势。首先,micro-CT检测是相对无创的,它能够获取准确的影像数据且不破坏标本,在进行micro-CT检查后,标本仍然可以做进一步的组织学或是化学、生物学检测;其次,micro-CT所得的图像分辨率高,能精确测定骨微结构的三维形态参数, 能够测得真正意义上的骨密度。 对比剂增强micro-CT检测骨微损伤:虽然micro-CT能够较好的对骨微结构进行扫描与三维重建,但对结构更加微小的骨微损伤进行检测有一定困难。为了在micro-CT扫描图像中加强骨微损伤的显像,人们开始尝试使用对比剂。由于骨结构本身在CT扫描中就表现为高CT值,因此对比剂的选择有一定困难。2005年Leng等[38]尝试使用“硫化铅”作为对比剂检测皮质骨中的微损伤;2006年Parkesh等[39-40]尝试使用“碘剂”作为对比剂对骨微损伤进行扫描,但他们使用的是自行合成的碘剂,且对微损伤的显像效果欠佳;2007年Tang等[41]将原本用于扫描电镜的“醋酸双氧铀”改用做micro-CT对比剂,获得了较为理想的效果;2007年以及2008年Leng等[42]以及Wang等[43]使用“硫酸钡”作为对比剂分别对松质骨和皮质骨中的微损伤进行了micro-CT扫描,也获得了较为理想的效果。相对于前几种对比剂,硫酸钡可能是相对合理且较有应用前景的选择,因为当前临床上普遍使用硫酸钡作为对比剂进行胃肠道造影,即所谓“钡餐”。2010年Turnbell 等[44-45]使用硫酸钡做对比剂对皮质骨微损伤进行了增强micro-CT扫描,并与传统碱性品红骨大块染色法进行对比,发现增强micro-CT能够无创的显示微损伤的三维空间分布和积累过程,且其显示结果与碱品骨大块染色结果显著相关,证实了硫酸钡增强micro-CT方法的有效性;此后,硫酸钡又被成功应用于多个增强micro-CT研究,进一步体现了硫酸钡作为对比剂应用于增强micro-CT检测骨微损伤的可靠性。 同步辐射光源micro-CT(synchrotron radiation μCT,SRμCT):现有商用micro-CT在可以接受的检测时长范围内,其空间分辨率在10-100 μm。如果需要达到更高的空间分辨率则可能需要使用同步辐射光源。同步辐射光源是一种利用或正电子在磁场中偏转时所产生的同步辐射的高性能新型强光源,它具有高纯净度和高亮度的特点。利用同步辐射光源的这些特性,将其应用于micro-CT扫描可以获得极高的空间分辨率和信噪比。1993年同步辐射光源被首次推荐应用于micro-CT[46],此后,SRμCT逐渐应用于骨微结构研究[47-50]。目前世界各地的第3代同步辐射光源中心的空间分辨率可以到达1 μm左右[51],特殊设置下,其分辨率还可以提高到100 nm[52]。尽管SRμCT相对于商用micro-CT有较大的优势,但同步辐射光源的产生需要昂贵庞大的设备,故进行SRμCT扫描必须前往相关地区的同步辐射光源中心站点,这也限制了SRμCT的广泛应用。 2003年Ito等[53]比较了SRμCT、micro-CT和扫描电镜对骨微结构的扫描效果,结果显示SRμCT的三维重建图像能够显示骨小梁表面的吸收陷窝,而它的二维扫描图像可以反映骨结构中不同位置的矿化程度,是研究骨微结构的有力工具;2006年Thurner等[54]以及Larrue等[55]将SRμCT应用于松质骨破坏时微裂纹积累过程的观察(分辨率3.5 μm);2009年Voide等[56]将SRμCT应用于皮质骨破坏时微裂纹发生发展过程的观察(分辨率700 nm),这些研究都表明SRμCT是骨微结构和微损伤检测的理想工具。 扫描电子显微镜:扫描电子显微镜发明于1965年,扫描电子显微镜使用极狭窄的电子束去扫描样品,通过电子束与样品的相互作用产生二次电子发射,进而使用二次电子信号成像来观察样品的表面形态。由于扫描电子显微镜的原理是使用电子束扫描样品表面并激发二次电子发射,因此扫描电子显微镜扫描要求样品表面能够导电,对于骨和其他许多不导电的试样,在扫描前需要进行镀膜处理,在材料表面形成一层导电膜。 扫描电镜的分辨率极高(< 1 μm),视野和景深大,成像富有立体感,可直接观察试样表面凹凸不平的细微结构。上世纪70年代研究者们就开始使用扫描电子显微镜对骨微结构进行研究[57-58],现在人们常使用扫描电子显微镜在纳米层级下观察微损伤的超微结构[59-60]。类似于增强micro-CT,为了加强微损伤的显像,人们使用“硫化铅”做对比剂对骨微损伤进行扫描电子显微镜扫描[61],因为硫化铅染色后可以使微损伤区域的电子密度增高,从而使显像中微损伤的亮度增强。 材料学中扫描电子显微镜常用于断口分析,人们也应用扫描电子显微镜对骨折进行了断口分析。1997年Braidotti等[62]使用扫描电子显微镜扫描检测了皮质骨的断裂面;2007年Wise等[63]使用扫描电镜对不同应变造成的骨折断面进行了比较分析。 在普通电镜基础上发展而成的“环境扫描电镜”能够对导电和不导电样品进行高分辨率的静态和动态观察。2014年Carriero等[64-65]使用环境扫描电镜观察了小鼠的骨折线形貌,发现基因缺陷小鼠的骨折线表现为线性路径,而野生型小鼠的骨折线会出现较多分叉。"

| [1] Hui SL, Slemenda CW, Johnston CC Jr. Age and bone mass as predictors of fracture in a prospective study. J Clin Invest. 1988;81(6): 1804-1809. [2] Knudtson M. Osteoporosis: Background and Overview. J Nurs Prac. 2009;5(6): S4-S12. [3] Hernandez CJ, Keaveny TM. A biomechanical perspective on bone quality. Bone. 2006;39(6): 1173-1181. [4] Diab T, Vashishth D. Effects of damage morphology on cortical bone fragility. Bone. 2005;37(1): 96-102. [5] Courtney AC, Hayes WC, Gibson LJ. Age-related differences in post-yield damage in human cortical bone. Experiment and model. J Biomech. 1996;29(11): 1463-1471. [6] Burr DB, Turner CH, Naick P, et al. Does microdamage accumulation affect the mechanical properties of bone? J Biomech. 1998;31(4): 337-345. [7] Vashishth D, Koontz J, Qiu SJ, et al. In vivo diffuse damage in human vertebral trabecular bone. Bone. 2000;26(2): 147-152. [8] Yeni YN, Hou FJ, Ciarelli T, et al. Trabecular Shear Stresses Predict In Vivo Linear Microcrack Density but not Diffuse Damage in Human Vertebral Cancellous Bone. Ann Biomed Eng. 2003;31(6): 726-732. [9] Fazzalari NL, Forwood MR, Manthey BA. Three-dimensional confocal images of microdamage in cancellous bone. Bone. 1998;23(4): 373-378. [10] Boyce TM, Fyhrie DP, Glotkowski MC, et al. Damage type and strain mode associations in human compact bone bending fatigue. J Orthop Res. 1998;16(3): 322-329. [11] Diab T, Condon Kwburr DB, Vashishth D. Age-related change in the damage morphology of human cortical bone and its role in bone fragility. Bone. 2006;38(3): 427-431. [12] Reilly GC, Currey JD. The development of microcracking and failure in bone depends on the loading mode to which it is adapted. J Exp Biol. 1999; 202(202): 543-52. [13] Seref-Ferlengez Z, Basta-Pljakic J, Kennedy OD, et al. Structural and Mechanical Repair of Diffuse Damage in Cortical Bone In Vivo. J Bone Miner Res. 2014;29(12): 2537-2544. [14] Frost H. Presence of microscopic cracks in vivo in bone. Henry Ford Hosp Med Bull. 1960;8(2): 35. [15] Burr DB, Stafford T. Validity of the bulk-staining technique to separate artifactual from in vivo bone microdamage. Clin Orthop Relat Res. 1990;260(260): 305-308. [16] Lee TC, Myers ER, Hayes WC. Fluorescence-aided detection of microdamage in compact bone. J Anatomy. 1998;193(Pt 2): 179-184. [17] Huja SS, Hasan MS, Pidaparti R, et al. Development of a fluorescent light technique for evaluating microdamage in bone subjected to fatigue loading. J Biomech. 1999;32(11): 1243-1249. [18] Lee TC, Arthur TL, Gibson LJ, et al. Sequential labelling of microdamage in bone using chelating agents. J Orthop Res. 2000;18(2):322-325. [19] O’Brien FJ, Taylor D, Lee TC. An improved labelling technique for monitoring microcrack growth in compact bone. J Biomech. 2002;35(4): 523-526. [20] O’Brien FJ, Taylor D, Lee TC. Microcrack accumulation at different intervals during fatigue testing of compact bone. J Biomech. 2003;36(36): 973-980. [21] Burt-Pichat B, Follet H, Toulemonde G, et al. Methodological approach for the detection of both microdamage and fluorochrome labels in ewe bone and human trabecular bone. J Bone Miner Metab. 2011;29(29): 756-764. [22] Beck JD, Canfield BL, Haddock SM, et al. Three-dimensional imaging of trabecular bone using the computer numerically controlled milling technique. Bone. 1997;21(3): 281-287. [23] Kazakia GJ, Lee JJ, Singh M, et al. Automated high-resolution three-dimensional fluorescence imaging of large biological specimens. J Microsc. 2007;225(Pt 2): 109-117. [24] Bigley RF, Singh M, Hernandez CJ, et al. Validity of serial milling-based imaging system for microdamage quantification. Bone. 2008;42(1): 212-215. [25] Slyfield CR, Niemeyer KE, Tkachenko EV, et al. Three-dimensional surface texture visualization of bone tissue through epifluorescence-based serial block face imaging. J Microsc. 2009;236(1): 52-59. [26] Tkachenko EV, Slyfield CR, Tomlinson RE, et al. Voxel size and measures of individual resorption cavities in three-dimensional images of cancellous bone. Bone. 2009;45(3): 487-492. [27] Slyfield CR, Tkachenko EV, Wilson DL, et al. Three-dimensional dynamic bone histomorphometry. J Bone Miner Res. 2012;27(2): 486-495. [28] Goff MG, Lambers FM, Sorna RM, et al. Finite element models predict the location of microdamage in cancellous bone following uniaxial loading. J Biomech. 2015;48(15): 4142-4148. [29] Zioupos P, Currey JD, Sedman AJ. An examination of the micromechanics of failure of bone and antler by acoustic emission tests and Laser Scanning Confocal Microscopy. Med Eng Phys. 1994;16(3): 203-212. [30] O'Brien FJ, Taylor D, Dickson GR, et al. Visualisation of three-dimensional microcracks in compact bone. J Anat. 2000;197 Pt 3(3): 413-420. [31] Zioupos P. Accumulation of in-vivo fatigue microdamage and its relation to biomechanical properties in ageing human cortical bone. J Microsc. 2001;201(201): 270-278. [32] Diab T, Vashishth D. Morphology, localization and accumulation of in vivo microdamage in human cortical bone. Bone. 2007;40(3): 612-618. [33] Poundarik AA, Diab T, Sroga GE, et al. Dilatational band formation in bone. Proc Nat Acad Scie. 2012; 109(47): 19178-19183. [34] Feldkamp LA, Davis LC, Kress JW. Practical cone-beam algorithm. J Opt Soc Am. 1984;1(6): 612-619. [35] Layton MW, Feldkamp LA, Ms DJ, et al. Examination of subchondral bone architecture in experimental osteoarthritis by microscopic computed axial tomography. Arthritis Rheum. 1988;31(11): 1400-1405. [36] Kuhn JL, Goldstein SA, Feldkamp LA, et al. Evaluation of a microcomputed tomography system to study trabecular bone structure. J Orthop Res. 1990;8(6): 833-842. [37] Feldkamp LA, Goldstein SA, Parfitt MA, et al. The direct examination of three-dimensional bone architecture in vitro by computed tomography. J Bone Miner Res.1989;4(1): 3-11. [38] Leng H, Vandersarl J, Niebur G, et al. Microdamage in bovine cortical bone measured using micro- computed tomography. Trans Orthop Res Soc. 2005;30: 665. [39] Parkesh R, Mohsin S, Tc L, et al. Histological, Spectroscopic, and Surface Analysis of Microdamage in Bone: Toward Real-Time Analysis Using Fluorescent Sensors. Chem Mater. 2007;19(7): 1656-1663. [40] Parkesh R, Lee TC, Gunnlaugsson T, et al. Microdamage in bone: surface analysis and radiological detection. J Biomech. 2006;39(39): 1552-1556. [41] Tang SY, Vashishth D. A non-invasive in vitro technique for the three-dimensional quantification of microdamage in trabecular bone. Bone. 2007;40(5): 1259-1264. [42] Leng H, Wang X, Ross RD, et al. Micro-computed tomography of fatigue microdamage in cortical bone using a barium sulfate contrast agent. J Mech Behav Biomed Mater. 2008;1(1):68-75. [43] Wang X, Masse DB, Leng H, et al. Detection of trabecular bone microdamage by micro-computed tomography. J Biomech. 2007;40(15): 3397-3403. [44] Turnbull TL, Gargac JA, Niebur GL, et al. Detection of Fatigue Microdamage in Whole Rat Femora Using Contrast-Enhanced Micro-Computed Tomography. J Biomech. 2011;44(13): 2395-2400. [45] Turnbull TL, Baumann AP, Roeder RK. Fatigue microcracks that initiate fracture are located near elevated intracortical porosity but not elevated mineralization. J Biomech. 2014;47(12): 3135-3142. [46] Grodzins L. Optimum energies for x-ray transmission tomography of small samples: Applications of synchrotron radiation to computerized tomography I. Nucl Instr Methods Phys Res. 1983;206(3): 541-545. [47] Bonse U, Busch F, Günnewig O, et al. 3D computed X-ray tomography of human cancellous bone at 8 μm spatial and 10- 4 energy resolution. Bone Miner. 1994; 25(1): 25-38. [48] Engelke K, Graeff W, Meiss L, et al. High Spatial Resolution Imaging of Bone Mineral Using Computed Microtomography: Comparison with Microradiography and Undecalcified Histologic Sections. Invest Radiol. 1993;28(4): 341-349. [49] Lane NE, Haupt D, Kimmel DB, et al. Early estrogen replacement therapy reverses the rapid loss of trabecular bone volume and prevents further deterioration of connectivity in the rat. J Bone Miner Res. 1999;14(2): 206-214. [50] Salomé M, Peyrin F, Cloetens P, et al. A synchrotron radiation microtomography system for the analysis of trabecular bone samples. Med Phys. 1999;26(10): 2194-2204. [51] Stampanoni M, Borchert G, Wyss P, et al. High resolution X-ray detector for synchrotron-based microtomography. Nucl Instr Methods Phys Res. 2002;491(1-2): 291-301. [52] Snigireva I, Snigirev A. X-Ray microanalytical techniques based on synchrotron radiation. J Environ Monit. 2006;8(1): 33-42. [53] Ito M, Ejiri S, Jinnai H, et al. Bone structure and mineralization demonstrated using synchrotron radiation computed tomography (SR-CT) in animal models : preliminary findings. J Bone Miner Metab. 2003;21(5): 287-293. [54] Thurner PJ, Wyss P, Voide R, et al. Time-lapsed investigation of three-dimensional failure and damage accumulation in trabecular bone using synchrotron light. Bone. 2006;39(2): 289-299. [55] Larrue A, Rattner A, Laroche N, et al. Feasibility of micro-crack detection in human trabecular bone images from 3D synchrotron microtomography. Conf Proc IEEE Eng Med Biol Soc. 2007;2007:3918-21. [56] Voide R, Schneider P, Stauber M, et al. Time-lapsed assessment of microcrack initiation and propagation in murine cortical bone at submicrometer resolution. Bone. 2009;45(2): 164-173. [57] Dyson ED, Jackson CK, Whitehouse WJ. Scanning electron microscope studies of human trabecular bone. Nature. 1970;225(5236): 957-959. [58] Whitehouse WJ, Dyson ED, Jackson CK. The scanning electron microscope in studies of trabecular bone from a human vertebral body. J Anat. 1971; 108 (Pt 3): 481-496. [59] Vashishth D, Behiri JC, Bonfield W. Crack growth resistance in cortical bone: concept of microcrack toughening. J Biomech. 1997;30(8): 763-769. [60] Goldstein JI, Newbury DE, Echlin P, et al. Scanning electron microscopy and X-ray microanalysis. A text for biologists, Mat Sci Geol. 1981: 469-484. [61] Schaffler MB, Pitchford WC, Choi K, et al. Examination of compact bone microdamage using back-scattered electron microscopy. Bone. 1994;15(5): 483-488. [62] Braidotti P, Branca F P, Stagni L. Scanning electron microscopy of human cortical bone failure surfaces. J Biomech. 1997;30(2): 155-162. [63] Wise LM, Wang Z, Grynpas MD. The use of fractography to supplement analysis of bone mechanical properties in different strains of mice. Bone. 2007;41(4): 620-630. [64] Carriero A, Zimmermann EA, Shefelbine SJ, et al. A methodology for the investigation of toughness and crack propagation in mouse bone. J Mech Behav Biomed Mater. 2014;39:38-47. [65] Carriero A, Zimmermann EA, Paluszny A, et al. How Tough Is Brittle Bone? Investigating Osteogenesis Imperfecta in Mouse Bone. J Bone Miner Res. 2014; 29(6):1392-1401. |
| [1] | Shi Bin, An Jing, Chen Long-gang, Zhang Nan, Tian Ye . Influencing factors for pain after total knee arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2017, 21(7): 993-997. |
| [2] | Wang Xian-xun. Impact of local compression cryotherapy combined with continuous passive motion on the early functional recovery after total knee arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2017, 21(7): 998-1003. |
| [3] | Yuan Wei, Zhao Hui, Ding Zhe-ru, Wu Yu-li, Wu Hai-shan, Qian Qi-rong. Association between psychological resilience and acute mental disorders after total knee arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2017, 21(7): 1015-1019. |
| [4] | Chen Qun-qun, Qiao Rong-qin, Duan Rui-qi, Hu Nian-hong, Li Zhao, Shao Min. Acu-Loc®2 volar distal radius bone plate system for repairing type C fracture of distal radius [J]. Chinese Journal of Tissue Engineering Research, 2017, 21(7): 1025-1030. |
| [5] | Huang Xiang-wang, Liu Hong-zhe. A new low elastic modulus of beta titanium alloy Ti2448 spinal pedicle screw fixation affects thoracic stability: biomechanical analysis [J]. Chinese Journal of Tissue Engineering Research, 2017, 21(7): 1031-1035. |
| [6] | Xie Qiang. Three-dimensional finite element model for biomechanical analysis of stress in knee inversion and external rotation after posterior cruciate ligament rupture [J]. Chinese Journal of Tissue Engineering Research, 2017, 21(7): 1036-1040. |
| [7] | He Ze-dong, Zhao Jing, Chen Liang-yu, Li Ke, Weng Jie. Multilevel finite element analysis on the biological tribology damage of water on bone tissue [J]. Chinese Journal of Tissue Engineering Research, 2017, 21(7): 1041-1045. |
| [8] | Li Jing, Yang Long, Wang Jian-ji, Liu Qin, Zou Qiang, Sun Yu, Ma Min-xian, Ye Chuan. Three-dimensional reconstruction based on DICOM data and its application for orthopedic implants [J]. Chinese Journal of Tissue Engineering Research, 2017, 21(7): 1046-1051. |
| [9] | Jiang Zi-wei, Huang Feng, Cheng Si-yuan, Zheng Xiao-hui, Sun Shi-dong, Zhao Jing-tao, Cong Hai-chen,Sun Han-qiao, Dong Hang. Design and finite element analysis of digital splint [J]. Chinese Journal of Tissue Engineering Research, 2017, 21(7): 1052-1056. |
| [10] | Wang Fei, Liu Zhi-bin, Tao Hui-ren, Zhang Jian-hua, Li Chang-hong, Cao Qiang, Zheng Jun, Liu Yan-xiong, Qu Xiao-peng. Clinical efficacy of preoperative osteotomy designs using paper-cut technology versus photoshop software for ankylosing spondylitis with kyphosis [J]. Chinese Journal of Tissue Engineering Research, 2017, 21(7): 1057-1063. |
| [11] | Li Hui, Ma Jun-yi, Ma Yuan, Zhu Xu . Establishment of a three-dimensional finite element model of ankylosing spondylitis kyphosis [J]. Chinese Journal of Tissue Engineering Research, 2017, 21(7): 1069-1073. |
| [12] | Ling Guan-han, Ou Zhi-xue, Yao Lan, Wen Li-chun, Wang Guo-xiang, Lin Heng-feng. Establishment of simulating three-dimensional model of China-Japan Friendship Hospital Classification for L type osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2017, 21(7): 1074-1079. |
| [13] | Fu Wei-min, Wang Ben-jie. Assessing the degree of necrotic femoral head, and association of blood supply with pathlogical changes: study protocol for a diagnostic animal trial [J]. Chinese Journal of Tissue Engineering Research, 2017, 21(7): 1086-1091. |
| [14] | Zhang Wen-qiang, Ding Qian, Zhang Na. Associations between alpha angle and herniation pit on oblique axial magnetic resonance imaging in asymptomatic hip joints of adults [J]. Chinese Journal of Tissue Engineering Research, 2017, 21(7): 1098-1103. |
| [15] | Sun Xiao-xin1, Zhou Wei2, Zuo Shu-ping3, Liu Hao1, Song Jing-feng1, Liang Chun-yu1. Morphological characteristics for the magnetic resonance imaging assessment of discoid lateral meniscal tears in children [J]. Chinese Journal of Tissue Engineering Research, 2017, 21(7): 1104-1109. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||