Chinese Journal of Tissue Engineering Research ›› 2022, Vol. 26 ›› Issue (27): 4393-4400.doi: 10.12307/2022.873
Previous Articles Next Articles
Latest research progress and application of bio-printing technology in tracheal tissue engineering
Pan Ziyin1, 2, 3 , Lu Yi1, 2, 3, Jin Liye3, Su Dingwen1, 2, Shi Hongcan1, 2, 3
- 1Department of Thoracic and Cardiovascular Surgery, Medical College of Yangzhou University, Yangzhou 225001, Jiangsu Province, China; 2Translational Medicine Research Center of Yangzhou University, Yangzhou 225001, Jiangsu Province, China; 3Key Laboratory of Integrative Medicine in Geriatrics Control of Jiangsu, Yangzhou 225001, Jiangsu Province, China
-
Received:2021-03-08Accepted:2021-04-15Online:2022-09-28Published:2022-03-12 -
Contact:Shi Hongcan, Chief physician, Doctoral supervisor, Department of Thoracic and Cardiovascular Surgery, Medical College of Yangzhou University, Yangzhou 225001, Jiangsu Province, China; Translational Medicine Research Center of Yangzhou University, Yangzhou 225001, Jiangsu Province, China; Key Laboratory of Integrative Medicine in Geriatrics Control of Jiangsu, Yangzhou 225001, Jiangsu Province, China -
About author:Pan Ziyin, Department of Thoracic and Cardiovascular Surgery, Medical College of Yangzhou University, Yangzhou 225001, Jiangsu Province, China; Translational Medicine Research Center of Yangzhou University, Yangzhou 225001, Jiangsu Province, China; Key Laboratory of Integrative Medicine in Geriatrics Control of Jiangsu, Yangzhou 225001, Jiangsu Province, China -
Supported by:the National Natural Science Foundation of China, No. 81770018 (to SHC); the Innovation and Entrepreneurship Training Program for College Students in Jiangsu Province, No. 201911117016Z (to PZY)
CLC Number:
Cite this article
Pan Ziyin , Lu Yi, Jin Liye, Su Dingwen, Shi Hongcan. Latest research progress and application of bio-printing technology in tracheal tissue engineering[J]. Chinese Journal of Tissue Engineering Research, 2022, 26(27): 4393-4400.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
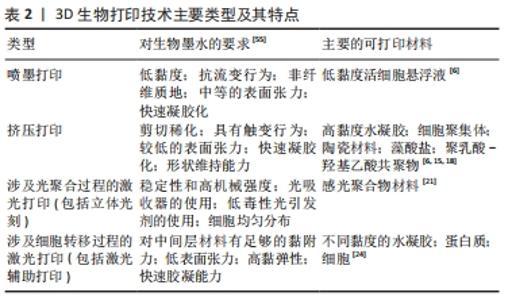
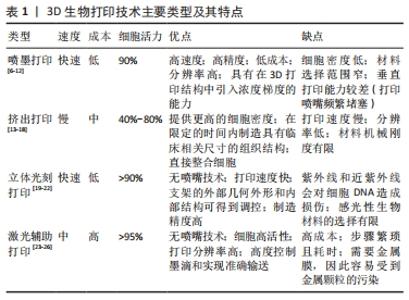
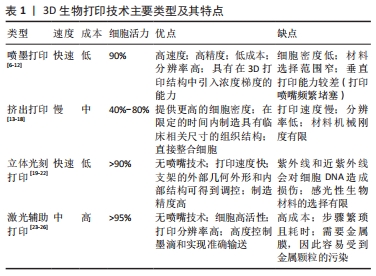
2.1.1 喷墨打印 喷墨打印是一种基于桌面喷墨打印机的原理而形成的打印工艺,这是一种非接触式印刷过程,在计算机控制下,通过压电或热驱动将生物墨水以精确微滴形式沉积到水凝胶基质或培养皿上。在压电液滴形成中,电压脉冲引起压力变化导致液滴形成;而在热驱动中,加热元件汽化生物材料并沉积液滴,墨滴的大小可以随墨水黏度和所施加的温度梯度而变化[7-8]。 喷墨打印可提供高达50 μm的高分辨率[9]。尽管在喷墨打印过程中强大的剪切力可能会破坏细胞,但在大部分情况下细胞活力能够得到保证。据报道,通过压电沉积的人成骨细胞、成纤维细胞和牛软骨细胞生存力超过90%[10-11]。此外,喷墨打印以其高速度、高精度著称,缺点主要为材料选择范围较窄和打印头频繁堵塞。GRAHAM研究小组[12]改良了现有的液滴打印法,构建绵羊间充质干细胞打印物,将其浸没在油滴中,随后封装在薄层凝胶中以便随后转移至含水介质中,结果显示在转化生长因子β3的诱导刺激下,间充质干细胞具有高活性、增殖能力及产生软骨样细胞外基质的能力。此外,在另一项创新性研究中对明胶进行了双重功能化,从而控制了生物墨水物化属性[13]。 2.1.2 挤出打印 挤出生物打印被认为是喷墨生物打印的进化,近年来应用广泛,主要得益于该技术操作的可预测性和可简化性。它使用气动或机械系统分配生物墨水,通过施加连续的压力将生物墨水以不间断的圆柱状细丝形式从喷嘴挤出,从而为打印产物提供了高度的结构完整性。目前有3个主要因素影响挤出打印的实际应用[14]:材料黏度的可调节性;挤压前的生物墨象;材料特定的生物加工窗口。 与喷墨打印相比,挤出打印能提供更高的细胞密度,但速度慢、分辨率低[15]。在该方法中,打印头通过气动压力和机械外力挤出材料,从而使得材料能够连续流动,以此达到简化操作的目的,并扩大了生物材料的选择范围,包括聚合物、脱细胞基质、载有细胞的水凝胶、球状体及细胞聚集体等[16]。目前的打印材料主要集中于高黏度水凝胶,效果较好。KUNDU等[17]选择藻酸盐水凝胶作为生物墨水,并证实其对软骨细胞活力的负性作用可忽略不计,解决了软骨细胞外基质形成与合成的难题。熔融沉积建模是一种基于挤出的3D打印技术,加热室内将热塑性聚合物加热至熔融状态,喷嘴将聚合物挤压喷射至平台,通过逐层沉积方法构建三维模型[18]。熔融沉积建模技术具有推动气管再生领域发展的潜能。有研究发现,使用四轴熔融沉积建模方法设计的3D打印气管具有可预定义的超微结构与相互连接的多孔结构,类似于天然组织;将该技术打印的聚己内酯支架植入新西兰兔体内修复缺损气管,结果显示该支架具有良好的机械性能,这种方法提高了患兔的气管修复效果[19]。 挤压打印法被认为是一种具有发展前景的技术,因其有望在限定的时间内制造适用于临床应用的组织工程气管。然而,生物材料及生物墨水浓度对于制造过程中细胞存活和功能的维持至关重要,需要后续进一步研究。 2.1.3 立体光刻打印 通过聚合过程,立体光刻技术可被用于稳固3D支架,通常是采用紫外线或电子束在层状/单体溶液上启动聚合链反应,一旦前一层完全稳固后,打印平台就会沿垂直方向(Z方向)降低一小段距离,开始打印下一层,重复步骤直至支架完成打印[20]。 与其他3D打印技术相比,立体光刻打印是一种具有高打印质量、高速度以及高细胞活力的技术。此外,立体光刻打印可同时打印多个对象且打印时间仅受结构厚度影响,显著减少了打印时间[21],提供了用最短的制造时间打印细胞装载结构的可能性,同时支架的外部几何外形和内部结构可以得到精确控制。该技术的局限性主要在于紫外线和近紫外线会对细胞DNA造成损伤,因此感光性聚合生物材料的选择十分有限。一些研究者已经针对此问题开始寻找优化方案,如使用光引发剂自由材料或可见光吸收光引发剂[5]。LAM等[22]运用甲基丙烯酸化水凝胶封装种子细胞,立体光刻打印后14 d细胞具有生物活性并向软骨细胞方向分化。因此可见在气管重建方案中,立体光刻打印与载细胞水凝胶的结合应得到更多关注。 2.1.4 激光辅助打印 激光辅助打印通常由三部分组成:脉冲激光源、涂有沉积在金属膜上的液态生物材料的色带及接收基 板[23]。激光辅助打印主要使用具有紫外线或近紫外线波长的激光作为能源,打印不同黏度水凝胶、细胞及蛋白质[24]。选择性激光烧结是一项激光辅助打印技术,在计算机辅助设计模型基础上逐层添加粉末材料来制造三维结构。激光束充当能量源,首先融化分布成粉末床形式的材料,再通过光束加热将其烧结成型[25]。选择性激光烧结技术目前已用于组织工程气管的构建,HAN等[26]采用选择性激光烧结技术制造自膨胀金属气管支气管支架,并将支架植入1例支气管软化患者的塌陷气管处,有效重建了气道。 虽然价格昂贵,但激光辅助打印技术具有其独特的优势,包括无需喷嘴、非接触式打印过程、细胞保持高活性、打印分辨率高、墨滴形状控制良好且输送准确等。 2.1.5 其他打印技术 3D打印领域中仍有许多技术在组织工程中的应用尚待探索,与上述介绍的技术相比,一些具有更高的分辨率,一些能够更好地将支架和细胞引入到打印过程中。与喷墨打印技术相似,Polyjet打印将光敏聚合物喷射到构建平台上,并同时利用紫外光源进行固化,与喷墨工艺不同的是,该技术可以同时喷射多种类型的材料并进行固化,能够制造复杂的多材质对象[27]。因此,可以认为具有多模块化强度的高分辨率气管可以尝试使用Polyjet技术以高空间精度进行3D打印。但该技术在3D打印领域还比较新颖,其可行性还需要得到时间的验证。除了Polyjet打印工艺,XU等[28]发现运用激光微孔技术制备的微孔脱细胞基质支架可以降低细胞外基质的损失,从而在原位条件下提供均匀的细胞分布和良好的移植物机械稳定性。除了直接打印技术,间接3D打印具有应用新颖胶原蛋白作为支架的能力,支持间充质干细胞在体外生长达4周,并且对种子细胞几乎没有细胞毒性。与购买3D打印机相比,间接3D打印可能是在实验室规模上制作组织工程支架的更有用且成本较低的替代方法[29]。 2.2 生物墨水 生物打印技术的重要组成部分是生物墨水,这对于器官功能和组织结构的优化至关重要。生物墨水需要具备良好的生物相容性、较高的孔隙率及匹配的机械性能[20]。目前已开发两种主要的生物墨水类型:支架型与无支架型,前者由细胞和生物材料组成,在打印过程中一起释放以构建组织,该结构主要起到组织支撑的作用,并营造一个适合细胞生长和分化的环境[30];后者特征为聚集细胞、组织链或球体,分泌细胞外基质样结构,将细胞组分紧密结合在一起[31]。基于支架的生物墨水当前的应用更为广泛且研究主要集中于对水凝胶和脱细胞基质的探索[32]。 2.2.1 生物墨水材料的主要分类 水凝胶:是目前性能最突出的一种3D生物打印生物墨水,具有聚合物链交联形成的三维网络结构,这种结构赋予其独特的溶胀性能与三维骨架。水凝胶参数可以用不同方式进行调节,以改善其在组织修复中的最终作用效果[10]。水凝胶墨水的流变行为对于挤出打印的帮助巨大,剪切稀化有利于控制挤出打印过程。水凝胶通常被分为三大类:天然水凝胶、合成水凝胶、改性水凝胶[33]。天然水凝胶主要来源包括丝素蛋白、胶原蛋白、透明质酸等,因为其固有的优良生物相容性、低毒性、对酶降解的易感性被广泛应用。除此以外,天然水凝胶能够更好地模拟细胞外基质的生物学特性,增强细胞附着力并更有效调节细胞增殖[34]。与天然水凝胶相比,合成水凝胶的机械性能能更精确地调节,获得更稳定的3D打印结构。在合成聚合物中,聚乙二醇是最常用的材料之一,已在3D打印中被应用与不同材料混合,以提高目标构建物的机械性能[33,35]。改性水凝胶通常通过对天然水凝胶某些官能团化学改性获得,该类水凝胶在保持天然水凝胶优良生物相容性的同时,兼具优异的光聚合性和可调节的机械性能。现广泛使用的改性水凝胶主要为甲基丙烯酸明胶[36]。 脱细胞基质:细胞外基质的作用是维持组织的三维结构及调节细胞行为。此外,细胞外基质可以作为诱导支架在组织受损后促进结构性重塑反应。脱细胞处理是一个严格的过程,因为即使是很小的宿主免疫反应也可能导致对移植物的排斥,这对于气道而言将是灾难性的。去污剂-联合酶法脱细胞处理能够有效去除气管抗原及细胞成分,保留与原生组织相似的主要结构特征,为细胞黏附、组织再生提供环境支持,同时可保留血管生成因子(如碱性成纤维细胞生长因子),对移植物体内血管再生具有重要意义[37]。SUN课题组[1]的一项研究结果表明,使用改良去污剂联合酶法处理的脱细胞兔气管基质,在结构和力学性能上均类似于天然气管,免疫原性也得到了有效降低。但在去污剂-联合酶法中脱细胞周期长,不适合紧急情况使用。此外,在脱细胞的过程中气管基质仍然存在着机械性能不稳定的问题[38]。BUTLER等[39]证实与去污剂-联合酶脱细胞处理法相比,真空辅助脱细胞法制备脱细胞气管基质只需9 d,这是一种加速方案。不仅如此,在研究中发现该脱细胞气管基质在抗压缩性和弹性方面可与天然气管相媲美。在过去几十年的时间里,除了上述两种脱细胞策略,研究人员还提出了多种包括物理、化学及生物酶等在内的适用于组织工程的脱细胞方案,金标准仍有待确定[40]。 无支架型生物墨水:虽然支架型生物墨水有种种得天独厚的优势,但在组织修复领域,无支架型生物墨水的打印方法逐渐引起了学者的关注。这种技术依赖于生物墨水的流动性和融合能力,通过细胞聚集体分泌的内源性细胞外基质稳定细胞功能,指导细胞通过相互作用进行自组装[41-42]。通过构建组织球体,大量细胞接种于微孔阵列中,细胞落入微孔的底部并彼此紧密接触,从而驱动细胞自发地相互黏附,将自由能降至最低,有利于新组织的形成。据报道,DIKINA团队[43]使用间充质干细胞衍生的软骨环加上定制的环-管组装系统形成的圆柱体成功构建自组装无支架组织工程气管,与大鼠原生气管相比,无支架气管显示出相似的生物力学性能,使大鼠气道保持通畅。传统的组织工程气管依赖于支架的存在,但存在一些缺陷,包括免疫原性、改变的细胞表型和修饰细胞之间的相互作用。由于无需细胞接种及外源体的植入,无支架组织工程方案可以在一定程度上规避了这些问题,弥补了传统方案的不足[2]。 2.2.2 生物墨水与打印产物的关键特征 孔隙率:材料的孔隙率和互联性对于细胞培养有着举足轻重的作用[44],它影响营养因子的输送与氧气的扩散,几乎决定了在组织工程微环境中能否产生微血管网络及重建组织能否得到充足的血供。原始材料一般不具备组织工程所需的孔隙率,为了解决这一问题,研究人员需要微调孔隙大小以实现重建组织功能的最大化。 已有研究证实,藻酸盐多孔泡沫支架支持间充质干细胞的增殖与分泌功能[45]。PAN等[46]利用3D打印制备了一种改性聚己内酯多孔气管支架,证明200 μm的孔径最有利于骨髓间充质干细胞的黏附。支架表面经纳米二氧化硅修饰改性后,细胞趋向性提高。PARK等[47]构建了一种新型的多层3D打印气管支架,共有聚己内酯材料3层,内层与外层材料带有网格状孔隙,中间层为无孔柱状,在每一层聚己内酯之间,研究团队分别利用海藻酸盐水凝胶包封家兔的自体鼻腔上皮细胞与耳郭软骨细胞;为了评价该组织工程气管的体内治疗效果,构建家兔气管部分切除模型,观察周期长达1年,结果显示一共15只家兔中有13只存活,组织学检查显示呼吸上皮细胞的再生,但软骨再生所需时间过长。该研究首次提供了一个适用于多种不同类型细胞与相适水凝胶材料结合运用以修复气管长段缺损的平台。 机械性能:水凝胶和脱细胞基质均能为3D打印结构提供卓越的机械支持,该特性在组织工程气管中尤为重要。气管C形软骨主要由透明软骨组成,在确保呼吸道通气和防止管腔塌陷中发挥巨大作用。水凝胶的机械和结构性能取决于其材料类型和浓度。较低的浓度虽然更能支持种子细胞的增殖生长,但显示出较差的机械性能。交联是一种改变生物墨水打印产物机械性能的方法,主要有两种形式:物理交联和化学交联[41]。物理交联是利用疏水相互作用、离子相互作用和氢键的非化学方法,将化学污染或化学诱导的风险降到最低。化学交联依赖于共价键的形成,与物理交联相比,化学交联后的水凝胶具有机械性能更为优异的网络结构。DAS等[48]利用酪氨酸酶交联丝素蛋白明胶水凝胶,观察到骨髓间充质干细胞能向软骨细胞分化。Pluronic是一种基于泊洛沙姆的三嵌段共聚物,在室温下容易凝胶化,但在低于10 ℃环境下具有流动性,已被广泛应用于挤出打印技术。KWON等[49]将Pluronic F-127与聚己内酯交联,设计出一种带有不对称多孔膜的气管假体,并在新西兰兔体内进行原位移植,12周后内窥镜检查未发现肉芽组织向气管腔内生长,CT扫描显示气道维护良好。京尼平是一种极好的低毒性和可生物降解的天然生物交联剂。ZHONG等[50]的一项研究显示,经去污剂-联合酶法脱细胞处理的气管基质经京尼平交联后,管腔的机械性能得到了保证,可能是由于京尼平可与氨基酸链或蛋白质反应可诱导分子内和分子间胶原环状化合物的交联,从而防止了气管支架被宿主降解酶(例如胶原酶和结缔组织蛋白酶)破坏[51-52]。 与3D打印技术的兼容性:尽管生物墨水材料种类多样,包括水凝胶、细胞外基质、细胞聚集体等,但是并非所有3D打印方式都与每种生物墨水材料兼容。总体来说,挤出打印具有最大的灵活性,可以推动水凝胶、细胞聚集体(球状、链状、细胞沉淀形式)、细胞外基质组分等介质在组织工程领域的运用,这归因于其挤出机制及较大的喷嘴直径。其余3D打印技术(包括喷墨及激光辅助3D打印)需要的打印材料较为局限[53]。喷墨打印技术由于喷嘴直径小,无支架型生物墨水的打印具挑战性,喷嘴尖端容易堵塞并且不支持液滴的形成[54]。而细胞聚集体、细胞外基质尚不能用于激光打印[55]。考虑材料特性时,可打印性是最重要的参数,其中黏度是生物墨水配方的最关键参数,直接影响打印保真度和细胞封装效率,因此应优先选择可调节黏度的生物墨水制剂,以与不同的生物打印技术相适配。在喷墨打印中,生物墨水的黏度要求接近10 mPa·s,而挤出与激光辅助打印生物墨水黏度的范围分别为30 mPa·s-6×107 mPa·s,1-300 mPa·s[41]。不同打印技术对生物墨水的性质要求见表2。"


2.3 4D打印技术 由智能生物材料合成的组织结构,受到微环境中存在的不同刺激(湿度、温度或化学物质)时催化自身转化为预定的形状或执行预定功能的过程被视为4D打印,4D打印成功将“时间与动态”的概念引入到了常规的3D打印技术中[56-57]。4D打印的两大重要特点为“形状记忆”和“自我激活”。与传统的3D打印技术相比,4D打印具有如下优势:制作过程中在暴露于特定刺激后,打印产物的形状或功能能够进行改变;具有材料可编程性。 影响4D打印的5个主要因素是[58]:增材制造技术的类型;相应材料的选择;外界刺激的类型;各因素之间的相互作用机制;物质转化的数学模型。与3D打印相同,许多常用的增材制造技术例如熔融沉积建模、立体光刻、选择性激光烧结等也适用于4D打印应用[59]。 4D打印中最重要的元素是响应材料,当前运用最为广泛的是形状记忆聚合物,具有较强的刚度及对刺激的快速反应性,在受到外部刺激后会产生较大的形状变化。形状记忆聚合物主要分为3类,热响应型、光响应性及化学响应型。温度响应聚合物是4D打印技术在组织工程及个性化医疗领域最常用的材料之一,利用人体温度37 ℃触发某些材料的期望响应,提供对生物支架形状和结构的极端控制。形状记忆聚合物受刺激后所产生的动态变化吸引了学者极大关注。已有研究使用紫外发光二极管数字光处理打印机,以聚己内酯和二甲基丙烯酸酯为生物墨水打印出了一种形状记忆热固性气管支架,首先在初始温度下变形为临时形状,植入人体后随着局部温度的升高调整为一种契合周边组织的永久形状。该4D打印支架成功解决了目前气管支架所面临的两个关键缺陷:首先,这种基于定制结构的设计方法将减轻人工气管移位的状况;此外,通过缩放数字模型可以缩小形状记忆聚合物结构的轮廓,从而减少植入支架对人体的损伤[60-61]。 为了获得针对特定应用的4D打印效果,研究人员通常使用理论模型与数值模型,这些模型通过在材料、外界刺激和所需的最终打印结构之间建立联系,帮助预测适当的刺激暴露顺序及结构变化所需时间。通过有限元分析及模型的帮助,目标4D打印产物结构中的材料分布、不同的材料特性、几何形状的变化情况可以得到预测[58]。 关于4D打印技术的一大争论是3D打印结构逐渐降解退化是否可以归类为时间依赖的4D效应。现在普遍认为如果生物降解过程是可编程的、具有时间依赖性,那么由生物可降解材料制造的支架应属于4D打印。对于组织工程气管,支架的可降解性是一个关键因素,其降解速率与组织再生速率应相匹配以防止气管管腔塌陷。4D打印技术的出现意味着支架性能的不断提升,未来能够以一种定制的方式修复长段气管缺损[62]。FAN等[63]运用选择性激光烧结技术制造3D打印生物可吸收支架,植入到严重支气管软化症猪模型中观察到症状明显缓解,随着时间延长支架逐渐被吸收,这一现象被认为是4D功能的展现。除了动物实验,MORRISON团队[64]以聚己内酯为材料在支气管软化患儿体内植入定制气道夹板,基于图像设计与生物材料集成的方法,该夹板随着时间的推移表现出形状变化(扩张或退化),以适应气道大小的变化和顺应支气管树的生长情况,这是一种典型的4D效应,为临床气管重建带来了曙光。 2.4 生物打印技术在组织工程气管领域的针对性研究 气管替代治疗的主要目标是:①生成具有天然气管生物力学性能的结构;②支持功能性黏膜的生长;③快速血管重建以确保细胞存活。软骨细胞和上皮细胞是组织工程气管必需的两种细胞类型。软骨细胞构成软骨环,为结构提供支撑,防止管腔塌陷;气道内壁覆有上皮组织,作为抵抗感染的屏障,防止瘢痕的形成。除此以外,建立血液供应对于组织工程气管的成功移植同样是必不可少的,以此方式允许移植微环境向种子细胞和天然内源细胞提供营养[65-66]。生物打印技术在这三方面的针对性研究皆已取得进展。 2.4.1 组织工程气管再上皮化 气管上皮细胞主要由基底膜及杯状细胞上的纤毛柱状上皮构成。杯状细胞产生黏液,纤毛上皮作为抵抗感染的物理屏障调节气道代谢功能。然而,上皮细胞的再生十分缓慢,必须经历4个过程:迁移到正确的部位、细胞对材料表面的黏附、细胞增殖、分化为成熟的细胞类型[67]。感染是导致气管长短缺损修复失败的一项重要因素[68],设计并使用理想的封闭性生物反应器已被证实能够有效杀菌、降低感染风险[66]。除此以外,移植物再上皮化对于组织工程气管抗感染具有重大意义,GO等[69]在猪模型中观察到未接种上皮细胞的气管构建体内表面发生了严重细菌和真菌感染。如今组织工程气管再上皮化的策略主要有2种,首先考虑直接通过移植种子细胞来介导上皮再生,其次选择将接种细胞作为生物敷料,提供屏障功能和信号以增强局部再生[65]。随着3D打印技术发展,组织工程在上皮再生方面取得了进展。CHANG等[70]在半环形3D打印聚己内酯支架上涂覆有包裹间充质干细胞的纤维蛋白,构建兔气管局部缺损模型,术后8周扫描电镜检查证实人工气管管壁纤毛再生,且摆动频率与邻近正常组织黏膜表面纤毛并无差异。REHMANI等[71]整合了CT成像和CAD建模,以临床相关规模和速度打印适合于受体的气管移植物,移植物表面实现再上皮化,且新生上皮功能得到证实。 2.4.2 组织工程气管软骨再生 气管中的C形软骨环主要由透明软骨组成,提供机械强度。与其他结缔组织不同,软骨无血管支持,正是由于这种性质,软骨再生能力极弱[72]。间充质干细胞具有分化为多种细胞谱系的能力,包括软骨细胞;应用生物打印技术能够对气管支架进行个性化设计,因此若将两者有机结合,有望克服气管重建中软骨再生的问题。GHORBANI等[73]通过3D打印制作聚己内酯/胶原蛋白支架,并将其插入脱细胞主动脉,在组织工程气管复合体最外层接种初级软骨细胞与脂肪来源间充质干细胞,最后异位植入新西兰兔中,观察结果显示该植入气管具有合适的管型形状、较强的机械性能和生物相容性。同时,PARK研究组[74]开发了一种新概念气管替代物,模仿天然气管的机械性能、径向强度、灵活性和管腔通畅性,通过3D打印制备中空波纹管结构的聚L-丙交酯-己内酯支架,在波纹管支架凹槽中装载有经功能化处理、持续释放转化生长因子β1的明胶海绵,从而增强了软骨再生。明胶海绵在体内具有持续降解的特性,能在软骨组织逐渐形成的过程中作为替代,提供适当强度的气管机械支持。 2.4.3 组织工程气管血运重建 血液供应是组织工程成功的另一关键因素。血管生成对于预防移植物坏死、协助神经支配、改善移植物功能至关重要。血管化问题是制约气管组织工程发展的主要因素之一,对于气管重建来说,血管生成能够支持管腔黏膜的生长,从而实现再上皮化[75]。3D打印将工程学与生物学各自的优势结合,为在体外复制血管网络提供了强有力的手段,从而在定位内皮细胞以诱导血管生成方面显示出令人鼓舞的结果。WU等[76]制造预血管化双层管状生物合成结构,该结构由聚乳酸-聚己内酯-胶原纤维组成,实验中将软骨细胞和上皮细胞包裹在气管筋膜内进行组织预血管化,并将其原位移植至小鼠气管缺损处进行生物相容性评估,结果表明移植物的微孔结构可实现更好的细胞增殖,促进移植前新血管形成;用预血管移植物治疗的气管缺损能有效减少免疫原性反应,形成新生毛细血管网并促进气管组织再生。另外,在3D打印过程中使用生物活性墨水可以指导细胞行为,从而促进整个组织构建体中微脉管系统的形成[43]。LI等[77]将丝素蛋白以水凝胶的形式注入大鼠后肢及背部皮下,术后20 d内运用多模超声技术持续探测丝素蛋白植入物表面新血管形成情况,结果证明,浓度为4%的丝素蛋白植入大鼠皮下后的第18-20天与周围微血管一并形成新生血管。3D打印的另一价值在于引入了生长因子的概念,对于组织工程气管血管化起到关键作用。WANG等[78]制备了聚己内酯/明胶3D支架,通过肝素固定为血管内皮生长因子提供结合位点,最终支架能够持续释放该生长因子,加速血管化进程。除去血管内皮生长因子,血小板衍生生长因子、碱性成纤维细胞生长因子均被证实能诱导新生血管形成[29,79]。"

| [1] SUN F, PAN S, SHI HC, et al. Structural integrity, immunogenicity and biomechanical evaluation of rabbit decelluarized tracheal matrix. J Biomed Mater Res A. 2015;103(4):1509-1519. [2] CHIANG T, PEPPER V, BEST C, et al. Clinical Translation of Tissue Engineered Trachea Grafts. Ann Otol Rhinol Laryngol. 2016;125(11): 873-885. [3] UDELSMAN B, MATHISEN DJ, OTT HC. A reassessment of tracheal substitutes-a systematic review. Ann Cardiothorac Surg. 2018;7(2): 175-182. [4] MACCHIARINI P, JUNGEBLUTH P, GO T, et al. Clinical transplantation of a tissue-engineered airway. Lancet. 2008;372(9655):2023-2030. [5] KACAREVIC ZP, RIDER PM, ALKILDANI S, et al. An Introduction to 3D Bioprinting: Possibilities, Challenges and Future Aspects. Materials (Basel). 2018;11(11):2199. [6] CHU H, YANG W, SUN L, et al. 4D Printing: A Review on Recent Progresses. Micromachines (Basel). 2020;11(9):796. [7] LI J, CHEN M, FAN X, et al. Recent advances in bioprinting techniques: approaches, applications and future prospects. J Transl Med. 2016;14:271. [8] JAMMALAMADAKA U, TAPPA K. Recent Advances in Biomaterials for 3D Printing and Tissue Engineering. J Funct Biomater. 2018;9(1):22. [9] MANDRYCKY C, WANG Z, KIM K, et al. 3D bioprinting for engineering complex tissues. Biotechnol Adv. 2016;34(4):422-434. [10] BOLAND T, XU T, DAMON B, et al. Application of inkjet printing to tissue engineering. Biotechnol J. 2006;1(9):910-917. [11] VEGA SL, KWON MY, BURDICK JA. Recent advances in hydrogels for cartilage tissue engineering. Eur Cell Mater. 2017;33:59-75. [12] GRAHAM AD, OLOF SN, BURKE MJ, et al. High-Resolution Patterned Cellular Constructs by Droplet-Based 3D Printing. Sci Rep. 2017;7(1): 7004. [13] HOCH E, HIRTH T, TOVAR GEM, et al. Chemical tailoring of gelatin to adjust its chemical and physical properties for functional bioprinting. J Mater Chem B. 2013;1(41):5675-5685. [14] HE Y, YANG F, ZHAO H, et al. Research on the printability of hydrogels in 3D bioprinting. Sci Rep. 2016;6:29977. [15] HöLZL K, LIN S, TYTGAT L, et al. Bioink properties before, during and after 3D bioprinting. Biofabrication. 2016;8(3):032002. [16] CUI H, NOWICKI M, FISHER JP, et al. 3D Bioprinting for Organ Regeneration. Adv Healthc Mater. 2017;6(1):10. [17] KUNDU J, SHIM JH, JANG J, et al. An additive manufacturing-based PCL-alginate-chondrocyte bioprinted scaffold for cartilage tissue engineering. J Tissue Eng Regen Med. 2015;9(11):1286-1297. [18] XU N, YE X, WEI D, et al. 3D artificial bones for bone repair prepared by computed tomography-guided fused deposition modeling for bone repair. ACS Appl Mater Interfaces. 2014;6(17):14952-14963. [19] PARK HS, PARK HJ, LEE J, et al. A 4-Axis Technique for Three-Dimensional Printing of an Artificial Trachea. Tissue Eng Regen Med. 2018;15(4): 415-425. [20] WANG Y, GAO M, WANG D, et al. Nanoscale 3D Bioprinting for Osseous Tissue Manufacturing. Int J Nanomedicine. 2020;15:215-226. [21] WANG Z, ANDULLA R, PARKER B, et al. A Simple and High-Resolution Stereolithography-Based 3D Bioprinting System Using Visible Light Crosslinkable Bioinks. Biofabrication. 2015;7(4):045009. [22] LAM T, DEHNE T, KRTGER JP, et al. Photopolymerizable gelatin and hyaluronic acid for stereolithographic 3D bioprinting of tissue-engineered cartilage. J Biomed Mater Res B Appl Biomater. 2019; 107(8):2649-2657. [23] JANA S, LERMAN A. Bioprinting a cardiac valve. Biotechnol Adv. 2015; 33(8):1503-1521. [24] CATROS S, FRICAIN JC, GUILLOTIN B, et al. Laser-assisted bioprinting for creating on-demand patterns of human osteoprogenitor cells and nano-hydroxyapatite. Biofabrication. 2011;3(2):025001. [25] LI Z, ZHOU W, YANG L, et al. Glass Fiber-Reinforced Phenol Formaldehyde Resin-Based Electrical Insulating Composites Fabricated by Selective Laser. Polymers (Basel). 2019;11(1):e135. [26] HAN Y, YANG S, HUANG W, et al. A Hem-o-Lok-Induced Tracheoesophageal Fistula Cured by Temporary Airway Stenting Modified With Three-Dimensional Printing. Ann Thorac Surg. 2018; 106(4):e219-e221. [27] TAPPA K, JAMMALAMADAKA U. Novel Biomaterials Used in Medical 3D Printing Techniques. J Funct Biomater. 2018;9(1):17. [28] XU Y, LI D, YIN Z, et al. Tissue-engineered trachea regeneration using decellularized trachea matrix treated with laser micropore technique. Acta Biomater. 2017;58:113-121. [29] DO AV, KHORSAND B, GEARY SM, et al. 3D Printing of Scaffolds for Tissue Regeneration Applications. Adv Healthc Mater. 2015;4(12): 1742-1762. [30] ROSETI L, PARISI V, PETRETTA M, et al. Scaffolds for Bone Tissue Engineering: State of the art and new perspectives. Mater Sci Eng C Mater Biol Appl. 2017;78:1246-1262. [31] GRUENE M, DEIWICK A, KOCH L, et al. Laser printing of stem cells for biofabrication of scaffold-free autologous grafts. Tissue Eng Part C Methods. 2011;17(1):79-87. [32] ROSETI L, CAVALLO C, DESANDO G, et al. Three-Dimensional Bioprinting of Cartilage by the Use of Stem Cells: A Strategy to Improve Regeneration. Materials (Basel). 2018;11(9):1749. [33] YOU S, LI J, ZHU W, et al. Nanoscale 3D printing of hydrogels for cellular tissue engineering. J Mater Chem B. 2018;6(15):2187-2197. [34] GOPINATHAN J, NOH I. Recent trends in bioinks for 3D printing. Biomater Res. 2018;22:11. [35] HOCKADAY LA, KANG KH, COLANGELO NW, et al. Rapid 3D printing of anatomically accurate and mechanically heterogeneous aortic valve hydrogel scaffolds. Biofabrication. 2012;4(3):035005. [36] ZHU W, QU X, ZHU J, et al. Direct 3D bioprinting of prevascularized tissue constructs with complex microarchitecture. Biomaterials. 2017; 124:106-115. [37] BAIGUERA S, JUNGEBLUTH P, BURNS A, et al. Tissue engineered human tracheas for in vivo implantation. Biomaterials. 2010;31(34):8931-8938. [38] HAYKAL S, SOLEAS JP, SALNA M, et al. Evaluation of the structural integrity and extracellular matrix components of tracheal allografts following cyclical decellularization techniques: comparison of three protocols. Tissue Eng Part C Methods. 2012;18(8):614-23. [39] BUTLER CR, HYNDS RE, CROWLEY C, et al. Vacuum-assisted decellularization: an accelerated protocol to generate tissue-engineered human tracheal scaffolds. Biomaterials. 2017;124:95-105. [40] FISHMAN JM, WILES K, LOWDELL MW, et al. Airway tissue engineering: an update. Expert Opin Biol Ther. 2014;14(10):1477-1491. [41] JI S, GUVENDIREN M. Recent Advances in Bioink Design for 3D Bioprinting of Tissues and Organs. Front Bioeng Biotechnol. 2017;5:23. [42] RICHARDS D, JIA J, YOST M, et al. 3D Bioprinting for Vascularized Tissue Fabrication. Ann Biomed Eng. 2017;45(1):132-147. [43] DIKINA AD, STROBEL HA, LAI BP, et al. Engineered cartilaginous tubes for tracheal tissue replacement via self-assembly and fusion of human mesenchymal stem cell constructs. Biomaterials. 2015;52:452-462. [44] FAN D, STAUFER U, ACCARDO A. Engineered 3D Polymer and Hydrogel Microenvironments for Cell Culture Applications. Bioengineering (Basel). 2019;6(4):113. [45] Ceccaldi C, Bushkalova R, Cussac D, et al. Elaboration and evaluation of alginate foam scaffolds for soft tissue engineering. Int J Pharm. 2017; 524(1-2):433-442. [46] PAN S, ZHONG Y, SHAN Y, et al. Selection of the optimum 3D-printed pore and the surface modification techniques for tissue engineering tracheal scaffold in vivo reconstruction. J Biomed Mater Res A. 2019; 107(2):360-370. [47] PARK JH, YOON JK, LEE JB, et al. Experimental Tracheal Replacement Using 3-dimensional Bioprinted Artificial Trachea with Autologous Epithelial Cells and Chondrocytes. Sci Rep. 2019;9(1):2103. [48] DAS S, PATI F, CHOI YJ, et al. Bioprintable, cell-laden silk fibroin-gelatin hydrogel supporting multilineage differentiation of stem cells for fabrication of three-dimensional tissue constructs. Acta Biomater. 2015;11:233-246. [49] KWON SK, SONG JJ, CHO CG, et al. Tracheal reconstruction with asymmetrically porous polycaprolactone/pluronic F127 membranes. Head Neck. 2014;36(5):643-651. [50] ZHONG Y, YANG W, PAN Z, et al. In vivo transplantation of stem cells with a genipin linked scaffold for tracheal construction. J Biomater Appl. 2019;34(1):47-60. [51] ORYAN A, KAMALI A, MOSHIRI A, et al. Chemical crosslinking of biopolymeric scaffolds: Current knowledge and future directions of crosslinked engineered bone scaffolds. Int J Biol Macromol. 2018; 107(Pt A):678-688. [52] MUZZARElLLI RA, EL MEHTEDI M, BOTTEGONI C, et al. Genipin-Crosslinked Chitosan Gels and Scaffolds for Tissue Engineering and Regeneration of Cartilage and Bone. Mar Drugs. 2015;13(12):7314-7338. [53] OZBOLAT IT, HOSPODIUK M. Current advances and future perspectives in extrusion-based bioprinting. Biomaterials. 2016;76:321-343. [54] GUDAPATI H, DEY M, OZBOLAT I. A comprehensive review on droplet-based bioprinting: Past, present and future. Biomaterials. 2016;102: 20-42. [55] HOSPODIUK M, DEY M, SOSNOSKI D, et al. The bioink: A comprehensive review on bioprintable materials. Biotechnol Adv. 2017;35(2):217-239. [56] SUN YC, WAN Y, NAM R, et al. 4D-printed hybrids with localized shape memory behaviour: Implementation in a functionally graded structure. Sci Rep. 2019;9(1):18754. [57] QASIM M, CHAE DS, LEE NY. Advancements and frontiers in nano-based 3D and 4D scaffolds for bone and cartilage tissue engineering. Int J Nanomedicine. 2019;14:4333-4351. [58] TAMAY DG, USAL DT, ALAGOZ AS, et al. 3D and 4D Printing of Polymers for Tissue Engineering Applications. Front Bioeng Biotechnol. 2019;7: 164. [59] CHU H, YANG W, SUN L, et al. 4D Printing: A Review on Recent Progresses. Micromachines (Basel). 2020;11(9):796. [60] MIAO S, CASTRO N, NOWICKI M, et al. 4D printing of polymeric materials for tissue and organ regeneration. Mater Today (Kidlington). 2017;20(10):577-591. [61] ZAREK M, MANSOUR N, SHAPIRA S, et al. 4D Printing of Shape Memory-Based Personalized Endoluminal Medical Devices. Macromol Rapid Commu. 2017;38(2). doi: 10.1002/marc.201600628. [62] BOGAN SL, TEOH GZ, BIRCHALL MA. Tissue Engineered Airways: A Prospects Article. J Cell Biochem. 2016;117(7):1497-1505. [63] FAN D, LI Y, WANG X, et al. Progressive 3D Printing Technology and Its Application in Medical Materials. Front Pharmacol. 2020;11:122. [64] MORRISON RJ, HOLLISTER SJ, NIEDNER MF, et al. Mitigation of tracheobronchomalacia with 3D-printed personalized medical devices in pediatric patients. Sci Transl Med. 2015;7(285):285ra64. [65] MAUGHAN EF, HYNDS RE, PROCTOR TJ, et al. Autologous Cell Seeding in Tracheal Tissue Engineering. Curr Stem Cell Rep. 2017;3(4):279-289. [66] CROWLEY C, BIRCHALL M, SEIFALIAN AM. Trachea transplantation: from laboratory to patient. J Tissue Eng Regen Med. 2015;9(4):357-367. [67] PEPPER V, BEST CA, BUCKLEY K, et al. Factors Influencing Poor Outcomes in Synthetic Tissue-Engineered Tracheal Replacement. Otolaryngol Head Neck Surg. 2019;161(3):458-467. [68] GO T, JUNGEBLUTH P, BAIGUERO S, et al. Both epithelial cells and mesenchymal stem cell-derived chondrocytes contribute to the survival of tissue-engineered airway transplants in pigs. J Thorac Cardiovasc Surg. 2010;139(2):437-443. [69] SAKSENA R, GAO C, WICOX M, et al. Tubular organ epithelialisation. J Tissue Eng. 2016;7:2041731416683950. [70] CHANG JW, PARK SA, PARK JK, et al. Tissue-engineered tracheal reconstruction using three-dimensionally printed artificial tracheal graft: preliminary report. Artif Organs. 2014;38(6):E95-E105. [71] REHMANI SS, AL-AYOUBI AM, AYUB A, et al. Three-Dimensional-Printed Bioengineered Tracheal Grafts: Preclinical Results and Potential for Human Use. Ann Thorac Surg. 2017;104(3):998-1004. [72] RAGHUNATH J, ROLLO J, SALES KM, et al. Biomaterials and scaffold design: key to tissue-engineering cartilage. Biotechnol Appl Biochem. 2007;46(Pt 2):73-84. [73] GHORBANI F, MORADI L, SHADMEHR MB, et al. In-vivo characterization of a 3D hybrid scaffold based on PCL/decellularized aorta for tracheal tissue engineering. Mater Sci Eng C Mater Biol Appl. 2017;81:74-83. [74] PARK JH, HONG JM, JU YM, et al. A novel tissue-engineered trachea with a mechanical behavior similar to native trachea. Biomaterials. 2015;62:106-115. [75] HAMILTON N, BULLOCK AJ, MACNEIL S, et al. Tissue engineering airway mucosa: a systematic review. Laryngoscope. 2014;124(4):961-968. [76] WU T , ZHENG H , CHEN J , et al. Application of a bilayer tubular scaffold based on electrospun poly(l-lactide-co-caprolactone)/collagen fibers and yarns for tracheal tissue engineering. J Mater Chem B. 2017; 5(1):139-150. [77] LI S, YU D, JI H, et al. In vivo degradation and neovascularization of silk fibroin implants monitored by multiple modes ultrasound for surgical applications. Biomed Eng Online. 2018;17(1):87. [78] WANG K, CHEN X, PAN Y, et al. Enhanced vascularization in hybrid PCL/gelatin fibrous scaffolds with sustained release of VEGF. Biomed Res Int. 2015;2015:865076. [79] LIU Q, HUANG Y, LAN Y, et al. Acceleration of skin regeneration in full-thickness burns by incorporation of bFGF-loaded alginate microspheres into a CMCS-PVA hydrogel. J Tissue Eng Regen Med. 2017;11(5):1562-1573. |
| [1] | Zhang Haobo, Zhao Yunan, Yang Xuejun. Role and therapeutic implications of pyroptosis in intervertebral disc degeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1445-1451. |
| [2] | Song Yuxin, Zhang Tongtong, Niu Jianxiong, Wang Zengping, Wen Jie, Zhang Qunli, Xue Wen, Liu Lin. Precise screw placement of 3D printing model and orthopedic robot in spinal deformity [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 904-907. |
| [3] | Wang Ruanbin, Cheng Liqian, Chen Kai. Application and value of polymer materials in three-dimensional printing biological bones and scaffolds [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 610-616. |
| [4] | Chen Xiaoxu, Luo Yaxin, Bi Haoran, Yang Kun. Preparation and application of acellular scaffold in tissue engineering and regenerative medicine [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 591-596. |
| [5] | Song Yan, Zheng Kun, Wei Haoxin, Lu Dezhi, Xu Yuanjing, Wang Xiaowen, Wang Jinwu. reliability of flat feet evaluated by foot posture index and its application in three-dimensional printing insoles [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(3): 344-349. |
| [6] | Maihemuti•Yakufu, Sun Qinqin, Chen Hongtao, Liu Xu, Yiliyaer•Abudusimu, Abudushalamu•Abudukelimu, Liu Jianjiang. Tension of 3D printed controllable tension band and skin regeneration of skin defect model rats [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(3): 371-375. |
| [7] | Li Lu, Tang Wen. Screw placement in posterior route pedicle on subaxial cervical spine: how to improve the therapeutic effect with the development of artificial intelligence [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(3): 474-479. |
| [8] | Wu Haineng, Geng Kang, Wang Jing, Xiong Aibing. Platelet-rich fibrin combined with curcumin nanoparticle hydrogel promotes wound healing in diabetic mice [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(27): 4300-4307. |
| [9] | Dong Liping, Luo Jia, Li Guangyi, Yuan Heng. Effect of aging on the ultrastructure of common iliac artery in rats [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(26): 4123-4126. |
| [10] | Jin Herong, Cui Jingbin, Shao Cang. Materials of interbody fusion cage: advantages and focus of clinical application [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(22): 3592-3597. |
| [11] | Meng Lulu, Liu Hao, Liu Han, Zhang Jun, Li Ruixin, Gao Lilan. Mechanical properties of silk fibroin/type I collagen/hydroxyapatite scaffolds based on low-temperature 3D printing [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(22): 3550-3555. |
| [12] | Zhang Chunyu, Hu Baoyang, Feng Yao, Zhang Wanfen, Sun Leiye, Yang Yan. Performance optimization of a new type of calcium silicate (based) scaffold matched with bone tissue regeneration in the bone defect area [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(21): 3421-3428. |
| [13] | Wang Kun, He Benxiang. Asperosaponin VI therapy for Achilles tendinopathy in rabbits [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(2): 211-217. |
| [14] | Wang Sizhe, Gao Kunfan, Xu Zhenzhen, Gao Haiyan, Huang Haoran, Dai Shiyou, Ma Jianlin, Wang Feng. 3D printing technology assisted traditional plate fixation for the treatment of complex tibial plateau fractures [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(18): 2823-2827. |
| [15] | Li Yaoming, Jiang Hong, Shi Yongfang. Preparation and characterization of chitosan/polylactic acid/hydroxyapatite/polyvinyl alcohol composite bone scaffold [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(18): 2888-2893. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||