Chinese Journal of Tissue Engineering Research ›› 2022, Vol. 26 ›› Issue (14): 2273-2278.doi: 10.12307/2022.494
Previous Articles Next Articles
Advances in animal models of pulmonary fibrosis induced by biotic and abiotic factors
Guo Qiqi1, Li Yi1, Weng Huanze1, Wang Qian2, Jia Min1, 2
- 1Institute of Basic and Translational Medicine, Xi’an Medical University, Xi’an 710021, Shaanxi Province, China; 2Department of Physiology, Institute of Basic Medicine Science, Xi’an Medical University, Xi’an 710021, Shaanxi Province, China
-
Received:2021-03-22Revised:2021-03-31Accepted:2021-06-15Online:2022-05-18Published:2021-12-22 -
Contact:Jia Min, MD, Associate professor, Institute of Basic and Translational Medicine, Xi’an Medical University, Xi’an 710021, Shaanxi Province, China; Department of Physiology, Institute of Basic Medicine Science, Xi’an Medical University, Xi’an 710021, Shaanxi Province, China -
About author:Guo Qiqi, Institute of Basic and Translational Medicine, Xi’an Medical University, Xi’an 710021, Shaanxi Province, China -
Supported by:Shaanxi Provincial Science and Technology Innovation Base-Science and Technology Resource Open Sharing Platform Project, No. 2019PT-26 (to CYL); Shaanxi Provincial Natural Science Basic Research Program, No. 2020JM-609 (to WQ); Doctoral Research Startup Fund of Xi'an Medical University, No. 2020DOC23 (to JM)
CLC Number:
Cite this article
Guo Qiqi, Li Yi, Weng Huanze, Wang Qian, Jia Min. Advances in animal models of pulmonary fibrosis induced by biotic and abiotic factors[J]. Chinese Journal of Tissue Engineering Research, 2022, 26(14): 2273-2278.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

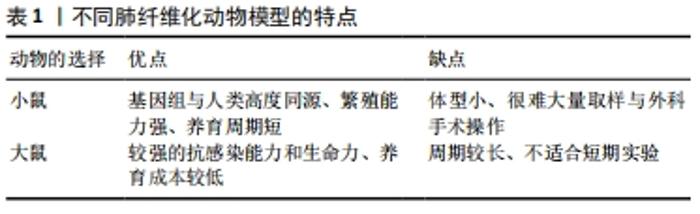
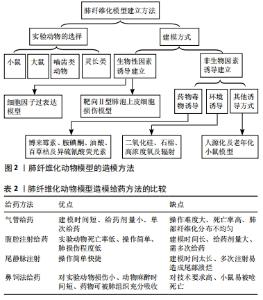
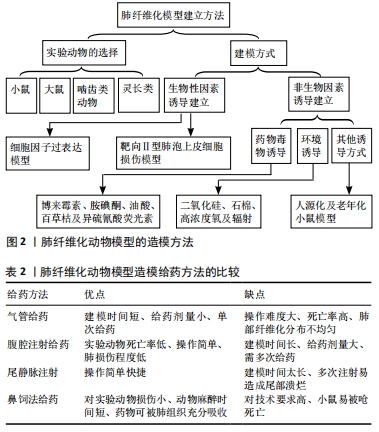
常见的生物因素诱导的肺纤维化模型有细胞因子过表达和在靶向Ⅱ型肺泡上皮细胞损伤模型。在细胞因子过表达模型中,通过转基因技术以腺病毒为载体通过调节某些基因的表达,促使细胞因子的过表达,进而诱导动物肺纤维化的产生。而在靶向Ⅱ型肺泡上皮细胞损伤模型中,将白喉毒素受体和载体结合导入小鼠体内,再进一步与小鼠SPC启动子结合,最终得到转基因小鼠模型。此模型阻断了小鼠Ⅱ型肺泡上皮细胞转换为Ⅰ型肺泡上皮细胞的途径,减少了Ⅰ型肺泡上皮细胞对受损部位进行的修补作用,从而导致损伤加重,出现间质瘢痕,进一步加重纤维化的程度。 此外,构造肺纤维化模型的方法还有非生物因素诱导建立的模型,此方法虽然在产生肺纤维化程度上较为不稳定,但在药物选择和给药途径方面具有多样性,且操作简单,价格低廉,所以在造模方式的选择上较为常见。常见的非生物性诱导建立的模型大多数是通过气管法给药建立的肺纤维化模型,比如使用博来霉素、异硫氰酸荧光素诱导的模型。此给药方法优点在于可以更好地模拟人类肺纤维化的病理变化过程,不仅如此还有建模时间短、给药剂量小、可以单次给药的特点。 除此之外还有部分模型的建立是可以通过尾静脉注射的形式,比如使用油酸构建的肺纤维化的模型(有研究者通过小鼠尾静脉注射0.12 mL/kg的油酸,诱导建立了肺纤维化模型),但此方法也有着明显的缺陷,即建模时间太长,多次注射可导致尾部溃烂或使用油酸进行尾静脉注射导致的脂肪栓塞等众多不良反应。 腹腔注射也常在实验中使用,在使用百草枯构建的动物模型中使用40-50 mg/kg的百草枯,该方法的优势在于实验动物的死亡率较低、操作简单、造成肺损伤的程度较轻但建模时间较长、给药剂量较大、常需要多次给药。 2.3 生物因素诱导的建立肺纤维化模型 2.3.1 细胞因子过表达模型 肿瘤坏死因子α、白细胞介素10、白细胞介素13、白细胞介素27、生长转化因子β等细胞因子过表达亦可诱导肺纤维化动物模型。常利用CRISPR-Cas9基因技术,或以腺病毒为载体,调节上述基因的表达,进而促进细胞因子的过表达,引起肺纤维化[6]。转化生长因子β1通过介导Smads通路和JNK通路引起肺纤维化[7];白细胞介素27激活JAK/STAT通路引起肺纤维化[8];白细胞介素10通过CCL2/CCR2激活巨噬细胞引起肺纤维化[9];白细胞介素13可通过转化生长因子β1途径造成肺纤维化[10]。细胞因子过表达模型,有着明确的靶点,对抗肺纤维化药物的筛查有重要作用,但腺病毒载体会被免疫系统清除,使得成功率下降,并且人体的肺纤维化是多因子共同的作用,单因子过表达模型具有一定的局限性[11]。 2.3.2 靶向Ⅱ型肺泡上皮细胞损伤模型 Ⅱ型肺泡上皮细胞在肺组织受到损伤后,可转换为Ⅰ型肺泡上皮细胞对受损部位进行修补,若此过程受阻,则会导致损伤加重,出现间质瘢痕,进一步导致肺纤维化。建立Ⅱ型肺泡上皮细胞损伤模型最常用的转基因技术,通过将白喉毒素受体与载体相结合,再进一步与小鼠SPC启动子结合,注入受精卵中,得到白喉毒素介导的转基因小鼠模型[12]。该模型通过测定肺胶原含量,观察肺病理变化等一系列数据,表明了肺泡上皮细胞损伤在肺纤维化中起到了一定的作用,同时也有助于研究Ⅱ型肺泡上皮细胞导致的肺泡破裂,胶原沉积等的下游机制。 2.4 非生物因素诱导的建立肺纤维化模型 "

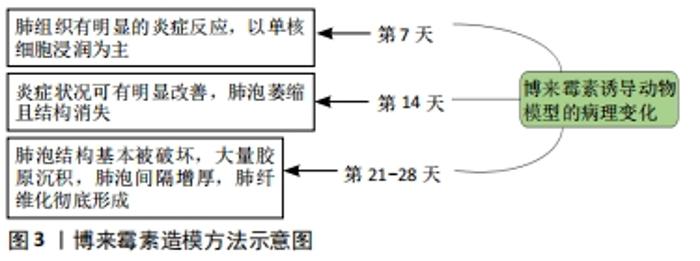
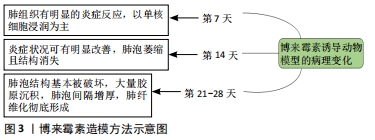
2.4.1 药物/毒物因素诱导的建模 博来霉素诱导的肺纤维化模型:博来霉素又名争光霉素,临床上常被用于治疗肿瘤相关疾病。当服用超过治疗剂量博来霉素时会引起肺纤维化,故常用于实验室中肺纤维化动物模型的造模。造模可选用小鼠、大鼠或兔等啮齿类动物、犬和各种灵长类动物[13],可通过气管给药、腹腔注射、尾静脉注射、鼻腔滴入及雾化吸入等方式[14],可单次给药也可重复给药。目前,最常用的给药途径是经气管给药[15],气管灌注单次给药剂量多为5 mg/kg[16];最常用的实验动物是小鼠和大鼠,常用品系为C57BL/6小鼠和Wistar大鼠[17]。 气管给药诱导的动物肺纤维化能够更好地模拟人类肺纤维化病理变化[18],有建模时间短、给药剂量小、单次给药的优点,同时也有操作难度大、死亡率高、肺部纤维化分布不均匀的不足之处;腹腔注射给药途径的优势在于实验动物死亡率低、操作简单、肺损伤程度低,但其建模时间长、给药剂量大、需多次给药[19];尾静脉注射操作简单快捷,可建模时间太长,多次注射易造成尾部溃烂[20];鼻腔滴入给药途径对实验动物损伤小,动物麻醉时间短、药物可被肺组织充分吸收,但对技术要求较高。 博来霉素诱导的肺纤维化动物模型在建模后第7天时肺组织有明显炎症病变,以单核巨噬细胞浸润为主,呈现出典型的肺纤维化早期病变。建模后第14天时炎症状况有所改善,但肺泡开始萎缩且结构消失,建模后第21-28天时,肺泡结构基本被完全破坏,大量胶原沉积,肺泡间隔增厚,肺纤维化彻底形成[21],见图3。"

虽然博来霉素诱导的肺纤维化模型被广泛应用,但其仍与临床的病理变化有所不同,例如:尽管特发性肺纤维化是一种独特的临床病理实体,原因不明,在不确定的时间内发展,但使用博来霉素诱导的肺纤维化模型只是复制间质性肺纤维化的一般形态,而不特定的复制任何肺疾病,因此具有一定的局限性,且肺纤维化有不可逆,进展慢的特点,因此还要进一步改善[20]。 胺碘酮诱导的肺纤维化模型:胺碘酮是含碘的苯呋喃类化合物,临床上常用来治疗心律失常,也可适用于心绞痛和难治性心动过速[22]。该药的不良反应较多,其中最严重也被关注最多的为肺毒性反应(弥漫性肺泡损伤)[23]。为探讨研究这一发病机制,有学者采用每天1次,连续5 d大鼠气管灌注0.1 mL盐酸胺碘酮(1.25 mg)生理盐水的方法,构建肺纤维化模型。该实验结果显示,第28天与第14天相比,血管和气管壁胶原沉积更加明显,出现灶状或大片的胶原沉积区,肺泡细胞增生,肺泡隔亦增宽[24]。有关胺碘酮诱导产生肺毒性的发病机制,至今未见确切的定论,因此复制动物模型进行进一步的研究显得尤为重要。 油酸诱导的肺纤维化模型:油酸虽可作为动物食物的营养素,但同时也可刺激肺组织产生肺纤维化,其给药途径大多是以尾静脉注射,但在剂量上尚未达到统一。周平等[21]通过小鼠尾静脉注射0.12 mL/kg的油酸,诱导建立了肺纤维化模型。有研究发现,油酸在肺纤维化模型复制过程中药物的剂型可影响模型成功率,可以通过注射盐形式的油酸来获得稳定的模型。该模型的优点是更接近人类肺纤维化病变分布特点,缺点是操作难度太大且成功率不高[25]。 百草枯诱导的肺纤维化模型:百草枯是农业中常用的除草剂,对人有很大毒性,且目前临床上没有对应解救药[26]。在中国部分地区,因口服百草枯中毒的现象较为多见,且口服致死率较高[19],常诱发肺纤维化,故建立百草枯诱导的肺纤维化模型尤为重要。发病机制为:百草枯进入人体后产生大量的氧自由基,诱发炎症反应,胶原蛋白大量合成,纤维增生,最终出现肺纤维化[27]。利用百草枯建立肺纤维化动物模型,一般选用小鼠和大鼠等,昆明小鼠及ICR小鼠在建立百草枯肺纤维化模型中均未能成功,所以C57BL/6J小鼠更较为适宜[28]。目前的给药途径有一次性口服灌注、腹腔注射,且一次性口服给药剂量为100 mg/kg[29];腹腔注射药物剂量40-50 mg/kg[19]。百草枯诱导的肺纤维化有死亡率高、操作困难、给药量难以控制等缺点[30]。由于目前药物治疗效果不佳,故建立相关动物模型是探究治疗百草枯引起的肺纤维化的重要工具。 异硫氰酸荧光素诱导的肺纤维化模型:异硫氰酸荧光素通过气管注入后,使肺泡和血管通透性增大,因此用来诱导建立肺纤维化模型。异硫氰酸荧光素有持续性刺激产生,致使肺纤维化持续时间长。有研究将异硫氰酸荧光素(溶于PBS中的0.007 mg/g)气管注射于小鼠,观察到其呼吸性细支气管周围有大量中性粒细胞和单核细胞浸润,在第21 天时肺纤维化最为严重[31-32]。此外研究也发现,异硫氰酸荧光素对C57BL/6和Balb/c小鼠均有不错的诱导作用[31]。该模型通过趋化因子受体2与配体CCL12相互作用,介导募集纤维细胞,成为刺激肺组织致损伤的主要因素。该实验操作时需要注意异硫氰酸荧光素在接种前必须现用现配,在制备时需给锥形瓶中加入PBS进行涡流处理,将混合物进行超声处理时应严格管控时间,否则会因降解的颗粒大小的不同而产生不同的结果[33],但该模型也具有独特的优势,作者可以根据绿色荧光识别定位肺纤维化的部位[34]。 各种模型特点比较:在药物/毒物因素诱导的建模中,博来霉素诱导法最为常用,建立的肺纤维化病理过程非常明显,但其只能复制肺纤维化的一般形态,具有局限性。此外还有胺碘酮诱导法,该药不良反应众多,在引起肺毒性的同时也造成了其他损伤,关于胺碘酮诱导产生肺毒性的发病机制,至今没有研究所得的确切结论。油酸诱导法所得的肺纤维化模型更接近人类的病变过程,可是油酸制剂的不同会影响造模成功率,因此在选择制剂时应慎重。百草枯诱导法死亡率过高,毒性大,实验操作有一定困难,故不推荐用作实验室构建肺纤维化模型。异硫氰酸荧光素诱导法可根据荧光标记观察肺纤维化部位,通过此方法构建的模型持续时间长,但异硫氰酸荧光素操作时必须现用现配,使用时要严格把控时间。综上所述,最推荐的是博来霉素诱导法,该法使用范围广泛,缺点相比于其他模型来说较为可控,因此在实验操作中经常使用。 2.4.2 环境因素诱导的肺纤维化模型 二氧化硅诱导的肺纤维化模型:尘肺病是由于在工作环境中长时间吸入的无机粉尘,超过了肺组织的自我清除限度,粉尘在肺组织中积聚发生炎性反应,从而引起以肺组织持续性、进行性、结节性纤维化为特征的全身性疾病[35],是一种常见的职业病。当前中国的尘肺病主要是矽肺、煤工尘肺,约占尘肺病例的80%,其中以矽肺最为多见,有着进展快、危害大的特点[36],并且没有有效的治疗措施。二氧化硅粉尘可诱发矽肺发生重要因素,故实验室中常以二氧化硅粉尘诱导动物模型的建立。动物模型以小鼠和大鼠最为多见,给药途径有一次性气管给药、雾化吸入和口喉抽吸等[36-37],其中一次性气管给药容易操作、成功率高、诱导的肺纤维化模型病理变化与人类更为相似[38],建模所需时间较短,大部分为14-28 d[39],故常被选用于肺纤维化中固有免疫调节的研究[40]。但二氧化硅动物模型有着纤维化种属差异、难以广泛应用和造模所需时间长等缺点。 石棉诱导的肺纤维化模型:石棉粉尘被吸入体内后,在肺部沉积,使肺内组织纤维化导致石棉肺。石棉可通过气管灌注给药和雾化吸入2种方式构建模型,一般气管内单次给药可较快的观察结果,在第7天时小鼠出现肺纤维化,并在第14天时纤维化程度彻底成熟[34]。但是这种建模法也存在着缺点,小鼠肺部的病变在双肺之间呈不均匀分布,多集中在肺中心而不是胸膜下[34]。雾化吸入法建模病变集中在胸膜下,但所需时间长且必须要用温石棉[41]。该模型的机制是:石棉吸入后沉积在肺组织,产生大量的氧自由基,刺激分泌出各种细胞因子,促使纤维母细胞和间质细胞增生,细胞外基质积聚,造成间质纤维化病变[42]。石棉建模法建模时间短,结果较为明显,但石棉有致癌风险,可诱发间皮瘤,因此在操作时实验人员应注意防护。 辐射诱导的肺纤维化模型:外源性辐射可引起组织纤维化损伤,放射性肺损伤造成的肺纤维化是较为普遍的肿瘤放射治疗副反应之一,因此建立肺纤维化模型尤为重要。辐射引起肺纤维化的机制主要是肺损伤使巨噬细胞产生多种细胞因子,它们促进成纤维细胞生成增加,间质蛋白大量合成,转化生长因子β是发挥主要细胞因子作用的细胞因子[43]。造模多用C57BL/6小鼠,存在全身和局部照射两种方式。全身照射时,剂量控制在12-15 Gy,大约在第20周可观察到肺纤维化[44],而局部照射则在第24周时观察到肺纤维化[45],该模型也可用来观察对比不同品系小鼠对放射线的敏感程度不同而造成损伤的严重度不一,但缺点是造模时间太长。 高浓度氧诱导的肺纤维化模型:临床上为了维持某些重患者的生命,持续高浓度的通氧是必不可少的,但持续的高氧也会造成多器官的损伤,由于肺是其首要作用部位[46],故损伤最为严重。支气管肺发育不良是新生早产婴儿较易好发的一种慢性病,是持续通高浓度氧气产生的并发症。随着医疗水平技术的提升,新生早产儿存活率上升,支气管肺发育不良发病率亦呈现出递增趋势[47],支气管肺发育不良有着高发病率和高死亡率的特点。实验动物以新生小鼠居多,急性肺纤维化常采用氧浓度为80%-100%;进行性肺纤维化常采用氧浓度为60%-70%,相比而言前者虽然造模所需时间短,但死亡率高;后者建模耗时长,但动物死亡率低,模型病例变化与临床相似[48]。徐凤丹等[49]在保持密封且排除二氧化碳影响的环境下,维持高浓度氧的供给,建立了肺纤维化模型,经上述研究所得,一般在建模后21 d时新生小鼠肺纤维化程度最为明显。 环境因素诱导的模型特点比较:二氧化硅诱导的肺纤维化模型易操作、成功率高,诱导的肺纤维化模型病理变化与人类更为相似,建模所需时间较短,常被选用于肺纤维化中固有免疫调节的研究,但二氧化硅动物模型有着纤维化种属差异、难以广泛应用、造模所需时间长等缺点。石棉诱导的肺纤维化模型建模时间短,结果较为明显,但石棉有致癌风险,可诱发间皮瘤,因此在操作时实验人员应注意防护。辐射诱导的肺纤维化模型可用来观察对比不同品系小鼠对放射线的敏感程度不同,而造成损伤的严重度不一,但缺点是造模时间太长。高浓度氧诱导的肺纤维化模型模型病例变化与临床相似但目前的机制研究仍不够全面。故在环境因素诱导的建模中,最推荐的诱导物为二氧化硅。 2.4.3 其他因素诱导的肺纤维化模型 人源化小鼠模型:近年来,有研究发现人源化小鼠模型可以更好地模拟肺纤维化病理特征,因此,将人类成纤维化细胞注射到非肥胖免疫缺陷型糖尿病小鼠体内构建人源化小鼠模型俨然成为当今研究的热点[50]。成纤维细胞在缺乏免疫反应的小鼠肺部组织生长,注射后30-50 d出现肺纤维化[34]。该模型可用具有细胞渗透性的染料标记成纤维细胞,能更加清楚地了解在肺纤维化不同阶段,成纤维细胞不同程度的分裂分化[34]。但免疫缺陷型小鼠价格昂贵,且需要专门的饲养环境,限制了该模型的广泛应用。 老龄化小鼠模型:临床研究表明,肺纤维化发病率与年龄成正相关[51],老年小鼠比青年小鼠更易受到博来霉素刺激而发生肺纤维化,因为在受到博来霉素等促纤维化诱导剂导致肺损伤时,老年小鼠的成纤维细胞能存留更多[41]。但目前尚未研究清楚具体诱导的年龄,且老年小鼠不方便饲养,使用困难。 肺纤维化动物模型建模信息汇总表,见表4。"

| [1] RAGHU G, GHEN SY, YEH WS, et al. Idiopathic pulmonary fibrosis in US medicare beneficiaries aged 65 years and older: incidence, prevalence and survival. Lancet Reapir Med. 2014;2(7):566-572. [2] RAGHU G, COLLARD HR, EGAN JJ, et al. An official ATS/ERS/JRS/ALAT statement: idiopathic pulmonary fibrosis: evidence-based guidelines for diagnosis and management. Am J Respir Crit Care Med. 2011;183(6):788-824. [3] COTTIN V, BERGOT E, BOURDIN A, et al. Adherence to guidelines in idiopathic pulmonary fibrosis: a follow-up national survey. ERJ Open Res. 2015;1(2):1-8. [4] 韩永禧,杨军,黄芪对博来霉素肺纤维化大鼠血清NO水平的影响[J].中国社区医师(医学专业),2012,14(302):8-9. [5] WOLLIN L, WEX E, PAUTSCH A, et al. Mode of action of nintedanib in the treatment of idiopathic pulmonary fibrosis. Eur Respir J. 2015;45(5):1434-1445. [6] 陈孟毅,孟爱民.肺纤维化动模型及研究进展[J].中国比较医学杂志,2016, 26(6):88-92. [7] 庄文越,马周义,赵娜,等.肺纤维化细胞因子参与机制及中药治疗研究进展[J].北华大学学报(自然科学版),2017,18(5):615-618. [8] SQUIRES MS, HUDSON EA, HOWELLS L, et al. Relevance of mitogen activated protein kinase (MAPK) and phosphotidy linositol-3-kinase/protein kinase B (PI3K/PKB) pathways to induction of apoptosis by curcumin in breast cells. Biochem Pharmacol. 2003;65(3):361-376. [9] SUN L, LOUIE MC, VANNELLA KM, et al. New concepts of IL-10-induced lung fibrosis: fibrocyte recruitment and M2 activation in a CCL2/CCR2 axis. Am J Physiol Lung Cell Mol Physiol. 2011;300(3):L341-L353. [10] 肖莉.白细胞介素13(IL-13)致肺纤维化作用及干预机制的研究[D].沈阳:中国医科大学,2004. [11] RAFII R, JUAREZ MM, ALBERTSON TE, et al. A review of current and novel therapies for idiopathic pulmonary fibrosis. J Thorac Dis. 2013;5(1):48-73. [12] SISSON TH, MENDEZ M, CHOI K, et al. Targeted injury of type II alveolar epithelial cells induces pulmonary fibrosis. Am J Respir Crit Care Med. 2010;181(3):254-263. [13] MOURATIS MA, AIDINIS V. Modeling pulmonary fibrosis with bleomycin. Curr Opin Pulm Med. 2011;17(5):355-361. [14] 邱雨雨,张港,王鸣尚,等.抗肿瘤药物博来霉素诱导小鼠肺纤维化模型[J].山东化工,2021,50(5):55. [15] CARRINGTON R, JORDAN S, PITCHFORD SC, et al. Use of animal models in IPF research. Pulm Pharmacol Ther. 2018;51:73-78. [16] SHEPPARD D. Transforming growth factor beta: a central modulator of pulmonary and airway inflammation and fibrosis. Proc Am Thorac Soc. 2006;3(5):413-417. [17] 卢锦辉,张丽,刘子豪,等.博来霉素诱导小鼠肺纤维化模型的建立及评价[J].兰州大学学报(医学版),2019,45(6):41. [18] DEGRYSE AL, TANJORE H, XU XC, et al. Repetitive intratracheal bleomycin models several features of idiopathic pulmonary fibrosis. Am J Physiol: 2010;299(4): L442-L452. [19] 王萍,李铁刚.百草枯中毒致小鼠肺纤维化模型的建立[J].实用药物与临床, 2020,23(10):886-889. [20] CHUA F, GAULDIE J, LAURENT GJ. Pulmonary fibrosis: searching for model answers. Am J Respir Cell Mol Biol. 2005;33(1):9-13. [21] 周平,王磊,何春香,等.博来霉素和油酸致大鼠肺纤维化病理模型的比较[J].世界最新医学信息文摘,2015,15(87):48. [22] 夏洪颖,任晓明.胺碘酮肺毒性的研究进展[J].医学先驱报,2010,29(6): 758. [23] DHOKARH R, LIG, SCHMICKL CN, et al. Drug associated acute lung injury: a population based cohort study. Chest. 2012;142(4):845-850. [24] 王和枚,瞿文生,余寿忠,等.胺碘酮所致大鼠肺毒性[J].中国药理学与毒理学杂志,1999,13(4):301-305. [25] GONCALVES-DE-ALBUQUERQUE CF, SILVA AR, BURTH P, et al. Acute respiratory distress syndrome: role of oleic acid-triggered lung injury and inflammation. Mediators Inflamm. 2015;2015:1-9. [26] BALTAZAR T, DINIS-OLIVEIRA RJ, DUARTE JA, et al. Paraquat research: do recent advances in limiting its toxicity make its use safer. Br J Pharmacol. 2013;168(1):44-45. [27] 李学军,崔社怀.肺纤维化治疗研究进展[J].中国综合临床,2001,17(10):725. [28] 杨珊珊,贾晓民,赵杰,等.三个品系小鼠百草枯肺纤维化模型的比较[J].山西医科大学学报,2014,45(6):456-459. [29] 杨晓燕,沈杰.肺纤维化动物模型的研究进展[J].生物技术通讯,2015,26(6):869. [30] ISHIDA Y, TAKAYASU T, KIMURA A, et al. Gene expression of cytokines and gro with factors in the lungs after paraquat adminstration in mice. Legal Med. 2006;8(2): 102-109. [31] MOORE BB, HOGABOAM CM. Murine Animal models of pulmonary fibrosis. Am J Physiol Lung Cell Mol Physiol. 2008;294(2):L154-L155. [32] CHRISTENSEN PJ, GOODMAN RE, PASTORIZA L, et al. Induction of lung fibrosis in the mouse by intratracheal instillation of fluorescein isothiocyanate is not T-cell-dependent. Am J Pathol. 1999;155(5):1775-1776. [33] O’ DWYER DN, MOORE BB. Animal models of pulmonary fibrosis. lung innate immunity and inflammation: methods and protocols. Methods Mol Biol. 2018; 1809:373-374. [34] MOORE B, LAWSON WE, OURY TD, et al. Animal models of fibrotic lung disease. Am J Respir Cell Mol Biol. 2013;49(2):167-179. [35] 蒋荣,陈明霞.二氧化硅诱导的内皮间质转化参与矽肺纤维化的实验研究[J].现代预防医学,2020,47(9):1665-1669. [36] 蔡婷峰,宋向荣,李宏玲,等.不同时间点大鼠矽肺模型病理改变观察[J].中国职业医学,2020,47(4):385-389. [37] Heather F, Lakatos, Heather A, et al. Oropharyngeal aspiration of a silica suspension produces a superior model of silicosis in the mouse when compared to intratracheal instillation. Exp Lung Res. 2006;32:181-199. [38] 张志斌,穆丹,李明,等.牛磺酸对大鼠肺纤维化的干预作用[J].工业卫生与职业病,2014,40(4):255-258. [39] LAKATOS HF, BURGESS HA, THATCHER TH, et al. Oropharyngeal aspiration of a silica suspension produces a superior model of silicosis in the mouse when compared to intratracheal instillation. Exp Lung Res. 2006;32(5):181-199. [40] CSAAEL SL, EISENBARTH SC, IYER SS, et al. The Nalp3 inflamma some is essential for the development of silicosis. Proc Natl Acad Sci. 2008;105(26):9035-9040. [41] TASHIRO J, RUBIO GA, LIMPER AH, et al. Exploring animal models that resemble idiopathic pulmonary fibrosis. Front Med. 2017;4:118. [42] 肖国兵.石棉致纤维化机制研究新进展[J].职业卫生与病伤,1997,12(1):51-53. [43] RUBIN P, FINKELSTEIN J, SCHAPIRO D. Molecular biology mechanisms in the radiation induction of pulmonary injury syndromes: interrelationship between the alveolar macrophage and the septal fibroblast. Int Radiat Oncol Biol Phys. 1992;24(1):93-101. [44] MCDONALD S, RUBIN P, CHANG AY, et al. Pulmonary changes induced by combined mouse beta-interferon (rMuIFN-beta) and irradiation in normal mice-toxic versus protective effects. Radiother Oncol. 1993;26(3):212-218. [45] LIU H, XUE JX, LI X, et al. Quercetin liposomes protect against radiation-induced pulmonary injury in a murine model. Oncol Lett. 2013;6(2):453-459. [46] VAN OOIJ PJ, HOLLMANN MW, VAN HULST RA, et al. Assessment of pulmonary oxygen toxicity: relevance to professional diving: a review. Respir Physiol Neurobiol. 2013;189(1):117-128. [47] RUDLOFF I, CHO SX, BUI CB, et al. Refining anti-inflammatory therapy strategies for bronchpulmonary dysplasia. J Cell Mol Med. 2017;21(6):1128-1138. [48] WARNER BB, STUART LA, PAPES RA, et al. Functional and pathological effects of prolonged hyperoxia in neonatal mice. Am J Physiol. 1998;275(1):L110-L117. [49] 徐凤丹,王优,吴文燊,等.高氧暴露对新生小鼠肺部炎性反应及纤维化的影响[J].中国医药导报,2017,14(26):21-24. [50] PIERCE EM, CARPENTER K, JAKUBZICK C, et al. Therapeutic targeting of CC ligand 21 or CC chemokine receptor 7 abrogates pulmonary fibrosis induced by the adoptive transfer of human pulmonary fibroblasts to immunodeficient mice. Am J pathol. 2007;170(4):1152-1164. [51] SUEBLINVONG V, NEVEU WA, NEUJAHR DC, et al. Aging promotes pro-fibrotic matrix production and increases fibrocyte recruitment during acute lung injury. Adv Biosci Biotechnol. 2014;5(1):19-30. |
| [1] | Tan Xinfang, Guo Yanxing, Qin Xiaofei, Zhang Binqing, Zhao Dongliang, Pan Kunkun, Li Yuzhuo, Chen Haoyu. Effect of uniaxial fatigue exercise on patellofemoral cartilage injury in a rabbit [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(在线): 1-6. |
| [2] | Xu Xinzhong, Wu Zhonghan, Yu Shuisheng, Zhao Yao, Xu Chungui, Zhang Xin, Zheng Meige, Jing Juehua. Biomechanical analysis of different ways of inserting Steinmann Pins into the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1313-1317. |
| [3] | Zhang Yufang, Lü Meng, Mei Zhao. Construction and verification of a full spine biomechanical model of adolescent scoliosis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1351-1356. |
| [4] | Wang Baojuan, Zheng Shuguang, Zhang Qi, Li Tianyang. Miao medicine fumigation can delay extracellular matrix destruction in a rabbit model of knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1180-1186. |
| [5] | Lü Yiyan, Li Hanbing, Ma Xiaoqing, Zhang Han, Zhang Yuhang, Li Genlin. Establishment and characteristic analysis of interior heat and diabetes mouse model using compound factors [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1187-1193. |
| [6] | Chen Shijian, Li Ge, Zhang Yu, Guan Yalun, Li Xuejiao, Liu Shuhua, Li Yongchao, Li Yunfeng, Gao Jinfeng, Wei Xiaoyue, Zhao Yuhong. Comparison and evaluation of MPTP-induced subacute and chronic models of Parkinson’s disease in mice [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1247-1252. |
| [7] | Zhu Chan, Han Xuke, Yao Chengjiao, Zhang Qiang, Liu Jing, Shao Ming. Acupuncture for Parkinson’s disease: an insight into the action mechanism in animal experiments [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1272-1277. |
| [8] | Wang Xinmin, Liu Fei, Xu Jie, Bai Yuxi, Lü Jian. Core decompression combined with dental pulp stem cells in the treatment of steroid-associated femoral head necrosis in rabbits [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1074-1079. |
| [9] | Liu Yuhang, Zhou Jianqiang, Xu Xuebin, Qu Xingyue, Li Ziyu, Li Kun, Wang Xing, Li Zhijun, Li Xiaohe, Zhang Shaojie. Establishment and validation of finite element model of lower cervical spine in 6-year-old children [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 870-874. |
| [10] | Feng Jianbo, Li Chencheng, Liu Jinyue, Wang Xiaomin, Peng Jiachen. Implantation of Kirschner wire with Staphylococcus aureus biofilm establishes a traumatic osteomyelitis model in rats [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 700-705. |
| [11] | Wang Shihui, Cheng Yang, Zhu Yunjie, Cheng Shaodan, Mao Jianying. Effect of arc edge needle-scalpel therapy on inflammatory factors and histomorphology of the frozen shoulder in rabbit models [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 706-711. |
| [12] | Li Weiming, Xu Qingwen, Li Yijun, Sun Yanbo, Cui Jin, Xu Pengyuan . Deep seawater promotes wound healing in diabetic mice by activating PI3K/Akt pathway [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 724-729. |
| [13] | Deng Shuang, Pu Rui, Chen Ziyang, Zhang Jianchao, Yuan Lingyan . Effects of exercise preconditioning on myocardial protection and apoptosis in a mouse model of myocardial remodeling due to early stress overload [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 717-723. |
| [14] | Deng Zhaoyang, Yang Zhaohui. Three-dimensional model analysis of tibial plateau fracture lines [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(3): 334-339. |
| [15] | Li Yanting, Chen Jian, Liu Menglan, Ren Manman, Zhong Weihong, Chen Changxing. Three-dimensional finite element analysis of Daogaijinbei manipulation on lumbar intervertebral disc biomechanics [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(3): 340-343. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||