Chinese Journal of Tissue Engineering Research ›› 2020, Vol. 24 ›› Issue (4): 643-649.doi: 10.3969/j.issn.2095-4344.2203
Previous Articles Next Articles
Antineoplastic mechanism of antimicrobial peptides: selective membrane destruction and non-membrane dissolution
Gong Lei1, Zhang Xi2
- 1Department of Esophageal Cancer, Cancer Hospital of Tianjin Medical University, National Clinical Research Center for Cancer, Tianjin Key Laboratory of Cancer Prevention and Treatment, Tianjin Clinical Medical Research Center of Malignant Tumor; 2Stomatology Hospital of Tianjin Medical University
-
Received:2019-06-15Revised:2019-06-19Accepted:2019-08-15Online:2020-02-08Published:2020-01-07 -
Contact:Zhang Xi, MD, Lecturer, Stomatology Hospital of Tianjin Medical University, Tianjin 300070, China -
About author:Gong Lei, MD, Attending physician, Department of Esophageal Cancer, Cancer Hospital of Tianjin Medical University, National Clinical Research Center for Cancer, Tianjin Key Laboratory of Cancer Prevention and Treatment, Tianjin Clinical Medical Research Center of Malignant Tumor, Tianjin 300060, China -
Supported by:the National Natural Science Foundation of China, No. 81501798 and 81501994; the Natural Science Foundation of Tianjin, No. 18JCYBJC95700; the Wu Jieping Medical Foundation-Excellent Surgery Foundation, No. 320.2730.1886
CLC Number:
Cite this article
Gong Lei, Zhang Xi. Antineoplastic mechanism of antimicrobial peptides: selective membrane destruction and non-membrane dissolution [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(4): 643-649.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
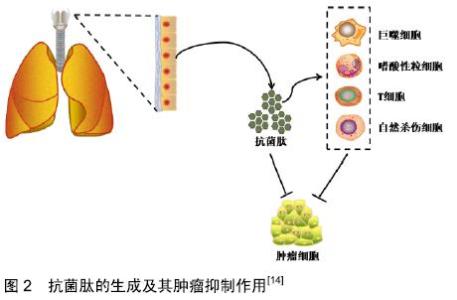
2.1 抗菌肽的概述 抗菌肽存在于所有形式的生命体中,包括原核生物、真菌、植物和人类[8]。尽管相同的多肽序列很少出现在不同的物种中,但抗菌肽仍具有一些共同的结构特征。抗菌肽具有阳离子和两亲性结构,可以通过静电和疏水作用选择性地与带负电荷的微生物膜结合,从而导致膜破裂或移位。因此,微生物膜通常被认为是抗菌肽的主要作用靶点,并根据这种认知提出了几种抗菌活性机制[9]。抗菌肽的抗菌机制从作用模式上可以分为2类主要的模式:直接致死模式和免疫调节模式,直接致死作用机制可进一步分为膜靶向和非膜靶向机制[10]。而发现抗菌肽抗菌活性的同时,其抗肿瘤机制也被逐渐阐明。 2.2 抗菌肽的性质 2.2.1 抗菌肽的生物转化及理化特性 抗菌肽是一类特殊的分子,通常具有5-40位氨基酸残基,带有正电荷且具有两亲结构[11];抗菌肽通过静电相互作用与带有负电的细胞膜脂质相互识别,进而作用于靶点之上[12-13]。在人体中抗菌肽可以在很多组织中表达,包括皮肤上皮细胞、呼吸系统、消化系统甚至是免疫系统中,见图2。根据合成位点的不同,抗菌肽又可分为非核糖体肽和核糖体肽,前者一般在细菌和真菌的胞质中合成,后者广泛合成于原核和真核细胞的核糖体中[15]。抗菌肽在结构上是不均匀的,可能呈线性(具有两亲性和疏水性的α-螺旋残基)、β-折叠、环状、脂质、大环或α-螺旋杆构象[9]。值得注意的是这种多样性结构来自翻译后修饰,包括糖基化、磷酸化和酰胺化等[16]。 "
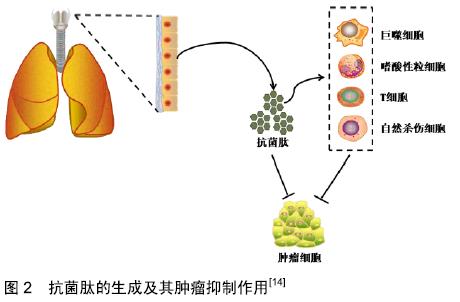
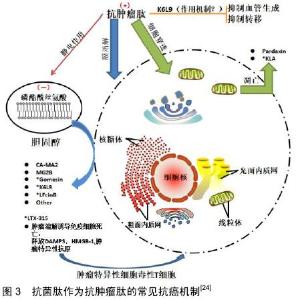
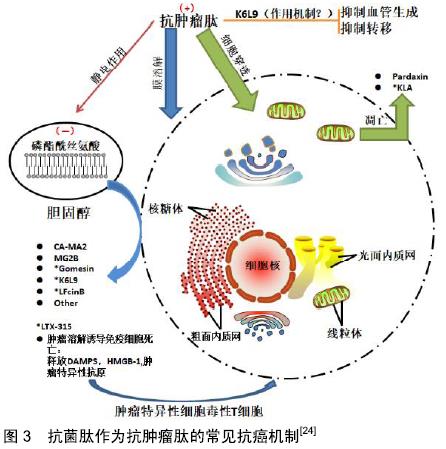
抗菌肽对于很多微生物均有效果,其中包括细菌、真菌及病毒。值得注意的是,内源性抗菌肽被认为对病原体具有高度的选择性。介导其抗菌作用的经典机制包括以下几方面:穿透质膜或细胞壁,从而导致离子梯度的溶解或破坏;与核酸连接并破坏其功能;破坏保持微生物细胞壁完整性的酶的功能[17]。 2.2.2 抗菌肽的免疫调节作用 抗菌肽除了在执行杀菌作用方面的典型功能外,亦可与宿主细胞相互作用。例如β-防御素,一种对革兰阳性菌、革兰阴性菌及病毒都有作用的抗菌肽,同样也是CCR6趋化因子受体的配体,可在T淋巴细胞和树突状细胞上表达;因此它能够作为宿主细胞主动与被动免疫的桥梁。此外,抗菌肽还对其他宿主免疫细胞产生影响:包括改变宿主基因表达,诱导趋化因子分泌,调节中性粒细胞,T淋巴细胞和树突状细胞的激活或死亡,以及调节细胞分化途径,促进免疫介导的伤口愈合等作用[18-19]。但上述的抗菌肽与宿主细胞之间的相互作用的具体机制迄今为止尚未阐明。 2.3 抗菌肽对抗肿瘤细胞的特性 2.3.1 抗菌肽的基本抗肿瘤特性 众所周知,革兰阴性细菌外膜上的脂多糖和革兰阳性细菌膜上的脂磷烯酸导致细菌表面上具有高密度的负电荷[20-21]。如前所述,抗菌肽表面带有正电荷,因此抗菌肽与细菌细胞膜具有很强的相互作用。值得注意的是,由于具有各种类型二级结构的阳离子抗菌肽(典型的携带电荷为+2或更多)和具有不同正电荷数的序列,均能够识别其微生物靶点,因此并没有一致的活性结合序列[22]。因此,阳离子两性基团是抗菌肽具有活性的主要特征,而氨基酸序列决定其活性特异性。虽然抗菌肽可能对哺乳动物细胞存在毒性,但毒性浓度通常比对细菌的最低抑菌浓度高一个对数数量级[23]。因此,合理地预测抗菌肽的最小治疗指数(最大耐受剂量/最小治疗剂量)是其抗肿瘤治疗的前提。 磷脂酰丝氨酸(占磷脂总量的3%-9%)通常存在于正常哺乳动物细胞胞质膜的内叶上。肿瘤细胞中磷脂酰丝氨酸表达转移至质膜的外叶中,这使得一些特殊的抗菌肽能够与之特异性靶定,见图3。当细胞发生凋亡时,磷脂酰丝氨酸可以被转移到质膜的外叶,从而破坏哺乳动物正常细胞膜的不对称性[25]。这种不对称性的改变通常存在于凋亡细胞和一些肿瘤细胞中,进而有助于其被单核细胞识别而被其清除。其他可能导致肿瘤细胞负电荷升高的因素包括硫酸肝素和肿瘤细胞表面存在O-糖基化黏蛋白[26]。然而,与细菌细胞膜上的负电荷相比,癌细胞上的负电荷密度相对较低,因此,抗菌肽对于癌细胞的亲和力弱于细菌。与正常细胞膜相比,肿瘤细胞膜存在抗菌肽的潜在靶点。一些肿瘤细胞因细胞膜中较低水平的胆固醇而导致细胞膜流动性增加。例如与正常白细胞和肺细胞相比,在白血病和肺癌患者中,其肿瘤细胞的细胞膜由于其膜中胆固醇水平较低而显示出其流动性增加[27],从而最终增强了抗菌肽的溶解作用[28]。肿瘤细胞另一个特性是其微绒毛数量增加,进而使细胞膜表面积随之增大,最终增强抗菌肽与肿瘤细胞的结合能力[24]。一旦与癌细胞结合,抗菌肽可能破坏细胞膜或穿透细胞,攻击线粒体,导致细胞凋亡。防御素(长29-45个氨基酸)是一类重要的富含半胱氨酸的抗菌肽,防御素α的抗肿瘤活性,特别是人类中性粒细胞肽1-3,已被证实可以通过膜溶解和促进凋亡及抑制血管生成等作用而发挥抗肿瘤活性[2]。然而,人类中性粒细胞肽也能杀死正常细胞,如成纤维细胞、上皮细胞和白细胞。此外,植物源性防御素对肿瘤细胞也缺乏选择性[29]。因此,防御素通常不是有效的酰基-载体蛋白质抗肿瘤药物,它们必须进行结构优化才能实现特异性的抗肿瘤作用。 "
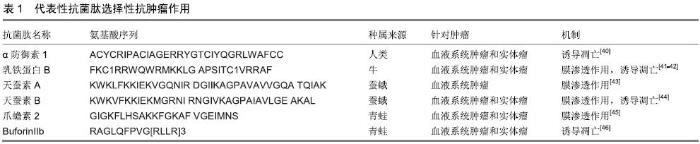
2.3.2 抗菌肽的选择性膜破坏作用 最早被发现的一种具有抗肿瘤治疗功能的抗菌肽是Magainin,它是一类在非洲爪蟾幼虫中发现的具有广谱抗菌活性的抗菌肽[30]。Magainin 2及其类似物对血液及实体肿瘤细胞都显示出具有选择性,12 mg/L的Magainin在1 h内便能迅速产生肿瘤杀伤作用;即使质量浓度升高至200 mg/L时,其对正常淋巴细胞仍未表现出细胞毒性。抗菌肽诱导的离子通道作用导致钠离子、钾离子和氯离子的泄漏。如果消除细胞膜的电离子梯度,抗菌肽的细胞毒性作用即被消除,表明膜电位对抗菌肽抗肿瘤活性至关重要。 由于抗菌肽在体内实验中没有表现出的抗肿瘤活性,且其抗肿瘤细胞活性比抗菌活性低很多,因此还有2个主要问题有待解决:抗肿瘤活性有限;对肿瘤细胞的特异性低。如果抗菌肽对肿瘤细胞的特异性能够增强,则可以克服以上2个问题。抗菌肽与肿瘤细胞的相互作用强度可能影响其活性和特异性。因此学者们对很多抗肿瘤肽进行结构优化来达到增强治疗效果的目的。由于天然抗菌肽在免疫系统中发挥多种作用,因此它们在预防宿主免受疾病侵害方面比治疗方面更有效[31]。因此,要提高治疗作用有效的做法是对抗菌肽结构进行优化,而不能直接使用自然的抗菌肽。而合理的抗菌肽设计需要建立一个对宿主靶细胞具有独特选择性的框架区域,以便区分阳离子和疏水结构域,最终设计出可增强治疗效果的合成抗菌肽。 2.3.3 抗菌肽的非膜溶解机制 研究者利用双亲性原理设计了一个理想化的双亲螺旋结构,该抗菌肽K6L9具有15个残基,其对癌细胞发挥直接膜溶解作用的同时,还显示出具有抗血管生成和抑制转移的作用,但其具体的抗肿瘤机制还有待进一步阐明。另一种常见的抗肿瘤机制是促进肿瘤细胞凋亡[32]。尽管与正常细胞膜相比,抗肿瘤肽对癌细胞的抑制作用具有选择性,但一些抗菌肽可能同时扰乱细胞膜并穿透细胞,而其他非溶解性抗肿瘤肽可能仅仅具有穿透细胞作用。当2种作用同时存在的情况下,抗肿瘤肽能够破坏线粒体,并导致细胞程序性死亡。这种凋亡机制可以通过线粒体肿胀、线粒体膜破裂及刺激凋亡标记物的活化来实现。曾有学者将抗肿瘤肽注射至肿瘤内部,使嵌合肽转移到肿瘤细胞的细胞质中,破坏软骨组织,并通过caspase-3激活凋亡酶级联。其他抗肿瘤肽具有穿透癌细胞的固有特性,不需要与细胞穿透肽结合。例如pardaxin(GFFALIPKIISSPLFKTLLSAVGSALSSSGGQE)可以通过caspase-3激活诱导鳞癌细胞凋亡[33]。某些抗菌肽导致的免疫原性细胞死亡,能够对相同肿瘤产生长期免疫保护作用。抗肿瘤肽LTX-315便具有上述特性[34],其相关应用目前已进入一期临床试验[35]。 综上所述,随着抗菌肽抗癌机制的逐步阐明,通过优化抗菌肽结构来增强抗癌效果将更容易实现,其抗肿瘤的临床作用在未来具有广泛的应用前景。 2.4 与抗肿瘤相关的抗菌肽 2.4.1 防御素 防御素是真核生物产生的阳离子肽,包含2个超家族,在序列、结构及功能上得到了不同的水平的改造。各种天然或合成的防御素在大量肿瘤细胞实验或肿瘤动物模型实验中已经被证实具有良好的肿瘤抑制作用。有研究表明,人类β-防御素3能够抑制血管内皮生长因子诱导的癌细胞迁移能力[2]。另一项研究发现人类β-防御素3是由肿瘤浸润性单核细胞产生的,并以剂量依赖和旁分泌的方式抑制结肠癌细胞的侵袭和转移能力[36]。以上体外实验结果所显示出的恶性表征与转移灶具有一致性,而防御素在抑制肿瘤细胞迁移方面的有效性,说明其可以作为潜在的转移抑制剂。此外,天然防御素似乎对肿瘤细胞亦可以起到抑制增殖和促进凋亡的作用,并诱导细胞周期停滞[37-38],该作用与视网膜母细胞瘤蛋白磷酸化水平的增加,转录和细胞周期依赖性激酶及其催化周期蛋白活性抑制,以及caspase-7和caspase-9等凋亡相关性标志物表达上调有关。除了天然衍生物,合成防御素类似物可以产生更大的抗癌效果:有研究证明将人β-防御素2和人血清白蛋白重组成特异性防御素后,其在抑制K-ras突变胰腺癌MIAPaCa-2细胞系的肿瘤增殖作用比天然β-防御素更有效[39],见表1。 "


人类防御素还具有另外2个重要的特性。第一,它们对肿瘤细胞具有显著的特异性,而对正常的细胞似乎没有明显的细胞毒性或细胞抑制作用[37-38,47]。已有研究表明,防御素通过内在途径诱导MCF-7细胞凋亡,增强MAPK p38磷酸化,增加细胞色素c、APAF-1、caspase-7和caspase-9的表达,但不影响膜电位和钙流量[37]。这一结果表明人类抗菌肽内源性衍生的特性,即可以避免在炎症反应过程中对正常健康组织造成非特异性杀伤。第二,抗菌防御素可能对一些尚未解决的临床问题提供了新的治疗机会,如化疗耐药问题。研究表明,防御素与细胞毒性化疗药物(如阿霉素)联合应用于多重耐药肿瘤细胞时可有效增强细胞杀伤作用[38]。 2.4.2 乳铁蛋白肽B 乳铁蛋白是一种分子质量80 kD的铁隔离糖蛋白,存在于乳汁等外分泌液和多形核白细胞颗粒中。乳铁蛋白B具有一定的抗肿瘤作用,因为它能够对肿瘤细胞的胞质膜和线粒体膜产生致命的、选择性的失稳作用[41],并且已被证明对结直肠癌、神经母细胞瘤和黑色素瘤癌细胞有效[42,48-49]。抗菌肽多具有多种构象,最近一项研究表明,牛乳铁蛋白(bLf)、环LfcinB和线性LfcinB均能激活多种抗肿瘤信号级联,通过转录组学分析其能够促进p53激活、凋亡发生以及抗血管生成信号通路的活化。此外,bLf和LfcinB均诱导了caspase-8、p53和p21介导的大肠癌细胞凋亡前通路[42]。与防御素一样,乳铁蛋白似乎具有免疫调节作用,并已被证明能使淋巴细胞定向根除癌细胞[50]。 2.4.3 天蚕素A和B 天蚕素是一类典型的短碱性肽,长度在31-39个氨基酸残基之间,具有一个强碱性的N末端和疏水性的C末端,其最初从天蚕中分离出来的,其抗癌机制和其他抗菌肽相类似,天蚕素A和B被证明对膀胱肿瘤有选择性的细胞毒性和细胞抑制作用,但对人类成纤维细胞株没有作用[43],而ABP-dHC-天蚕素A及其类似物ABP-dHC-天蚕素A-K对白血病细胞株有细胞毒性,但对正常体细胞株没有毒性作用[44]。天蚕素A通过ROS信号传导通路在早幼粒细胞系HL-60中诱导凋亡[44],并通过Fas、Fas-l、caspase-3和caspase-8的表达在人肝癌细胞中诱导凋亡[51]。天蚕素XJ通过caspase-3和多聚(ADP-核糖)多聚酶的表达及对Bcl-2的下调诱导肝细胞癌细胞的生长抑制、S期阻滞和凋亡[45]。在体外实验中,天蚕素A增强了常用化疗药物对鳞状皮肤癌细胞的作用,这也为该肿瘤提供了新的治疗策略。 2.4.4 爪蟾素Ⅱ 爪蟾素Ⅱ是一种从非洲爪蛙的皮肤中分离出来的抗菌肽,在严重的造血和实体恶性肿瘤中显示出有效的抗癌作用。作为一种具有螺旋结构的离子载体肽,它已被证明能够穿透癌细胞膜,起到离子通道的作用,导致癌细胞的细胞溶解[52],从而显著增强了细胞毒性化疗药物的抗肿瘤作用。例如,当与治疗非小细胞肺癌细胞的化疗药物一起使用时,爪蟾素A和G具有协同作用。爪蟾素Ⅱ也表现出抗肿瘤的选择性,例如,它们已被证明能溶解各种造血肿瘤和实体肿瘤细胞,但对正常人成纤维细胞和外周血淋巴细胞几乎没有影响[15]。同时,爪蟾素Ⅱ的衍生物可以增强对肿瘤细胞的特异性细胞毒性[52]。 2.4.5 其他具有抗肿瘤特性的代表性抗菌肽 在结构上,LTX-302是一种源于其亲本肽LfcinB的9-聚体肽,具有优化的α-螺旋二级结构,从而发挥巨大的抗肿瘤活性。LTX-302在BALB/c小鼠体内建立的A20-B细胞淋巴瘤模型中已被证实具有明显的抗肿瘤作用,其抗肿瘤活性依赖于CD4和CD8淋巴T细胞的活化,且最终LTX-302给药诱导了针对淋巴瘤细胞的长效细胞免疫,最终导致肿瘤消退[14]。Buforin II是一种具有21残基的α-螺旋抗菌肽,其序列与组蛋白H2A的N末端区域相似。Buforin IIB是一种合成衍生的类似于Buforin II的化合物,经修饰后在2个α-螺旋之间含有脯氨酸残基[53]。在一项研究中发现Buforin IIB对乳腺癌细胞MX-1和MCF-7具有抗癌活性,并通过抗血管生成机制抑制小鼠动物模型中种植瘤的生长[53]。由于此次综述篇幅有限,在该部分仅涉及到以上具有代表性的抗菌肽。 2.5 抗菌肽的临床试验 一些阳离子抗菌肽可能主要通过诱导宿主免疫反应而不是直接作用方式发挥其杀菌作用。因此在过去几年中,它们作为抗癌药物的辅助药物而被广泛研究,同时近年来肿瘤免疫治疗相关临床试验也证实了这一作用机制。 商业上开发的第一个抗菌肽是乙酸培昔甘南(MSI-78)[46]。此外,已经有很多抗菌肽正在系统研发中。例如,一种正在处于临床试验阶段的抗菌肽是omiganan,它是从牛中性粒细胞中纯化的吲哚菌素衍生物,它以凝胶的方式被用作预防中心静脉导管污染[54]。此外,与氧氟沙星相比,吡昔甘南可以作为治疗糖尿病患者轻度感染足部溃疡的有效替代品[55]。 目前抗菌肽刚开始应用于肿瘤领域,其疗效数据相对有限。然而,从既往感染相关性临床试验中所得到的安全性数据,间接支持抗菌肽将在癌症患者中具有较好的耐受性。正在进行的肿瘤临床试验是NCT0225366,其中LL37对转移性黑色素瘤的最佳生物剂量和治疗有效性正在临床一期评估中。LL37通过瘤内注射的方式来治疗转移性黑色素瘤患者。 "

| [1] TANISHIKI N, YANO Y, MATSUZAKI K. Endowment of pH responsivity to anticancer peptides by introducing 2,3-diaminopropionic acid residues. Chembiochem. 2019; 20(16):2109-2117. [2] GHOSH SK, MCCORNICK TS, WEINBERG A. Human Beta Defensins and Cancer: Contradictions and Common Ground. Front Oncol. 2019; 3(9):341-348. [3] DASKIVICH TJ. Life Expectancy and Treatment Choice for Men with High-risk Prostate Cancer. Eur Urol. 2015; 68(1):59-60. [4] BOWER H, BJORKHOLM M, DICKMAN PW, et al. Life Expectancy of Patients With Chronic Myeloid Leukemia Approaches the Life Expectancy of the General Population. J Clin Oncol. 2016; 34(24):2851-2857. [5] LIN J, XIA L, LIANG J, et al. The roles of glucose metabolic reprogramming in chemo- and radio-resistance. J Exp Clin Cancer Res. 2019;38(1):218-230. [6] DUTTA P, DAS S.Mammalian Antimicrobial Peptides: Promising Therapeutic Targets Against Infection and Chronic Inflammation. Curr Top Med Chem. 2016;16(1):99-129. [7] HIEMSTRA PS, AMATNGALIM GD, VAN DER DOES AM, et al. Antimicrobial Peptides and Innate Lung Defenses: Role in Infectious and Noninfectious Lung Diseases and Therapeutic Applications.Chest. 2016;149(2):545-551. [8] AGEITOS JM, SANCHEZ-PEREZ A, CALO-MATA P, et al. Antimicrobial peptides (AMPs): Ancient compounds that represent novel weapons in the fight against bacteria. Biochem Pharmacol. 2017;1(133):117-138. [9] KUMAR P, KIZHAKKEDATHU JN, STRAUS SK. Antimicrobial Peptides: Diversity, Mechanism of Action and Strategies to Improve the Activity and Biocompatibility In Vivo. Biomolecules.2018;8(1):4-27. [10] MORAVEJ H, MORAVEJ Z, YAZDANPARAST M, et al. Antimicrobial Peptides: Features, Action, and Their Resistance Mechanisms in Bacteria. Microb Drug Resist. 2018;24(6):747-767. [11] PIRTSKHALAVA M,GABRIELIAN A,CRUZ P, et al. DBAASP v.2: an enhanced database of structure and antimicrobial/cytotoxic activity of natural and synthetic peptides. Nucleic Acids Res. 2016;44(13):6503-6507. [12] HASAN M, MOGHAL MMR, SAHA SK, et al.The role of membrane tension in the action of antimicrobial peptides and cell-penetrating peptides in biomembranes. Biophys Rev. 2019;11(3):431-448. [13] HASAN M, YAMAZAKI M.Elementary Processes and Mechanisms of Interactions of Antimicrobial Peptides with Membranes-Single Giant Unilamellar Vesicle Studies. Adv Exp Med Biol. 2019;1117(2):17-32. [14] ROUDI R, SYN NL, ROUDBARY M. Antimicrobial Peptides As Biologic and Immunotherapeutic Agents against Cancer: A Comprehensive Overview. Front Immunol. 2017; 13(8): 1320-1329. [15] SIKANDAR A, KOEHNKE J.The role of protein-protein interactions in the biosynthesis of ribosomally synthesized and post-translationally modified peptides. Nat Prod Rep. 2019;28. doi: 10.1039/c8np00064f. [Epub ahead of print]. [16] CHUNG CR, KUO TR, WU LC, et al. Characterization and identification of antimicrobial peptides with different functional activities. Brief Bioinform. 2019; pii: bbz043. doi: 10.1093/bib/bbz043. [Epub ahead of print] [17] SHER KHAN R, IQBAL A, MALAH R, et al. Plant defensins: types, mechanism of action and prospects of genetic engineering for enhanced disease resistance in plants. 3 Biotech 2019;9(5):192-218. [18] JI P, ZHOU Y, YANG Y, et al.Myeloid cell-derived LL-37 promotes lung cancer growth by activating Wnt/beta-catenin signaling. Theranostics. 2019;9(8):2209-2223. [19] HOLLY MK, DIAZ K, SMITH JG.Defensins in Viral Infection and Pathogenesis. Annual review of virology. 2017;4(1): 369-91. [20] AIDOUKOVITCH A, ANDERS E, DAHL S, et al. The host defense peptide LL-37 is internalized by human periodontal ligament cells and prevents LPS-induced MCP-1 production.J Periodontal Res.2019;28.doi: 10.1111/jre.12667. [Epub ahead of print]. [21] HASHEMI MM, HOLDEN BS, COBURN J, et al. Proteomic Analysis of Resistance of Gram-Negative Bacteria to Chlorhexidine and Impacts on Susceptibility to Colistin, Antimicrobial Peptides, and Ceragenins. Front Microbiol. 2019;10(18):210-222. [22] HU WW, HUANG SC, JIN SC. A novel antimicrobial peptide-derived vehicle for oligodeoxynucleotide delivery to inhibit TNF-alpha expression. Int J Pharm. 2019;10(558): 63-71. [23] HOLLMANN A, MARTINEZ M, NOGUERA ME, et al. Role of amphipathicity and hydrophobicity in the balance between hemolysis and peptide-membrane interactions of three related antimicrobial peptides. Colloids Surf B Biointerfaces. 2016;1(141):528-536. [24] DESLOUCHES B, DI YP. Antimicrobial peptides with selective antitumor mechanisms: prospect for anticancer applications. Oncotarget. 2017;8(28):46635-46651. [25] BEVERS EM, WILLIAMSON PL. Getting to the Outer Leaflet: Physiology of Phosphatidylserine Exposure at the Plasma Membrane. Physiol Rev. 2016;96(2):605-645. [26] OLIVEIRA-FERRER L, LEGLER K, MILDE-LANGOSCH K. Role of protein glycosylation in cancer metastasis. Semin Cancer Biol. 2017;8(44):141-152. [27] DIMITRAKOPOULOS FD, KOTTOROU AE, ANTONACOPOULOU AG, et al.Expression of Immune System-Related Membrane Receptors CD40, RANK, BAFFR and LTbetaR is Associated with Clinical Outcome of Operated Non-Small-Cell Lung Cancer Patients. J Clin Med. 2019; 8(5): 741-758. [28] LI X, SHEN B, CHEN Q, et al. Antitumor effects of cecropin B-LHRH' on drug-resistant ovarian and endometrial cancer cells. BMC Cancer. 2016;3(16):251-259. [29] GUZMAN-RODRIGUEZ JJ, OCHOA-ZARZOSA A, LOPEZ-GOMEZ R, et al. Plant antimicrobial peptides as potential anticancer agents. Biomed Res Int. 2015;2015: 735087-735097. [30] TIAN L, ZHANG D, SU P, et al. Design, recombinant expression, and antibacterial activity of a novel hybrid magainin-thanatin antimicrobial peptide. Prep Biochem Biotechnol. 2019;49(5):427-434. [31] HANET EF, STRAUS SK, HANCOCK REW. Reassessing the Host Defense Peptide Landscape. Front Chem. 2019;7(1): 43-64. [32] THEANSUNGNOEN T, MAIJAROEN S, JANGPROMMA N, et al. Cationic Antimicrobial Peptides Derived from Crocodylus siamensis Leukocyte Extract, Revealing Anticancer Activity and Apoptotic Induction on Human Cervical Cancer Cells. Protein J. 2016;35(3):202-211. [33] HAN Y, CUI Z, LI YH, et al. In Vitro and in Vivo Anticancer Activity of Pardaxin against Proliferation and Growth of Oral Squamous Cell Carcinoma. Mar Drugs. 2015;14(1):2-13. [34] CAMILIO KA, WANG MY, MAUSETH B, et al. Combining the oncolytic peptide LTX-315 with doxorubicin demonstrates therapeutic potential in a triple-negative breast cancer model. Breast Cancer Res. 2019;21(1):9-20. [35] ZHOU H, FORVEILLE S, SAUVAT A, et al. The oncolytic peptide LTX-315 triggers immunogenic cell death. Cell Death Dis. 2016;10(7):e2134-e2144. [36] URAKI S, SUGIMOTO K, SHIRAKI, et al.Corrigendum: Human beta-defensin-3 inhibits migration of colon cancer cells via downregulation of metastasis-associated 1 family, member 2 expression. Int J Oncol. 2015;46(4):1858-1864. [37] BAINDARA P, GAUTAM A, RAGHAVA GPS, et al. Anticancer properties of a defensin like class IId bacteriocin Laterosporulin10. Sci Rep. 2017;19(7):46541-46549. [38] STREZLECKA P, CZAPLINSKA D, SADEJ R, et al. Simplified, serine-rich theta-defensin analogues as antitumour peptides. Chem Biol Drug Des. 2017;90(1):52-63. [39] DU Y, SHANG BY, SHENG WJ, et al.A recombinantly tailored beta-defensin that displays intensive macropinocytosis-mediated uptake exerting potent efficacy against K-Ras mutant pancreatic cancer. Oncotarget. 2016;7(36):58418-58434. [40] PAUSCH T, ADOLPH S, FELIX K, et al. Antimicrobial Peptide Human Neutrophil Peptide 1 as a Potential Link Between Chronic Inflammation and Ductal Adenocarcinoma of the Pancreas. Pancreas. 2018;47(5):561-567. [41] VARGAS CASANOVA Y, RODRIGUEZ GUERRA JA, UMANA PEREZ YA, et al. Antibacterial Synthetic Peptides Derived from Bovine Lactoferricin Exhibit Cytotoxic Effect against MDA-MB-468 and MDA-MB-231 Breast Cancer Cell Lines. Molecules. 2017;22(10): E1641-1651. [42] JIANG R, LONNERDAL B. Bovine lactoferrin and lactoferricin exert antitumor activities on human colorectal cancer cells (HT-29) by activating various signaling pathways. Biochem Cell Biol. 2017;95(1):99-109. [43] FATIMA I, KANWAL S, MAHMOOD T. Natural Products Mediated Targeting of Virally Infected Cancer. Dose Response. 2019;17(1):1559325818813227. [44] SANG M, ZHANG J, ZHUGE Q.Selective cytotoxicity of the antibacterial peptide ABP-dHC-Cecropin A and its analog towards leukemia cells. Eur J Pharmacol. 2017;15(803):138-147. [45] XIA L, WU Y, MA JI, et al. The antibacterial peptide from Bombyx mori cecropinXJ induced growth arrest and apoptosis in human hepatocellular carcinoma cells. Oncol Lett. 2016;12(1):57-62. [46] GOLDSTEIN EJC, CITRON DM, TYRRELL KL, et al. In Vitro Activities of Pexiganan and 10 Comparator Antimicrobials against 502 Anaerobic Isolates Recovered from Skin and Skin Structure Infections. Antimicrob Agents Chemother. 2017; 61(12):e01401-417. [47] GUZMAN-RODRIGUEZ JJ, LOPEZ-GOMEZ R, SALGADO-GARCIGLIA R, et al. The defensin from avocado (Persea americana var. drymifolia) PaDef induces apoptosis in the human breast cancer cell line MCF-7. Biomed Pharmacother. 2016;6(82):620-627. [48] FAN R, YUAN Y, ZHANG Q, et al. Isoleucine/leucine residues at "a" and "d" positions of a heptad repeat sequence are crucial for the cytolytic activity of a short anticancer lytic peptide. Amino Acids. 2017;49(1):193-202. [49] HUANG HC, LIN H, HUANG MC. The lactoferricin B-derived peptide, LfB17-34, induces melanogenesis in B16F10 cells. Int J Mol Med. 2017;39(3):595-602. [50] BO LY, LI TJ, ZHAO XH. Effect of Cu/Mn-Fortification on In Vitro Activities of the Peptic Hydrolysate of Bovine Lactoferrin against Human Gastric Cancer BGC-823 Cells. Molecules. 2019;24(7): E1195-1208. [51] WU C, GENG X, WAN S, et al. Cecropin-P17, an analog of Cecropin B, inhibits human hepatocellular carcinoma cell HepG-2 proliferation via regulation of ROS, Caspase, Bax, and Bcl-2. J Pept Sci. 2015;21(8):661-668. [52] MORET F, GOBBO M, REDDI E.Conjugation of photosensitisers to antimicrobial peptides increases the efficiency of photodynamic therapy in cancer cells. Photochem Photobiol Sci. 2015;14(7):1238-1250. [53] PARKER JP, DEVOCELLE M, MORGAN MP, et al. Derivatisation of buforin IIb, a cationic henicosapeptide, to afford its complexation to platinum(ii) resulting in a novel platinum(ii)-buforin IIb conjugate with anti-cancer activity. Dalton Trans. 2016;45(33):13038-13041. [54] NG SMS, TEO SW, YONG YE, et al. Preliminary investigations into developing all-D Omiganan for treating Mupirocin-resistant MRSA skin infections. Chem Biol Drug Des. 2017;90(6): 1155-1160. [55] DUMVILLE JC, LIPSKY BA, HOEY C, et al. Topical antimicrobial agents for treating foot ulcers in people with diabetes. Cochrane Database Syst Rev. 2017;14(6):CD011038. [56] NARAYANA JL, HUANG HN, WU CJ, et al. Efficacy of the antimicrobial peptide TP4 against Helicobacter pylori infection: in vitro membrane perturbation via micellization and in vivo suppression of host immune responses in a mouse model. Oncotarget. 2015;6(15):12936-12954. [57] YUAN Y, ZAI Y, XI X, et al. A novel membrane-disruptive antimicrobial peptide from frog skin secretion against cystic fibrosis isolates and evaluation of anti-MRSA effect using Galleria mellonella model. Biochim Biophys Acta Gen Subj. 2019;1863(5):849-856. [58] SHIN JM, GWAK JW, KAMAJAPAN P, et al.Biomedical applications of nisin.J Appl Microbiol. 2016;120(6):1449-1465. |
| [1] | Li Shengqiang, Xie Bingying, Chen Juan, Xie Lihua, Huang Jingwen, Ge Jirong. Interaction proteomics of long noncoding RNA uc431+ gene in postmenopausal osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(11): 1641-1646. |
| [2] | Liu Sijie, E Xiaoqiang, Pan Qi, Yao Guijun. Standardized treatment of infection around the prosthesis after joint replacement [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(32): 5195-5202. |
| [3] | Xu Chun-gui, Zhang Ji-sen, Xu Xin-zhong, Jing Jue-hua . Effect of modified rabbit defensin 1 on peripheral nerve regeneration [J]. Chinese Journal of Tissue Engineering Research, 2017, 21(24): 3833-3838. |
| [4] | Sun Zhi-bang, Zhou Yi-qin, Chen Song, Wu Hai-shan. Human beta defense 3/poly(lactic-co-glycolic acid) controlled-release microspheres: preparation and in vitro releasing performance [J]. Chinese Journal of Tissue Engineering Research, 2017, 21(10): 1514-1519. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||