Chinese Journal of Tissue Engineering Research ›› 2026, Vol. 30 ›› Issue (26): 6916-6922.doi: 10.12307/2026.827
Previous Articles Next Articles
Selenium effect on human bone health and its application in bone materials
Ye Gaoqi, Gong Yukang, Chen Dejin, Gao Wenshan
- Department of Orthopedics, Affiliated Hospital of Hebei University, Baoding 071000, Hebei Province, China
-
Accepted:2025-12-31Online:2026-09-18Published:2026-03-16 -
Contact:Gao Wenshan, MD, Chief physician, Professor, Doctoral supervisor, Department of Orthopedics, Affiliated Hospital of Hebei University, Baoding 071000, Hebei Province, China -
About author:Ye Gaoqi, MS candidate, Department of Orthopedics, Affiliated Hospital of Hebei University, Baoding 071000, Hebei Province, China -
Supported by:2024 In-Hospital Fund Project of Affiliated Hospital of Hebei University, No. 2024ZA01 (to GWS)
CLC Number:
Cite this article
Ye Gaoqi, Gong Yukang, Chen Dejin, Gao Wenshan. Selenium effect on human bone health and its application in bone materials[J]. Chinese Journal of Tissue Engineering Research, 2026, 30(26): 6916-6922.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
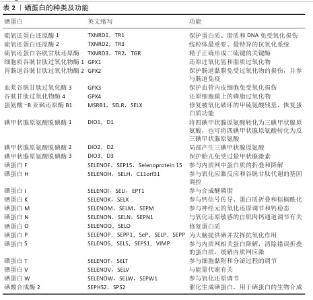
2.1.1 硒在自然界存在的形式 硒(Se)是一种必需的微量元素,于1817年由瑞典化学家Jons Jacob Berzelius发现。在过去,硒甚至被认为是一种致癌物质,经过200年后,硒在人类健康中的作用开逐渐受到重视,被认为是一种重要的营养素。在自然界中,硒分为有机和无机两种形式,无机硒主要包括硒酸盐和亚硒酸盐以及非天然的纳米硒,有机硒主要是硒多糖、含硒的氨基酸、硒蛋白。与无机硒相比,有机硒更容易被人体吸收和利用,有机硒主要存在于植物和动物食品中,如粗粮、肉制品、乳制品和海鲜。硒的生物利用度主要来自有机形式(一般超过80%)[3-4],所以硒的化学形式很重要。除硒代蛋氨酸外,有机硒和无机硒在活体内的代谢途径基本相似[5]。硒被肝脏吸收,合成并输出硒蛋白P,最终通过血液循环为其他组织和器官提供硒[6-7]。硒蛋白P具有多个半胱氨酸残基,将硒转运到其他组织和器官[8],并通过细胞内硒代谢途径将转运的硒转化为磷酸硒。硒主要以硒蛋白的形式发挥生物学作用。摄入的无机硒首先通过谷胱甘肽和硫氧还蛋白系统还原为硒化氢(H2Se),硒化物进一步转化为硒氨基酸以结合到硒蛋白的特定位点,如硒酶的催化位点[9]。在人类中有25个已确定的基因编码硒蛋白[10],如表2所示。若小鼠胚胎缺乏翻译硒蛋白所需的半胱氨酸tRNA 基因,则会导致胚胎死亡,这表明硒蛋白对生命至关重要[11]。几乎所有的硒蛋白在其酶活性位点上都含有单半胱氨酸残基,这是硒蛋白活性所必需的。在人类中,半胱氨酸是唯一天然存在的氨基酸,缺乏同源的氨基酰基-tRNA合成酶,需要特定的生物合成途径[12]。 "
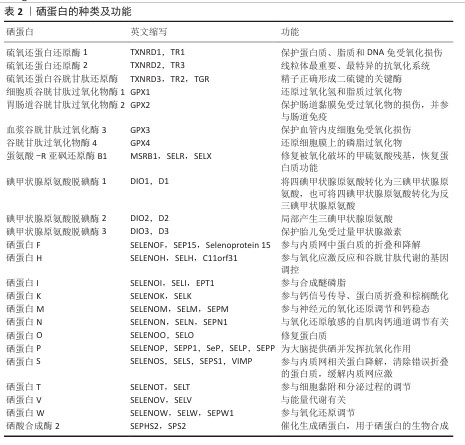
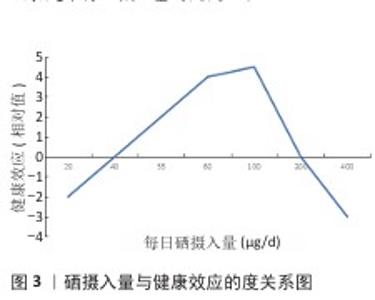
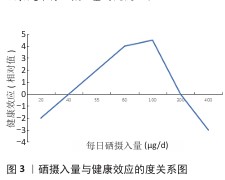
2.1.2 硒的摄入 日常生活中,硒的主要来源是肉制品(31%),其次是鱼类(19%)、大米(12%)、谷物(11%)。大部分硒是在小肠中被吸收的(50%-80%),由肾脏以三甲基硒离子的形式排出(60%)[13]。与无机硒相比,硒氨基酸具有更高的生物利用度,并且植物性食物中(如绿豆、洋葱、西兰花)所含的硒往往比动物性食物中(如牛肉、猪肉、虾)的硒具有更高的生物利用度[14]。食物中的硒被摄入后以硒半胱氨酸和硒蛋白的形式存在于人体器官和组织中:30%在肝脏,30%在肌肉,15%在肾脏,10%在血浆,15%在其他器官。硒代蛋氨酸是硒的主要营养形式,不能由高等生物合成[15],存在于蔬菜(尤其是谷物)、酵母硒和其他硒补充剂中[16]。植物中大约90%的硒以硒代蛋氨酸的形式存在,由于硒代蛋氨酸的合成依赖于植物和真菌,而土壤是植物中硒的主要来源,当土壤中总硒含量低于0.1 mg/kg为缺硒,0.2-0.3 mg/kg为一般缺硒,超过0.4 mg/kg为富硒[17]。植物对土壤中不同形态硒的生物可利用性各不相同,一般表现为:硒酸>有机硒>亚硒酸>硒>硒化。此外,植物对硒的吸收还受到土壤pH值、微生物活性和有机质的影响。 据估计,全世界约有15%的人口患有与硒缺乏相关导致的病症,为了使硒发挥保护作用,人体内的硒水平必须保持在一定范围内(图3)。血硒正常质量浓度范围为90-120 μg/L,世界卫生组织(WHO)推荐的成人硒摄入量水平为55 μg/d,对于孕妇和哺乳期妇女,需要量根据年龄增加到60-70 μg/d。1-3岁儿童为70 μg/d,4-6岁为95 μg/d,7-10岁为130 μg/d,11-14岁为180 μg/d,青少年为230 μg/d。硒摄入量小于40 μg/d极有可能出现硒缺乏症状,可导致免疫力下降、甲状腺功能异常、心脏疾病风险增加等;300-400 μg/d为成年人可耐受的最高每日摄入量,当长期摄入400 μg/d,出现硒中毒的风险显著增加,表现为面色苍白、精神疲惫、呼吸有大蒜气味,严重者可导致中枢神经系统中毒。因此,适度的硒摄入量和均衡的饮食是维持硒摄入量的关键[18]。"
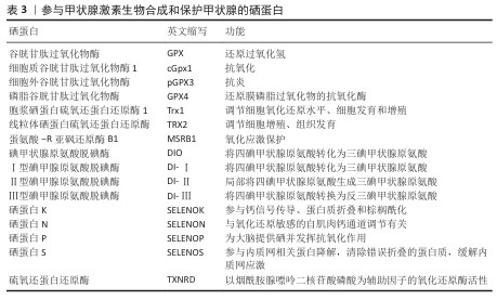
2.1.3 硒在体内存在的形式以及生物学效应 硒的生物学效应主要是由硒蛋白介导,硒蛋白主要以谷胱甘肽过氧化物酶和硫氧还蛋白还原酶存在于组织中[19]。谷胱甘肽过氧化物酶参与抗氧化,催化过氧化氢生成水和氧,并催化过氧化氢还原为醇和氧。硒蛋白具有多种功能,硒半胱氨酸是硒的生物活性形式,参与超过20种不同硒蛋白酶的活性,包括免疫反应调节[20-21]、抗氧化作用、甲状腺激素代谢调节[22](表3),还具有成骨和抗肿瘤功能[23-26],这些功能强调了硒在日常生活中的关键作用。 Na2SeO3是临床最常用的补硒试剂,而食物作为硒最重要的来源,这种必需元素的摄入量取决于含硒食物的摄入量及其在食物中的含量[27]。作为维持人体正常生理功能所必需的微量营养素,硒在甲状腺激素代谢、免疫和抗氧化防御中起着重要的生理作用[28],是产生甲状腺激素代谢酶所必需的,被认为可以改善甲状腺细胞和免疫细胞的功能[29],同时还与慢性代谢性疾病、肝纤维化、关节病、癌症的发生发展密切相关[30-32]。硒还参与蛋白质折叠的质量控制、细胞分化和增殖等[33],对砷、铅和汞等重金属的毒性作用具有拮抗作用[34]。 虽然不同硒化合物在体内的代谢途径相似,但这些化合物化学成分和结构的不同意味着它们对人体抵抗氧化应激以及促进生长发育的作用是不同的[35]。有机硒化合物,如硒代蛋氨酸和硒代半胱氨酸,通过钠依赖性运输系统在小肠中被吸收。对于无机化合物,硒酸盐通过类似的钠依赖转运系统被吸收,而亚硒酸盐通过非介导的被动扩散转移[36]。体内大部分硒储存在骨骼肌中,但硒在体内的分布遵循组织层次,即在硒缺乏期间,大脑和睾丸会分到更多的硒,因为它们的功能需要硒[37]。硒摄入不足可导致硒蛋白表达不足,增加罹患某些疾病的风险,包括自身免疫性甲状腺疾病[38],还可导致活性氧和磷酸化水平升高,从而抑制Ⅰ型胶原、碱性磷酸酶的表达和成骨细胞分化[39]。对软骨而言,硒具有增强软骨功能和维持软骨稳态的潜力,硒摄入不足可导致软骨细胞损伤和炎症因子上调(如诱导一氧化氮合成酶和环氧合酶2),升高血管内皮生长因子、血管内皮细胞生长因子受体2、基质金属蛋白酶13、Ⅹ型胶原抗体、血管生成素1的表达,加速细胞外基质降解,介导软骨损伤,进一步促进软骨相关疾病的发生[40]。 "
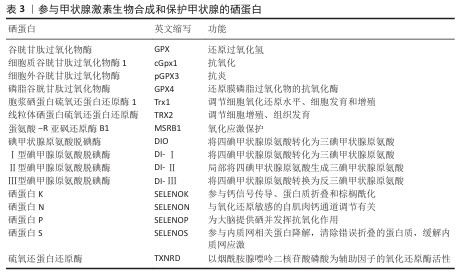
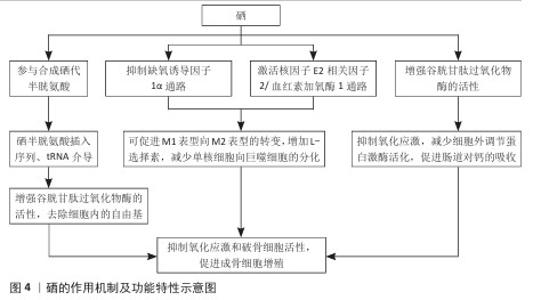
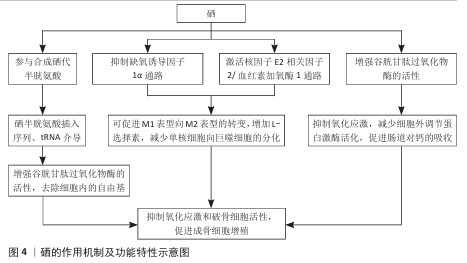
2.1.4 硒的生物性能及作用机制 硒的抗氧化机制:硒可以增强谷胱甘肽过氧化物酶的活性[41],分解脂质过氧化物,将生物体内的氢过氧化物或脂过氧化物转变为有机醇类,清除细胞内的自由基,保护细胞免受氧化损伤(图4);还可通过调控p38丝裂原活化蛋白激酶/细胞外调节蛋白激酶、核转录因子kB、凋亡信号调节激酶1/ c-Jun氨基末端激酶、磷脂酰肌醇3-激酶/蛋白激酶B/哺乳动物雷帕霉素靶蛋白等多条信号通路调节线粒体膜的渗透性,抑制促凋亡蛋白释放,从而抑制细胞凋亡,发挥抗氧化作用[42-43]。 硒的抗炎机制:M1巨噬细胞样细胞可分泌一氧化氮合成酶、白细胞介素1β和肿瘤坏死因子α促进炎症,白细胞介素1β和白细胞介素6的协同活性还可促进辅助性T细胞17释放白细胞介素17,这一级联反应与多种形式的皮炎(如银屑病、特应性、溃疡性等)的发生有关,而M2巨噬细胞被认为是抗炎细胞,释放精氨酸酶1和白细胞介素10等因子抑制炎症。硒可促进M1表型向M2表型的转变,从而表现出抗炎活性(图4)。另外,硒还可以增加L-选择素、减少单核细胞向巨噬细胞的分化。在炎症因子作用下,单核细胞附着在内皮上并发育成巨噬细胞,巨噬细胞又可分泌大量炎症因子加重炎症。L-选择素可调节单核细胞与内皮细胞的黏附,在炎症反应中促进中性粒细胞迁移,抑制单核细胞黏附到内皮细胞上,从而减少巨噬细胞的产生[44]。 硒促成骨的作用机制:在破骨细胞和成骨细胞中,硒可以通过抑制氧化应激和细胞外调节蛋白激酶活化来降低活性氧水平(图4),促进成骨分化[45],抑制病理信号转导,恢复血管内皮细胞中的线粒体功能,上调血管内皮生长因子、骨形态发生蛋白2和重组人Noggin蛋白的表达,进而重建对骨再生至关重要的血管生成-成骨耦合[46]。 另外,硒蛋白W依赖性的受体相关因子6/p38信号通路可降低破骨细胞活性,从而促进成骨[15]。硒还可以促进肠道对钙的吸收,从而促进成骨,增强骨骼强度。 "
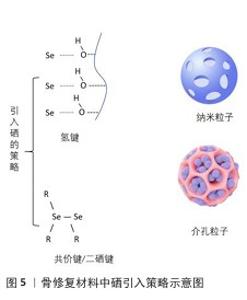
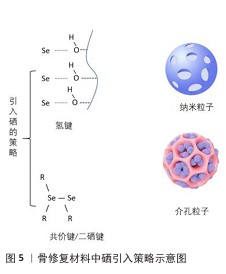
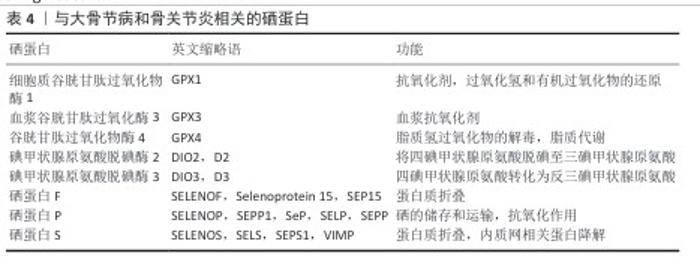
2.2 硒基骨材料的构建 健康的骨重建由骨生成和骨吸收介导,是由成骨细胞和破骨细胞之间的平衡维持的,而骨重塑过程中会产生大量的活性氧抑制成骨细胞分化、促进破骨细胞分化,破坏人体内正常的骨平衡[47],因此,维持活性氧在正常水平是保证骨骼健康的重要条件之一。骨缺损部位的炎症反应和缺氧环境、损伤后的缺血再灌注过程、创伤和手术、新毛细血管的形成均会造成大量的活性氧自由基产生,加重骨缺损部位损伤;活性氧也会扩散骨材料中,从而严重影响植入材料内部和周围细胞的存活、增殖和分化,影响骨重塑过程,从而导致骨修复困难[17]。近年来,研究人员研发了大量应用于骨修复的材料,如水凝胶、骨水泥、生物活性玻璃等,这些材料具有良好的骨缺损修复效果。水凝胶具有良好的生物相容性,其孔隙结构有利于营养物质的交换、新生毛细血管长入,还可以设计成不同的形状和尺寸,用于不规则骨缺损的治疗;另外,水凝胶具有大量的可修饰位点,易于物理/化学掺杂各种材料。骨水泥具有优异的机械性能、抗压强度以及良好的可塑性和填充性,能填充各种不规则形状的骨缺损空腔。硒在骨修复材料中常见的反应/相互作用引入模式有:氢键、共价键(二硒键)、介孔粒子、纳米粒子等(图5)。氢键可提供交联网络,赋予材料自修复能力并改善其力学性能和机械性能。共价相互作用、纳米粒子等可表现缓释效果,并改善材料的力学性能和机械性能。因此,通过引入不同硒的骨修复材料调控骨损伤部位的微环境,对于骨疾病和骨再生修复治疗至关重要。"
2.3 硒基材料在骨修复中的应用 硒常被分为三类,包括无机硒、有机硒和硒纳米颗粒。该文选择了几种常见用于骨修复领域的硒以及相关专利进行了总结阐述分析。 2.3.1 骨缺损 由肿瘤、创伤和其他疾病引起的骨缺损越来越普遍[48],目前骨移植仍然是骨缺损的主要治疗方法,但该方法主要受供体短缺、手术复杂性、免疫排斥的限制。随着骨组织工程技术的发展,研究人员已经将含有骨诱导因子的生物材料支架作为修复骨缺损的方法,然而,这些生物材料支架可能无法调节炎症微环境,甚至可能加重炎症。骨缺损后迅速产生高浓度的活性氧,导致骨髓间充质干细胞活性下降甚至死亡,而生物材料支架植入后的排斥反应则加剧了这一现象;此外,持续升高的活性氧浓度会破坏骨修复过程中的氧化还原平衡,抑制骨髓间充质干细胞的募集和成骨分化,延迟骨缺损的愈合。因此,开发一种在早期快速清除活性氧,还能长期提高干细胞的抗氧化应激能力的多功能骨组织修复材料,对骨缺损愈合至关重要。LIN等[49]制备了一种具有硒蛋白介导抗氧化作用的创新型超声可调节水凝胶,该水凝胶平台封装富氧硒薄壳硅在甲基丙烯酸酯明胶中,超声用于调节水凝胶的孔径以释放含硒纳米颗粒,并促进细胞内高效选择蛋白的原位合成和过氧化氢消耗,研究表明,甲基丙烯酸酯明胶在超声控制下迅速释放硒半胱氨酸([Sec]2)以清除活性氧,并维持骨髓间充质干细胞的稳态;在大鼠模型中,甲基丙烯酸酯明胶增强了骨髓间充质干细胞体外和在活体内的抗氧化能力,改善了缺氧环境,促进了成骨分化。硒蛋白通过激活Wnt/β-catenin通路促进了骨髓间充质干细胞的分化[50]。SHARMA等[29]制备了以槲皮素、硒纳米颗粒组成的水凝胶,该水凝胶可改善成骨细胞中槲皮素-硒纳米颗粒的摄取和分布,增加成骨活性,提高早期和晚期成骨细胞分化标志物表达,还能降低成骨细胞核因子κB受体活化因子配体/骨保护素比值,抑制破骨细胞形成;在机制上,槲皮素-硒纳米颗粒激活关键信号通路WNT和骨形态发生蛋白,并利用miR-206/缝隙连接蛋白43通路促进成骨;小鼠钻孔骨缺损模实验表明,该水凝胶介导的局部递送槲皮素-硒纳米颗粒可显著加速骨愈合,恢复骨重塑。磷脂酰肌醇3-激酶/蛋白激酶B信号通路可促进成骨细胞成骨,加速骨修复[51]。CHEN等[35]研制了一种由超声控制,结合明胶-甲基丙烯酰和香薰烯的硒纳米粒子的复合水凝胶(LNT-SeNPs@Gel),该水凝胶可在骨修复的炎症阶段调节硒纳米粒子的释放,抑制活性氧和炎症因子的过量产生,最终重塑炎症微环境;另外,该水凝胶还可通过激活硒蛋白调控的磷脂酰肌醇3-激酶/蛋白激酶B信号通路促进骨缺损部位的修复。 以上研究表明,硒具有优异的成骨能力和独特的化学性质,可以将不同材料和硒纳米粒子结合,同时发挥材料和硒的功能,通过发挥抗氧化、抗炎能力和调节免疫微环境和促进成骨基因表达,为骨缺损修复再生构建理想的微环境。 2.3.2 骨质疏松症 尽管缺硒已被证明会增加大鼠的骨吸收和降低骨矿物质密度,并对小鼠的骨微结构产生负面影响,但缺硒对骨骼的主要影响表现为软骨异常[52]。骨质疏松的骨质流失通常与炎性细胞因子(如干扰素γ、肿瘤坏死因子、白细胞介素1、白细胞介素6等)的释放有关,抑制了成骨细胞功能、过度活化破骨细胞,导致骨质疏松症[53]。最近的研究表明,活性氧可以通过诱导成骨细胞死亡导致骨质流失和骨质疏松症[54-56],因此,补充硒有助于维持骨骼稳态,促进损伤后的骨再生。硒以各种形式与各种骨相关蛋白和酶相互作用,增强其功能并促进骨形成。例如,亚硒酸钠、硒蛋白P能刺激成骨细胞增殖和分化,从而促进骨生长和修复。ALAJMI等[37]利用硒纳米粒子的结构稳定性和天然聚合物的生物学特性,制备了具有分子结构互联的硒纳米粒子功能化、可注射、热响应水凝胶,该水凝胶由硒纳米颗粒、壳聚糖、胶原组成,体内外研究结果表明,该水凝胶可以促进成骨早期(RUNX2、碱性磷酸酶)和晚期(骨钙素)标志物相关基因的表达,并且硒纳米粒子固有的抗炎和抗氧化特性可减少氧化应激和炎性因子,从而促进成骨细胞分化,抑制破骨细胞表达,促进成骨。HUANG等[39]研究采用一锅法,引入聚乳酸酸-碳酸酯、β-三钙磷酸盐与硒纳米粒,开发了一种可注射、抗塌陷、自适应形状和黏附骨移植替代材料,研究表明该材料在生物微环境中具有足够的黏附性,在体内外具有骨诱导活性、促血管生成作用和抗炎、抗氧化作用,还可通过骨髓间充质干细胞中的沉默信息调节因子1/核因子E2相关因子2 /谷胱甘肽过氧化酶4信号通路有效缓解氧化应激,减轻炎症,增强M2巨噬细胞的极化;此外,该材料可以通过沉默信息调节因子1/核因子E2相关因子2 /谷胱甘肽过氧化酶4抗氧化途径保护骨髓间质干细胞免受骨质疏松诱导的铁凋亡。 以上研究表明,硒具有优异的成骨能力和抗氧化功能,可以将不同材料和硒纳米粒子结合同时发挥材料和硒的功能。硒用于骨质疏松症治疗取得了良好效果,为骨质疏松症的治疗提供了潜在方向。"
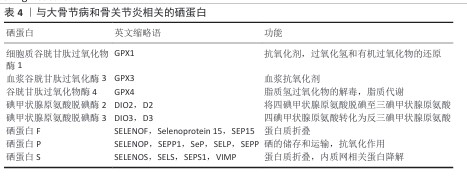
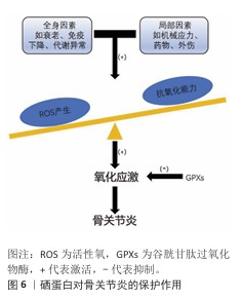
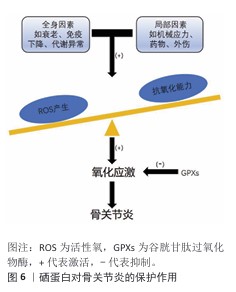
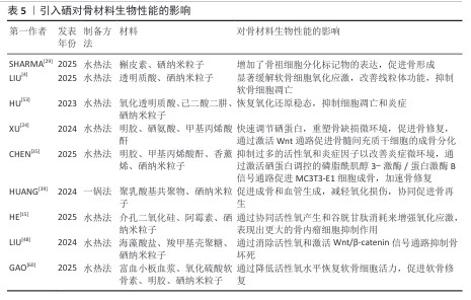
2.3.3 大骨节病 大骨节病是一种地方性、与环境相关的退行性软骨疾病,高发于俄罗斯西伯利亚东部、韩国以及中国东北至西南地区,大骨节病患者的主要临床特征是身材矮小和关节畸形。硒缺乏会导致软骨细胞的细胞外基质合成代谢和分解代谢失衡,并减少硒蛋白的生物合成,造成谷胱甘肽过氧化物酶活性缺乏,导致氧化应激增加。关节软骨代谢紊乱和硒蛋白生物合成紊乱共同诱导软骨细胞凋亡,导致软骨破坏和骨骺板病变。目前,已证明部分硒蛋白与大骨节病相关(表4)。ZHANG等[43]将人C28/I2软骨细胞系作为实验对象,发现硒缺乏可能通过激活Notch/Hes1信号通路诱导软骨细胞过度凋亡、加重氧化损伤,硒补充可逆转这一过程,从而参与大骨节病的病理过程。LIN等[49]通过T-2毒素作用于C28/I2软骨细胞24 h复制大骨节病软骨细胞自噬的抑制作用,发现T-2毒素可激活磷脂酰肌醇3-激酶/TSCR/脑ras同源蛋白/哺乳动物雷帕霉素靶蛋白信号通路,抑制人C28/I2软骨细胞自噬,引起软骨细胞损伤;给予硫酸软骨素A纳米元素硒处理后,发现硫酸软骨素A纳米元素硒可通过磷脂酰肌醇3-激酶/TSCR/脑ras同源蛋白/哺乳动物雷帕霉素靶蛋白信号通路减轻T-2毒素对自噬的抑制,从而对软骨细胞起到保护作用。MENG等[57]为了研究硒蛋白缺乏对骨骼的影响,使用Cre重组酶转基因小鼠系触发骨软骨祖细胞中Trsp基因缺失,Trsp编码硒代半胱氨酸tRNA[Ser]Sec,这是硒代半胱氨酸残基整合到硒蛋白中所必需的,结果显示突变小鼠表现出生长迟缓、骨骺生长板异常、骨骼骨化延迟以及关节、耳廓和气管软骨明显的软骨坏死,从表型上看,小鼠复制了许多大骨节病的病理特征,研究结果支持硒缺乏是大骨节病骨骼异常发病机制关键因素的观点。 以上研究表明,硒可以改善软骨细胞的周围环境,通过抗凋亡、促进软骨细胞自我更新以及调节细胞微环境为大骨节病治疗提供了潜在方向。 2.3.4 骨关节炎 骨关节炎是一种以关节软骨退变为主要特征的慢性疾病,由凋亡、细胞外基质降解和氧化应激引起。以往研究表明,骨关节炎与高浓度活性氧有关,当活性氧产生过多时引发氧化应激,导致炎症、软骨细胞凋亡、软骨功能障碍以及骨吸收和骨重塑的不平衡[58]。而清除活性氧的谷胱甘肽过氧化物酶是一个硒依赖的抗氧化酶家族,它催化许多过氧化物,包括过氧化脂质和过氧化DNA,分别转化为水和乙醇,保护细胞免受氧化应激。因此,抑制氧化应激已成为治疗骨关节炎的关键组成部分[59],对防止软骨细胞进一步损伤至关重要(图6)。 LIU等[4]设计了透明质酸修饰的硒纳米颗粒,并将透明质酸-硒纳米颗粒加载到醛功能化水凝胶微球中,通过微球的醛基与软骨氨基之间的希夫碱反应选择性地黏附在受损软骨表面,实现微米级靶向,同时不断释放透明质酸-硒纳米颗粒;透明质酸-硒纳米颗粒通过透明质酸表面与CD44结合实现纳米级靶向,CD44在骨关节炎软骨细胞膜上高度表达,透明质酸修饰硒纳米颗粒一旦被细胞摄取可直接清除活性氧,并通过生成亚硒酸盐促进硒蛋白合成,从而发挥作用,形成一个多功能的抗氧化防御系统,体内外实验结果表明,该系统通过级联靶向受损软骨和持久活性氧清除显著缓解软骨细胞氧化应激、抑制软骨细胞凋亡、延缓骨关节炎的进展。HU等[53]以氧化透明质酸与透明质酸-己二酸二肼交联制备水凝胶,通过希夫碱反应负载硒纳米颗粒,被硒纳米颗粒包裹的水凝胶具有毒性小和可持续的药物释放性能,通过清除活性氧和抑制细胞凋亡的协同作用促进软骨修复;在机制上,水凝胶通过靶向谷胱甘肽过氧化物酶1来恢复氧化还原稳态,在骨关节炎大鼠模型中证明了负载硒纳米颗粒水凝胶的治疗效果,包括软骨保护、炎症减轻和疼痛缓解。GAO等[60]将硒纳米颗粒与富血小板血浆结合在氧化硫酸软骨素-明胶支架中,利用硒纳米颗粒清除活性氧缓解氧化应激、恢复氧化还原平衡,从而减少骨关节炎微环境中的细胞外损伤和调节炎症;同时,利用富血小板血浆中的生长因子(如转化生长因子β、胰岛素样生长因子、成纤维细胞生长因子)回复衰老软骨细胞的活力,研究结果表明,硒纳米颗粒-富血小板血浆-氧化硫酸软骨素-明胶支架具有良好的生物相容性,可降低活性氧水平、缓解软骨细胞衰老、平衡细胞外基质稳态;此外,在骨关节炎大鼠模型中,该支架可促进软骨修复、缓解疼痛和加速功能恢复。CHENG等[36]用不同浓度硒处理SW1353细胞一定时间后,发现0.3 μmol/L硒可通过核因子E2相关因子2途径促进谷胱甘肽合成相关酶的基因表达,从而保护SW1353细胞免受小鼠细胞凋亡抑制因子诱导的损伤;此外,谷胱甘肽、超氧化物歧化酶、谷胱甘肽过氧化物酶等的表达也会升高,以消除过量的活性氧;下调核因子kB,导致细胞因子、基质蛋白酶和糖胺聚糖的减少,这些结果表明,硒摄入对骨关节炎有益。以上研究表明,硒可以改善软骨细胞的周围环境,通过抗凋亡、抗氧化、抗衰老、增强软骨的合成代谢,为骨关节炎治疗提供了新的视角。 "
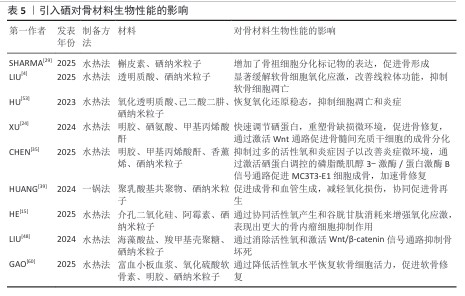
2.3.5 骨肉瘤 骨肉瘤是一种起源于间充质的类骨质恶性肿瘤,在组织病理学上可分为低、中、高级别,90%以上的骨肉瘤为高级别恶性肿瘤。由于代谢活动紊乱,骨肉瘤细胞固有的活性氧水平升高。通过特异性地使骨肉瘤细胞中活性氧水平超过临界阈值,可以选择性地靶向骨肉瘤细胞,同时不影响健康细胞。为了应对升高的活性氧,骨肉瘤细胞也上调谷胱甘肽的产生以维持骨肉瘤细胞的氧化还原稳态[61],这些水平远高于正常骨细胞内的谷胱甘肽水平,因此,消耗谷胱甘肽提供了加剧氧化应激和选择性破坏氧化还原稳态的机会[62-63]。利用骨肉瘤细胞与正常细胞的这些固有差异,上调氧化应激是一种通过程序性细胞死亡激活癌症选择性抑制的方法,有效提升骨肉瘤治疗效果。目前,鉴于硒的抗癌潜力,它对骨肉瘤的治疗作用已被广泛探索,有可能作为骨肉瘤的预防或治疗选择。在高剂量下,硒纳米颗粒可作为一种促氧化剂,与谷胱甘肽相互作用触发活性氧的产生和谷胱甘肽的消耗,从而促进氧化应激,破坏氧化还原稳态[64]。HE等[15]开发了一种pH值/氧化还原反应的MS递送系统(SeMSDox-SS-HA),使用二硫键和透明质酸来共包封硒纳米颗粒和阿霉素,用于骨肉瘤治疗,研究结果表明,低pH值和升高的谷胱甘肽水平可以激活硒纳米颗粒-阿霉素-介孔二氧化硅-透明质酸,导致骨肉瘤细胞内快速的阿霉素/硒释放,明显上调氧化应激;此外,SeMSDox-SS-HA通过协同活性氧产生和谷胱甘肽消耗增强氧化应激,显示出对骨肉瘤细胞的更强抑制作用,同时对人间充质干细胞无明显影响,这种选择性抑制可能源于骨肉瘤细胞中硒纳米颗粒-阿霉素-介孔二氧化硅-透明质酸的靶向活性氧上调和谷胱甘肽消耗。 表5总结了硒对各种骨材料生物性能的影响。 "
| [1] JAIN VK, PRIYADARSINI KI. Selenium: A Wonder Element in Life and for Life. Proc Natl Acad Sci, India A: Phys Sci. 2024;94:1-10. [2] OLDFIELD JE. The two faces of selenium. J Nutr. 1987;117(12):2002-2008. [3] WANG L, SAGADA G, WANG R, et al. Different forms of selenium supplementation in fish feed: The bioavailability, nutritional functions, and potential toxicity. Aquaculture. 2022;549:737819. [4] LIU J, LIU J, LIU S, et al. Cascade targeting selenium nanoparticles-loaded hydrogel microspheres for multifaceted antioxidant defense in osteoarthritis. Biomaterials. 2025;318:123195. [5] WANG Y, HAO H, LIU H, et al. Selenite‐Releasing Bone Mineral Nanoparticles Retard Bone Tumor Growth and Improve Healthy Tissue Functions In Vivo. Adv Healthc Mater. 2015;4:1813-1818. [6] ZOU X, WANG Y, SUN R, et al. An analysis of the content changes in free and combinative forms of organic selenium in radish sprouts cultivated with solutions of selenoamino acids. Food Res Int. 2022;158:111558. [7] LIU H, BIAN W, LIU S, et al. Selenium Protects Bone Marrow Stromal Cells Against Hydrogen Peroxide-Induced Inhibition of Osteoblastic Differentiation by Suppressing Oxidative Stress and ERK Signaling Pathway. Biol Trace Elem Res. 2012;150(1-3):441-450. [8] LEITER O, ZHUO Z, RUST R, et al. Selenium mediates exercise-induced adult neurogenesis and reverses learning deficits induced by hippocampal injury and aging. Cell Metabolism. 2022;34:408-423.e408. [9] WU Z, HOU Q, QIN L, et al. GPx-mimetic selenium-enriched yeast nanozymes ameliorate diabetic bone disease via dual-targeting of ROS scavenging and angiogenesis-osteogenesis coupling. Mater Today Bio. 2025;32:101836. [10] KIM H, LEE K, KIM JM, et al. Selenoprotein W ensures physiological bone remodeling by preventing hyperactivity of osteoclasts. Nat Commun. 2021;12(1):2258. [11] TURCK D, BOHN T, CASTENMILLER J, et al. Scientific opinion on the tolerable upper intake level for selenium. EFSA J. 2023;21(1):e07704. [12] VENTURA M, MELO M, CARRILHO F. Selenium and Thyroid Disease: From Pathophysiology to Treatment. Int J Endocrinol. 2017;2017:1297658. [13] YANG H, YANG X, NING Z, et al. The beneficial and hazardous effects of selenium on the health of the soil-plant-human system: An overview. J Hazard Mater. 2022;422:126876. [14] ZHANG F, LI X, WEI Y. Selenium and Selenoproteins in Health. Biomolecules. 2023;13:799. [15] HE L, JAVID ANBARDAN Z, HABIBOVIC P, et al. pH- and redox-sensitive selenium-incorporated mesoporous silica nanoparticles for osteosarcoma-targeted treatment. Mater Design. 2025;253:113883. [16] ZHOU H, HE Z, CAO Y, et al. An injectable magnesium-loaded hydrogel releases hydrogen to promote osteoporotic bone repair via ROS scavenging and immunomodulation. Theranostics. 2024;14:3739-3759. [17] AVERY J, HOFFMANN P. Selenium, Selenoproteins, and Immunity. Nutrients. 2018;10:1203. [18] SCHOMBURG L. Selenium, selenoproteins and the thyroid gland: interactions in health and disease. Nat Rev Endocrinol. 2011;8(3):160-171. [19] GUILLIN O, VINDRY C, OHLMANN T, et al. Selenium, Selenoproteins and Viral Infection. Nutrients. 2019;11:2101. [20] ZHOU Q, CHEN W, GU C, et al. Selenium-modified bone cement promotes osteoporotic bone defect repair in ovariectomized rats by restoring GPx1-mediated mitochondrial antioxidant functions. Regen Biomater. 2023;10:rbad011. [21] CHEN X, CAI K, FANG J, et al. Fabrication of selenium-deposited and chitosan-coated titania nanotubes with anticancer and antibacterial properties. Colloids Surf B Biointerfaces. 2013; 103:149-157. [22] XUE N, DING X, HUANG R, et al. Bone Tissue Engineering in the Treatment of Bone Defects. Pharmaceuticals (Basel). 2022;15:879. [23] SRINIVASAN A, RAJENDRAN N. Surface characteristics, corrosion resistance and MG63 osteoblast-like cells attachment behaviour of nano SiO2–ZrO2coated 316L stainless steel. RSC Adv. 2015;5:26007-26016. [24] XU R, YOU Y, ZHENG W, et al. Selenoprotein‐Regulated Hydrogel for Ultrasound‐Controlled Microenvironment Remodeling to Promote Bone Defect Repair. Adv Funct Mater. 2024;34:1-15. [25] KANG D, LEE J, WU C, et al. The role of selenium metabolism and selenoproteins in cartilage homeostasis and arthropathies. Exp Mol Med. 2020;52(8):1198-1208. [26] SHIMADA BK, SWANSON S, TOH P, et al. Metabolism of Selenium, Selenocysteine, and Selenoproteins in Ferroptosis in Solid Tumor Cancers. Biomolecules. 2022;12:1581. [27] SANTOS LR, NEVES C, MELO M, et al. Selenium and Selenoproteins in Immune Mediated Thyroid Disorders. Diagnostics. 2018;8:70. [28] DUNTAS LH. BENVENGA S. Selenium: an element for life. Endocrine. 2014;48:756-775. [29] SHARMA G, LEE YH, KIM JC, et al. Bone Regeneration Enhanced by Quercetin-Capped Selenium Nanoparticles via miR206/Connexin43, WNT, and BMP signaling pathways. Aging Dis. 2025. doi: 10.14336/AD.2025.0025. [30] MOJADADI A, AU A, SALAH W, et al. Role for Selenium in Metabolic Homeostasis and Human Reproduction. Nutrients. 2021;13:3256. [31] SEALE LA, HA HY, HASHIMOTO AC, et al. Relationship between selenoprotein P and selenocysteine lyase: Insights into selenium metabolism. Free Radic Biol Med. 2018;127:182-189. [32] MANOLAGAS SC. From Estrogen-Centric to Aging and Oxidative Stress: A Revised Perspective of the Pathogenesis of Osteoporosis. Endocr Rev. 2010;31(3):266-300. [33] RODRÍGUEZ-HERNÁNDEZ Á, ZUMBADO M, HENRÍQUEZ-HERNÁNDEZ LA, et al. Dietary Intake of Essential, Toxic, and Potentially Toxic Elements from Mussels (Mytilus spp.) in the Spanish Population: A Nutritional Assessment. Nutrients. 2019;11:864. [34] CHEN L, YANG J, CAI Z, et al. Cerium Dioxide Nanoparticles‐Based Inspector Enhances Mitochondrial Quality Control to Maintain Chondrocyte Homeostasis in Osteoarthritis Therapy. Adv Healthc Mater. 2025;14:2405069. [35] CHEN Y, XU R, XIE B, et al. Ultrasound-Driven Selenium Nanoparticles Realize Bone Defect Repair through Activating Selenoproteins to Regulate PI3K/AKT Signaling Pathway. ACS Nano. 2025;19:18256-18269. [36] CHENG HL, YEN CC, HUANG LW, et al. Selenium Lessens Osteoarthritis by Protecting Articular Chondrocytes from Oxidative Damage through Nrf2 and NF-κB Pathways. Int J Mol Sci. 2024; 25(5):2511. [37] ALAJMI K, HARTFORD M, ROY S, et al. Correction: Selenium nanoparticle-functionalized injectable chitosan/collagen hydrogels as a novel therapeutic strategy to enhance stem cell osteoblastic differentiation for bone regeneration. J Mater Chem B. 2024;12(40):10434. [38] QIAO L, GUO Z, LIU H, et al. Protective Effect of Mitophagy Regulated by mTOR Signaling Pathway in Liver Fibrosis Associated with Selenium. Nutrients. 2022;14:2410. [39] HUANG L, ZHANG S, BIAN M, et al. Injectable, anti-collapse, adhesive, plastic and bioactive bone graft substitute promotes bone regeneration by moderating oxidative stress in osteoporotic bone defect. Acta Biomater. 2024;180:82-103. [40] BRYLIŃSKI Ł, KOSTELECKA K, WOLIŃSKI F, et al. Effects of Trace Elements on Endocrine Function and Pathogenesis of Thyroid Diseases—A Literature Review. Nutrients. 2025;17:398. [41] STEINBRENNER H, SPECKMANN B, KLOTZ LO. Selenoproteins: Antioxidant selenoenzymes and beyond. Arch Biochem Biophys. 2016;595:113-119. [42] DING Y, DAI Y, WU M, et al. Glutathione-mediated nanomedicines for cancer diagnosis and therapy. Chem Eng J. 2021;426:128880. [43] ZHANG D, ZHANG D, YANG X, et al. The Role of Selenium-Mediated Notch/Hes1 Signaling Pathway in Kashin–Beck Disease Patients and Cartilage Injury Models. Biol Trace Elem Res. 2023; 201(6):2765-2774. [44] LI H, JIA L, DENG Z, et al. The effects of selenium on the growth and bone development in the weaned rats. Food Biosci. 2023;55:103018. [45] MENG B, WU D, CHENG Y, et al. Interleukin‐20 differentially regulates bone mesenchymal stem cell activities in RANKL‐induced osteoclastogenesis through the OPG/RANKL/RANK axis and the NF‐κB, MAPK and AKT signalling pathways. Scand J Immunol. 2020;91(5):e12874. [46] RAHMAN MS, AKHTAR N, JAMIL HM, et al. TGF-β/BMP signaling and other molecular events: regulation of osteoblastogenesis and bone formation. Bone Res. 2015;3:1-20. [47] ZHAN Z, ZHANG J, XIAO J. Selenoproteins and selenium status in bone physiology and pathology. Biochim Biophys Acta. 2014;1840(11):3246-3256. [48] LIU C, WANG C, LIU Y, et al. Selenium nanoparticles/carboxymethyl chitosan/alginate antioxidant hydrogel for treating steroid-induced osteonecrosis of the femoral head. Int J Pharm. 2024;653:123929. [49] LIN X, LIU H, QIAO L, et al. Chondrocyte autophagy mediated by T-2 toxin via AKT/TSC/Rheb/mTOR signaling pathway and protective effect of CSA-SeNP. Osteoarthritis Cartilage. 2024; 32(10):1283-1294. [50] HSU YH, KIEL DP. Genome-Wide Association Studies of Skeletal Phenotypes: What We Have Learned and Where We Are Headed. J Clin Endocrinol Metab. 2012;97:1958-1977. [51] HUANG Y, JIA Z, XU Y, et al. Selenium protects against LPS-induced MC3T3-E1 cells apoptosis through modulation of microRNA-155 and PI3K/Akt signaling pathways. Genet Mol Biol. 2020;43(3):e20190153. [52] KIELISZEK M. Selenium–Fascinating Microelement, Properties and Sources in Food. Molecules. 2019; 24(7):1298. [53] HU W, YAO X, LI Y, et al. Injectable hydrogel with selenium nanoparticles delivery for sustained glutathione peroxidase activation and enhanced osteoarthritis therapeutics. Materials Today Bio. 2023;23:100864. [54] RADOMSKA D, CZARNOMYSY R, RADOMSKI D, et al. Selenium Compounds as Novel Potential Anticancer Agents. Int J Mol Sci. 2021;22(3):1009. [55] WANG W, WANG C, LIU G, et al. In‐vivo two‐photon visualization and quantitative detection of redox state of cancer. J Biophotonics. 2022; 15(5):e20210035. [56] WU Q, RAYMAN MP, LV H, et al. Low Population Selenium Status Is Associated With Increased Prevalence of Thyroid Disease. J Clin Endocrinol Metab. 2015;100(11):4037-4047. [57] MENG X, MENG X, HE Z, et al. Selenium Deficiency Can Promote the Expression of VEGF and Inflammatory Factors in Cartilage Differentiation and Mediates Cartilage Injury. Biol Trace Elem Res. 2024;202(9):4170-4179. [58] ZENG H, CAO J, COMBS G. Selenium in Bone Health: Roles in Antioxidant Protection and Cell Proliferation. Nutrients. 2013;5:97-110. [59] HORWITZ MS, DOWNEY CM, HORTON CR, et al. Osteo-Chondroprogenitor–Specific Deletion of the Selenocysteine tRNA Gene, Trsp, Leads to Chondronecrosis and Abnormal Skeletal Development: A Putative Model for Kashin-Beck Disease. PLoS Genet. 2009;5(8):e1000616. [60] GAO WY, LI SC, MIAO Y, et al. Selenium Nanozyme-Crosslinked Composite Hydrogel for Promoting Cartilage Regeneration in Osteoarthritis via an Integrated ‘OutsideIn’ and ‘Inside-Out’ Strategy. J Colloid Interf Sci. 2025;693:137612. [61] COSTA NSD, LIMA LS, GALICIOLLI MEA, et al. Drug-induced osteoporosis and mechanisms of bone tissue regeneration through trace elements. J Trace Elem Med Biol. 2024;84:127446. [62] HAO S, YAO C, MENG P, et al. HT-2 mycotoxin and selenium deficiency: Effects on Femur development and integrity in Young mice. Toxicon. 2024;245:107767. [63] WEN X, ZHOU Q, LIN S, et al. Selenium-modified hydroxyapatite titanium coating: enhancing osteogenesis and inhibiting cancer in bone invasion by head and neck squamous cell carcinoma. Front Bioeng Biotechnol. 2025;13: 1552661. [64] ZOU B, XIONG Z, YU Y, et al. Rapid Selenoprotein Activation by Selenium Nanoparticles to Suppresses Osteoclastogenesis and Pathological Bone Loss. Adv Mater. 2024;36:2401620. |
| [1] | Wang Songpeng, Liu Yusan, Yu Huanying, Gao Xiaoli, Xu Yingjiang, Zhang Xiaoming, Liu Min. Bidirectional regulation of reactive oxygen species based on zeolitic imidazolate framework-8 nanomaterials: from tumor therapy and antibacterial activity to cytoprotection [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(8): 2033-2013. |
| [2] | Liu Dawei, Cui Yingying, Wang Fanghui, Wang Zixuan, Chen Yuhan, Li Yourui, Zhang Ronghe. Epigallocatechin gallate-mediated bidirectional regulation of reactive oxygen species and its application in nanomaterials [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(8): 2101-2112. |
| [3] | Yuan Qian, Zhang Hao, Pang Jie. Characterization and biological properties of naringin-loaded chitosan/beta-tricalcium phosphate scaffold [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(2): 424-432. |
| [4] | Gong Yukang, Ye Gaoqi, Wang Chenhao, Chen Dejin, Gao Wenshan. Effects and mechanisms of natural polyphenol-based hydrogels in promoting bone repair [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(14): 3675-3686. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||

