Chinese Journal of Tissue Engineering Research ›› 2024, Vol. 28 ›› Issue (9): 1426-1435.doi: 10.12307/2023.904
Previous Articles Next Articles
Advantages and application strategies of machine learning in diagnosis and treatment of lumbar disc herniation
Yu Weijie1, 2, 3, Liu Aifeng1, 2, Chen Jixin1, 2, 3, Guo Tianci1, 2, 3, Jia Yizhen1, 2, 3, Feng Huichuan1, 2, 3, Yang Jialin1, 2, 3
- 1First Teaching Hospital of Tianjin University of Traditional Chinese Medicine, Tianjin 300381, China; 2National Clinical Research Center of Chinese Medicine Acupuncture and Moxibustion, Tianjin 300381, China; 3Tianjin University of Traditional Chinese Medicine, Tianjin 301617, China
-
Received:2022-11-25Accepted:2023-01-18Online:2024-03-28Published:2023-07-26 -
Contact:Liu Aifeng, MD, Chief physician, Doctoral supervisor, First Teaching Hospital of Tianjin University of Traditional Chinese Medicine, Tianjin 300381, China; National Clinical Research Center of Chinese Medicine Acupuncture and Moxibustion, Tianjin 300381, China -
About author:Yu Weijie, Doctoral candidate, First Teaching Hospital of Tianjin University of Traditional Chinese Medicine, Tianjin 300381, China; National Clinical Research Center of Chinese Medicine Acupuncture and Moxibustion, Tianjin 300381, China; Tianjin University of Traditional Chinese Medicine, Tianjin 301617, China -
Supported by:Tianjin Science and Technology Plan Project, No. 21KPXMRC00050 (to LAF); Tianjin Traditional Chinese Medicine Rehabilitation Appropriate Technology Promotion Project (to LAF)
CLC Number:
Cite this article
Yu Weijie, Liu Aifeng, Chen Jixin, Guo Tianci, Jia Yizhen, Feng Huichuan, Yang Jialin. Advantages and application strategies of machine learning in diagnosis and treatment of lumbar disc herniation[J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1426-1435.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
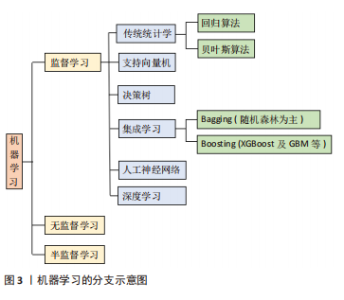
2.1 机器学习分类 目前,机器学习在腰椎间盘突出症的应用包括机器学习监督学习、无监督学习和半监督学习方式,见图3。虽然机器学习的类别较多,但不同模型具有其自身的特点和优势。回归算法临床应用较多,可探究腰椎间盘突出症危险因素和解决临床预测问题;贝叶斯基于分类算法的特点可用于腰椎间盘突出症诊断;支持向量机适用于高维特征的小数据集,可对正常或退变椎间盘进行识别、分割、分类;决策树凭借其模型可解释性强多应用于分析腰椎间盘突出症危险因素;集成学习弥补了单一模型的不足,可实现椎间盘分类和腰椎间盘突出症术后预测;人工神经网络模仿生物神经元间的相互连接作用,提高算力和性能,可用于椎间盘识别、分类,制作临床预测模型;深度学习是具有深层结构的神经网络,在具有以上用途的基础上,还能优化图像,辅助手术操作;而无监督学习和半监督学习目前应用相对较少,主要在椎间盘分割、分类以及图像优化领域。此部分将根据不同算法在腰椎间盘突出症中的应用特点和优缺点进行具体分析。"
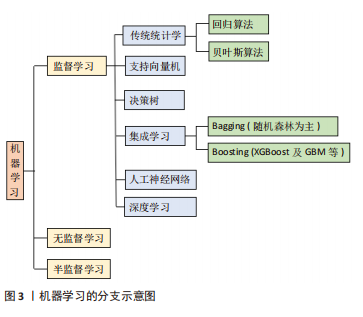

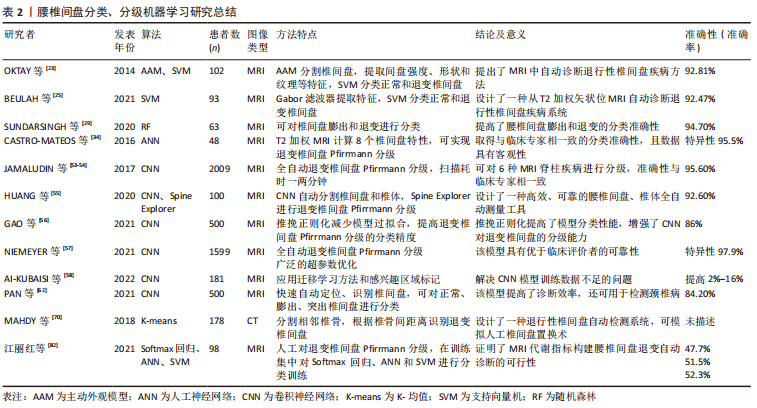
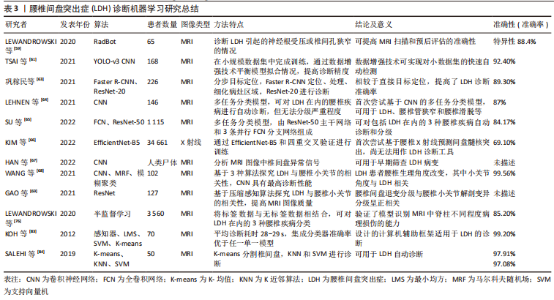
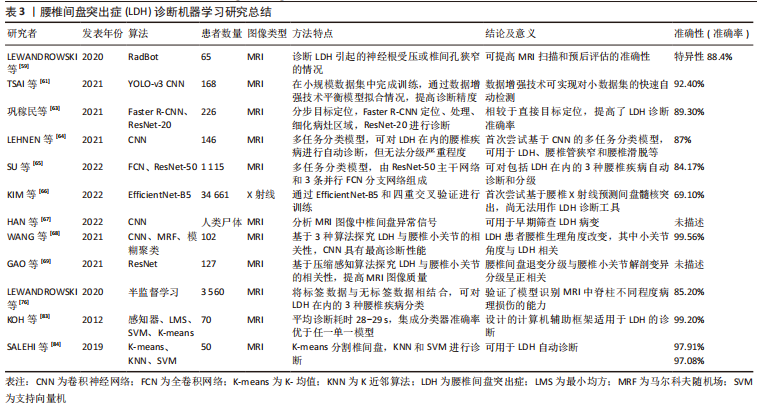
2.1.1 监督学习算法 监督学习是通过将已知特征的数据输入计算机,分析获得对应的输出数据作为训练集,从而预测其他输入数据的输出结果,目前,临床应用较为广泛,包括传统统计学方法、支持向量机(support vector machine,SVM)、决策树、集成学习、人工神经网络和深度学习等[12]。 传统统计学分析:基于传统统计学方法的机器学习算法主要包括回归算法和贝叶斯算法。回归算法以线性回归和Logistic回归为主,多解决临床预测问题,可分析腰椎间盘突出症与其危险因素的相关性。由于其操作的简易性,常作为对比模型进行分析[14]。贝叶斯算法则是基于统计概率实施的分类算法,在假设数据特征彼此独立的前提下,通过联合计算独立特征概率获取最终类别的概率,适用于小规模多分类数据。 回归算法是临床探究腰椎间盘突出症危险因素、分析治疗预后的常用算法。YU等[15]基于200例腰椎间盘突出症患者影像组学特征,通过多元Logistic模型制作列线图预测工具,可用于保守治疗的疗效预测,ROC曲线下面积(area under the curve,AUC)值为0.93,准确率为91%。HIRAYAMA等[16]利用多元回归模型分析影响腰椎间盘突出症患者腰椎牵引疗效的因素,其中主要包括腰椎活动范围、心理因素、症状发作频率和时间等。而在手术治疗研究中,邱洪波等[17]构建经皮椎间孔镜(percutaneous transforaminal endoscopic discectomy,PTED)治疗腰椎间盘突出症术后复发临床预测模型,通过回归分析筛选危险因素,将患者年龄、糖尿病史、病程、工作强度、椎间盘退变程度纳入模型实现预测,AUC值为0.944,具有良好的区分度,有利于降低术后复发率。另一项研究则构建了经皮内镜腰椎间盘切除(percutaneous endoscopic lumbar discectomy,PELD)术后复发预测模型,基于回归分析筛选出年龄、手术节段、椎间盘退变、吸烟史和职业为主要危险因素,模型AUC值为0.909[18]。国外学者基于1 706例接受经皮内镜腰椎间盘切除治疗的腰椎间盘突出症患者资料,通过回归分析筛选出包含椎间盘退变在内的11个危险因素,构建相同用途的预后模型,准确率为97.6%[19]。除此以外,LI等[20]通过表面肌电图获取下肢参数,利用回归模型诊断腰椎间盘突出症受压神经根水平,AUC值达到0.95。 贝叶斯算法在腰椎间盘突出症诊断中具有一定优势。SUSTERSIC等[21]提出一种基于贝叶斯理论的腰椎间盘突出症诊断方法,与常规MRI辅助诊断不同,基于56例腰椎间盘突出症患者和15名健康受试者的数据集,分析正常站立、前足站立和脚跟站立时下肢力量差异,从而明确腰椎间盘突出症突出节段,朴素贝叶斯网络的平均准确率为83.1%,灵敏度为57.6%,特异性为88.2%。不难看出,传统统计学方法适用于探究腰椎间盘突出症危险因素,其构建的临床诊断模型可明确腰椎间盘突出症受压神经根水平,而预后模型则应用于腰椎间盘突出症保守、椎间孔镜治疗中,并且主要以Logistic回归分析为主。然而,受限于模型特征,难以拟合数据的真实分布以及无法筛选特征,目前多以对比模型的形式应用于预后分析中,作为深度学习或其他机器学习方法的对照组。 支持向量机:是一种基于核函数的分类算法,泛化能力强,其试图找到与最近点(支持向量)距离最大的分离超平面,适用于高维特征的小数据集,缺点是在处理海量数据时,会占用较大内存资源,提高了计算和数据空间的复杂性,造成运算时间延长[12]。 支持向量机可识别、分割和分类正常或退变椎间盘。2013年,OKTAY等[22]采用支持向量机对椎间盘边缘和方向进行特征提取,结合马尔科夫随机场同时定位椎体,将腰椎几何结构与局部图像信息相结合,分类准确率达到89.41%。2014年,OKTAY等[23]加入T1加权的腰椎矢状位MRI图像,利用计算机辅助系统分类正常和退变椎间盘,将102例受试者的612份椎间盘图像特征输入支持向量机训练模型,分类准确率达92.81%。GHOSH等[24]利用支持向量机训练椎间盘定向梯度直方图特征,可同时分割椎骨、椎间盘及硬膜囊等,定位准确率达到98%,误差小于2.08 mm。在2021年,BEULAH等[25]基于腰椎矢状位MRI分割椎间盘,利用Gabor滤波器提取特征,最后通过支持向量机分类正常和退变椎间盘,达到92.47%的准确率。除此以外,支持向量机适用于腰椎间盘突出症的临床诊断和分类。LI等[26]将支持向量机应用于识别腰椎间盘突出症诊断生物标志物,检测髓核中相关基因的表达水平,为腰椎间盘突出症靶向治疗提供理论基础。 综上可知,支持向量机可应用于正常或退变椎间盘的识别、分割、分类,有效提高了精度和准确性,为下一步提取腰椎间盘影像数据开展生物力学分析、组织工程构建提供精确数据保障;同时可对正常和退变椎间盘进行鉴别分类,提高了对退变间盘的早期识别和诊断效率,还能筛查腰椎间盘突出症基因表达水平。然而,作为一种二分类算法,难以解决多分类问题,同时难以训练大规模数据集,近年来,深度学习的快速发展有效弥补了其缺点和不足。 决策树:是一种基于实例的归纳学习算法,可从给定的无序训练集中归纳出有效的分类模型,由于决策流程形似一棵树的枝干,故称决策树。该算法属于线性结构,数据处理效率较高,可解释性强,适用于实时分类场景,然而,在面对较多类别时可增加分类错误概率[12]。目前,决策树主要适用于分析腰椎间盘突出症危险因素。PAPIC等[27]基于145例接受显微椎间盘切除的腰椎间盘突出症患者数据,通过决策树模型筛选影响患者术后重返工作的危险因素,其中包括心理社会因素、脊柱的活动性、小关节改变和体态姿势等。WIRRIES等[28]则利用决策树模型分析腰椎间盘突出症术后根性神经痛的影响因素,以筛选出的心理状态、体质量和年龄等因素为输入变量,以目测类比评分和Oswestry功能障碍分数(Oswestry disability index,ODI)改善情况为输出变量构建预测模型,可避免不必要的手术所造成的术后神经症状,为腰椎间盘突出症保守或手术治疗选择提供评估工具。 由此可知,决策树在分析腰椎间盘突出症危险因素方面应用广泛,具有效率高和易于理解的优点,相较于黑盒模型更易观察。但是,此算法容易产生复杂模型,出现过拟合的情况,降低泛化性能;除此以外,模型对于数据微小变化可出现不同的树模型,稳定性较低。 集成学习:包含数个弱监督学习模型,可对相关学习任务进行分类,根据个体学习模型的生成方式可分为并行训练的Bagging和串行训练的Boosting,其中随机森林(random forest,RF)是最常用的Bagging模型,而极端梯度提升(extreme gradient boosting,XGBoost)和梯度提升机(gradient boosting machine,GBM)是较常用的Boosting模型。集成学习可相互弥补单一模型的不足,具有处理高维数据的能力,可在降低误诊率的同时提高运算速度[12]。 目前,集成学习可应用于椎间盘分类和腰椎间盘突出症术后预测等方面。在2020年,SUNDARSINGH等[29]分别利用定向梯度直方图提取椎间盘形状特征,新型局部二值模式提取纹理特征,最后随机森林分类器对椎间盘膨出和退变进行分类,达到94.7%的准确率。KARHADE等[30]针对腰椎间盘突出症患者腰椎间盘切除术的手术记录资料,采用自然语言处理(natural language processing,NLP)对XGBoost模型进行训练,构建90 d内因感染再次手术的预后模型,在外部验证时AUC值达到0.999,Brier评分为0.003。鲍军平等[31]则基于395例接受经皮内镜腰椎间盘切除治疗的腰椎间盘突出症患者资料,通过梯度提升机构建术后疗效预测模型,通过多因素Logistic回归分析确定年龄、突出物矢状径、突出方向、椎间盘退变水平等因素是术后疗效不佳的危险因素,AUC值可达0.92,模型灵敏度和特异性分别为93.46%和83.33%,可有效预测经皮内镜腰椎间盘切除术后近期疗效。2021年,HARADA等[32]基于XGBoost模型,将2 630例腰椎间盘突出症患者术前目测类比评分及Oswestry功能障碍评分、腰椎矢状面参数、体质量指数、症状持续时间和年龄等预测因子作为输入端,复发性髓核突出作为输出端,构建腰椎显微间盘切除术后复发性腰椎间盘突出症的风险预测模型,准确率为70%,AUC值为0.72,可为患者手术选择提供参考。2022年,ZHAO等[33]则针对142例接受物理治疗的腰椎间盘突出症患者临床数据,以目测类比评分改善度作为疗效评估指标,通过梯度提升机构建疗效预测模型,AUC值为0.936,敏感性为93.3%,特异性为87.5%。 集成学习有效弥补了单一模型的不足,在椎间盘分类和腰椎间盘突出症术后预测方面应用广泛,有效提高了模型精度和准确性。其中,Boosting模型较多应用于术后疗效和腰椎间盘突出症复发预测中;而随机森林集成了决策树的优点,可视为大量树模型构成的算法,提高了模型稳定性和处理数据能力。然而,过拟合、训练耗时、模型解释性较差等仍是集成学习目前应用存在的不足。 人工神经网络:是一种模仿生物神经元间的相互连接作用而建立的信息处理系统,将输入信息通过人工神经元流向输出端口,通过调整神经元间连接权重获得最佳值,使输出结果无限接近真实情况,从而减少诊断过程中人为干扰。目前,其可用于非线性统计数据、模糊数据和随机性数据建模,临床上以诊断预测、疾病分类和图像分析为主[12]。 人工神经网络可对腰椎间盘突出症退变椎间盘进行识别和分类。CASTRO-MATEOS等[34]基于48名受试者的240份腰椎椎间盘MRI图像,选取8个特征进行提取,利用人工神经网络进行退变椎间盘Pfirrmann分级,特异性达95.5%,敏感性为87.3%,与专家分类结果相符。除此以外,OYEDOTUN等[35]借助人工神经网络自动诊断腰椎间盘突出症和腰椎滑脱,通过有限元分析技术,提取患者骨盆投射角、骶骨倾斜角和腰椎前凸角等6个力学参数进行分析,可达到99.05%的精度。 人工神经网络可进行腰椎间盘突出症预后分析,构建相关预测模型。针对腰椎间盘突出症早期保守治疗,WIRRIES等[36]收集60例腰椎间盘突出症患者资料,通过人工神经网络预测临床保守和手术治疗6个月后的Oswestry功能障碍评分发现,其与实际评分差值仅为3.4%,既可以在腰椎间盘突出症病变早期识别从保守治疗中受益的患者,也避免延误适宜手术患者的最佳治疗时机。在2015年,AZIMI等[37]基于402例接受显微椎间盘切除术治疗的腰椎间盘突出症患者年龄、性别、腰椎间盘突出症类型等临床数据,构建人工神经网络模型预测腰椎间盘突出症术后复发,准确率为94.1%,AUC值为0.83。在2016年,AZIMI等[38]继续利用人工神经网络模型对203名腰椎间盘突出症患者的数据进行训练和验证,可预测腰椎间盘突出症患者手术疗效,准确率为95.8%,AUC值达到0.82。MATIS等[39]则利用人工神经网络构建预测模型,评估了腰椎间盘突出症治疗后患者满意度,其中女性、高龄和较高学历患者满意度更高,准确率为96%,AUC值达到0.985。2018年,KARHADE等[40]依据美国国家外科质量改进计划数据库,从中选取26 364例接受手术治疗的腰椎间盘疾病患者数据,通过随机森林筛选出年龄、性别和体质量指数等预测因子,基于人工神经网络构建非常规出院预测模型,AUC值为0.815,有助于对接受择期手术的腰椎间盘突出症患者进行术前风险分层。在2019年,STOPA等[41]在此基础上完成了模型的外部验证,通过对144例相同纳入标准的患者进行分析,模型AUC值为0.89,证明了模型的泛化能力和外推性。同年,STAARTJES等[42]发现人工神经网络同样可以预测腰椎间盘突出症患者报告结局(patient-reported outcome,PRO),基于患者腿痛、腰痛和功能障碍改善情况,在422例接受显微椎间盘切除术的腰椎间盘突出症患者样本中准确率分别达到85%、87%和75%,AUC值为0.87、0.90和0.84。因此,人工神经网络可实现较高精度的腰椎间盘突出症术后预测,且适用于Oswestry功能障碍分数评分、复发率、满意度和PRO量表评分等各种评价指标。 目前,人工神经网络主要应用于椎间盘识别、分类,制作临床预测模型,由于具有处理海量、高维数据的能力,有效提高了模型的学习能力,成为近年来机器学习快速发展的原因之一。然而,人工神经网络的黑箱属性使得模型的可解释性较差,同时将问题属性以数值运算代替,可造成信息丢失。未来,有必要针对算法理论和模型评价进一步完善,并且与传统机器学习方法相结合,发挥各自优势,提高模型性能。 深度学习:是一种具有深层结构的神经网络,包含更多隐藏层,通过逐层变换将低层特征数据转化为更加抽象的高层特征数据,尽可能逼近真实情况,可对未知数据进行预测,包括卷积神经网络(convolutional neural network,CNN)、全卷积网络(fully convolutional network,FCN)等,其在图像识别和处理方面的巨大优势,有利于腰椎间盘突出症的临床诊断和分类。 深度学习算法可提高椎间盘识别、标记的精度。NATALIA等[43]基于48 345份腰椎MRI图像,通过CNN提取图像特征,可实现自动标记椎间盘一半高度的最佳横切面。WIMMER等[44]通过将局部熵优化纹理模型与CNN相结合,构建跨模态自动标记学习框架,适用于不同序列的MRI T1,T2加权、MR Dixon和CT扫描,可同时定位椎间盘和椎体,达到92.5%标记精度。 深度学习算法还可以提高腰椎间盘的分割精度。2018年,LI等[45]提出一个使用3D多尺度FCN结合随机模态体素缺失训练的学习框架,分割MRI中椎间盘,基于MICCAI挑战赛的24组数据集验证结果,平均Dice值可达到91.2%,定位误差为0.62 mm。KIM等[46]基于CNN的BSU-Net分割椎间盘,应用级联学习法克服U-Net最大池化层结构限制,Dice值优于U-Net(89.44%比86.44%)。而HAN等[47]基于253例患者MRI数据,采用递归生成对抗网络Spine-GAN同时分割椎间盘、椎骨和椎间孔,达到96.2%精度,Dice值为87.1%。2020年,FAN等[48]首先通过CNN的3D U-Net同时自动分割腰骶神经、椎骨和椎间盘,Dice值分别为0.94、0.92和0.92,之后在L5/S1水平三维重建Kambin三角,模拟椎间孔成形术,有利于经皮椎间孔镜的手术难度预测。2021年,SUSTERSIC等[49]采用U-Net进行全自动间盘分割,不同于传统轮廓分割技术,无需对参数进行校正和优化,Dice值为87.57%,同时能计算椎间盘中心到椎间盘边缘点的距离,鉴别突出或正常椎间盘。2022年,NAZIR等[50]基于FCN中的2D U-Net分割网络,通过3个平面分割椎间盘,利用聚类算法提取椎间盘模块,最后融合集成ECSU-Net,Dice值可达到95.6%,分类准确率为96.2%。LIU等[51]基于3D U-Net在L5/S1水平分割腰椎结构,其中椎间盘分割Dice值为90.39%,可快速生成3D腰骶椎间孔模型,帮助医生规划腰椎间盘突出症经椎间孔手术入路方案。除此以外,国内学者基于腰椎CT图像,通过3D V-Net识别、分割椎间盘,同时提取DICOM数据生成图像,可实现椎间盘自动识别、分割及重建[52]。 深度学习算法还在正常或退变椎间盘的分类、分级中具有明显优势。在2017年,JAMALUDIN等[53-54]基于12 018份腰椎间盘MRI图像,利用CNN实现全自动化退变椎间盘Pfirrmann分级,无需人工干预,准确率达95.6%,可标注出分级依据图像热区,与放射科医师分类结果相一致,同时可对6种MRI脊柱疾病进行分级。在2020年,HUANG等[55]研制了Spine Explorer深度学习模型,借助CNN的分割优势,可在半秒内完成椎间盘和椎体的分割和Pfirrmann分级,达到92.6%的准确率。2021年,GAO等[56]基于500名受试者腰椎MRI图像,在VGG-M、VGG-16、GoogleNet和ResNet-34这4个CNN模型中利用推挽正则化防止模型过拟合情况,有效提高Pfirrmann分级中不同程度退变椎间盘的分类精度和准确率。NIEMEYER等[57]根据1 599名受试者的7 948份椎间盘MRI,通过CNN实现退变椎间盘Pfirrmann自动分级,利用广泛的超参数优化,取得高于放射科医生间的可靠性(к =0.92比0.87),特异性为97.9%,敏感性达到90.2%。在2022年, AI-KUBAISI等[58]应用迁移学习方法和感兴趣区域标记,解决CNN模型训练数据不足的问题,提高VGG19、ResNet-50、MobileNet-V2和VGG16模型的腰椎间盘分类性能。 近年来,深度学习算法的应用提高了腰椎间盘突出症诊断分级的准确率。在2020年,LEWANDROWSKI等[59]基于RadBot算法诊断MRI中腰椎间盘突出症引起的神经根受压或椎间孔狭窄的情况,AUC值为0.808,基于该模型还能预测靶向内镜椎间孔减压手术的治疗效果[60]。在2021年,TSAI等[61]利用YOLO-v3在小规模数据集中完成训练,通过数据增强技术平衡模型拟合情况,提高腰椎间盘突出症诊断精度,最高可达92.4%。PAN等[62]首先基于R-CNN快速自动定位、识别椎间盘,准确率达100%,最后利用ResNet-101对正常、膨出、突出椎间盘进行分类,L4/5节段分类准确率可达90.4%。巩稼民等[63]同样利用分步目标定位方法,首先通过Faster R-CNN定位、处理、细化病灶区域,最后利用ResNet-20诊断腰椎间盘突出症,相较于直接目标定位的 ResNet-20 分类方法,将腰椎间盘突出症的诊断准确率提升5.1%。LEHNEN等[64]首次尝试基于CNN的多任务分类模型,可对MRI中多种腰椎疾病进行自动诊断,腰椎间盘突出症诊断准确率为87%,但无法分级腰椎间盘突出症严重程度。2022年,SU等[65]进一步优化算法,将ResNet-50作为主干网络,设立3条并行FCN分支网络,构成多任务分类模型,基于1 115例患者的16 527份腰椎MRI数据,可对腰椎间盘突出症、腰椎管狭窄症和腰部神经根受压3种疾病进行分级,准确率可达84.17%。除此以外,KIM等[66]首次尝试利用腰椎X射线片预测间盘髓核突出,基于31 149例受试者腰椎X射线图像,通过EfficientNet-B5和四重交叉验证进行训练,最后利用3 512例患者完成验证,AUC值为0.73,具有一定的预测潜力,但尚无法用作腰椎间盘突出症诊断工具。HAN等[67]则尝试早期评估腰椎间盘突出症,利用CNN分析MRI图像中椎间盘异常信号,检出的最小钙化灶尺寸为0.32 mm,同时能分析纤维化信号强度,可用于腰椎间盘突出症早期临床筛查。 深度学习还可以优化MRI图像质量,提高诊断性能,应用于腰椎间盘突出症相关性研究中。WANG等[68]在腰椎间盘突出症与腰椎小关节的相关性研究中,比较了CNN、马尔科夫随机场、模糊聚类3种不同算法的MRI诊断性能发现,CNN算法下的MRI具有最高诊断性能,准确率高达99.56%,证实了腰椎间盘突出症患者腰椎小关节角度出现不规则变化。GAO等[69]基于ResNet的MRI图像,获取腰椎丰富结构信息,同样发现腰椎间盘退变分级与腰椎小关节解剖变异分级呈正相关,除此以外,研究还发现61-70岁腰椎间盘突出症患者术后残留神经症状发生率高达63.77%,可用于术后神经评价。 综上所述,深度学习可广泛应用于椎间盘识别、分割、分类及构建临床预测模型,提高腰椎间盘突出症诊断分级准确性,还能优化图像等。作为目前机器学习的研究热点,深度学习凭借其强大的学习能力和算法先进性应用于腰椎间盘突出症诊治的各个方面。然而,由于计算量较大、模型设计复杂和硬件成本较高等不足,在基层推广仍有待进一步提高。未来着眼于深度学习算法的挖掘将有助于实现腰椎间盘突出症智能化诊疗的发展。 2.1.2 无监督学习算法 是通过对未标注数据进行学习,识别输入数据的特征和模式,并依据结果对输入数据进行聚类和降维操作。聚类是一种常用的无监督学习算法,以K-均值(K-means)聚类为代表[12]。除此以外,常用无监督学习算法还包括PCA降维、马尔科夫随机场和自回归模型等。 聚类算法:是基于给定的样本,依据其特征相似度或距离,将其归并到若干个小组中,输出聚类标签,从而预测归类结果。目前以K-means聚类应用最为广泛,还包括模糊聚类、层次聚类、网格聚类等。在腰椎间盘突出症研究中,聚类算法可用于椎间盘分割和不同突出节段的分类。MAHDY等[70]基于K-means分割相邻椎骨,计算椎间间隙,根据相邻椎骨间距离识别退变椎间盘,还能进行人工间盘置换模拟。PEULIC等[71]通过模糊聚类算法对L4/5或L5/S1节段腰椎间盘突出症进行分类,通过放置在足底的4个不同位置传感器,分析18例腰椎间盘突出症患者正常站立、前足站立和脚跟站立时的足底力值差异,明确腰椎间盘突出症突出节段,准确率可达72%。STAARTJES等[72]针对262例患者5次重复坐立测试数据,采用模糊聚类算法对3种腰椎疾病进行归类,准确率为96.2%,其中腰椎间盘突出症分类的敏感性和特异性分别达到95.7%和100%。 其他算法:除了聚类算法,常用无监督学习算法还包括PCA降维、马尔可夫随机场和独立成分分析(independent components analysis,ICA)等。其中,ICA可将多元信号分解为不同的非高斯信号,从多个维度分离有用数据,常应用于模型降噪。ZHAO等[73]通过改进的白化矩阵优化ICA,将其应用于功能MRI的降噪处理,可提高图像质量,有利于评估腰椎间盘突出症神经根受压程度,反映出根性疼痛导致的脑部功能区颞叶、丘脑、胼胝体等区域发生变化。 目前,无监督学习算法在腰椎间盘突出症中应用相对较少,主要在椎间盘分割、分类以及图像优化领域。其中,K-means算法相对简单,容易实现;而ICA在探究危险因素方面效果良好,可用于图像数据优化和评估。然而,无监督学习模型的性能与未标记的数据质量密切相关,提高模型性能必须以高质量的临床数据集为基础。 2.1.3 半监督学习算法 半监督学习通过标记数据和未标记数据相结合,在减少工作量的同时提高准确性,是一种监督学习与无监督学习相结合的算法,适用于数据庞大,部分数据难以标记的情况[74]。2015年,HAQ等[75]采用半监督学习方式,利用单纯形网格法自动分割椎间盘,当无法准确获取突出的椎间盘边界时,允许评估者放置约束点促进分割,与专家分割误差小于1 mm,Dice值为0.917,可用于正常或突出椎间盘分割。在2020年,LEWANDROWSKI等[76]面对3 560名患者的17 800份椎间盘数据,将腰椎的三维解剖模型拟合到患者MRI图像中训练分割模型,并将其中5 000份作为标签数据,其余为无标签数据,对3种腰椎疾病分类效果优于放射科医师,其中腰椎间盘突出症诊断准确率为85.2%,灵敏度为81.8%,特异性达到87.4%。不难看出,半监督学习算法适用于海量数据集,尤其是存在部分数据标记困难的情况,可有效提高运算效率。 2.2 机器学习在腰椎间盘突出症中的诊治优势 机器学习的不同算法具有各自的应用特点及优势,可服务于腰椎间盘突出症诊治全流程。临床诊断腰椎间盘突出症时,椎间盘退变程度是其诊查要点,支持向量机、随机森林、人工神经网络、深度学习等算法提高了椎间盘识别、分割精度,实现了半自动甚至全自动的检测、量化,可早期鉴别正常或退变椎间盘,还能实现Pfirrmann分级,其准确性可达到甚至超过临床专家水平。除此以外,在腰椎间盘突出症诊断中,以人工神经网络和深度学习为主的模型提高了腰椎间盘突出症诊断准确率,还能对腰椎间盘突出症、腰椎管狭窄和腰椎滑脱等脊柱疾病进行分类、分级。腰椎间盘突出症预后研究中,监督学习中的各种算法均能构建风险预测模型,在对腰椎间盘突出症保守、经皮内镜腰椎间盘切除、显微腰椎间盘摘除术等术后疗效预测中应用广泛,可实现对大数据集的模型构建,提高预测精度,有助于临床治疗方案的选择。而深度学习在医学影像方面的优势将有助于构建手术辅助系统,降低手术风险。此部分将从椎间盘图像识别、分割、分类和分级,腰椎间盘突出症诊断、分类、风险预测研究和手术辅助等方面进行具体介绍。 2.2.1 椎间盘图像识别与分割 椎间盘的识别与分割对于腰椎间盘突出症的诊断准确性至关重要,有利于制定下一步临床诊疗计划。基于算法的椎间盘自动识别、分割可提高腰椎间盘突出症的诊断效率和准确性[77-81],表1对腰椎间盘识别、分割的机器学习方法进行了总结。"
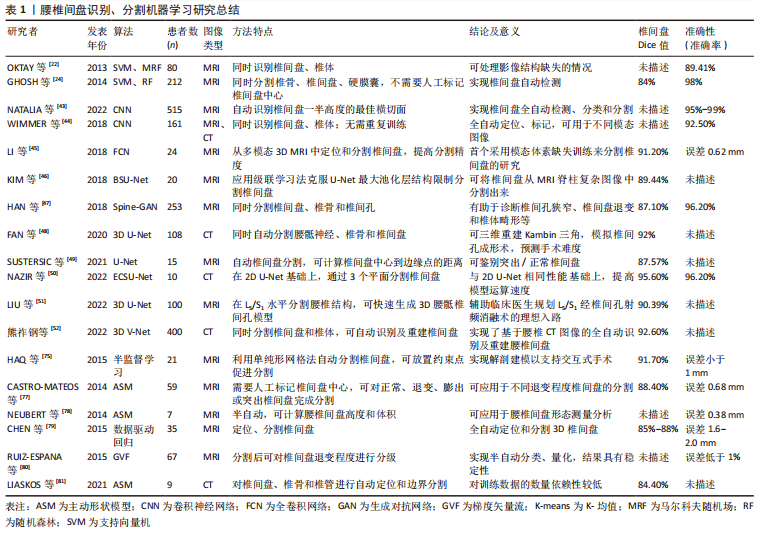
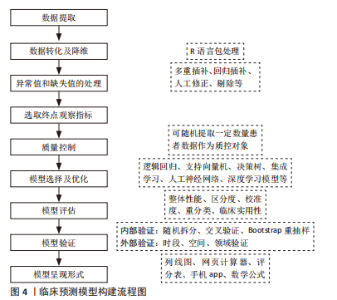
不同于常规MRI辅助诊断,临床也常采用力学信号传导、生物力学分析、客观功能测试和表面肌电等方式进行腰椎间盘突出症诊断。SUSTERSIC团队基于腰椎间盘突出症受累节段与下肢神经支配区的肌肉力量对应关系,在2019年利用模糊聚类算法设计无创下肢肌力测量硬件平台,通过足力传感器信号以诊断L4/5或L5/S1椎间盘突出[71]。在与徒手肌力测定的比较中,平台测量更精确,可提供用于诊断正常肌肉力量的参考值[85]。 2020年,SUSTERSIC等[21]在先前硬件平台基础上,基于贝叶斯理论对腰椎间盘突出症患者进行诊断识别,平均准确率为83.1%,通过进一步优化算法,与机器学习、Logistic回归、支持向量机和K-NN算法相比,归一化后决策树或朴素贝叶斯显示出更高的诊断准确率,分别为78.79%和72.73%[86]。除此以外,OYEDOTUN等[35]通过有限元分析技术,提取患者骨盆投射角、骶骨倾斜角和腰椎前凸角等6个力学参数,利用人工神经网络自动诊断腰椎间盘突出症和腰椎滑脱,可达到99.05%的分类精度。STAARTJES等[72]针对262例患者5次重复坐立测试数据,采用模糊聚类算法对3种腰椎疾病进行归类,准确率为96.2%,其中腰椎间盘突出症分类的敏感性和特异性分别达到95.7%和100%。李祥蓉等[87]基于47例腰椎间盘突出症合并神经根受压患者表面肌电参数,应用Logistic回归、决策树和人工神经网络构建受压神经根的诊断模型,AUC值分别为0.97、0.90和0.98,其中人工神经网络诊断效能优于其余两模型。REN等[88]开发基于NLP的腰椎间盘突出症诊断模型,借助深度学习中的长短期记忆网络算法,通过患者病例资料中阳性症状自动鉴别腰椎间盘突出症和腰椎管狭窄症,诊断性能优于XGBoost 模型(准确率:78.18%比69.61%)。 2.2.4 腰椎间盘突出症分类 JAFARI等[14]利用KNN、支持向量机和 Logistic模型对腰椎间盘突出症进行分类,研究发现支持向量机适用于小样本,随着样本量增加,KNN模型的效率逐渐提高,而Logistic模型效率最低。LI等[89]则比较了腰椎间盘突出症和健康人在左右侧弯运动时的表面脑电图变化,通过决策树、Logistic回归、支持向量机、KNN等模型对运动图像进行分类,四者准确率均在96%以上。 2.2.5 腰椎间盘突出症危险因素分析和预后预测 目前,引起腰椎间盘突出症的危险因素众多,也对治疗预后产生了重要影响。基于机器学习分析腰椎间盘突出症危险因素,在此基础上构建风险预测模型,有助于疾病预后分析。临床预测模型构建流程见图4。"
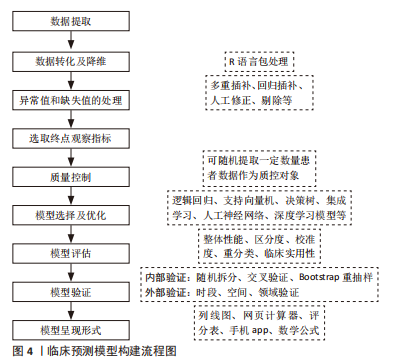
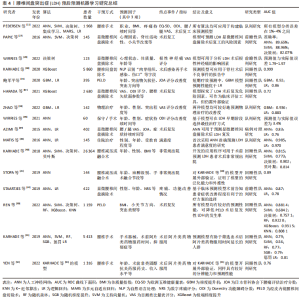
既往研究发现,腰痛用药史、腰椎间盘突出症相关病史、水烟史是腰椎间盘突出症患者排名靠前的危险因素,其中吸烟者发生腰椎间盘突出症的概率是不吸烟者的近4倍[14]。而在预后研究中,PEDERSEN等[11]基于丹麦国家脊柱手术数据库中1 968例腰椎间盘突出症患者资料,比较了人工神经网络、决策树、随机森林及支持向量机等7种模型预测腰椎间盘突出症手术结局的准确率,研究发现所有模型分类误差为1%-4%,机器学习模型优于传统统计学模型。REN等[90]基于1 159例接受经皮椎间孔镜治疗的腰椎间盘突出症患者资料构建机器学习模型,通过单因素分析确定高体质量指数、小关节方向、腰椎间盘突出症类型和椎间盘钙化是腰椎间盘突出症复发的危险因素,其中XGBoost、随机森林和人工神经网络模型的AUC值分别可达到0.931 5,0.922 0和0.881 4,具有良好预测性能,可降低经皮椎间孔镜术后腰椎间盘突出症复发的概率。除了比较手术预后的预测性能,2019年,KARHADE等[91]对腰椎间盘突出症术后90-180 d阿片类药物使用情况进行预测,数据集来自5 413例接受手术治疗的腰椎间盘突出症患者,发生率为7.7%,以惩罚Logistic模型区分度最高,AUC值为0.81,最终将手术器械、阿片类药物服药持续时间和抑郁症作为3个最重要的预测因素。2022年,YEN等[92]对KARHADE等[91]的模型进行了外部验证,基于中国台湾省1 316例腰椎间盘突出症患者资料预测术后阿片类药物使用情况,发生率为3.1%,AUC值为0.76,Brier得分为0.028,模型同样取得不错的区分能力和整体性能。表4对腰椎间盘突出症预后预测的机器学习方法进行了总结。"
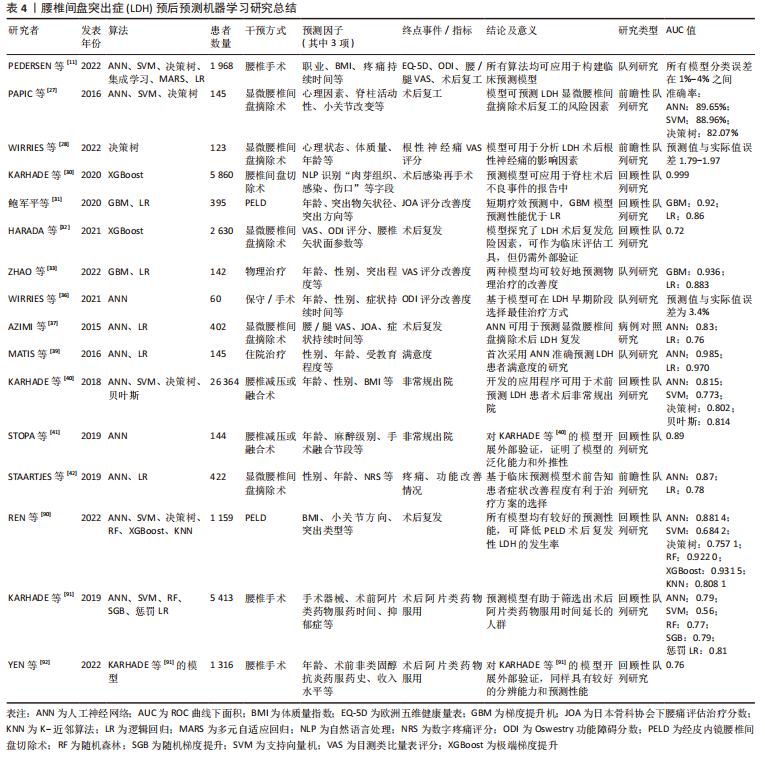

2.2.6 辅助术中操作 PAN等[10]设计了一种基于增强现实技术的经皮椎间孔镜手术导航系统,通过YOLO-v3算法构建具备标记功能的深度学习相机,可术中实时显示穿刺针和周围组织的空间关系,定位精度可达1.98 mm,降低了术中透视成像频率。FORESTIER等[93]将既往腰椎间盘切除的操作流程、解剖结构和使用的手术器械作为训练集,通过动态时间规整(dynamic time warping,DTW)算法进行训练,可在术中预测下一步操作步骤,准确率达95%,降低手术操作失误率。CUI等[94]设计了一种基于CNN的手术辅助系统,具有自动识别经皮椎间孔镜术中的神经、硬脑膜图像的能力,准确率达92.29%,可帮助临床医师提高解剖组织分辨能力。 2.3 机器学习在腰椎间盘突出症中的应用策略 综上,在探究腰椎间盘突出症危险因素时可考虑采用传统统计学方法,以Logistic 回归应用为主,或使用决策树进行分析,但需注意避免模型过拟合的情况;椎间盘影像分析研究中,以支持向量机、随机森林、人工神经网络、深度学习和聚类算法等为主,其中针对小数据集可采用传统机器学习方法,例如支持向量机、随机森林和聚类算法,而对于海量数据则可使用人工神经网络或深度学习算法。同时,在选择算法时若考虑模型可解释性时应注意人工神经网络的黑箱效应,经济成本较高的为深度学习算法,但目前人工神经网络和深度学习模型的准确性也较高。在构建腰椎间盘突出症临床预测模型研究中,机器学习应用广泛,尤其是近年来人工神经网络和深度学习算法提高了模型诊断和预测的准确性,基于临床大数据库的模型构建可考虑采用人工神经网络和深度学习算法,与传统机器学习方法相比性能更好。除此以外,深度学习还可辅助术中操作,提高手术疗效。"

| [1] 中华医学会骨科学分会脊柱外科学组,中华医学会骨科学分会骨科康复学组.腰椎间盘突出症诊疗指南[J].中华骨科杂志,2020,40(8):477-487. [2] CIEZA A, CAUSEY K, KAMENOV K, et al. Global estimates of the need for rehabilitation based on the Global Burden of Disease study 2019: a systematic analysis for the Global Burden of Disease Study 2019. Lancet. 2021;396(10267):2006-2017. [3] HARTVIGSEN J, HANCOCK MJ, KONGSTED A, et al. What low back pain is and why we need to pay attention. Lancet. 2018;391(10137):2356-2367. [4] KIM YK, KANG D, LEE I, et al. Differences in the incidence of symptomatic cervical and lumbar disc herniation according to age, sex and national health insurance eligibility: a pilot study on the disease’s association with work. Int J Environ Res Public Health. 2018;15(10):2094. [5] FAUR C, PATRASCU JM, HARAGUS H, et al. Correlation between multifidus fatty atrophy and lumbar disc degeneration in low back pain. BMC Musculoskelet Disord. 2019;20(1):414. [6] AZIMI P, YAZDANIAN T, BENZEL EC, et al. A Review on the Use of Artificial Intelligence in Spinal Diseases. Asian Spine J. 2020;14(4):543-571. [7] 张新新,刘华东.出版+人工智能:未来出版的新模式与新形态——以《新一代人工智能发展规划》为视角[J].科技与出版,2017(12):38-43. [8] 李晓理,张博,王康,等.人工智能的发展及应用[J].北京工业大学学报,2020, 46(6):583-590. [9] SUN S, TAN ET, MINTZ DN, et al. Evaluation of deep learning reconstructed high-resolution 3D lumbar spine MRI. Eur Radiol. 2022;32(9):6167-6177. [10] PAN J, YU D, LI R, et al. Multi-Modality guidance based surgical navigation for percutaneous endoscopic transforaminal discectomy. Comput Methods Programs Biomed. 2021;212:106460. [11] PEDERSEN CF, ANDERSEN MØ, CARREON LY, et al. Applied machine learning for spine surgeons: predicting outcome for patients undergoing treatment for lumbar disc herniation using PRO data. Global Spine J. 2022;12(5):866-876. [12] Deo RC. Machine learning in medicine. Circulation. 2015;132(20):1920-1930. [13] 刘彤彤,杨环,西永明,等.机器学习在脊柱疾病智能诊治中的应用综述[J].计算机科学,2021,48(S2):597-607. [14] JAFARI S, DEHESH T, IRANMANESH F. Classifying patients with lumbar disc herniation and exploring the most effective risk factors for this disease. J Pain Res. 2019;12: 1179-1187. [15] YU G, YANG W, ZHANG J, et al. Application of a nomogram to radiomics labels in the treatment prediction scheme for lumbar disc herniation. BMC Med Imaging. 2022;22(1):51. [16] HIRAYAMA K, TSUSHIMA E, ARIHARA H, et al. Developing a clinical prediction rule to identify patients with lumbar disc herniation who demonstrate short-term improvement with mechanical lumbar traction. Phys Ther Res. 2019;22(1):9-16. [17] 邱洪波,唐乐,何甜,等.椎间孔镜治疗腰椎间盘突出症患者术后复发的个体化预警模型的建立[J].西安交通大学学报(医学版),2021,42(6):817-822. [18] 李鑫,罗鸣然,李根,等.建立与验证经皮内窥镜腰椎间盘切除后复发风险的预测模型[J].中国组织工程研究,2023,27(13):2087-2092. [19] LI Y, WANG B, LI H, et al. Adjuvant surgical decision-making system for lumbar intervertebral disc herniation after percutaneous endoscopic lumber discectomy: a retrospective nonlinear multiple logistic regression prediction model based on a large sample. Spine J. 2021;21(12):2035-2048. [20] LI W, LIU YC, ZHENG CF, et al. Diagnosis of compressed nerve root in lumbar disc herniation patients by surface electromyography. Orthop Surg. 2018;10(1):47-55. [21] SUSTERSIC T, RANKOVIC V, PEULIC M, et al. An early disc herniation identification system for advancement in the standard medical screening procedure based on bayes theorem. IEEE J Biomed Health Inform. 2020;24(1):151-159. [22] OKTAY AB, AKGUL YS. Simultaneous localization of lumbar vertebrae and intervertebral discs with SVM-based MRF. IEEE Trans Biomed Eng. 2013;60(9):2375-2383. [23] OKTAY AB, ALBAYRAK NB, AKGUL YS. Computer aided diagnosis of degenerative intervertebral disc diseases from lumbar MR images. Comput Med Imaging Graph. 2014;38(7):613-619. [24] GHOSH S, CHAUDHARY V. Supervised methods for detection and segmentation of tissues in clinical lumbar MRI. Comput Med Imaging Graph. 2014;38(7):639-649. [25] BEULAH A, SHARMILA TS, PRAMOD VK. Degenerative disc disease diagnosis from lumbar MR images using hybrid features. Vis Comput. 2021;38:2771-2783. [26] LI K, LI S, ZHANG H, et al. Computational analysis of the immune infiltration pattern and candidate diagnostic biomarkers in lumbar disc herniation. Front Mol Neurosci. 2022;15:846554. [27] PAPIC M, BRDAR S, PAPIC V, et al. Return to work after lumbar microdiscectomy - personalizing approach through predictive modeling. Stud Health Technol Inform. 2016;224:181-183. [28] WIRRIES A, GEIGER F, HAMMAD A, et al. AI prediction of neuropathic pain after lumbar disc herniation-machine learning reveals influencing factors. Biomedicines. 2022;10(6):1319. [29] SUNDARSINGH S, KESAVAN R. Diagnosis of disc bulge and disc desiccation in lumbar MRI using concatenated shape and texture features with random forest classifier. Int J Imaging Syst Technol. 2020;30(2):340-347. [30] KARHADE AV, BONGERS MER, GROOT OQ, et al. Can natural language processing provide accurate, automated reporting of wound infection requiring reoperation after lumbar discectomy? Spine J. 2020;20(10):1602-1609. [31] 鲍军平,刘磊,时睿,等.梯度提升机模型对腰椎间盘突出症经皮内镜切除术近期疗效的预测作用[J].中华骨科杂志,2020,40(19):1327-1336. [32] HARADA GK, SIYAJI ZK, MALLOW GM, et al. Artificial intelligence predicts disk re-herniation following lumbar microdiscectomy: development of the “RAD” risk profile. Eur Spine J. 2021;30(8):2167-2175. [33] ZHAO P, XUE J, XU X, et al. Logistic model and gradient boosting machine model for physical therapy of lumbar disc herniation. Comput Math Methods Med. 2022; 2022:4799248. [34] CASTRO-MATEOS I, HUA R, POZO JM, et al. Intervertebral disc classification by its degree of degeneration from T2-weighted magnetic resonance images. Eur Spine J. 2016;25(9):2721-2727. [35] OYEDOTUN OK, OLANIYI EO, KHASHMAN A. Disk hernia and spondylolisthesis diagnosis using biomechanical features and neural network. Technol Health Care. 2016;24(2):267-279. [36] WIRRIES A, GEIGER F, HAMMAD A, et al. Artificial intelligence facilitates decision-making in the treatment of lumbar disc herniations. Eur Spine J. 2021;30(8):2176-2184. [37] AZIMI P, MOHAMMADI HR, BENZEL EC, et al. Use of artificial neural networks to predict recurrent lumbar disk herniation. J Spinal Disord Tech. 2015;28(3):E161-E165. [38] AZIMI P, BENZEL EC, SHAHZADI S, et al. The prediction of successful surgery outcome in lumbar disc herniation based on artificial neural networks. J Neurosurg Sci. 2016; 60(2):173-177. [39] MATIS GK, CHRYSOU OI, SILVA D, et al. Prediction of lumbar disc herniation patients’ satisfaction with the aid of an artificial neural network. Turk Neurosurg. 2016;26(2):253-259. [40] KARHADE AV, OGINK P, THIO Q, et al. Development of machine learning algorithms for prediction of discharge disposition after elective inpatient surgery for lumbar degenerative disc disorders. Neurosurg Focus. 2018;45(5):E6. [41] STOPA BM, ROBERTSON FC, KARHADE AV, et al. Predicting nonroutine discharge after elective spine surgery: external validation of machine learning algorithms. J Neurosurg Spine. 2019;26:1-6. [42] STAARTJES VE, DE WISPELAERE MP, VANDERTOP WP, et al. Deep learning-based preoperative predictive analytics for patient-reported outcomes following lumbar discectomy: feasibility of center-specific modeling. Spine J. 2019;19(5):853-861. [43] NATALIA F, YOUNG JC, AFRILIANA N, et al. Automated selection of mid-height intervertebral disc slice in traverse lumbar spine MRI using a combination of deep learning feature and machine learning classifier. PLoS One. 2022;17(1):e0261659. [44] WIMMER M, MAJOR D, NOVIKOV AA, et al. Fully automatic cross-modality localization and labeling of vertebral bodies and intervertebral discs in 3D spinal images. Int J Comput Assist Radiol Surg. 2018;13(10):1591-1603. [45] LI X, DOU Q, CHEN H, et al. 3D multi-scale FCN with random modality voxel dropout learning for Intervertebral Disc Localization and Segmentation from Multi-modality MR Images. Med Image Anal. 2018;45:41-54. [46] KIM S, BAE WC, MASUDA K, et al. Fine-grain segmentation of the intervertebral discs from MR spine images using deep convolutional neural networks: BSU-Net. Appl Sci (Basel). 2018;8(9):1656. [47] HAN Z, WEI B, MERCADO A, et al. Spine-GAN: Semantic segmentation of multiple spinal structures. Med Image Anal. 2018;50:23-35. [48] FAN G, LIU H, WANG D, et al. Deep learning-based lumbosacral reconstruction for difficulty prediction of percutaneous endoscopic transforaminal discectomy at L5/S1 level: a retrospective cohort study. Int J Surg. 2020;82:162-169. [49] SUSTERSIC T, RANKOVIC V, KOVACEVIC V, et al. Machine learning-based image processing in support of discus hernia diagnosis. IEEE BIBE. 2021. [50] NAZIR A, CHEEMA MN, SHENG B, et al. ECSU-Net: an embedded clustering sliced u-net coupled with fusing strategy for efficient intervertebral disc segmentation and classification. IEEE Trans Image Process. 2022;31:880-893. [51] LIU Z, SU Z, WANG M, et al. Computerized characterization of spinal structures on MRI and clinical significance of 3D reconstruction of lumbosacral intervertebral foramen. Pain Physician. 2022;25(1):E27-E35. [52] 熊祚钢,吴敏,叶喜林,等.基于腰椎螺旋CT图像以卷积神经网络技术全自动识别并重建椎间盘的可行性[J].中国介入影像与治疗学,2022,19(2):99-103. [53] JAMALUDIN A, LOOTUS M, KADIR T, et al. ISSLS PRIZE IN BIOENGINEERING SCIENCE 2017: Automation of reading of radiological features from magnetic resonance images (MRIs) of the lumbar spine without human intervention is comparable with an expert radiologist. Eur Spine J. 2017;26(5):1374-1383. [54] JAMALUDIN A, KADIR T, ZISSERMAN A. SpineNet: automated classification and evidence visualization in spinal MRIs. Med Image Anal. 2017;41:63-73. [55] HUANG J, SHEN H, WU J, et al. Spine Explorer: a deep learning based fully automated program for efficient and reliable quantifications of the vertebrae and discs on sagittal lumbar spine MR images. Spine J. 2020;20(4):590-599. [56] GAO F, LIU S, ZHANG X, et al. Automated grading of lumbar disc degeneration using a push-pull regularization network based on MRI. J Magn Reson Imaging. 2021;53(3): 799-806. [57] NIEMEYER F, GALBUSERA F, TAO Y, et al. A deep learning model for the accurate and reliable classification of disc degeneration based on MRI data. Invest Radiol. 2021; 56(2):78-85. [58] AI-KUBAISI A, KHAMISS NN. A transfer learning approach for lumbar spine disc state classification. electronics. 2022;11(1):85. [59] LEWANDROWSKI KU, MURALEEDHARAN N, EDDY SA, et al. Reliability analysis of deep learning algorithms for reporting of routine lumbar MRI scans. Int J Spine Surg. 2020;14(s3):S98-S107. [60] LEWANDROWSKI KU, MURALEEDHARAN N, EDDY SA, et al. Artificial intelligence comparison of the radiologist report with endoscopic predictors of successful transforaminal decompression for painful conditions of the lumber spine: application of deep learning algorithm interpretation of routine lumbar magnetic resonance imaging scan. Int J Spine Surg. 2020;14(s3):S75-S85. [61] TSAI JY, HUNG IY, GUO YL, et al. Lumbar Disc Herniation Automatic Detection in Magnetic Resonance Imaging Based on Deep Learning. Front Bioeng Biotechnol. 2021;9:708137. [62] PAN Q, ZHANG K, HE L, et al. Automatically diagnosing disk bulge and disk herniation with lumbar magnetic resonance images by using deep convolutional neural networks: method development study. JMIR Med Inform. 2021;9(5):e14755. [63] 巩稼民,杨红蕊,郭庆庆,等.基于分步目标定位的腰椎间盘自动诊断方法[J].中国医学物理学杂志,2021,38(3):317-322. [64] LEHNEN NC, HAASE R, FABER J, et al. Detection of degenerative changes on MR images of the lumbar spine with a convolutional neural network: a feasibility study. Diagnostics (Basel). 2021;11(5):902. [65] SU ZH, LIU J, YANG MS, et al. Automatic grading of disc herniation, central canal stenosis and nerve roots compression in lumbar magnetic resonance image diagnosis. Front Endocrinol (Lausanne). 2022;13:890371. [66] KIM JH, LEE SE, JUNG HS, et al. Development and validation of deep learning-based algorithms for predicting lumbar herniated nucleus pulposus using lumbar X-rays. J Pers Med. 2022;12(5):767. [67] HAN M, LIU L, HU M, et al. Medical expert and machine learning analysis of lumbar disc herniation based on magnetic resonance imaging. Comput Methods Programs Biomed. 2022;213:106498. [68] WANG C, YUAN JB, HUANG ZB, et al. Deep learning-based correlation analysis between spine surgery lumbar facet joint and lumbar disc herniation using magnetic resonance images. Scientific Programming. 2021;2021:9623991. [69] GAO F, WU M. Deep learning-based denoised MRI images for correlation analysis between lumbar facet joint and lumbar disc herniation in spine surgery. J Healthc Eng. 2021;2021:9687591. [70] MAHDY LN, EZZAT KA, HASSANIEN AE. Automatic detection system for degenerative disk and simulation for artificial disc replacement surgery in the spine. ISA Trans. 2018;81:244-258. [71] PEULIC A, SUSTERSIC T, PEULIC M. Non-invasive improved technique for lumbar discus hernia classification based on fuzzy logic. Biomed Tech (Berl). 2019;64(4):421-428. [72] STAARTJES VE, QUDDUSI A, KLUKOWSKA AM, et al. Initial classification of low back and leg pain based on objective functional testing: a pilot study of machine learning applied to diagnostics. Eur Spine J. 2020;29(7):1702-1708. [73] ZHAO B, YANG F, GUAN L, et al. Fast independent component analysis algorithm-based diagnosis of L5 nerve root compression and changes of brain functional areas using 3D functional magnetic resonance imaging. J Healthc Eng. 2021;2021:5063021. [74] UNNIKRISHNAN B, NGUYEN C, BALARAM S, et al. Semi-supervised classification of radiology images with NoTeacher: a teacher that is not mean. Med Image Anal. 2021;73:102148. [75] HAQ R, ARAS R, BESACHIO DA, et al. 3D lumbar spine intervertebral disc segmentation and compression simulation from MRI using shape-aware models. Int J Comput Assist Radiol Surg. 2015;10(1):45-54. [76] LEWANDROWSKI KU, MURALEEDHARAN N, EDDY SA, et al. Feasibility of deep learning algorithms for reporting in routine spine magnetic resonance imaging. Int J Spine Surg. 2020;14(s3):S86-S97. [77] CASTRO-MATEOS I, POZO JM, ELTES PE, et al. 3D segmentation of annulus fibrosus and nucleus pulposus from T2-weighted magnetic resonance images. Phys Med Biol. 2014;59(24):7847-7864. [78] NEUBERT A, FRIPP J, ENGSTROM C, et al. Validity and reliability of computerized measurement of lumbar intervertebral disc height and volume from magnetic resonance images. Spine J. 2014;14(11):2773-2781. [79] CHEN C, BELAVY D, YU W, et al. Localization and segmentation of 3D intervertebral discs in MR images by data driven estimation. IEEE Trans Med Imaging. 2015;34(8): 1719-1729. [80] RUIZ-ESPANA S, ARANA E, MORATAL D. Semiautomatic computer-aided classification of degenerative lumbar spine disease in magnetic resonance imaging. Comput Biol Med. 2015;62:196-205. [81] LIASKOS M, SAVELONAS MA, ASVESTAS PA, et al. Vertebrae, IVD and spinal canal boundary extraction on MRI, utilizing CT-trained active shape models. Int J Comput Assist Radiol Surg. 2021;16(12):2201-2214. [82] 江丽红,吴晓锋,欧阳林,等.基于代谢组学腰椎间盘退变的计算机辅助诊断[J].中国组织工程研究,2021,25(24):3796-3803. [83] KOH J, CHAUDHARY V, DHILLON G. Disc herniation diagnosis in MRI using a CAD framework and a two-level classifier. Int J Comput Assist Radiol Surg. 2012;7(6):861-869. [84] SALEHI E, YOUSEFI H, RASHIDI H, et al. Automatic diagnosis of disc herniation in two-dimensional MR images with combination of distinct features using machine learning methods. In Proceedings of the 2019 Scientific Meeting on Electrical-Electronics & Biomedical Engineering and Computer Science (EBBT). 2019. [85] PEULIC M, JOKOVIC M, SUSTERSIC T, et al. A noninvasive assistant system in diagnosis of lumbar disc herniation. Comput Math Methods Med. 2020;2020:6320126. [86] SUSTERSIC T, MILOVANOVIC V, RANKOVIC V, et al. A comparison of classifiers in biomedical signal processing as a decision support system in disc hernia diagnosis. Comput Biol Med. 2020;125:103978. [87] 李祥蓉,程琳,席家宁,等.三种模式识别模型诊断腰椎间盘突出症受压神经根的准确率[J].中国组织工程研究,2018,22(19):3005-3013. [88] REN G, YU K, XIE Z, et al. Differentiation of lumbar disc herniation and lumbar spinal stenosis using natural language processing-based machine learning based on positive symptoms. Neurosurg Focus. 2022;52(4):E7. [89] LI H, DU W, IVANOV K, et al. The EEG Analysis of actual left/right lateral bending movements in patient of lumbar disc herniation. Annu Int Conf IEEE Eng Med Biol Soc. 2019;2019:4707-4711. [90] REN G, LIU L, ZHANG P, et al. Machine learning predicts recurrent lumbar disc herniation following percutaneous endoscopic lumbar discectomy. Global Spine J. 2022:21925682221097650. [91] KARHADE AV, OGINK PT, THIO QCBS, et al. Development of machine learning algorithms for prediction of prolonged opioid prescription after surgery for lumbar disc herniation. Spine J. 2019;19(11):1764-1771. [92] YEN HK, OGINK PT, HUANG CC, et al. A machine learning algorithm for predicting prolonged postoperative opioid prescription after lumbar disc herniation surgery. An external validation study using 1,316 patients from a Taiwanese cohort. Spine J. 2022;22(7):1119-1130. [93] FORESTIER G, PETITJEAN F, RIFFAUD L, et al. Automatic matching of surgeries to predict surgeons’ next actions. Artif Intell Med. 2017;81:3-11. [94] CUI P, SHU T, LEI J, et al. Nerve recognition in percutaneous transforaminal endoscopic discectomy using convolutional neural network. Med Phys. 2021;48(5):2279-2288. [95] 郭琼,冯堃,龙囿霖,等.创新医疗器械临床研究方法学框架解读[J].中国胸心血管外科临床杂志,2022,29(7):828-833. [96] DECIDE-AI Steering Group. DECIDE-AI: new reporting guidelines to bridge the development-to-implementation gap in clinical artificial intelligence. Nat Med. 2021;27(2):186-187. |
| [1] | Yu Jingbang, Wu Yayun. Regulatory effect of non-coding RNA in pulmonary fibrosis [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(8): 1659-1666. |
| [2] | Wang Qiuyue, Jin Pan, Pu Rui . Exercise intervention and the role of pyroptosis in osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(8): 1667-1675. |
| [3] | Yuan Weibo, Liu Chan, Yu Limei. Potential application of liver organoids in liver disease models and transplantation therapy [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(8): 1684-1692. |
| [4] | Wang Mi, Ma Shujie, Liu Yang, Qi Rui. Identification and validation of characterized gene NFE2L2 for ferroptosis in ischemic stroke [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(7): 1466-1474. |
| [5] | Peng Hongcheng, Peng Guoxuan, Lei Anyi, Lin Yuan, Sun Hong, Ning Xu, Shang Xianwen, Deng Jin, Huang Mingzhi . Role and mechanism of platelet-derived growth factor BB in repair of growth plate injury [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(7): 1497-1503. |
| [6] | Zhi Fang, Zhu Manhua, Xiong Wei, Lin Xingzhen. Analgesic effect of acupuncture in a rat model of lumbar disc herniation [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(5): 936-941. |
| [7] | Liu Yani, Yang Jinghuan, Lu Huihui, Yi Yufang, Li Zhixiang, Ou Yangfu, Wu Jingli, Wei Bing . Screening of biomarkers for fibromyalgia syndrome and analysis of immune infiltration [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(5): 1091-1100. |
| [8] | Yang Bin, Tao Guangyi, Yang Shun, Xu Junjie, Huang Junqing . Visualization analysis of research hotspots of artificial intelligence in field of spinal cord nerve injury and repair [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(4): 761-770. |
| [9] | Liu Haoyang, Xie Qiang, Shen Mengran, Ren Yansong, Ma Jinhui, Wang Bailiang, Yue Debo, Wang Weiguo . Application, research hotspots, and shortcomings of degradable zinc-based alloys in bone defect repair and reconstruction [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(4): 839-845. |
| [10] | Zhang Yu, Xu Ruian, Fang Lei, Li Longfei, Liu Shuyan, Ding Lingxue, Wang Yuexi, Guo Ziyan, Tian Feng, Xue Jiajia. Gradient artificial bone repair scaffold regulates skeletal system tissue repair and regeneration [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(4): 846-855. |
| [11] | Yang Cheng, Li Weimin, Ran Dongcheng, Xu Jiamu, Wu Wangxiang, Xu Jiafu, Chen Jingjing, Jiang Guangfu, Wang Chunqing. Ferroptosis and osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(3): 554-562. |
| [12] | He Kai, Xing Wenhua, Liu Shengxiang, Bai Xianming, Zhou Chen, Gao Xu, Qiao Yu, He Qiang, Gao Zhiyu, Guo Zhen, Bao Aruhan, Li Chade. Constructing a model of degenerative scoliosis using finite element method: biomechanical analysis in etiology and treatment [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(3): 572-578. |
| [13] | Song Haoran, Zhang Yuqiang, Gu Na, Zhi Xiaodong, Wang Wei. Visualization analysis of artificial intelligence in bone trauma research based on Citespace [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(3): 493-502. |
| [14] | Wu Yingkai, Shi Gaolong, Xie Zonggang . Weighted gene co-expression network analysis and machine learning identification of key genes in rheumatoid arthritis synovium [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(2): 294-301. |
| [15] | Wei Mengli, Zhong Yaping, Gui Huixian, Zhou Yiwen, Guan Yeming, Yu Shaohua. Sports injury prediction model based on machine learning [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(2): 409-418. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||