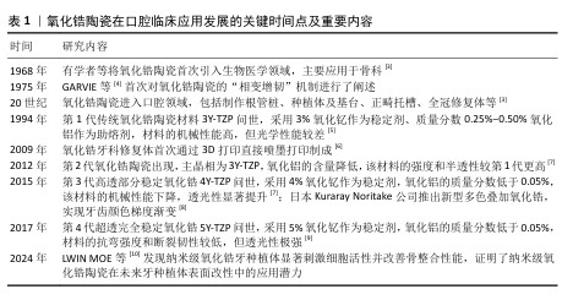
Chinese Journal of Tissue Engineering Research ›› 2026, Vol. 30 ›› Issue (14): 3717-3725.doi: 10.12307/2026.613
Previous Articles Next Articles
Key points of zirconia all-ceramic restoration materials in clinical application
Tang Yiyang1, Xiao Yuxin1, Sun Hening1, Li Chunxiao1, Zhang Yutong1, Fu Jiale2
- 1School of Stomatology, China Medical University, Shenyang 110002, Liaoning Province, China; 2Department of Dental Materials, Digital Prosthodontics Center, School and Hospital of Stomatology, China Medical University, Shenyang 110002, Liaoning Province, China
-
Received:2025-05-06Accepted:2025-06-05Online:2026-05-18Published:2025-09-15 -
Contact:Fu Jiale, Associate chief physician, Associate professor, Department of Dental Materials, Digital Prosthodontics Center, School and Hospital of Stomatology, China Medical University, Shenyang 110002, Liaoning Province, China -
About author:Tang Yiyang, School of Stomatology, China Medical University, Shenyang 110002, Liaoning Province, China
CLC Number:
Cite this article
Tang Yiyang, Xiao Yuxin, Sun Hening, Li Chunxiao, Zhang Yutong, Fu Jiale. Key points of zirconia all-ceramic restoration materials in clinical application[J]. Chinese Journal of Tissue Engineering Research, 2026, 30(14): 3717-3725.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
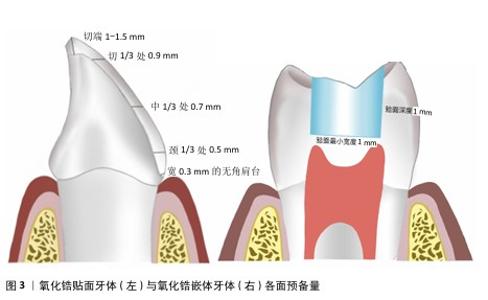
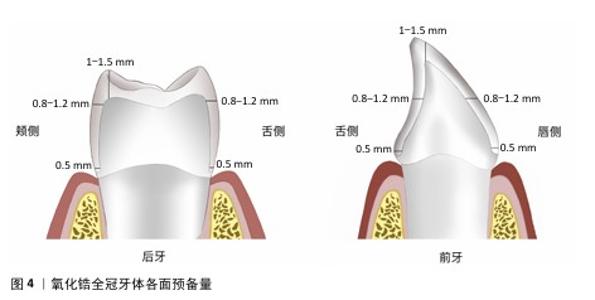
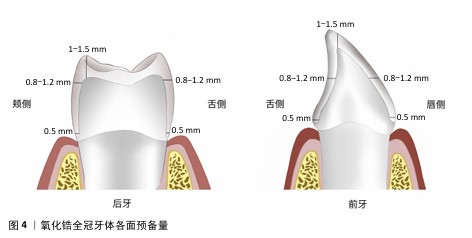
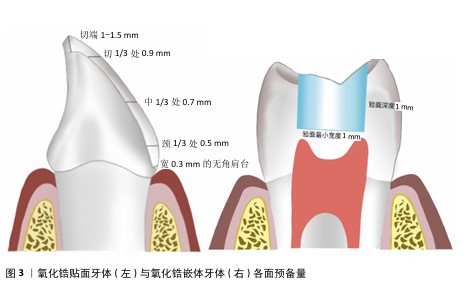
2.2 牙体预备 氧化锆全瓷冠的牙体预备流程与金属铸造冠和烤瓷冠基本相似,但全瓷冠要求的牙体预备量更大,临床医生需要综合考量牙齿颜色、受力情况及抗折性能来决定牙体预备量和修复体厚度,细致规划咬合面、轴面及边缘设计,注意各面平整光滑连续、聚合度一致、轴壁无倒凹、肩台宽度一致,以确保修复体具备优良的机械性能和美观度[11]。 2.2.1 牙体预备量 牙体预备量对于氧化锆全瓷冠的应力分布及断裂强度有显著影响,减少预备量可以增加全瓷冠内的应力,但同时减少预备体上的应力;反之,增加预备量会在基牙上产生更高的应力,增加牙齿折裂的风险。应根据修复体类型确定各面的最小预备厚度,见图3,4[12],当轴面倒凹较大时,轴面预备量可相应变大[13]。 随着材料的发展,氧化锆强度的增加使全冠要求的最小厚度越来越薄,相应的牙体预备量逐渐减少。例如,后牙氧化锆全冠的龈边缘宽度可降低至0.3-0.5 mm;即使咬合面厚度减至0.5 mm,氧化锆也能提供可接受的抗断裂性,厚度为1.0 mm全氧化锆冠与厚度为1.5 mm双层氧化锆冠或烤瓷冠的抗折性能相当[14-15]。 2.2.2 预备形态 有研究发现,按照牙尖和窝沟解剖轮廓制备牙尖斜度为30°解剖式预备的边缘和内部适合性明显优于半解剖式(牙尖斜度为15°-30°)和非解剖式预备(牙尖斜度为0°)[16-17]。解剖式牙体预备后的牙体形态与天然牙相似,牙尖与窝沟明显[18],优势为上下颌能达到更佳的尖窝锁结关系[19],分散咬合力,减少对牙体和牙周组织的损伤;同时还能提供更强的侧向力,提升咀嚼效率;此外,能更好地恢复前牙形态,满足美学需求。因此,咬合面预备形态以解剖式为佳。 轴面预备的核心在于控制总聚合度,适当的聚合度能够增强修复体的固位,通常建议将聚合度维持在10°-22°之间,这样不仅有助于修复体的稳固,还能减轻对基牙的压力。聚合度过大会导致固位力的减弱,过小则可能增加粘接剂的静水压力,从而妨碍多余粘接剂排出[20]。具体设定可以根据基牙类型来调整,例如,对于下颌第一磨牙,推荐的聚合度值为近远中方向24°、颊舌方向22°[21]。 "

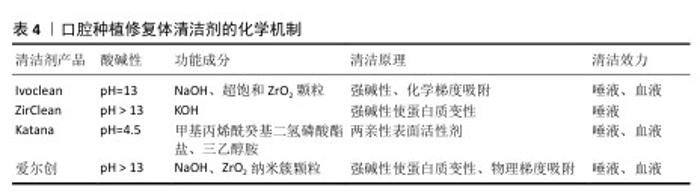
2.2.3 边缘设计 边缘设计是影响全瓷修复体断裂强度的重要因素之一,氧化锆全瓷冠常采用肩台边缘、凹槽边缘和羽状边缘(图5),以增强边缘的强度和减少应力集中[22]。肩台边缘是在牙体预备边缘处形成一个直角或钝角的平台,根据肩台内线角又分为锐内角肩台边缘和钝内角肩台边缘。凹槽边缘是在牙体预备边缘处制备出一道浅槽状结构。羽状边缘呈羽毛状逐渐变薄,边缘过渡平缓。不同边缘设计的具体优缺点见表2。 合理的边缘设计能够使氧化锆全瓷修复体与天然牙之间实现自然过渡,减少边缘黑线的出现,使修复体更加逼真自然,提高修复体的美学效果。良好的边缘密合度还能够有效减少微渗漏的发生,防止细菌侵入,从而降低继发龋和牙周炎的发生风险[23]。 凹面边缘和肩台边缘在提高边缘密合度方面具有明显优势,能够更好地保护牙体组织和牙周组织的健康。 关于修复体龈边缘设置,存在龈上、齐龈和龈下3种观点,如图6所示。龈上的修复体边缘有更强的密合性,并且不会刺激牙周组织,可降低龋病和龈炎的发生率。有研究证明,2 mm龈上边缘有最高的抗断裂强度[24]。 2.2.4 针对高透氧化锆的特殊注意事项 由于高透氧化锆的强度相对较低,需要更谨慎地设计牙冠厚度。建议透明氧化锆冠的最小厚度为0.8 mm[25],对于颜色正常的基牙,可以选择0.8-1.5 mm厚的透明氧化锆[26]。边缘设计建议采用凹槽边缘或钝内角肩台,并适当增加宽度[25]。当高透氧化锆修复体的厚度较薄时,种植基台背景色及粘接剂颜色均会对修复体颜色造成影响。因此在种植义齿修复过程中,当设计的修复体厚度< 2.5 mm时,推荐使用与修复体颜色一致的有色粘接剂;当修复体厚度≥2.5 mm时,种植基台背景色和粘接剂颜色对修复体的颜色影响较小,对粘接剂使用的限制也较小[27]。 "


2.3 取模 传统印模为实体印模技术,包括单一印模法、双重一步印模法和双重两步印模法。单一印模法操作相对简便,直接将印模材料一次注入口腔相应部位获取印模。双重一步印模法则是利用2种不同流动性的印模材料同时进行操作,一步到位获取印模。双重两步印模法分两步进行,先使用流动性较低的印模材料制取初印模,再用流动性高的材料在初印模基础上制取终印模。目前临床常用的全瓷固定修复印模材料有硅橡胶、聚醚橡胶等。 随着数字化技术的发展,三维扫描技术可高效、精确地获得口内软硬组织形态并转化为数字模型,进行计算辅助设计与辅助制作,因而口腔数字印模技术应运而生,包括直接和间接数字印模两种。直接数字印模借助先进的口内扫描技术,医生可直接在患者口腔内进行扫描操作,实时获取牙齿及周围组织的三维数据,间接数字印模通过牙颌印模或模型的三维扫描技术来获取所需数据。 不同取模方法的优缺点见表3。"


2.4 试戴 修复体试戴包括3个步骤[31]:在模型上对牙冠进行评估、将牙冠安装到基牙上调试、对安装好的牙冠进行最终检查确认。①试戴前在模型上检查牙冠密合度等。②将牙冠安装到基牙上:去除临时修复体,用探针去除牙面临时黏固材料,尤其是固位沟内的残留物,之后通过浮石粉和抛光杯清洁基牙表面,以清除残余的粘接材料[3]。为了不影响患者的触觉,以便评估咬合和接触紧密性,试戴过程通常不需要局部麻醉。试戴时不应将牙冠强行固定在预备体上,如未能就位,应按照以下步骤逐一排查:确保没有滞留的临时粘接剂或卡住牙龈;检查并调整过紧的接触点,然后重新检查牙冠是否存在铸造瑕疵、边缘过长、模型损坏或崩裂等问题。铸造瑕疵可用车针去除,边缘过长可用Soflex磨盘从轴向进行调整,为避免磨盘在边缘上拖曳金属,使用时应沿咬合面方向移动,而不应朝向牙冠边缘。随着口腔印模材料的迭代升级,硅橡胶印模材在临床应用越来越广,如今印模变形已不再是导致修复体不合的常见原因,但若在修复体或石膏模型上都未发现问题,应排查印模准确性,问题可能出现在印模取出过早,或手套污染导致印模材料未完全固化。遇到这种情况,需重新取印模。③仔细检查并评估安装好的牙冠的邻面接触点,确保修复体边缘与基牙预备体边缘密合,避免食物嵌塞或继发龋;评估咬合功能,调整咬合高点,避免咬合干扰或长期应力导致的牙齿损伤;验证美观效果,检查修复体的颜色、形态是否与天然牙协调(尤其前牙修复);测试舒适度,确认修复体无压迫点、不刺激软组织。 修复体试戴过程中常见的问题和解决方案如下:①修复体就位困难:首先排除基牙上残留粘接剂而导致就位失败,然后检查邻面接触状态,用咬合纸确定过紧的接触点,并进行打磨和抛光;检查技师制作时的误差;对于过于扩展的边缘,可在冠的轴面进行修整并抛光。在冠就位困难的所有不完善区域均需用车针轻轻磨除调整,随后再次试戴。②咬合过高:用咬合纸检查咬合接触,确定接触高点,用磨具调磨修复体咬合面后再次试戴,直至咬合正常。③口腔内软组织刺激:如果发现修复体边缘过于伸展或形状不规则,应对边缘进行重新修整;如修整后患者仍存在刺激感,则需重新制作修复体。如果是印模和代型问题所致的修复体边缘与实际牙体不匹配,则需重新取模制作。④修复体颜色存在偏差:首先检查在试戴时是否使用了与树脂水门汀配套的试色糊剂;如全瓷冠本身颜色与预期效果存在偏差,则可在粘接时选择颜色适当的水门汀进行调整。 "

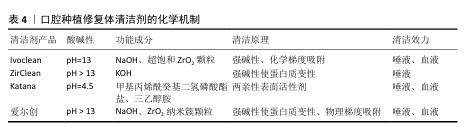
2.5 粘接 临床上,粘接是影响陶瓷及类陶瓷修复材料成功率的非常重要的因素。进行氧化锆修复体粘接操作时,应在充分清洁的基础上对基牙和修复体进行适宜的表面处理,选择性能良好的水门汀,以获得最佳的粘接强度和美观性。 2.5.1 清洁 在调整和试戴过程中唾液等对氧化锆修复体和基牙的污染难以避免,对粘接强度和持久性存在显著影响,故在粘接前对修复体和基牙表面的充分清洁不可或缺[32]。 近年来的临床应用和研究结果显示,对于氧化锆修复体的清洁,较为有效的方法是修复体清洁剂和氧化铝喷砂,而用浮石或水清洗唾液污染的氧化锆并不足以达到粘接强度[33-34]。市面上的清洁剂主要有Ivoclean(Ivoclar Vivadent,Schaan,列支敦士登)、ZirClean(BISCO,美国伊利诺伊州绍姆堡)、Katana(Kuraray Noritake Dental,日本冈山)、爱尔创(中国),它们发挥清洁功能的化学机制并不相同,见表4[35]。 "

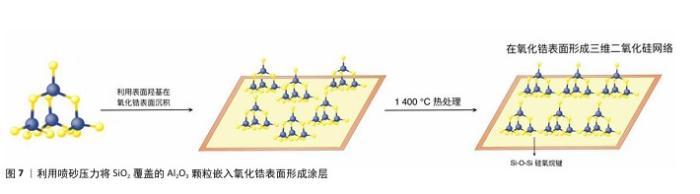
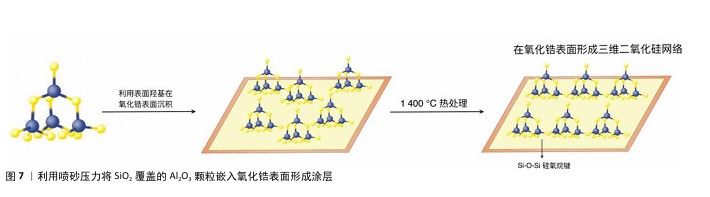
2.5.2 修复体的表面处理 未经处理的氧化锆陶瓷是一种相对惰性的基板,直接在其表面进行粘接无法获得理想的粘接效果[36],可通过物理或化学方法对氧化锆修复体进行表面处理,以增加材料表面粗糙度、湿润度和接触面积。 (1)物理处理 空气颗粒磨损(喷砂):喷砂是氧化锆全冠表面处理最常用的方法。喷砂处理后的氧化锆显示出相当的单斜相含量,单斜相变增韧会产生残余压应力,防止裂纹扩展,从而增加材料的强度[37]。然而,喷砂可能导致修复体表面损坏、机械强度减弱和使用寿命缩短[38-39]。影响喷砂效果的因素包括颗粒直径、形状、气压强度、距离和处理时间等[40]。建议使用110 μm 氧化铝(Al2O3)颗粒,在压力为0.2 MPa、距离为15 mm的条件下喷砂15 s[41]。目前临床最常使用的喷砂粒子是Al2O3或二氧化硅(SiO2)涂层铝颗粒。研究表明,使用直径30-50 μm的人造金刚石、60-80 μm的立方氮化硼及125 μm的碳化硅颗粒喷砂处理后,氧化锆修复体有较好的粘接强度[42-43],但最适条件还需进一步研究。根据氧化锆陶瓷中氧化钇含量的不同,所选择的喷砂粒子大小有所不同,以Al2O3为例,氧化锆陶瓷3Y-TZP选择110 μm,氧化锆陶瓷4Y-PSZ选择90 μm,而氧化锆陶瓷5Y-PSZ最好选用25 μm[44]。对氧化锆全瓷修复体组织面进行喷砂可形成微机械嵌合,但由于过度机械处理会影响氧化锆材料的力学性能,因此喷砂压力不宜过高,一般不超过3个大气压(304 kPa)且喷砂时间一般为20 s[45]。 激光:激光束的能量被氧化锆吸收,产生热感应过程,在陶瓷表面产生壳状破裂,增强结合、提供微机械互锁,提高表面粗糙度以及氧化锆与树脂、水门汀和瓷贴面的粘接强度[46]。 最常用于口内材料处理的激光包括CO2、铒(Er)∶YAG 和 Nd∶YAG激光等[47]。使用激光对陶瓷表面进行热感应过程中出现的贝壳状撕裂,可以在树脂复合材料和陶瓷之间提供机械保持力[48],但辐照功率过高时会导致材料表面裂纹和缺陷的产生[49-51]。由于缺乏统一标准,不同激光的辐照效果难以比较,亟待进一步研究[51]。研究发现,飞秒激光(脉冲持续时间为90 fs)是一种有效的表面处理方法,可以增加氧化锆表面的粗糙度和剪切粘接强度[52-53]。亦有研究表明,使用超短脉冲激光(1 030 nm,6 ps)对氧化锆陶瓷Y-TZP进行表面处理可显著增加材料表面粗糙度、润湿性和粘接强度[42]。 电火花加工:是一种非常规方法,通过电脉冲导致材料侵蚀,可增强材料的剪切结合强度。有研究对ZrO2-Y2O3绝缘陶瓷进行了电火花加工[54],结果表明密度为85%的铜多孔电极是最适加工材料。但有报道称,电火花加工可能导致材料出现表面裂纹[55]。 摩擦化学二氧化硅涂层:摩擦化学二氧化硅涂层用SiO2覆盖的Al2O3颗粒进行喷砂,将其嵌入氧化锆表面形成涂层,颗粒撞击陶瓷表面时释放SiO2并产生不规则表面[55],如图7所示。单独使用摩擦化学二氧化硅涂层可能出现长期黏附力不足、粘接强度受损等问题[46],一般与硅烷偶联剂合用。摩擦化学二氧化硅涂层主要有两种方法:Cojet系统和新型的Rocatec系统。Cojet系统使用SiO2(30 μm)涂层的Al2O3颗粒对氧化锆表面进行喷砂处理[55],可以在诊椅上应用;有研究通过喷砂对陶瓷粘接剂进行摩擦化学处理,然后使用硅烷溶液,速度快、准确性高、可以目视检查,并且避免了对金属框架的热应力[56]。但摩擦化学二氧化硅涂层可能引起氧化锆表面下损伤,从而影响材料的力学性能[57]。 选择性渗透蚀刻:选择性渗透蚀刻技术包含特殊的玻璃渗透剂,在半液态状态下渗入修复体表面,再用氢氟酸溶解其玻璃成分,形成纳米孔隙[58]。选择性渗透蚀刻对氧化锆的蚀刻具有选择性,操作者可自主控制与渗透剂接触的表面范围。利用选择性渗透蚀刻可与氧化锆基材料建立牢固而持久的结合,有研究表明,热诱导选择性渗透蚀刻结合喷砂与适当的热处理可以达到更好的粘接强度,从而延长修复体的使用寿命[59]。 (2)化学处理 硅涂层与硅烷化:氧化锆无法与硅烷偶联剂发生反应,故需运用一定手段在氧化锆表面涂覆一层含硅氧化物,使材料表面具有玻璃特性。有研究表明,硅涂层与硅烷化处理能显著提高材料的粘接强度[60]。目前主要用于硅涂层的方法有摩擦化学法、溶胶-凝胶法和气相沉积法。硅烷可在树脂水门汀和陶瓷表面间形成硅氧烷网络[61]:硅烷分子一端的甲氧基与SiO2共价结合形成稳定的硅氧烷(Si-O-Si),连接瓷表面;另一端的有机基团能与树脂水门汀发生共聚反应,连接树脂表面,从而增强硅基陶瓷与树脂水门汀的粘接强度[62-63]。然而,氧化锆修复体内表面沉积的微晶玻璃层所占厚度会导致边缘密合性下降;此外,玻璃层的脆弱性可能会引发材料表面缺陷和裂纹扩展[57]。 酸蚀:陶瓷类材料酸蚀通常使用氢氟酸(浓度5%-9.5%)选择性地溶解硅基陶瓷的玻璃成分,产生多孔、不规则的表面,增加材料表面积,促进树脂的渗透,但由于氧化锆为不含二氧化硅的晶体结构,传统酸蚀方法对其无效。有研究者将氧化锆陶瓷在含有800 mL乙醇、200 mL 37%盐酸和2 g氯化铁的酸溶液于100 ℃反应1 h,进行热化学蚀刻[55];还有实验对氧化锆陶瓷在室温下用40%氢氟酸进行10 min超声波蚀刻[64],超声暴露条件可增强氢氟酸的蚀刻效果,溶解氧化锆表面。 甲基丙烯酰癸基二氢磷酸酯:大量研究和临床应用表明,将含有磷酸酯单体10-甲基丙烯酰基十烷基磷酸二氢的产品应用于表面粗化后的修复体,可以得到更好的黏合效果;还有一些研究将甲基丙烯酰癸基二氢磷酸酯与硅烷化相比较,发现甲基丙烯酰癸基二氢磷酸酯可以提供更强的粘接强度和更长的持久性[65-67],单体浓度越高粘接剂的粘接效果越好,并且这种优势与甲基丙烯酰癸基二氢磷酸酯浓度呈非线性相关[68-69]。将甲基丙烯酰癸基二氢磷酸酯应用于氧化锆粘接的产品包括:含甲基丙烯酰癸基二氢磷酸酯的粘接剂(通用型或自酸蚀型)、含甲基丙烯酰癸基二氢磷酸酯的氧化锆底漆和含甲基丙烯酰癸基二氢磷酸酯的树脂水门汀[66]。当使用不同种类的含甲基丙烯酰癸基二氢磷酸酯产物时,甲基丙烯酰癸基二氢磷酸酯和氧化锆陶瓷Y-TZP的键耐久性、微泄漏和键水解存在差异。研究表明,含甲基丙烯酰癸基二氢磷酸酯的通用型粘接剂和自粘接树脂水门汀对氧化锆陶瓷Y-TZP的粘接强度高于含甲基丙烯酰癸基二氢磷酸酯的氧化锆底漆[70]。 "


2.5.3 基牙的表面处理 在粘接操作前,除了使用物理手段清洁基牙并隔湿,还应进行必要的化学处理以增强基牙与修复体之间的粘接强度。传统化学处理方法是将酸蚀剂、底漆、粘接剂3种物质按序渗透到牙体表面。根据粘接策略的不同,基牙粘接剂可分为酸蚀-冲洗型、自酸蚀型和通用型粘接剂。 酸蚀-冲洗型粘接剂分为三步型和两步型两种;自酸蚀型黏合剂有两步型、一步单瓶型和一步双瓶型。虽然两步型酸蚀-冲洗型粘接剂和一步型自酸蚀型黏合剂在临床操作上有所简化,但其粘接性能、稳定性和与树脂水门汀的相容性等却有所减弱。通用型粘接剂的“通用性”可通过2个方面体现:第一,该类粘接剂可以用于任何粘接策略,临床医生可根据临床操作中的具体情况选择酸蚀-冲洗、自酸蚀或选择性酸蚀模式[71];第二,部分通用型粘接剂可粘接操作过程中的各种其他基材,如陶瓷、金属材料和复合材料[72]。 虽然一步型自酸蚀型黏合剂和通用型粘接剂都将“酸蚀”“底漆”“粘接”三步合一,但它们的化学组成有所不同:一步单瓶型自酸蚀粘合剂含有羧酸盐或磷酸盐单体,如最常见的10-甲基丙烯酰氧基十二烷基磷酸二氢酯;通用型粘接剂中则还有几种其他功能性单体,例如甘油磷酸二甲基丙烯酸酯、4-甲基丙烯酰氧基乙基偏苯三酸、4-甲基丙烯酰氧基乙基偏苯三酸酐和二季戊四醇五丙烯酸酯磷酸酯[35]。 需要强调的是,应用磷酸对牙本质进行清洁时需使用技术敏感性高的湿粘接技术,会激活牙本质中的金属基质蛋白酶,故应谨慎操作,建议采用选择性酸蚀技术处理粘接界面并用0.2%-2%氯己定涂布磷酸处理过的粘接面,以抑制金属基质蛋白酶活性,增加粘接耐久性[73]。 "

2.5.4 树脂水门汀材料的选择 研究结果显示,磷酸锌、常规和树脂改性的玻璃离子水门汀均不能与氧化锆形成持久结合[74],氧化锆全冠需通过树脂水门汀黏合到牙本质上[75]。按照使用前基牙是否需要涂布粘接剂,树脂水门汀可分为全酸蚀树脂水门汀、自酸蚀树脂水门汀和自粘接树脂水门汀。全酸蚀系统粘接效果良好,但粘接方法复杂,需要先对牙体组织进行酸蚀处理,并且技术敏感性强、临床操作时间长[76];自酸蚀系统直接涂布表面处理剂,省略了独立的酸蚀步骤,无需水洗[75],酸蚀剂与粘接剂混合在一起,可直接作用于牙体组织,对牙本质小管的封闭效果较好,能有效降低微渗漏风险;自粘接树脂水门汀将酸蚀、底漆、粘接三步简化合一,具有机械性能强、易于粘接且操作简便等优点[77]。 树脂水门汀还可按固化方式分为光固化型、自凝型和双重固化型3种。光固化型树脂水门汀操作时间充分,聚合反应在材料暴露于光线后立即开始,但由于修复材料对光线的吸收、折射或反射使得光强度不足,树脂转化率降低[78]。自凝型树脂单体转化率高、粘接强度高,但操作时间受限 [79]。双重固化型则兼具两者的优点[80]。 自粘接树脂水门汀的固化模式多为双重固化。光照条件下的双重固化粘接效果显著强于自固化[81],但在临床实际操作中光照无法到达的部分广泛存在,故研究者未来应致力于提升自粘接树脂水门汀的自固化粘接强度,使其接近或超过光固化效果[82]。此外多项研究显示,自粘接型树脂水门汀中的酸性单体如10-甲基丙烯酰基十烷基磷酸二氢等成分有效提高了对氧化锆的粘接强度,并且使用通用型粘接剂也可优化粘接效果[83-84],但还需更多临床验证。 需要明确的是,虽然全酸蚀树脂水门汀系统操作步骤多、技术敏感性高,自粘接树脂水门汀操作步骤简单、节省时间,但它们的粘接强度相对全酸蚀系统却有所降低。故在实际应用中粘接瓷贴面应首选全酸蚀系统,而对于一些固位性较好的修复体,可以选择自粘接树脂水门汀来简化操作流程、降低技术敏感性。另外,树脂水门汀的颜色稳定性也不容忽视,尤其是对于前牙修复,应选择颜色稳定、不易变色的材料,以确保修复后的美观效果能长期维持。 "
| [1] JAIN S, SAYED ME, SHETTY M, et al. Physical and Mechanical Properties of 3D-Printed Provisional Crowns and Fixed Dental Prosthesis Resins Compared to CAD/CAM Milled and Conventional Provisional Resins: A Systematic Review and Meta-Analysis. Polymers (Basel). 2022;14(13):2691. [2] BAPAT RA, YANG HJ, CHAUBAL TV, et al. Review on synthesis, properties and multifarious therapeutic applications of nanostructured zirconia in dentistry. RSC Adv. 2022;12(20): 12773-12793. [3] 王剑,杨林新.氧化锆全冠的临床应用原则及新进展[J].华西口腔医学杂志, 2024,42(2):135-141. [4] GARVIE RC, HANNINK RH, PASCOE RT. Ceramic Steel? Nature. 1975;258(5537): 703-704. [5] KONGKIATKAMON S, ROKAYA D, KENGTANYAKICH S, et al. Current classification of zirconia in dentistry: an updated review. PeerJ. 2023;11:e15669. [6] EBERT J, OZKOL E, ZEICHNER A, et al. Direct inkjet printing of dental prostheses made of zirconia. J Dent Res. 2009;88(7):673-676. [7] 万乾炳.口腔氧化锆修复材料分代之我见[J].国际口腔医学杂志,2021,48(2):125-128. [8] 李雪菁.新型多色叠加的牙科氧化锆种植修复体的疲劳力学和透色性研究[D].沈阳:中国医科大学,2021. [9] SULAIMAN TA, SULIMAN AA, ABDULMAJEED AA, et al. Zirconia restoration types, properties, tooth preparation design, and bonding. A narrative review. J Esthet Restor Dent. 2024;36(1):78-84. [10] LWIN MOE A, TING-YI R, JERRY CHIN-YI L, et al. Nanorough Surface of Fibronectin Grafted Bioactive Zirconia Dental Implants by Using Glow Discharge Plasma Promotes Osseointegration in a Rabbit Model. Int J Nanomedicine. 2024;19:12615-12631. [11] 赵林箫,裴锡波,王剑.全解剖式氧化锆冠牙体预备原则的研究进展[J].中国现代医学杂志,2022,32(13):69-74. [12] 刘晓强,谭建国.一步一步做好微创修复的贴面牙体预备[J].中华口腔医学杂志, 2021,56(3):306-310. [13] 中华口腔医学会口腔修复学专业委员会. 椅旁计算机辅助设计与辅助制作全瓷修复技术指南[J].中华口腔医学杂志, 2022,57(10):992-996. [14] TEKIN YH, HAYRAN Y. Fracture resistance and marginal fit of the zirconia crowns with varied occlusal thickness. J Adv Prosthodont. 2020;12(5):283-290. [15] TAN J. Tooth preparation for esthetic restoration. Beijing: China Science and Technology Press, 2020. [16] HABIB SR, ASIRI W, HEFNE MJ. Effect of anatomic, semi-anatomic and non-anatomic occlusal surface tooth preparations on the adaptation of zirconia copings. J Adv Prosthodont. 2014;6(6):444-450. [17] SADID-ZADEH R, LI R, PATEL R, et al. Impact of Occlusal Intercuspal Angulation on the Quality of CAD/CAM Lithium Disilicate Crowns. J Prosthodont. 2020;29(3):219-225. [18] 王莹,刘欣然,刘峰.生物导向性预备技术的临床研究与应用现状[J].口腔颌面修复学杂志,2021,22(5):390-394. [19] 赵林箫,裴锡波,王剑.全解剖式氧化锆冠牙体预备原则的研究进展[J].中国现代医学杂志,2022,32(13):69-74. [20] ALAMMARI MR, ABDELNABI MH, SWELEM AA. Effect of total occlusal convergence on fit and fracture resistance of zirconia-reinforced lithium silicate crowns. Clin Cosmet Investig Dent. 2019;11:1-8. [21] CORAZZA PH, FEITOSA SA, BORGES AL, et al. Influence of convergence angle of tooth preparation on the fracture resistance of Y-TZP-based all-ceramic restorations. Dent Mater. 2013;29(3):339-347. [22] 叶倩倩,赵静,郑园娜.边缘设计对全锆冠强度、密合性和边缘质量影响的体外研究进展[J].口腔颌面修复学杂志,2022, 23(4):316-320. [23] PANIZ G, ZAROW M, NART J, et al. Dual-Center Cross-Sectional Analysis of Periodontal Stability Around Anterior All-Ceramic Crowns with a Feather-Edge or Chamfer Subgingival Preparation. Int J Periodontics Restorative Dent. 2020;40(4): 499-507. [24] MOHSENI P, SOUFI A, CHRCANOVIC BR. Clinical outcomes of zirconia implants: a systematic review and meta-analysis. Clin Oral Investig. 2023;28(1):15. [25] LAWSON NC, JURADO CA, HUANG CT, et al. Effect of Surface Treatment and Cement on Fracture Load of Traditional Zirconia (3Y), Translucent Zirconia (5Y), and Lithium Disilicate Crowns. J Prosthodont. 2019;28(6):659-665. [26] CHO YE, LIM YJ, HAN JS, et al. Effect of Yttria Content on the Translucency and Masking Ability of Yttria-Stabilized Tetragonal Zirconia Polycrystal. Materials (Basel). 2020; 13(21):4726. [27] WOO M, ANUNMANA C, EIAMPONGPAIBOON T. Influence of zirconia/glass veneer thickness and implant abutment material on the final shade of implant restorations. J Indian Prosthodont Soc. 2022;22(3):272-278. [28] LEE SJ, KIM SW, LEE JJ, et al. Comparison of Intraoral and Extraoral Digital Scanners: Evaluation of Surface Topography and Precision. Dent J (Basel). 2020;8(2):52. [29] ALBANCHEZ-GONZÁLEZ MI, BRINKMANN JC, PELÁEZ-RICO J, et al. Accuracy of Digital Dental Implants Impression Taking with Intraoral Scanners Compared with Conventional Impression Techniques: A Systematic Review of In Vitro Studies. Int J Environ Res Public Health. 2022;19(4):2026. [30] AHMED S, HAWSAH A, RUSTOM R, et al. Digital Impressions Versus Conventional Impressions in Prosthodontics: A Systematic Review. Cureus. 2024;16(1):e51537. [31] WASSELL RW, BARKER D, STEELE JG. Crowns and other extra-coronal restorations: try-in and cementation of crowns. Br Dent J. 2002;193(1):17-20,3-8. [32] KOKO M, TAKAGAKI T, ABDOU A, et al. Influence of 10-methacryloyloxydecyl dihydrogen phosphate (MDP) incorporated experimental cleaners on the bonding performance of saliva-contaminated zirconia ceramic. Clin Oral Investig. 2022; 26(2):1785-1795. [33] DEMIR N, GENC O, AKKESE IB, et al. Bonding Effectiveness of Saliva-Contaminated Monolithic Zirconia Ceramics Using Different Decontamination Protocols. Biomed Res Int. 2024;2024:6670159. [34] SULAIMAN TA, ALTAK A, ABDULMAJEED A, et al. Cleaning Zirconia Surface Prior To Bonding: A Comparative Study of Different Methods and Solutions. J Prosthodont. 2022;31(3):239-244. [35] ARANDI NZ. The Classification and Selection of Adhesive Agents; an Overview for the General Dentist. Clin Cosmet Investig Dent. 2023;15:165-180. [36] ABDOU A, HUSSEIN N, KUSUMASARI C, et al. Alumina and glass-bead blasting effect on bond strength of zirconia using 10-methacryloyloxydecyl dihydrogen phosphate (MDP) containing self-adhesive resin cement and primers. Sci Rep. 2023; 13(1):19127. [37] ZHANG X, LIANG W, JIANG F, et al. Effects of air-abrasion pressure on mechanical and bonding properties of translucent zirconia. Clin Oral Investig. 2021;25(4):1979-1988. [38] ZHANG Y, LAWN BR, MALAMENT KA, et al. Damage accumulation and fatigue life of particle-abraded ceramics. Int J Prosthodont. 2006;19(5):442-448. [39] FINGER C, STIESCH M, EISENBURGER M, et al. Effect of sandblasting on the surface roughness and residual stress of 3Y-TZP (zirconia). SN Appl Sci. 2020;2(10):1700. [40] OZCAN M, NIJHUIS H, VALANDRO LF. Effect of various surface conditioning methods on the adhesion of dual-cure resin cement with MDP functional monomer to zirconia after thermal aging. Dent Mater J. 2008;27(1): 99-104. [41] CHEN H, FENG S, JIN Y, et al. Comparison of bond strength of universal adhesives using different etching modes: A systematic review and meta-analysis. Dent Mater J. 2022;41(1):1-10. [42] KULUNK S, KULUNK T, URAL C, et al. Effect of air abrasion particles on the bond strength of adhesive resin cement to zirconia core. Acta Odontol Scand. 2011;69(2):88-94. [43] SATO H, YAMADA K, PEZZOTTI G, et al. Mechanical properties of dental zirconia ceramics changed with sandblasting and heat treatment. Dent Mater J. 2008;27(3): 408-414. [44] KIM HK, AHN B. Effect of Al(2)O(3) Sandblasting Particle Size on the Surface Topography and Residual Compressive Stresses of Three Different Dental Zirconia Grades. Materials (Basel). 2021;14(3):610. [45] TZANAKAKIS EG, TZOUTZAS IG, KOIDIS PT. Is there a potential for durable adhesion to zirconia restorations? A systematic review. J Prosthet Dent. 2016;115(1):9-19. [46] KHAN AA, AL KHERAIF AA, JAMALUDDIN S, et al. Recent Trends in Surface Treatment Methods for Bonding Composite Cement to Zirconia: A Reveiw. J Adhes Dent. 2017; 19(1):7-19. [47] BINRAYES A. An Update on the Use of Lasers in Prosthodontics. Cureus. 2024;16(3): e57282. [48] ERSU B, YUZUGULLU B, RUYA YAZICI A, et al. Surface roughness and bond strengths of glass-infiltrated alumina-ceramics prepared using various surface treatments. J Dent 2009;37(11):848-856. [49] LIU L, LIU S, SONG X, et al. Effect of Nd: YAG laser irradiation on surface properties and bond strength of zirconia ceramics. Lasers Med Sci. 2015;30(2):627-634. [50] LIN Y, SONG X, CHEN Y, et al. Effect of Er:YAG laser irradiation on bonding property of zirconia ceramics to resin cement. Photomed Laser Surg. 2013;31(12):619-625. [51] BITENCOURT SB, FERREIRA LC, MAZZA LC, et al. Effect of laser irradiation on bond strength between zirconia and resin cement or veneer ceramic: A systematic review and meta-analysis. J Indian Prosthodont Soc. 2021;21(2):125-137. [52] OKUTAN Y, KANDEMIR B, GUNDOGDU Y, et al. Combined application of femtosecond laser and air-abrasion protocols to monolithic zirconia at different sintering stages: Effects on surface roughness and resin bond strength. J Biomed Mater Res B Appl Biomater. 2021;109(4):596-605. [53] ESTEVES-OLIVEIRA M, JANSEN P, WEHNER M, et al. Surface Characterization and Short-term Adhesion to Zirconia after Ultra-short Pulsed Laser Irradiation. J Adhes Dent. 2016;18(6):483-492. [54] FUKUZAWA Y, YUKIHIRO K, YAMASITA K. Machining Properties of Insulating ZrO2 Ceramics Using Porous Copper Electrodes. Key Eng Mater. 2010;443:608-613. [55] SCAMINACI RUSSO D, CINELLI F, SARTI C, et al. Adhesion to Zirconia: A Systematic Review of Current Conditioning Methods and Bonding Materials. Dent J. 2019;7(3):74. [56] GUGGENBERGER R. [Rocatec system--adhesion by tribochemical coating]. Dtsch Zahnarztl Z. 1989;44(11):874-876. [57] LUNG CY, LIU D, MATINLINNA JP. Silica coating of zirconia by silicon nitride hydrolysis on adhesion promotion of resin to zirconia. Mater Sci Eng C Mater Biol Appl. 2015;46: 103-110. [58] ABOUSHELIB MN. Evaluation of zirconia/resin bond strength and interface quality using a new technique. J Adhes Dent. 2011; 13(3):255-260. [59] KUMAR NK, NAIR A, THOMAS PM, et al. Zirconia surface infiltration with low-fusing glass: A surface treatment modality to enhance the bond strength between zirconia and veneering ceramic. J Conserv Dent. 2022;25(5):492-497. [60] MAHMOODI N, HOOSHMAND T, HEIDARI S, et al. Effect of sandblasting, silica coating, and laser treatment on the microtensile bond strength of a dental zirconia ceramic to resin cements. Lasers Med Sci. 2015; 31(2):205-211. [61] MATINLINNA JP, LASSILA LV, OZCAN M, et al. An introduction to silanes and their clinical applications in dentistry. Int J Prosthodont. 2004;17(2):155-164. [62] 江楠,王楠,张懿范,等.氧化锆粘接处理剂的临床应用与前景[J].中国组织工程研究,2021,25(10):1635-1640. [63] 孙瑞瞳,李享宜,胡一淳,等.硅基陶瓷的临床应用现状与展望[J].中华口腔医学研究杂志(电子版),2021,15(2):72-78. [64] XIE H, CHENG Y, CHEN Y, et al. Improvement in the Bonding of Y-TZP by Room-temperature Ultrasonic HF Etching. J Adhes Dent. 2017;19(5):425-433. [65] WEGNER SM, KERN M. Long-term resin bond strength to zirconia ceramic. J Adhes Dent. 2000;2(2):139-147. [66] GO EJ, SHIN Y, PARK JW. Evaluation of the Microshear Bond Strength of MDP-containing and Non-MDP-containing Self-adhesive Resin Cement on Zirconia Restoration. Oper Dent. 2019;44(4):379-385. [67] COMINO-GARAYOA R, PELÁEZ J, TOBAR C, et al. Adhesion to Zirconia: A Systematic Review of Surface Pretreatments and Resin Cements. Materials (Basel). 2021; 14(11):2751. [68] YOSHIHARA K, NAGAOKA N, OKIHARA T, et al. Functional monomer impurity affects adhesive performance. Dent Mater. 2015;31(12):1493-1501. [69] LLERENA-ICOCHEA AE, COSTA RM, BORGES A, et al. Bonding Polycrystalline Zirconia With 10-MDP–containing Adhesives. Oper Dent. 2017;42(3):335-341. [70] YANG L, CHEN B, XIE H, et al. Durability of Resin Bonding to Zirconia Using Products Containing 10-Methacryloyloxydecyl Dihydrogen Phosphate. J Adhes Dent. 2018; 20(4): 279-287. [71] TIAN F, LONDONO J, VILLALOBOS V, et al. Effectiveness of different cleaning measures on the bonding of resin cement to saliva-contaminated or blood-contaminated zirconia. J Dent. 2022;120:104084. [72] ZICARI F, MONACO C, VIVAN CARDOSO M, et al. Bonding Effectiveness of Veneering Ceramic to Zirconia after Different Grit-Blasting Treatments. Dent J (Basel). 2024; 12(7):219. [73] ALZAHRANI SJ, HAJJAJ MS, ABU HAIMED TS, et al. Effect of Dentin Contamination with Hemostatic Agents and Cleaning Techniques on Bonding with Self-Adhesive Resin Cement. Med Sci Monit. 2024;30:e943353. [74] PIWOWARCZYK A, LAUER HC, SORENSEN JA. The shear bond strength between luting cements and zirconia ceramics after two pre-treatments. Oper Dent. 2005;30(3): 382-388. [75] MANSO AP, CARVALHO RM. Dental Cements for Luting and Bonding Restorations: Self-Adhesive Resin Cements. Dent Clin North Am. 2017;61(4):821-834. [76] SOKOLOWSKI G, SZCZESIO A, BOCIONG K, et al. Dental Resin Cements-The Influence of Water Sorption on Contraction Stress Changes and Hydroscopic Expansion. Materials (Basel). 2018;11(6):973. [77] CALHEIROS-LOBO MJ, VIEIRA T, CARBAS R, et al. Effectiveness of Self-Adhesive Resin Luting Cement in CAD-CAM Blocks—A Systematic Review and Meta-Analysis. Materials (Basel). 2023;16(8):2996. [78] KUGUIMIYA RN, RODE KM, CARNEIRO PM, et al. Influence of Curing Units and Indirect Restorative Materials on the Hardness of Two Dual-curing Resin Cements Evaluated by the Nanoindentation Test. J Adhes Dent. 2015;17(3):243-248. [79] 林双,黄艳苓,王晓晴,等.树脂水门汀的临床应用进展[J].中华口腔医学研究杂志(电子版) 2018,12(6):379-382. [80] ODA Y, TAKAHASHI R, NIKAIDO T, et al. Influence of the resin-coating technique on the bonding performance of self-adhesive resin cements in single-visit computer-aided design/computer-aided manufacturing resin restorations. J Esthet Restor Dent. 2022;34(4):721-728. [81] FIDALGO-PEREIRA R, TORRES O, CARVALHO Ó, et al. A Scoping Review on the Polymerization of Resin-Matrix Cements Used in Restorative Dentistry. Materials (Basel). 2023;16(4):1560. [82] 王淑君,张楚晗,唐一阳,等.自粘接树脂水门汀的临床应用及展望[J].中华口腔医学研究杂志(电子版),2024,18(4):276-286. [83] COMINO-GARAYOA R, PELÁEZ J, TOBAR C, et al. Adhesion to Zirconia: A Systematic Review of Surface Pretreatments and Resin Cements. Materials(Basel). 2021; 14(11):2751. [84] LE M, LARSSON C, PAPIA E. Bond strength between MDP-based cement and translucent zirconia. Dent Mater J. 2019; 38(3):480-489. [85] BONA, DELLA A, PECHO, et al. Zirconia as a Dental Biomaterial Materials. Materials (Basel). 2015;8(8):4978-4991. |
| [1] | Tan Fengyi, Xie Jiamin, Pan Zhenfeng, Zhang Xinxu, Zheng Zetai, Zeng Zhiying, Zhou Yanfang. Effect and mechanism of collagen combined with microneedles in treatment of skin photoaging [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(2): 451-458. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||