Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (3): 427-433.doi: 10.12307/2023.024
Previous Articles Next Articles
Application of biological materials in vital pulp therapy
Wang Ziyang, Zuo Enjun
- School of Stomatology, Dalian Medical University, Dalian 116044, Liaoning Province, China
-
Received:2021-08-26Accepted:2022-01-15Online:2023-01-28Published:2022-05-24 -
Contact:Zuo Enjun, MD, Associate chief physician, School of Stomatology, Dalian Medical University, Dalian 116044, Liaoning Province, China -
About author:Wang Ziyang, Master candidate, School of Stomatology, Dalian Medical University, Dalian 116044, Liaoning Province, China
CLC Number:
Cite this article
Wang Ziyang, Zuo Enjun. Application of biological materials in vital pulp therapy[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 427-433.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
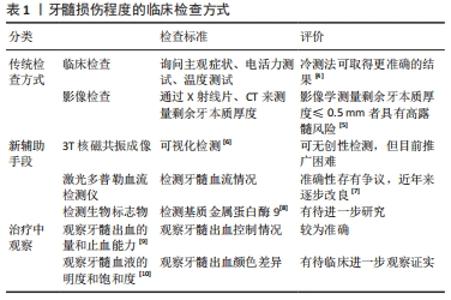
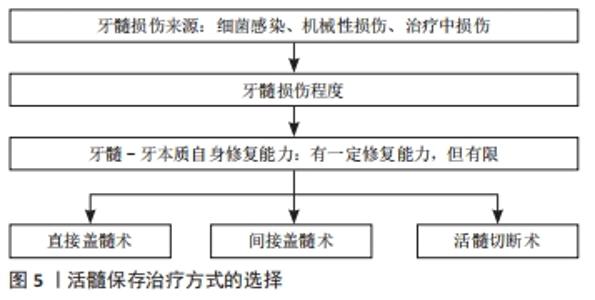
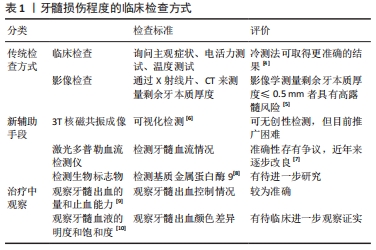
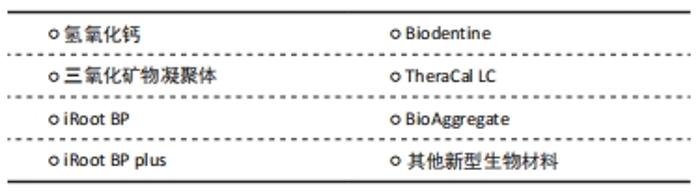
2.1.1 牙髓损伤来源 牙髓损伤来源是关键因素。临床上细菌感染是导致牙髓损伤最常见的原因,其常见的感染途径包括龋病、楔状缺损、牙隐裂、牙周病等。宿主因自身免疫机制对细菌感染产生的炎症反应和免疫反应在杀灭细菌的同时也会造成牙髓组织更进一步的损伤[2]。 机械性损伤也会对牙髓活力产生重要影响。机械性损伤包括急性创伤和慢性创伤,急性创伤常见于意外事故、暴力斗殴、咀嚼时突然咬到硬物等,慢性创伤常见于磨牙症、创伤性咬合、不良修复体等[3]。 治疗中对牙髓的损伤不容忽视。高速手机在去腐、备洞过程中产生的机械摩擦、温度刺激、各种口腔修复材料对于牙髓的化学刺激、矫正时加力过大、拔牙时误伤邻牙、深牙周袋刮治时损伤根尖血管等也都有可能对牙髓造成不同程度的损伤。临床上比较容易忽视的情况包括电流和激光对牙髓的刺激。电流刺激常见于邻牙或对颌牙存在异种金属修复体的情况,在咬合时通过唾液导电,长时间的刺激也会引起牙髓病变。不同种类的激光也会对牙髓造成不同程度的损伤,关键在于控制好合适的能量、照射时间以及采用水汽喷雾冷却。 2.1.2 牙髓损伤程度 在明确损伤来源后,活髓保存能否成功的前提在于正确诊断牙髓损伤程度,可通过主观症状、牙髓电活力测试和温度测试加以判断。在JESPERSEN等[4]的临床研究中,发现冷测法和牙髓电活力测试都是可靠的牙髓活力测试方式,对于21-50岁年龄区间的患者采用冷测法可以取得更加准确的结果。但这些方法都存在患者主观因素过多的问题,有时患者的生理和心理状态会对诊断产生影响。有学者提出可通过X射线片或者CT测量损伤距牙髓的距离来作为一种比较客观的辅助诊断方式并进行了相关实验,但目前为止尚未取得可通过影像学测量准确评估实际剩余牙本质厚度的计算方式[5]。但值得一提的是,通过实验,他们发现在影像上测量剩余牙本质厚度≤0.5 mm者具有高露髓风险。 这些常用的临床方法都无法精准地判断牙髓的损伤状态,对此有学者在不断探索检测牙髓活力的新辅助手段。ASSAF等[6]采用3T 核磁共振成像(MRI)对外伤牙进行了可视化检测,其认为3T MRI是一种非常有前景的无创性检测工具。但目前仍存在临床采集时间长、成本较高等问题。有学者提出,可通过在治疗前使用激光多普勒血流检测仪检测牙髓组织的血流情况来客观检测牙髓活性状态,但其检测结果受到多种混杂因素的影响,准确性存在争议。近年来随着仪器改良和操作规范化,激光多普勒血流检测仪的准确性有所上升。在黄定明等[7]的临床试验中激光多普勒血流检测仪取得了准确的结果,在未来有望成为更加可靠的牙髓活力诊断方式。还有学者提出通过检测牙髓血液中相关生物标志物来判断牙髓炎症程度的方式,MENTE等[8]认为基质金属蛋白酶9对于区分牙髓不同炎症阶段具有重要意义,但样本量少,仍需进一步研究。 由此可见,到目前为止还需治疗中观察牙髓状态,结合术中所见正确评估。MATSUO等[9]认为可通过在治疗中观察牙髓出血的量和止血能力来更加准确地判断牙髓状态。近年来,有学者提出可通过牙髓血液颜色的明度和饱和度来作为判断牙髓炎症状态的辅助方式。AAMINABADI等[10]对103例3-6岁患者的211颗乳磨牙进行了牙髓炎症状态和牙髓血液颜色的相关性实验,发现血液的明度和饱和度越低牙髓炎症程度越重,且这种颜色的差异在临床通过肉眼即可观察。 结合前人的研究,基于微创牙髓治疗的理念,WOLTERS等[11]提出了评估牙髓炎症状态和指导后续治疗计划的新诊断系统。摒弃了以往将牙髓炎分为可复性牙髓炎与不可复性牙髓炎的诊断方式,根据不同的临床症状,WOLTERS等[11]将牙髓炎的诊断分为初期牙髓炎、轻度牙髓炎、中度牙髓炎、重度牙髓炎。初期牙髓炎表现为对冷刺激一过性敏感,无自发痛和叩痛,推荐采用间接盖髓术;轻度牙髓炎对温度刺激和甜食产生的刺激可产生持续20 s的敏感反应,可能有叩诊敏感,此时炎症局限于冠髓,推荐采用间接盖髓术;中度牙髓炎对冷刺激可产生持续数分钟的重度敏感反应,可能有叩诊敏感和自发性钝痛,疼痛症状可或多或少地被药物压制,此时炎症在冠髓内广泛扩散,推荐采用部分或者完全的冠髓切断术;重度牙髓炎对温度刺激重度敏感,有强烈的自发痛,常有搏动性跳痛,影响睡眠,对触诊和叩诊敏感,此时冠髓的炎症向根髓蔓延,视牙髓出血的控制情况采取冠髓切断术或者根管治疗。若根管口没有持续性出血,成熟恒牙可行冠髓切断术并覆盖三氧化矿物凝聚体,然后行修复治疗。若采用2 mL 2%次氯酸钠溶液冲洗过后仍有1个或1个以上根管口持续性出血,应行浅部牙髓切断术,出血停止者在残余活髓上方采用牙胶尖和糊剂充填,出血仍持续者应行根管治疗。 牙髓损伤程度的临床检查方式,见表1。 "
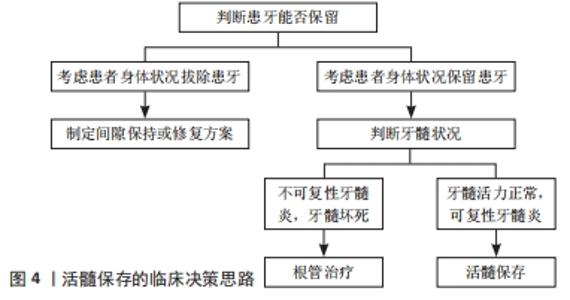
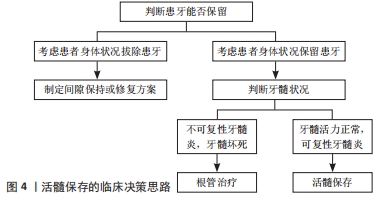
2.1.3 牙髓-牙本质复合体自身修复能力 牙髓-牙本质复合体自身的修复能力可表现为软组织愈合和硬组织愈合两个方面。轻度的外界刺激只涉及受损部位相对应的牙髓组织,重度的刺激则会对整个牙髓组织造成影响。牙髓组织可分为4层,包括成牙本质细胞层、乏细胞层、多细胞层、固有牙髓[1]。 1966年KAKEHASHI等曾将无菌鼠磨牙的牙髓在不做任何充填的情况下暴露于口腔环境中,在第14天时有钙化屏障的生成并且其下方的牙髓组织未发生炎症。这个实验说明,在遭受外界刺激时,牙髓-牙本质复合体自身就具有修复能力,关键在于彻底清除细菌感染[12]。 需要注意的是牙髓-牙本质复合体自身的修复能力是有限的。随着年龄的增加,牙髓中的细胞成分减少,根尖孔变窄且血管数目减少,自我修复功能也会逐渐降低,其解剖结构的特殊性也对其修复再生能力产生了限制。 2.2 各种盖髓剂及优缺点比较 清除感染源并有效止血后,在存活的牙髓上直接或者间接覆盖的生物医用材料称为盖髓剂。理想的盖髓剂应具备以下的性能:①具有良好的封闭性;②能引导形成高质量的牙本质桥;③能够与牙本质和修复材料形成粘接;④抗菌抑菌;⑤消除炎症;⑥可保存牙髓活力;⑦具有放射线阻射性等[13]。临床上常用的盖髓剂包括氢氧化钙和三氧化矿物凝聚体,近年来随着生物医学材料的发展,生物医学陶瓷材料、生物牙本质修补材料、硅酸钙类材料也逐渐进入临床视野中。 "
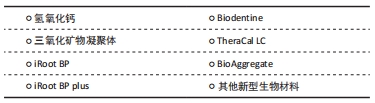

2.2.1 氢氧化钙 作为最常使用且价格低廉的盖髓制剂,氢氧化钙曾是临床活髓保存的金标准。它含有灭活细菌内毒素,抑菌性能良好,溶于水后具有强碱性,可中和细菌酸性产物[14]。氢氧化钙可提高碱性磷酸酶的活性,促进矿物质的沉积,诱导修复性牙本质生成。但随着临床研究的不断深入,人们发现其无法保证远期封闭效果。氢氧化钙溶解性大,因而不能与牙本质形成紧密连接,且诱导形成的牙本质桥多不完整且孔洞多,称为隧道样缺损。外界不良刺激可通过这些缺陷造成牙髓组织感染,后续可能引发牙髓退变及弥漫性钙化等问题。针对氢氧化钙的4种不同的制剂(氢氧化钙粉剂、Metapex、Dyca、Calcimol LC),有学者对其直接盖髓的效果进行了临床试验,并最终认为Metapex和Dyca的效果更佳[15]。另有学者指出,在根管内长期放置氢氧化钙可能会增加根折的风险[16],其临床应用范围包括直接盖髓术、间接盖髓术、活髓切断术。随着口腔材料学的发展,现氢氧化钙逐渐被多种生物材料所取代。 2.2.2 三氧化矿物凝聚体 三氧化矿物凝聚体是以三钙硅酸盐为主要成分的钙硅生物陶瓷材料。在高碱性环境下,三氧化矿物凝聚体可发生水合反应生成钙硅水合物和氢氧化钙,因而具有与氢氧化钙相似的抑菌能力[17]。除了具有良好的消炎和抑菌能力外,三氧化矿物凝聚体同时有良好的生物活性和组织兼容性,可提高促进矿化的转化生长因子β1、白细胞介素6、白细胞介素8水平,增加碱性磷酸酶、骨钙蛋白及骨形态发生蛋白2的表达[18],它的粘接性能优于氢氧化钙,溶解度低,凝固后硬度和密封能力好,诱导形成的修复性牙本质桥相较于氢氧化钙更加致密,对炎症的控制优于氢氧化钙,作为直接盖髓剂时可拥有长效作用[19],术后较少引起牙髓组织的充血和炎症反应,盖髓成功率高于氢氧化钙[20]。尽管性能优良,但三氧化矿物凝聚体仍存在价格高、技术敏感性高、固化时间较长、无法完全抵抗微渗漏[21]、酸性环境粘接性差等问题。需要注意的是,三氧化矿物凝聚体与牙齿结构接触时其中所含的氧化铋成分会与牙本质基质中胶原蛋白发生反应,导致呈现出灰色的变色反应[22],其临床应用范围包括直接盖髓术、间接盖髓术、活髓切断术,推荐在非前牙美学区使用。 2.2.3 iRoot BP和iRoot BP plus(Innovative Bioceramix Inc, Vancouver,加拿大) IRoot BP和iRoot BP plus成分相似,为预混合生物陶瓷的不同剂型,iRoot BP为注射糊剂,iRoot BP Plus为膏体。在固化过程中可释放OH-使周围环境pH值升高,通过改变环境中的pH值可产生良好的抑菌作用[23],其在潮湿环境下发生水合反应产生硅酸钙凝胶和氢氧化钙,并与磷酸钙反应形成羟基磷灰石,且不产生凝固收缩,有良好的边缘封闭性[24]。近年来多组实验证明iRoot BP plus和三氧化矿物凝聚体诱导形成修复性牙本质的性能相近,具有相似的生物兼容性和密封性[25],有体外实验发现相较于三氧化矿物凝聚体,iRoot BP促进矿化的能力更强[26]。iRoot BP的临床操作更加方便,固化时间相对较短。此外iRoot BP和iRoot BP plus中采用氧化钽和氧化锆作为X射线阻射成分,不含三氧化二铋,相较于三氧化矿物凝聚体具有更好的颜色稳定性。有体外实验显示iRoot BP可募集牙髓干细胞、早期促进成牙本质细胞分化并且细胞毒性低,生物相容性好[27]。 但有学者发现,iRoot BP相较于三氧化矿物凝聚体更易导致一过性冷刺激疼痛症状的发生[28],怀疑与牙髓炎症状态和自身免疫反应有关。针对于外伤露髓的年轻恒牙的盖髓治疗,有学者进行了相关的临床研究,发现iRoot BP组所形成的钙化桥厚度低于氢氧化钙组[29]。针对于以上矛盾的实验结果,iRoot BP的疗效仍有待于进一步的研究。 2.2.4 Biodentine Biodentine为具有生物活性的钙硅材料,主要成分为硅酸三钙和氯化钙,能通过促进转化生长因子β释放和诱导成牙本质细胞增生分化形成矿化组织,抗菌性能好,具有生物活性与生物相容性[30]。Biodentine除了可在牙本质表面形成一层致密钙化层之外,还可深入牙本质小管内形成条索状结构,形成良好的矿物浸润层,可严密封闭牙髓形成良好的微观机械固位。ABUELNIEL等[31]进行Biodentine作为活髓切断术盖髓材料的临床试验,证实其临床效果和影像学表现与三氧化矿物凝聚体相似。Biodentin具有与三氧化矿物凝聚体相似的性能且有X射线阻射性,可操作性、粘接性能优于三氧化矿物凝聚体,引起牙齿变色效应小[32]。AWAWDEH等[33]为比较三氧化矿物凝聚体和Biodentine治疗因龋露髓患牙的临床疗效进行了长达3年的临床研究,认为二者具有相似的临床疗效。在LINU等[34]的实验中,尽管Biodentine相较于三氧化矿物凝聚体表现出了更高的成功率,但有23.1%的患者出现了髓腔弥散性钙化。同时,关于Biodentine是否会导致牙齿变色,近年来也有越来越多的学者提出了不同的观点。SLABOSEVICIUTE等[35]对此进行了系统性回顾,其认为在临床操作过程中Biodentine与血液直接接触会提高变色的可能性,在无血液影响的情况下导致其变色的原因仍不明确。Biodentine具有极高的研究价值,但目前在国内关于其应用效果尚且缺乏足够的临床试验和研究。 2.2.5 TheraCal LC 为一种光固化、树脂改良硅酸钙材料,主要成分为波特兰水门汀,pH值为10,属于碱性材料,相较于ProRoot MTA和Dycal可释放更多且不易被溶解的Ca2+,促进牙本质桥形成[36];可操作性好,具有X射线阻射性且粘接性好,拥有良好的封闭性,减少了边缘微渗漏。有学者分别采用TheraCal LC和Dycal对龋源性露髓的乳牙和恒牙进行直接盖髓治疗,结果显示TheraCal作为盖髓剂在乳牙组中的治疗效果优于Dycal,在恒牙组中的治疗效果两者取得了相似的成功率[37]。另有学者比较了iRoot BP Plus、Theracal LC和三氧化矿物凝聚体在龋源性露髓恒牙中直接盖髓术的临床疗效,认为3者的临床疗效相当[28]。马小红等[38]针对于乳牙行活髓保存的临床研究中也取得了三氧化矿物凝聚体和TheraCal LC疗效相当的结果。牙髓暴露止血后,其可用于龋源性、机械性、外伤性露髓的直接盖髓术、间接盖髓术。 此外,也有学者提出了不同的观点,有动物实验和人体临床试验显示,TheraCal形成牙本质桥的能力低于三氧化矿物凝聚体,有可能引起更强的炎症反应[39-40]。但上述实验的局限性在于样本数量不足,目前国内关于TheraCal LC的临床试验研究仍有不足。 2.2.6 BioAggregate 属于新型生物陶瓷纳米材料,主要成分为硅酸三钙、硅酸二钙,能促进牙髓细胞分化为成牙本质细胞和形成矿化节[41]。BioAggregate具有良好的生物相容性和生物安全性,可诱导形成修复性牙本质。有学者回顾了既往的体外实验结果,认为BioAggregate相较于三氧化矿物凝聚体具有更好的诱导能力和促进矿化的能力[42]。为比较三氧化矿物凝聚体和Biodentine两者的临床治疗效果,有学者以需行活髓切断术的龋源性露髓患牙为研究对象,进行了长达2年的临床试验,最终认为二者都有良好的治疗效果[43]。但有动物实验显示其形成牙本质桥的能力低于三氧化矿物凝聚体和Biodentine[44],而且凝固时间长,操作性不佳。BioAggregate是在三氧化矿物凝聚体基础上成分有所改良的一种材料,最初应用于根管充填,目前的研究结果尚且不足以证明其是否具有形成高质量牙本质桥的能力。 2.2.7 其他新型生物材料 釉基质衍生物主要由釉原蛋白和海藻酸丙二醇组成,具有杀菌作用和诱导牙本质生成的能力。在张贝蒂[45]的实验研究中,釉基质衍生物在体外和体内都可促进人牙髓干细胞成牙本质向分化、成血管向分化以及促进硬组织矿化。为研究Emdogain作为活髓保存制剂的使用疗效,NAJEEB等[46]进行了回顾性研究,认为目前尚无法证实其是否可以替代其他传统的盖髓制剂。除此之外,目前关于生物支架材料、藻朊酸盐、壳聚糖、透明质酸、胶原、纤维蛋白、自组装肽纳米纤维、生长因子等都处于积极的实验研究过程中[47]。 各盖髓剂的优缺点比较,见表2。 "

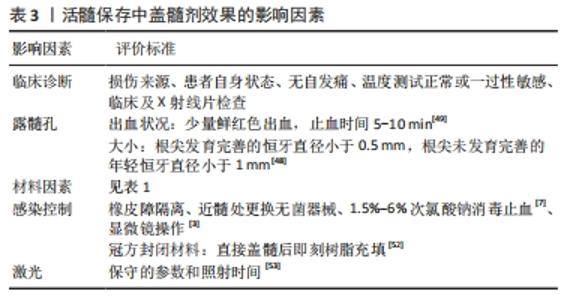
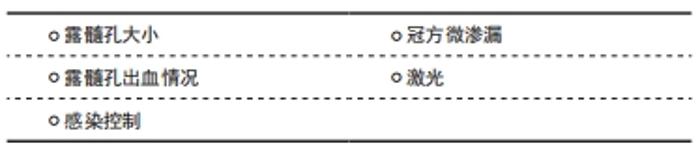
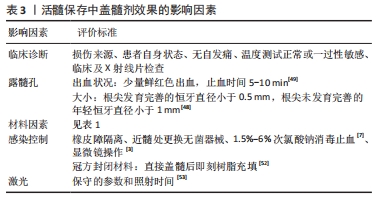
2.3.1 露髓孔大小 牙髓暴露的范围越小预后越好。若行直接盖髓术,根尖发育完善的患牙因机械性或外伤性露髓者,露髓孔应不超过0.5 mm,根尖孔未发育完全的患牙露髓孔直径应小于1 mm。根尖未发育完善的年轻恒牙露髓孔直径大于1 mm者,为使牙根继续发育应尽量保留未受感染的根髓,行活髓切断术[48]。 2.3.2 露髓孔出血情况 露髓后的出血和止血状态也是治疗中观察牙髓状况的重要指标。少量鲜红色出血,止血时间为5-10 min为直接盖髓术的适应证。露髓点有不可控的出血则不宜行直接盖髓术,此时应考虑部分或完全去除冠髓,若出血仍无法控制,则应考虑牙髓摘除术[49]。关于哪种止血剂效果更佳目前尚无定论,目前常推荐使用1.5%-6%的次氯酸钠与牙髓直接接触[7]。 2.3.3 感染控制 活髓保存中医师需将“无菌”观念贯穿于整个治疗过程中。在治疗过程中控制感染的措施包括采用橡皮障隔离、碘伏术区消毒、在显微镜下精确操作、去腐至近髓处更换无菌器械、1.5%-6%次氯酸钠局部消毒止血等[3]。 2.3.4 冠方微渗漏 冠方的严密封闭可隔绝外界感染来源,提供牙本质桥的形成环境。洞形、洞位、冠方封闭材料、行封闭的时间都会对冠方微渗漏情况产生影响。有研究发现,直接盖髓后采用玻璃离子充填疗效较差[50],另一项研究表明,术后超过2 d再行永久充填的牙齿预后差[51]。为保证冠方的严密封闭,目前临床上推荐直接盖髓后即刻树脂充填[52]。 2.3.5 激光 低能量激光在临床上活髓保存的辅助治疗中也有着广阔的前景,在辅助活髓保存中具有以下优势:①杀菌;②止血;③协助封闭牙本质小管;④处理牙髓组织断面;⑤促进细胞增殖和控制活髓局部钙化;⑥减少患者痛苦。临床上常用的激光器包括CO?激光、Nd: YAG激光、Er, Cr:YSGG激光、Er:YAG激光、二极管激光等,都具有不同的主要特性。低能量激光可提高活髓保存的成功率,但是照射次数存在阈值,否则会导致牙髓坏死以及继发性炎症等不可逆性损伤,建议使用保守的参数和照射时间[53]。但需要注意的是,活髓保存治疗中,盖髓剂的选择更加重要。BIDAR等[54]所进行的动物实验发现,盖髓剂的性能比是否使用激光治疗更加重要。在观察单独使用ProRoot MTA和ProRoot MTA联合Er:YAG激光进行直接盖髓术的临床疗效观察中,二者间也并无明显差异[55]。 活髓保存中盖髓剂效果的影响因素,见表3。 "
| [1] 高岩,孙宏晨,李江.口腔组织病理学[M].北京:人民卫生出版社, 2020:57-62. [2] 陈杰,徐华兴,程抒华,等.细胞自噬在牙髓损伤修复过程中的作用[J].口腔医学研究,2019,35(6):531-536. [3] 周学东,黄定明,刘建国,等.牙髓损伤的活髓保存治疗[J].华西口腔医学杂志,2017,35(4):339-347. [4] JESPERSEN JJ, HELLSTEIN J, WILLIAMSON A, et al. Evaluation of dental pulp sensibility tests in a clinical setting. J Endod. 2014;40(3):351-354. [5] JHANY NA, HAWAJ BA, HASSAN AA, et al. Comparison of the Estimated Radiographic Remaining Dentine Thickness with the Actual Thickness Below the Deep Carious Lesions on the Posterior Teeth: An in vitro Study. Eur Endod J. 2019;4(3):139-144. [6] ASSAF AT, ZRNC TA, REMUS CC, et al. Early detection of pulp necrosis and dental vitality after traumatic dental injuries in children and adolescents by 3-Tesla magnetic resonance imaging. J Craniomaxillofac Surg. 2015;43(7):1088-1093. [7] 黄定明,陆倩,廖茜,等.活髓保存之惑及解决之道[J].华西口腔医学杂志,2017,35(3):227-231. [8] MENTE J, PETROVIC J, GEHRIG H, et al. A Prospective Clinical Pilot Study on the Level of Matrix Metalloproteinase-9 in Dental Pulpal Blood as a Marker for the State of Inflammation in the Pulp Tissue. J Endod. 2016;42(2):190-197. [9] MATSUO T, NAKANISHI T, SHIMIZU H, et al. A clinical study of direct pulp capping applied to carious-exposed pulps. J Endod. 1996;22(10):551-556. [10] AMINABADI NA, PARTO M, EMAMVERDIZADEH P, et al. Pulp bleeding color is an indicator of clinical and histohematologic status of primary teeth. Clin Oral Investig. 2017;21(5):1831-1841. [11] WOLTERS WJ, DUNCAN HF, TOMSON PL, et al. Minimally invasive endodontics: a new diagnostic system for assessing pulpitis and subsequent treatment needs. Int Endod J. 2017;50(9):825-829. [12] JEERUPHAN T, JANTARAT J, YANPISET K, et al. Mahidol study 1: comparison of radiographic and survival outcomes of immature teeth treated with either regenerative endodontic or apexification methods: a retrospective study. J Endod. 2012;38(10):1330-1336. [13] QURESHI A, SOUJANYA E, NANDAKUMAR P. Recent advances in pulp capping materials: an overview. J Clin Diagn Res. 2014;8(1):316-321. [14] 张瑶,曹钰,万领,等.三氧化钙无机聚合物或氢氧化钙直接盖髓对因龋露髓恒牙活髓保存疗效的Meta分析[J].口腔医学,2016,36(9): 841-844,856. [15] 聂二民,姜瑞,张春元,等.不同氢氧化钙制剂深龋意外穿髓直接盖髓的临床研究[J].实用医学杂志,2015,31(19):3278-3279. [16] ANDREASEN JO, FARIK B, MUNKSGAARD EC. Long-term calcium hydroxide as a root canal dressing may increase risk of root fracture. Dent Traumatol. 2002;18(3):134-137. [17] 文静,洪席超,于世德,等.2种盖髓剂体内直接盖髓后的组织病理学变化[J].实用医学杂志,2016,32(13):2175-2177. [18] 史爽.矿物三氧化物凝聚体在修复性牙本质形成中作用研究进展[J].中国实用口腔科杂志,2015,8(6):374-377. [19] MENTE J, GELETNEKY B, OHLE M, et al. Mineral trioxide aggregate or calcium hydroxide direct pulp capping: an analysis of the clinical treatment outcome. J Endod. 2010;36(5):806-813. [20] CUSHLEY S, DUNCAN HF, LAPPIN MJ, et al. Efficacy of direct pulp capping for management of cariously exposed pulps in permanent teeth: a systematic review and meta-analysis. Int Endod J. 2021;54(4):556-571. [21] 黄伟曼,张栋杰,胡旭初,等.iRoot BP Plus和MTA用于年轻恒牙直接盖髓的临床疗效观察[J].中华口腔医学研究杂志(电子版),2017, 11(6):366-370. [22] MARCIANO MA, COSTA RM, CAMILLERI J, et al. Assessment of color stability of white mineral trioxide aggregate angelus and bismuth oxide in contact with tooth structure. J Endod. 2014;40(8):1235-1240. [23] ALSALLEEH F, CHUNG N, STEPHENSON L. Antifungal activity of endosequence root repair material and mineral trioxide aggregate. J Endod. 2014;40(11):1815-1819. [24] 李羽弘,韦曦.iRoot BP和iRoot BP Plus应用于牙髓治疗的研究现状[J].中华口腔医学研究杂志(电子版),2016,10(3):208-211. [25] 周瑾,王丁.iRoot BP Plus和MTA直接盖髓临床效果及影响因素研究[J].临床口腔医学杂志,2020,36(3):147-149. [26] WANG J, FANGTENG JZ, LIU H. Effect of iRoot BP Plus on biological behavior of deciduous tooth pulp stem cells and human pulp stem cells. Shanghai Kou Qiang Yi Xue. 2019;28(3):251-258. [27] ÖNCEL TORUN Z, TORUN D, DEMIRKAYA K, et al. Effects of iRoot BP and white mineral trioxide aggregate on cell viability and the expression of genes associated with mineralization. Int Endod J. 2015;48(10):986-993. [28] 范博文,于飞.硅酸钙类盖髓剂用于深龋恒牙直接盖髓的临床疗效观察[J].临床口腔医学杂志,2021,37(8):480-482. [29] YANG Y, XIA B, XU Z, et al. The effect of partial pulpotomy with iRoot BP Plus in traumatized immature permanent teeth: A randomized prospective controlled trial. Dent Traumatol. 2020;36(5):518-525. [30] RAJASEKHARAN S, MARTENS LC, CAUWELS RGEC, et al. Biodentine material characteristics and clinical applications: a 3 year literature review and update. Eur Arch Paediatr Dent. 2018;19(1):1-22. [31] ABUELNIEL GM, DUGGAL MS, KABEL N. A comparison of MTA and Biodentine as medicaments for pulpotomy in traumatized anterior immature permanent teeth: A randomized clinical trial. Dent Traumatol. 2020;36(4):400-410. [32] YOLDAŞ SE, BANI M, ATABEK D, et al. Comparison of the Potential Discoloration Effect of Bioaggregate, Biodentine, and White Mineral Trioxide Aggregate on Bovine Teeth: In Vitro Research. J Endod. 2016; 42(12):1815-1818. [33] AWAWDEH L, AL-QUDAH A, HAMOURI H, et al. Outcomes of Vital Pulp Therapy Using Mineral Trioxide Aggregate or Biodentine: A Prospective Randomized Clinical Trial. J Endod. 2018;44(11):1603-1609. [34] LINU S, LEKSHMI MS, VARUNKUMAR VS, et al. Treatment Outcome Following Direct Pulp Capping Using Bioceramic Materials in Mature Permanent Teeth with Carious Exposure: A Pilot Retrospective Study. J Endod. 2017;43(10):1635-1639. [35] SLABOSEVICIUTE M, VASILIAUSKAITE N, DRUKTEINIS S, et al. Discoloration Potential of Biodentine: A Systematic Review. Materials (Basel). 2021;14(22):6861. [36] GANDOLFI MG, SIBONI F, PRATI C. Chemical-physical properties of TheraCal, a novel light-curable MTA-like material for pulp capping. Int Endod J. 2012;45(6):571-579. [37] 梁秋娟,朱丽德孜·托列别克,古力巴哈·买买提力.TheraCalLC和Dycal两种盖髓剂用于乳牙和恒牙直接盖髓的疗效比较[J].口腔材料器械杂志,2018,27(3):178-180. [38] 马小红,谢妮娜.不同生物材料在乳牙牙髓保存术中的应用:前瞻性、单中心、随机对照临床试验[J].中国组织工程研究,2017,21(22): 3494-3500. [39] LEE H, SHIN Y, KIM SO, et al. Comparative Study of Pulpal Responses to Pulpotomy with ProRoot MTA, RetroMTA, and TheraCal in Dogs’ Teeth. J Endod. 2015;41(8):1317-1324. [40] BAKHTIAR H, NEKOOFAR MH, AMINISHAKIB P, et al. Human Pulp Responses to Partial Pulpotomy Treatment with TheraCal as Compared with Biodentine and ProRoot MTA: A Clinical Trial. J Endod. 2017; 43(11):1786-1791. [41] JUNG JY, WOO SM, LEE BN, et al. Effect of Biodentine and Bioaggregate on odontoblastic differentiation via mitogen-activated protein kinase pathway in human dental pulp cells. Int Endod J. 2015;48(2):177-184. [42] SONG W, LI S, TANG Q, et al. In vitro biocompatibility and bioactivity of calcium silicate-based bioceramics in endodontics (Review). Int J Mol Med. 2021;48(1):128. [43] KIM J, SONG YS, MIN KS, et al. Evaluation of reparative dentin formation of ProRoot MTA, Biodentine and BioAggregate using micro-CT and immunohistochemistry. Restor Dent Endod. 2016;41(1):29-36. [44] ÇELIK BN, MUTLUAY MS, ARIKAN V, et al. The evaluation of MTA and Biodentine as a pulpotomy materials for carious exposures in primary teeth. Clin Oral Investig. 2019;23(2):661-666. [45] 张贝蒂.釉基质蛋白在人牙髓干细胞成牙本质向分化过程中的作用及机制研究[D].沈阳:中国医科大学,2021. [46] NAJEEB S, KHURSHID Z, SOHAIL ZAFAR M, et al. Efficacy of Enamel Matrix Derivative in Vital Pulp Therapy: A Review of Literature. Iran Endod J. 2017;12(3):269-275. [47] HANNA SN, PEREZ ALFAYATE R, PRICHARD J. Vital Pulp Therapy an Insight Over the Available Literature and Future Expectations. Eur Endod J. 2020;5(1):46-53. [48] 周学东,陈智,岳林.牙体牙髓病学[M].北京:人民卫生出版社, 2020:141-142. [49] AGUILAR P, LINSUWANONT P. Vital pulp therapy in vital permanent teeth with cariously exposed pulp: a systematic review. J Endod. 2011; 37(5):581-587. [50] HARMS CS, SCHÄFER E, DAMMASCHKE T. Clinical evaluation of direct pulp capping using a calcium silicate cement-treatment outcomes over an average period of 2.3 years. Clin Oral Investig. 2019;23(9):3491-3499. [51] MENTE J, HUFNAGEL S, LEO M, et al. Treatment outcome of mineral trioxide aggregate or calcium hydroxide direct pulp capping: long-term results. J Endod. 2014;40(11):1746-1751. [52] 刘思毅,宫玮玉,刘木清,等.成熟恒牙因龋露髓行生物陶瓷材料直接盖髓术的临床疗效观察[J].中华口腔医学杂志,2020,55(12): 945-951. [53] 张英,崔丹.激光在直接盖髓术中应用的研究进展[J].中国实用口腔科杂志,2018,11(11):645-649. [54] BIDAR M, MOUSHEKHIAN S, GHARECHAHI M, et al. The Effect of Low Level Laser Therapy on Direct Pulp Capping in Dogs. J Lasers Med Sci. 2016;7(3):177-183. [55] KERMANSHAH H, RANJBAR OMRANI L, GHABRAEI S, et al. Direct Pulp Capping With ProRoot MTA Alone and in Combination With Er:YAG Laser Irradiation: A Clinical Trial. J Lasers Med Sci. 2020;11(Suppl 1):S60-S66. [56] 文静,洪席超,郜文秀,等.MTA用于年轻恒前牙直接盖髓术的临床效果观察[J].口腔疾病防治,2017,25(5):320-322. |
| [1] | Zhao Ying, Liang Guangzhi, Zhou Yuqi, Wang Tianqi, Liu Yunxia, Liu Xiaoying, Zhang Juanjuan, Sun Yan. Effects of iRoot BP Plus combined with Yunnan Baiyao on mineralization of dental pulp stem cells under inflammatory conditions [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(19): 2960-2967. |
| [2] | Yan Qifang, Xie Cuiliu, Yan Guowei. Effect of concentrated growth factor and bioceramic material iRoot BP on survival, proliferation and mineralization of human dental pulp cells in vitro [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(21): 3363-3368. |
| [3] | Yang Yanan, Li Junfeng, Wang Li, Liu Hengquan, Lai Xuefei . Calcium citrate: an interesting organic calcium biomedical material [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(10): 1609-1615. |
| [4] | Zhao Binbin, Qiu Zewen, Ma Chenghui, Zhong Weijian, Ma Guowu. Effect of different techniques on the osteogenic property of undecalcified heterogeneous dentin particles [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(26): 4154-4159. |
| [5] | Chen Ruihong, Ge Hongqing, Chen Wenzhi. Comparison of one-year follow-up effectiveness between high tibial osteotomy and unicompartmental knee arthroplasty for treating medial compartment osteoarthritis of the knee [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(20): 3143-3147. |
| [6] | Nie Er-min, Chen Xia-yun, Zhang Chun-yuan, Jiang Rui, Xia Yin-hua. Apexification of abnormal central cusp teeth with four kinds of calcium hydroxide preparations [J]. Chinese Journal of Tissue Engineering Research, 2013, 17(8): 1398-1403. |
| [7] | Yang Liu-cheng, Xu Shuai, Li Shi-si, Wu Kai, Wang Jian-jun. In vitro cytotoxicity of nanoAg-SiO2 polyurethane materials [J]. Chinese Journal of Tissue Engineering Research, 2013, 17(3): 392-399. |
| [8] | Pang Li-yun, Wang Hai, Chen Yong-xia, Liu Shuai, Yang Jing, Sun Hong-fan. Paclitaxel poly lactide-co-glycolic acid nanoparticles inhibit human hepatocellular carcinoma cells HepG2 [J]. Chinese Journal of Tissue Engineering Research, 2013, 17(3): 412-418. |
| [9] | Zhou Ji-hui, Yao Meng, Wang Yan-song, Liu Yu-gang, Sui Fu-ge, Zhao Cong-ran, Tian Fei-peng, He Xiao-feng. New-type nano-scaffolds and neural stem cell apoptosis [J]. Chinese Journal of Tissue Engineering Research, 2013, 17(3): 419-426. |
| [10] | Xu Ning, Chen Yu-yun, Zhong Jian, Xu Guo-hua, Ye Xiao-jian. Effect of silk fibroin on the regulation of nano-hydroxyapatite crystal growth [J]. Chinese Journal of Tissue Engineering Research, 2013, 17(3): 427-432. |
| [11] | Feng Xue-yi, Liu Zheng-ni, Tang Rui, Hu Heng-yao. Constructing a vascular endothelial growth factor sustained-released multi-wall carbon nanotube composite scaffold [J]. Chinese Journal of Tissue Engineering Research, 2013, 17(3): 433-439. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||