Chinese Journal of Tissue Engineering Research ›› 2026, Vol. 30 ›› Issue (25): 6610-6620.doi: 10.12307/2026.295
Previous Articles Next Articles
Role of bone–blood axis in bone mass regulation and hematopoietic function maintenance
Hong Linling1, 2, Zhang Kunpeng1, 2, Zheng Liming3, Ye Baodong1, 2, Liu Jingjing1, 2
- 1First Affiliated Hospital of Zhejiang Chinese Medical University, Hangzhou 310060, Zhejiang Province, China; 2First Clinical Medical College, Zhejiang Chinese Medical University, Hangzhou 310053, Zhejiang Province, China; 3Orthopedics Department, The Second Affiliated Hospital, Zhejiang University School of Medicine, Hangzhou 310009, Zhejiang Province, China
-
Received:2025-11-11Revised:2025-12-23Online:2026-09-08Published:2026-04-23 -
Contact:Liu Jingjing, PhD, First Affiliated Hospital of Zhejiang Chinese Medical University, Hangzhou 310060, Zhejiang Province, China; First Clinical Medical College, Zhejiang Chinese Medical University, Hangzhou 310053, Zhejiang Province, China Co-corresponding author: Zheng Liming, PhD, Distinguished Research Fellow, Orthopedics Department, The Second Affiliated Hospital, Zhejiang University School of Medicine, Hangzhou 310009, Zhejiang Province, China Co-corresponding author: Ye Baodong, PhD, Professor/Chief physician, First Affiliated Hospital of Zhejiang Chinese Medical University, Hangzhou 310060, Zhejiang Province, China; First Clinical Medical College, Zhejiang Chinese Medical University, Hangzhou 310053, Zhejiang Province, China -
About author:Hong Linling, First Affiliated Hospital of Zhejiang Chinese Medical University, Hangzhou 310060, Zhejiang Province, China; First Clinical Medical College, Zhejiang Chinese Medical University, Hangzhou 310053, Zhejiang Province, China -
Supported by:National Natural Science Foundation of China, No. 32401092 (to ZLM); “Renhe Excellent Doctoral Talent Program” of The First Affiliated Hospital of Zhejiang Chinese Medical University (to LJJ)
CLC Number:
Cite this article
Hong Linling, Zhang Kunpeng, Zheng Liming, Ye Baodong, Liu Jingjing, . Role of bone–blood axis in bone mass regulation and hematopoietic function maintenance[J]. Chinese Journal of Tissue Engineering Research, 2026, 30(25): 6610-6620.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
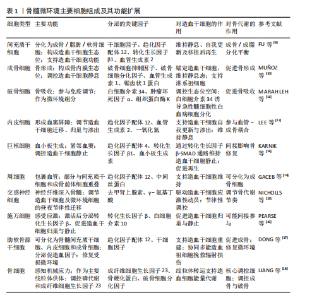
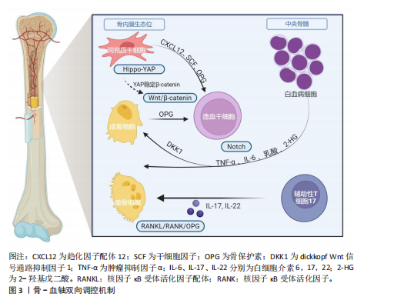
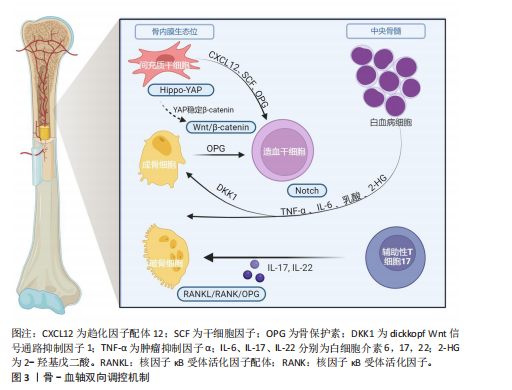
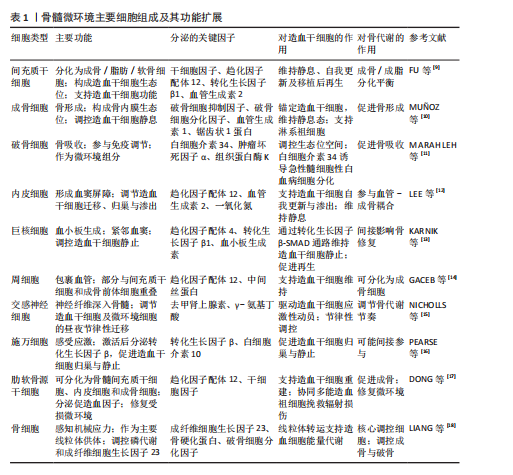
2.1 骨与血液系统间相互调控机制的研究进展 2.1.1 骨与血液系统通过骨髓微环境双向调控 骨骼与血液系统间存在的共病关系提示二者存在相互作用。众所周知,骨髓是最主要的造血场所,而作为血液细胞的祖细胞,造血干细胞在其中的作用尤为重要,因此重点针对造血干细胞与骨髓细胞间的相关性展开了回顾研究。如前所述,随着“骨髓壁龛”这一概念的提出,骨髓微环境对造血系统的作用受到广泛重视,而其在骨量维持中亦起到了关键作用。骨髓微环境是一个复杂的动态调控网络,由非细胞成分与夹杂其中的细胞共同构成。其中非细胞组分主要包括细胞外基质(纤连蛋白、层粘连蛋白)和关键信号分子(例如趋化因子配体12/干细胞因子[5]、Wnt/β-连环蛋白、干扰素-γ通路)等[6]。细胞外基质为细胞提供了合适的生长分化“土壤”,主要通过机械因素与黏附作用等调控细胞行为。而信号分子则通过与细胞的相互作用,通过化学方式激活细胞中相关信号转导通路调控其行为。而在其中的细胞种子主要包括基质细胞及其分化谱系(如间充质干细胞、成骨细胞[7]、骨细胞、软骨细胞、脂肪细胞)、血管与神经细胞(如内皮细胞、周细胞)和免疫细胞(如巨噬细胞、中性粒细胞、T淋巴细胞)等多种细胞类型。为清晰呈现,现将各主要细胞组成、其功能、分泌产物及作用系统归纳于表1。随着单细胞测序技术的兴起与普及,针对细胞亚群的分型越来越细,如瘦素受体阳性间充质基质细胞、N-钙黏蛋白阳性的成骨前体细胞等具有功能特异性的细胞群体被不断的鉴定出来[8]。而随着空间转录组技术的应用,细胞与细胞外基质的相互作用也引起了大量关注,这也为研究骨与骨髓这两种空间位置毗邻的组织提供了新的手段。总的来说,随着研究手段的迭代,骨与血液系统间通过骨髓微环境的相互作用也被不断揭示(图3)。 2.1.2 骨对造血干细胞的支持与调控作用 在生理稳态下,骨髓微环境通过其组分的对称性动态变化,精准调控造血干细胞的静息状态,从而对其起到重要的保护作用。然而一旦骨髓微环境的稳态失调,其信号网络将发生重编程,"
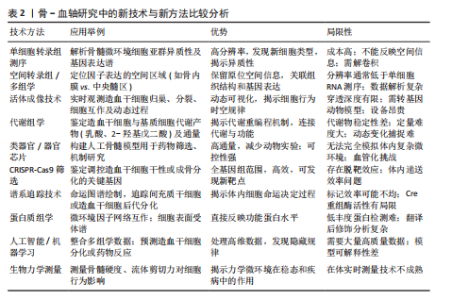
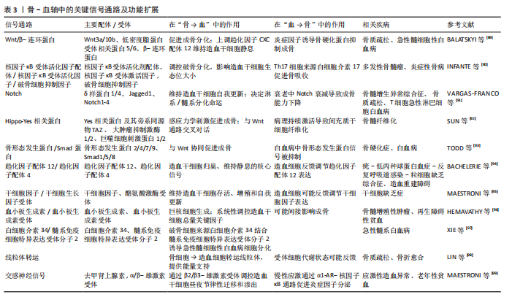
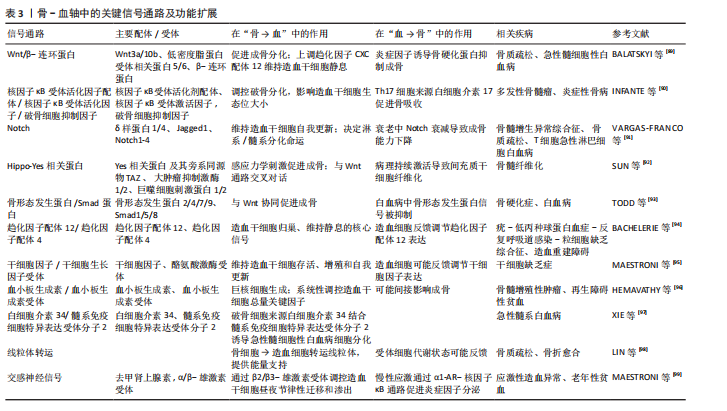
进而激活造血干细胞进入细胞周期。若微环境持续处于病理状态,扰乱造血干细胞的正常功能,甚至诱发其恶性转化[18]。骨髓微环境中的各种类型细胞(如骨相关细胞、内皮细胞、髓系细胞、淋系细胞)及其分泌的细胞因子、趋化因子等信号分子,共同参与了对造血干细胞的自我更新、迁徙、分化和凋亡等生命过程的精细调控[19-27]。 成骨谱系细胞对造血干细胞的静息和活化状态具有调控作用。SUGIMURA等[28]的研究表明,成骨细胞缺陷小鼠的造血功能受到抑制,而异位骨小体可通过机械/化学因素在体外维持造血干细胞的干性与活性。在体外培养中发现,成骨细胞可通过与造血干细胞黏附增强其自我更新能力。因此,研究人员揭示N-钙黏蛋白阳性的成骨前体细胞与静息状态下的造血干细胞间存在受体-配体接触,发现这些排列在骨内膜表面的细胞可通过骨形态发生蛋白信号通路和非经典的Wnt信号通路支持造血干细胞并调控其状态和功能,而在体内清除N-钙黏蛋白阳性的成骨细胞会使得造血干细胞的增殖与造血谱系分化功能发生不可逆变化[29-30]。而甲状旁腺激素可通过激活成骨细胞表面Notch受体水平,与造血干细胞表面相应的Jagged-1配体相结合,刺激造血干细胞的增殖与扩增。与此同时,研究发现如趋化因子配体12、干细胞因子、血管生成素1、白细胞介素7和血管细胞黏附分子 1在巢蛋白阴性的间充质干细胞中富集,而这些早期巢蛋白阴性、瘦素受体阴性的间充质干细胞分泌的趋化因子配体12是维持造血干细胞的关键因素。 除此之外,成骨谱系细胞亦可以通过旁分泌/内分泌途径,通过合成如血小板生成素[31]、血管生成素1和骨桥蛋白等细胞因子[32],与造血干细胞表面酪氨酸激酶受体Tie2/β-1 integrin 等受体结合通过增强造血干细胞与骨髓微环境的相互识别与作用,使其在“骨髓壁龛”中保持静止和自我增殖。同时,有研究表明偏早期的成骨谱系间充质干细胞可以通过分泌含Jagged-1的外泌体,作用于造血干细胞表面的Notch受体,从而增强其增殖能力[33-35]。而YU等[36]发现,表达瘦素受体的成骨谱系骨髓基质细胞可通过分泌内皮细胞衍生的血管生成素样蛋白2增强造血干细胞在“骨髓壁龛”中的活性。 2.1.3 血液细胞对骨相关细胞的反馈调节机制 造血干细胞在分化过程中,对其周围的骨髓微环境存在调控作用。如前所述,骨髓微环境主要由细胞与细胞外基质共同组成,而细胞外基质的主要提供者正是骨相关细胞,如成骨谱系的间充质干细胞、成骨细胞、骨细胞、破骨细胞等。鉴于破骨细胞正是起源于造血干细胞的融合多核巨细胞,其向破骨细胞的分化是容易理解的。而前人研究表明,那些接受造血干细胞移植的患者在术后早期12个月会出现快速骨量丢失,这可能与造血干细胞的功能多样性修复有着密切联系[37]。但是,目前针对造血干细胞对间充质干细胞及成骨谱系细胞的研究仍匮乏,有待进一步开展。 除造血干细胞外,多种其分化产生的细胞(如巨噬细胞、淋巴细胞、白血病细胞等)对骨相关细胞的作用已得到大量研究证实。在生理状态下,巨噬细胞通过分泌转化生长因子β1抑制成骨细胞分化[38],而由辅助性T淋巴细胞17分泌而来的白细胞介素17通过激活核因子κB受体活化因子配体信号促进破骨细胞生成[39]。在骨折等病理状态下,骨髓微环境发生炎症反应,刺激巨噬细胞极化为M1型(炎症型)和M2型(修复性)[40]。炎症早期,M1型巨噬细胞的外泌体通过microRNA-21A-5P促进骨髓间充质干细胞成骨分化[41];M2型巨噬细胞则通过分泌microRNA-5106直接靶向骨髓间充质干细胞中的盐诱导激酶2,3[42],抑制其功能并促成骨分化[43]。另有研究表明,M2型巨噬细胞的细胞外囊泡中携带的microRNA-22-3p可通过抑制周期昼夜节律蛋白2,解除对Wnt/β-连环蛋白信号通路的抑制作用,进而促进骨髓间充质干细胞成骨分化[44]。在其他病理状态下,如白血病细胞通过异常表达破骨细胞分化因子直接激活破骨细胞,导致病理性骨吸收[45];同时其分泌的肿瘤坏死因子α和白细胞介素6等炎症因子抑制成骨细胞活性。在骨髓增生异常综合征中,造血细胞衍生的外泌体携带脂代谢酶CPT-1A,被间充质干细胞摄取后抑制其成骨分化能力[46]。此外,衰老造血干细胞出现胆碱代谢紊乱会改变细胞膜流动性,通过减弱基质细胞衍生因子信号传导进一步破坏骨重塑平衡[47]。 2.2 骨骼-血液系统失稳态在疾病中的作用研究 众多的临床发现也提示了二者的共病性,在一项针对范可尼贫血患者的长期预后观察中,发现有51%的患者出现了骨密度的降低[48]。此外还有众多的临床研究报道,地中海贫血患者中骨折发生率很高[49]。在多发性骨髓瘤中常见溶骨性病变和骨折,这主要是由于成骨细胞减少和破骨细胞活性增加而无法愈合,但浆细胞与骨相关细胞的对话目前仍不十分清楚[50]。在骨髓增生性疾病中,其中真性红细胞增多症和原发性血小板增多症患者中,少部分提示骨质流失可导致骨质疏松性骨折。原发性骨髓纤维化的患者骨量通常增加,这种异常的成骨细胞增殖和分化导致的骨硬化,最终会导致骨髓衰竭[51]。上述临床上的报道揭示了骨代谢紊乱和血液系统紊乱二者之间的紧密联系。 多种血液疾病伴随骨-血对话失调,目前主流的观点是以代谢失衡来揭示二者间的联系。以白血病为例,其中“瓦博格效应”导致糖酵解亢进引起的乳酸堆积(局部pH 6.5-6.8),乳酸一方面直接激活破骨细胞活化 T 细胞核因子 1通路以促进骨吸收,另一方面抑制成骨细胞中Runt相关转录因子2表达,从而阻碍骨形成[52]。乳酸在微环境中堆积通过缺氧诱导因子1亚基α/C-X-C基序趋化因子受体4轴进一步增强白血病细胞的化疗抵抗能力[53]。异柠檬酸脱氢酶突变型急性髓系白血病细胞产生2-羟基戊二酸可抑制十-十一碳双加氧酶2活性,进而重编程间充质干细胞,削弱其成骨分化能力并促进促炎因子白细胞介素6等高表达[54]。白细胞介素6则通过激活信号传导及转录激活蛋白3/硬化蛋白轴拮抗Wnt通路,进一步抑制骨形成[55]。此外白血病细胞分泌的肿瘤坏死因子α通过激活肿瘤坏死因子受体相关因子6/核因子κB受体激活蛋白通路刺激破骨细胞活性,扩大骨吸收陷窝并破坏骨结构。 近年来,为进一步研究骨骼-血液系统失稳态在疾病中的作用,如单细胞转录测序、空间转录组/多组学等新技术和新方法逐渐应用于这一领域。为分析比较各项新技术新方法,归纳总结其优势和局限性见表2[56-65]。 2.3 骨-血轴中的核心信号通路 骨-血轴是维持骨稳态与正常造血功能的核心枢纽,其双向调控不仅依赖于细胞间的直接接触与旁分泌作用,还涉及多条信号通路构成的复杂交叉对话网络。下文将详细归纳阐述Wnt/β-连环蛋白、Notch、核因子κB受体活化因子/核因子κB受体活化因子配体/骨保护素、Hippo-Yes相关蛋白等核心通路。 2.3.1 Wnt/β-连环蛋白通路的枢纽作用与双向调节 Wnt/β-连环蛋白通路在骨-血轴中扮演核心枢纽角色,其双向调节能力体现在“骨→"
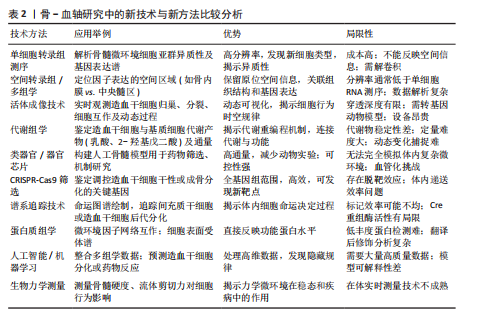
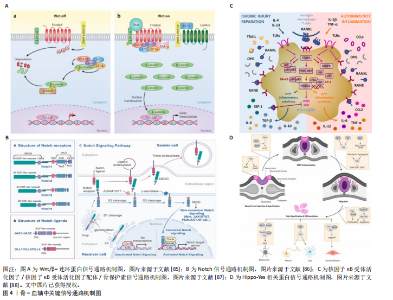
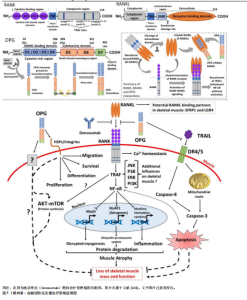
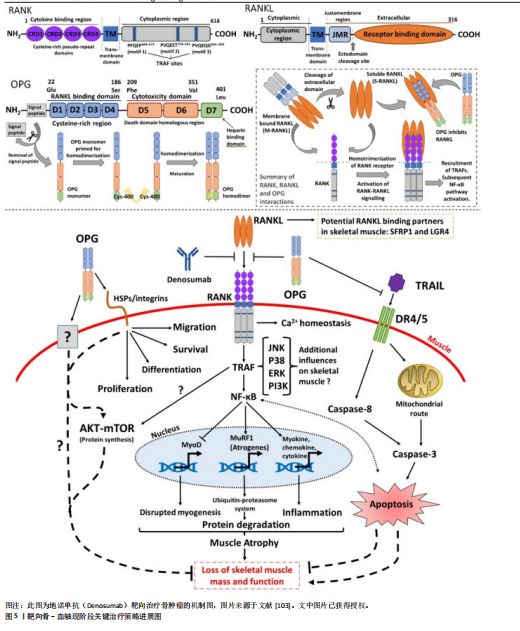
血”的支撑作用和“血→骨”的反馈机制中。 “骨→血”方面,成骨细胞谱系细胞的Wnt信号激活是骨形成的关键驱动力。β-连环蛋白在成骨前体细胞中累积并入核,与TCF/LEF转录因子家族结合,直接启动成骨转录因子Osterix、骨钙素等特异性基因的转录。更重要的是,活化的Wnt信号同时上调成骨细胞和骨基质细胞中趋化因子配体12的表达。趋化因子配体12与造血干细胞表面的受体趋化因子受体4结合,将造血干细胞锚定于骨内膜生态位,并通过下调细胞周期蛋白p21,来维持其静息状态与自我更新能力[66]。在衰老的间充质干细胞中Wnt通路抑制因子Dickkopf相关蛋白1的启动子区域呈现去甲基化状态,导致Dickkopf相关蛋白1持续高表达,进而抑制Wnt信号,削弱其成骨和造血支持的能力[67]。 在“血→骨”方向,造血系统来源的细胞通过分泌因子对Wnt通路进行精细的反向调控。活化的T淋巴细胞、巨噬细胞等免疫细胞在炎症状态下释放的肿瘤坏死因子α、白细胞介素1β及白细胞介素6等因子,可通过激活核因子κB信号通路诱导骨细胞和成骨细胞高表达硬化蛋白。硬化蛋白作为Wnt通路的经典拮抗剂,可与Wnt受体复合物中的低密度脂蛋白受体相关蛋白5/6结合,促进其内吞和降解,从而有效抑制Wnt信号传导,最终阻碍成骨细胞分化和骨形成过程[68]。这一负反馈环路在类风湿关节炎等炎症性骨病和年龄相关性骨质疏松的病理过程中被显著增强[69]。此外,最新单细胞转录组研究发现,骨髓中性粒细胞亚群(特别是TREM1+CD10+群体)可通过分泌Dickkopf相关蛋白1抑制Wnt通路,在抑制成骨的同时削弱CD8+ T细胞的抗肿瘤功能,从而在骨髓瘤等骨病中形成“免疫-骨代谢”双重抑制微环境Wnt通路与其他信号通路也存在着复杂的交叉对话。研究表明,骨形态发生蛋白9可通过激活Smad1/5/8信号上调多种Wnt配体的表达,其中Wnt通路中核心元件β-连环蛋白在细胞核内积累后又能反过来增强骨形态发生蛋白受体的转录,从而形成一个促进成骨过程的正反馈循环[70]。这种通路间的互作不仅放大了促成骨信号,也为靶向治疗提供了新的节点。但在急性髓系白血病等病理状态下,这一正反馈循环常被破坏[71]。白血病细胞不仅通过分泌Dickkopf相关蛋白1等Wnt抑制剂抑制成骨细胞分化,还经常利用自身Wnt信号的异常激活来维持其增殖优势[72]。因此,靶向Wnt通路可有效增加骨量和改善造血功能。现临床前研究已发现应用抗骨硬化蛋白抗体具有此双重效益,展现出Wnt通路在骨-血轴治疗策略中的核心潜力。 2.3.2 Notch通路的细胞命运决定作用 Notch信号通路作为高度保守的细胞间通讯机制,通过细胞间接触依赖方式,在骨髓微环境中精确调控多种细胞的命运决定,包括造血干细胞的自我更新、谱系分化及间充质干细胞的成骨与成脂平衡。研究表明,Notch信号通路则直接参与调控破骨细胞前体细胞的分化命运。破骨细胞前体细胞上的Notch受体被其配体(如Jagged1)激活后,可诱导下游靶基因Hes1的表达,进而抑制骨细胞活化 T 细胞核因子 1的活性,实现对破骨细胞生成的负向调控[73]。此外Notch通路则通过与成骨细胞表达的Jagged-1配体相结合直接,直接参与造血干细命运的调控。 骨系细胞(成骨细胞和骨细胞)表达的Notch配体δ样蛋白1/δ样蛋白4可与造血干细胞表面Notch受体结合后,将触发γ-分泌酶介导的蛋白水解切割,释放Notch胞内结构域。Notch胞内结构域转移至细胞核内,与转录因子CSL结合,激活Hes1、Hey等下游靶基因的表达,从而促进造血干细胞的自我更新[74]。应激条件下,骨髓微环境中的δ样蛋白1/δ样蛋白4表达会下调,使得造血干细胞过早分化及造血再生障碍。Notch与Wnt通路之间存在复杂交叉对话[75]。Notch胞内结构域可诱导Hes1表达抑制Wnt靶基因(如Cyclin D1、Axin2等)的转录,从而拮抗 Wnt/β-连环蛋白通路促进的细胞周期进程和分化;然而,在成骨分化过程中,间充质干细胞中的Notch表现出相反的作用,Notch激活后通过Jagged1增强Wnt响应,促进成骨特异性基因(如Runx2、Osterix等)的表达和基质矿化[76]。这种双向调控网络确保了骨髓中骨形成与造血维持的精细平衡。 在年龄相关的骨质疏松症中,衰老相关的Notch信号衰减将导致间充质干细胞成骨分化能力下降,造血干细胞支持能力减弱[77]。这种衰减与间充质干细胞的成骨分化能力下降和脂肪堆积密切相关。机制上,衰老相关的炎症微环境(如肿瘤坏死因子α、白细胞介素6水平升高)通过核因子κB信号抑制Notch配体的转录;同时,间充质干细胞中沉默信息调节因子2同源蛋白1表达随年龄升高而下降,导致Notch胞内结构域的乙酰化水平升高及其蛋白质稳定性降低。Notch信号的减弱不仅损害了骨形成,也削弱了成骨细胞对造血干细胞生态位的支持功能,表现为趋化因子配体12和干细胞因子等关键因子分泌减少,最终导致造血干细胞功能减退和髓系分化偏斜。 2.3.3 核因子κB受体活化因子/核因子κB受体活化因子配体/骨保护素轴的免疫-骨代谢桥梁 破骨细胞分化和活化主要由核因子κB受体活化因子配体介导,该因子由成骨细胞和淋巴细胞等多种细胞分泌,通过与破骨细胞前体表面的核因子κB受体活化因子受体结合,激活核因子κB和骨细胞活化 T 细胞核因子1信号通路,从而驱动破骨细胞生成。同时,由成骨细胞和间充质干细胞分泌的骨保护素作为诱骗受体可竞争性结合核因子κB受体活化因子配体,有效抑制破骨细胞的生成和功能。免疫细胞在这一调控网络中至关重要。活化的T淋巴细胞,尤其是辅助性T淋巴细胞17亚群,通过分泌白细胞介素17显著上调核因子κB受体活化因子配体表达,并促进肿瘤坏死因子α、白细胞介素1β等促破骨因子的释放,从而驱动炎症性骨流失[78],破骨细胞调控系统与造血功能之间存在密切的双向交互。有研究表明骨保护素缺失小鼠表现为造血干细胞生态位扩张和髓系偏斜分化,而核因子κB受体活化因子配体除了抑制破骨细胞生成外,也可反向调控造血[79]。 2.3.4 Hippo-Yes相关蛋白通路的机械感应与代谢调控 Hippo-Yes相关蛋白通路作为机械应力感受器,在骨-血轴中发挥独特作用。生理状态下,成骨细胞和骨细胞通过感应流体剪切力等力学刺激,激活Yes相关蛋白/TAZ转录共激活因子,继而调控结缔组织生长因子、富半胱氨酸蛋白61等靶基因的表达以促进骨形成[80]。研究发现,溶血磷脂酸通过G蛋白偶联受体溶血磷酸酯1抑制大肿瘤抑制激酶,促进Yes相关蛋白发生去磷酸化并核转位,从而激活Rho-Rho相关蛋白激酶信号轴,驱动成骨前体细胞迁移和分化[81]。在造血支持方面,Yes相关蛋白的激活可上调趋化因子配体12和干细胞因子等关键因子的表达,增强骨髓微环境对造血干细胞生态位支持功能[82]。值得注意的是,该通路与Wnt/β-连环蛋白通路存在显著交叉对话,激活的Yes相关蛋白可结合lial并阻止其降解,协同促进成骨基因转录[83]。病理状态下,如骨髓纤维化,力学微环境紊乱将导致Yes相关蛋白信号持续激活,反而诱导间充质干细胞向纤维化方向转分化,最终破坏造血干细胞的稳态[84]。 图4及表3归纳了各通路的核心组件、在“骨→血”与“血→骨”双向调控中的具体功能、相关疾病及其代表性研究,为理解多通路协同调控提供参考。 2.4 靶向骨-血轴的转化医学前景分析 当前治疗策略已呈现出从单一疗法向协同干预发展的趋势。多发性骨髓瘤细胞通过异常表达核因子κB受体活化因子配体激活破骨细胞,导致溶骨性病变和骨髓腔扩大,为肿瘤细胞增殖提供空间和营养支持;同时破骨细胞分泌的白细胞介素6和肿瘤坏死因子α进一步支持肿瘤生长,形成“肿瘤生长-骨破坏”的恶性循环。全人源化核因子κB受体活化因子配体抑制剂地诺单抗(Denosumab)通过高亲和力结合并中和核因子κB受体活化因子配体,阻断其与破骨细胞前体表面核因子κB受体活化因子受体的结合。该药物不仅显著提高了绝经后骨质疏松患者的骨密度,还通过抑制病理性骨吸收,减少实体瘤骨转移及多发性骨髓瘤患者骨骼相关事件的发生,并间接削弱了肿瘤在骨髓微环境中的生存支持,展现出“骨-血共治”的临床价值[100]。 在代谢干预层面,针对IDH2突变型急性髓系白血病研发的靶向药恩西地平(Enasidenib),通过特异性抑制突变型IDH2酶的活性,降低致癌代谢物2-羟基戊二酸在骨髓中的水平,从而解除2-羟基戊二酸对成骨细胞分化过程中关键表观遗传调控酶的抑制,间接恢复骨髓微环境的成骨功能[101]。此外,针对肿瘤代谢引发的微环境酸化,乳酸转运蛋白MCT1的抑制剂AZD3965在临床前模型中有效阻断了肿瘤细胞与基质细胞间的“乳酸穿梭”,逆转了肿瘤微环境的低pH值状态,这不仅直接抑制了依赖于糖酵解的肿瘤细胞生长,还有助于改善成骨细胞的功能状态,并可能增强化疗药物的疗效[102-103]。见图5。"
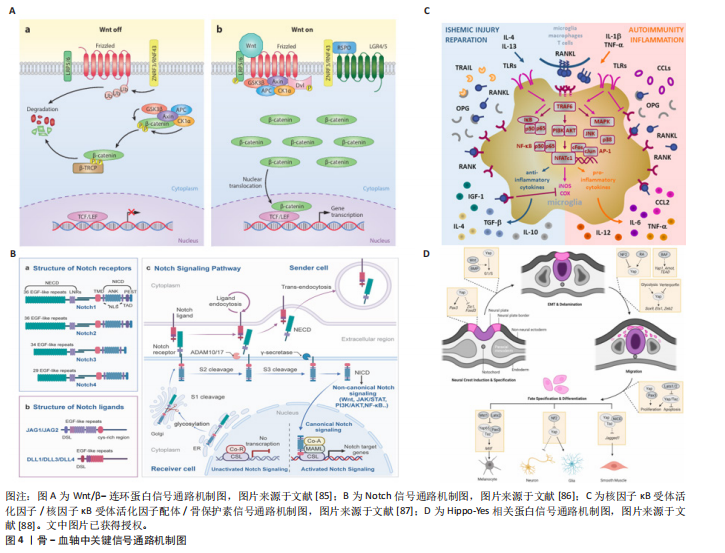
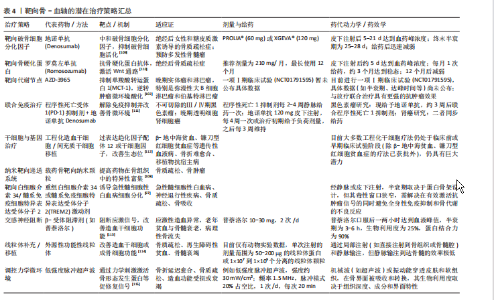
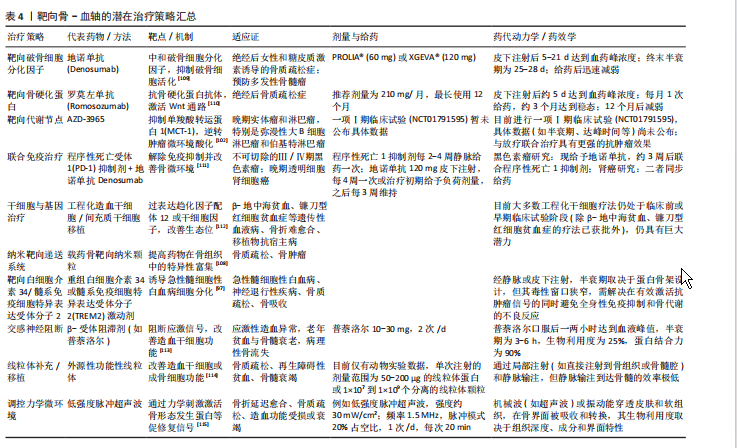
此外靶向Notch通路治疗骨髓增生异常综合征等骨相关疾病的方案(γ-分泌酶抑制剂)现被应用于治疗骨髓增生异常综合征的实验室研究[104],它可通过抑制过度活化的Notch信号,逆转间充质干细胞的成骨分化阻滞并改善造血功能,表现出巨大潜力。但因为Notch通路在人体内各种组织中广泛作用,未来需关注Notch的组织特异性靶向策略以避免全身性副作用。 近年来中国团队在骨-血轴转化研究中也取得了重要进展。北京大学周永胜教授团队在2022年已发现人脂肪间充质干细胞来源外泌体可促进骨质疏松小鼠骨髓间充质干细胞的成骨分化,于2025年发现其在体外可促进小鼠骨髓间充质干细胞成骨分化,在体内可有效预防去势小鼠骨质疏松症的发生,揭示了脂肪间充质干细胞外泌体治疗骨质疏松的机制[105]。张曦教授团队于2025年在《Journal of Clinical Oncology》的研究纳入半相合造血干细胞移植患者192例,2年内间充质干细胞组慢性移植物抗宿主病累计发病率为5.5%,对照组为14.8%(P=0.033),间充质干细胞组显著低于对照组;急性移植物抗宿主病的累计发病率对照组为47.9%,而间充质干细胞组为17.7% (P < 0.001),显著低于对照组[106],这证实了间充质干细胞可有效预防急性和慢性移植物抗宿主病。四川大学团队开发了源自骨髓基质细胞的仿生纳米囊泡可以穿过骨髓-血液屏障,能有效递送骨质疏松药物特立帕肽和抗癌药阿霉素以抑制乳腺癌骨转移和骨溶解病变[107]。浙江大学团队开发了基于中性粒细胞的药物递送平台,利用衰老中性粒细胞会自发返回骨髓凋亡的自然生命周期,使得载药纳米颗粒能够进入骨髓,靶向治疗骨质疏松和骨转移癌[108]。 但目前多数靶向骨-血轴的策略仍处于早期研发阶段,未来的临床试验应设立“骨密度+造血重建”双终点,并关注药代动力学/药效学参数如骨组织分布、代谢物清除率、免疫细胞亚群变化等。在联合治疗时也应需注意用药顺序,如先改善骨髓微环境再行免疫治疗,可提升疗效。 随着对骨-血轴调控机制的深入解析,技术方法的革新与多模态治疗策略的开发已成为核心驱动力。为系统梳理并比较关键新技术的发展进程、应用场景及治疗策略的进展,此文对靶向骨-血轴的潜在治疗策略进行了汇总(表4),希望为未来骨-血轴靶向研究与多模态联合治疗提供系统性参考。"
| [1] 赵国峰,宋克东,刘天庆,等.低氧条件下微囊化成骨细胞调控造血干/祖细胞扩增的研究[J].高校化学工程学报,2009, 23(4):623-631. [2] LlESVELD JL. Trouble in the niche? Send in astatin. Blood. 2016;128(25):2877-2878. [3] 张灵莉,刘晓倩,黄晓芹.成骨细胞对造血的调控及传统药物在该调控中的作用研究进展[J].中药与临床,2018,9(3):64-66+63. [4] LIU H, HE J, BAGHERI-YARMAND R, et al. Osteocyte CIITA aggravates osteolytic bone lesions in myeloma. Nat Commun. 2022; 13(1):3684. [5] BOSCH-FORTEA M, MARCIANO D, GAUTROT JE. Biomimetic artificial bone marrow niches for the scale up of hematopoietic stem and progenitor cells. Biomaterials. 2026;325:123612. [6] BAUER M, VAXEVANIS C, JAEKEL N, et al. Association of the composition of the bone marrow tumor microenvironment in BCR: ABL1-negative myeloproliferative neoplasms with IFN-γ signaling and driver mutations. Leukemia. 2025;39(10): 2391-2405. [7] DU L, FREITAS-CORTEZ MA, ZHANG J, et al. Periarteriolar niches become inflamed in aging bone marrow, remodeling the stromal microenvironment and depleting lymphoid progenitors. Proc Natl Acad Sci U S A. 2025; 122(11):e2412317122. [8] TIKHONOVA AN, DOLGALEV I, HU H, et al. The bone marrow microenvironment at single-cell resolution. Nature. 2019;569(7755): 222-228. [9] FU J, WANG Y, JIANG Y, et al. Systemic therapy of MSCs in bone regeneration: a systematic review and meta-analysis. Stem Cell Res Ther. 2021;12(1):377. [10] MUÑOZ J, AKHAVAN NS, MULLINS AP, et al. Macrophage Polarization and Osteoporosis: A Review. Nutrients. 2020;12(10):2999. [11] MARAHLEH A, KITAURA H, OHORI F, et al. The osteocyte and its osteoclastogenic potential. Front Endocrinol (Lausanne). 2023; 14:1121727. [12] LEE C, KIM MJ, KUMAR A, et al. Vascular endothelial growth factor signaling in health and disease: from molecular mechanisms to therapeutic perspectives. Signal Transduct Target Ther. 2025;10(1):170. [13] KARNIK SJ, NAZZAL MK, KACENA MA, et al. Megakaryocyte Secreted Factors Regulate Bone Marrow Niche Cells During Skeletal Homeostasis, Aging, and Disease. Calcif Tissue Int. 2023;113(1):83-95. [14] GACEB A, BARBARIGA M, ÖZEN I, et al. The pericyte secretome: Potential impact on regeneration. Biochimie. 2018;155:16-25. [15] NICHOLLS AJ, WEN SW, HALL P, et al. Activation of the sympathetic nervous system modulates neutrophil function. J Leukoc Biol. 2018;103(2):295-309. [16] PEARSE DD, MARCILLO AE, OUDEGA M, et al. Transplantation of Schwann cells and olfactory ensheathing glia after spinal cord injury: does pretreatment with methylprednisolone and interleukin-10 enhance recovery? J Neurotrauma. 2004;21(9):1223-1239. [17] DONG R, LING Z, FAN P, et al. A Novel Therapeutic Strategy for Bone Marrow Failure: Niche Rejuvenation Using Costal Cartilage-Derived Stem Cells. Adv Sci (Weinh). Published online August 27, 2025. [18] LIANG W, WEI T, HU L, et al. An integrated multi-omics analysis reveals osteokines involved in global regulation. Cell Metab. 2024; 36(5):1144-1163.e7. [19] FRÖBEL J, LANDSPERSKY T, PERCIN G, et al. The Hematopoietic Bone Marrow Niche Ecosystem. Front Cell Dev Biol. 2021;9:705410. [20] KANDARAKOV O, BELYAVSKY A, SEMENOVA E. Bone Marrow Niches of Hematopoietic Stem and Progenitor Cells. Int J Mol Sci. 2022; 23(8):4462. [21] LI D, XUE W, LI M, et al. VCAM-1+ macrophages guide the homing of HSPCs to a vascular niche. Nature. 2018;564(7734):119-124. [22] GHAFOURI-FARD S, GLASSY MC, ABAK A, et al. The interaction between miRNAs/lncRNAs and Notch pathway in human disorders. Biomed Pharmacother. 2021;138:111496. [23] BRUNS I, LUCAS D, PINHO S, et al. Megakaryocytes regulate hematopoietic stem cell quiescence through CXCL4 secretion. Nat Med. 2014;20(11):1315-1320. [24] ZHAN H, KAUSHANSKY K. Megakaryocytes as the Regulator of the Hematopoietic Vascular Niche. Front Oncol. 2022;12:912060. [25] TSIRKINIDIS P, TERPOS E, BOUTSIKAS G, et al. Bone metabolism markers and angiogenic cytokines as regulators of human hematopoietic stem cell mobilization. J Bone Miner Metab. 2018;36(4):399-409. [26] BISWAS L, CHEN J, DE ANGELIS J, et al. Lymphatic vessels in bone support regeneration after injury. Cell. 2023;186(2):382-397.e24. [27] RAMASAMY SK, KUSUMBE AP, WANG L, et al. Endothelial Notch activity promotes angiogenesis and osteogenesis in bone. Nature. 2014;507(7492):376-380. [28] SUGIMURA R, HE XC, VENKATRAMAN A, et al. Noncanonical Wnt signaling maintains hematopoietic stem cells in the niche. Cell. 2012;150(2):351-365. [29] ZHAO M, PERRY JM, MARSHALL H, et al. Megakaryocytes maintain homeostatic quiescence and promote post-injury regeneration of hematopoietic stem cells. Nat Med. 2014;20(11):1321-1326. [30] ZHAO M, TAO F, VENKATRAMAN A, et al. N-Cadherin-Expressing Bone and Marrow Stromal Progenitor Cells Maintain Reserve Hematopoietic Stem Cells. Cell Rep. 2019; 26(3):652-669.e6. [31] KAJIUME T, KAWAHARA Y, YUGE L, et al. Osteoblastic adherence regulates hematopoietic stem cell self-renewal and differentiation: a conceptional in vitro and in vivo study. Stem Cell Investig. 2021;8:21. [32] LEE S, ZHAN H. Deciphering the differential impact of thrombopoietin/MPL signaling on hematopoietic stem/progenitor cell function in bone marrow and spleen. Stem Cell Reports. 2024;19(2):211-223. [33] HIMBURG HA, TERMINI CM, SCHLUSSEL L, et al. Distinct Bone Marrow Sources of Pleiotrophin Control Hematopoietic Stem Cell Maintenance and Regeneration. Cell Stem Cell. 2018;23(3):370-381.e5. [34] NIAZI V, GHAFOURI-FARD S, VERDI J, et al. Hypoxia preconditioned mesenchymal stem cell-derived exosomes induce ex vivo expansion of umbilical cord blood hematopoietic stem cells CD133+ by stimulation of Notch signaling pathway. Biotechnol Prog. 2022;38(1):e3222. [35] GILCHRIST AE, HARLEY BAC. Connecting secretome to hematopoietic stem cell phenotype shifts in an engineered bone marrow niche. Integr Biol (Camb). 2020;12(7): 175-187. [36] YU Z, YANG W, HE X, et al. Endothelial cell-derived angiopoietin-like protein 2 supports hematopoietic stem cell activities in bone marrow niches. Blood. 2022;139(10):1529-1540. [37] LIM Y, BAEK KH, KIM HJ, et al. Changes in trabecular bone score and bone mineral density following allogeneic hematopoietic stem cell transplantation. Bone. 2019;124: 40-46. [38] CANTONE AF, BURGALETTO C, DI BENEDETTO G, et al. Rebalancing Immune Interactions within the Brain-Spleen Axis Mitigates Neuroinflammation in an Aging Mouse Model of Alzheimer’s Disease. J Neuroimmune Pharmacol. 2025;20(1):15. [39] HETTIARACHCHI SU, LI YH, ROY J, et al. Targeted inhibition of PI3 kinase/mTOR specifically in fibrotic lung fibroblasts suppresses pulmonary fibrosis in experimental models. Sci Transl Med. 2020;12(567):eaay3724. [40] PÉPIN CM, ANDRÉ R, OCCELLI F, et al. Metastable water at several compression rates and its freezing kinetics into ice VII. Nat Commun. 2024;15(1):8239. [41] 石琰,郭昊,郑凯娟,等.免疫细胞对骨髓间充质干细胞成骨分化作用及机制的研究进展[J].口腔颌面外科杂志,2024,34(2):150-153. [42] XIONG Y, CHEN L, YAN C, et al. Retraction Note: M2 macrophagy-derived exosomal miRNA-5106 induces bone mesenchymal stem cells towards osteoblastic fate by targeting salt-inducible kinase 2 and 3. J Nanobiotechnology. 2024;22(1):238. [43] LIU K, LUO X, LV ZY, et al. Macrophage-Derived Exosomes Promote Bone Mesenchymal Stem Cells Towards Osteoblastic Fate Through microRNA-21a-5p. Front Bioeng Biotechnol. 2022;9:801432. [44] 徐枭喻,廖礼彬,张馨怡,等.剪切应力通过M2型巨噬细胞外泌体miR-5106促进骨髓间充质干细胞向成骨细胞分化[J].中国组织化学与细胞化学杂志,2024,33(3):209-216. [45] NIKLASON LE, LAWSON JH. Bioengineered human blood vessels. Science. 2020; 370(6513):eaaw8682. [46] RICHOZ N, TUONG ZK, LOUDON KW, et al. Distinct pathogenic roles for resident and monocyte-derived macrophages in lupus nephritis. JCI Insight. 2022;7(21):e159751. [47] YUAN W, LIU M, YANG D, et al. Improvement in long-term survival with mesenchymal stem cell transplantation in systemic sclerosis patients: a propensity score-matched cohort study. Stem Cell Res Ther. 2025;16(1):128. [48] WANG YM, LOVELESS M, MILLER E, et al. Phenotypes of adults with Fanconi anaemia. Br J Haematol. 2023;201(1):133-139. [49] CHAROENNGAM N, RITTIPHAIROJ T, PONVILAWAN B. Fracture prevalence in thalassemia: a systematic review and meta-analysis. Arch Osteoporos. 2021;16(1):171. [50] REAGAN MR, LIAW L, ROSEN CJ, et al. Dynamic interplay between bone and multiple myeloma: emerging roles of the osteoblast. Bone. 2015;75:161-169. [51] KARAGIANNI A, RAVID K. Myeloproliferative disorders and their effects on bone homeostasis: the role of megakaryocytes. Blood. 2022;139(21):3127-3137. [52] LALIOTI ME, ROMERO-MULERO MC, KARABACZ N, et al. Differentiation, ageing and leukaemia alter the metabolic profile of human bone marrow haematopoietic stem and progenitor cells. Nat Cell Biol. 2025; 27(8):1367-1380. [53] WILLYANTO SE, ALIMSJAH YA, TANJAYA K, et al. Comprehensive analysis of the efficacy and safety of CAR T-cell therapy in patients with relapsed or refractory B-cell acute lymphoblastic leukaemia: a systematic review and meta-analysis. Ann Med. 2024; 56(1):2349796. [54] RETTKOWSKI J, ROMERO-MULERO MC, SINGH I, et al. Modulation of bone marrow haematopoietic stem cell activity as a therapeutic strategy after myocardial infarction: a preclinical study. Nat Cell Biol. 2025;27(4):591-604. [55] LI H, BAI L. Advances in mesenchymal stem cell and exosome-based therapies for aging and age-related diseases. Stem Cell Res Ther. 2025;16(1):401. [56] KIM J, BIXEL MG. Intravital Multiphoton Imaging of the Bone and Bone Marrow Environment. Cytometry A. 2020;97(5):496-503. [57] ALHARITHI YJ, PHILLIPS EA, WILSON TD, et al. Metabolomic and transcriptomic remodeling of bone marrow myeloid cells in response to maternal obesity. Am J Physiol Endocrinol Metab. 2025;328(2):E254-E271. [58] FRENZ-WIESSNER S, FAIRLEY SD, BUSER M, et al. Generation of complex bone marrow organoids from human induced pluripotent stem cells. Nat Methods. 2024;21(5):868-881. [59] AJORE R, MATTSSON J, PERTESI M, et al. Genome-wide CRISPR/Cas9 screen identifies regulators of BCMA expression on multiple myeloma cells. Blood Cancer J. 2024;14(1):21. [60] WENG C, YU F, YANG D, et al. Deciphering cell states and genealogies of human haematopoiesis. Nature. 2024;627(8003): 389-398. [61] KRAMER MH, ZHANG Q, SPRUNG R, et al. Proteomic and phosphoproteomic landscapes of acute myeloid leukemia. Blood. 2022;140(13):1533-1548. [62] 肖宇俊,张燕,杨建民,等. 基于人工智能深度学习的骨髓细胞形态学检测的研究进展[J]. 中华生物医学工程杂志,2023, 29(4):457-461. [63] JANSSEN E, VAN DEN DRIES K, VENTRE M, et al. Mechanobiology of myeloid cells. Curr Opin Cell Biol. 2024;86:102311. [64] ZHANG D, DUQUE-JIMENEZ J, FACCHINETTI F, et al. Transferrin receptor targeting chimeras for membrane protein degradation. Nature. 2025;638(8051):787-795. [65] HOFMAN MS, EMMETT L, SANDHU S, et al. Overall survival with [177Lu]Lu-PSMA-617 versus cabazitaxel in metastatic castration-resistant prostate cancer (TheraP): secondary outcomes of a randomised, open-label, phase 2 trial. Lancet Oncol. 2024;25(1):99-107. [66] NA J, YANG Z, SHI Q, et al. Extracellular matrix stiffness as an energy metabolism regulator drives osteogenic differentiation in mesenchymal stem cells. Bioact Mater. 2024;35:549-563. [67] LUO HH, REN WY, YE AH, et al. DDIT3 switches osteogenic potential of BMP9 to lipogenic by attenuating Wnt/β-catenin signaling via up-regulating DKK1 in mesenchymal stem cells. Aging (Albany NY). 2024;16(18):12543-12558. [68] WANG J, XIE W, LI N, et al. Generation of a humanized mesonephros in pigs from induced pluripotent stem cells via embryo complementation. Cell Stem Cell. 2023;30(9): 1235-1245.e6. [69] FAZIO A, DI MARTINO A, BRUNELLO M, et al. The involvement of signaling pathways in the pathogenesis of osteoarthritis: An update. J Orthop Translat. 2024;47:116-124. [70] YAO XT, LI PP, LIU J, et al. Wnt/β-Catenin Promotes the Osteoblastic Potential of BMP9 Through Down-Regulating Cyp26b1 in Mesenchymal Stem Cells. Tissue Eng Regen Med. 2023;20(5):705-723. [71] ZOLGHADR F, SADEGHIZADEH M, AMIRIZADEH N, et al. How benzene and its metabolites affect human marrow derived mesenchymal stem cells. Toxicol Lett. 2012; 214(2):145-153. [72] GUO Z, XU Q, ZHANG K, et al. Sclerostin: A Potential Link between Osteoporosis and Alzheimer’s Disease. Neurodegener Dis. 2025;23:1-9. [73] CHEN Y, LIU Z, ZOU J, et al. Low-dose tyrosine kinase inhibitors in patients with chronic myeloid leukemia: a retrospective study in China. Haematologica. 2022;107(8):1966-1970. |
| [1] | Fan Tingting, Xiang Miaomiao, Yuan Xiaoshuang, Yang Xu, Yang Bo, Tian Ting, Chen Xiaoxu, Tang Dongxin, Wang Feiqing, Liu Yang, Li Yanju. Senescent bone marrow mesenchymal stem cells promote multiple myeloma cell proliferation through galectins-3 [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(19): 4836-4842. |
| [2] | Zhang Shilei, Qin Chuanhong, Wang Jianxu, Sun Shui. Osteogenic-adipogenic differentiation imbalance of bone marrow mesenchymal stem cells and osteonecrosis of the femoral head: from molecular mechanisms to therapeutic strategies [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(13): 3350-3358. |
| [3] | Yu Manya, Cui Xing. Contribution and interaction of various cells in bone marrow microenvironment to exosomal circular RNA associated with multiple myeloma bone disease [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(1): 101-110. |
| [4] |
Gao Kunli, Xing Hongyun, Bian Tierong, Han Liying.
Transplantation of human umbilical cord blood mesenchymal stem cells in the repair of hematopoietic injury in bone marrow [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(25): 3966-3972. |
| [5] | Liu Yang, Zheng Yuanyuan, Chen Yizhu, Zhao Jing, Li Jianyou, Wu Mingyuan, Sun Quan. Clinical progress in the treatment of non-hematopoietic diseases by human umbilical cord blood cell transplantation [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(25): 4094-4100. |
| [6] | Xu Ruohao, Li Chao, Wu Ping, Li Minming, Deng Chengxin, Geng Suxia, Lai Peilong, Lu Zesheng, Weng Jianyu, Du Xin. Bone marrow colony forming units-fibroblast in patients with chronic myelomonocytic leukemia: functions and clinical significance [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(21): 3398-3403. |
| [7] | Yao Guan-ping, Yu Li-mei, Fan Zhen-hai, Fang Ning, Ren Fei, Luo Jiao, Zhang Xiao-yu, Wang Yu-ying, Liu Jin-wei. Human amnion-derived mesenchymal stem cells transplantation improveshematopoietic function of myelosuppression mice [J]. Chinese Journal of Tissue Engineering Research, 2013, 17(23): 4248-4255. |
| [8] | Liu Yin, Tian Jing. Monoclonal antibody for treatment of multiple myeloma [J]. Chinese Journal of Tissue Engineering Research, 2013, 17(20): 3746-3755. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||