Chinese Journal of Tissue Engineering Research ›› 2020, Vol. 24 ›› Issue (31): 5071-5078.doi: 10.3969/j.issn.2095-4344.2125
Previous Articles Next Articles
Factors influencing differentiation of stem cells from the apical papilla into odontoblasts
Wang Wenhong, Li Yanjun, Cui Caiyun
- Department of Oral Medicine, Affiliated Hospital of Binzhou Medical University, Binzhou 256600, Shandong Province, China
-
Received:2020-01-11Revised:2020-01-15Accepted:2019-03-03Online:2020-11-08Published:2020-09-05 -
Contact:Cui Caiyun, MD, Attending physician, Department of Oral Medicine, Affiliated Hospital of Binzhou Medical University, Binzhou 256600, Shandong Province, China -
About author:Wang Wenhong, Master candidate, Physician, Department of Oral Medicine, Affiliated Hospital of Binzhou Medical University, Binzhou 256600, Shandong Province, China -
Supported by:the Natural Science Foundation of Shandong Province, No. ZR2019PH083; the Project of Medical, Health Science and Technology Development Plan of Shandong Province, No. 2017WS552
CLC Number:
Cite this article
Wang Wenhong, Li Yanjun, Cui Caiyun. Factors influencing differentiation of stem cells from the apical papilla into odontoblasts[J]. Chinese Journal of Tissue Engineering Research, 2020, 24(31): 5071-5078.
share this article

2.1 细胞因子 细胞因子是细胞受到外界刺激后合成、分泌的一类具有生物活性的小分子蛋白质,与相应受体结合调控细胞生长、分化及免疫应答等,其中转化生长因子β、骨形态发生蛋白、碱性成纤维细胞生长因子、肝细胞生长因子、炎症细胞因子、肿瘤坏死因子等多种细胞因子影响根尖牙乳头干细胞的增殖和分化[3],近几年研究主要集中于转化生长因子β1、骨形态发生蛋白2、基质细胞源性因子1α及肿瘤坏死因子α对根尖牙乳头干细胞成牙本质方向分化的影响。 2.1.1 转化生长因子β1 转化生长因子β是一族具有多种生物学功能的细胞因子,能刺激或抑制多种细胞的增殖,参与胚胎发生、损伤愈合、骨的重建以及免疫调节等生理和病理过程[4-5]。转化生长因子β1促进根尖牙乳头干细胞成牙本质方向分化的作用与其浓度相关,低浓度转化生长因子β1促进根尖牙乳头干细胞成牙本质方向分化,高浓度转化生长因子β1抑制其分化。丁芳 等[6]研究发现转化生长因子β1(5 μg/L)体外促进人根尖牙乳头干细胞增殖,增强碱性磷酸酶活性,促进DSPP、OCN和COL-ⅠmRNA表达。BELLAMY等[7]研究表明持续分泌转化生长因子β1生物活性支架比游离转化生长因子β1更显著促进根尖牙乳头干细胞成牙本质方向分化。顾雪凝等[8]将转化生长因子β1(5 mg/L)与矿化诱导液共同诱导人根尖牙乳头干细胞,发现转化生长因子β1抑制矿化结节的形成、抑制ALP、RUNX2、DSPP表达。当成牙本质细胞分泌胞外基质并开始矿化时,转化生长因子β1表达较强并通过自分泌和旁分泌参与基质形成和矿化的调控,还可通过调节紧密连接蛋白的表达来保证成牙本质细胞的有序排列[9]。转化生长因子β1能诱导人根尖牙乳头干细胞成牙本质方向分化,但转化生长因子β1作用浓度范围、作用机制及体内作用仍需进一步研究。 2.1.2 骨形态发生蛋白2 骨形态发生蛋白2是牙发育的重要调控因子,参与牙胚细胞的分化、牙胚的形态发生、牙的萌出和乳恒牙替换各阶段的调控[10],骨形态发生蛋白2在体外及动物体内异位移植均可促进人根尖牙乳头干细胞成牙本质方向分化。WANG等[11]采用骨形态发生蛋白2(100 μg/L)诱导后人根尖牙乳头干细胞碱性磷酸酶活性增强,COL-Ⅰ、DSPP、BSP、OCN mRNA和DSPP蛋白表达量增强,将根尖牙乳头干细胞复合含骨形态发生蛋白2 (5,25 μg)缓释聚乳酸-羟基乙酸共聚物微球的左旋聚乳酸纳米纤维化支架移植于裸鼠皮下,可见牙本质样硬组织形成且COL-Ⅰ、DSPP、BSP、OCN表达量增强。 2.1.3 基质细胞源性因子1α 基质细胞源性因子1α是CXC细胞因子家族的成员,通过激活CXC趋化因子4来介导细胞迁移,SDF-1α/CXC4通路是造血干细胞、间充质干细胞、内皮祖细胞迁移和分化的关键因素[12],基质细胞源性因子1α与骨形态发生蛋白2体内外协同促进根尖牙乳头干细胞成牙本质方向分化,基质细胞源性因子1α通过Erk/Smad信号通路参与骨形态发生蛋白2诱导根尖牙乳头干细胞成牙本质方向分化。XIAO等[13]用基质细胞源性因子1α(100 μg/L)与骨形态发生蛋白2 (100 μg/L)共同处理接种于VitroGel 3D支架的人根尖牙乳头干细胞,两者协同促进细胞ALP、DSPP、DMP-1、Runx2、OCN mRNA和蛋白表达,移植于裸鼠皮下可见骨样牙本质及血管样组织形成;骨形态发生蛋白2诱导人根尖牙乳头干细胞成牙本质方向分化后,阻断基质细胞源性因子1α信号显著降低骨形态发生蛋白2诱导的人根尖牙乳头干细胞矿化结节形成、碱性磷酸酶活性和RUNX2、DSPP、DMP-1的表达,Smad1/5和Erk1/2蛋白磷酸化水平降低[14]。 2.1.4 肿瘤坏死因子α 肿瘤坏死因子α是由巨噬细胞分泌的一种小分子蛋白,根据细胞类型和生理背景激活有利于细胞生存和凋亡的通路,在牙齿发育、创伤后修复中高表达。肿瘤坏死因子α体外能够激活人根尖牙乳头干细胞的NF-κB信号通路促进人根尖牙乳头干细胞成牙本质方向分化。李俊俊[15]用肿瘤坏死因子α(10 μg/L)作用于人根尖牙乳头干细胞,促进NF-κB信号通路相关蛋白IκBα和P65磷酸化,促进细胞增殖、碱性磷酸酶活性、矿化结节形成,OCN、BSP、OSX、RUNX2、DSPP、OPN、DMP-1 mRNA及蛋白表达增强,NF-κB信号通路抑制剂BMS-345541(1 μmol/L)作用于人根尖牙乳头干细胞,细胞增殖、碱性磷酸酶活性、矿化结节形成减弱,上述各基因及蛋白表达减弱,表明NF-κB信号通路在人根尖牙乳头干细胞成牙本质方向分化中有一定调节作用。 综上所述,转化生长因子β1、骨形态发生蛋白2、基质细胞源性因子1α及肿瘤坏死因子α体外促进根尖牙乳头干细胞成牙本质方向分化,其中基质细胞源性因子1通过Erk/Smad信号通路协同骨形态发生蛋白2、肿瘤坏死因子α通过NF-κB信号通路发挥作用,仅骨形态发生蛋白2进行动物实验证实牙本质样硬组织形成。各种细胞因子的作用机制及体内作用效果仍需进一步研究,多种细胞因子复合、构建细胞因子缓释支架显著增强细胞因子的诱导作用,可能成为今后研究的重要方向。 2.2 基因转染 主要是利用基因转染技术将某些信号转导成分的基因转入根尖牙乳头干细胞中,使促进细胞成牙本质方向分化的基因在根尖牙乳头干细胞中过表达,从而有效诱导根尖牙乳头干细胞成牙本质方向分化。近几年研究主要集中在采用慢病毒转染根尖牙乳头干细胞过表达骨形态发生蛋白、核因子C、环磷酸腺苷反应元件结合蛋白、Wnt5a、组蛋白去甲基化酶KDM4B和雌激素受体等研究对其成牙本质方向分化的影响。 2.2.1 骨形态发生蛋白 骨形态发生蛋白2基因促进根尖牙乳头干细胞成牙本质方向分化。ZHANG等[16]用慢病毒转染人根尖牙乳头干细胞过表达骨形态发生蛋白2基因,细胞碱性磷酸酶活性增强,矿化结节形成增多,ALP、OCN、DSPP、DMP-1高表达;ZHANG等[17-18]进一步用慢病毒分别将血管内皮生长因子或Fox2与骨形态发生蛋白2基因共同转染人根尖牙乳头干细胞,细胞矿化结节形成增多,ALP、OCN、DSPP、DMP-1 mRNA和蛋白均高表达,研究表明骨形态发生蛋白2基因能与血管内皮生长因子或Fox2基因协同促进人根尖牙乳头干细胞成牙本质方向分化。 骨形态发生蛋白9由肝脏非实质细胞表达,能促进脂质代谢,抑制葡萄糖生成和降血糖作用,其在胆碱能神经表型的发育和维持中起作用,并诱导间充质干细胞向软骨细胞谱系分化[19]。王金华[20]构建永生化小鼠根尖牙乳头干细胞模型,骨形态发生蛋白9腺病毒转染后小鼠根尖牙乳头干细胞碱性磷酸酶活性增强,Runx2、Sox9、PPARγ2、MEPE、DSPP、DMP-1、OPN、OCN、BSP表达增强,在裸鼠皮下及后肢肌肉能形成含骨、软骨及脂肪样组织的异位类牙本质块;孔令姣等[21]进一步使用ERK5抑制剂BIX02189干预骨形态发生蛋白9腺病毒转染后小鼠根尖牙乳头干细胞,P-ERK5蛋白表达减少,Runx2、DMP-1、OPN、OCN表达和矿化基质形成减少;陈冰等[22]进一步利用显性负性突变技术得到骨形态发生蛋白9的特异Ⅰ型受体ALK1的显性突变性受体dnALK1,用dnALK1和骨形态发生蛋白9腺病毒转染小鼠根尖牙乳头干细胞,P-Smad1/5/8蛋白表达减少,Runx2、DMP-1、OPN、OCN表达和矿化基质形成减少。上述研究表明骨形态发生蛋白9能够在体内外促进小鼠根尖牙乳头干细胞成牙本质方向分化和牙本质样组织形成,且ERK5及Smad信号通路参与骨形态发生蛋白9诱导小鼠根尖牙乳头干细胞成牙本质方向分化过程,但骨形态发生蛋白9对人根尖牙乳头干细胞成牙本质方向分化的作用有待进一步研究。 2.2.2 核因子C 核因子C是核因子家族的成员,核因子C缺失小鼠牙根发育异常,在调控磨牙牙根成牙本质细胞分化和牙根发育过程中发挥重要作用[23]。GAO等[24]将人根尖牙乳头干细胞异位移植后可分化为类成牙本质细胞并观察到细胞内核因子C表达,体外沉默核因子C的siRNA转染人根尖牙乳头干细胞后,细胞G1期延长,DSPP表达降低,DMP-1表达升高,细胞增殖、迁移和ALP、OCN、COL-1表达不受影响,研究表明核因子C参与人牙根部牙本质形成和人根尖牙乳头干细胞的成牙本质方向分化,且核因子C可能通过DMP-1-DSPP信号通路发挥作用。张菁[25]通过慢病毒转染人根尖牙乳头干细胞过表达核因子C基因,细胞碱性磷酸酶活性增强,ALP、OCN、COL-1表达增强,DSP蛋白表达增强,沉默核因子C的siRNA转染人根尖牙乳头干细胞之后上述基因表达降低,矿化结节形成减少,研究表明体外过表达核因子C可以促进人根尖牙乳头干细胞的成牙本质方向分化。梁妍等[26]用Forskolin(环磷酸腺苷信号通路激动剂)作用根尖牙乳头干细胞后矿化结节形成增多,RUNX2、ALP、OCN表达增强,进一步通过慢病毒转染过表达核因子C基因,矿化结节形成及上述基因表达进一步增强,表明核因子C基因与cAMP信号通路在调控根尖牙乳头干细胞成牙本质方向分化中具有协同促进作用。上述研究提示体外过表达核因子C基因促进根尖牙乳头干细胞成牙本质方向分化,可能通过DMP-1-DSPP信号通路和cAMP信号通路作用,但过表达核因子C基因的临床应用效果有待研究。 2.2.3 环磷酸腺苷反应元件结合蛋白(cAMP- responsive element-binding protein,CREB) 环磷酸腺苷反应元件结合蛋白是一种调节转录的细胞核内蛋白质,静息期细胞中环磷酸腺苷反应元件结合蛋白以去磷酸化状态存在,与DNA结合但无转录活性;细胞激活后环磷酸腺苷反应元件结合蛋白磷酸化,与环磷酸腺苷反应元件结合蛋白共同作用而诱导其转录活性[27]。cAMP/PKA/CREB信号通路是骨新陈代谢的重要信号通路,环磷酸腺苷反应元件结合蛋白磷酸化参与间充质干细胞向成骨细胞分化[28]。苏圣哲[29]通过慢病毒转染过表达环磷酸腺苷反应元件结合蛋白基因,人根尖牙乳头干细胞矿化结节形成增多,ALP、OCN、COL-1、RUNX2、osterix(OSX)表达增强,DSP、RUNX2蛋白表达增强,相反慢病毒转染沉默环磷酸腺苷反应元件结合蛋白基因,细胞矿化结节形成减少,上述各基因表达降低,提示环磷酸腺苷反应元件结合蛋白能促进人根尖牙乳头干细胞的成牙本质方向分化。顾雪凝等[8]在人根尖牙乳头干细胞中过表达环磷酸腺苷反应元件结合蛋白可逆转转化生长因子β1对人根尖牙乳头干细胞成牙本质方向分化的抑制作用,促进RUNX2、DSPP和ALP表达,提示过表达环磷酸腺苷反应元件结合蛋白后激活 cAMP,可能通过抑制ERK1/2、Smad等间接抑制转化生长因子β1信号通路,也可能直接抑制转化生长因子β1信号通路下游信号分子与转录因子的结合,发挥调控根尖牙乳头干细胞分化的作用。 2.2.4 Wnt5a Wnt5a是非经典Wnt信号通路的一种分泌型糖蛋白,可调控牙源性间充质干细胞的增殖、分化和迁移等,在牙和牙根的发育中发挥重要作用[30]。李由由[30]将Wnt5a过表达和沉默的根尖牙乳头干细胞系与羟基磷灰石-碳酸三钙复合移植于裸鼠背部皮下,组织学染色观察Wnt5a过表达组可见成牙本质细胞分化、牙本质样组织和牙髓牙本质复合体样组织形成,且ALP、DSPP、BSP、OCN蛋白表达增强,Wnt5a沉默组仅见细胞向成牙本质细胞分化,未见牙本质样组织形成,研究表明Wnt5a促进根尖牙乳头干细胞体内外成牙本质方向分化和牙本质样组织形成,Wnt5a调控的作用机制以及与其他因素之间的相互作用仍然需要进一步的研究。 2.2.5 组蛋白去甲基化酶KDM4B KDM4B是组蛋白去甲基化酶LSD1家族一员,KDM4B可通过调节DLX基因促进骨髓间充质干细胞成骨分化。姚睿等[31]用慢病毒转染人根尖牙乳头干细胞过表达KDM4B,促进细胞碱性磷酸酶活性和矿化结节形成,慢病毒转染基因敲除KDM4B,抑制细胞碱性磷酸酶活性及矿化结节形成,促进PPAR-γ的表达,研究表明KDM4B通过负向调节转录因子PPAR-γ促进根尖牙乳头干细胞成牙本质分化,但作用机制需要进行深入研究。 2.2.6 雌激素受体 雌激素受体是核受体超家族成员之一,属于典型的类固醇受体,分为雌激素受体α和雌激素受体β亚型,在间充质干细胞成骨分化中,雌激素受体α起着关键的调节作用[32]。卢亚蝶等[33]用慢病毒转染人根尖牙乳头干细胞过表达雌激素受体α,促进细胞矿化结节形成和ALP、OSX、DSP、OCN表达,研究表明体外高表达雌激素受体α能够诱导人根尖牙乳头干细胞成牙本质方向分化,但其作用机制仍需研究。 综上所述,近6年文献中约1/3采用慢病毒转染方法将目的基因转染到根尖牙乳头干细胞中,进一步研究根尖牙乳头干细胞成牙本质方向分化。骨形态发生蛋白2基因协同血管内皮生长因子和Fox2促进人根尖牙乳头干细胞成牙本质方向分化;骨形态发生蛋白9基因通过ERK5及Smad信号通路促进小鼠根尖牙乳头干细胞成牙本质方向分化和牙本质样组织形成,但其对人来源根尖牙乳头干细胞作用需要进一步研究明确;KDM4B受BMP信号通路作用调控促进人根尖牙乳头干细胞成牙本质方向分化。另外,核因子C基因通过DMP-1-DSPP和cAMP信号通路促进人根尖牙乳头干细胞成牙本质方向分化,环磷酸腺苷反应元件结合蛋白基因激活cAMP信号通路可逆转转化生长因子β1对人根尖牙乳头干细胞成牙本质方向分化的抑制作用。Wnt5a和雌激素受体α基因促进根尖牙乳头干细胞体内外成牙本质方向分化,此外Wnt5a还能促进牙本质样组织形成。慢病毒转染促进上述各基因表达利于研究促进根尖牙乳头干细胞成牙本质方向分化的作用及机制,继续探寻引入操作简单有效的基因转染技术,更深入研究各基因的作用途径仍旧是未来研究的重点和方向。 2.3 生物活性材料及支架材料 2.3.1 细胞外基质衍生物 细胞外基质来源的生物材料因富含细胞因子、生物活性蛋白及天然支架材料结构等在促进根尖牙乳头干细胞成牙本质方向分化中发挥重要作用,近年主要研究包括牙本质非胶原蛋白、条件培养基、血小板裂解液、细胞外基质支架等。 牙本质非胶原蛋白主要包括牙本质特异性蛋白、非特异性蛋白、生长因子以及蛋白多糖、少量脂质等[34]。牙本质非胶原蛋白在牙胚发育过程中能够充当细胞间信号分子,诱导成牙本质细胞分化、基质分泌和启动牙本质矿化。马兆峰等[35]用牙本质非胶原蛋白(10 mg/L)体外诱导培养后人根尖牙乳头干细胞碱性磷酸酶活性增强,ALP、COL-1、OCN表达增强,提示牙本质非胶原蛋白促进人根尖牙乳头干细胞成牙本质方向分化。牙本质非胶原蛋白包含多种成分,其对根尖牙乳头干细胞的体内作用、机制以及各组分之间的相互作用仍需进一步研究。 条件培养基是将培养过细胞的培养基去除细胞后取其上清液,因其含有大量由细胞分泌的细胞因子,可直接用于培养其他细胞或作为其他细胞培养基的添加成分以促进细胞生长分化。WU等[36]采用含30%牙囊细胞条件培养基诱导人根尖牙乳头干细胞,促进细胞增殖、碱性磷酸酶活性和DSPP、ALP、OCN表达,提示牙囊细胞的条件培养基能促进根尖牙乳头干细胞成牙本质方向分化。付越等[37]制备人富血小板纤维蛋白条件培养基体外诱导人根尖牙乳头干细胞,促进细胞增殖和DSPP、DMP-1、OCN表达,说明富血小板纤维蛋白能促进根尖牙乳头干细胞成牙本质方向分化。但上述各条件培养基的作用机制仍需进一步研究。 血小板裂解液是自体或异体血小板富集物经细胞裂解后的产物,作为胎牛血清的替代品用于间充质干细胞的大规模扩增培养。ABUARQOUB等[38]用5%血小板裂解液诱导人根尖牙乳头干细胞,促进细胞增殖、碱性磷酸酶活性和DSPP、OCN、BSP表达,提示5%血小板裂解液能促进根尖牙乳头干细胞成牙本质方向分化,但其在动物及临床模型中的有效性及调控机制仍需进一步研究探索。 此外,黄奕智[39]将人根尖牙乳头干细胞装载于SD大鼠富血小板血浆支架上植入制备好的人牙根管内,复合材料整体移植于SD大鼠皮下,可见牙髓牙本质复合体样组织形成,表明富血小板血浆异位体内促进根尖牙乳头干细胞成牙本质方向分化。SONG等[40]将根尖牙乳头干细胞接种于脱细胞牙髓支架,促进细胞增殖和ALP、DSPP、OCN表达,表明人脱细胞牙髓支架能够诱导根尖牙乳头干细胞成牙本质方向分化,但脱细胞支架中易残留细胞成分可能导致机体免疫排斥反应。 牙本质非胶原蛋白、牙囊细胞及富血小板纤维蛋白条件培养基、血小板裂解液、富血小板血浆和脱细胞牙髓支架因富含大量天然生物活性成分促进人根尖牙乳头干细胞成牙本质方向分化,具有极好的应用前景,但由于生物活性成分可能引起机体免疫排斥反应,在以后应将作用机制及免疫反应研究作为重要研究方向。 2.3.2 生物陶瓷材料 生物陶瓷材料是指具有特定的生物属性或生物功能的一类陶瓷材料,即直接用于人体或与人体直接相关的生物、医用、生物化学等陶瓷材料[41],表面具有生物活性或者具有生物吸收性的陶瓷材料是生物活性陶瓷。近年来与根尖牙乳头干细胞成牙本质方向分化有关的硅钙磷酸盐类生物活性材料主要是iRoot FM和Biodentine,其中iRoot FM主要成分是硅酸钙、氧化锆、磷酸二氢钙和氢氧化钙,Biodentine主要成分是硅酸三钙、碳酸钙和氧化锆,见表1。 "

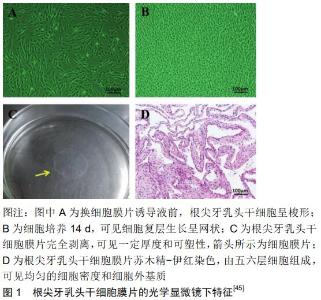
BI等[42]用iRoot FM(0.5 g/L)体外诱导后促进人根尖牙乳头干细胞增殖、矿化结节形成、ALP和DMP-1 mRNA及蛋白表达,表明iRoot FM体外促进根尖牙乳头干细胞成牙本质方向分化。WONGWATANASANTI等[43]用Biodentine(0.14 g/L)体外诱导后促进人根尖牙乳头干细胞增殖、矿化结节形成和DMP-1、DSPP、OCN、MEPE表达;MILLER等[44]用Biodentine体外诱导后促进人根尖牙乳头干细胞增殖、矿化结节形成和ALP、DSPP表达;上述表明Biodentine体外可以促进根尖牙乳头干细胞成牙本质方向分化。随着生物活性陶瓷类材料的研发和在牙体牙髓治疗中的广泛应用,其对根尖牙乳头干细胞成牙本质方向分化研究也逐渐开始,但其对根尖牙乳头干细胞体内成牙本质分化的能力并未见研究报道,作用机制仍不明确。兼具生物活性和支架材料的可塑性,生物活性陶瓷材料成为能够尽早用于诱导根尖牙乳头干细胞成牙本质方向分化的生物材料。 2.3.3 支架材料 3D培养较传统2D培养模式显著促进根尖牙乳头干细胞成牙本质方向分化。马学娟等[45]用 48 mg/L维生素C连续培养人根尖牙乳头干细胞形成细胞膜片,见图1,Runx2、ALP、CoL-Ⅰ表达增强,Runx2、ALP蛋白表达增强,研究表明细胞膜片培养人根尖牙乳头干细胞与单独培养相比促进细胞成牙本质方向分化。NA等[46]采用改良细胞膜片技术培养人根尖牙乳头干细胞三维无支架干细胞膜片衍生颗粒,促进ALP、DSPP、BSP、RUNX2 mRNA和蛋白表达,进一步将衍生颗粒复合处理人牙本质基质移植入裸鼠皮下可见牙本质样组织形成,研究表明三维无支架干细胞膜片衍生颗粒促进根尖牙乳头干细胞成牙本质方向分化。细胞膜片及其衍生颗粒体外及异位体内移植促进根尖牙乳头干细胞成牙本质方向分化及牙本质样组织形成,其临床应用仍需进一步研究。 构建复合支架材料达到生长因子或药物缓释利于根尖牙乳头干细胞成牙本质方向分化。WANG等[11]将根尖牙乳头干细胞复合含骨形态发生蛋白2(5,25 μg)缓释聚乳酸-羟基乙酸共聚物微球的左旋聚乳酸纳米纤维化支架移植于裸鼠皮下,可见牙本质样硬组织形成且COL-Ⅰ、DSPP、BSP、OCN表达量增强。SHRESTHA等[47]用包裹法和吸附法合成负载地塞米松的壳聚糖纳米颗粒诱导根尖牙乳头干细胞,促进ALP、DSPP、DMP-1表达,研究表明缓释地塞米松体外促进根尖牙乳头干细胞成牙本质方向分化。但缓释控制系统仍有下述问题需要解决:①增强所含生物活性分子的稳定性;②允许生物活性分子长时间释放;③由于与聚合物的相互作用而释放生物活性分子。 此外,可塑及可操作性能更优的凝胶类支架也能促进根尖牙乳头干细胞成牙本质方向分化。透明质酸在牙齿发育过程中参与牙齿硬组织矿化,CHREPA等[48]将根尖牙乳头干细胞接种于透明质酸凝胶支架,促进细胞碱性磷酸酶活性和DSPP、DMP-1、MEPE表达,说明其能促进根尖牙乳头干细胞成牙本质方向分化,但材料的理化性能、生物相容性及稳定性尚不明确。 支架材料表面微尺寸对根尖牙乳头干细胞的成牙本质分化也有一定影响。HA等[49]将根尖牙乳头干细胞接种于不同硬度及表面微尺寸的水凝胶表面,GelMA水凝胶(10%)促进根尖牙乳头干细胞增殖,光蚀刻技术形成60 μm和120 μm微图案的支架材料表面可见细胞有沿材料表面几何图形自校准生长趋势,且碱性磷酸酶活性增强,研究表明直角材料表面微尺寸促进根尖牙乳头干细胞的成牙本质分化,微图案沟槽和牙本质小管之间结构相似性可能是其机制。 目前促进根尖牙乳头干细胞成牙本质方向分化的支架材料包括缓释微球、细胞外基质衍生材料、可注射凝胶、支架表面蚀刻,支架材料还有许多问题需探索和解决,如细胞与支架材料的相互作用机制、支架材料的机械强度和可塑性、安全性与易操作性等还需进一步研究。 2.4 化学因素 促进根尖牙乳头干细胞成牙本质方向分化的化学诱导剂主要包括瘦素、毛喉素和乙酰水杨酸。 瘦素(leptin)是由脂肪组织分泌的一种蛋白类激素,在间充质干细胞的增殖和分化中有着重要的调节作 用[50]。尹小萍等[51]用1.5 mg/L瘦素体外诱导人根尖牙乳头干细胞,促进细胞增殖、碱性磷酸酶活性和ALP、DMP-1、DSPP、OCN表达,说明瘦素在体外能促进根尖牙乳头干细胞成牙本质方向分化,参与的相关信号通路及具体机制仍需进一步研究。 毛喉素(Forskolin)是一种在印度植物毛喉鞘蕊花中天然产生的双萜,可激活腺苷酸环化酶,因此会使胞内cAMP 浓度升高,作用于其受体PKA进一步激活下游信号分子,作为cAMP/PKA信号通路的激活剂参与调节多种细胞的增殖、迁移、凋亡和分化等[52]。苏圣哲等[53]用毛喉素(5 μmol/L)及抑制剂H-89(10 μmol/L)体外诱导人根尖牙乳头干细胞,毛喉素组细胞矿化结节形成增多,ALP、OCN、OSX、RUNX2表达上升,H-89组细胞矿化结节形成减少,OCN、OSX、RUNX2表达降低,毛喉素可通过激活cAMP/PKA信号通路促进根尖牙乳头干细胞成牙本质分化。 乙酰水杨酸是水杨酸的衍生物,临床常用于缓解疼痛、退热。TANAKA等[54]用乙酰水杨酸(100 mg/L)诱导人根尖牙乳头干细胞,促进矿化结节形成、DSPP的基因和蛋白表达,抑制RUNX2的基因和蛋白表达,异位移植裸鼠皮下有新生矿化组织形成,LY294402 (50 μmol/L,PI3K-AKT通路的特异性抑制剂)和AKT- siRNA(20 nmol/L)分别处理经过乙酰水杨酸诱导的人根尖牙乳头干细胞,也可促进矿化结节形成,促进SP7、NFIC及DSPP表达,抑制RUNX2的表达,研究表明乙酰水杨酸联合抑制AKT信号通路可促进根尖牙乳头干细胞的成牙本质方向分化,其临床应用效果有待研究。 2.5 物理因素 促进根尖牙乳头干细胞成牙本质方向分化的物理因素主要包括牵张应力和机械压应力。杜希希等[55]采用重物加压牵张弹性硅胶膜对贴壁生长人根尖牙乳头干细胞施加牵张应力,200 g机械牵张应力显著促进ALP、OSX、DSP mRNA和蛋白表达升高,研究表明人根尖牙乳头干细胞能承受生理水平的机械牵张应力促进人根尖牙乳头干细胞成牙本质方向分化。肖 敏[56]对人根尖牙乳头干细胞施加周期性机械压应力 30 min/d,210 g机械压应力显著促进碱性磷酸酶活性、矿化结节形成和DSPP、RUNX-2、OCN、OSX、DMP-1表达,结果表明周期性机械压应力能促进根尖牙乳头干细胞成牙本质方向分化。上述研究表明体外机械刺激能促进根尖牙乳头干细胞成牙本质方向分化,但尚未进行体内研究,接近体内状况的加力条件尚不明确。 "
|
[1] SONOYAMA W, LIU Y, FANG D, et al. Mesenchymal stem cell-mediated functional tooth regeneration in swine. PLoS One. 2006;1:e79.
[2] CHUEH LH, HUANG GT. Immature teeth with periradicular periodontitis or abscess undergoing apexogenesis: a paradigm shift. J Endod. 2006;32(12):1205-1213.
[3] 张羽,吴家媛.生长因子对根尖牙乳头干细胞增殖及分化的影响[J].中国实用口腔科杂志,2016,9(3):187-190.
[4] 张莹,张郁,金岩.转化生长因子-β受体在人牙髓中的表达和意义[J].实用口腔医学杂志,1999,15(5):361-363.
[5] 张莹,张郁,金岩.转化生长因子β受体在牙胚发育过程中的表达和意义[J].牙体牙髓牙周病学杂志,1999,9(1):11.
[6] 丁芳,吴家媛,贾谦,等. TGF-β1对人根尖牙乳头干细胞增殖和分化的影响[J].牙体牙髓牙周病学杂志,2011,21(7):375-379.
[7] BELLAMY C, SHRESTHA S, TORNECK C, et al. Effects of a Bioactive Scaffold Containing a Sustained Transforming Growth Factor-β1-releasing Nanoparticle System on the Migration and Differentiation of Stem Cells from the Apical Papilla. J Endod. 2016;42(9):1385-1392.
[8] 顾雪凝,权家苗,郭雨晴,等.环磷酸腺苷反应元件结合蛋白调控转化生长因子β1对人根尖牙乳头干细胞分化的作用[J].口腔疾病防治, 2018,26(7): 428-433.
[9] 陈尽欢,孙建勋,陈新梅.转化生长因子-β超家族成员在牙本质发生发育中的作用[J].国际口腔医学杂志,2016,43(4):477-481.
[10] 程敏,程琳,冯志远,等.骨形态发生蛋白-2在牙发育各阶段中的表达[J].国际口腔医学杂志,2009,36(6):639-642.
[11] WANG W, DANG M, ZHANG Z, et al. Dentin regeneration by stem cells of apical papilla on injectable nanofibrous microspheres and stimulated by controlled BMP-2 release. Acta Biomater. 2016;36: 63-72.
[12] LI J, GUO W, XIONG M, et al. Effect of SDF-1/CXCR4 axis on the migration of transplanted bone mesenchymal stem cells mobilized by erythropoietin toward lesion sites following spinal cord injury. Int J Mol Med. 2015;36(5):1205-1214.
[13] XIAO M, QIU J, KUANG R, et al. Synergistic effects of stromal cell-derived factor-1α and bone morphogenetic protein-2 treatment on odontogenic differentiation of human stem cells from apical papilla cultured in the VitroGel 3D system. Cell Tissue Res. 2019;378(2):207-220.
[14] XIAO M, YAO B, ZHANG BD, et al. Stromal-derived Factor-1α signaling is involved in bone morphogenetic protein-2-induced odontogenic differentiation of stem cells from apical papilla via the Smad and Erk signaling pathways. Exp Cell Res. 2019;381(1): 39-49.
[15] 李俊俊. NF-κB信号通路在人根尖牙乳头干细胞增殖及定向分化中的作用机制研究[D].南京:南京医科大学, 2014.
[16] ZHANG W, ZHANG X, LING J, et al. Proliferation and odontogenic differentiation of BMP2 gene‑transfected stem cells from human tooth apical papilla: an in vitro study. Int J Mol Med. 2014;34(4):1004-1012.
[17] ZHANG W, ZHANG X, LING J, et al. Osteo-/odontogenic differentiation of BMP2 and VEGF gene-co-transfected human stem cells from apical papilla. Mol Med Rep. 2016;13(5): 3747-3754.
[18] ZHANG W, ZHANG X, LI J, et al. Foxc2 and BMP2 Induce Osteogenic/Odontogenic Differentiation and Mineralization of Human Stem Cells from Apical Papilla. Stem Cells Int. 2018; 2018:2363917.
[19] 赵丹,罗进勇. BMP9促进间充质干细胞C3H10T1/2成骨分化的研究[J].临床和实验医学杂志,2011,10(16):1225-1226.
[20] 王金华. BMP9调控小鼠根尖牙乳头干细胞成牙本质分化及其机制的初步研究[D].重庆:重庆医科大学,2013.
[21] 孔令姣,王金华. BMP9通过ERK5信号通路调控根尖牙乳头干细胞成骨/成牙本质分化[J].中国医科大学学报,2017,46(6):527-531.
[22] 陈冰,孔令姣,雷金霞,等.BMP9经Smad信号通路调控iSCAP成骨/成牙本质分化[J].中国生物工程杂志,2016,36(8):16-22.
[23] KIM TH, BAE CH, YANG S, et al. Nfic regulates tooth root patterning and growth. Anat Cell Biol. 2015;48(3):188-194.
[24] GAO S, ZHAO YM, GE LH. Nuclear factor I-C expression pattern in developing teeth and its important role in odontogenic differentiation of human molar stem cells from the apical papilla. Eur J Oral Sci. 2014;122(6):382-390.
[25] 张菁.转录因子NFIC在人根尖牙乳头干细胞分化中的作用及其机制研究[D].西安:第四军医大学,2013.
[26] 梁妍,张菁,李颂.转录因子NFIC在cAMP信号通路调控根尖牙乳头干细胞分化中的作用[J].安徽医科大学学报, 2017,52(2):190-193.
[27] 肖佩芳,柴忆欢,何军,等.环磷酸腺苷反应元件结合蛋白在儿童急性淋巴细胞白血病中表达的意义[J].实用儿科临床杂志,2008,23(3): 200-202.
[28] SIDDAPPA R, MARTENS A, DOORN J, et al. cAMP/PKA pathway activation in human mesenchymal stem cells in vitro results in robust bone formation in vivo. Proc Natl Acad Sci U S A. 2008; 105(20):7281-7286.
[29] 苏圣哲.转录因子CREB在根尖牙乳头干细胞定向分化中的作用[D].合肥:安徽医科大学,2016.
[30] 李由由. Wnt5a对根尖牙乳头干细胞体内成牙/成骨分化的影响[D].遵义:遵义医学院,2016.
[31] 姚睿,范志朋.组蛋白去甲基化酶KDM4B促进根尖牙乳头干细胞中成骨和成牙本质分化[J].北京口腔医学,2013,21(4):181-184.
[32] 岑洪,林茂芳,黄河,等.雌激素受体α和β在间充质干细胞体外成骨、成脂肪分化中的表达变化[J].广西医科大学学报,2005,22(6):883-885.
[33] 卢亚蝶,闫明,于金华.雌激素受体α高表达慢病毒载体对根尖牙乳头干细胞成牙/成骨分化的影响[J].口腔医学,2016,36(6):485-488.
[34] BUTLER WT, RITCHIE H. The nature and functional significance of dentin extracellular matrix proteins. Int J Dev Biol. 1995;39(1): 169-179.
[35] 马兆峰,李石,翁希里,等.牙本质非胶原蛋白对人根尖牙乳头干细胞增殖及分化能力的影响[J].牙体牙髓牙周病学杂志,2016,26(5): 283-287.
[36] WU J, JIA Q, HE W, et al. Conditioned medium from periapical follicle cells induces the odontogenic differentiation of stem cells from the apical papilla in vitro. J Endod. 2013;39(8):1015-1022.
[37] 付越,刘尧,陈旭.富血小板纤维蛋白应用于口腔组织再生研究进展[J].中国实用口腔科杂志,2016,9(1):59-62.
[38] ABUARQOUB D, AWIDI A, ABUHARFEIL N. Comparison of osteo/odontogenic differentiation of human adult dental pulp stem cells and stem cells from apical papilla in the presence of platelet lysate. Arch Oral Biol. 2015;60(10):1545-1553.
[39] 黄奕智.根尖牙乳头干细胞和富含血小板血浆在SD大鼠模型中进行牙髓牙本质再生的研究[D].南昌:南昌大学,2017.
[40] SONG JS, TAKIMOTO K, JEON M, et al. Decellularized Human Dental Pulp as a Scaffold for Regenerative Endodontics. J Dent Res. 2017;96(6):640-646.
[41] 卢陈佩,王旭东,沈国芳.生物陶瓷在骨组织工程中的应用进展[J].中国组织工程研究,2017,21(22):3576-3582.
[42] BI J, LIU Y, LIU XM, et al. iRoot FM exerts an antibacterial effect on Porphyromonas endodontalis and improves the properties of stem cells from the apical papilla. Int Endod J. 2018;51(10): 1139-1148.
[43] WONGWATANASANTI N, JANTARAT J, SRITANAUDOMCHAI H, et al. Effect of Bioceramic Materials on Proliferation and Odontoblast Differentiation of Human Stem Cells from the Apical Papilla. J Endod. 2018;44(8):1270-1275.
[44] MILLER AA, TAKIMOTO K, WEALLEANS J, et al. Effect of 3 Bioceramic Materials on Stem Cells of the Apical Papilla Proliferation and Differentiation Using a Dentin Disk Model. J Endod. 2018;44(4): 599-603.
[45] 马学娟,刘雪梅,毕静,等.根尖牙乳头干细胞细胞膜片构建及其成骨/成牙本质分化性能研究[J].上海口腔医学,2018,27(2):123-128.
[46] NA S, ZHANG H, HUANG F, et al. Regeneration of dental pulp/dentine complex with a three-dimensional and scaffold-free stem-cell sheet-derived pellet. J Tissue Eng Regen Med. 2016; 10(3):261-270.
[47] SHRESTHA S, DIOGENES A, KISHEN A. Temporal-controlled Dexamethasone Releasing Chitosan Nanoparticle System Enhances Odontogenic Differentiation of Stem Cells from Apical Papilla. J Endod. 2015;41(8):1253-1258.
[48] CHREPA V, AUSTAH O, DIOGENES A. Evaluation of a Commercially Available Hyaluronic Acid Hydrogel (Restylane) as Injectable Scaffold for Dental Pulp Regeneration: An In Vitro Evaluation. J Endod. 2017;43(2):257-262.
[49] HA M, ATHIRASALA A, TAHAYERI A, et al. Micropatterned hydrogels and cell alignment enhance the odontogenic potential of stem cells from apical papilla in-vitro. Dent Mater. 2020;36(1): 88-96.
[50] UM S, CHOI JR, LEE JH, et al. Effect of leptin on differentiation of human dental stem cells. Oral Dis. 2011;17(7):662-669.
[51] 尹小萍,熊华翠,陈柯,等.瘦素对人根尖乳头干细胞成骨/成牙本质相关基因表达的影响[J].口腔疾病防治,2019,27(1):23-29.
[52] FU SP, WANG W, LIU BR, et al. β-Hydroxybutyric sodium salt inhibition of growth hormone and prolactin secretion via the cAMP/PKA/CREB and AMPK signaling pathways in dairy cow anterior pituitary cells. Int J Mol Sci. 2015;16(2):4265-4280.
[53] 苏圣哲,朱永娜,张菁,等. cAMP信号通路在根尖牙乳头干细胞定向分化中的作用[J].实用口腔医学杂志,2016,32(5):650-654.
[54] TANAKA Y, SONODA S, YAMAZA H, et al. Acetylsalicylic Acid Treatment and Suppressive Regulation of AKT Accelerate Odontogenic Differentiation of Stem Cells from the Apical Papilla. J Endod. 2019;45(5):591-598.
[55] 杜希希,李波,袁小平.机械牵张应力对人根尖牙乳头干细胞增殖分化的影响[J].医学研究生学报, 2017,30(10):1041-1047.
[56] 肖敏.机械压应力刺激对人牙髓干细胞和根尖牙乳头干细胞增殖、分化影响的体外研究[D].西安:第四军医大学, 2015. |
| [1] | Wei Jianghong, Jia Aijun, Ma Libing, Wang Yueling, Qiu Lulu, Xiao Bing. Th-17 regulatory cytokines promote interleukins-17A and 17F production by neutrophils during asthma [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(31): 5044-5051. |
| [2] |
Yang Jiayi, Zhang Guanghao, Zhang Cheng, Li Ke, Huo Xiaolin, Wu Changzhe.
Stem cell expansion and hepatic differentiation: measurement of related indicators and detection methods [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(25): 4039-4045. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||