Chinese Journal of Tissue Engineering Research ›› 2014, Vol. 18 ›› Issue (16): 2582-2587.doi: 10.3969/j.issn.2095-4344.2014.16.020
Previous Articles Next Articles
Artificial bone materials for bone defect repair: biomechanical characteristics of multiple composites
Yang Yi, Bi Xin, Li Duo-yu, Tang Yi-ping, Li Biao
- Department of Orthopedics, First Affiliated Hospital of Kunming Medical University, Kunming 650031, Yunnan Province, China
-
Revised:2014-02-02Online:2014-04-16Published:2014-04-16 -
Contact:Li Biao, Associate chief physician, Master’s supervisor, Department of Orthopedics, First Affiliated Hospital of Kunming Medical University, Kunming 650031, Yunnan Province, China -
About author:Yang Yi, Studying for master’s degree, Department of Orthopedics, First Affiliated Hospital of Kunming Medical University, Kunming 650031, Yunnan Province, China -
Supported by:the Applied Basic Research of Yunnan Province, No. 2013FB144
CLC Number:
Cite this article
Yang Yi, Bi Xin, Li Duo-yu, Tang Yi-ping, Li Biao. Artificial bone materials for bone defect repair: biomechanical characteristics of multiple composites[J]. Chinese Journal of Tissue Engineering Research, 2014, 18(16): 2582-2587.
share this article
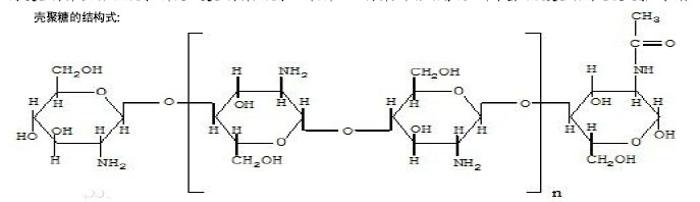
2.1 天然高分子材料 2.1.1 甲壳素及其衍生物 甲壳素广泛存在于甲壳类动物、昆虫和霉菌中,是一种天然的生物高分子物质。有学者用浓碱处理后得到的壳聚糖是甲壳素最重要的衍生物之一[5]。甲壳素及其衍生物之所以能用于骨缺损修复,主要有以下几方面原因:①可降解性,甲壳素和壳聚糖所制成的生物材料进入人体后,在体内许多酶系的作用下,壳聚糖降解成为对人体无毒的N-乙酰氨基葡萄糖及氨基葡萄糖,这两种单糖能被人体完全吸收[6-7]。②生物相容性:壳聚糖的性质不活泼,不与体液和体内组织产生异物反应。VandeVord等[8]将壳聚糖支架植入小鼠骨缺损模型中,未见材料植入部位发生明显的炎症排斥反应。Aspden等[9]也对壳聚糖进行了一系列的动物毒性实验,结果发现壳聚糖具有很好的生物相容性和安全性,其降解产物对人体无毒,无溶血性、刺激性、热源性和致突变性。③抗菌活性:近年来研究发现,壳聚糖可抑制大肠埃希菌、沙门杆菌、金葡菌、绿脓杆菌及某些真菌等的生长[10]。有学者研究发现,壳聚糖中带正电的铵根与细菌带负电荷细胞膜之间的静电作用使细菌细胞壁和细胞膜上的负电荷分布不均,从而减退了细胞壁和细胞膜的功能。水溶性壳聚糖能穿过损伤的细胞壁进入细菌细胞内,吸附带负电的细胞质,扰乱细菌的代谢[11]。④促进止血及伤口愈合:壳聚糖能使伤口处上皮增生速度加快,促进真皮层胶原的沉积,同时其抗菌活性能抑制外界微生物的侵袭[12]。 2.1.2 胶原及其复合材料 胶原作为生物材料被广泛应用于临床,在骨缺损部位的填充修复领域有着举足轻重的地位[13],它是天然骨组织中有机质的主要成分,是钙盐沉积的支架和骨基质矿化的促进剂,可为成骨细胞的附着提供支架;而且它具有无毒、低抗原性、良好的生物相容性、生物可降解性,能够促进细胞迁移、分化及黏附。 胶原海绵产品的主要成分是I型胶原,佟刚等[14]研究发现胶原海绵具有良好的安全性,不同pH胶原海绵对组织无明显的安全性影响,低pH条件在一定程度上可促进缺损组织愈合。胶原具有许多优点,但也有不足,如缺乏一定的机械强度、降解快,难以作为支撑材料,且容易变形,在应用过程中受到诸多限制,故其应用主要集中在胶原复合材料方面,如胶原-磷灰石复合材料,胶原-双相磷酸钙生物陶瓷复合材料,胶原-天然生物衍生骨复合材料等。近年来,许多学者对胶原复合材料进行了探索与研究,有研究评估纳米羟基磷灰石/胶原骨材料在骨折后骨缺损应用中的临床效果,研究对21例骨折后骨缺损患者应用纳米羟基磷灰石/胶原骨修复材料进行手术植入治疗,连续6-13个月临床观察随访。结果显示21例中2例失访,获随访的19例患者无局部或全身不良反应,19例中2例因外伤或过早负重,致内固定钢板折断再骨折,予重新手术内固定,其余17例均达临床愈合。X射线片显示,术后1-3个月材料植入区与缺损周围的骨组织间界限模糊有新骨形成,3-6个月材料植入区内有明显的新骨长入,骨修复材料与骨组织融合一体,达到骨性连接,骨缺损己基本修复,6-12个月植骨塑形改建,提示纳米羟基磷灰石/胶原骨修复材料具有良好的生物相容性和骨传导性,其良好的材 料-细胞界面使材料本身便具备与骨键合的能力,其三维多孔结构便于骨组织的长入,其生物降解性有利于骨组织的改建和塑形,具有良好的临床应用前景。杨春蓉等[15]将纳米羟基磷灰石粉体、胶原蛋白溶液和磷酸丝氨酸按比例混合得到具有三维多孔的微观结构,该复合支架具有良好的生物相容性,说明纳米羟基磷灰石-胶原蛋白-磷酸丝氨酸(nHA-COL-PS)支架材料是性能良好的组织工程支架材料,可用于骨缺损的修复。也有学者发现骨形态发生蛋白2基因修饰的β-磷酸三钙/胶原复合材料具有良好的生物相容性,骨诱导和传导性佳,是很有潜力的新型骨缺损修复材料[16]。 2.1.3 纤维蛋白胶 纤维蛋白胶是一种天然的细胞外基质,生物相容性好、可注射及弹性和黏附能力好,易被人体组织吸收,无毒性,可以促进细胞外基质的合成,且不会导致炎症反应,故近年来被广泛用于骨组织工程中。纤维蛋白胶凝固后可以任意塑型并具有一定的黏弹性,临床中可将各种骨替代材料黏附在一起,用于骨缺损的修复。 有研究采用浓缩自体骨髓复合纤维蛋白胶修复陈旧性骨缺损,初步探讨其促进成骨的机制。实验将36只新西兰大白兔随机平均分为3组:单纯纤维蛋白胶组、纤维蛋白胶复合自体骨髓组、纤维蛋白胶复合浓缩自体骨髓组。每只动物均在左侧桡骨中段制造长1.5 cm的段缺性骨与骨膜缺损,1个月后在骨缺损处分别植入3种组织工程复合材料。取浓缩骨髓、纤维蛋白胶复合物行电镜观察、长期培养及细菌学培养。术后4,8,12周行X射线检查、硬组织切片观察成骨效果,并行半定量分析。电镜下可见骨髓有核细胞与纤维蛋白胶相容性良好,无细菌污染,长期培养无致瘤性。X射线观察显示纤维蛋白胶复合自体骨髓组和纤维蛋白胶复合浓缩自体骨髓组的修复效果明显高于单纯纤维蛋白胶组。术后8,12周,纤维蛋白胶复合浓缩自体骨髓组的Yang氏评分分别为(9.348±0.364)和(12.664±0.388)分,明显高于纤维蛋白胶复合自体骨髓组的(7.984±0.229)分(F=40.167,P=0.001)和(10.584±0.836)分(F=20.3647,P=0.004)。纤维蛋白胶复合自体骨髓组(F=36.004,P=0.001)和纤维蛋白胶复合浓缩自体骨髓组(F=155.141,P=0.000)术后12周的Yang氏评分均明显高于术后8周。随着时间的延长,组织学切片见纤维蛋白胶复合自体骨髓组和纤维蛋白胶复合浓缩自体骨髓组均有不同程度的骨缺损修复,提示自体骨髓或浓缩自体骨髓复合纤维蛋白胶可修复兔桡骨陈旧性骨缺损,单纯纤维蛋白胶无此作用。Pei等[17]提取自体膝关节滑膜细胞与纤维蛋白胶复合后旋转培养1个月,见细胞保持原有形态,将其与材料复合后成功修复了兔股骨髁的骨软骨缺损。Abiraman等[18-19]将纤维蛋白胶包被羟基磷灰石颗粒、生物活性玻璃陶瓷和磷酸钙硅酸钙系统分别植入鼠股四头肌,结果表明纤维蛋白胶有骨诱导作用,且纤维蛋白胶可以促进形成新的毛细血管及胶原沉积。姚旺祥等[20]发现自体骨髓或浓缩自体骨髓复合纤维蛋白胶可修复兔桡骨陈旧性骨缺损,而单纯纤维蛋白胶无此作用,肖裕华等[21]的研究表明纤维蛋白胶复合血管内皮生长因子和骨形态发生蛋白具有良好的诱导异位成骨的作用,两者均说明纤维蛋白胶作为支架与其他材料复合更能发挥其优势。但纤维蛋白胶降解时间较快、强度低,如何这两个问题需要更进一步的研究。"
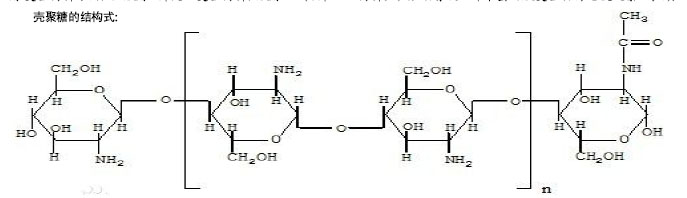
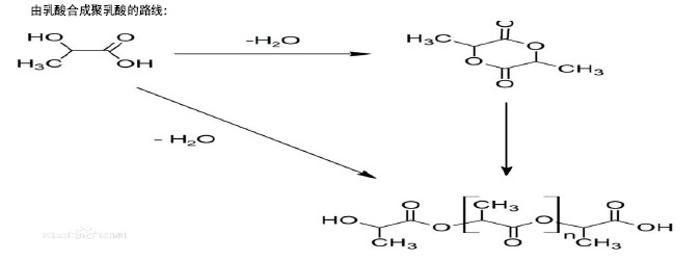
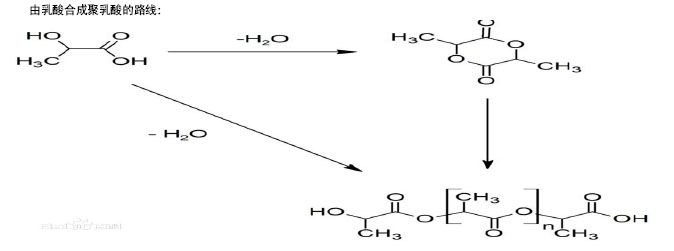
2.2 人工合成高分子 2.2.1 聚乳酸及其复合物 聚乳酸是以乳酸为单体化学合成的一类聚合物,它有3种构型:聚右旋乳酸、聚左旋乳酸和聚消旋乳酸。根据材料降解及力学性能分析,晶态聚左旋乳酸和聚右旋乳酸适宜于骨折固定,但由于它们具有较高的结晶度,易致迟发性组织反应,且降解吸收时间较长不利于骨长入[22],而聚消旋乳酸为非晶态,无迟发性组织反应,降解时间短,骨修复干扰小,故用作骨修复材料的大多是聚消旋乳酸。聚乳酸已被美国FDA批准为生物降解性医用材料,是当前仿生细胞外基质中最受重视的生物材料之一[23],其优点主要表现为:①生物可降解性好,能在人体内微环境中完全降解生成二氧化碳和水。②机械性能及物理性能良好。③组织相容性好,不对周围组织产生毒副作用,也不引起强烈的排斥反应。但聚乳酸容易降解,产生酸性物质,从而易引起炎症反应,有可能改变新生骨的机械强度,故聚乳酸适合于制作复合材料,例如将聚乳酸材料与纳米羟基磷灰石复合制备聚乳酸/纳米羟基磷灰石复合材料,可有效改善聚乳酸植入体内后的酸性环境,有利于新生骨组织的生长,达到良好的治疗效果[24]。 聚乳酸与聚羟基乙酸按照一定比例聚合而成的聚乳酸聚乙醇酸共聚物,既保留了聚乳酸的优点又提高了材料的降解速度和力学强度,已被广泛地应用于骨、软骨、血管、神经及皮肤等组织的修复。聚乳酸聚乙醇酸共聚物在体内的降解时间与骨骼修复周期相似,所以聚乳酸聚乙醇酸共聚物仅在骨修复过程中起作用,在骨修复完后已完全降解,且在降解过程中聚乳酸聚乙醇酸共聚物的强度逐渐下降,应力可转移至骨折部位,刺激成骨细胞生长,促进骨愈合。但聚乳酸聚乙醇酸共聚物材料在应用中也出现了一些问题,如聚乳酸聚乙醇酸共聚物降解过程中产生的酸性产物可致材料植入部位出现无菌性炎症,这个问题有待解决。 2.2.2 聚己内酯 聚己内酯有组织相容性强、生物降解速度快和通透性好,易于塑形,价格低廉等优点,因此研究甚多[25]。艾合麦提·玉素甫等[26]发现聚己内酯与骨界面没有出现无菌性积液及骨质溶解,随着聚己内酯的降解有新骨生长,局部代谢活跃,术后出现纤维组织和松质骨交织在一起的情况,表明聚己内酯具有良好的组织相容性,且在体内骨缺损修复中与骨组织有良好的骨引导能力,为今后进一步研究和探讨提供了理论依据。"

2.3 无机材料 2.3.1 生物降解类陶瓷 生物降解类陶瓷主要指磷酸三钙(A-TCP及B-TCP )及其混合物等磷酸钙陶瓷,其成分与骨矿物类似,植入体内后可发生陶瓷生物降解。目前应用较为广泛的为β-磷酸三钙,它具有良好的生物相容性和骨传导作用,生物降解性优于羟基磷灰石,是一种非常理想的、临床应用前景十分诱人的硬组织缺损修复材料。侯喜君等[27]发现骨缺损部位植入β-磷酸三钙煅烧骨试件后,实验动物的切口愈合良好,在术后4周骨缺损周边开始形成新骨,且随着时间的延长逐渐增多,术后12周时材料中心部位也可见新骨长入,材料逐渐降解。杨华清等[28]研究表明成骨细胞复合骨β-磷酸三钙成骨能力强,β-磷酸三钙材料来源丰富,可根据需要填充不同尺寸和形状的骨缺损,能用于修复各种形状的骨缺损,是一种具有高效成骨活性的植骨材料。 2.3.2 羟基磷灰石 羟基磷灰石是天然骨无机盐的主要成分,具有良好的生物相容性、骨传导性,被视为骨缺损修复的理想材料,尤其是纳米级的羟基磷灰石,与天然骨中的无机成分近似,引入到复合材料中可使材料在力学和生物学方面具有更大的优越性和应用潜力,并且其机械强度好,细胞亲和性佳,体内降解速率快,可很好地填充骨缺损并进行骨传导,是一种可吸收的人工骨材料[29]。大量实验证明纳米羟基磷灰石及其复合材料无明显细胞毒性、无免疫原性,不仅可以起到支撑作用,还可通过药物缓慢释放抑制细菌及肿瘤细胞生长,促进骨折愈合。张文志等[29]探讨纳米羟基磷灰石/聚酰胺66(n-HA/PA66)复合人工椎体在颈椎前路次全切除术中应用的短中期临床疗效。他们自2008年5月至2009年6月对44例脊髓型颈椎病行前路椎体次全切除、椎管减压、纳米羟基磷灰石/聚酰胺66复合人工椎体植骨融合+钢板内固定术治疗,以JOA评分改善率评价神经功能恢复情况,并依据X射线片判断椎间稳定性和融合情况。结果显示本组无术中并发症,伤口均一期愈合。患者获随访12-26个月,症状均明显改善,JOA评分由术前(6.4±1.8)分提高到术后(15.2±1.5)分,JOA改善率83.0%,优良率86.4%,问卷调查满意度97.6%。X射线检查证实无人工椎体移位、下沉,融合率100%,证实纳米羟基磷灰石/聚酰胺66复合人工椎体具有良好的生物相容性及安全性,是一种较理想的骨移植材料,适用于颈椎病前路次全切除术中。 目前纳米羟基磷灰石应用非常广泛,如复合纳米羟基磷灰石材料、载抗生素类纳米羟基磷灰石复合材料、载纳米金属类纳米羟基磷灰石复合材料、载促骨愈合类纳米羟基磷灰石复合材料及载抗肿瘤药物类纳米羟基磷灰石复合材料等,但它也有其自身的缺点,如脆性高、韧性差、强度低等[30]。 2.3.3 珊瑚及乌贼骨 珊瑚的主要成分为CaCO3和少量有机质,强度与人的松质骨相似,为管束状结构,纵向的管道间有大量横向连接孔,孔隙直径190-230 μm,孔隙率为40%-50%,没有盲孔,很适合骨单位内向生长。生物珊瑚的三维结构有利于成骨细胞的生长、增殖,有利于细胞和体液在孔道内流动,有助于组织代谢,并保证长入材料深部组织的营养供应,故被用于临床骨缺损的修复。但孟志斌等[31]发现天然珊瑚在体内的降解速度快于骨缺损的修复速度,降解过快,缺损区即会失去支架作用,不利于骨缺损的完全修复,且珊瑚无骨诱导活性,只能单纯作为支架,骨折修复速度较慢。目前珊瑚主要用于复合材料,如珊瑚羟基磷石灰具有成骨的潜力,其骨传导作用效果非常理想,而且无任何免疫原性和毒性,生物相容性好,原材料来源丰富,可弥补生物珊瑚的不足。郝思春等[32]以珊瑚为支架,接种兔骨髓基质干细胞进行诱导分化,成功的修复了骨缺损,推断如结合珊瑚的表面修饰、生长因子及基因疗法等应用,则更具广阔的应用前景。 乌贼骨的化学成分主要为碳酸钙,具有良好的骨活性和组织相容性,作为骨组织支架材料有着良好的天然条件。通过水热法可将乌贼骨转变成为羟基磷灰石结构,转变后不仅保持了原来的三维通道结构,而且具有丰富的微球构成,这些微观结构变化增加了其表面积和生物活性,有利于细胞吸附和血管长入,成为一种新型的骨组织支架材料。 2.4 纳米材料 纳米材料是指材料颗粒的直径在 100 nm以下,当一种物质改变到纳米级的结构单元,其物理、化学特性已和原来在微观和宏观状态下迥然而异。纳米材料具有以下优点:生物降解性好,因其可增加材料表面的粗糙度,减少表面的大小及孔隙的直径,可使材料的溶解性提高;组织相容性好,它可吸附更多的细胞在材料表面,提高蛋白质的吸附作用,进而提高其组织相容性;促进骨再生,纳米材料内部的孔隙(100-1 000 µm)可使新骨穿过长入种植体表面,通过种植体内互通的小孔(100 µm)和微孔(<10 µm)可交换液体并传递营养,从而促进骨再生;纳米颗粒直径(100 nm)可使细胞介导的种植体吸收变得更加容易,孔隙和亲水性使血液、骨髓和营养成分容易进入到种植体内部。目前常用的主要是一些复合材料,如纳米羟基磷灰石/胶原材料、纳米羟基磷灰石/聚乳酸纳米复合材料、纳米羟基磷灰石/壳聚糖/羧甲基纤维素三元复合骨修复材料、纳米骨浆、纳米羟基磷灰石-聚羟基丁酸戊酯/聚乙二醇人工骨等,这些复合材料在临床应用中都体现了其优势,显示出广阔的应用前景,随着纳米技术的发展,将会出现新一代的纳米材料,为骨缺损修复提供更好的选择。"

| [1] 刘岩,马信龙.人工骨修复材料及金属钛材料在骨组织工程中的应用[J].中国组织工程研究,2012,16(12):2229-2232.
[2] 张志宏,刘志礼,高志增,等.骨修复替代材料修复骨缺损的选择与应用[J].中国组织工程研究,2012,16(52):9836-9843.
[3] 马育林,戴如春,盛志峰,等.骨细胞密度对骨生物力学性能的影响[J].中华老年医学杂志,2009,28(6):500-504.
[4] 辛雷,苏佳灿.人工骨修复材料的现状与展望[J].创伤外科杂志, 2011,13(3):272-284.
[5] 蒋挺大.甲壳素[M].北京:化学工业出版社,2003:1-4.
[6] Kim IY,Seo SJ,Moon HS,et al.Chitosan and its derivatives for tissue engineering applications.Biotechnol Adv.2008;26(1): 1-21.
[7] 徐政,顾其胜,侯春林.实用生物医用材料学[M].上海:上海科学技术出版社,2005:127-128.
[8] VandeVord PJ,Matthew HW,Desiwa SP,et al.Evaluation of the biocompatibility of a chitosan scaffold in mice.J Biomed Mater Res.2002;59(3):585-590.
[9] Aspden TJ,Mason JD,Jones NS,et al.Chitosan as a nasal delivery system:The effect of chitosan solutions on in vitro and in vivo mucociliary transport rates in human turbinates and volunteers.J Pharm Sci.1997;86(4):509-513.
[10] 宋雪莲,于静涛,刘扬,等.壳聚糖在骨组织工程中应用研究进展[J].中国实用口腔科杂志,2013,6(5):306-310.
[11] No HK,Park NY,Lee SH,et al.Antibacterial activity of chitosans and chitosan oligomers with different molecular weights.Int J Food Microbiol.2002;74(1/2):65-72.
[12] Mi FL,Shyu SS,Wu YB,et al.Fabrication and characterization of a sponge-like asymmetric chitosan membrane as a wound dressing.Biomaterials.2001;22(2):165-173.
[13] Monica S,Anna T,Luca S,et al.Collagen based scaffold for biomedical applications.J Biotechnol.2010;150:29.
[14] 佟刚,雷静,钟翠红,等.不同PH与蛋白含量的胶原海绵植入缺损骨组织部位的疗效及安全性考察[J].生物医学工程学杂志,2012, 29(6):1125-1130.
[15] 杨春蓉,王迎军,陈晓峰.纳米羟基磷灰石/胶原/磷酸丝氨酸仿生复合骨组织工程支架材料的制备及表征[J].中国科学杂志,2013, 58(3):267-271.
[16] 李娟,郑闱颖,卢岩,等.骨形成蛋白-2基因修饰的β磷酸三钙/胶原复合材料修复颅骨缺损[J].材料科学与工程学报, 2013,31(2): 248-252.
[17] Pei M,He F,Boyce BM,et al.Repair of full-thickness femoral condyle cartilage defects using allogeneic synovial cell-engineered tissue constructs. Osteoarthritis Cartilage. 2009;17(6):714-722.
[18] Abiraman S,Varma HK,Umashankar PR,et al.Fibrin glue as an osteoinductive protein in a mouse model. Biomaterials. 2002;23(14):3023-3031.
[19] Ornelas L,Padilla L,Di Silvio M,et al.Fibrin glue: an alternative technique for nerve coaptation-Part I. Wave amplitude, conduction velocity, and plantar-length factors.J Reconstr Microsurg.2006;22(2):119-122.
[20] 姚旺祥,马安,朱六龙,等.浓缩自体骨髓复合纤维蛋白胶修复兔桡骨陈旧性骨缺损[J].中国医学科学院学报,2011,33(4):387-392.
[21] 肖裕华,李绍琴,潘文峰,等.纤维蛋白胶复合骨形态发生蛋白与VEGF修复兔桡骨缺损的实验研究[J].实用临床医学, 2013, 14(6): 17-19.
[22] Ignatius AA,Betz O,Augat P,et al.In vivo investigations on composites made of resorb able ceramics and poly( lactide) used as bone substitutes.J Biomed Mater Res. 2001;58(6): 701-709.
[23] Bohner M. Resorbable biomaterials as bone graft substitutes. Mater Today.2010; 13(1):24-30.
[24] Shen L,Yang H,Ying J ,et al. Preparation and mechanical properties of carbon fiber reinforced hydroxyapatite/ polylactide biocomposites.J Mater Sci Mater Med.2009; 20(11):2259-2265.
[25] Matthew R,Eric F,Allan GA,et al.Cell attachment and proliferation on novel polycaprolact on efibres having application in soft tissue engineering.Eur Cells Mater.2002; 4(2):62-63.
[26] 艾合麦提•玉素甫,陈统一,陈中伟,等.可降解聚己内酯修复骨缺损的实验研究[J].中国修复重建外科杂志,2005,19(6):439-442.
[27] 侯喜君,王春华,李 霖,等.β-磷酸三钙煅烧骨修复兔股骨远端骨缺损[J].中国组织工程研究,2013,17(3):400-406.
[28] 杨华清,张明宇,党晓谦,等.复合同种异体成骨细胞的β-磷酸三钙人工骨修复桡骨缺损[J].中国组织工程研究, 2013,17(34): 6061-6066.
[29] 张文志,王潇,段丽群,等.纳米羟基磷灰石/聚酰胺66 复合人工椎体在颈椎病前路椎体次全切除术中的临床应用[J].中国骨与关节损伤杂志,2012,27(9):783-785.
[30] Swetha M,Sahithi K,Moorthi A,et al. Synthesis, characterization, and antimicrobial activity of nano-hydroxyapatite-zinc for bone tissue engineering applications. J Nanosci Nanotechnol.2012;12(1):167-172.
[31] 孟志斌,李德豪,周健强,等.可吸收珊瑚羟基磷灰石与天然珊瑚修复骨缺损的组织学及影像学分析[J].生物骨科材料与临床研究, 2007,4(5):10-15.
[32] 郝思春,蒋建农,周建刚,等.兔骨髓基质干细胞复合珊瑚修复兔骨缺损的实验研究[J].南京医科大学学报,2006,26(9):846-848. |
| [1] | Li Xuan, Shi Chun-lai, Wang Xue-yan, Zhang Ming. Cardiovascular stent biocompatibility: bibliometric analysis of the international developmental trend [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(8): 1267-1271. |
| [2] | He Yan-ping, Ma De-chun, Li Lei, Zhang Li, Zheng Shuang, Dong Ke-xin. Hemocompatibility and surface modification of artificial blood vessel materials [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(8): 1272-1276. |
| [3] | Wu Qiong, Hu Wei-ping. Clinical common problems after restoration with telescopic crown-retained removable partial dentures [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(8): 1301-1305. |
| [4] | Li Bing-ting, Jia Ying-zhen, Liu Zhi-fang, Song Yuan, Hou Xiao-wei. Effect of freeze-dried bone xenograft and platelet-rich fibrin compound on osteogenesis and osseointegration of alveolar bone defects [J]. Chinese Journal of Tissue Engineering Research, 2014, 18(52): 8376-8381. |
| [5] | Wang Xiao-dong, Zhang Yong-hong. Preparation and performance of recombinant human bone morphogenetic protein-2-poly(hydroxybutyrate-co-hydroxyoctanoate) nanospheres [J]. Chinese Journal of Tissue Engineering Research, 2014, 18(52): 8405-8408. |
| [6] | Lu Miao, Wang Xiang-ming, Wang Sen, Zhou Chuan-wei. Effects of different drug eluting stents on inflammatory factors in elderly patients with non-ST-segment elevation acute coronary syndrome [J]. Chinese Journal of Tissue Engineering Research, 2014, 18(52): 8414-8419. |
| [7] |
Wang Xue-ming, Xing Chang-min, Li Nan.
Preparation methods and in vitro release of Resina Draconis-loaded biodegradable polymeric hollow nanoparticles
|
| [8] | Feng Chao, Li Zhe, Lv Xiang-guo, Xu Yue-min, Fu Qiang. In vitro preparation and biochemical evaluation of oxygen generative keratin/silk fibroin compound biomaterial [J]. Chinese Journal of Tissue Engineering Research, 2014, 18(52): 8480-8486. |
| [9] | Li Tian-shi, Zeng Wen-ni, He Jun-jun. Chitin and its derivatives inhibit scar formation [J]. Chinese Journal of Tissue Engineering Research, 2014, 18(52): 8504-8508. |
| [10] | Ma Song-feng, Cao Hui, Zheng Feng, Qiao Jun, Zhang Guo-ming. Concomitant cardiac valve replacement and coronary artery bypass grafting [J]. Chinese Journal of Tissue Engineering Research, 2014, 18(5): 699-704. |
| [11] | Ruan Guang-ping, Yao Xiang, Liu Ju-fen, Shu Fan, He Jie, Yang Jian-yong, Pang Rong-qing, Pan Xing-hua. Role of human umbilical cord mesenchymal stem cells: cell transplantation, immuoregulation and target cells [J]. Chinese Journal of Tissue Engineering Research, 2014, 18(41): 6714-6718. |
| [12] | Lu Hua-ding, Lian Li-yi, Chen Ming-wei, Dai Yu-hu. Cloning and expression of Asperguillus endo-chitosanase gene in Escherichia coli [J]. Chinese Journal of Tissue Engineering Research, 2014, 18(34): 5490-5496. |
| [13] | Fan Zhong-bao, Rong Da-qing, Liu Qing-feng. Prolene hernia system versus polypropylene mesh plug in tension-free hernia repair [J]. Chinese Journal of Tissue Engineering Research, 2014, 18(34): 5535-5539. |
| [14] | Li A-li. Absorbable ligating clip in laparoscopic hysterectomy [J]. Chinese Journal of Tissue Engineering Research, 2014, 18(34): 5561-5565. |
| [15] |
Zeng Xian-li, Yang Chun-lu.
Repairing critical-size segmental defects: morphology of tissue engineering bone scaffolds and its effects on cell loading
|
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||