Chinese Journal of Tissue Engineering Research ›› 2020, Vol. 24 ›› Issue (2): 312-319.doi: 10.3969/j.issn.2095-4344.1430
Previous Articles Next Articles
Training variables and autonomic nervous system adaption
Chen Yanlin1, Hu Fei2, Xu Shengjia3
- 1Department of Physical Education, Hohai University, Nanjing 210098, Jiangsu Province, China; 2Jiangsu Research Institute of Sports Science, Nanjing 210014, Jiangsu Province, China; 3Research Center of Military Physical Training, the PLA University of Science and Technology, Nanjing 211101, Jiangsu Province, China
-
Received:2019-02-20Revised:2019-03-02Accepted:2019-04-19Online:2020-01-18Published:2019-12-25 -
Contact:Xu Shengjia, Master, Lecturer, Research Center of Military Physical Training, the PLA University of Science and Technology, Nanjing 211101, Jiangsu Province, China -
About author:Chen Yanlin, Lecturer, Department of Physical Education, Hohai University, Nanjing 210098, Jiangsu Province, China -
Supported by:the Military Project of Graduates, No. 2016JY374
CLC Number:
Cite this article
Chen Yanlin, Hu Fei, Xu Shengjia. Training variables and autonomic nervous system adaption[J]. Chinese Journal of Tissue Engineering Research, 2020, 24(2): 312-319.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
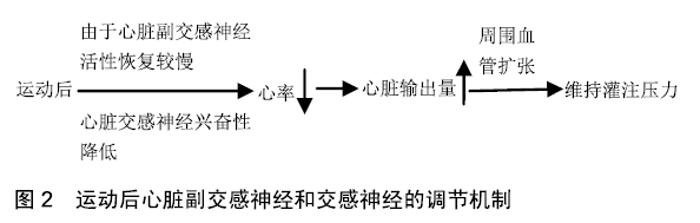
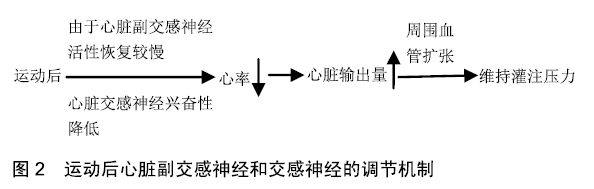
2.1 运动中心脏自主神经系统调节 研究认为,当开始运动指令发出后,高级脑中枢(中枢指令)释放“前馈”信号下行至脊髓心血管中枢,重置动脉压力感受器反射,将其升至更高水平,通过降低心副交感神经活性(副交感神经撤离)触发心率快速增加,同时来自肌肉机械性感受器的快速“反馈”信号促进副交感神经撤离,此外,心肺压力感受器的负荷增加(由于肌肉泵作用使得静脉回心血量增加)可能也会诱导心副交感神经撤离,以及运动开始时心交感神经活性降低[11]。随后,心副交感神经和心交感神经通过整体运动强度持续对心率进行调节。作为心脏自主神经的2个分支,始终保持两者的动态平衡转换,如安静状态和低强度运动中副交感神经占优,而在大强度运动中,主要由交感神经控制[13]。当运动强度进一步增加时,压力反射感受器逐渐重置,肌肉中代谢受体传入“反馈”信号触发更强的心副交感神经撤离,以及心交感神经的激活。而当运动强度从中等强度增加至最大强度时,激活交感肾上腺,通过正性变时效应、正性变力效应和正性变传导效应,促进去甲肾上腺素分泌,与心肌细胞膜上的肾上腺素能β受体结合,进一步增加心交感神经活性,诱导心肌收缩能力和心率增加[11-13]。 运动中心脏自主神经的调节,通常由多重神经机制调控,尤其是交感神经活性流出,通过复杂的交互控制动脉血压和血流动力学变化,满足运动中机体代谢需求。当前研究表明,主要涉及中枢指令、运动压力反射、动脉压力感受器反射和心肺压力反射4个方面[14-15]。研究发现,当机体运动开始时,心率同时迅速增加,这可能与副交感神经活性降低有关(或者是抑制中枢的正常抑制作用)。此外,在运动早期,代表心副交感神经活性的心率变异性衍生指标降低,与此相反,进行骑车运动开始阶段,β-肾上腺素阻滞并不影响心脏加速程度,提示此时交感神经活性的影响最小[11,14-15]。研究结果表明,早期心率对运动的反应主要是通过心脏副交感神经撤离介导,而交感神经的调节需要更长的潜伏期。这一观点在随后的研究中得到证实,刺激心脏副交感传出神经引起心率迅速下降,而对交感神经刺激后,反应稍加迟缓(3-6 s)[14-15]。 TSUCHIMOCHI等[16]认为,运动开始时,心交感神经活性的增加导致心率增加。这一结果在活体动物实验中得到印证,在跑台运动开始7 s内,心交感神经活性迅速增加168%-297%,但这一结果尚无在人体试验中得到实证。此外,用于直接评估人体心交感神经活性的技术不能提供足够的瞬时分辨率捕捉起效反应的动力学反应(如心脏血浆去甲肾上腺素溢出)。也有研究认为,运动开始的心率增加,是由迷走神经活性降低和位于骨骼肌和肌腱内的本体感受器受到强烈的信号刺激,并且随着运动时间的增加,交感神经活性逐渐被激活,体内发生β-肾上腺素能刺激,加之变时效应,此时血液中儿茶酚胺浓度的增加,是诱导心率增加的主要原因,促进心肌需氧量提高,通过Bowditchl阶梯效应,进行性地促进心室收缩[9,17]。此外,受到β-肾上腺素能刺激,又通过正性收缩能效应,提高心肌的收缩能力。运动时,骨骼肌小动脉代谢性扩张,而外周阻力降低[17]。与此相反,由于收缩能力增加,收缩期血压上升,壁应力提高,后负荷增加,可通过Anrep效应,提高心肌收缩能力[17]。原因可能是左室壁应力的增加,将作用于心肌的牵张受体,增加胞质溶胶中的Na+,随之通过Na+-Ca2+泵,提高胞质溶胶中的Ca2+,心肌收缩力总效应提高,促进心肌的松弛效应,提高心血管系统功能[10,16-17]。 2.1.1 运动强度 研究表明,在持续性大肌群参与的动力性运动中,心率和运动强度几乎呈线性相关[15]。马继政等[18]研究发现,优秀运动员和普通大学生进行相同运动负荷的运动,前者最大心率相对较低,而随着运动负荷递增,每搏量相对较高。研究还发现,在低强度时,两者的心输出量基本一致,而在高强度下,前者心肌收缩力更强,同时,运动时交感神经的兴奋,会导致去甲肾上腺释放增多,降低胞浆内肌钙蛋白对Ca2+的亲和力,促进两者的解离速度,诱导肌质网重新摄取Ca2+和肌膜上的Na+-Ca2+交换,使舒张期内胞浆Ca2+浓度下降较快,心肌舒张加速[10]。研究表明,在进行全身性运动时,血液在内脏器官、骨骼肌和肾脏进行重新分配,增加骨骼肌血流量,降低肾血流量和肾小球滤过量,肾小球滤过量降低会迅速激活肾素-血管紧张素-醛固酮系统,调节体激素水平发生适应,如长期训练后诱导的热效应促进体内血容量和心脏舒张末容积增加,β-肾上腺素功能提高以及促心脏自主神经功能的调节能力增加[17];长期训练后,机体血液中去甲肾上腺素浓度和β肾上腺素受体密度的变化,可能会导致心脏自主神经调节功能紊乱。 一般认为,当运动强度增加,尤其是心率超过100次/min时,心副交感神经撤离对心率反应的调节作用增强,而随着运动强度的增加,调节效益逐渐降低。相反,随着运动负荷的增加,心交感神经刺激对运动中心率升高的调节作用逐渐增加[15,19]。研究认为,在较高的运动强度下β-肾上腺素能阻滞显著地减弱了心率反应的大小,这表明心交感神经神经活性和血液循环中的儿茶酚胺在该负荷下起着非常重要的作用[15,19]。运动中,与从中等强度到大强度运动相比,高频功率谱密度出现运动强度依赖性降低,表明心脏副交感神经进行性撤离,这一过程在从安静状态到低强度运动时表现更为明显,而在心脏移植患者中并无心脏自主神经调节的变化[19-20]。前期研究发现,进行静力性运动时,运动中内部负荷(心率)基本一致,而外部负荷(负重)增加,但整体心率变异性指标变化相似[21];同样的,在持续跑和负重跑的研究中发现,运动中两者的心率变异性指标变化一致[22];3种不同强度的力量训练中,心脏自主神经应答存在差 异[23];在组合训练(力量训练和耐力训练)实验中,运动强度不影响运动中心率变异性指标的变化[24];而在大强度的有氧耐力和无氧耐力组合练习中,研究发现运动中心脏自主神经功能应答相似[25]。相似的研究发现,当运动达到一定强度时,RR间期达到最小值(<5 ms),心率为120-140次/min,或者50%-60%VO2 max,心率变异性时域指标和频域指标均会达到一个最小阈值,即使强度在增加,心率变异性指标可能并不会变化或小幅度增加[11,27]。因此,研究认为运动中心脏自主神经功能变化可能具有强度依赖性。 2.1.2 运动时长 一项系统性研究表明,持续运动时间的增加,运动中心率可能保持稳定,即内在负荷保持不变,在长时间运动中体温调节因素(尤其是体液丢失)可诱导心血管循环发生转换,促进血压稳定和血液重新分配,进而影响自主神经的调节。KAIKKONEN等[28]研究久坐不动女性进行不同强度不同持续时间训练中频域指标的变化,运动强度为低强度(45%VO2 max)和高强度(77%VO2 max),运动持续时间分别为38 min和70 min,以及30 min和60 min。结果显示,尽管持续时间增加至一倍,但不同强度下运动中心率变异性指标无显著变化。而高水平运动员在66%VO2 max强度下持续运动时为20 min和90 min,持续运动时间延长至300%-400%,运动中心率变异性指标仍无明显变化[28]。PICHON等[29]进行急性短时训练对运动中心率变异性频域指标影响,受试者进行运动强度为60%和70%VO2 max持续时间为 3 min、6 min和9 min,以及强度为80%VO2 max持续时间为3 min和6 min的运动,结果发现运动中3 min组高频成分(HF)高于其他2组,低频成分(LF)随着持续时间增加而降低,而低频/高频比值(LF/ HF)无明显变化。然而,3次运动强度均达到中等至大强度,运动期间心率有着明显差异,在60%VO2 max时心率分别为143次/min、161次/min和167次/min。这些差异随着运动强度的增加而增加,原因可能是运动开始时心率动力学和达到稳态时间所决定的。同样地,受试者进行中等强度(60% VO2 peak)训练中心率变异性指标SDRR、RMSSD、低频成分和高頻成分均显著降低[11]。因此,更长的持续运动时间可能降低运动中心率变异性,也有少量研究发现运动中心率变异性指标随着心率增加而增加,这可能与没有达到强度剂量的最小值。运动中心率增加(代表内在负荷的增加),在低强度下抑制迷走神经活性引起心率变异性降低,随着强度增加,交感神经逐渐占优同样表现为较低的心率变异性,而随着运动时长增加,迷走神经撤离可能是运动中较低心率变异性的主要原因。因此,自主神经系统在运动中控制、调节心血管功能,以期满足运动中机体代谢需求[11]。 2.1.3 运动形式 有研究表明,运动形式可能影响运动中心自主神经功能的调节。但关于动态运动中不同运动形式对心率变异性影响的研究较少,这可能与实验方案的复杂性和评价指标较难选择有关。有研究发现,在相对运动强度一致运动中,与下肢骑车运动相比,上肢曲柄运动心率峰值可能会下降10-20次/min;在相同比率能耗或运动频率的情况下,进行上肢曲柄运动比下肢骑车运动引起更高的心率[30];此外,相同强度下的上肢练习诱导的生理反应(如心率或VO2一致),而下肢练习诱导的生理反应存在差异[31]。 相似的,TULPPO等[32]采用SD1和SD1n(从RR间期分离出SD1)作为副交感神经指标,评估递增式上肢运动与下肢运动的心率变异性变化。在2种运动中,心率变异性指标随着强度的增加而降低,直到维持在一个中等功率输出(50%VO2 max)。低于靶功率,与下肢锻炼相比,进行上肢锻炼运动心率较高而心率变异性较低。研究者认为,与递增负荷的下肢运动相比,进行上肢递增负荷运动导致更快的迷走撤离[32],心率变异性与心率呈负关系,结果提示,不同运动形式之间无显著差异[32]。但这一结果与LEICHT等[31]研究发现不一致,该研究认为,进行下肢运动(骑车)、上肢运动(曲柄运动)和全身性运动(跑步)的心率变异性应答满足心率需求,骑车运动和跑步VO2绝对值相似,但低于曲柄运动,主观感觉疲劳程度量表(RPE)值较高;忽略心率变化,骑车运动和跑步运动的时域、频域指标均相似,但显著高于曲柄运动,结果证实运动形式影响心率变异性变化,不受潜在的心率影响,而研究对象、实验方法可能影响实验结果。 COTTIN等[33]评估2种不同的高强度运动形式(骑车和柔道),运动中心率相似(高于180次/min),但频域指标和Poincaré心率变异性指标高于柔道。由于较高的心率,非神经机制可能影响实验结果,如呼吸对心率变异性产生极大影响。此外,代谢因素对心率反应以及激素应激预期应答,均代表不同运动形式引起机体内部的变化。GONZALEZ-CAMARENA等[34]比较动力性运动(骑车30% vs 60%VO2 max)和静力性运动(30%MCV膝关节等长收缩)心率变异性的变化。心率变异性(时域和频域指标)指标在动态运动中降低,尽管在运动中心率并不相等。胡斐等[21]研究显示,静力性训练(负重站立)中,外部负荷增加,整体心率变异性呈下降趋势,表明心脏自主神经功能发生调整。WEIPPERT等[35]也发现相似的变化,评估静力性运动(仰卧位膝关节等长收缩)和动力性运动(仰卧位骑车)心率变异性的变化,基于相似的低强度心率水平(88次/min)。心率变异性指标中反应整体变异性的SDRR以及代表心副交感神经活性的RMSSD、高頻成分和SD1均显著高于动力性运动(受试者努力程度、血压和心率收缩压乘积)。 运动中心率变异性指标变化可用于评估个体的体适能水平,而由运动训练引起的机体疲劳或机体适应性变化及其机制尚不清楚。研究认为,运动中心率变异性指标变化具有可能运动强度依赖性[36]。当运动强度低于第一通气阈时,心率变异性指标变化更多的是由迷走神经调节占主导,在更大强度时,呼吸波动决定心率变异性变化,尤其是当运动进行至呼吸补偿点后[37]。因此,在研究运动中心率变异性变化与自主神经系统的关系时,运动强度可能是关键因素。此外,运动形式(力量练习、耐力练习或力量和耐力组合练习)、持续时间等可能也会影响运动中心率变异性变化。 2.2 运动后心脏自主神经系统调节 运动停止后,中枢指令不再释放“前馈”信号,以及骨骼肌中机械感受器“反馈”信号消失重置动脉压力反射至一个较低的水平,共同调节运动后即刻心率降低,这一过程可能与心副交感神经活性增加有关。因此,“快速恢复期”(如运动后即刻)心率恢复通常被认为是副交感神经重新激活[38-39],但也有一些研究提示交感神经也参与其中调节[40-41]。随着恢复时间的持续增加,心交感神经逐渐撤离以及心副交感神经逐渐重新激活共同调节“慢速恢复期”的心率降低。在“慢速恢复期”自主神经调节主要是受运动强度引起的代谢物清除(如代谢反射输入信号降低)和循环中的儿茶酚胺降低的共同影响,而体温调节因素(温度感受器传入/血流再分布)也可能参与其中调节。 运动停止即刻,心率通常会在数分钟内逐渐下降,其具体动力学变化取决于先前运动的强度和持续时间[15,42]。有研究发现,心脏移植患者心率恢复延迟,表明心脏自主神经传出活性在恢复期具有一定的作用。运动后心率迅速恢复归因于心脏副交感神经活性的迅速恢复,而这一过程并不受β-肾上腺素阻滞的影响[43]。此外,耐力运动员的心脏副交感神经活性增加,表现出较快的心率恢复[15,42-43](见图2)。 "

现有研究显示,心率恢复动力学已被证明具有预后价值,恢复功能不佳(如在仰卧位恢复期1 min内,心率峰值下降值<12次/min)是预测心血管疾病死亡率的重要指标之一,这可能与心脏副交感神经活性的心脏保护机制作用有关[15,44]。 2.2.1 动脉压力反射 有研究认为,动脉压力反射是影响恢复期心脏自主神经功能的关键因素[45]。运动后出现的低血压症,主要原因就是动脉反射被抑制,导致交感神经流出,因而副交感神经激活被延迟[45]。运动后动脉压降低,涉及复杂的调节,如动脉压力反射感受器重置、组胺释放和受体激活等因素。一般来说,中等强度并持续的全身动力性运动(如耐力性运动),血管传导能力(或血管阻力降低)增加的幅度大于心输出量增加的幅度,意味着血管舒张是减压的关键[45]。然而,在直立位被动恢复的情况下,依赖肢体的血液引力池中肌肉泵作用降低减少静脉回流、中心静脉压和心脏前负荷,会导致严重的低血压和晕厥,此时迷走神经张力是否与之有关,仍有待进一步研究[9,46]。持续运动后血管舒张,主要发生在先前活动的骨骼肌的血管床内,而在非参与运动骨骼肌内的作用较小,内脏、皮肤和大脑、血管床中的血管传导相对于运动前保持不变。研究发现,运动后血管舒张可持续数小时,并且这一现象有中枢神经机制(动脉压力反射重置)和局部血管舒张机制共同介导[45]。运动后恢复期,动脉压力感受器发生转换并撤离,即使在较低的血压下,交感神经活性降低。这与心率在恢复期的变化和R-R间期波动(如心率变异性)有关。有氧训练后心率快速恢复期可能完全依赖于副交感神经再激活,而在缓慢恢复阶段,认为是交感神经流出撤离,一般持续至运动后90 min[45,47]。非参与运动骨骼肌内的血管舒张可能通过重置动脉压力感受性反射,导致交感神经血管收缩降低。相反的,先前活动的骨骼肌中由于动脉压力反射重置、血管传导能力增加以及局部血管舒张基质释放,导致血管舒张,这一过程可能与组胺(通过组合高剂量组胺H1和H2受体拮抗剂)调节作用有关[45]。 相比与耐力运动,力量训练运动期间,心率具有一定的间歇性[45,47],动脉压力伴随心率的逐渐增加而产生大幅度快速波动。训练监控中发现,力量训练有显著的降压作用,尽管力量训练的手段、重复次数、运动负荷等存在差异,但力量训练之后动脉血压降低可持续数小时,主要是由于心搏量减少导致的心输出量减少[48]。研究认为,力量训练后血流动力学调节机制可能由中枢神经系统调节,可能与心脏迷走神经张力撤离有关[49]。研究表明,力量训练后的心迷走神经张力降低和心率增加,不足以维持每搏输出量的减少[40,44]。此外,动脉压力感受性反射缓冲血压降低的能力,因心血管压力反射敏感性降低而受到抑制[50]。在长期耐力训练个体中,非病理性的心肌肥大、左室舒张末舒张容积增加也可能促进运动后心率恢复[51]。 2.2.2 运动强度 最近已有研究表明不同运动强度对心率变异性恢复产生影响。一篇系统性回顾研究结果显示,较高的运动强度与cPNA-心率变异性指标较慢的恢复交感神经活性有关,尤其是经对数转换后的RMSSD和高頻成分指标[11]。另一些研究发现cPNA-心率变异性相似的结果,以及在大强度后导致较慢的心率和心率变异性恢复[52]。从机制角度来看,运动强度对心率变异性恢复的影响,这可能与非氧化能量的贡献量和运动后对肌肉代谢反射器的刺激有关[53]。 然而,运动强度的剂量效应仍不清楚,尤其是在中等和大强度运动后起初的10 min心率恢复。试验方案中运动强度不同,不同强度之间存在差异,但并不是所有的试验结果均表现出类似情况,研究认为,第一个通气阈值可能会区分于心率变异性恢复的自主“二值化阈值”,即进行低于该强度的运动与快速心率变异性恢复相关,高于此强度的运动后导致心率变异性恢复延迟,但这并不具有强度依赖性(至少在高水平运动员中)[11]。相反的,运动强度可能引起心率变异性恢复的等级效应(运动后1 h恢复期)。这与最近的研究结果是一致,该研究表明,在3种不同的运动强度下,运动后心率变异性应答程度均不相同[54]。 有研究证实,大强度运动后导致心率和心率变异性恢复减慢,需要更长的时间才能恢复[11],前期研究显示,先进行力量练习,随后进行有氧耐力练习,与有氧耐力练习先于力量练习的练习方式相比,组合训练中后者进行的运动强度可能影响运动后恢复期自主神经系统的调节[24]。前期研究发现,参与运动肌群和能量消耗影响恢复期心率和心率变异性的恢复[55]。于文兵等[23]进行3种不同强度(40%1RM、70%1RM和90%1RM)的急性力量训练,结果显示,在运动期间,RMSSD显著降低,不同强度之间无差异,但在恢复期最大力量组心率和RMSSD高于其他2组,结果提示运动后交感神经撤离较快,可能与副交感神经重新激活以及受试者个体有关。因此,运动强度、运动时间和运动形式,以及它们的交互效应,均可能会影响运动后心率和心率变异性应答。 2.2.3 运动时长 急性运动持续时间对心率变异性影响的研究相对较少,试验方案中需要对其他变量进行相对统一。SEILER等[56]研究发现,高水平耐力运动员进行60或120 min低强度跑(运动强度低于VT1,约60%VO2 max)后,在恢复期早期阶段(5-10 min),心率变异性(包括RMSSD)恢复至运动前水平,在4 h恢复期间,心率变异性指标没有明显影响,与4 h恢复期并无差异。这一结果与CASONATTO等[57]研究结果一致,该研究发现健康的受试者进行30 min或45 min的60%VO2 max的骑车运动,运动后恢复期持续60 min,而恢复期心率变异性指标(RMSSD、LF-nu、HF-nu以及LF:HF)并无差异。KAIKKONEN等[58]研究建议,增加即刻恢复期间心率变异性随时间效应变化的研究。该研究中,通过傅里叶转换法分析久坐不动女性运动后即刻恢复期心率变异性指标随时间变化。受试者进行低强度(45%VO2 max)和中等—高强度(77%VO2 max)跑步,持续时间分别为38 vs. 76 min和30 vs. 60 min。忽略运动强度对心率变异性恢复期的时间效应,任一运动强度下运动持续时间对恢复期心率变异性并无影响(恢复期从1 min持续到30 min)。 现有文献建议,运动持续时间翻倍增加并不改变运动后心率变异性恢复,KAIKKONEN等[59]研究表明,运动持续时间可能延长至300%-400%,才可能影响运动后恢复期心率变异性指标。该研究中,职业运动员分别完成20 min和90 min运动强度为66%VO2 max跑步练习,在15 min恢复期的开始3 min,较长的持续时间导致更低的Ln-LF、Ln-HF和Ln-TP。 2.2.4 运动形式 现有文献中,关于运动形式和恢复期心率变异性指标变化的实验研究较少,运动形式仅局限于有氧运动。前期研究结果显示,先力量后耐力的运动方案在恢复期交感活性和心率显著高于先耐力后力量的运动方案,研究推测,先力量后耐力的运动方案在恢复期心率恢复可能依赖于副交感神经重新激活,而先耐力后力量的运动方案恢复期心率恢复与心迷走神经撤离有关[24]。CUNHA等[60]研究发现,3种有氧运动形式:快走、骑车和跑步,在5 min快速恢复期,运动后较快的心率、RMSSD恢复速度,与较小的参与运动的肌肉量以及较低能量消耗(即骑自行车>步行>跑步)有关,研究认为,参与运动的肌肉量和/或能量消耗是运动后副交感神经再激活的决定因素。相似的,有研究证实,积极运动的青少年进行递增负荷值最大强度的曲柄运动和骑车运动,恢复期心率和心率变异性恢复更快[52]。这一结论与进行不同运动模式(如骑车vs.跑步和骑车vs.曲柄运动)后心率(并未测心率变异性)恢复一致[30,52]。这些研究均采用最大强度递增负荷运动,而进行次最大强度的不同形式运动后心率变异性恢复期变化尚不清楚。 研究表明,恢复期心率降低通常受到交感神经活性降低和副交感神经再激活的调节,而在训练干预后,通过副交感神经活性增加或交感神经调节降低促进恢复期心率恢复[61]。一些纵向研究证实上述自主神经活动,在静息状态下通过心率变异性指标,间接评估副交感神经活性,发现运动员比非运动员有更快的心率恢复,即快速恢复至自稳态[62]。运动后心率变异性变化被认为是副交感神经重新激活而交感活性降低的结果。在运动结束后即刻进行评估(0-5 min),运动后心率变异性受血浆肾上腺素水平、血乳酸浓度、以及血液中、骨骼肌和动脉氧耗产生的代谢应激累积诱导的血液酸中毒等影 响[62]。而动脉压力感受反射器活性,通常受到血压、血管舒张和代谢感受性反射(优化氧气运输至骨骼肌)累积影响[62-63],这些影响因素决定副交感神经重新激活水平,以及运动后心率变异性变化。也有研究认为,急性运动后即刻心脏副交感神经的重新激活可能很大程度上取决于骨骼肌和血液中应激代谢物的积累,而运动后间歇恢复期(1-48 h)心脏副交感神经活性很可能取决于运动引起的血浆容量的变化以及动脉压力反射[64]。因此,可以通过监控安静状态或运动后心率和心率变异性指标变化,依据个体反应给予下一次训练刺激[65]。 研究建议,对训练阶段进行整体的监控和评估,有助于对运动训练诱导心脏自主神经系统调节适应的认识和开展进一步研究[66]。运动后心率变异性指标变化,受多种因素影响,如血压调节、压力反射活动、年龄、体质量、体适能水平、训练水平、心理状态、中枢疲劳、液体丢失等,尤其是运动后代谢压力反射刺激,促进交感神经撤离和副交感神经再激活,以及影响副交感神经重新激活水平[67]。研究认为,相对运动强度增加,血液中酸液含量增加,代谢压力反射增加,导致更慢的心率恢复以及与迷走神经相关的心率变异性指标恢复,因此,评估心脏自主神经系统对心率恢复期的影响,建议只使用亚极量运动强度(≤第一通气阈值),可以有效避免代谢反射刺激[68]。大量的实验研究已经证实,运动强度可能是影响运动后即刻心率和心率变异性恢复的主要影响因素,但两者的强度剂量效应并不清楚。此外,不同运动形式、持续时间等训练学参数,以及它们的交互效应,均可能是影响恢复期心率和心率变异性变化的主要因素,但目前尚无一致的研究意见,仍有待进一步研究。此外,也有研究认为,随着运动强度的增加,心率变异性指标变化不能完全反应心交感神经活性,而采用心缩间期(Systolic time intervals,STI)输出量,如射血前期、左心室射血时间以及射血前期/左室射血时间比值,可以更有效的评估交感神经活性对心肌产生的影 响[11,69],这为探索运动诱导心脏自主神经调节适应机制提供新的路径,但仍需要进一步实验研究。 "

| [1] POWELL C, HERRING MP, DOWD KP, et al. The cross-sectional associations between objectively measured sedentary time and cardiometabolic health markers in adults-a systematic review with meta-analysis component. Obesity Reviews. 2017;19(3):381-386. [2] BERMEJO CA, ÁLVAREZ BC, MARTINEZ VV, et al. Association between physical activity, sedentary behavior, and fitness with health related quality of life in healthy children and adolescents: A protocol for a systematic review and meta-analysis. Medicine (Baltimore). 2017;96(12):e6407. [3] 马继政,孙飙,吕远远.运动性心肌肥大大鼠心肌蛋白差异表达研究[J].西安体育学院学报,2010,27(2):202-205. [4] 马继政,牛洁.大强度间歇训练心肌细胞分子适应机制[J].体育科技文献通报,2010,18(3):33-34. [5] 马继政,张仁祥,谷波,等.大强度间歇训练研究与进展[J].南京体育学院学报(自然科学版) ,2013,12(4):8-14. [6] 马继政. 运动诱导心脏保护机制[J].辽宁体育科技, 2009,31(3):29-31. [7] 马继政,孙飙,吕远远. IGF-PI3K-Akt信号通路在生理性心肌肥大中的作用研究进展[J].南京体育学院学报(自然科学版) , 2007,6(3):6-10. [8] CIPRYAN L.The effect of fitness level on cardiac autonomic regulation, IL-6, total antioxidant capacity, and muscle damage responses to a single bout of high-intensity interval training.J Sport Health Sci.2018; 7(3):363-371. [9] 孙飙,马继政.直立位递增运动负荷时左室收缩期血流动力学变化[J].中国康复医学杂志,2003,18(12):44-47. [10] 马继政,孙飙,牛洁.有氧运动和左室的舒张功能[J].中国临床康复, 2004, 5(6):1138-1139. [11] MICHAEL S, GRAHAM KS, DAVIS GM OAM. Cardiac Autonomic Responses during Exercise and Post-exercise Recovery Using Heart Rate Variability and Systolic Time Intervals-A Review.Front Physiol, 2017,29(8):301-307. [12] HANSEN J, SANDER M, HALD CF, et al. Metabolic modulation of sympathetic vasoconstriction in human skeletal muscle: role of tissue hypoxia. Jour Physio.2010; 527(2):387-396. [13] MICHELINI LC, O'LEARY DS, RAVEN PB, et al.Neural control of circulation and exercise: a translational approach disclosing interactions between central command, arterial baroreflex, and muscle metaboreflex[J]. Am J Physiol Heart Circ Physiol. 2015; 309(3): H381-392. [14] MUELLER PJ, CLIFFORD PS, CRANDALL CG, et al. Integration of Central and Peripheral Regulation of the Circulation during Exercise: Acute and Chronic Adaptations. Compr Physiol. 2017;8(1):103-151. [15] FISHER JP, YOUNG CN, FADEL PJ. Autonomic adjustments to exercise in humans.Compre Physiol, 2015; 5:475-512. [16] TSUCHIMOCHI H, MATSUKAWA K, KOMINE H, et al. Direct measurement of cardiac sympathetic efferent nerve activity during dynamic exercise. Am J Physiol Heart Circ Physiol. 2002;283(5): H1896-1906. [17] 孙飙,马继政.递增运动负荷时男性青年左室舒张期血流动力学变化[J].中国运动医学杂志, 2003,22(6):548-552. [18] 马继政,孙飙,张爱军,等. 运动负荷递增时优秀运动员心输出量和摄氧量之间关系的研究[J].南京体育学院学报(自然科学版), 2007, 6(2):7-10. [19] VESTERINEN V, NUMMELA A, LAINE T, et al.A Sub-maximal Running Test With Post-exercise Cardiac Autonomic and Neuromuscular Function in Monitoring Endurance Training Adaptation.J Strength Cond Res.2017; 31(1):233-243. [20] TAKAHASHI M, MATSUKAWA K, NAKAMOTO T, et al. Control of heart rate variability by cardiac parasympathetic nerve activity during voluntary static exercise in humans with tetraplegia.J Appl Physiol. 2007;103(5): 1669-1677. [21] 胡斐,王金之,黄佩玲,等.不同负重量站立30 min对健康青年心脏自主神经功能产生的影响[J].中国应用生理学杂志, 2017,33(2):193-196. [22] 王增刚,胡斐,徐盛嘉,等. 18 km中等强度负重行军对心脏自主神经功能产生的影响[J].军事体育学报, 2018,37(1):118-121. [23] 于文兵,高丽丽,李天义,等. 三种力量训练方案对健康青年心脏自主神经功能的影响[J].中国康复医学杂志, 2017,32(5):548-553. [24] 胡斐,徐盛嘉,王晓磊,等.力量和耐力组合训练对青年男性心脏自主神经功能影响的研究[J].辽宁体育科技,2018,40(2):48-53. [25] 胡斐,徐盛嘉,沈铭彬,等. 大强度的无氧间歇练习、有氧耐力练习及其组合练习的次序对恢复期心脏自主神经功能的影响[J].体育科研, 2017,38(6): 87-92. [26] FU Q, LEVINE BD.Exercise and the autonomic nervous system[M]. Handb Clin Neurol.2013;117(117C):147-160. [27] ROSENWINKEL ET, BLOOMFIELD DM, ARWADY MA, et al. Exercise and autonomic function in health and cardiovascular disease. Cardiol Clin.2001;19(3):369-87. [28] KAIKKONEN P, NUMMELA A, RUSKO H. Heart rate variability dynamics during early recovery after different endurance exercises. Eur J Appl Physiol.2007;102(1):79-86. [29] PICHON AP, DE BISSCHOP C, ROULAUD M, et al. Spectral analysis of heart rate variability during exercise in trained subjects. Med Sci Sports Exerc.2004;36(10):1702-1708. [30] RANADIVE SM, FAHS CA, YAN H, et al. Heart rate recovery following maximal arm and leg-ergometry. Clin Auton Res. 2011;21(2):117-120. [31] LEICHT AS, SINCLAIR WH, SPINKS WL. Effect of exercise mode on heart rate variability during steady state exercise. Eur J Appl Physiol. 2008; 102(2):195-204. [32] TULPPO MP, MÄKIKALLIO TH, LAUKKANEN RT, et al. Differences in autonomic modulation of heart rate during arm and leg exercise. Clin Physiol.1999;19(4):294-299. [33] COTTIN F, DURBIN F, PAPELIER Y. Heart rate variability during cycloergometric exercise or judo wrestling eliciting the same heart rate level. Eur J Appl Physiol.2004;91(2-3):177-184. [34] GONZÁLEZ-CAMARENA R, CARRASCO-SOSA S, ROMÁN-RAMOS R, et al. Effect of static and dynamic exercise on heart rate and blood pressure variabilities. Med Sci Sports Exerc. 2000;32(10):1719-1728. [35] WEIPPERT M, BEHRENS M, GONSCHOREK R, et al. Muscular contraction mode differently affects autonomic control during heart rate matched exercise. Front Physiol. 2015;19(6):156-167. [36] BUCHHEIT M. Monitoring training status with HR measures: do all roads lead to Rome. Front Physiol.2014; 27(5):73-80. [37] BLAIN G, MESTE O, BOUCHARD T, et al. Assessment of ventilatory thresholds during graded and maximal exercise test using time varying analysis of respiratory sinus arrhythmia.Br J Sports Med.2005;39(7): 448-452. [38] FADEL PJ. Reflex control of the circulation during exercise. Scand J Med Sci Sports.2015;4(25):74-82. [39] COOTE JH. Recovery of heart rate following intense dynamic exercise. Exp Physiol.2010;95(3):431-440. [40] PEÇANHA T, SILVA-JÚNIOR ND, FORJAZ CL. Heart rate recovery: autonomic determinants, methods of assessment and association with mortality and cardiovascular diseases. Clin Physiol Funct Imaging. 2014; 34(5):327-339. [41] MICHAEL S, JAY O, HALAKI M, et al. Submaximal exercise intensity modulates acute post-exercise heart rate variability. Eur J Appl Physiol. 2016;116(4):697-706. [42] HAUTALA A,TULPPO MP,MÄKIKALLIO TH,et al.Changes in cardiac autonomic regulation after prolonged maximal exercise. Clin Physiol. 2001;21(2):238-45. [43] FISHER JP, SEIFERT T, HARTWICH D, et al. Autonomic control of heart rate by metabolically sensitive skeletal muscle afferents in humans. J Physiol.2010; 588(7):1117-1127. [44] VIVEKANANTHAN DP, BLACKSTONE EH, POTHIER CE, et al. Heart rate recovery after exercise is a predictor of mortality, independent of the angiographic severity of coronary disease.J Am Coll Cardiol.2003; 42(5):831-838. [45] ROMERO SA , MINSON CT, HALLIWILL JR. The cardiovascular system after exercise. J Appl Physiol.2017;122(4):925-932. [46] 马继政,孙飙,牛洁,等. 恒定负荷运动中和运动后左室舒张功能的变化[J].体育学刊, 2004,11(2):132-135. [47] PEÇANHA T, BARTELS R, BRITO L C, et al. Methods of assessment of the post-exercise cardiac autonomic recovery: A methodological review. Int J Cardiol.2017;227(15):795-802. [48] CASONATTO J, GOESSLER KF, CORNELISSEN VA, et al. The blood pressure-lowering effect of a single bout of resistance exercise: A systematic review and meta-analysis of randomised controlled trials. Eur J Prev Cardiol. 2016, 23(16):1700-1714. [49] CASONATTO J,TINUCCI T, DOURADO AC, et al. Cardiovascular and autonomic responses after exercise sessions with different intensities and durations. Clinics.2011;66(3):453-458. [50] NIEMELÄ TH, KIVINIEMI AM, HAUTALA AJ, et al. Recovery pattern of baroreflex sensitivity after exercise. Med Sci Sport Exerc. 2008;40(5): 864-870. [51] 马继政. PGC-1α、运动与心肌能量代谢[J].贵州体育科技, 2009,(4):42-46. [52] AHMADIAN M, ROSHAN VD, HOSSEINZADEH M. Parasympathetic reactivation in children: influence of two various modes of exercise. Clin Auton Res.2015;25(4):207-212. [53] STANLEY J, PEAKE JM, BUCHHEIT M . Cardiac Parasympathetic Reactivation Following Exercise: Implications for Training Prescription. Sports Med.2013;43(12):1259-1277. [54] MICHAEL S, JAY O, HALAKI M, et al. Submaximal exercise intensity modulates acute post-exercise heart rate variability. Eur J Appl Physiol. 2016;116(4):697-706. [55] 巩绪伟,王增刚,胡斐,等. 两种运动形式对健康青年心脏自主神经系统功能产生的运动效果[R].杭州:中华人民共和国第十三届学生运动会科学论文报告会,2017,9. [56] SEILER S, HAUGEN O, KUFFEL E. Autonomic recovery after exercise in trained athletes: intensity and duration effects. Med Sci Sports Exerc. 2007;39(8):1366-1373. [57] CASONATTO J, TINUCCI T, DOURADO AC, et al. Cardiovascular and autonomic responses after exercise sessions with different intensities and durations. Clinics.2011;66(3):453-458. [58] KAIKKONEN P, NUMMELA A, RUSKO H. Heart rate variability dynamics during early recovery after different endurance exercises. Eur J Appl Physiol.2007;102(1):79-86. [59] KAIKKONEN P, HYNYNEN E, MANN T, et al. Can HRV be used to evaluate training load in constant load exercises. Eur J Appl Physiol. 2010; 108(3):435-342. [60] CUNHA FA, MIDGLEY AW, GONÇALVES T, et al. Parasympathetic reactivation after maximal CPET depends on exercise modality and resting vagal activity in healthy men. Springerplus.2015;27(4):100-110. [61] 马继政,徐盛嘉,丁明超,等.基本运动训练原则在促进新入校大学生基础运动技能方面的实践研究[J].体育科技, 2018(2):136-142. [62] BELLENGER CR, FULLER JT, THOMSON RL, et al. Monitoring Athletic Training Status Through Autonomic Heart Rate Regulation: A Systematic Review and Meta-Analysis. Sports Med.2016;46(10): 1461-1486 [63] NELSON MJ, THOMSON RL, ROGERS DK, et al. Maximal rate of increase in heart rate during the rest-exercise transition tracks reductions in exercise performance when training load is increased. J Sci Med Sport.2014; 17:129–133. [64] PANISSA VL, CAL ABAD CC, JULIO UF, et al. High-Intensity Intermittent Exercise and its Effects on Heart Rate Variability and Subsequent Strength Performance. Front Physiol. 2016;7:81-91. [65] BUCHHEIT M. Monitoring training status with HR measures: do all roads lead to Rome?.Front Physiol.2014;5:73-82. [66] 马继政,丁明超,黄强年. 现役人员人类能力最佳化——训练负荷的监控策略[J].湖北体育科技,2018,37(5):426-429. [67] STANLEY J, PEAKE JM, BUCHHEIT M. Cardiac parasympathetic reactivation following exercise: implications for training prescription. Sports Med.2013;43(12):1259-1277. [68] BUCHHEIT M, LAURSEN PB, AHMAIDI S. Parasympathetic reactivation after repeated sprint exercise. Am J Physiol Heart Circ Physiol. 2007;293(1):H133-141 [69] LA GERCHE A, GEWILLIG M. What Limits Cardiac Performance during Exercise in Normal Subjects and in Healthy Fontan Patients. Int J Pediatr.2010;331(5):1-7. |
| [1] | Gu Zhengqiu, Xu Fei, Wei Jia, Zou Yongdi, Wang Xiaolu, Li Yongming. Exploratory study on talk test as a measure of intensity in blood flow restriction training [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1154-1159. |
| [2] | Wei Xing, Liu Shufang, Mao Ning. Roles and values of blood flow restriction training in the rehabilitation of knee joint diseases [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 774-779. |
| [3] | Wang Yongsheng, Wu Yang, Li Yanchun. Effect of acute high-intensity exercise on appetite hormones in adults: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1305-1312. |
| [4] |
Yu Liang, Zhao Zeming, Zhao Binting, Li Lin, Liu Ziming, Wang Zhen, Wang Ruiyuan.
Effects of different intensities of exercises on BNIP3-mediated mitophagy
in skeletal muscle |
| [5] | Shao Lian-jie. Autonomic nervous system: its response and adaptation to exercises [J]. Chinese Journal of Tissue Engineering Research, 2015, 19(46): 7509-7516. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||