Chinese Journal of Tissue Engineering Research ›› 2021, Vol. 25 ›› Issue (13): 2103-2107.doi: 10.3969/j.issn.2095-4344.3502
Previous Articles Next Articles
Pathological changes and functional reconstruction of radiation-induced salivary glands repaired by stem cells and biomaterials
Liu Lu1, 2, Zhang Nini1, 2, Dai Min1, 2, Huang Guilin1, 2
- 1Department of Scientific Research, 2Department of Oral and Maxillofacial Surgery, Hospital of Stomatology, Zunyi Medical University, Zunyi 563000, Guizhou Province, China
-
Received:2020-07-01Revised:2020-07-07Accepted:2020-08-07Online:2021-05-08Published:2020-12-29 -
Contact:Huang Guilin, MD, Professor, Master’s supervisor, Department of Scientific Research, and Department of Oral and Maxillofacial Surgery, Hospital of Stomatology, Zunyi Medical University, Zunyi 563000, Guizhou Province, China -
About author:Liu Lu, Master candidate, Department of Scientific Research, and Department of Oral and Maxillofacial Surgery, Hospital of Stomatology, Zunyi Medical University, Zunyi 563000, Guizhou Province, China -
Supported by:the National Natural Science Foundation of China, No. 81760201 (to HGL); the National Natural Science Foundation of China, No. 81860198 (to ZNN); the Science and Technology Fund Project of Guizhou Province, No. [2016]1171 (HGL)
CLC Number:
Cite this article
Liu Lu, Zhang Nini, Dai Min, Huang Guilin. Pathological changes and functional reconstruction of radiation-induced salivary glands repaired by stem cells and biomaterials[J]. Chinese Journal of Tissue Engineering Research, 2021, 25(13): 2103-2107.
share this article
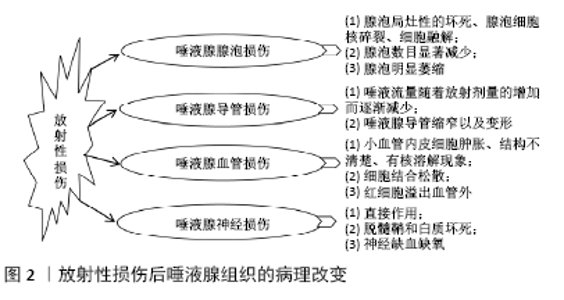
2.1 放射性损伤的机制 2.1.1 DNA间接损伤 当电离辐射的高能粒子穿透人体并从原子和分子释放电子时,单个化学键被破坏,导致高反应离子和活性氧物质的产生。研究表明活性氧是放射治疗诱导大多数细胞遗传学损伤的主要因素。当在整个身体中以高浓度存在的水被电离辐射分解时,产生诸如羟基活性氧的自由 基[6]。DNA的间接损伤是由羟基活性氧的自由基导致的[7],由于羟基自由基与DNA、蛋白质和脂质高度反应,氧化活性反应会加速染色体端粒缩短[8],所以使 DNA极易受到破坏导致细胞的失调。 2.1.2 DNA直接损伤 电离辐射还能够直接破坏DNA和调节蛋白,通过在螺旋骨架上分裂化学键,电离辐射能够产生单链断裂和双链断裂[9]。与单链断裂相比,双链断裂对基因组的破坏作用更加明显,双链断裂通常是由于DNA不精确的复制起点和复制叉被破坏而引起的,双链断裂会通过阻止细胞分裂,从而抑制DNA的修复功能,使其对细胞基因的稳定性有着消极影响[10],很难再实现自我修复,可能导致基因缺失和嵌饰等突变[11]。 2.2 放射性损伤后唾液腺组织的病理改变 2.2.1 唾液腺腺泡损伤 腺泡为连接于导管末端的盲囊,由单层腺上皮细胞组成,组成了唾液腺的分泌部分,其外侧为薄的基底膜包绕。在涎腺细胞和基底膜之间含有肌上皮细胞,它具有收缩能力,有助于涎腺细胞分泌物的排出;涎腺上皮细胞属于发育成熟的高分化细胞,虽然细胞分裂率较低,但它容易受到放射线的损害。MARZI等[12]研究发现在对40例口咽细胞癌患者(年龄>18岁)进行8周的放射治疗后,腮腺体积从 (32.3±9.4) cm3减少至(26.7±9.0) cm3。当放射剂量大于70 Gy,涎腺细胞会出现坏死、腺泡细胞萎缩、脱颗粒、胞浆均质红染、胞核染色质边集、胞浆颗粒空泡成群分布和胞核浓染[13],逐渐伴发炎症和纤维化,唾液腺的分泌功能会持续下降,发生不可逆的口干症。很多学者都认为是放射剂量越大就越容易损伤腺泡组织[14],刘学奎等[15]研究显示健康新西兰兔经过照射6 Gy和 8 Gy 的颌下腺组织中腺泡细胞间隙增宽、腺泡明显萎缩、腺泡数目明显减少,间质纤维组织增生、增厚、毛细血管散在分布;照射 10,12 和 14 Gy 的颌下腺组织腺泡的间隙较正常者明显增宽,腺泡局灶性的坏死、腺泡细胞核碎裂、细胞融解,腺泡数目显著减少,腺泡明显萎缩。 2.2.2 唾液腺导管损伤 有研究表明辐射会引起唾液腺导管的损伤[16],陈希[17]利用核磁共振加权成像对23例头颈部放疗的患者进行唾液腺造影,并评估其唾液腺的损伤情况,根据核磁共振成像发现唾液流量随着放射剂量的增加而逐渐减少,唾液腺导管缩窄以及变形。李碧霞等[18]采用一次性 18 Gy照射Wistar 大鼠,发现颌下腺导管结构变形、管壁缩窄、管腔扩大,浆液小导管分泌颗粒减少,导管可见坏死细胞碎屑,管腔内有分泌物,但相比较腺泡来说,导管对射线的耐受力较腺泡好。GRUNDMANN等[19]报道恒河猴腮腺组织对放射性特别敏感,经过12 h放疗后腺泡明显破坏,但唾液腺导管并没有明显改变。正因为唾液腺导管对辐射呈低敏感性的这种特性,使其利用干细胞修复的时候会比其他组织更有优势[20]。 2.2.3 唾液腺血管损伤 射线会导致涎腺的血管密度降低[21],这是因为血管当中有一种血管内皮生长因子受到辐射后会降低其生物活性,并使血管系统结构和功能改变,包括内皮细胞的变异和凋亡、细胞间紧密连接完整性的改变、纤维素样物沉积、血管壁的增厚、管径的扩张、血管密度长度的减少及通透性的增加等等,导致血管损伤、血管周围间隙渗出增多[22]。陈晨[23]对小鼠下颌下腺进行放射治疗后发现,由于活性氧和神经酰胺的产生使小鼠的涎腺微血管密度明显降低,血管内皮细胞增殖减少,涎腺大血管横截面积增大,血管扩张、充血以及组织内出血现象;透射电镜发现小血管内皮细胞肿胀,结构不清楚,有核溶解现象,细胞结合松散,红细胞溢出血管外。 2.2.4 唾液腺神经损伤 头颈部肿瘤放射治疗后可引起迷走神经、舌下神经、视神经、动眼神经、外展神经和喉返神经等颅神经的损伤。由于唾液腺细胞均受自主神经系统调节,大唾液腺都有交感和副交感神经纤维的分布,但个体细胞所受的神经支配却有较大变异。交感与副交感神经纤维虽然发自不同的部位,但它们与神经胶质细胞并成一束,一起走行并分布到上皮或血管细胞。唾液腺的神经纤维可在任何部位释放神经介质,但由于射线的影响,导致神经反射弧中的感受器以及节后神经元遭到损害,破坏了整个反射弧的完整性,从而导致唾液腺无法接收到神经系统的支配,以至于不能正常的运转。LIN等[24]研究了在术后6个月左右,被诊断有放射性神经病变的19例鼻咽癌患者(22-65周岁),大多数患者每天接受的射线剂量为180 cGy或200 cGy,证明了放射治疗相关的神经麻痹可能发生在鼻咽癌患者接受常规放疗后。舌下神经麻痹患者的数量占比最多,其次是迷走神经麻痹和喉返神经麻痹,而引起这些并发症的原因可能是由于颈部纤维化(纤维化是一种常见的晚期并发症,指实质细胞损伤、基质重塑和组织收缩的动态病理过程。在基质中观察到的变化包括胶原和其他细胞外基质成分的过度沉积和非典型成纤维细胞的存在)及颅神经(是整个头颅及颌面部重要的神经分支,与唾液腺的分泌有着密切的联系)的分布有关[25]。 多数学者认为放射引起中枢神经损伤的原因包括3个方面:一是射线对神经髓鞘、许旺细胞、神经微血管和神经纤维蛋白的直接作用; 二是放射线引起少突胶质细胞型O-2A祖细胞丢失,导致不能形成髓鞘所需的少突胶质细胞,最终导致脱髓鞘和白质坏死;三是射线所引起的神经周围组织纤维化对神经的挤压和牵拉、神经周围血管纤维化增生,血管壁发生炎性坏死以及内皮细胞消失从而导致神经缺血缺氧,最终受到损伤[26-27]。放射性损伤后唾液腺组织的病理改变示意图见图2。 2.3 放射性涎腺损伤的修复 由于放射线会损害涎腺的腺泡、导管系统、神经系统以及血管系统等等,在头颈癌治疗期间接受不可避免的唾液腺辐射的患者中观察到,40%患者会出现口干症[28],这是一种不可逆的症状,无法自愈。对于这种口干症的治疗,目前临床上还缺乏有效的治疗方法,主要采用改变患者生活习惯、补充人工合成唾液、使用毛果云香碱等催涎剂来缓解口干症状[29-30]。这些治疗方法的临床效果十分有限并且有一定的不良反应,无法从根本上恢复涎腺原有的功能。也有不少的研究人员为求进一步修复唾液腺功能开始在转基因技术以及在外科手术移植唾液腺方面进行尝 试[31-32],均证实有一定的治疗效果,但因转基因技术本身的问题、唾液腺供体、长期服用免疫抑制剂和手术难度等因素难以应用于临床[32-33]。近年来随着干细胞的迅速发展,细胞治疗以及类器官修复开始广为关注。 2.3.1 干细胞修复放射性损伤的涎腺 挽救被放射损伤的唾液腺的另一种潜在方法是涎腺来源的干细胞/祖细胞治 疗[34-35]。临床前研究表明,干细胞移植不仅可以挽救唾液分泌不足[36],而且还可以恢复辐照腺体组织稳定状态,这对于维持唾液腺的再分泌是有促进作用的[37]。干细胞则在放疗开始之前从唾液腺中收获,并在放疗完成后将其移植入唾液腺中,然后这些唾液干/祖细胞就会重新唤醒因为射线而导致休眠的唾液腺功能细胞[38],正如之前所提到的导管对射线的敏感程度通常较腺泡更低,所以唾液腺导管复合体是放疗后输送干细胞和祖细胞的适合途径。更为有利的是干细胞既可以是动物来源,也可以是人来源。王英鑫[38]将间充质干细胞移植入经过射线照射的C57小鼠模型中,移植后2个月,苏木精-伊红染色发现腺泡细胞数量增多,浆液性腺泡轻度水肿,可见少量散在炎性细胞浸润,间质纤维化明显好转;细胞凋亡率相比未经干细胞治疗的有所降低。王涛等[39]将脂肪干细胞混悬液注射入雌性 C3H 小鼠(经放射后的小鼠模型)体内,10周后观察到小鼠唾液实验组分泌率由0.3 μL/(min·g) 上升至0.4 μL/(min·g);对照组的分泌率由0.3 μL/(min·g)下降至0.2 μL/(min·g);鼠腺泡细胞表面积占下颌下腺总表面积的百分比为 (65±13)% 相比对照组(34±9)%的面积要大;涎腺细胞的实验组的增殖率为(8.1±0.18)%,对照组为(3.6±0.14)%。以上结果表示,脂肪干细胞治疗能够明显改善放射损伤的唾液腺功能,促进唾液分泌,提高腺体细胞的增殖率,有望将来用于临床治疗放疗引起的唾液腺功能损伤。 ANDREADIS等[40]首次较为系统地对小涎腺进行分离培养获得了具有多项分化潜能和免疫细胞表型的干细胞,并发现其为成纤维样细胞和部分扁平型上皮细胞的混合细胞,同时具有间充质和部分的上皮特性[41]。SUI等[42]从1例男性和2例女性患有成釉细胞瘤的患者(20-45岁)的下颌下腺中提取出了人来源的涎腺干细胞,免疫荧光显示CK9(上皮导管细胞特殊标记物),Ki67(增殖标志物),K5,CD49f(人涎腺干细胞的标记物)为强阳性表达[43],将其进行为期7 d 的3D培养,观察得出了有自我分化及增殖的能力。PRINGLE等[44]研究发现成人唾液腺干/祖细胞可通过细胞分离技术进行提取,并证明在单细胞水平体外自我更新和分化成多系类器官。将其移植入放射性损伤的小鼠的腺体中,未移植的涎腺细胞的唾液流速为(46±4)%,在移植了10万细胞球体两三个月后,唾液流速增加到了(79±8)%,移植的人类源的细胞群体恢复了唾液的产生,并显著提高了被辐射的唾液腺再生潜力,涎腺功能上涨了10%,有趣的是,移植细胞与受体腺体的相互作用也可能激发功能恢复。因此,SARAH首次表明,从人类唾液腺培养的涎腺球体含有能够自我更新和分化并拯救唾液产生的干/祖细胞。ZHANG等[45]研究出人羊膜上皮细胞移植入8周龄小鼠C57后30 d,免疫荧光结果发现 CD29,CD73 和 CK19均成阳性,CD44,CD34,CD45 和CD71呈阴性,移植的细胞在接受者腺体内的腺泡、导管结构已形成,移植后的小鼠唾液流速从15 min (87.3±8.29) μL,上升至15 min (125.68±18.64) μL,表明唾液腺的形态和功能得到改善。 2.3.2 涎腺类器官修复放射性损伤的涎腺 类器官是应用体外 3D 培养技术建立的结构和功能上类似于器官的小型组 织[46],因其在组织再生医学中有很大的发展前景,与此同时也为治疗放射性损伤的涎腺组织提供了新的治疗思路。从传统观念来说,普遍认为3D类器官不论是从外形上还是功能上都应接近于原始器官。但随着再生医学的不断进步,涎腺类器官是利用3D培养技术原理[47-48],将涎腺细胞培养成涎腺细胞球体,与正常的涎腺组织有着相似的组织构成结构以及分泌功能,而在外形上与正常涎腺组织并没有相似性。近年来有研究表明生物材料脱细胞基质水凝胶(主要成分脱细胞基质、胶原[49]、透明质酸[50])作为底物可以更好地为细胞提供外环境[51],其中细胞外基质主要成分为 Ⅰ,Ⅱ,Ⅲ型胶原蛋白及纤维连接蛋白,这种成分所构成的框架结构,具有颌下腺细胞生长的原始外部结构和环境,在颌下腺组织工程中起到临时细胞外基质的作用,暂时为颌下腺细胞提供附着、增殖、分化和代谢的场所。将细胞外基质与肝素水凝胶进行交联后与涎腺细胞共培养,可以为其提供生长所需的三维环境。 将涎腺细胞与生物材料水凝胶共同培养后所形成的功能以及结构上都类似于涎腺的细胞球体,虽然外观上并非类似于原始涎腺,但仍然可以发挥涎腺的功能,然后植入体内发挥分泌功能,以达到治疗目的[52-53]。董娇等[51]提取8周龄SD大鼠的下颌下腺细胞并与透明质酸肝素细胞外基质水凝胶共培养,实验组(细胞外基质水凝胶与涎腺细胞)和对照组(单纯涎腺细胞组)通过1,3,5,7 d检测,得出实验组中的细胞死亡率(分别为2%,3%,1%,1%)要比对照组(分别为3%,5%,2%,1.8%)低。SHIN等[54]发现了第一只大鼠涎腺组织衍生的脱细胞细胞外基质水凝胶作为一种功能性正交异性生物支架,用于未来有效的涎腺干细胞治疗。通过流变学或生化分析对水凝胶进行了表征,然后在水凝胶中对大鼠涎腺干细胞/祖细胞进行了三维培养。有趣的是,水凝胶嵌入的干细胞/祖细胞存活并表达了淀粉酶IA的涎腺功能分化标记,并在蛋白质水平上提高了α-淀粉酶的酶活性,而它们显示成人导管茎/祖细胞标记水平降低,包括c-Kit、c-Met和 CD44。此外,基本上皮紧密连接标记的表达水平在转录水平上恢复到与水凝胶培养后的裸鼠涎腺组织相似的水平。 因此,他们的研究结果表明,水凝胶可以为干细胞 /祖细胞的存活提供一个合适的微环境,干细胞在此环境中可以形成细胞球体,相比较单纯的2D培养,细胞活性及稳定性更强。刘磊[55]所培养的鼠胶原水凝胶生物支架与干细胞进行立体共培养后并移植入裸鼠体内,模拟体内唾液腺的再生重建,发现有新的血管长入,组织成活。因此涎腺类器官的构建为腺涎功能障碍的治疗带来了新的希望。 以上通过涎腺干细胞移植或者3D培养的类器官来修复已受损的涎腺,这无疑是一种治疗放射性涎腺损伤所引起的口干症的好方法,并且应用这种生物工程技术,不存在类似胚胎干细胞的道德伦理问题。就国内外研究表明,该生物技术目前还停留在动物实验阶段,培养细胞的操作步骤繁琐,暂不能大量培育[56]。如何快速地分离和获取自体干细胞,以及将获取后的干细胞如何大量培养和储存、仍然能保持其生物学活性、移植后是否能够长期发挥干细胞的功能,都是目前所面临的挑战。 "
| [1] DU Y, DU S, LIU L, et al. Radiation-Induced Bystander Effect can be Transmitted Through Exosomes Using miRNAs as Effector Molecules.Radiat Res. 2020;194(1): 89-100. [2] WIDEL M. Radiation induced bystander effect: from in vitro studies toclinical application.Int J Med Phys Clin Eng Radiat Oncol.2016;5(1):1-17. [3] LANGENDIJK JA, DOORNAERT P, VERDONCK-DELEEUW IM, et al. Impact of late treatment-related toxicity on quality of life among patients with head and neck cancer treated with radiotherapy.J. Clin. Oncol. 2008;26:3770-3776. [4] DIRIX P, NUYTS S. Evidence-based organ-sparing radiotherapy in head and neck cancer.Lancet Oncol. 2010;11:85-91. [5] CHOI J, KIM SH, KOH YW, et al. Tumor Stage-Related Role of Radiotherapy in Patients with an External Auditory Canal and Middle Ear Carcinoma.Cancer Res Treat. 2017;49(1):178-184. [6] MOLONEY JN, COTTER TG.ROS signalling in the biology of cancer.Semin Cell Dev Biol. 2018;80:50-64. [7] BORREGO-SOTO G, ORTIZ-LÓPEZ R, ROJAS-MARTÍNEZ A. Ionizing radiation-induced DNA injury and damage detection in patients with breast cancer. Genet Mol Biol. 2015;38(4):420-432. [8] VON ZGLINICKI T. Oxidative stress shortens telomeres.Trends Biochem Sci. 2002; 27(7):339-44. [9] HUBENAK J, ZHANG Q, BRANCH CD, et al.Mechanisms of injury to normal tissue after radiotherapy: a review.Plast Reconstr Surg. 2014;133(1):49e-56e. [10] CAMPISI J. Aging, cellular senescence, and cancer.Annu Rev Physiol. 2013;75: 685-705. [11] 陈犹白,柴密,乌兰哈斯,等.放射性损伤:类型、症状和机制[J].中华损伤与修复杂志(电子版),2017,12(3):203-206. [12] MARZI S, FARNETI A, VIDIRI A, et al. Radiation-induced parotid changes in oropharyngeal cancer patients: the role of early functional imaging and patient-/treatment-related factors.Radiat Oncol. 2018;13(1):189. [13] STEPHENS LC, SCHULTHEISS TE, PRICE RE, et al. Radiation apoptosis of serous acinar cells of salivary and lacrimal glands.Cancer. 1991;67(6):1539-1543. [14] WADA A, UCHIDA N, YOKOKAWA M, et al. Radiation-induced xerostomia: objective evaluation of salivary gland injury using MR sialography.AJNR Am J Neuroradiol. 2009;30(1):53-58. [15] 刘学奎,曾宗渊,张书旭,等.兔颌下腺移位术防治放疗后口干燥症[J].中华放射医学与防护杂志,2005,25(5):445-446. [16] ZHOU S, QIAN J J, XU L, et al. The quantitative evaluation of early radiation-induced changes in the salivary glands using MRI.Zhonghua Yi Xue Za Zhi. 2017;97:492-495. [17] 陈希.基于磁共振弥散加权成像的唾液腺放射性损伤剂量-效应相关性研究[J].中国医学创新,2017,14(35):45-48. [18] 李碧霞,陈倩怡,戴振晖,等.放射性口干症动物模型建立及颌下腺放射性组织损伤的生物学效应[J].中国组织工程研究,2017,21(32):5164-5169. [19] GRUNDMANN O, MITCHELL GC, LIMESAND KH. Sensitivity of salivary glands to radiation: from animal models to therapies.J Dent Res. 2009;88(10):894-903. [20] EMMERSON E, KNOX SM. Salivary gland stem cells: A review of development, regeneration and cancer.Genesis.2018;56: e23211. [21] 颜兴,武鸿毅,许诺,等.放疗对小型猪腮腺颌下腺舌下腺微血管损伤影响的实验研究[J].口腔医学研究,2017,33(1):15-18. [22] Cotrim AP, Sowers A, Mitchell JB, et al. Prevention of irradiation-induced salivary hypofunction by microvessel protection in mouse salivary glands.Mol Ther. 2007;15(12):2101-2106. [23] 陈晨. 海带多糖调节P38MAPK通路保护放射诱导损伤的下颌下腺血管[D].南宁:广西医科大学,2018. [24] LIN YS, JEN YM, LIN JC. Radiation-related cranial nerve palsy in patients with nasopharyngeal carcinoma.Cancer. 2002;95:404-409. [25] MOLONEY EC, BRUNNER M, ALEXANDER AJ, et al. Quantifying fibrosis in head and neck cancer treatment: An overview.Head Neck. 2015;37(8):1225-1231. [26] JOHANSSON S, SVENSSON H, LARSSON LG, et al. Brachial plexopathy after postoperative radiotherapy of breast cancer patients--a long-term follow-up.Acta Oncol. 2000;39:373-82. [27] 薛兵,卢宏.放射性神经系统损伤2例分析并文献回顾[J].神经损伤与功能重建,2019,14(2):72-75. [28] VAN LUIJK P, PRINGLE S, DEASY JO, et al. Sparing the region of the salivary gland containing stem cells preserves saliva production after radiotherapy for head and neck cancer.Sci Transl Med. 2015;7(305):305ra147. [29] YOO C, VINES JB, ALEXANDER G, et al. Adult stem cells and tissue engineering strategies for salivary gland regeneration: a review. Biomater Res.2014;18:9. [30] OGAWA M, TSUJI T. Functional salivary gland regeneration as the next generation of organ replacement regenerative therapy. Odontology. 2015;103(3):248-257. [31] NEZU A, MORITA T, NAGAI T, et al. Simultaneous monitoring of Ca2+ responses and salivary secretion in live animals reveals a threshold intracellular Ca2+ concentration for salivation.Exp Physiol. 2019;104(1):61-69. [32] TANAKA ISOMURA E, YOSHITOMI K, HAMAGUCHI M, et al.Transplantation of vascularized submandibular gland in dogs.J Oral Maxillofac Surg.2006;64: 1561-1565. [33] SHIP JA.Diagnosing, managing, and preventing salivary gland disorders.Oral Dis. 2002;8:77-89. [34] NEUMANN Y, DAVID R, STIUBEA-COHEN R, et al. Long-term cryopreservation model of rat salivary gland stem cells for future therapy in irradiated head and neck cancer patients.Tissue Eng Part C Methods. 2012;18(9):710-718. [35] SU X, LIU Y, BAKKAR M, et al. Labial Stem Cell Extract Mitigates Injury to Irradiated Salivary Glands.J Dent Res. 2020;99:293-301. [36] VISSINK A, VAN LUIJK P, LANGENDIJK JA, et al. Current ideas to reduce or salvage radiation damage to salivary glands. Oral Dis. 2015;21(1):e1-10. [37] LOMBAERT I, MOVAHEDNIA MM, ADINE C, et al. Concise Review: Salivary Gland Regeneration: Therapeutic Approaches from Stem Cells to Tissue Organoids.Stem Cells. 2017;35(1):97-105. [38] 王英鑫. 低氧预处理人羊膜间充质干细胞修复放射性涎腺损伤功能的研究[D].遵义:遵义医学院,2018. [39] 王涛,强艳丽.脂肪干细胞对小鼠放射性唾液腺损伤的治疗作用[J].山东医药,2017,57(33):32-34. [40] ANDREADIS D, BAKOPOULOU A, LEYHAUSEN G, et al. Minor salivary glands of the lips: a novel, easily accessible source of potential stem/progenitor cells.Clin Oral Investig.2014;18: 847-856. [41] NANDURI LS, BAANSTRA M, FABER H, et al.Purification and ex vivo expansion of fully functional salivary gland stem cells.Stem Cell Reports. 2014;3(6):957-964. [42] SUI Y, ZHANG S, LI Y, et al. Generation of functional salivary gland tissue from human submandibular gland stem/progenitor cells.Stem Cell Res Ther. 2020; 11(1):127. [43] ZHANG C, LI Y, ZHANG XY, et al. Therapeutic potential of human minor salivary gland epithelial progenitor cells in liver regeneration.Sci Rep. 2017;7(1):12707. [44] PRINGLE S, MAIMETS M, VAN DER ZWAAG M, et al. Human Salivary Gland Stem Cells Functionally Restore Radiation Damaged Salivary Glands.Stem Cells. 2016;34(3):640-652. [45] ZHANG NN, HUANG GL, HAN QB, et al. Functional regeneration of irradiated salivary glands with human amniotic epithelial cells transplantation.Int J Clin Exp Pathol. 2013;6(10):2039-2047. [46] LANCASTER MA,KNOBLISH JA. Organogenesis in a dish: modeling development and disease using organoid technologies. Science.2014;345(6194):1247125. [47] MORITANI Y, USUI M, SANO K, et al. Spheroid culture enhances osteogenic potential of periodontal ligament mesenchymal stem cells. J Periodont Res. 2018; 53:870-882. [48] TANAKA J, MISHIMA K. In vitro three-dimensional culture systems of salivary glands. Pathol Int. 2020;70(8):493-501. [49] 吴婷,李朝晖,崔占峰,等.应用多种水凝胶支架材料构建三维神经干细胞培养模型[J].中国细胞生物学学报,2015,37(1):66-73. [50] GASTON J, THIBEAULT SL. Hyaluronic acid hydrogels for vocal fold wound healing.Biomatter.2013;3(1):e23799. [51] 董娇,张霓霓,姚礼,等.HP-HA-肝ECM水凝胶制备及细胞相容性研究[J].实用口腔医学杂志,2019,35(6):779-784. [52] Shin HS, Hong HJ, Koh WG, et al. Organotypic 3D Culture in Nanoscaffold Microwells Supports Salivary Gland Stem-Cell-Based Organization.ACS Biomater Sci Eng. 2018;4(12):4311-4320. [53] JEE JH, LEE DH, KO J, et al. Development of Collagen-Based 3D Matrix for Gastrointestinal Tract-Derived Organoid Culture.Stem Cells Int. 2019;2019: 8472712. [54] SHIN K, KOO KH, JEONG J, et al. Three-Dimensional Culture of Salivary Gland Stem Cell in Orthotropic Decellularized Extracellular Matrix Hydrogels. Tissue Eng Part A. 2019;25(19-20):1396-1403. [55] 刘磊. 生物工程化人唾液腺类器官构建的实验研究[D].北京:北京协和医学院,2017. [56] KHALILI S, LIU Y, KORNETE M, et al. Mesenchymal stromal cells improve salivary function and reduce lymphocytic infiltrates in mice with Sjögren’s-like disease.PLoS One. 2012;7(6):e38615. [57] EMMERSON E, KNOX SM. Salivary gland stem cells: A review of development, regeneration and cancer.Genesis. 2018;56(5):e23211. |
| [1] | Lin Qingfan, Xie Yixin, Chen Wanqing, Ye Zhenzhong, Chen Youfang. Human placenta-derived mesenchymal stem cell conditioned medium can upregulate BeWo cell viability and zonula occludens expression under hypoxia [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 4970-4975. |
| [2] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [3] | Zhang Chao, Lü Xin. Heterotopic ossification after acetabular fracture fixation: risk factors, prevention and treatment progress [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1434-1439. |
| [4] | Zhou Jihui, Li Xinzhi, Zhou You, Huang Wei, Chen Wenyao. Multiple problems in the selection of implants for patellar fracture [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1440-1445. |
| [5] | Wang Debin, Bi Zhenggang. Related problems in anatomy mechanics, injury characteristics, fixed repair and three-dimensional technology application for olecranon fracture-dislocations [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1446-1451. |
| [6] | Ji Zhixiang, Lan Changgong. Polymorphism of urate transporter in gout and its correlation with gout treatment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1290-1298. |
| [7] | Yuan Mei, Zhang Xinxin, Guo Yisha, Bi Xia. Diagnostic potential of circulating microRNA in vascular cognitive impairment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1299-1304. |
| [8] | Zhang Xiumei, Zhai Yunkai, Zhao Jie, Zhao Meng. Research hotspots of organoid models in recent 10 years: a search in domestic and foreign databases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1249-1255. |
| [9] | Wang Zhengdong, Huang Na, Chen Jingxian, Zheng Zuobing, Hu Xinyu, Li Mei, Su Xiao, Su Xuesen, Yan Nan. Inhibitory effects of sodium butyrate on microglial activation and expression of inflammatory factors induced by fluorosis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1075-1080. |
| [10] | Wang Xianyao, Guan Yalin, Liu Zhongshan. Strategies for improving the therapeutic efficacy of mesenchymal stem cells in the treatment of nonhealing wounds [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1081-1087. |
| [11] | Wan Ran, Shi Xu, Liu Jingsong, Wang Yansong. Research progress in the treatment of spinal cord injury with mesenchymal stem cell secretome [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1088-1095. |
| [12] | Liao Chengcheng, An Jiaxing, Tan Zhangxue, Wang Qian, Liu Jianguo. Therapeutic target and application prospects of oral squamous cell carcinoma stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1096-1103. |
| [13] | Zhao Min, Feng Liuxiang, Chen Yao, Gu Xia, Wang Pingyi, Li Yimei, Li Wenhua. Exosomes as a disease marker under hypoxic conditions [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1104-1108. |
| [14] | Xie Wenjia, Xia Tianjiao, Zhou Qingyun, Liu Yujia, Gu Xiaoping. Role of microglia-mediated neuronal injury in neurodegenerative diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1109-1115. |
| [15] | Li Shanshan, Guo Xiaoxiao, You Ran, Yang Xiufen, Zhao Lu, Chen Xi, Wang Yanling. Photoreceptor cell replacement therapy for retinal degeneration diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1116-1121. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||