Chinese Journal of Tissue Engineering Research ›› 2021, Vol. 25 ›› Issue (20): 3210-3218.doi: 10.3969/j.issn.2095-4344.3209
Previous Articles Next Articles
Epigenetic reprogramming and exercise regulation of bone metabolism disorders
Liu Bo1, Chen Xianghe1, Yang Kang2, Sun Changliang3, Yu Huilin1, Lu Pengcheng1
- 1School of Physical Education, Yangzhou University, Yangzhou 225127, Jiangsu Province, China; 2Department of Rehabilitation, the Northern Jiangsu People’s Hospital, Yangzhou 225001, Jiangsu Province, China; 3School of Physical Education and Health, Hebei Normal University of Science and Technology, Qinhuangdao 066000, Hebei Province, China
-
Received:2020-08-11Revised:2020-08-12Accepted:2020-09-25Online:2021-07-18Published:2021-01-15 -
Contact:Chen Xianghe, MD, Associate professor, School of Physical Education, Yangzhou University, Yangzhou 225127, Jiangsu Province, China -
About author:Liu Bo, Master candidate, School of Physical Education, Yangzhou University, Yangzhou 225127, Jiangsu Province, China -
Supported by:Academic Science and Technology Innovation Fund of Yangzhou University, No. X20200325 (to LB); China Postdoctoral Science Foundation (General Project), No. 2019M661957 (to CXH)
CLC Number:
Cite this article
Liu Bo, Chen Xianghe, Yang Kang, Sun Changliang, Yu Huilin, Lu Pengcheng. Epigenetic reprogramming and exercise regulation of bone metabolism disorders[J]. Chinese Journal of Tissue Engineering Research, 2021, 25(20): 3210-3218.
share this article

2.1 骨代谢稳态与表观遗传学 2.1.1 骨代谢稳态与组蛋白修饰 真核生物中DNA以基本单位为核小体的染色质形式存在。在核小体中,长约146 bp的DNA分子缠绕在球状的八聚体组蛋白上,暴露出组蛋白亚基的氨基端,核小体之间再通过DNA分子连接起来。组蛋白是一种碱性小分子蛋白质,有5种类型,包括H1、H2A、H2B、H3、H4,众多修饰位点就位于组蛋白N端氨基酸残基上。参与组蛋白修饰的酶主要包括组蛋白甲基转移酶、组蛋白去甲基化酶、组蛋白乙酰转移酶、组蛋白去乙酰化酶(histone deacetytlase,HDAC)等,根据修饰位点以组蛋白酶的不同修饰类型也有多种,其中以甲基化、乙酰化、磷酸化、泛素化等修饰较为常见[4]。 目前表观遗传学在骨代谢中的作用正被逐渐放大,越来越多的研究致力于探究其调控机制,一些体外实验表明组蛋白甲基转移酶和组蛋白去甲基化酶在骨形成中发挥重要作用。缺失的、小的同源异形1是一种高度保守的组蛋白甲基化转移酶,能与同源盒基因和Smads基因的启动子结合并改变H3K4me水平来调控这两个基因表达,进而调节骨髓间充质干细胞成骨分化[5]。Zeste基因同源蛋白2是另一种甲基转移酶,可催化H3K27三甲基化从而抑制靶基因转录,如T细胞特定转录因子7、核心结合因子2等,导致间充质干细胞向成骨分化过程受阻。WEI等[6]通过体外实验证明,蛋白依赖性激酶1活化可通过增加ZESTE基因同源蛋白2磷酸化来减少H3K27三甲基化,促进成骨标志基因核心结合因子2和骨桥蛋白表达增加,最终影响间充质干细胞成骨分化。组蛋白乙酰化指在组蛋白乙酰转移酶作用下将疏水的乙酰基引入组蛋白N端赖氨酸残基,减弱DNA与组蛋白之间的相互作用力,促进转录因子与DNA模板结合进而激活基因转录;而HDACs与组蛋白乙酰转移酶作用相反,其可加强DNA与组蛋白之间的作用力并使两者紧密结合,抑制基因转录。根据其对酵母蛋白的同源性可分为5类[7](Ⅰ类、Ⅱa类、Ⅱb类、Ⅲ类和Ⅳ类),与成骨分化相关的主要是Ⅰ类HDACs(HDAC1/2/3/8)。高糖环境会引起HDAC1/3过表达,在破坏成骨细胞功能的同时诱导大量促炎性细胞因子如白细胞介素1β、白细胞介素6、肿瘤坏死因子α和环氧合酶2等产生,激活核因子κB并活化破骨细胞,从而导致骨形成被破坏以及骨吸收增加[8]。HDAC8与膜内成骨密切相关,可通过使H3K9脱乙酰并抑制核心结合因子2转录活性进而抑制骨髓间充质干细胞成骨分化[9]。周华等[10]通过体外培养大鼠骨髓间充质干细胞并转染HDAC8过表达慢病毒载体,成骨诱导7 d后发现核心结合因子2、成骨细胞特异性转录因子Osterix(OSX)、骨桥蛋白、骨钙素等成骨转录因子表达均显著降低,用组蛋白去乙酰化酶抑制剂——曲古抑菌素A处理后,以上基因表达以及矿化结节形成能力均显著提升,证明HDAC8对骨髓间充质干细胞成骨分化具有抑制作用。Ⅱa类HDACs(HDAC4/5/7/9)特异性表达于骨骼肌、骨骼、心肌等细胞中,可通过靶向Smad3来抑制核心结合因子2基因表达并且与骨发育密切联系。其中HDAC7与HDAC3相似,可以通过去乙酰化方式抑制核心结合因子2活性进而影响成骨细胞矿化[11],而骨形态发生蛋白2可激活蛋白依赖性激酶1,蛋白依赖性激酶1的激活会磷酸化HDAC7并使其游离出细胞核,从而保护核心结合因子2不被HDAC7抑制[12],但目前对HDAC7抑制核心结合因子2的机制研究还不清晰,仍有待研究。HDAC4的N端存在一个肌细胞增强因子2结合区,当其与肌细胞增强因子2结合以后会诱导HDAC4入核并乙酰化核心结合因子2特定位点赖氨酸残基,增加赖氨酸残基敏感性,这使得核心结合因子2更易受到Smad泛素化调节因子1降解,最终抑制核心结合因子2活性[13]。沉默交配型信息调节因子2同源蛋白1(silent matingtype information regulator 2 homolog 1,Sirt1)是第Ⅲ类去乙酰化酶,可以调控多种成骨转录因子,对骨代谢有重要作用[14]。在对大龄小鼠的研究中发现,随着年龄增加小鼠Sirt1表达降低[15],切除大鼠双侧卵巢后用白藜芦醇进行处理,发现Sirt1表达增加且核因子κB活性被抑制,减弱了破骨细胞活性及骨吸收过程,提高了间充质干细胞活性并促进成骨细胞分化进而增加骨形成[16]。 组蛋白修饰在破骨细胞分化中发挥作用。DOT1L蛋白是少有的不含SET结构域的组蛋白赖氨酸甲基转移酶之一,能特异性催化组蛋白H3K79发生单甲基化、二甲基化、三甲基化[17],可以在抑制破骨细胞分化同时又不影响成骨细胞分化。用DOT1L甲基酶活性抑制剂处理后,H3K79me1/2水平被抑制并伴随活化T细胞核因子1(nuclear factor-activated T cell 1,NFATc1)和核因子κB转录活性升高,导致破骨细胞表面积增加进而提高骨吸收能力[18]。另一种组蛋白甲基转移酶-混合连锁白血病因子1可通过招募DOT1L,导致H3K79异常高甲基化,而EPZ5676作为一种小分子药物可通过与S-腺苷甲硫氨酸竞争性地结合DOT1L从而抑制H3K79甲基化[19]。含Jumonji结构域蛋白3是一种组蛋白去甲基化酶,不仅可以通过转录因子核心结合因子2和Osx来调节骨涎蛋白和骨钙素表达进而调控成骨细胞分化,对破骨细胞也有重要作用,JUMONJI结构域蛋白3可以去除破骨细胞中NFATc1启动子区H3K27的甲基化,活化后的NFATc1使得核因子κB受体活化因子配体(receptor activator of nuclear factor kappa B ligand,RANKL)通路激活进而促进破骨细胞分化[20]。除了组蛋白甲基转移酶对破骨细胞活性的影响,组蛋白乙酰转移酶和HDACs及其抑制剂对破骨细胞也有重要作用。KIM等[21]研究发现,RANKL可以和组蛋白乙酰转移酶相互作用提高破骨细胞中NFATc1乙酰化水平并促进其表达,增加骨吸收,而过表达HDAC5可以降低NFATc1乙酰化水平,进一步使用HDAC抑制剂丁酸钠处理后,NFATc1乙酰化水平升高并促进破骨细胞分化,HDAC9作用机制与HDAC5相似,均可通过减弱NFTAc1信号传导抑制破骨细胞分化[22]。HDAC1和HDAC2可通过复合其他蛋白体来发挥作用,MS-275作为HDAC1的抑制剂可通过下调C-fos和NFATc1表达进而抑制破骨细胞形成,降低骨吸收,HDAC1/2抑制剂NW-21可以下调肿瘤坏死因子受体相关因子6和NFATc1进而减弱破骨细胞功能[23]。另外一些非选择性HDAC抑制剂也表现出强烈的破骨细胞抑制作用,如1179.4b可以通过抑制肿瘤坏死因子受体相关因子6进而抑制C-fos来影响破骨细胞分化成熟,FR901228可以抑制NFATc1等[23]。综合来看,组蛋白修饰在影响成骨细胞、破骨细胞分化成熟中起重要作用,组蛋白的甲基化、乙酰化既可以调节骨形成,还可以调节骨吸收,其中重要的一个点为靶向HDACs抑制剂的研究,通过研发新型靶向抑制剂,可以有效治疗不同情况骨破坏引起的疾病,见表1。 "

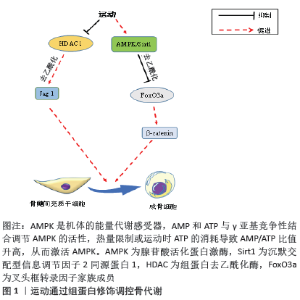
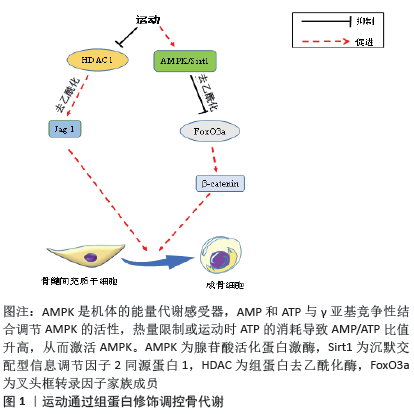
2.1.2 骨代谢稳态与DNA甲基化 DNA甲基化是研究最多的表观遗传特征,由于它的共价化学键而使其高度稳定,因此可以在一系列组织和细胞中进行定量。在人类基因组中,大概存在29 000个CPG岛[24],启动子区的DNA甲基化能通过影响转录因子结合或招募甲基CPG结合蛋白来诱导或抑制转录,调控成骨细胞/破骨细胞分化、成熟,进而影响骨形成/骨吸收平衡,并介导相关骨疾病产生,如骨质疏松、骨关节炎、股骨头坏死等。 DNA甲基化可发生在早期胚胎发育过程中调节细胞特性和基因组稳定性的的基因座中。研究表明,胚胎骨骼发育过程中,软骨细胞的DNA甲基转移酶3b消融会抑制其在E14.5和E18.5处的肥大分化和骨骼生长[25],整体敲除小鼠中的DNA甲基转移酶3b会导致多种发育缺陷如骨骼畸形,进而导致妊娠中期致死[26]。在破骨细胞形成过程中,则会持续表达DNA甲基转移酶3a进而调节破骨细胞分化和成熟[25]。DNA甲基转移酶3a和DNA甲基转移酶3b之间还存在功能重叠,如DNA甲基转移酶3a-/-、DNA甲基转移酶3b-/-双纯合子胚胎的异常形态和致死率明显高于DNA甲基转移酶3a-/-或DNA甲基转移酶3b-/-单突变胚胎[26],表明DNA甲基化对机体骨骼发育的调控机制较为复杂。核心结合因子2极易受DNA甲基化影响,仅转录起始位点上游0.6 kb的序列就足以驱动核心结合因子2 P1启动子活性[27],在特定CPG位点去甲基化后,核心结合因子2过表达会显著提高未甲基化的基质金属蛋白酶13基因活性,增加深层软骨细胞中蛋白降解酶水平,最终导致骨关节炎产生。骨硬化蛋白是由骨细胞通过旁分泌作用于成骨细胞的功能蛋白,对骨组织具有高度选择性[28],骨质疏松患者血浆骨硬化蛋白甲基化阳性率显著低于无骨质疏松者,且前者骨硬化蛋白mRNA相对表达量明显高于后者,表明骨硬化蛋白基因甲基化异常会引发骨质疏松[29]。此外,股骨头坏死患者间充质干细胞中Wnt受体Frizzled1基因转录水平较低,同时伴有Frizzled1基因启动子异常高甲基化,这使得Wnt/β-catenin通路功能被抑制并直接影响间充质干细胞成骨分化及骨形成[30]。总之,与骨形成相关的多个基因及信号通路受DNA甲基化调控且它们之间存在交互影响,共同作用调节骨形成。 在骨吸收过程中,DNA甲基转移酶3a介导S-腺苷甲硫氨酸发生的DNA甲基化可通过抗破骨细胞生成基因的表观遗传抑制来调节破骨细胞生产。干扰素调节因子8是调控破骨细胞分化的关键负性调节因子,DNA甲基转移酶3a通过其自身生物学作用提高干扰素调节因子8远侧调节元件甲基化从而抑制其发挥作用,促进破骨细胞分化[31],而当破骨细胞中DNA甲基转移酶3a特异性缺失或使用DNA甲基转移酶3a抑制剂处理均会减少骨丢失[32]。在对多发性骨髓瘤患者的研究中发现,多发性骨髓瘤分泌的胸苷磷酸化酶可上调干扰素调节因子8甲基化并抑制其表达,从而减弱对破骨细胞分化的负性调节作用并促进骨吸收过程,而这直接导致多发性骨髓瘤患者产生溶骨性改变[33]。骨保护素/RANKL/RANK系统主要由RANKL、RANK、骨保护素组成,在调节骨代谢中也受DNA甲基化影响。对高同型半胱氨酸血症导致骨丢失而形成骨质疏松的小鼠进行研究发现,机体在高同型半胱氨酸血症条件下DNA甲基转移酶1表达升高,活化后的c-Jun氨基末端激酶与DNA甲基转移酶1启动子结合使骨保护素出现超甲基化,在抑制骨保护素转录的同时促进RANKL表达激活,最终加速破骨细胞形成及骨吸收[34]。另一研究发现,诱导分化的骨髓间充质干细胞中RANKL基因启动子附近的CPG出现甲基化,导致基因沉默并抑制RANKL表达[35],使用5-氮胞苷处理高甲基化的HEK-293细胞后,发现RANKL和骨保护素表达明显上调,这会影响破骨细胞形成从而导致骨稳态失衡[36]。 2.1.3 骨代谢稳态与非编码RNA 非编码RNA在调控mRNA稳定性、加工RNA、运输蛋白质以及染色质结构改变方面发挥重要作用[37],主要包括微小RNA、长链非编码RNA和环状RNA等。目前已知长链非编码RNA是调控细胞增殖、分化的重要因子,研究表明长链非编码RNA与骨代谢有关,通过分析人骨髓间充质干细胞成骨分化过程中长链非编码RNA的表达及其网络功能,共检测到1 408个长链非编码RNA,其中785个长链非编码RNA表达显著上调,623个长链非编码RNA表达显著下调[38]。AK045490是新确定的长链非编码RNA,富含于骨骼组织,衰老及卵巢摘除小鼠骨组织中AK045490表达升高同时伴随骨骼微结构恶化和骨减少。LI等[39]研究证实,利用AK045490 siRNA可明显提高小鼠颅骨矿物沉积,增加骨形成,而这一过程可能是通过β-catenin/T细胞特定转录因子1/核心结合因子2信号传导系统进行的;长链非编码RNA-OG可以显著促进骨髓间充质干细胞成骨分化,其启动子H3K27乙酰化可被异质性胞核核糖核蛋白K激活,从而促进长链非编码RNA-OG转录活性。另外,异质性胞核核糖核蛋白K还可以与长链非编码RNA-OG外显子相互作用进而促进下游骨形态发生蛋白家族蛋白表达,诱导间充质干细胞成骨分化,但其相互调节下游基因的机制还不清楚[40]。抗分化非编码RNA是一种抵抗分化的长链非编码RNA,可以负性调控成骨细胞分化成熟[41]。TONG等[42]在对绝经后骨质疏松患者的研究中发现,其血液单核细胞中长链非编码RNA抗分化非编码RNA表达异常升高,这可能使白细胞介素6和肿瘤坏死因子α mRNA表达增加进而促进破骨细胞成熟,增加骨吸收;在破骨细胞成熟过程中,还伴随Lnc‐AK077216表达上升,研究证实AK077216可通过抑制T细胞核因子蛋白45进而促进NFATc1表达,最终促破骨细胞生成,增加骨吸收[43]。 微小RNA对基因表达具有抑制和促进的双重作用[44],在过去研究中发现了大量与骨形成/骨吸收相关的微小RNA。在小鼠MC3T3-E1中,miR-141和miR-200可通过靶向抑制远端缺失同源盒基因5来调节成骨细胞分化[45];Dickkopf同源物1是Wnt信号通路的可溶性胞外抑制剂,miR-335-5p通过与Dickkopf同源物1 mRNA 3’UTR结合下调Dickkopf同源物1表达,进而增加 β-catenin的转录活性并促进成骨分化[46];miR-29a还可靶向HDAC4 3’UTR来维持核心结合因子2乙酰化水平,同时逆转HDAC4介导的β-catenin泛素化,促进成骨细胞分化并减少糖皮质激素诱导的骨量减少[47]。不同的微小RNA对破骨细胞的抑制/促进作用不同。miR-218-5p和miR-124通过负调控 NFATc1来抑制破骨细胞形成;而作用于NFATc1上游的微小RNA-7-5p和微小RNA-26则通过抑制树突状细胞特异性跨膜蛋白来阻止破骨细胞成熟[48]。与上述微小RNA作用相反,另一部分微小RNA可以促进破骨细胞生成。miR-148a表达上升可以抑制NFATc1等破骨细胞促进因子的负调节因子,促进破骨细胞成熟,使用抑制剂特异性处理miR-148a后,骨吸收减弱,骨形成以及骨量增加[49];miR-214兼具抑制成骨细胞/促进破骨细胞分化的功能,可以与10号染色体缺失的磷酸酶基因的3’非编码区域结合,通过激活磷脂酰肌醇3-激酶/蛋白激酶B/NFATc1信号通路来促进破骨细胞分化[50]。综上所述,作为转录后调控的重要手段,微小RNA可以对许多转录因子及信号通路进行调控,在骨形成/骨吸收过程中发挥重要作用。不过由于认识有限,对微小RNA的研究还需进一步深入,这也有助于更好地了解微小RNA在骨代谢中的作用机制。 2.2 表观遗传学在运动调控骨代谢稳态中的作用机制 2.2.1 运动通过组蛋白修饰来调控骨代谢的机制 机械拉伸刺激可在体内外抑制HDACs酶活性,降低其对基因转录的抑制并促进成骨分化和骨形成。通过建立循环机械拉伸诱导的骨质疏松患者骨髓间充质干细胞成骨分化模型,2周后检测到HDAC1 mRNA和蛋白表达明显下降,3周后检测到Notch通路Jag1、Hes1和Hey1及其下游基因mRNA和蛋白表达显著上升,茜素红染色结果表明循环机械拉伸促进了骨髓间充质干细胞成骨分化,进一步实验表明,循环机械拉伸通过降低HDAC1活性,使得Jag1基因启动子区组蛋白H3乙酰化水平升高,促进Jag1表达并激活Jag1-Notch信号,即机械拉伸通过HDAC1/Jag1-Notch通路诱导骨髓间充质干细胞成骨分化[51]。老年骨质疏松患者骨代谢紊乱与衰老密切相关,随着衰老,机体会发生氧化应激反应并产生较多的活性氧,活性氧的过度积累会引起骨髓间充质干细胞产生氧化应激损伤以及线粒体功能障碍,激活叉头框转录因子O(forkhead box O,FoxO)信号通路,而FoxO的激活会与大量β-catenin结合形成复合物,从而降低β-catenin在细胞核中的积累,抑制Wnt/β-catenin信号通路[52],使骨髓间充质干细胞的增殖和分化受到限制并导致骨形成受阻进而发生骨质疏松。Sirt1作为第Ⅲ类去乙酰化酶,是细胞衰老、能量代谢、骨骼重塑等环节的交汇点,对骨代谢稳定有重要作用。Sirt1能直接或间接促进β-catenin在核内积累来激活Wnt通路进而促进骨形成:Sirt1直接去乙酰化β-catenin,使其大量聚集于细胞核并激活Wnt信号通路;Sirt1去乙酰化FoxO,减弱其对β-catenin的结合作用,使β-catenin积累并激活Wnt信号通路[53]。CHEN等[54]对人体来源的骨髓间充质干细胞分别施加2.5%,5%和10%的机械拉伸,结果表明适当的机械刺激(2.5%,5%)能有效提高细胞内超氧化物歧化酶1表达并降低活性氧水平,激活骨髓间充质干细胞抗氧化系统,而骨髓间充质干细胞抗氧化系统的激活增加了其向成骨分化的能力。进一步研究表明,机械拉伸是通过激活AMPK来上调Sirt1,之后Sirt1使FoxO3a脱乙酰并促进其从细胞浆易位到细胞核,进而诱导抗氧化酶超氧化物歧化酶1、过氧化氢酶等的转录。机械拉伸引起的活性氧水平降低会减少对FoxO3a的激活,进而减弱对β-catenin的抑制并促进其积累[55],激活Wnt/β-catenin进而促进骨髓间充质干细胞成骨分化,增加骨形成。这说明机械刺激能通过AMPK/Sirt1/FoxO3a/β-catenin途径改善衰老骨髓间充质干细胞的能量代谢失衡进而来调节成骨分化,促进骨形成,见图1。 "
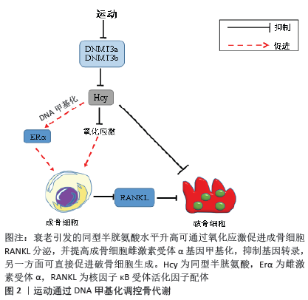
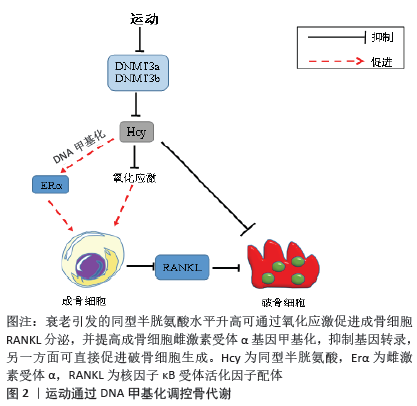
运动还能够通过Sirt1来调控2型糖尿病引起的骨代谢失衡。2型糖尿病患者体内的高糖环境会抑制核因子κB抑制蛋白的降解,使核因子κB抑制蛋白对核因子κB的抑制作用降低,促进核因子κB转移入核并促进破骨细胞形成,而运动能逆转这一过程。BOYLE等[56]发现,2型糖尿病大鼠经8周运动后,其骨中Sirt1表达上调,在乙酰化核因子κB同时抑制其穿梭入核,导致下游RANKL/C-fos/NFATC1途径无法激活,使破骨细胞分化受阻并抑制骨吸收。在体外对高糖环境下的RAW264.7施加力学刺激时,检测到Sirt1蛋白表达上调,同时观察到破骨细胞生成减少且骨吸收能力下降,说明运动可能通过Sirt1/核因子κB/RANKL途径来调节骨代谢[57]。 2.2.2 运动通过DNA甲基化调控骨代谢的机制 目前,部分研究试图找出DNA甲基化与骨代谢之间的关系以及其中的机制,但由于研究较少,其具体机制仍不清楚。胡晓青等[58]曾做过实验,在体外诱导骨髓间充质干细胞向成骨分化并检测到核心结合因子2 mRNA表达在3 d时达到最高峰,之后利用ChIP 实验方法检测到核心结合因子2基因启动子区域DNA甲基化下降了将近一半。这些实验目前仅仅证明了DNA甲基化可以调节骨代谢,但并未将运动与之联系起来,当前也有关于运动通过改变DNA甲基化治疗疾病的研究。何标等[59]对APP/PS1转基因小鼠施加10周跑台运动后,小鼠海马中DNA甲基转移酶1、DNA甲基转移酶3a、DNA甲基转移酶3b mRNA表达显著增加,造成小鼠海马甲基化水平升高,降低了APP/PS1/Aβ42等蛋白表达水平,从而提高小鼠空间记忆能力。田雪文[60]分别采用低氧运动和常氧运动来处理肥胖大鼠后发现,低氧运动能有效降血脂、调节脂代谢进而降低体质量、体脂,对相关因子mRNA和蛋白表达进行检测后发现,与脂代谢相关的基因表达出现显著变化,并用RRBS技术检测到2种运动方式使大鼠全基因组中675个基因的CPG岛发生显著的甲基化变化,其中Wnt信号通路相关基因的mRNA表达和甲基化最明显。这些研究直接证明了运动可以通过改变DNA甲基化来对机体产生影响。 衰老体弱会引起高同型半胱氨酸血症,并伴随DNA甲基转移酶3a和DNA甲基转移酶3b的升高,同型半胱氨酸一方面能通过激活蛋白磷酸酯酶2A/FoxO1/丝裂原活化蛋白激酶级联反应,调控成骨细胞中的氧化还原机制并提高RANKL/骨保护素比值,增加破骨细胞活性;另一方面同型半胱氨酸还能通过刺激细胞内活性氧生成来直接刺激破骨细胞活性增加[61]。小鼠进行4周游泳运动后DNA甲基转移酶3a和DNA甲基转移酶3b水平显著降低,并且同型半胱氨酸浓度降低,提示运动能通过降低DNA甲基转移酶介导的甲基化水平来减少同型半胱氨酸生成[62],进而抑制蛋白磷酸酯酶A/FoxO1/丝裂原活化蛋白激酶级联反应的激活,最终抑制骨吸收。但DEMINICE等[63]研究表明,只有抗阻训练能有效降低同型半胱氨酸水平,而有氧运动并无作用,且同型半胱氨酸水平与运动量显著相关,与运动强度无关,因此造成两者结果矛盾的原因可能是运动时间差异。另外,同型半胱氨酸可以增加骨髓间充质干细胞和成骨细胞中雌激素受体α基因启动子A区的甲基化程度,减少雌激素受体α基因转录,从而介导骨质疏松的产生[64]。结合运动能有效降低同型半胱氨酸水平,推测运动能通过降低同型半胱氨酸来减少雌激素受体α基因甲基化水平,进而改善骨质疏松,见图2。 "
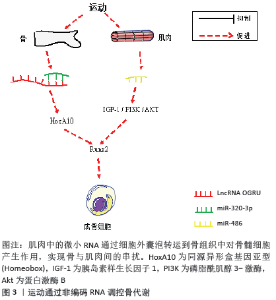
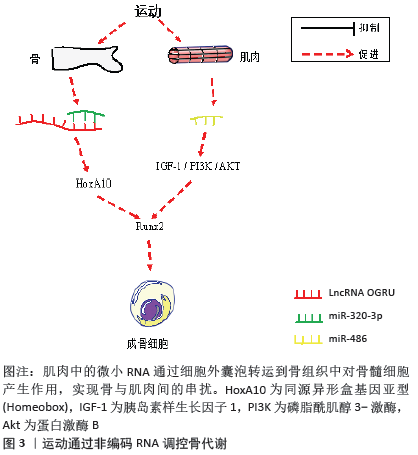
2.2.3 运动通过非编码RNA调控骨代谢的机制 微小RNA作为与骨代谢密切相关的生物标志物,可受力学刺激调控进而影响骨代谢过程,近年来对微小RNA在运动调节骨代谢中的作用研究较多。miR-21能通过下调程序性细胞死亡因子4蛋白并诱导RANKL表达进而促进C-fos的浓度升高,刺激破骨细胞生成,适当的体力活动可以抑制miR-21表达,减少RANKL的生成并促进骨保护素的生成,从而减少骨吸收[65]。与miR-21促进骨吸收的作用不同,miR-214是通过抑制活化转录因子4、Osx、碱性磷酸酶、β-catenin等成骨因子表达来抑制骨形成的,在对成骨细胞施加3%的牵张强度,0.5 Hz,4 h的持续牵张刺激下,采用3 d或7 d的周期能有效降低miR-214表达进而减弱其对上述成骨因子的抑制作用,增强成骨作用[66-67]。miR-103是近年来发现的一种机械敏感型微小RNA,早期研究发现其高表达于肿瘤细胞,参与细胞癌变与肿瘤的发生过程,但并未发现miR-103在循环机械拉伸诱导成骨细胞分化中的作用。ZUO等[68]首次将 miR-103、机械拉伸、骨形成联系起来,并通过实验证明机械负荷可能通过下调泛酸酶3的表达来抑制miR-103生成,进而减弱miR-103对靶基因核心结合因子2的抑制作用,促进骨形成。众所周知,肌肉与骨之间存在串扰,肌肉可分泌一定数量肌源性因子作用于骨组织细胞来促进或抑制成骨。miR-486富集于肌肉组织,在接受运动刺激后可通过细胞外囊泡作用于骨组织细胞进而调节骨代谢[69]。研究表明,训练有素的老年人和健壮运动员全血中miR-486水平要显著高于久坐老人和不运动的年轻人[70],先前已证明胰岛素样生长因子1/磷脂酰肌醇3-激酶/蛋白激酶B信号的激活可促进骨骼生长,并且miR-486可正向调控胰岛素样生长因子1[71],因此运动可能通过提高miR-486来靶向调控胰岛素样生长因子1/磷脂酰肌醇3-激酶/蛋白激酶B通路进而提高骨形成。除微小RNA外,长链非编码RNA在运动缺失引起的失用性骨质疏松中发挥重要作用。长链非编码RNA OGRU是一种具有1 816个核苷酸的新型长链非编码RNA,对力学刺激卸载非常敏感,在后肢卸载小鼠中被显著下调进而导致骨形成减少和骨吸收增加,而活化的长链非编码RNA OGRU可以促进成骨细胞形成,增加骨量并改善骨微结构和生物力学特性[72]。研究表明,OGRU过表达会竞争性地结合miR-320-3p 进而促进同源盒A10蛋白表达,而同源盒A10又能通过活化核心结合因子2来直接调节碱性磷酸酶、骨钙素等成骨基因表达,促进成骨细胞分化[72]。鉴于长链非编码RNA OGRU对运动缺失较为敏感,因此可将长链非编码RNA OGRU/miR-320-3p/同源盒A10/核心结合因子2作为运动调控骨代谢一个新的通路,见图3。 目前已有多种微小RNA被证实可以响应运动刺激进而对骨质产生影响,且它们的作用机制互不相同;更重要的是,不同强度、时间、形式的运动对微小RNA的影响也不同。例如对雄性大鼠施加8周不同形式和强度的训练,结果表明,相对于耐力训练,中等强度和高强度抗阻训练更能降低 miR-133a、miR-103a和miR-204等靶向调控核心结合因子2的微小RNA水平,但与FARSANI等[73]的16周训练相比,其效果要优于8周。鉴于大多数对骨骼重塑有明显影响的研究多持续150-200 d以上,且年轻大鼠对运动的响应更好,因此,建议采用周期较长的中等强度和高等强度抗阻训练方式,以期更有效地改善骨代谢紊乱引起的骨疾病。 "
| [1] THIAGALINGAM S. Epigenetic memory in development and disease: Unraveling the mechanism. Biochim Biophys Acta Rev Cancer. 2020; 1873(2):188349. [2] YU M, HAZELTON WD, LUEBECK GE, et al. Epigenetic Aging: More Than Just a Clock When It Comes to Cancer. Cancer Res. 2020;80(3):367-374. [3] DENHAM J. Exercise and epigenetic inheritance of disease risk. Acta Physiologica (Oxford, England). 2018;222(1):1-20. [4] BANNISTER AJ, KOUZARIDES T. Regulation of chromatin by histone modifications. Cell Res. 2011;21(3):381-395. [5] 崔立欣,田雅晴,郝海生,等.组蛋白甲基转移酶ASH1L的研究进展[J]. 中国畜牧杂志,2020,56(11):7-12. [6] WEI Y, CHEN Y, LI L, et al. CDK1-dependent phosphorylation of EZH2 suppresses methylation of H3K27 and promotes osteogenic differentiation of human mesenchymal stem cells. Nat Cell Biol. 2011; 13(1):87-94. [7] YI S, LEE H, LEE J, et al. Bone Remodeling: Histone Modifications as Fate Determinants of Bone Cell Differentiation. Int J Mol Sci. 2019; 20(13):3147. [8] GUO C, XIE J, HONG R, et al. Puerarin alleviates streptozotocin (STZ)-induced osteoporosis in rats through suppressing inflammation and apoptosis via HDAC1/HDAC3 signaling. Biomed Pharmacother. 2019;115:108570. [9] FAN X, LI L, YE Z, et al. Regulation of osteogenesis of human amniotic mesenchymal stem cells by sodium butyrate. Cell Biol Int. 2018;42(4): 457-469. [10] 周华, 傅瑜, 戈杰, 等. 组蛋白去乙酰化酶8对大鼠骨髓间充质干细胞成骨分化的影响[J]. 口腔生物医学,2014,5(3):113-117. [11] WANG R, ZHANG H, DING W, et al. miR-143 promotes angiogenesis and osteoblast differentiation by targeting HDAC7. Cell Death Dis. 2020;11(3):179. [12] ENSEN ED, GOPALAKRISHNAN R, WESTENDORF JJ. Bone morphogenic protein 2 activates protein kinase D to regulate histone deacetylase 7 localization and repression of Runx2. J Biol Chem. 2009;284(4): 2225-2234. [13] 梁大伟, 卫小春, 魏垒. 组蛋白去乙酰化酶4在软骨与骨发育中的调控机制[J]. 中华关节外科杂志(电子版),2015,9(3):394-399. [14] 王娜, 薛鹏, 李子怡, 等. 组蛋白去乙酰化酶Sirtuin 1在糖尿病和骨代谢中的研究进展[J]. 中国糖尿病杂志,2019,27(3):234-237. [15] HONG W, XU X, QIU Z, et al. Sirt1 is involved in decreased bone formation in aged apolipoprotein E-deficient mice. Acta Pharmacologica Sinica. 2015;36(12):1487-1496. [16] FENG J, LIU S, MA S, et al. Protective effects of resveratrol on postmenopausal osteoporosis: regulation of SIRT1-NF-κB signaling pathway. Acta Biochim Biophys Sin (Shanghai). 2014;46(12):1024-1033. [17] 李呈贞, 韩振格, 何东仪. Dot1及其同源物的研究进展[J]. 复旦学报(医学版),2018,45(4):555-560. [18] 高延盼. 组蛋白甲基转移酶DOT1L在骨质疏松发病中的作用机制研究[D]. 北京:北京协和医学院,2018. [19] 黎彦璟, 陈勇. 组蛋白甲基转移酶MLL1的结构与功能研究进展[J]. 中国细胞生物学学报,2014,36(7):857-868. [20] YASUI T, HIROSE J, TSUTSUMI S, et al. Epigenetic regulation of osteoclast differentiation: possible involvement of Jmjd3 in the histone demethylation of Nfatc1. J Bone Miner Res. 2011;26(11):2665-2671. [21] KIM JH, KIM K, YOUN BU, et al. RANKL induces NFATc1 acetylation and stability via histone acetyltransferases during osteoclast differentiation. Biochem J. 2011;436(2):253-262. [22] JIN Z, WEI W, HUYNH H, et al. HDAC9 Inhibits Osteoclastogenesis via Mutual Suppression of PPARγ/RANKL Signaling. Mol Endocrinol (Baltimore, Md.). 2015;29(5):730-738. [23] 陈青骁, 蔡真. 组蛋白去乙酰化酶及其抑制剂在多发性骨髓瘤溶骨性病变中的研究进展[J]. 实用肿瘤杂志,2018,33(5):397-401. [24] FERNANDEZ-TWINN DS, HJORT L, NOVAKOVIC B, et al. Intrauterine programming of obesity and type 2 diabetes. Diabetologia. 2019; 62(10):1789-1801. [25] XU T, WANG C, SHEN J, et al. Ablation of Dnmt3b in chondrocytes suppresses cell maturation during embryonic development. J Cell Biochem. 2018;119(7):5852-5863. [26] OKANO M, BELL DW, HABER DA, et al. DNA methyltransferases Dnmt3a and Dnmt3b are essential for de novo methylation and mammalian development. Cell. 1999;99(3):247-257. [27] TAKAHASHI A, DE ANDRÉS MC, HASHIMOTO K, et al. DNA methylation of the RUNX2 P1 promoter mediates MMP13 transcription in chondrocytes. Sci Rep. 2017;7(1):7771. [28] 张爽, 高艳虹. sclerostin在骨代谢中的作用和机制[J]. 上海交通大学学报(医学版),2015,35(4):589-593. [29] CAO Y, WANG B, WANG D, et al. Expression of Sclerostin in Osteoporotic Fracture Patients Is Associated with DNA Methylation in the CpG Island of the SOST Gene. Int J Genomics. 2019;2019:7076513. [30] WU F, JIAO J, LIU F, et al. Hypermethylation of Frizzled1 is associated with Wnt/β-catenin signaling inactivation in mesenchymal stem cells of patients with steroid-associated osteonecrosis. Exp Mol Med. 2019; 51(2):1-9. [31] NISHIKAWA K, IWAMOTO Y, KOBAYASHI Y, et al. DNA methyltransferase 3a regulates osteoclast differentiation by coupling to an S-adenosylmethionine-producing metabolic pathway. Nature Med. 2015;21(3):281-287. [32] 张丽君, 王艺璇, 胡泽兵, 等. 表观遗传学调控骨骼细胞功能的研究进展[J]. 解放军医学院学报,2019,40(12):1199-1202. [33] LIU H, LIU Z, DU J, et al. Thymidine phosphorylase exerts complex effects on bone resorption and formation in myeloma. Sci Trans Med. 2016;8(353):113r-353r. [34] BEHERA J, GEORGE AK, VOOR MJ, et al. Hydrogen sulfide epigenetically mitigates bone loss through OPG/RANKL regulation during hyperhomocysteinemia in mice. Bone. 2018;114:90-108. [35] KITAZAWA S, KITAZAWA R. Epigenetic control of mouse receptor activator of NF-kappa B ligand gene expression. Biochem Biophys Res Commun. 2002;293(1):126-131. [36] DELGADO-CALLE J, SAÑUDO C, FERNÁNDEZ AF, et al. Role of DNA methylation in the regulation of the RANKL-OPG system in human bone. Epigenetics. 2012;7(1):83-91. [37] SLACK F J, CHINNAIYAN A M. The Role of Non-coding RNAs in Oncology. Cell. 2019;179(5):1033-1055. [38] ZHANG W, DONG R, DIAO S, et al. Differential long noncoding RNA/mRNA expression profiling and functional network analysis during osteogenic differentiation of human bone marrow mesenchymal stem cells. Stem Cell Res Ther. 2017;8(1):30. [39] LI D, TIAN Y, YIN C, et al. Silencing of lncRNA AK045490 Promotes Osteoblast Differentiation and Bone Formation via β-Catenin/TCF1/Runx2 Signaling Axis. Int J Mol Sci. 2019;20(24):6229. [40] TANG S, XIE Z, WANG P, et al. LncRNA-OG Promotes the Osteogenic Differentiation of Bone Marrow-Derived Mesenchymal Stem Cells Under the Regulation of hnRNPK. Stem Cells (Dayton, Ohio). 2019;37(2):270-283. [41] 张蓓蓓, 商玮, 蔡辉. 骨质疏松症的表观遗传学调控[J]. 中华骨质疏松和骨矿盐疾病杂志,2017,10(3):290-296. [42] TONG X, GU P, XU S, et al. Long non-coding RNA-DANCR in human circulating monocytes: a potential biomarker associated with postmenopausal osteoporosis. Biosci Biotechnol Biochem. 2015;79(5): 732-737. [43] LIU C, CAO Z, BAI Y, et al. LncRNA AK077216 promotes RANKL-induced osteoclastogenesis and bone resorption via NFATc1 by inhibition of NIP45. J Cell Physiol. 2019;234(2):1606-1617. [44] 夏文祯, 李海鹏, 许顺江. 阿尔茨海默病与癌症发病负相关的表观遗传学机制研究进展[J]. 生理学报,2020,72(4):506-512. [45] ITOH T, NOZAWA Y, AKAO Y. MicroRNA-141 and -200a are involved in bone morphogenetic protein-2-induced mouse pre-osteoblast differentiation by targeting distal-less homeobox 5. J Biol Chem. 2009; 284(29):19272-19279. [46] 潘虹旭. MiRNA对成骨分化调控及骨质疏松发生的研究进展[J]. 中国骨质疏松杂志,2018,24(1):121-124. [47] KO J, CHUANG P, KE H, et al. MicroRNA-29a mitigates glucocorticoid induction of bone loss and fatty marrow by rescuing Runx2 acetylation. Bone. 2015;81:80-88. [48] 邓亚军, 解琪琪, 李文洲, 等. miRNAs在破骨细胞中的研究进展[J]. 生命科学研究,2019,23(1):54-58. [49] CHENG P, CHEN C, HE H, et al. miR-148a regulates osteoclastogenesis by targeting V-maf musculoaponeurotic fibrosarcoma oncogene homolog B. J Bone Miner Res. 2013;28(5):1180-1190. [50] 王爱飞, 王亮, 徐又佳. MicroRNAs对骨质疏松症发病机制的研究进展[J]. 中国骨质疏松杂志,2018,24(1):135-140. [51] WANG J, WANG CD, ZHANG N, et al. Mechanical stimulation orchestrates the osteogenic differentiation of human bone marrow stromal cells by regulating HDAC1. Cell Death Dis. 2016;7(5):e2221. [52] FAIENZA MF, LASSANDRO G, CHIARITO M, et al. How Physical Activity across the Lifespan Can Reduce the Impact of Bone Ageing: A Literature Review. Int J Environ Res Public Health. 2020;17(6):1862. [53] 杨宜锜, 汤亭亭. SIRT1信号通路对于骨代谢的调节作用[J]. 上海交通大学学报(医学版),2019,39(11):1335-1340. [54] CHEN X, YAN J, HE F, et al. Mechanical stretch induces antioxidant responses and osteogenic differentiation in human mesenchymal stem cells through activation of the AMPK-SIRT1 signaling pathway. Free Radic Biol Med. 2018;126:187-201. [55] 成鹏, 白银亮, 胡彩莉, 等. 黄芪甲苷通过调控FoxO3a/Wnt2/β-catenin通路抑制去卵巢大鼠骨质疏松的作用[J]. 中国实验方剂学杂志,2018,24(15):161-166. [56] BOYLE WJ, SIMONET WS, LACEY DL. Osteoclast differentiation and activation. Nature. 2003;423(6937):337-342. [57] 张路遥. 能量代谢分子SIRT1在运动改善2型糖尿病骨代谢中的作用机制[J]. 中国组织工程研究,2020,24(2):276-281. [58] 胡晓青, 张辛, 代岭辉, 等. 骨髓间充质干细胞成骨分化过程中Runx2的表观遗传学修饰[J]. 中国生物化学与分子生物学报,2014, 30(2):150-155. [59] 何标, 徐波, 张宪亮. 运动通过提高DNA甲基化水平改善阿尔茨海默病小鼠空间学习记忆能力[J]. 天津体育学院学报,2016,31(4): 333-339. [60] 田雪文. 基于iTRAQ的低氧运动肥胖大鼠肝脏蛋白质组学及Wnt/β-catenin信号通路的作用机制研究[D]. 上海:上海体育学院, 2018. [61] BEHERA J, BALA J, NURU M, et al. Homocysteine as a Pathological Biomarker for Bone Disease. J Cell Physiol. 2017;232(10):2704-2709. [62] VEERANKI S, WINCHESTER LJ, TYAGI SC. Hyperhomocysteinemia associated skeletal muscle weakness involves mitochondrial dysfunction and epigenetic modifications. Biochim Biophys Acta. 2015; 1852(5):732-741. [63] DEMINICE R, RIBEIRO DF, FRAJACOMO FTT. The Effects of Acute Exercise and Exercise Training on Plasma Homocysteine: A Meta-Analysis. PloS One. 2016;11(3):e151653. [64] LV H, MA X, CHE T, et al. Methylation of the promoter A of estrogen receptor alpha gene in hBMSC and osteoblasts and its correlation with homocysteine. Mol Cell Biochem. 2011;355(1-2):35-45. [65] SUARJANA IN, ISBAGIO H, SOEWONDO P, et al. The Role of Serum Expression Levels of Microrna-21 on Bone Mineral Density in Hypostrogenic Postmenopausal Women with Osteoporosis: Study on Level of RANKL, OPG, TGFβ-1, Sclerostin, RANKL/OPG Ratio, and Physical Activity. Acta Medica Indonesiana. 2019;51(3):245-252. [66] YUAN Y, GUO J, ZHANG L, et al. MiR-214 Attenuates the Osteogenic Effects of Mechanical Loading on Osteoblasts. Int J Sports Med. 2019; 40(14):931-940. [67] 元宇. MiR-214在机械应力促进成骨分化中的作用研究[D]. 上海:上海体育学院, 2017. [68] ZUO B, ZHU J, LI J, et al. microRNA-103a functions as a mechanosensitive microRNA to inhibit bone formation through targeting Runx2. J Bone Miner Res. 2015;30(2):330-345. [69] 史宏利, 姜鑫, 程群. 外泌体与骨代谢[J]. 中华骨质疏松和骨矿盐疾病杂志,2018,11(4):397-402. [70] NAIR VD, GE Y, LI S, et al. Sedentary and Trained Older Men Have Distinct Circulating Exosomal microRNA Profiles at Baseline and in Response to Acute Exercise. Front Physiol. 2020;11:605. [71] 黎鑫. IGF-1通过PI3K/Akt信号通路对BMSCs增殖和凋亡的影响[D]. 重庆:重庆医科大学,2018. [72] WANG K, WANG Y, HU Z, et al. Bone-targeted lncRNA OGRU alleviates unloading-induced bone loss via miR-320-3p/Hoxa10 axis. Cell Death Dis. 2020;11(5):382. [73] FARSANI ZH, BANITALEBI E, FARAMARZI M, et al. Effects of different intensities of strength and endurance training on some osteometabolic miRNAs, Runx2 and PPARγ in bone marrow of old male wistar rats. Mol Biol Rep. 2019;46(2):2513-2521. |
| [1] | Shen Jinbo, Zhang Lin. Micro-injury of the Achilles tendon caused by acute exhaustive exercise in rats: ultrastructural changes and mechanism [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1190-1195. |
| [2] | Chen Jiming, Wu Xiaojing, Liu Tianfeng, Chen Haicong, Huang Chengshuo. Effects of silymarin on liver injury and bone metabolism induced by carbon tetrachloride in mice [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1224-1228. |
| [3] | Wang Mengting, Gu Yanping, Ren Wenbo, Qin Qian, Bai Bingyi, Liao Yuanpeng. Research hotspots of blood flow restriction training for dyskinesia based on visualization analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1264-1269. |
| [4] | Wang Yongsheng, Wu Yang, Li Yanchun. Effect of acute high-intensity exercise on appetite hormones in adults: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1305-1312. |
| [5] | Liu Bo, Chen Xianghe, Yang Kang, Yu Huilin, Lu Pengcheng. Mechanism of DNA methylation in exercise intervention for osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 791-797. |
| [6] | Zhao Xiang, Wei Cuilan, Zhang Yeting. Neurogenesis and neuroinflammation under exercise: alteration and regulation [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 813-820. |
| [7] | Zheng Xiaolong, He Xiaoming, Gong Shuidi, Pang Fengxiang, Yang Fan, He Wei, Liu Shaojun, Wei Qiushi. Bone turnover characteristics in patients with alcohol-induced osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 657-661. |
| [8] | Chen Ziyang, Pu Rui, Deng Shuang, Yuan Lingyan. Regulatory effect of exosomes on exercise-mediated insulin resistance diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(25): 4089-4094. |
| [9] | Jiang Xiaoyan, Zhu Haifei, Lin Haiqi, Lin Wentao. Cold therapy promotes self-limited recovery of delayed-onset muscle soreness [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(23): 3609-3613. |
| [10] | Bai Shengchao, Gao Yang, Wang Bo, Li Junping, Wang Ruiyuan. Dynamic changes of mitochondrial function of the skeletal muscle after acupuncture intervention in rats with heavy load exercise-induced injury [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(23): 3648-3653. |
| [11] | Lu Jie, Li Xue, Wang Lu, Fan Jia, Zhang Yeting, Lu Xiaobin, Yuan Qiongjia. Effects of different-intensity swimming exercises on spatial learning and memory ability and the expression of Orexin A in the rat cerebellum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(23): 3697-3703. |
| [12] | Wang Zhen, Lin Haiqi, He Fei, Lin Wentao. Exercise activates skeletal muscle satellite cells: exercise prevention and treatment for age-related sarcopenia and muscle injury [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(23): 3752-3759. |
| [13] | Wang Chaoge, Weng Xiquan, Lin Baoxuan, Chen Lina, Xu Guoqin. Exercises under cold exposure change fat type and function in obese rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(20): 3162-3167. |
| [14] | Wang Jing, Wu Jiangbo. Irisin mediates protective effects on failing heart via integrin alpha V receptors [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(20): 3219-3225. |
| [15] | Lu Yi, Deng Wenchong. Regulation and difference of different exercise styles on brain structure and cognitive function [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(20): 3252-3258. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||