Chinese Journal of Tissue Engineering Research ›› 2021, Vol. 25 ›› Issue (16): 2605-2611.doi: 10.3969/j.issn.2095-4344.3051
Previous Articles Next Articles
Research and application of bone connection and anti-adhesion of nanomaterial artificial ligaments
Yan Hao, Qi Zhiming
- Department of Sports Medicine, Dalian Municipal Central Hospital, Dalian 116000, Liaoning Province, China
-
Received:2020-05-07Revised:2020-05-15Accepted:2020-06-12Online:2021-06-08Published:2021-01-07 -
Contact:Qi Zhiming, Chief physician, Department of Sports Medicine, Dalian Municipal Central Hospital, Dalian 116000, Liaoning Province, China -
About author:Yan Hao, Master candidate, Department of Sports Medicine, Dalian Municipal Central Hospital, Dalian 116000, Liaoning Province, China -
Supported by:the Natural Science Foundation of Liaoning Province, No. 201800935 (to QZM)
CLC Number:
Cite this article
Yan Hao, Qi Zhiming. Research and application of bone connection and anti-adhesion of nanomaterial artificial ligaments[J]. Chinese Journal of Tissue Engineering Research, 2021, 25(16): 2605-2611.
share this article
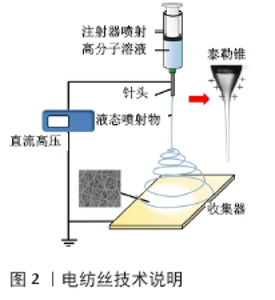
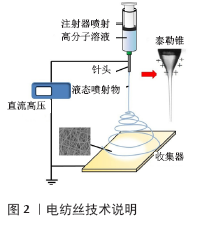
2.1 韧带移植物的选择 2.1.1 自体骨-膑腱-骨 自体骨-膑腱-骨因具有良好的远期疗效而曾作为前交叉韧带重建的首选,具有失败率较低和术后轴移试验稳定性良好等优点,但后期髌前区疼痛、跪地痛等髌骨关节并发症发生率较高,目前已经较少采用。 2.1.2 自体韧带 用自体腘绳肌肌腱重建韧带可显著减少髌股弹响、膝前跪痛的发生,并且无免疫排斥等风险。自体韧带在术后一段时间内会发生一系列形态学变化,韧带重建后短期内韧带的重塑会降低其强度[5]。相较于接受人工韧带移植的患者来说,接受自体韧带移植患者将花费更长的时间才能重返运动[6],这或许和血管重建需要一定的时间有关(异体移植的血管重建所需时间更长,可能导致延迟愈合[7])。自体韧带重建还面临供区病变、因缺损而取材受限等问题,有数据显示自体移植术后供区并发症发生率高达40%[8]。 2.1.3 同种异体韧带 同种异体韧带移植虽然可以达到理想的效果,但是如同其他器官移植一样,受者可能遭受较为严重的免疫原性后果[9]。潜在的传播疾病风险也不能忽视,在韧带处理上,低剂量的伽马射线使得HIV病毒和肝炎病毒残留,而高剂量的射线将导致移植物性能下降。其他的试剂处理技术因移植物中较高水平化学试剂含量而导致部分患者出现严重的关节内炎症反应。这种韧带处理方式和韧带性能之间的矛盾也是同种异体韧带应用受限的原因之一。 2.1.4 人工韧带 目前采用的人工韧带多为第三代人工韧带LARS韧带,由聚对苯二甲酸乙二醇酯合成,拥有良好的组织兼容性、较高的抗疲劳性能和较强的韧度[8],韧带设计的多孔结构可以允许人体结缔组织长入并包裹。人工韧带术后存在关节滑膜炎的问题,起初由于人工韧带材料和技术问题导致韧带磨损产生的碎屑沉积在关节腔内引起,在使用LARS韧带后明显改善。但陈天午等[10]报道过1例LARS韧带移植术后发生严重滑膜炎的案例,关节镜下观察到在胫骨隧道附近发生人工韧带断裂,关节腔内大量滑膜组织增生并伴有含铁血黄素的沉积,这表明使用LARS韧带仍有可能发生滑膜炎。值得注意的是,轻度的滑膜炎难以仅通过体格检查来明确,因此体征的缺乏在一定程度上掩盖了可能发生的滑膜炎。人工韧带移植也面临腱骨愈合的问题,聚对苯二甲酸乙二醇酯人工韧带由于材质的原因导致活性基团较少,不利于骨髓间充质干细胞的黏附和生长,因此单纯依靠纤维组织建立的韧带和骨道之间的连接并不牢固,而必须依赖两端内固定维持[11]。其次,长入人工韧带的纤维组织质量较差;LARS术后骨隧道平均直径明显增大[12],同样影响其远期疗效。 2.2 纳米材料镀层对人工韧带的表面修饰 人们试图对人工韧带进行表面修饰来弥补因韧带自身材料特性所致的后续问题,因此生物活性物质对聚对苯二甲酸乙二醇酯人工韧带表面修饰成为解决腱骨愈合问题的方案之一。人工韧带植入后细胞和韧带表面作用需要经历3个阶段:黏附、增殖和分化。其中黏附是细胞与人工韧带相互作用的第一个阶段,也是最重要的阶段,将直接影响之后的增殖和分化阶段。换而言之,人工韧带的材料表面特性通过影响骨髓间充质干细胞的增殖分化进而对骨组织是否能够长入韧带两端起关键作用。纳米材料的结构特点增加了韧带的亲水性,使细胞(例如在腱-骨愈合中起关键作用的骨髓间充质干细胞[13])有效黏附在韧带表面并促进进一步增殖分化。 纳米羟基磷灰石:是目前研究比较广泛的纳米材料。人工韧带植入后随着纤维组织长入包裹韧带,韧带的强度得到一定增强,但仍有研究表明长入韧带两端的纤维组织不能达到理想的效果而导致重建失败。促使骨长入韧带是解决这一问题的思路之一[14]。纳米羟基磷灰石的超微结构与生物骨组织相似,并且拥有优异的生物相容性[15]。KUBASIEWICZ-ROSS等[16-18]用实验证实了纳米羟基磷灰石能促进成骨细胞的增殖分化,从而促进新骨形成。骨的长入可以提高人工韧带韧度和强度,同时能够明显促进LRAS人工韧带在骨隧道内与骨界面的愈合。 纳米羟基磷灰石复合材料:纳米羟基磷灰石复合材料也是可供选择的材料之一。找到可以和纳米羟基磷灰石产生协同作用,促进骨髓间充质干细胞活性或者提高生物兼容性,更好地模拟细胞外环境,增强细胞黏附作用的材料,与羟基磷灰石形成复合材料所制作的涂层也是解决人工韧带缺陷的途径。HE 等[19]发现壳聚糖-纳米羟基磷灰石复合材料在仿生过程中具有良好的矿化活性,提高成骨水平,并且人们发现这种复合材料拥有促进骨髓间充质干细胞附着和增殖的功能。JIANG等[20]发现纳米羟基磷灰石与丝素蛋白的复合物有明显促进韧带-骨界面愈合的效果,其诱导成骨细胞黏附和增殖分化的能力也比较明显。 生物活性玻璃是一种主要由Si、Na、Ca、P的氧化物组成,具有良好生物活性和生物兼容性的优良生物材料,能够改善人工韧带表面生物学性能,显著提高细胞与韧带之间的黏附性,并能减少炎症反应的发生。STROBEL等[21]合成了一种直径为30-35 nm的Sr-掺杂纳米生物活性玻璃,评估其对人骨髓间充质干细胞成骨分化能力的影响,结果发现这种纳米生物活性玻璃显著增强了骨钙蛋白、Ⅰ型胶原蛋白和血管内皮生长因子的表达,促进人骨髓间充质干细胞的成骨分化和血管生成。LI等[22]发现纳米羟基磷灰石和生物活性玻璃的复合材料在增加人工韧带的生物相容性、刺激骨形态发生蛋白和血管内皮生长因子的表达、诱导腱骨愈合等方面都有不错的效果。 透明质酸、壳聚糖:透明质酸是一种在软组织中广泛存在的天然多糖,对正常细胞外基质结构的维持有关键作用。BARBUCCI等[23]发现透明质酸涂层能够促进骨细胞黏附、增殖及分化。壳聚糖为可降解聚阳离子多糖,氨基葡萄糖是其降解产物,具有良好的生物兼容性有。YANG等[24]发现壳聚糖可促进前成骨细胞的黏附增殖,通过提高碱性磷酸酶的活性来加速细胞分化。陈世益等[25]的研究证实,聚对苯二甲酸乙二醇酯人工韧带材料表面经壳聚糖、透明质酸纳米自装涂层处理后,植入体内后能通过增强整合素β1(一种介导细胞和细胞外基质、细胞和细胞间黏附的膜糖蛋白,调控成骨和骨吸收)表达来促进人骨髓间充质干细胞的黏附、增殖和分化,这两种材料的作用与纳米羟基磷灰石作用相似,但作用稍弱。有研究称壳聚糖、纳米羟基磷灰石复合材料能促进成纤维细胞的黏附,效果优于单纯纳米羟基磷灰石[26]。 纳米Fe3O4:磁性纳米粒子是一种良好的成骨诱导材料,能够明显促进骨髓基质干细胞向成骨细胞分化,提高碱性磷酸酶活性,增加骨钙蛋白基因和Ⅰ型胶原基因的表达[27],因此可以作为修饰聚对苯二甲酸乙二醇酯韧带的涂层材料。俞斌等[28]的实验表明,纳米Fe3O4对细胞增殖具有一定的促进作用,但自身对细胞黏附并无促进作用,因此需要依赖其他材料来促进细胞与纳米材料的黏附,进而产生作用。在海洋生物贻贝体内提取的含有邻苯二酚基团的左旋多巴胺(贻贝分泌的黏附蛋白的一种,使贻贝能够黏附在各种有机物表面)可以成为解决方法。LI等[29]发现多巴胺涂层有效增加了材料对细胞的促进黏附作用。俞斌等实验中制作的纳米Fe3O4多巴胺涂层能够有效促进细胞黏附和增殖,同样证明了这一点。 2.3 纳米纤维韧带支架 传统韧带移植的失败多与复制韧带复杂的分级结构上存在技术困难,以及肌腱和韧带的固有力学性能有关。纳米支架应用于韧带肌腱的重建目的在于模仿肌腱和韧带组织的层次结构。与促进细胞生长相结合材料的选择是决定损伤部位组织结构能否再生的关键因素,对于年轻患者和运动员来说应该提供天然或合成生物可吸收材料,因为他们的细胞代谢活动比较旺盛[30];相反,非吸收(惰性)材料常是老年人韧带替换的首选[31]。理想的支架应该满足以下几点:能够提供良好的细胞界面,利于细胞黏附、增殖和分化;良好的生物相容性,材料和代谢产物不会产生炎症和毒性反应;合适的生物降解性;三维立体多孔结构,提供细胞生长空间;合适的生物力学强度[32-33]。有一种很有前途的模拟肌腱韧带分层结构的方法:将纳米纤维束紧密排列,以获取令人满意的机械强度和刚度,避免产生孔隙而降低韧带性能;并且用一层仿生鞘将紧密排列的纳米纤维束包裹,使支架内的纳米纤维束进一步紧实,从而更容易达到理想的力学性能。同时,包绕纳米纤维的鞘需要具备一定孔隙结构,以使得细胞可以穿越这层鞘,至少也应该允许体液将营养物质带给支架内的细胞。目前,静电纺丝技术在生产单束纳米纤维及组装韧带支架层次结构方面是最有前途的技术之一[34]。静电纺丝技术示意图见图2,静电纺丝技术制备的纳米纤维示意图见图3。 "

2.3.1 纳米纤维韧带支架的进展 共纳入5篇文献,将分别介绍5种韧带支架的性能,性能总结见表1。 静电纺丝聚(ε-己内酯)/丝素蛋白纳米纤维支架:丝素蛋白是从蚕丝中提取出的天然高分子蛋白,能够为细胞提供丰富的黏附位点,并促进细胞增殖。聚己内酯具有良好的可降解吸收性和力学性能。钱宇娜等[35]通过乳化静电纺丝技术制备的聚ε-己内酯/丝素蛋白混合纤维支架具备“壳-心”结构,并可以保持丝素蛋白天然的β-折叠结构。在实验中随着丝素蛋白的加入,改善了纳米纤维的形态,减小了纳米纤维的直径,增加了材料的亲水性。在细胞增殖方面,这种混纺形式的纳米纤维能够促进韧带成纤维细胞的增殖。由此证明该材质的纳米纤维是一个具有应用潜力的生物材料,适合于韧带组织工程修复。 多尺度电纺聚-L-乳酸纳米纤维支架:SENSINI等[36]报告了一种多尺度电纺聚-L-乳酸纳米纤维支架,在高速旋转的滚筒收集器上利用静电纺丝技术制备了类似于肌腱韧带束状纤维的聚-L-乳酸单束,将多个单束紧密排列形成聚-L-乳酸束,将多个聚-L-乳酸束用通过电纺得到类似腱鞘的鞘结构来模拟完整的肌腱、韧带结构。所有的束紧密放置并沿轴向排列,呈现多孔结构的外鞘完全包裹所有的束。将鞘内的纳米纤维旋转,使得支架的总直径减小,并且在同一截面上可以得到更多的纳米纤维束,提高了机械强度。最终得到的支架既具有类似于肌腱和韧带宏观结构的组织层次,也具有纳米层次的微观结构。扫描电镜观察下聚-L-乳酸单束纳米纤维光滑连续无缺损。 该支架的力学性能也得到了测试,单束纤维和支架均表现出类似于肌腱韧带的非线性脚趾区,在脚趾区之后又同样表现出类似于天然肌腱和韧带的线性弹性行为。这种支架和单束纤维也表现出极高的延展性,支架需要较高的能量才足以破坏,这无疑提供了一个广泛的安全系数。对于单束纤维来说,支架刚度和最大表面应力和人体韧带相当,而最大形变范围超过了正常人体肌腱,这表示在受到破坏之前可以吸收更多的能量。支架的表观刚度和最大形变范围与人体相似。在单个纤维束被破坏后,外鞘的紧密包裹使其和其他未被破坏的纤维束保持在一起,这种效应能够提供更好的结构性能。 细胞增殖培养测试显示,人体的成纤维细胞可以附着在这种支架上,并且细胞活性及数量随着时间推移不断增加,外鞘上的多孔结构允许细胞在静态培养条件下14 d后向支架内部生长和迁移。利用苏木精-伊红染色可以观察到在多尺度层次支架的所有区域都存在细胞,细胞在支架的各个空间内紧密排列,类似于肌腱韧带束内的细胞排列。 聚乙烯醇纳米纤维支架:白利明等[37]利用聚乙烯醇制备类一种纳米纤维支架,用喷丝技术得到单束纳米纤维,将20条聚乙烯醇纤维平行编成1股作为编织的丝束,用3股这样的丝束编织韧带支架。通过在支架上培养韧带细胞和用电子拉力机分别对支架的细胞增殖能力和力学性能进行测试,结果发现支架的最大负荷为(169.78±9.18)N,线性刚度为(71.17±3.52)N/mm,最大应变为(11.67±1.38)%,极限应力为(52.21±2.88)MPa,弹性模量为(435.57±43.99)MPa。应力-应变曲线显示出非线性变化的特征,从曲线中可以清晰地看到脚趾区、线性区和断裂区,这种力学变化特征与肌腱韧带组织相似。极限抗张强度也达到了人膝关节韧带的力学要求。在细胞增殖实验中,亲水性材料有助于细胞黏附[38],聚乙烯醇亲水性较好,通过与黏附蛋白结合增加细胞黏附性。前交叉韧带细胞和NIH3T3(成纤维细胞系)细胞均可在支架上黏附生长,在支架材料上可以观察到较多的细胞分泌的纤维丝状物质,同时前交叉韧带细胞可以在支架上分泌Ⅰ、Ⅲ型胶原蛋白,并且表达水平增高,证明该支架可以为细胞增殖分化提供良好的环境。 聚羟基丁酸己酯/聚左旋乳酸纳米纤维支架:陈辉等[39]将聚羟基丁酸己酯和聚左旋乳酸按1∶1的比例融合,预先将聚羟基丁酸己酯/聚左旋乳酸制备成瓦片状形态膜片,表面以羟基丁酸己酯/聚左旋乳酸制成的纺丝进行反复缠绕,形成“三明治”样结构,即在一个瓦片状的膜片前后以纺丝编织成网状,总厚度为1.5 mm,内层膜片1 mm,外层缠丝0.5 mm。在力学测试中该支架具有良好的力学性能,同时在支架中加入胶原形成羟基丁酸己酯/聚左旋乳酸胶原杂化纳米纤维支架依旧具有良好的力学性能。将成纤维细胞移植至杂化支架上培养,观察到大量细胞在支架上黏附,生长良好,在支架材料内长入大量伪足。 聚己内酯的仿生纳米纤维支架:林子锋[40]利用静电纺丝技术制备聚己内酯纳米纤维支架,该支架纳米纤维具有“随机-取向-随机”的结构,包括插入骨隧道的区域(纤维随机区域)和韧带区域(纤维取向区域),两两区域之间分别存在一个纤维方向过渡的区域。纤维表面光滑,结构完整,两端随机取向区域表面覆盖一层磷酸钙矿物晶体(属于缺钙型羟基磷灰石)。通过力学测试发现该支架具有较高的极限抗张强度,达到(38.7±6.2)MPa,接近于天然韧带。在细胞增殖方面,这种具有“随机-取向-随机”纤维排列方向的聚己内酯支架能够控制不同区域细胞的形貌和排列方向,在取向区域细胞平行排列并呈现出与肌腱细胞相似的长梭形,在随机区域则呈与骨细胞相似的多边形或圆形。另外,取向区域的干细胞成腱基因表达增强,腱调蛋白表达量提高,而随机区域成骨基因和骨钙素表达增强。 2.3.2 无机纳米材料对纳米纤维韧带的修饰 氧化石墨烯表面含有大量例如羟基、环氧基和酚基等含氧集团,易于进行结构功能化修饰,可以和其他材料制作复合支架,是组织工程中具有广阔前景的新型纳米材料。单纯氧化石墨烯具有一定的毒性,这种毒性和氧化石墨烯浓度有关,将氧化石墨烯进行功能化可有效降低这种毒性,例如在小鼠体内放置聚乙二醇修饰的氧化石墨烯,经肝脏代谢后随尿液和粪便排出体外而未形成明显的毒性反应[41]。用碳纳米管和氧化石墨烯修饰的聚乳酸支架表面粗糙度增加,增加了与细胞的接触面积,并且提升了骨髓间充质干细胞的成骨分化和Ⅰ型胶原的形成[42]。值得注意的是,氧化石墨烯促进骨髓间充质干细胞增殖分化的作用具有一定的浓度依赖性,即高浓度的氧化石墨烯抑制骨髓间充质干细胞增殖分化,而较低浓度的氧化石墨烯促进其增殖分化。 2.3.3 纳米纤维韧带的骨连接问题 受体骨骼和韧带的充分连接是再生韧带应用于临床的关键点之一。纳米纤维韧带与骨的连接必须拥有足够的强度,避免应力集中,并促进组织生长。LI等[43]着重于研究骨与韧带连接界面,他们制备了拥有磷酸三钙矿化梯度的聚乳酸-羟基乙酸共聚物和聚己内酯混合纳米纤维支架,聚己内酯支架具有支持成骨的作用,他们发现随着矿化作用的增强应变值降低而杨氏模量增大。他们随后植入了小鼠前成骨细胞,发现磷酸三钙矿化浓度较高的地方前成骨细胞黏附与增殖十分迅速,这类似于生理韧带-骨界面的非钙化和钙化过渡[44]。为了模拟这种连接产生的界面,研究采用了一种负载纳米羟基磷灰石的聚氨酯脲酯弹性体和聚己内酯混合纳米纤维支架[45],施加模拟体液以促进矿物沉积,在模拟体液作用下矿物梯度变得十分明显。支架上存在的矿物质促进了形态发生蛋白2和蛋白样骨桥蛋白mRNA的表达,同时抑制碱性磷酸酶mRNA的表达。骨髓间充质干细胞在这种支架上由于矿物梯度的作用成熟和分化变得明显,并形成成骨表型的空间梯度。KOLLURU等[46]专注于韧带与骨之间的插入问题,他们开发了聚乳酸-羟基乙酸共聚物纳米纤维支架,支架用钙和磷酸盐组成的溶液进行处理形成不同程度的矿化,他们发现矿化程度的不同决定了韧带的形态和力学性能。这种材料的高韧度得到保持,不会因为添加了羟基磷灰石而降低强度。HE等[47]提出了一种韧带和骨插入问题的解决方法,用静电纺丝技术得到纳米纤维,在聚左旋丙交酯乙交酯纳米纤维的任意一端和中心放置纳米羟基磷灰石,从而获得所需的梯度,他们描述了纳米纤维的形态和组成,解决了纳米纤维排列的梯度。还有一种比较有意思的解决骨-韧带连接问题的方法,首先将聚己内酯进行3D打印,得到一种网状结构,这类似于骨-韧带连接的骨界面,随后将3D打印得到支架的一部分用电纺聚-L乳酸纳米纤维覆盖,在3D打印支架上形成部分重叠。支架不同位置测到的力学性能如下:杨氏模量:3D打印部分为(43.6±8.1)MPa,电纺部分为(88.96±15.1)MPa,混合部分为(50.6±5.1)MPa;破坏应力:3D打印部分为(1.62±0.27)MPa,电纺部分为(5.21±1.11)MPa,混合部分为(2.57±0.51)MPa。在支架上植入培养的骨髓间充质干细胞,7 d后观察到增殖水平增加[48]。 2.3.4 纳米纤维韧带的抗粘连问题 预防炎症和粘连是成功再生组织的基础,韧带植入后的粘连问题在一定程度上由于成纤维细胞在受伤的肌腱或者韧带表面过度增殖所致,载有抗炎镇痛药物塞来昔布的纳米支架或可成为防止粘连的方案。LI等[49]用静电纺丝法制备了一种双层仿生腱鞘,在鸡模型上的活体数据显示,外层负载释放的塞来昔布足以起到防止粘连的作用。ZHAO等[50]将纳米羟基磷灰石和丝裂霉素溶液加载到聚-L-乳酸支架上获得核-壳纳米纤维,成纤维细胞活力实验结果显示,支架上丝裂霉素的释放可以有效降低细胞粘连和促进细胞凋亡。在大鼠体内模型中这种支架通过介导成纤维细胞的凋亡和胶原蛋白的合成,有效阻止了韧带肌腱损伤处周围的粘连,但并不影响损伤肌腱的愈合效果。LIU等[51]利用电纺技术得到一个聚己内酯纳米纤维作为外层,内层是聚己内酯/纳米羟基磷灰石的混合物,将这种支架放置在受伤肌腱上表现出令人鼓舞的抗黏附性能。在一项研究中制备了一种纳米纤维双层支架,首先利用电纺技术得到第一层纳米纤维,在第一层的基础上利用静电纺丝技术得到载有血小板衍生生长因子BB的1,3-二苯基-2-吡唑啉纳米纤维,这种支架上释放的血小板衍生生长因子可以促进肌腱细胞的增殖[52]。 "

| [1] LIU CF, ASCHBACHER-SMITH L, BARTHELERY NJ, et al. What we should know before using tissue engineering techniques to repair injured tendons: a developmental biology perspective. Tissue Eng. 2011;B(17): 165-176. [2] FRANK CB, JACKSON DW. The science of reconstruction of the anterior cruciate ligament. J Bone Joint Surg Am.1997;79(10):1556-1576. [3] LANGE R, VACANTI JP. Tissue engineering. Science. 1993;260(5110): 920-926. [4] SUBRAMONY SD, SU A, YEAGER K, et al. Combined effects of chemical priming and mechanical stimulation on mesenchymal stem cell differentiation on nanofiber scaffolds. J Biomech. 2014;4(9):2189-2196. [5] HAMIDO F, Al HARRAN H, Al MISFER AR, et al. Augmented short undersized hamstring tendon graft with LARS artificial ligament versus fourstrand hamstring tendon in anterior cruciate ligament reconstruction:preliminary results. Orthop Traumatol Surg Res. 2015; 101(5):535-538. [6] 施犇,陈烁,周立武,等.自体腘绳肌腱与LARS韧带重建前交叉韧带中期疗效比较[J].中国矫形外科杂志,2018,26(16):1005-8478. [7] LI H, TAO H, CHO S, et al. Difference in graft maturity of the reconstructed anterior cruciate ligament 2 years postoperatively: a comparison between autografts and allografts in young men using clinical and 3.0-T magnetic resonance imaging evaluation. Am J Sports Med.2012;40(7):1519-1526. [8] 潘知常.前交叉韧带重建移植材料的进展[J].世界最新医学信息文摘,2018,18(5):1671-3141. [9] SACCOMANNI B. Graft fixation alternatives in anterior cruciate ligament reconstruction. Musculoskelet Surg. 2011;95(3):183-191. [10] 陈天午,蒋佳,陈世益.人工韧带的临床应用现状及进展[J].宁夏医学杂志,2016,38(8):1001-5949. [11] 黄建明.GRGDSPC多肽表面修饰PET人工韧带促进腱骨愈合的实验[D].上海:中国人民解放军海军军医大学,2013. [12] HUANG JM, LIU HY, CHEN FR, et al. Characteristics of bone tunnel changes after anterior cruciate ligament reconstruction using Ligament Advanced Reinforcement System artificial ligament. Chin Med J. 2012; 125(22):3961-3965. [13] KOBAYASHI M, WATANABE N, OSHIMA Y, et al. The fate of host and graft cells in early healing of bone tunnel after tendon graft. Am J Sports Med. 2005;33(12):1892-1897. [14] NEBELUNG W, WUSCHECH H. Thirty-five years of follow-up of anterior cruciate Ligament-deficient knees in high-level athletes. Arthroscopy. 2005;21(6):696-702. [15] WANG X, LI Y, WEI J, et al. Development of biomimetic nanohydroxyapatite/poly(hexamethylene) composites. Biomaterials. 2002;23(24):4787-4791. [16] KUBASIEWICZ-ROSS P, HADZIK J, SEELIGER J, et al. New Nano-Hydroxyapatite in Bone Defect Regeneration: A Histological Study in Rats. Ann Anat. 2017;213:83-90. [17] OLIVEIRA HL, DA ROSA WLO, CUEVAS-SUAREZ CE.Histological Evaluation of Bone Repair With Hydroxyapatite: A Systematic Review.Calcif Tissue Int. 2017;101(4):341-354. [18] LIU Y, WANG G, GAI Y, et al. In vitro effects of nanophase hydroxyapatite Particles on proliferation and osteogenic differentiation of bone marrow-Derived mesenchymal stem cells. J Biomed Mater Res A. 2009; 90(4):1083-1091. [19] HE Y, DONG Y, CUI F, et al. Ectopic osteogenesis and scaffold biodegradation of nano-hydroxyapatite-chitosan in a rat mode. PLoS One. 2015;10(8):e0135366. [20] JIANG J, WAN F, YANG J, et al.Enhancement of osseointegration of polyethylene terephthalate artificial ligament by coating of silk fibroin and depositing of hydroxyapatite. Int J Nanomedicine. 2014;9: 4569-4580. [21] STROBEL LA, HILD N, MOHN D, et al. Novel strontium-doped bioactive glass nanoparticles enhance proliferation and osteogenic differentiation of human bone marrow stromal cells. Nanopart Res. 2013;15(7):1-9. [22] LI H, GE Y, WU Y, et al. Hydroxyapatite coating enchances polyethylene terephthalate artificial ligament graft osseiontegration in the bone tunnel. Int Orthop. 2011;35(10):1561-1567. [23] BARBUCCI R, TORRICELLI P, MILENA F, et al. Proliferative and re-defferentiative effects of photo-immobilized mi-cro-patterned hyaluronan surfaces on chondrocyte calls. Biomaterials. 2005;26(36): 7596-7605. [24] YANG X, CHEN X, WANG H. Acceleration of osteogenic differentiation of preosteoblastic cells by chitosan containing nanofibrous scaffolds. Biomacromolecules.2009;10(10):2772-2778. [25] 陈世益,蒋佳,吴凌翔,等.PET人工韧带材料纳米化对骨髓基质干细胞粘附、增殖及分化影响的实验研究[J].中国运动医学杂志, 2010,29(5):1000-6710. [26] 黄棣,李吉东,左奕,等.壳聚糖修饰纳米羟基磷灰石/聚酰胺复合多孔支架的制备和性能研究[J].功能材料,2009,40(7):1175-1178. [27] MARKAKI AE, WILLIAM C. Magneto-mechanical stimulation of bone growth in a bonded array of ferromagnrtic fibres. Biomaterials. 2004; 25(19):4805-4815. [28] 俞斌,丁惠锋,杨超华,等.Fe3O4涂层多巴胺修饰PET人工韧带对MC3T3-E1细胞粘附、分化影响的实验研究[J].中国运动医学杂志,2016,35(5):438-444. [29] LI Y, SHI Y, DUAN S, et al. Electrospun biodegradable polyorganophosphazene fibrous matrix with poly(dopamine)coating for bone regeneration. Biomed Mater Res A.2014;102(11):3894-902. [30] WOO SL, DEBSKI RE, ZEMINSKI J, et al. Injury and repair of ligaments and tendons. Annu Rev Biomed.2000;2:83-118. [31] CHEN J, XU J, WANG A, et al. Scaffolds for tendon and ligament repair:Review of the efficacy of commercial products. Expert Rev Med Devices. 2014;6(1):61-73. [32] MOSHIRI A, ORYAN A. Tendon and Ligament Tissue Engineering,Healing and Regenerative Medicine. Sport Med.Doping Stud. 2013;3(3): 2161-0673. [33] MOSHIRI A, ORYAN A. Role of tissue engineering in tendon reconstructive surgery and regenerative medicine: Current concepts, approaches and concerns. Hard Tissue. 2012;1(1):2050-2303. [34] WALDEN G, LIAO X, DONELL S, et al. A Clinical,Biological,and Biomaterials Perspective into Tendon Injuries and Regeneration. Tissue Eng. 2017;23(1):44-58. [35] 钱宇娜,李林昊,李海滨,等.静电纺丝聚(ε-己内酯)/丝素蛋白纳米纤维支架应用于韧带组织工程修复[J].医用生物力学,2009, 24(S1):147. [36] SENSINI A, GUALANDI C, FOCARETE ML. Multiscale hierarchical bioresorbable scaffolds for the regeneration of tendons and Ligaments. Biofabrication. 2019;11(3):035026. [37] 白利明,陈鸿辉,叶春婷,等.编织聚乙烯醇支架材料构建前交叉韧带的生物相容性和力学性能分析[J].中国矫形外科杂志,2009, 17(10):769-773. [38] 葛泉波,何淑兰,毛津淑,等.生物材料与细胞相互作用及表面修饰[J].化学通报,2005,68(1):43-48. [39] 陈辉,张春礼,杨清芳,等.新型前交叉韧带支架材料的构建及其生物相容性的实验[J].科学技术与工程,2007,7(24):6305-6308. [40] 林子锋.基于聚己内酯的仿生韧带构建前十字交叉韧带组织工程的实验研究[D].广州:华南理工大学,2017. [41] YANG K, WAN J, ZHANG S, et al. In vivo pharmacokinetics,long-term biodistribution,and toxicology of PEGylated graphene in mice. ACS Nano. 2011;5(1):516-22. [42] LA WG, PARK S, YOON HH, et al. Delivery of a therapeutic protein for bone regeneration from a substrate coated with graphene oxide. Small. 2013;9(23):4051-4060. [43] LI X, XIE J, LIPNER J, et al. Nanofiber scaffolds with gradations in mineral content for mimicking the tendon-to-bone insertion site. Nano Lett. 2009;9(7):2763-2768. [44] RAMALINAGM M, YOUNG MF, THOMAS V, et al. Nanfibe scaffold gardients for tissue engineering. J Biomater Appl. 2013;27(6):695-705. [45] CROSS LM, THAKUR A, JALILI NA, et al. Nanoengineered biomaerials for repair and regeneration of orthopedic tissue interfaces. Acta Biomater. 2016;42:2-17. [46] KOLLURU PV, LIPNER J, LIU W, e tal. Strong and tough mineralized PLGA nanofibers for tendon-to-bone scaffolds. Acta Biomater. 2013; 9(12):9442-9450. [47] HE J, QIN T, LIU Y, et al. Electrospinning of nanofibrous scaffolds with continuous structure and material gradients. Mater Lett.2014;137:393-397. [48] CRISCENTI G, LONGONI A, LUCA AD,et al.Triphasic scaffolds for the regeneration of the bone-ligament interface. Biobabrication. 2016; 8(1):015009. [49] LI L, ZHENG X, FAN D, et al. Release of celecoxib from a bi-layer biomimetic tendon sheath to prevent tissue adhesion. Mater Sci Eng C. 2016;61:220-226. [50] ZHAO X, JIANG S, LIU S, et al. Optimization of intrinsic and extrinsic tendon healing through controllable watersoluble mitomycin-C release from electrospun fibers by mediating adhesion-related gene expression. Biomaterials. 2015;61:61-74. [51] LIU S, ZHAO J, RUAN H, et al. Biominmetic Sheath Membrane via Electrospinning for Antiadhesion of Repaired Tendon.Biomacromolecules. 2012;13(11):3611-3619. [52] EVROVA O, HOUSKA J, WELTI M, et al. Bioactive, Elastic, and Biodegradable Emulsion Electrospun DegraPol Tube Delivering PDGF-BB for Tendon Rupture Rapair. Macromol Biosci. 2016;16(7): 1048-1063. |
| [1] | Che Yanjun, Hu Dan, Si Weibing, Gu Xueping, Hao Yuefeng. Bone cement interval perfusion in hyperextension position for treatment of senile osteoporotic vertebral compression fractures [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(10): 1555-1561. |
| [2] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [3] | Xu Feng, Kang Hui, Wei Tanjun, Xi Jintao. Biomechanical analysis of different fixation methods of pedicle screws for thoracolumbar fracture [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1313-1317. |
| [4] | Jiang Yong, Luo Yi, Ding Yongli, Zhou Yong, Min Li, Tang Fan, Zhang Wenli, Duan Hong, Tu Chongqi. Von Mises stress on the influence of pelvic stability by precise sacral resection and clinical validation [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1318-1323. |
| [5] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [6] | Zhang Yu, Tian Shaoqi, Zeng Guobo, Hu Chuan. Risk factors for myocardial infarction following primary total joint arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1340-1345. |
| [7] | Wei Wei, Li Jian, Huang Linhai, Lan Mindong, Lu Xianwei, Huang Shaodong. Factors affecting fall fear in the first movement of elderly patients after total knee or hip arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1351-1355. |
| [8] | Wang Jinjun, Deng Zengfa, Liu Kang, He Zhiyong, Yu Xinping, Liang Jianji, Li Chen, Guo Zhouyang. Hemostatic effect and safety of intravenous drip of tranexamic acid combined with topical application of cocktail containing tranexamic acid in total knee arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1356-1361. |
| [9] | Xiao Guoqing, Liu Xuanze, Yan Yuhao, Zhong Xihong. Influencing factors of knee flexion limitation after total knee arthroplasty with posterior stabilized prostheses [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1362-1367. |
| [10] | Huang Zexiao, Yang Mei, Lin Shiwei, He Heyu. Correlation between the level of serum n-3 polyunsaturated fatty acids and quadriceps weakness in the early stage after total knee arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1375-1380. |
| [11] | Zhang Chong, Liu Zhiang, Yao Shuaihui, Gao Junsheng, Jiang Yan, Zhang Lu. Safety and effectiveness of topical application of tranexamic acid to reduce drainage of elderly femoral neck fractures after total hip arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1381-1386. |
| [12] | Wang Haiying, Lü Bing, Li Hui, Wang Shunyi. Posterior lumbar interbody fusion for degenerative lumbar spondylolisthesis: prediction of functional prognosis of patients based on spinopelvic parameters [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1393-1397. |
| [13] | Lü Zhen, Bai Jinzhu. A prospective study on the application of staged lumbar motion chain rehabilitation based on McKenzie’s technique after lumbar percutaneous transforaminal endoscopic discectomy [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1398-1403. |
| [14] | Chen Xinmin, Li Wenbiao, Xiong Kaikai, Xiong Xiaoyan, Zheng Liqin, Li Musheng, Zheng Yongze, Lin Ziling. Type A3.3 femoral intertrochanteric fracture with augmented proximal femoral nail anti-rotation in the elderly: finite element analysis of the optimal amount of bone cement [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1404-1409. |
| [15] | Du Xiupeng, Yang Zhaohui. Effect of degree of initial deformity of impacted femoral neck fractures under 65 years of age on femoral neck shortening [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1410-1416. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||

