Chinese Journal of Tissue Engineering Research ›› 2013, Vol. 17 ›› Issue (52): 9055-9061.doi: 10.3969/j.issn.2095-4344.2013.52.019
Previous Articles Next Articles
Bone inductive potential of electron beam melting rapid prototyping technology in the repair of orthopedic implants
Wang Cai-mei, Zhang Wei-ping, Wang Gang, Yan Hui, Yang Xiao-jie, Li Zhi-jiang
- Beijing AKEC Medical Co., Ltd., Beijing 102200, China
-
Revised:2013-11-12Online:2013-12-24Published:2013-12-24 -
About author:Wang Cai-mei☆, Doctor, Senior engineer, Beijing AKEC Medical Co., Ltd., Beijing 102200, China wangcaimei2@163.com
CLC Number:
Cite this article
Wang Cai-mei, Zhang Wei-ping, Wang Gang, Yan Hui, Yang Xiao-jie, Li Zhi-jiang. Bone inductive potential of electron beam melting rapid prototyping technology in the repair of orthopedic implants[J]. Chinese Journal of Tissue Engineering Research, 2013, 17(52): 9055-9061.
share this article

2.1 EBM RP技术简介 EBM RP技术是一种集成了计算机设计、数控、高能电子束和新材料等技术而发展起来的先进制造技术。首先,将零件的三维数字模型进行分层切片处理,得到零件的二维截面信息;进而,运用电子束熔融(EBM)设备专用程序将该截面信息转化成电子束的扫描路径并导入电子束熔融设备之中;之后,设备内控系统通过操作磁偏转线圈控制高能电子束流对设备工作舱内的金属粉末进行逐行扫描,从而按零件截面轮廓的信息有选择地熔化金属粉末,微小的金属熔池相互融合并凝固,连接形成线状和面状金属层,如此层层堆积,直至整个零件全部完成;最后,除去未熔融的粉末便得到所需的三维产品[1-2]。该技术是以逐层增加材料的方法进行制造,与传统去除材料成形的机械加工方式明显不同,属于增材制造(Additive manufacturing,AM)技术。 EBM RP是一种以电子束为能量源的直接金属成型工艺,与以激光为能量源的金属成型工艺相比,EBM RP工艺具有能量利用率高、无反射、功率密度高、聚焦方便、真空环境无污染等优点,在快速原型和快速制造领域的应用具有广阔的前景[3-10]。自20世纪90年代开始国外已经开始了电子束快速成形技术的研究,2001年,瑞典Arcam公司确立EBM RP为其重点开发方向,2003年,Arcam公司在世界上首先推出了商业化的成型设备,并用于外科植入物的生产,之后又凭借其在粉末技术、快速成型精度、效率、成本及零件性能等方面的独特优势,占领国际领先地位。美国Calcam公司采用电子束快速制造技术制备出了全致密、力学性能优于锻件的Ti6Al4V叶轮部件。瑞典Arcam公司采用电子束快速成型技术制造了特殊的钛合金点阵结构及复杂的发动机部件,美国航空航天局、波音公司、洛克希德•马丁公司等计划将该技术应用于空间站、海军无人机、F-35战斗机等型号上,以降低制造成本,缩短研制周期。国内在无法获得设备及相关技术的条件下进行自主开发研究,在钛合金电子束快速成型研究方面也取得了较大的进展:西北有色金属研究院多孔材料国家重点实验室开展了电子束快速成型工艺的研究工作,在钛及钛合金复杂结构及多孔结构的电子束快速制造工艺、应力及变形控制方面积累了实践经验,并制造出复杂的钛合金叶轮样件;清华大学开发的电子束选区同步烧结工艺及三维分层制造设备,已在国内申请专利,并解决了用电子束烧结316 L不锈钢粉末的问题;中航工业制造所从2006年开展该技术的研究,经过多年艰苦努力,在国内实现了电子束快速成形技术在飞机上的首次应用。电子束熔融快速成型已在航空航天、汽车和医疗植入器材等领域显示独特的应用优势,EBM RP技术进入了蓬勃发展的新世代[11-16]。 2.2 EBM RP加工钛合金(Ti6Al4V)产品的性能特点 2.2.1 无模具、复杂形态成型 EBM RP技术属于“分层制造,逐层叠加”的可直接面向产品的成型模式,犹如一台“立体打印机”,理论上不需要任何模具便可以制造工艺许可的任何形状的产品,尤其适合形状复杂金属部件的小批量生产,任何外表奇异内部结构复杂的金属部件都可以一次快速成型。 EBM RP技术高度的柔性加工能力实现了制造业的“所见即所得”,解放了设计者的创作空间,提高了设计的灵活性[16],设计者可以通过改变CAD零件模型不同部分的宏观及微观结构,使零件具有优异的综合性能。在骨科植入物领域,EBM RP的优势不仅在于个性化制造,而且对产品内部及表面结构的可实现性也十分突出,在构建骨科植入物的微观结构方面明显优于传统工艺,特别是对产品的孔形态、孔径、孔隙率以及联通孔隙成型。它可以在特定部位制作成所需的三维多孔结构,不仅实现梯度孔径、自由孔径、三维连通,见图1,而且,金属假体的孔隙率及弹性模量完全由设计决定[17-19],这些特性为骨科植入物的轻量化以及生物固定提供了重要的技术支撑。"

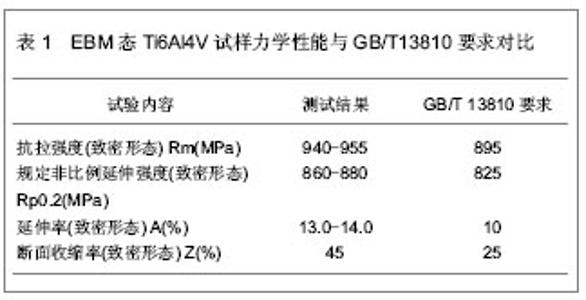
2.2.2 力学性能及显微结构 骨科植入物是医疗器械类高风险产品,其安全性、有效性须经严格的验证。Ti6Al4V是使用最为广泛的钛合金之一,也是骨科植入物常用材料,有70年以上的临床成功应用历史,其力学及生物学性能已得到广泛的认可[20]。 EBM RP技术在金属骨科植入物的应用始于对EBM态Ti6Al4V产品性能的研究。EBM加工Ti6Al4V产品时,成型舱内处于10-2 Pa以上的高真空环境,具有高真空保护的优点,该环境能有效避免空气中氧元素的混入以及其他有害杂质对原材料的影响,这对钛合金类活性金属尤为重要。EBM成型过程中,电子束熔化金属粉末形成熔池并迅速凝固,由于真空环境的保护,散热困难,热量容易累积,致使零件整体温度保持在较高的水平,同时,工件成型舱室内温度维持于600-700 ℃,相当于零件在加工过程中始终保持钛合金的回火温度,起到了消除残余应力退火的作用,有利于零件强度及塑性的良好匹配和零件组织及性能均一化[21-23]。 GB/T13810(外科植入物用钛及钛合金加工材)标准[22]是锻造Ti6Al4V作为外科植入物材料需执行的国家标准。为了验证EBM态Ti6Al4V材料的力学性能是否符合医疗器械国家标准的要求,作者也运用EBM RP技术制备了Ti6Al4V 试样,其拉伸及延伸性均达到了锻造的质量水平,见表1。"
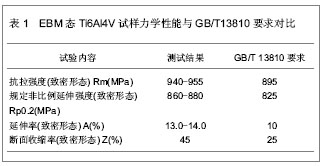

事实上,EBM态Ti6Al4V力学性能已达到飞机锻件的水平。锁红波等[23]研究表明用EBM RP技术制造的EBM态Ti6Al4V试样性能优异:与HB5432-89飞机锻件标准的下限值相比,抗拉强度高出19%,屈服强度提高12%,延伸率提高49%,断面收缩率提高121%,塑性指标提高明显。 杨鑫等[24]研究了EBM态Ti6Al4V的内部质量。他认为,EBM态Ti6Al4V产品的显微组织主要为针状α+β相,在晶界残余了少量原始β相,相与相之间互相交织而成为网篮状,这是由于在扫描结束的瞬间,熔池温度猝然下降使得高温相来不及扩散而保存下来所致;试样显微组织均为细小的针状相,且截面中均无孔隙和裂纹存在,这是因为该工艺过程中一直存在着固态金属粉末、液态熔池和已凝固部分这3种状态;凝固的顺序自下而上,自然冷却,具有明显快速凝固技术中晶粒细小的特征,晶粒越细小产生的晶界越多,而晶界不但可以阻碍滑移还能够阻碍裂纹的扩展,随着晶界数量的增多,在每一晶界处的应力集中就更小。因此细化晶粒不仅可以提高金属材料的强度,同时还可以提高其韧性[25]。作者也将自制EBM态Ti6Al4V试棒进行电子扫描镜观察,得到相似的结果,见图2。"


由此可知,由EBM RP技术制备的Ti6Al4V产品,其力学性能均达到或超过了骨科领域钛合金锻件的标准,其显微组织致密、均匀,EBM 态的Ti6Al4V骨科植入物产品机械性能得到了充分保障。 2.3 EBM RP技术在骨科植入物领域中应用 2.3.1 个性化的植入物 人体骨骼存在个体的差异性,这种差异包括骨骼解剖学差异及由于骨质缺失导致的骨骼变异,个性化的植入物源于对个体骨骼的匹配及适应。人体骨骼具有不规则性及个体差异性,而标准化的骨科植入物最大的问题是就是缺乏个体匹配性,因此常常无法适应不同个体骨组织解剖形态的要求,直接导致软组织形态及功能受限、植入系统功能及性能不良、生物力学效果不佳、植入物假体寿命受到影响等问题。另外,骨科临床中常见的棘手问题之一是由于感染、肿瘤、创伤等原因造成的骨质缺失,而且骨缺损的状态更为多样、不可预测。通常,缺损的重建需依靠骨移植来完成,由于人体自身的骨质在强度、弹性和再生能力等方面具有明显的优势,自体骨移植是较常用的方法,但需要在患者自己身体的另一个部位取骨,这会造成额外创伤并面临取骨部位伤口感染和愈合的问题,而且骨源有限,因此,很多情况下,需要采用异体骨,即骨库中储存的他人捐赠的骨质。异体骨有较强的骨传导作用,但骨诱导作用较弱,且没有成骨潜能,即使经过了严格的消毒,仍存在感染和传播疾病的风险[26-27]。因此,最理想的治疗方法便是根据患者骨骼解剖或缺失情况进行定制化治疗及定制化植入体的设计,同步解决内植物功能及骨骼解剖修复问题。 EBM技术制造的个性化植入物所依据的是患者自身的骨骼数据。首先,通过CT或MRI提取患者的骨骼信息(即使在患者骨质完全缺失的情况下仍可以根据对侧健骨数据镜像生成),以保证人工植入体最大限度符合解剖学需要;之后,根据医生的治疗方案以及该患者的数据进行个性化植入体的计算机辅助设计,并加以仿真模拟及力学验证;最后,通过EBM技术完成个性化植入物的快速制作。EBM的个性化技术可以应用于个体化人工关节置换、个体化接骨钣、个体化骨盆修复等临床手术。过去,在骨盆肿瘤手术等高难度骨科手术中,定制化设计只能根据平面X射线片,数据的准确性也受到严重质疑,现在,依托快速成型技术,可精确定制出一个与患者一模一样的骨盆。2005年,一位来自江西的普通工人,右侧骨盆生了一个头颅大小的肉瘤,中国工程院院士戴尅戎教授准备给他施行人工半骨盆置换以保全他的臀部和下肢,但是,传统的半骨盆假体很难跟患者骨盆的残余部分完全吻合。为了解决这个问题,戴尅戎教授将快速成型技术引入临床,手术非常成功[28]。快速成型技术除了用于骨科,在整复外科、口腔科、眼科也能发挥出独特的作用。2011年比利时和荷兰的科学家成功为一个83岁的女性植入了通过快速成型制造的下颌骨[29],该人工下颌骨仅比生理下颌骨重30 g,手术历时4 h,比传统的手术节约近16 h,且患者功能恢复良好。在国内,运用快速成型技术进行的定制化骨科植入物的开发技术也已经成熟,但该类产品的应用尚需经历进一步的临床验证以及严格的注册审评才能面世[30]。 2.3.2 多孔类骨小梁植入物假体 骨科植入物领域中一个重要课题就是如何降低植入假体的远期松动的风险,核心是解决假体固定的问题。骨科植入物的生物固定根据骨组织长入假体方式及深度分为骨长入与骨长上两种模式[31]。常见的粗糙表面(喷砂、喷丸),等离子喷涂表面(钛粉、羟基磷灰石),烧结表面(钛珠、钛丝)等[32],骨质只能对植入物假体产生包饶型附着,被称为“骨长上”,而具有骨长入能力的金属植入物可诱导骨细胞长入植入物内部,被称为“骨长入”。“骨长入”比“骨长上”有更强的骨床与假体的结合力,可进一步促进假体-骨界面的骨性愈合,减轻假体与宿主骨之间的机械剪切应力, 降低应力遮挡的发生,最大限度延长假体使用寿命。研究表明,具有孔隙结构的材料能促进营养物质和代谢产物的运输,加速细胞的黏附及血管与神经的长入,为“骨长入”提供结构性骨诱导条件,引导骨细胞长入植入物内部[33],这种具有孔隙结构的材料被称为多孔金属植入物材料,该类植入物亦被称为多孔金属植入物。 从骨的结构来看,松质骨为骨小梁连接构成的网状框架结构,见图3,孔隙率为50%-90%,孔径约 1.0 mm,皮质骨结构致密,孔隙率为3%-12%。当多孔金属植入物具有与人体骨小梁相似的3D连通的孔隙的立体网状结构以及接近人体骨组织的弹性模量时,被称为金属骨小梁或3D骨小梁金属,见图4[34],该金属多孔结构亦被称为“类骨小梁结构”。研究表明,类骨小梁结构的金属骨植入物具有很好的骨长入能力,可以支持人体骨骼细胞在其中生长,使植入物与骨骼之间形成坚强的绞锁,极大地增加了植入物与骨床的结合能力,促进假体-骨界面的骨性愈合,从而延长假体使用寿命,有望成为高质量的骨替代材料[6]。由于孔径及孔隙率影响细胞黏附、细胞向内生长的速度及深度,因此,探索孔径大小对骨形成的影响以及骨缺损修复和新骨长入的最佳孔径已引起国内外专家与学者的关注,目前认为大于300-1 500 μm的孔径、孔隙率60%-90%有利于骨的生成,而且不同的部位对孔隙的要求也不尽一致,目前尚缺乏统一的标准[35-36]。"


EBM 技术“所见即所得”的特点使EBM RP成为制备金属骨小梁的有效方法之一。EBM技术能够根据需要设定孔隙率、孔径的大小、形态以及孔隙间的连通率,甚至可以根据需要设定具有功能梯度的孔径,从而达到微孔表面和植入物强度、刚度之间的平衡[37]。以金属骨小梁生物固定髋臼杯为例,EBM技术可以在臼杯表面形成功能梯度孔径的微孔表面(即类骨小梁结构层),而在臼杯的内部根据配合的要求或强度的需要制作成微孔结构或致密结构,其中,类骨小梁层具有结构性骨长入条件,术后将形成良好的骨长入,封闭溶骨素侵入通路,有效减缓骨质退化萎缩;致密层可以确保与相关部件配合及强度的可靠;功能梯度孔径结构同时可以降低假体的弹性模量,使之与宿主骨更加接近,减少或消除应力遮挡,获得假体长期的坚强固定,延长人工关节使用寿命[38];该技术可以使假体和表面处理一次成型,节省制造时间和费用。 EBM 态Ti6Al4V多孔材料具有类骨小梁结构,理论上具有良好的结构性骨诱导作用,专家学者力图从实验室验证这一特点。Palmquist等[39]评估了用EBM RP加工而成的Ti6Al4V植入物的远期骨整合和生物相容性的效果。他将电子束熔融加工的多孔式和实心式植入物植入到羊的股骨两侧和背部皮下,植入物以及其周边包围的组织在26周后被取出,组织反应的定性和定量检测使用了组织学和光学显微形态测量学方法,评价方式采用了扫描式电子显微镜、能量色散X射线光谱仪和微计算机断层扫描。结果显示,多孔和实心的植入物双双出现了骨整合,而且在多孔植入物上观察到了程度很高的骨-植入物交联现象,骨整合效果更佳。 EBM态多孔材料具有与传统制作的产品不同的形貌,因此,EBM态Ti6Al4V金属骨小梁和传统金属臼杯的离子水平是否有差异是值得探讨的问题。Bistolfi等[40]通过实际临床验证消除了这一顾虑,他对比了10例采用传统锻造钛金属臼杯和10例采用EBM态的Ti6Al4V金属骨小梁假体,分析了术后1周、3个月和6个月患者尿液和血液中铝离子、钒离子和钛离子的浓度,事实表明两组间在各时间段都不存在差异,同组在不同时间段也不存在差异,因此,可以说EBM态Ti6Al4V金属骨小梁和传统金属臼杯的离子水平无差异。 2.4 EBM技术制作骨科植入物的成功应用 2003 年,瑞典的Arcam AB 公司在全球首先推出了商业化的成型设备,并用于外科植入物的生产。2007年,这项技术获得了CE认证,2009年通过FDA认证。从2007到2010年1月1日为止,采用EBM RP技术制造的髋关节产品,仅Lima公司DELTA TT一种产品的临床已经超过5 000例。有文献表明截止到2011年3月,同样采用多孔型外表面的Lima髋臼产品临床已经超过10 000例,临床评价优良[41-42],目前该数字已超过30 000例。 在国内,北京爱康宜诚医疗器材股份有限公司制作的具有3D骨小梁结构的髋关节产品已完成临床,脊柱产品也进入临床观察阶段。从2009年开始北医三院骨科主任刘忠军教授就与北京爱康宜诚医疗器材股份有限公司合作,运用这种EBM RP技术研制具有连通孔隙的空间结构的多孔骨科植入物产品,并进行了一系列的动物实验及临床研究。目前,该项技术已经通过动物实验,其中颈椎椎间融合器、颈椎人工椎体两个产品进入临床观察阶段,人工髋关节已顺利获得临床报告进入注册流程,北京爱康宜诚医疗器材股份有限公司也成为国内第一个将该类产品进行产业化的企业。 2.5 EBM技术在骨科植入物的应用面临的制约及挑战 EBM RP技术因其无需模具、快捷、准确性的优势成为“第三次工业革命”主力军,同时也以其独特的个性化制造满足患者个性化的差异性需求的能力,在人工假体、人工硬组织器官的制造方面有望发挥巨大的推动效应[43]。然而,EBM RP技术在骨科植入物方面的发展仍面临着多方面的瓶颈和挑战: 其一,高成本、高费用、高耗材。EBM电子束熔融快速成型设备由电子发射系统、真空系统、电气控制系统、温度检测控制系统等组成,涉及高能电子束生成技术、计算机和数控等技术,技术含量高,造价昂贵,日常维护费用高;金属粉末材料制作工艺复杂,粉末纯度、稳定性、物理性能、微观形貌将直接影响成型件的成型精度、物化性能[44-47]。目前,国内制粉技术并不成熟;金属粉末都由国外快速成型设备厂家直接提供,尚未实现第三方供应材料的模式,再一次推高了原材料的价格。以上三种因素给EBM RP技术的普及应用带来了困难。 其二,工艺难度高。国外对电子束熔融快速成型设备及材料以及工艺的研究比较成熟,而国内相对滞后,特别是在工艺制作方面的技术难点(扫描线宽与电子束电流、加速电压和扫描速度、扫描方式等[48])尚未成功攻克,国外进口设备厂通常将最优化的方案提供给用户,并将设备与工艺参数绑定,任何一个工艺参数的更改都需要厂家专业人士的参与并通过严格实验的验证,此番举措虽保障了产品质量的稳定,但提高了技术封锁增加了使用者的成本。 其三,精度、效率方面还不尽人意[49]。EBM RP技术的精度受到材料、工艺、设备能力等多方面限制,难以实现高精度零部件直接面向产品的制造;打印精度与速度之间存在严重冲突。因此,如何在保证产品的表面质量、力学和物理性能的基础上,实现快速制造是设备开发商应解决的问题。 其四,配套软件尚需改进[50]。目前,快速成型软件(RP软件)远不如计算机辅助设计软件(CAD、CAE)成熟,诸如骨科植入物多孔微观结构3D数字化模型的几何拓扑的建立仍是难点;其次,RP软件与CAD的集成度也不高,RP软件的辅助设计能力还尚处初级水平,在质量及效率方面难以满足进一步设计优化的要求,这无疑也增加了EBM RP技术运用的障碍。"

| [1] 颜永年,张伟,卢清萍,等.基于离散堆积成形概念的RPM原理与发展[J].中国机械工程,1994,5(4):64-66. [2] 杨鑫,汤慧萍,贺卫卫,等.电子束烧结快速成形技术[J].钛工业进展,2007,24(3)10-14. [3] Simchi A, Petzoldt F, Pohl H. On the development of direct metal laser sintering for rapid tooling.Journal of Materials Processing Technology. 2003;141(3):319-328. [4] Santos EC, Shiomi M,Osakada K,et al.Rapid manufacturing of metal components by laser forming.International Journal of Machine Tools & Manufacture.2006;46 (12/13): 1459-1468. [5] Hollander DA, von Walter M, Wirtz T,et al. Structural, mechanical and in vitro characterization of individually structured Ti-6Al-4V produced by direct laser forming. Biomaterials. 2006;27(7):955-963. [6] 张伟,姚建华,胡晓冬,等.激光直接金属堆积成形技术的研究与应用进展[J].制造业自动化,2008,30(2):4-9. [7] 贾文鹏,汤慧萍,贺卫卫,等.电子束快速成形研究进展及关键问题分析[J].电加工与模具,2010(2):41-44. [8] 周旭光.特种加工技术[M].2版.西安:西安电子科技大学出版社, 2011. [9] Melchels FPW,Domingos MAN,Klein TJ,et al.Additive manufacturing of tissues and organs.Prog Polym Sci. 2010; 37:1079-1104. [10] Murr LE.Additive Layered Manufacturing of Reticulated Ti-6Al-4V Biomedical Mesh Structures by Electron Beam Melting.IFMBE Proc.2009;24:23. [11] Zhou C,Chen Y. Additive manufacturing based on optimized mask video projection for improved accuracy and resolution. Journal of Manufacturing Processes.2012;14(2):107-118. [12] Matz JE,EagarTW.Carbide formation in alloy 718 during electron-beam solid freeform fabrication.Metallurgical and Materials Transection A.2002;33(8):2559-2567. [13] Taminger KMB,Hafley RA.Characterization of 2219 aluminiunl produced by electron beam freeform fabrication[C]. In:Proceedings of the 13th Solid Freeform Fabrication Symposium,eds:Bourell DL,Crawford RH, Beaman JJ,et al. University of Texas At Austin. 2002: 482-489. [14] Taminger KMB,Harley RA,Fahringer DT,et al.Effect of surface treatments on electron beam freeforill fabricated aluminium structures[C].In:15th Solid Freefornl Fabrication Symposium, eds:Bourell DL,Crawford RH,Beanlan JJ,et al.University of Texas,2004:460-470. [15] Cormier D,Harrysson O,West H.Charaeterization of H13 steel produced via electron beam melting.Rapid Prototyping J. 2004;10(1):35-41. [16] 许廷涛.3D打印技术——产品设计新思维[J].电脑与电信,2012 (9): 5-7.[17] Parthasarathy J, Starly B, Raman S,et al.Mechanical evaluation of porous titanium (Ti6Al4V) structures with electron beam melting (EBM).J Mech Behav Biomed Mater. 2010;3(3):249-259. [18] Murr LE, Gaytan SM, Medina F,et al.Next-generation biomedical implants using additive manufacturing of complex, cellular and functional mesh arrays.Philos Trans A Math Phys Eng Sci. 2010;368(1917):1999-2032. [19] Harrysson O,Cansizoglu OD, Marcellin-Little DJ,et al.Direct metal fabrication of titanium implants with tailored mteriaIs and mechanical properties using electron beam melting technology.Materials Science and Engineering: C.2008;28(3): 366-373. [20] Habibovic P, Li J, van der Valk CM,et al.Biological performance of uncoated and octacalcium phosphate-coated Ti6Al4V.Biomaterials. 2005;26(1):23-36. [21] 颜永年,齐海波,林峰,等.三维金属零件的电子束选区熔化成形术[J].机械工程学报,2007, 43(6):87-92. [22] GB/T 13810-2007,外科植入物用钛及钛合金加工材[S].陕西:全国有色金属标准化技术委员会,2008. [23] 锁红波,陈哲源,李晋炜.电子束熔融快速制造Ti-6Al-4V的力学性能[J].航天制造技术,2009,12(6):18-22. [24] 杨鑫,奚正平,刘咏,等.电子束选区熔化技术对钛合金组织和力学性能的影响[J].稀有金属材料与工程, 2009,38(7):1272-1275. [25] Murr LE, Quinones SA, Gaytan SM,et al.Microstructure and mechanical behavior of Ti-6Al-4V produced by rapid-layer manufacturing, for biomedical applications.J Mech Behav Biomed Mater. 2009;2(1):20-32. [26] 邱贵兴,孙世荃.同种异体骨植入材料的临床应用[J].中华骨科杂志, 2004,24(10):635-637.[27] De Long WG Jr, Einhorn TA, Koval K,et al.Bone grafts and bone graft substitutes in orthopaedic trauma surgery. A critical analysis.J Bone Joint Surg Am. 2007;89(3):649-658.[28] 戴尅戎.采用3D打印人骨[N].东方早报,2013-02-02 (A10). [29] 世界首例3D打印下颌移植手术公布[J].世界科学,2012(3):67. [30] 彭如恕,王剑彬,姚奇志.快速原型技术在医学中的应用研究[J].激光杂志,2005,26(3):87-88. [31] Svehla M, Morberg P, Zicat B,et al.Morphometric and mechanical evaluation of titanium implant integration: comparison of five surface structures.J Biomed Mater Res. 2000;51(1):15-22. [32] 李青.人工关节用金属材料的表面处理[J].医疗卫生装备,2000, 21(5):22-24. [33] Thomsen P, Malmström J, Emanuelsson L,et al. Electron beam-melted, free-form-fabricated titanium alloy implants: Material surface characterization and early bone response in rabbits.J Biomed Mater Res B Appl Biomater. 2009; 90(1): 35-44.[34] 陈刚,徐卫东.生物学固定骨小梁金属杯在髋臼翻修中的应用[J].中国矫形外科杂志, 2008,16(20):1544-1546. [35] Palmquist A, Snis A, Emanuelsson L,et al.Long-term biocompatibility and osseointegration of electron beam melted, free-form-fabricated solid and porous titanium alloy: experimental studies in sheep.J Biomater Appl. 2013;27(8): 1003-1016.[36] 李国臣,王林,桑宏勋,等.可控微结构EBM钛合金支架与成骨细胞的体外三维复合培养[J].中国矫形外科杂志,2009,17(24): 1883-1887. [37] 李祥,王成焘,王林,等.可控多孔结构生物活性钛的制备及其体外细胞培养[J].稀有金属材料与工程,2010,39(10):1697-1701. [38] Murr LE,Gaytan SM,Ramirez DA,et al.Metal fabrication by additive manufacturing using laser and electron beam melting technologies. J Mater sci Techn.2012;28(1):1-14. [39] Palmquist A, Snis A, Emanuelsson L,et al. Long-term biocompatibility and osseointegration of electron beam melted, free-form-fabricated solid and porous titanium alloy: experimental studies in sheep.J Biomater Appl. 2013;27(8): 1003-1016.[40] Bistolfi A. Lon levels in trabecular and conventional titanium cups.Orthopaed Traumatol ,2011.[41] Perticarini L.Clinical Outcomes of DELTA TT Cup in Hip Arthroplasty. Reconstructive Review of JISRF,2012. [42] Perticarini L.Delta TT Revision: A New Cup for Hip Revisions.Reconstructive Review of JISRF,2012. [43] Wohlers T.Rapid prototyping,tooling and manufacturing state of the industry annual worldwide progress report. Colorado: Wohlers Associates Inc.,2005. [44] 杨鑫,汤慧萍,葛渊.粉末性能对电子束选区熔化快速成形的影响[J].稀有金属材料与工程,2007,36(Suppl.3):574-576. [45] 齐海波,颜永年,林峰,等.电子束直接熔化技术中的粉末状态分析[J].清华大学学报, 2005,48(8):1012-1015. [46] 韩建栋,林峰,齐海波,等.粉末预热对电子束选区熔化成形工艺的影响[J].焊接学报, 2008,29(10):77-80. [47] 郑元春,齐乐华.原材料制约3D打印发展[J].中国经济和信息化, 2013(13):53. [48] 刘海涛,赵万华,唐一平.电子束熔融直接金属成型工艺的研究[J].西安交通大学学报, 2007,41(11):1307-1310. [49] 杨鑫,汤慧萍,葛渊.粉末性能对电子束选区熔化快速成形的影响[J].稀有金属材料与工程,2007,36(3):574-577. [50] 姜明,齐海波,林峰.电子束选区熔化技术的控制系统设计[J].机械设计与制造,2008(1):189-190. |
| [1] | Liu Jian-kun, Deng Shu-cai. Status and role of three-dimensional printing technology in spine surgery [J]. Chinese Journal of Tissue Engineering Research, 2017, 21(7): 1131-1136. |
| [2] | Wei Zhi-hui, Zhang Ming-hua, Zhao Bo, Min Jing, Qiu Hao, Lu Min-peng. Different doses of rivaroxaban versus enoxaparin for prevention of venous thromboembolism after total hip arthroplasty: a meta-analysis of safety and efficacy [J]. Chinese Journal of Tissue Engineering Research, 2016, 20(53): 8022-8031. |
| [3] | Nuerhanati•Shayilanbieke, Jin Ge-le, Yang Yi, Li Zhong-wei, Yeerzhati•Hazhaheman. Reamed versus unreamed intramedullary nailing for tibial fractures in adults: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2016, 20(39): 5912-5918. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||