Chinese Journal of Tissue Engineering Research
Previous Articles Next Articles
Protein synthesis and resistance in aging skeletal muscle
Wang Shun-li, Shi Reng-fei
- School of Kinesiology, Shanghai University of Sport, Shanghai 200438, China
-
Received:2012-09-03Revised:2012-10-24Online:2013-04-09Published:2013-04-09 -
Contact:Shi Reng-fei, Doctor, Associate professor, School of Kinesiology, Shanghai University of Sport, Shanghai 200438, China rfshi@hotmail.com -
About author:Wang Shun-li★, Studying for master’s degree, School of Kinesiology, Shanghai University of Sport, Shanghai 200438, China qimeng2000@126.com -
Supported by:the National Natural Science Foundation of China for the Youth, No. 30800542*; Shanghai Key Laboratory of Human Sport Competence Development and Maintenance (Shanghai University of Sport), No. 11DZ2261100*
CLC Number:
Cite this article
Wang Shun-li, Shi Reng-fei. Protein synthesis and resistance in aging skeletal muscle[J]. Chinese Journal of Tissue Engineering Research, doi: 10.3969/j.issn.2095-4344.2013.15.025.
share this article
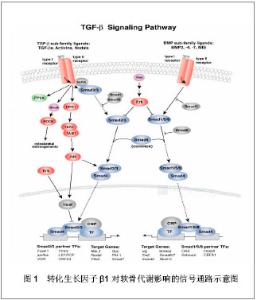
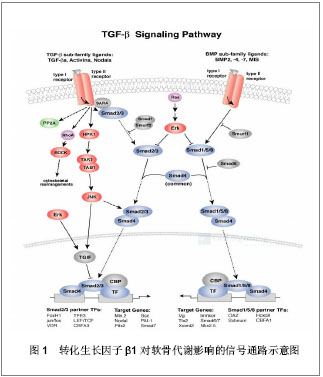
2.1 纳入文献基本情况 纳入的文献包括骨骼肌衰老机制研究类文章15篇,衰老骨骼肌蛋白合成抵抗相关研究类文章22篇,抗阻训练和补充蛋白质相关研究类文章18篇。 2.2 纳入资料的研究结果特征 老年人骨骼肌蛋白质合成抵抗:机体蛋白质不断更新,处于合成与分解的动态变化中,当合成大于分解时,骨骼肌生长,反之则出现萎缩。机体内蛋白质的合成和分解之差称作蛋白质净平衡。蛋白质净平衡由食物蛋白质来维持,进食后会引起血液中氨基酸含量升高,后者可刺激蛋白质的合成[2-3],即表现为骨骼肌质量的增加。骨骼肌总蛋白含量从总体上反映了骨骼肌蛋白质代谢的状况,对于评价骨骼肌的功能具有十分重要的作用[4]。随着年龄的增长,老年人骨骼肌对较低浓度的氨基酸敏感性下降,蛋白质合成速率减弱,最终表现为骨骼肌质量下降。鉴于此,作者效仿“胰岛素抵抗”的定义方法,把老年人骨骼肌对较低浓度的氨基酸敏感性下降,蛋白质合成速率减弱的现象称作“蛋白质合成抵抗(Protein Synthesis Resistance)”。 随着年龄的增加,骨骼肌组织中蛋白质合成代谢率会逐渐低于分解代谢率,出现所谓的“负氮平衡”,最终导致骨骼肌总蛋白含量的减少[5],表现为骨骼肌质量的下降和肌力的减退。有报道指出:老年人骨骼肌蛋白质的合成速率以每年20%-30%的速度下降。同时,肌原纤维蛋白的分解速率以50%的速度增 长[6]。然而,最近Kimball等[7]人对大鼠的研究发现,在衰老过程中蛋白质合成水平是有所升高的, 只是这种升高还是不能阻止骨骼肌质量的下降。同样,Cuthbertson等[8]的研究发现,健康老年人骨骼肌蛋白质的合成代谢减弱和分解代谢增强并没有引起骨骼肌蛋白质净平衡的障碍。这种差异可能是目前的检测手段不够精确,难以检测出老年人骨骼肌蛋白质代谢的微小变化。有研究表明在口服一定剂量的氨基酸后,老年人和年轻人骨骼肌蛋白质的合成代谢都出现了增加[9]。但后来Volpi将氨基酸和葡萄糖混合物注入体内,并抑制小肠吸收,发现年轻人蛋白质的合成增加,而老年人则没有—这第一次证明了骨骼肌蛋白质合成抵抗[10]。 目前认为主要有两种因素导致了老年人骨骼肌蛋白质合成抵抗,一种是活动水平的降低,另一种是炎症反应。活动能力的减弱对蛋白质的合成速率影响很大,即使短时间的骨骼肌废用也会引起蛋白质合成速率下降。例如,因伤而固定双腿的年轻人,由于活动受限而导致骨骼肌蛋白质合成减弱,在补充氨基酸后蛋白质的合成增加[11]。短期的抗阻运动或耐力运动均导致老年人蛋白质合成的急剧增加,这进一步证实了衰老骨骼肌的蛋白质合成抵抗[12]。 炎症对骨骼肌质量和蛋白质代谢产生不利的影响。有研究认为炎症可能影响老年人骨骼肌合成代谢的敏感性,这一点已经从动物的研究中获得了强有力的证据,例如,成年败血症大鼠骨骼肌质量的丢失伴随着蛋白质合成速率的下降。另外,还有研究证实低度炎症抑制大鼠骨骼肌蛋白质的合成[13]。mTOR(雷帕霉素靶蛋白)是蛋白质合成信号传导网络中的关键信号蛋白,感受和整合来自细胞内、外各种因素的变化(细胞能量状况、营养状况以及生长因子刺激),研究表明mTOR信号蛋白对氨基酸有敏感性[14],而衰老骨骼肌合成代谢敏感性的下降将使 mTOR信号蛋白的磷酸化减弱[15]。老年人骨骼肌内的信号敏感性下降或许可以解释老年人蛋白质的合成为何减弱,但仍然需要进一步的研究。 补充蛋白质与骨骼肌蛋白质合成抵抗:蛋白质的摄入量对于维持骨骼肌质量非常重要。蛋白质的摄入量直接决定着血液中氨基酸的浓度和持续时间,而血液中氨基酸的浓度和持续时间又影响着骨骼肌蛋白质的合成速率[16]。研究证实,血浆必需氨基酸参与骨骼肌蛋白质合成速率的调控,当血浆氨基酸浓度下降时,骨骼肌蛋白质合成速率下降[17]。相反,骨骼肌蛋白质的合成速率随可利用必需氨基酸的增加呈线性增 长[18]。例如,牛程麟等[19]的研究发现,受试者在补充蛋白营养制剂(成分为60%酪蛋白、40%麦芽糊精)后,机体骨骼肌和蛋白质显著增加。因此,采用富含必需氨基酸的蛋白质膳食干预,可以增加和维持血液中必需氨基酸的浓度,这将有助于刺激骨骼肌蛋白质的合成。 Welle等发现低蛋白(占总能量的7%)、中蛋白(占总能量的14%)和高蛋白(占总能量的28%)饮食对蛋白质合成的影响相似。但Cuthbertson等人的数据表明在摄入10-20 g氨基酸后出现了蛋白质合成抵抗现象,但是在摄入2.5 g氨基酸后,老年人和年轻人肌原纤维中蛋白质合成都有明显的增加。这说明中、低剂量的氨基酸可明显的刺激骨骼肌蛋白质合成增加[11],而高浓度的氨基酸则不能。但不管怎样,补充5-20 g氨基酸后,老年人骨骼肌蛋白质合成速率总比年轻人低。目前老年人在补充氨基酸后蛋白质合成速率较低的机制还不确定,尤其是补充亮氨酸,已知亮氨酸是骨骼肌蛋白质合成的重要调控因子,亮氨酸补充物可以通过胰岛素依赖性或非依赖性机制,刺激蛋白质合成[20]。有人推测摄入蛋白质的量必须超过亮氨酸的“阈值”才可能刺激蛋白质合成增加[21],不过目前这个“阈值”还不确定。但是可以肯定的是在年轻人中,这个“阈值”比较低,而在老年人中则比较高。可能原因是年轻人骨骼肌对亮氨酸的敏感性比较高,即使摄入1 g的亮氨酸就可以刺激蛋白质合成明显的增加[22]。而老年人骨骼肌对亮氨酸的敏感性下降,则需要较多的亮氨酸才可以刺激蛋白质合成升高。因此,补充含亮氨酸丰富且易吸收的优质蛋白质对促进老年人骨骼肌蛋白质的合成非常重要。 亮氨酸可以通过促进骨骼肌蛋白质多肽链合成来促进蛋白质的合成,并且这种作用仅限于骨骼肌,补充亮氨酸能明显刺激骨骼肌蛋白质的合成[23]。但是目前还不清楚长期补充亮氨酸对维持或增加老年人骨骼肌质量的影响。Verhoeven等[24]首次证明了长期补充适量氨基酸对老年人骨骼肌的影响。与对照组相比,补充亮氨酸对骨骼肌质量和力量没有明显影响。一种解释是亮氨酸虽然参与了mRNA翻译过程,但是亮氨酸对合成的易化以及对肥大的促进需要其他氨基酸的参与。 蛋白质对骨骼肌蛋白质合成及降解影响的实验研究: 文献来源:罗钧秋等[25],不同蛋白源对生长大鼠骨骼肌蛋白质代谢相关基因表达的影响,2012. 观察指标:研究酪蛋白(CAS)、大豆分离蛋白(SPI)和玉米醇溶蛋白(ZEIN)对大鼠骨骼肌蛋白质代谢基因表达的影响。 结果与结论:蛋白源对蛋白质代谢基因表达产生的差异,可能主要由饲料蛋白质氨基酸组成模式不同所体现,尤其表现为亮氨酸对组织蛋白质代谢进行调控。可见,蛋白质合成代谢调控与mTOR途径有关,蛋白质分解代谢与泛素一蛋白酶蛋白降解途径有关。 文献来源:毛湘冰等[26],日粮中添加亮氨酸对生长大鼠血浆瘦素水平和骨骼肌蛋白质代谢的影响,2011. 观察指标:探讨添加亮氨酸的日粮对生长大鼠生长性能、骨骼肌蛋白质代谢和瘦素分泌的影响。 结果与结论:长期饲喂添加L-亮氨酸的日粮可以提高生长大鼠血浆中瘦素浓度,并可显著调节生长大鼠骨骼肌蛋白质代谢。 文献来源:周济宏等[27],肿瘤坏死因子对谷氨酰胺调控大鼠骨骼肌蛋白质合成的影响,2006. 观察指标:研究促炎细胞因子肿瘤坏死因子α对谷氨酰胺调控大鼠骨骼肌蛋白质合成的影响。 结果与结论:肿瘤坏死因子可升高血浆及骨骼肌组织中谷氨酰胺的浓度;谷氨酰胺能促进骨骼肌蛋白质合成;而谷氨酰胺这种促骨骼肌蛋白质合成作用可被肿瘤坏死因子α抑制。 另外,乔璇等[28]报道β-羟基-β-丁酸甲酯对骨骼肌代谢的调控引起了运动、医学和畜牧领域的广泛关注。运动员在阻力训练后服用β-羟基-β-丁酸甲酯可加速骨骼肌的修复,代谢病患者服用β-羟基-β-丁酸甲酯能减少肌肉的损伤,动物生产中应用β-羟基-β-丁酸甲酯可提高生长性能、增加瘦肉含量。β-羟基-β-丁酸甲酯发挥作用的可能机制与调节蛋白质周转和维护细胞膜完整性有关。运动医学领域以降低骨骼肌蛋白质降解为目的进行的研究揭示出,β-羟基-β-丁酸甲酯的作用效果与训练经历和代谢状态有关。 抗阻运动与骨骼肌蛋白质合成抵抗:抗阻运动是增加老年人蛋白质合成的重要措施。经常性抗阻运动不仅可以增加蛋白质的合成,还可促进老年人骨骼肌的相对肥大[29-30]。研究发现一周三次连续12周的低强度(40%1RM)抗阻运动可以提高老年人腿部力量,但没有引起骨骼肌肥大。相反,老年人进行高强度(80%1RM)的抗阻运动比低强度的抗阻运动更能提高骨骼肌力量,同时还出现了股四头肌的肥大[31]。这种差异可能是老年人运动时所选的运动负荷不同引起的。研究表明小强度的抗阻运动(20%-50%1RM)结合工作肌的血流限制对骨骼肌肥大的刺激和力量的增加与大强度的抗阻运动相似[32]。另外Fry等[33]人证实在血流限制情况下,低强度的抗阻运动3 h内老年人mTOR信号蛋白的磷酸化和蛋白质合成均显著升高。相反,强度为20%1RM、没有血液限制的抗阻运动对蛋白质合成的升高并不明显。由于运动能力的减退,老年人进行大强度的抗阻练习显得不切实际。因此,小强度结合血流限制的抗阻运动就尤为重要。 目前认为大于70%1RM的高强度抗阻运动才能较好的刺激骨骼肌蛋白质合成,然而衰老使得心血管机能下降,大强度力量训练可能增加心脏后负荷,使从事运动的老年个体发生危险,且过重的负荷也易导致运动损伤的发生[34]。20%-50% 1RM强度抗阻运动结合工作肌血流限制就可产生类似的肌肉体积和力量增加。说明工作肌的血流阻断和运动中静脉回流封闭所导致的局部代谢环境的改变才是促进蛋白质合成的真正原因[35]。 另外,关于运动负荷对骨骼肌蛋白质合成方面,与以往研究相左的是,贾华等[36]对亚急性骨骼肌衰变的大鼠的研究发现,负重跑训练干预可以有效提高大鼠骨骼肌组织总蛋白的含量,并以小负重组的效果更为明显。贾华等的发现提示:中低强度的负重跑训练对骨骼肌刺激更为明显,特别是对骨骼肌组织蛋白代谢过程产生积极影响。同样,Burd等[37]人的研究发现低强度大运动量至力竭的抗阻运动比高强度小运动量至力竭的抗阻运动更有利于蛋白质的合成。例如,强度为30%1RM的举重至力竭的运动和强度为90%1RM的举重至力竭的运动在运动后4 h内蛋白质合成的增加效应相似。这一研究表明抗阻运动对蛋白质合成主要由运动量决定。即如果想要达到与高强度运动相同的骨骼肌质量和力量变化,就必须进行更大运动量的低强度抗阻运动。需要指出的是Burd的研究针对的是年轻人,而对于老年人仍然需要做进一步的研究。 相关运动对骨骼肌蛋白质合成及降解影响的实验研究: 文献来源:马延超等[38],一次大强度耐力运动对大鼠骨骼肌蛋白质降解和AMPK活性变化的影响,2011. 观察指标:探讨一次大强度耐力运动过程中,AMPK活性变化对骨骼肌蛋白质降解的作用。 结果与结论:一次性大强度耐力运动后1-6 h,骨骼肌蛋白质降解可能增强,其原因可能是AMPK活化,促进MAFbx mRNA、MuRF1 mRNA基因表达,促进骨骼肌蛋白质的降解。 文献来源:叶鸣等[39],低氧和运动经AR-IGF-1对骨骼肌蛋白质合成的作用,2010. 观察指标:探讨低氧、运动对骨骼肌蛋白质合成的作用。 结果与结论:运动后进行低氧暴露比单纯运动更能通过AR含量-AR活性水平抑制蛋白质合成;低氧、运动或低氧运动通过睾酮调节AR数量及活性,最终影响骨骼肌蛋白含量;低氧、运动或低氧运动可通过调节AR转录活性影响IGF-1mRNA表达,最终调节骨骼肌蛋白质合成。 文献来源:叶鸣等[40],高住低训对骨骼肌蛋白质及MHC含量作用及其机理研究,2009. 观察指标:高住低训对骨骼肌蛋白质及MHC含量作用及其机制研究。 结果与结论:本实验耐力运动模型的选取是有利于蛋白质合成的,在此基础上进行低氧暴露模拟高住低训研究骨骼肌蛋白质合成的调控是可行的;动后进行低氧暴露比单纯运动通过AR含量-AR活性水平抑制蛋白质合成,影响机体恢复;低氧、运动或低氧运动通过AR水平最终影响骨骼肌蛋白含量。 补充蛋白质、抗阻运动与骨骼肌蛋白质合成抵抗:抗阻运动结合补充蛋白质可以更好地促进骨骼肌蛋白质的合成。刘丰彬等[41]对衰老大鼠的研究发现,负重训练和补充大豆多肽两种干预方式均可以有效提高大鼠骨骼肌组织总蛋白的含量,但两者的交互作用比单一干预因素作用效果更为明显。提示:补充蛋白质并结合抗阻运动可以有效改善骨骼肌组织蛋白质合成代谢与分解代谢的不平衡,从而促进大鼠骨骼肌蛋白质合成。另有研究发现,抗阻运动结合补充蛋白质可以减少骨骼肌蛋白质的分解。例如,金宏等[42]人对小鼠的研究表明游泳后补充支链氨基酸可减少骨骼肌蛋白质的分解。而对人的研究证实,抗阻运动后 3 h内补充乳清蛋白可以较好地刺激骨骼肌蛋白质合成[43]。另有研究发现,补充蛋白质并结合抗阻运动对老年人和年轻人骨骼肌蛋白质合成都有积极影响[44]。例如,年轻人只要4.2 g的氨基酸(10 g乳蛋白)就可以促进运动后蛋白质的合成[45]。Moore等[46]的研究证实运动对年轻人蛋白质合成的刺激作用可由20 g鸡蛋蛋白完成。但是对运动后依次摄入不同剂量的乳清蛋白的研究发现,在摄入40 g乳清蛋白时蛋白质合成增加最明显。最近的研究发现年轻人运动后摄入20 g的优质蛋白质合成就可以达到最大值,而老年人在运动后需要摄入较多的蛋白质,蛋白质合成的速率才可以达到最大值[47]。但是,老年人在运动后摄入40 g蛋白质的可行性依然需要进一步的研究。 经常进行抗阻训练的人群其蛋白质需要量要高于久坐习惯人群。但是,骨骼肌功能的改善不仅对蛋白质数量有要求,而且对摄入时间要求也较高。谷氨酰胺也是一种能够促进骨骼肌生长,抑制蛋白质降解的重要氨基酸。研究发现谷氨酰胺在人体内浓度相对较高,并具有维持机体内环境稳定的重要作用[48]。目前研究并没有证实运动何时(运动前,运动中或运动后)补充蛋白质可以更好地促进老年人骨骼肌蛋白质的合成。有研究表明,抗阻运动后的恢复阶段蛋白质合成增加[49]。Fujita等[50]的研究表明在运动过程中mTOR的信号调节和蛋白质合成可能受到抑制,但是在运动后60分钟内恢复正常。而Esmark等[51]对老年人的研究发现抗阻运动后立即补充10 g的蛋白质(和运动后2 h再补充蛋白质相比)引起了骨骼肌横截面积和力量的增加。最近的研究表明即使是健康年轻人在小强度抗阻运动至力竭后24 h内骨骼肌摄取蛋白质的能力提高[52]。因此,可以推测在抗阻运动后即刻或24 h内补充20-40 g优质蛋白质将可以更好地促进老年人蛋白质合成。 骨骼肌的生长即是上述多种机制共同调节的结果之一,然而这仅是调节过程外化的一种表现,其本质仍在于骨骼肌蛋白质合成率超过了其降解率,导致蛋白质积聚和肌纤维面积增大[53]。合理的蛋白质营养与正确的运动训练会促进肌肉蛋白质的合成,从而有利于骨骼肌的肥大及肌肉力量的增长。通常不同的运动方式引起骨骼肌蛋白代谢的形式会有所差异,耐力运动趋向于蛋白质降解,而力量训练趋向于增加蛋白质合成代谢,最终引起肌肉增长以及力量增加。为达到理想的合成状态,饮食蛋白补充应充分而及时。适合运动人群补充的氨基酸主要有支链氨基酸,谷氨酰胺等,尤其注意亮氨酸的补充[54-55]。"
| [1] Fujita S, Dreyer HC, Drummond MJ, et al. Nutrient signalling in the regulation of human muscle protein synthesis. J Physiol. 2007;582(Pt 2):813-823. [2] 闫万军,赵斌.衰老性肌肉丢失及其训练效应[J].武汉体育学院学报,2008,42(11):96-100.[3] Burd NA, West DW, Rerecich T, et al. Validation of a single biopsy approach and bolus protein feeding to determine myofibrillar protein synthesis in stable isotope tracer studies in humans. Nutr Metab (Lond). 2011;8:15. [4] Karakelides H, Nair KS. Sarcopenia of aging and its metabolic impact. Curr Top Dev Biol. 2005;68:123-148.[5] Paddon-Jones D. Interplay of stress and physical inactivity on muscle loss: nutritional counter measures. J Nut. 2006;136(8): 2123-2126.[6] Trappe T, Williams R, Carrithers J, et al. Influence of age and resistance exercise on human skeletal muscle proteolysis: a microdialysis approach. J Physiol. 2004;554(Pt 3):803-813. [7] Kimball SR, O'Malley JP, Anthony JC, et al. Assessment of biomarkers of protein anabolism in skeletal muscle during the life span of the rat: sarcopenia despite elevated protein synthesis. Am J Physiol Endocrinol Metab. 2004;287(4): E772-780. [8] Cuthbertson D, Smith K, Babraj J, et al. Anabolic signaling deficits underlie amino acid resistance of wasting, aging muscle. FASEB J. 2005;19(3):422-424.[9] Volpi E, Sheffield-Moore M, Rasmussen BB, et al. Basal muscle amino acid kinetics and protein synthesis in healthy young and older men. JAMA. 2001;286(10): 1206-1212.[10] Volpi E, Mittendorfer B, Rasmussen BB, et al. The response of muscle protein anabolism to combined hyperaminoacidemia and glucose-induced hyperinsulinemia is impaired in the elderly. J Clin Endocrinol Metab. 2000;85 (12):4481-4490.[11] Glover EI, Phillips SM, Oates BR, et al. Immobilization induces anabolic resistance in human myofibrillar protein synthesis with low and high dose amino acid infusion. J Physiol. 2008;586(Pt 24):6049-6061.[12] Durham WJ, Casperson SL, Dillon EL, et al. Age-related anabolic resistance after endurance-type exercise in healthy humans. FASEB J. 2010;24(10):4117-4127.[13] Balage M, Averous J, Rémond D, et al. Presence of low-grade inflammation impaired postprandial stimulation of muscle protein synthesis in old rats. J Nutr Biochem. 2010;21(4):325-331.[14] Fujita S, Dreyer HC, Drummond MJ, et al. Nutrient signalling in the regulation of human muscle protein synthesis. J Physiol. 2007;582(Pt 2):813-823.[15] Fry CS, Drummond MJ, Glynn EL, et al. Aging impairs contraction-induced human skeletal muscle mTORC1 signaling and protein synthesis. Skelet Muscle. 2011;1(1):11.[16] Tang JE, Moore DR, Kujbida GW, et al. Ingestion of whey hydrolysate, casein, or soy protein isolate: effects on mixed muscle protein synthesis at rest and following resistance exercise in young men. J Appl Physiol. 2009;107(3):987-992.[17] Low A, Wolfe RR, Rennie MJ, et al. Human muscle protein synthesis is modulated by extracellular, not intramuscular amino acid availability: a dose-response study. J Physiol. 2003;552(1):315-324.[18] Bohé J, Low JF, Wolfe RR, et al. Latency and duration of stimulation of human muscle protein synthesis during continuous infusion of amino acids . J Physiol.2001; 532(2): 575-579.[19] 牛程麟,王新颖,金丽,等.蛋白强化的营养制剂对高运动量人员骨骼肌含量及营养状况的影响[J].肠外与肠内营养,2010, 17(4): 217.[20] 赵法伋.膳食蛋白质与老年肌肉衰减综合征[J].上海预防医学杂志,2011,23(3):134.[21] Norton LE, Layman DK, Bunpo P, et al. The leucine content of a complete meal directs peak activation but not duration of skeletal muscle protein synthesis and mammalian target of rapamycin signaling in rats. J Nutr. 2009;139(6):1103-1109.[22] Moore DR, Robinson MJ, Fry JL, et al. Ingested protein dose response of muscle and albumin protein synthesis after resistance exercise in young men. Am J Clin Nutr. 2009; 89(1):161-168.[23] Blomstrand E, Eliasson J, Karlsson HK, et al. Branched- chain amino acids activat e key enzymes in protein synthesis after physical exercise. J Nutr. 2006;136(1):269S-73S.[24] Verhoeven S, Vanschoonbeek K, Verdijk LB, et al. Long-term leucine supplementation does not increase muscle mass or strength in healthy elderly men. Am J Clin Nutr. 2009;89(5): 1468-1475.[25] 罗钧秋,陈代文,余冰. 不同蛋白源对生长大鼠骨骼肌蛋白质代谢相关基因表达的影响[J]. 中国畜牧杂志,2012,48(15):37-40.[26] 毛湘冰,曾祥芳,蔡传江,等. 日粮中添加亮氨酸对生长大鼠血浆瘦素水平和骨骼肌蛋白质代谢的影响[J]. 中国畜牧杂志,2011, 47(15):26-30.[27] 周济宏,李幼生,解伟光,等. 肿瘤坏死因子对谷氨酰胺调控大鼠骨骼肌蛋白质合成的影响[J]. 医学研究生学报,2006,19(10): 884-887.[28] 乔璇,张海军,齐广海,等.β-羟基-β-丁酸甲酯调控肌肉代谢的研究进展[J]. 动物营养学报,2011,23(12):2064-2070.[29] Drummond MJ, Dreyer HC, Pennings B, et al. Skeletal muscle protein anabolic response to resistance exercise and essential amino acids is delayed with aging. J Appl Physiol. 2008;104(5):1452-1461.[30] Kosek DJ, Kim JS, Petrella JK, et al. Efficacy of 3 days/wk resistance training on myofiber hypertrophy and myogenic mechanisms in young vs. older adults. J Appl Physiol. 2006; 101(2):531-544.[31] Onambélé-Pearson GL, Breen L, Stewart CE. Influence of exercise intensity in older persons with unchanged habitual nutritional intake: skeletal muscle and endocrine adaptations. Age (Dordr). 2010;32(2):139-153.[32] Suliman IA, Lindgren JU, Elhassan AM, et al. Effects of short- and long-term rat hind limb immobilization on spinal cord insulin-like growth factor-I and its receptor. Brain Res. 2001; 912(1):17-23.[33] Fry CS, Glynn EL, Drummond MJ, et al. Blood flow restriction exercise stimulates mTORC1 signaling and muscle protein synthesis in older men. J Appl Physiol. 2010;108(5): 1199-1209. [34] Arthur ST, Cooley ID. The effect of physiological stimuli on sarcopenia; impact of Notch and Wnt signaling on impaired aged skeletal muscle repair. Int J Biol Sci. 2012;8(5):731-760. [35] Van Kan GA, Cderbaum JM, Cesari M, et al. Sarcopenia: biomarkers and imaging (International Conference on Sarcopenia research). J Nutr Health Aging. 2011;15(10): 834-846.[36] 贾华,刘丰彬,黄丽敏,等.负重跑训练延缓大鼠骨骼肌衰变效果的研究[J].中国康复医学杂志,2010,25(12):1169.[37] Burd NA, West DW, Staples AW, et al. Low-load high volume resistance exercise stimulates muscle protein synthesis more than high-load low volume resistance exercise in young men. PLoS One. 2010;5(8):e12033. PMID:20711498[38] 马延超,朱荣,许寿生,等. 一次大强度耐力运动对大鼠骨骼肌蛋白质降解和AMPK活性变化的影响[J]. 体育学刊,2011,18(2): 139-144.[39] 叶鸣,贺道远,刘霞,等. 低氧和运动经AR-IGF-1对骨骼肌蛋白质合成的作用[J]. 天津体育学院学报,2010,2:125-129.[40] 叶鸣,贺道远,曾凡星.高住低训对骨骼肌蛋白质及MHC含量作用及其机理研究[J]. 西安体育学院学报,2009,26(6):708-712.[41] 刘丰彬,赵斌,闫万军,等.负重训练和补充大豆多肽干预大鼠骨骼肌衰老过程的实验研究[J].天津体育学院学报,2010,25(1):37.[42] 金宏,许志勤,王先远.支链氨基酸提高大鼠游泳耐力作用探讨[J].营养学报,2001,23(1):48-51.[43] Pennings B, Boirie Y, Senden JM, et al. Whey protein stimulates postprandial muscle protein accretion more effectively than do casein and casein hydrolysate in older men. Am J Clin Nutr. 2011;93(5):997-1005. [44] Moore DR, Tang JE, Burd NA, et al. Differential stimulation of myofibrillar and sarcoplasmic protein synthesis with protein ingestion at rest and after resistance exercise. J Physiol. 2009;587(Pt 4):897-904.[45] Tang JE, Manolakos JJ, Kujbida GW, et al. Minimal whey protein with carbohydrate stimulates muscle protein synthesis following resistance exercise in trained young men. Appl Physiol Nutr Metab. 2007;32(6):1132-1138.[46] Moore DR, Robinson MJ, Fry JL, et al. Ingested protein dose response of muscle and albumin protein synthesis after resistance exercise in young men. Am J Clin Nutr. 2009; 89(1):161-168.[47] 陈巍,李娟,陈庆合. 运动促进骨骼肌功能康复改善代谢综合征的研究进展[J]. 中国康复医学,2012,27(6):577-581.[48] Yang Y, Breen L, Burd NA, et al. Resistance exercise enhances myofibrillar protein synthesis with graded intakes of whey protein in older men. Br J Nutr. 2012 Feb 7:1-9.[49] Kimball SR,Farrell PA,Jefferson LS. Invited Review:Role of insulin in translational control of protein synthesis in skeletal muscle by amino acids or exercise. J Appl Physiol. 2002; 93(3): 1168-1180.[50] Fujita S, Dreyer HC, Drummond MJ, et al. Essential amino acid and carbohydrate ingestion before resistance exercise does not enhance postexercise muscle protein synthesis. J Appl Physiol. 2009;106(5):1730-1739.[51] Esmarck B, Andersen JL, Olsen S, et al. Timing of postexercise protein intake is important for muscle hypertrophy with resistance training in elderly humans. J Physiol. 2001;535(Pt 1):301-311. [52] Burd NA, West DW, Moore DR, et al. Enhanced amino acid sensitivity of myofibrillar protein synthesis persists for up to 24 h after resistance exercise in young men. Enhanced amino acid sensitivity of myofibrillar protein synthesis persists for up to 24 h after resistance exercise in young men.2011;141(4): 568-573.[53] 姜伟,王修启,束刚,等. 雷帕霉素靶蛋白(mTOR)结构功能及其对骨骼肌蛋白质合成影响的研究进展[J]. 中国畜牧兽医,2010, 37(6):21-25.[54] 马延超,朱荣,李俊平. 腺苷酸活化蛋白激酶与骨骼肌蛋白质降解[J]. 中国组织工程研究与临床康复,2012,16(2):341-344.[55] 毛湘冰,黄志清,陈小玲,等. 亮氨酸调节哺乳动物骨骼肌蛋白质合成的研究进展[J]. 动物营养学报,2011,23(5):709-714. |
| [1] | Luo Lin, Song Naiqing, Huang Jin, Zou Xiaodong. Review and prospect of international research on preschool children’s movement development assessment: a CiteSpace-based visual analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1270-1276. |
| [2] | Shu Wenbo, Chen Mengchi, Li Hua, Huang Liqian, Huang Binbin, Zhang Wenhai, Wu Yachen, Wang Zefeng, Li Qiaoli, Liu Peng. Correlation between body fat distribution and characteristics of daily physical activity in college students [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1277-1283. |
| [3] | Yang Fengjiao, Wang Xiangbin, Hou Meijin, Yu Jiao, Li Zhenhui, Fu Shengxing, Lin Ziling, Liu Benke. Comparison of gait characteristics between young and elderly people under dual tasks using three-dimensional gait analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 344-349. |
| [4] | Zhang Shuang, Tan Rui, Wang Chunxiao, Wu Fengyu, Guo Hongyu. MicroRNAs for assessing the motion control of human skeletal muscles [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(17): 2755-2760. |
| [5] | Shui Xiaoping, Li Chunying, Cao Yanxia, Su Quansheng. Effects of aerobic and resistance exercises on endoplasmic reticulum stress-related proteins in diabetic peripheral neuropathy rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(11): 1693-1698. |
| [6] | Zhao Weibiao, He Ziwei, Li Ji, Li Yi. Application value of 3D printing guide plate in SuperPATH technology for elderly hip arthroplasty: retrospective study and evidence analysis of literature retrieval [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(9): 1324-1330. |
| [7] | Zhao Chuntao, Qing Mingsong, Yu Langbo, Peng Jiachen . Meta-analysis of total knee arthroplasty guided by kinematic alignment and mechanical alignment [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(9): 1435-1442. |
| [8] |
Zhang Cong, Zhao Yan, Du Xiaoyu, Du Xinrui, Pang Tingjuan, Fu Yining, Zhang Hao, Zhang Buzhou, Li Xiaohe, Wang Lidong.
Biomechanical analysis of the lumbar spine and pelvis in adolescent
idiopathic scoliosis with lumbar major curve |
| [9] | Xu Guofeng, Li Xuebin, Tang Yifan, Zhao Yin, Zhou Shengyuan, Chen Xiongsheng, Jia Lianshun. The role of autophagy in ossification of the human ligamentum flavum [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(8): 1174-1181. |
| [10] |
Cen Yanhui, Xia Meng, Jia Wei, Luo Weisheng, Lin Jiang, Chen Songlin, Chen Wei, Liu Peng, Li Mingxing, Li Jingyun, Li Manli, Ai Dingding, Jiang Yunxia.
Baicalein inhibits the biological behavior of hepatocellular
carcinoma stem cells by downregulation of Decoy receptor 3 expression |
| [11] | Liu Qun, Sun Dongdong, Gao Lilan, He Zhijiang, Sun Minglin. Risk factors for fractures secondary to percutaneous kyphoplasty: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(6): 976-984. |
| [12] | He Yujie, Wang Haiyan, Li Zhijun, Li Xiaohe, Cai Yongqiang, Dai Lina, Xu Yangyang, Wang Yidan, Xu Xuebin. Digital measurements of the anatomical parameters of pedicle-rib unit screw fixation in thoracic vertebrae of preschoolers [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(6): 869-876. |
| [13] | Yan Shu, Lu Yan, Ouyang Zhaolian. Analysis of programs on tissue engineering funded by the National Natural Science Foundation of China between 2013 and 2018 [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(5): 731-735. |
| [14] | Chen Yanlin, Xu Lin, Xu Shengjia. Effects of physical activity on hippocampal plasticity and cognition [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(5): 773-779. |
| [15] | Sun Jian, Fang Chao, Gao Fei, Wei Laifu, Qian Jun. Clinical efficacy and complications of short versus long segments of internal fixation for the treatment of degenerative scoliosis: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(3): 438-445. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||