Chinese Journal of Tissue Engineering Research ›› 2021, Vol. 25 ›› Issue (34): 5552-5560.doi: 10.12307/2021.254
Previous Articles Next Articles
Development prospect and research value of biodegradable poly(lactic acid) for bone repair
Liu Zichen1, 2, Yu Baoqing2
- 1University of Shanghai for Science and Technology, Shanghai 200093, China; 2Shanghai Pudong Hospital, Fudan University Pudong Medical Center, Shanghai 201399, China
-
Received:2020-08-05Revised:2020-08-11Accepted:2020-09-11Online:2021-12-08Published:2021-07-28 -
Contact:Yu Baoqing, Professor, Chief physician, Doctoral supervisor, Shanghai Pudong Hospital, Fudan University Pudong Medical Center, Shanghai 201399, China -
About author:Liu Zichen, Master candidate, University of Shanghai for Science and Technology, Shanghai 200093, China; Shanghai Pudong Hospital, Fudan University Pudong Medical Center, Shanghai 201399, China -
Supported by:the Fund of Key Disciplines Group Construction Project of Pudong Health Bureau of Shanghai, No. PWZxq2017-11 (to YBQ); Program for Medical Key Department of Shanghai, No. ZK2019C01 (to YBQ); the Outstanding Clinical Discipline Project of Shanghai Pudong Health Committee, No. PWYgy2018-09 (to YBQ); National Natural Science Foundation of China, No. 81971753 (to YBQ)
CLC Number:
Cite this article
Liu Zichen, Yu Baoqing. Development prospect and research value of biodegradable poly(lactic acid) for bone repair[J]. Chinese Journal of Tissue Engineering Research, 2021, 25(34): 5552-5560.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
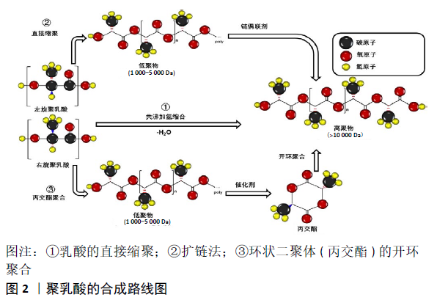
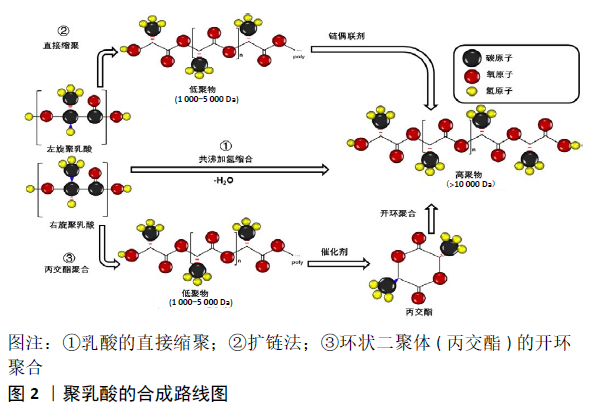
2.1 聚乳酸的合成方法 聚乳酸是一种脂肪族聚酯,由乳酸小分子聚合而成,其单体为2-羟基丙酸,有L-乳酸和D-乳酸2种对映异构体。其中,乳酸可由可再生农业资源的微生物发酵获得,例如玉米中的葡萄糖、甘蔗中的蔗糖、干酪乳清中的乳糖和废纸中的纤维素,因此合成聚乳酸的原料是可再生作物,并且聚乳酸可被完全降解为CO2和H2O,实现了从合成源头到废弃产物的无污染[4]。所合成的聚乳酸可分为L-旋光异构体(左旋异构体)和D-旋光异构体(右旋异构体)[5]。常见合成聚乳酸的方法有3种(图2):第一是乳酸分子脱水聚合成聚乳酸;第二是通过添加链偶联剂以来增加聚合物的链长,实现高分子质量;第三种方法是通过环状二聚体(丙交酯)的开环聚合反应,这是获得高分子质量聚乳酸的主要方法。这种方法具体是将乳酸脱水形成聚乳酸低聚物(1 000-5 000 Da),然后在高温、高真空度转化为环状二聚体的丙交酯,熔融的丙交酯混合物通过蒸馏进行纯化,并最终得到不同分子质量的聚乳酸[6]。"
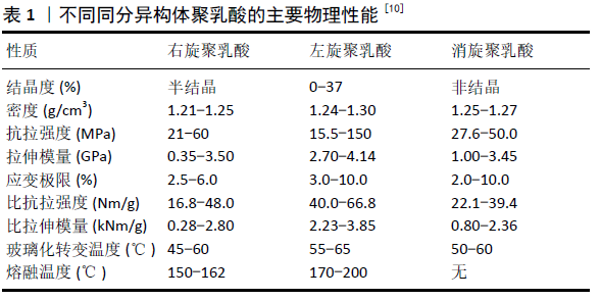
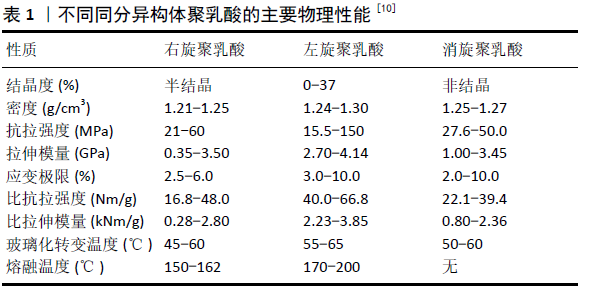
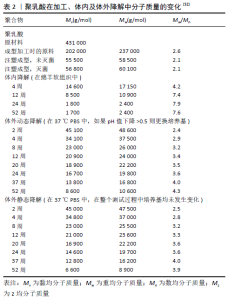
2.2 聚乳酸的性能 相比于其他脂肪族聚酯,聚乳酸具有高机械强度、高模量、生物降解性、生物相容性、生物可吸收性、透明性、低毒性及易加工性[7]。其中,聚乳酸的物理化学性能尤其是降解性能对于其在骨科材料的应用至关重要。 2.2.1 物理化学性能 聚乳酸存在3种立体构型:聚(L-丙交酯)、聚(DL-丙交酯)和聚(D-丙交酯),对应的聚合物分别被称为左旋异构体聚乳酸、消旋异构体聚乳酸和右旋异构体聚乳酸。他们的物理化学性能不同,左旋异构体聚乳酸和右旋异构体聚乳酸是热塑性结晶型聚合物,最大结晶率高达60%,而消旋异构体聚乳酸为非结晶型聚合物[8];对于非结晶的聚乳酸,其玻璃化转变温度(Tg)为50-60 ℃[7];在玻璃化转变温度以下,聚乳酸呈刚性和脆性,塑性变形能力很低,在玻璃化转变温度以上其强度和模量都会有所下降[2];结晶型的聚乳酸的玻璃化转变温度约为60 ℃,熔融温度(Tm)在180 ℃左右[9],与非结晶型聚乳酸相比具有更高的弹性模量、较好的耐热性和更小的变形性(表1)。"
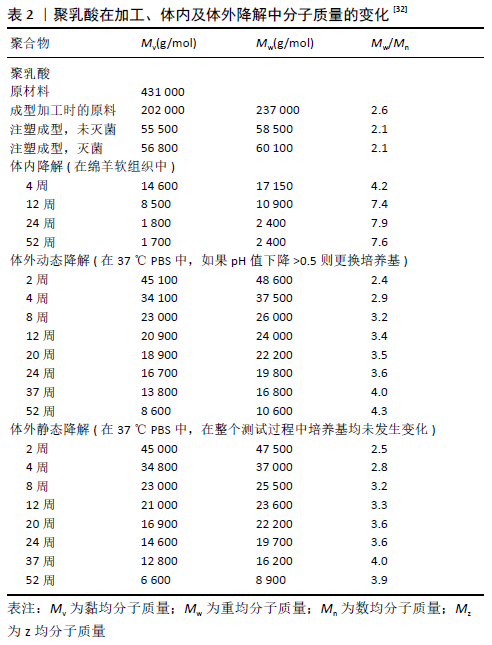
2.2.2 降解性能 聚乳酸的降解性能与分子结构有关,在降解过程中酯键水解成乳酸。聚乳酸在体内降解的速率对于骨折修复、固定及术后恢复至关重要,其降解机制主要有3种:水解,生物及酶降解,辐照降解。依照聚乳酸聚合物的初始的分子质量、形态和结晶度等,聚乳酸降解的速度可从几周到几个月甚至是两三年。 (1)水解降解:水解是聚乳酸最主要的降解方式,其酯基可在水境中被降解产生羧酸,遵循如下反应: -COO-+H2O→-COOH + OH- (1) 水解会导致末端羧基含量增加,并进一步加快降解。水解过程包括聚合物吸水、酯键的水解断裂和可溶性低聚物的扩散溶解3个阶段[3]。从水解途径来说,聚乳酸及其共聚物降解包括表面降解、本体降解和自身催化的本体降解[11]。聚乳酸的水解降解速率很大程度上取决于分子质量及其分子构型、结晶度、pH值和温度[12]。 分子质量是影响聚乳酸水解降解的关键因素之一,通常与聚乳酸的降解速率呈反比,较长的链倾向于以较慢的速率水解,而较短链的降解速率较快。较高分子质量的聚乳酸具有更紧密的结构,使得酯基不易被破坏同时也会进一步加强聚乳酸的疏水性,使得其降解相对缓慢、氢离子生成量减少。SAHA等[13]研究了不同分子质量值对中性条件下左旋聚乳酸水解降解的影响,他们发现数均分子量(Mn)在8×104– 4×105 g/mol的范围内,分子质量对聚乳酸降解速率的影响并不显著;然而在低于4×104 g/mol时,分子质量的降低会加速水解。因为低分子质量的分子迁移率高,亲水性末端羧基和羟基的密度越高,水溶性低聚物和单体形成的可能性越大,从而增加了水分扩散速率,进一步催化聚乳酸降解[14]。聚乳酸的分子构型同样影响着降解速率。TSUJI等[15]通过调控右旋聚乳酸和左旋聚乳酸的比例实现聚乳酸基共聚物的不同水解速率。GORRASI等[14]发现左旋聚乳酸链中少量的右旋-丙交酯单元分布可以增强水解降解。在聚乳酸降解后期,分子质量的减小使得材料的力学性能显著下降。但在中性条件下的早期降解过程中,低温退火时水分子作为塑性剂,无定形区域稳定链的填充会使得某些力学性能增强[16]。另一研究发现,60周的水解降解对左旋聚乳酸薄膜的拉伸强度和杨氏模量没有显著影响,而在第一阶段0-32周的降解中,其断裂伸长率显著下降,此后保持不变[13]。通过跟踪左旋聚乳酸在24 h的断裂韧性变化,发现结晶型左旋聚乳酸的断裂韧性减少的速率比无定形左旋聚乳酸要大,主要源于球晶表面链的裂解所导致裂纹形成的恶化[17]。 聚合物结晶度的增加可以降低聚合物的降解速率。由于聚乳酸结晶区的分子片段紧密堆积,因此水不易渗透,晶体的存在不仅迫使分子以曲折的路径扩散,而且保护有序区域中的聚合物分子[18]。除此之外,聚乳酸的结晶度会随着降解而增加,这种现象可归因于无定形区域中的水解链断裂导致聚合物的整体结晶度增加。与非晶区相比,结晶区的化学链具有抗水解性,因为严格限制了水分子在刚性结晶区中的扩散[19]。通过研究部分结晶的左旋聚乳酸发现,水首先穿透左旋聚乳酸的非晶区,酯键断裂,最后降解到结晶区的中心[20]。在无定形区域进行水解的过程中会形成具有规则结构的低分子物质,并且左旋聚乳酸的结晶度增加,从而可以加速水解过程。结晶段的耐水解性比非晶区更持久。HOGLOND等[21]研究温度和结晶度之间聚乳酸降解速率的差异,结晶度比环境温度对水解速率的影响更大。 一些报告已经研究了pH值对聚乳酸水解降解的影响[22]。LYU等[23]研究了聚乳酸在pH=0-14四氢呋喃溶液中的水解,研究得出:pH > 4的溶液可以产生乳酸,其主要是离解形式,可以加速水解;在pH < 4的溶液中,链末端的乳酸以缔合的酸形式存在,这也可以通过乳酸在降解过程中的自催化来加速水解反应。聚乳酸的水解降解是酯基的水解,水解过程是在H+和OH-的催化下进行的。碱性介质中的高浓度OH-有效促进了聚乳酸基构建体酯基的水解,因而碱性pH值对于增强聚乳酸降解是较佳的。由于人体的pH值范围从强酸性(胃中的pH值为1.0-2.0)到弱碱性(pH值通常在7到8之间)环境,内部器官的pH值范围为7.2-7.45,而皮肤(pH=4-6)、皮下组织(pH=6.7-7.1)、肿瘤(pH < 6.9)和内部组织长时间出血(pH < 7)的酸性更高[24]。不可否认pH值对聚乳酸植入物或药物释放载体的水解降解会产生一定的影响[14]。 聚乳酸及其复合材料有许多水解降解实验研究,以模拟人体(T≈37 ℃)和自然介质(例如土壤或堆肥)(25 ℃ < T < 58 ℃)[25]条件下的降解为例,聚乳酸可以水解为水溶性低聚物。聚乳酸纤维在37 ℃和pH =7.4的磷酸盐缓冲溶液中可以保持完整6个月,几乎没有质量和强度损失[26],当温度升至 100 ℃时可在50 h内检测到聚乳酸纤维质量的减少,因此较高的温度可促进聚乳酸降解。 (2)生物及酶降解:目前,聚乳酸的生物降解有2种解释机制:一种理论是,聚乳酸首先会发生酯基的无规非酶断链反应,从而导致分子质量降低,此步骤可通过酸或碱来加速,其中也与温度和湿度有关,所形成的较低分子质量的聚乳酸进一步与酶反应生成二氧化碳和水;另一个理论是,当聚乳酸的分子质量下降到20 000 g/mol左右时,材料开始变脆,当降至约10 000 g/mol时变成具有不同形状和大小的碎片,并产生大量的二氧化碳,通过代谢逐渐释放出来[27]。聚乳酸基材料在体内的生物降解还涉及到酶降解,酶作用于聚乳酸形成乳酸,最终通过呼吸、粪便和尿液以CO2和H2O的形式从人体中代谢清除[28]。半结晶型左旋聚乳酸高分子的降解吸收速度较慢,在体内完全降解吸收时间可达3年及以 上[29];而消旋异构体聚乳酸为非结晶型,降解后不产生微晶体颗粒,降解速度较快。 聚乳酸及其共聚物的生物降解通常通过微生物分泌的酯酶、蛋白酶和脂肪酶等来完成。聚乳酸的酶促降解比其水解降解更快[10]。早期研究报道,聚乳酸可以被K-蛋白酶、羧酸酯酶和脂肪酶等酶分解[30]。在37 ℃和pH值为8.6的条件下,蛋白酶K对左旋聚乳酸降解速率的影响较对右旋聚乳酸的影响更加显著[10]。尽管蛋白酶K和其他丝氨酸蛋白酶(胰蛋白酶、弹性蛋白酶和枯草杆菌蛋白酶)可降解左旋聚乳酸和消旋异构体聚乳酸,但它们不能降解右旋聚乳酸。尽管脂肪酶通常不能水解聚乳酸,但是假丝酵母和根瘤菌脂肪酶可以裂解无定形消旋异构体聚乳酸,这表明脂肪酶在降解具有低熔融温度的无定形聚酯时是有效的,但不能降解具有光学活性碳的聚酯[31]。经过大量的体外模拟降解实验和体内动物实验后,MAINIL-VARLET等[32]发现在12个月后左旋聚乳酸经历了98%的生物降解,具体数据见表2。MIDDLETON等[33]得出基于聚乳酸的骨科器械在12-16个月内发生明显的生物降解,体内聚乳酸的降解会显著降低周围组织的pH值,这可能导致延迟骨损伤愈合。"

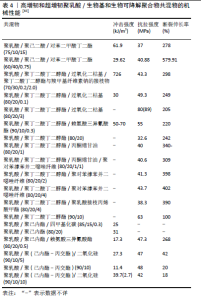
(3)辐照降解:作为医用材料,聚乳酸及其复合材料必须经过严格的灭菌处理以及术后的X射线片、CT(计算机断层扫描)和MRI检查,材料无法避免地会经历辐照降解和力学性能的损失。通常在光线照射下,大多数聚合物化学键会断裂发生降解,这种现象导致宏观层面的脆性断裂,加速材料的老化[34]。研究表明,紫外线(UV)和高能量源(例如X射线、γ射线和电子束)直接发射到聚合物材料上会严重影响其物理和化学性质,这个过程通过能量或电子转移反应导致聚合物降解[35]。254 nm波长的紫外线照射会打断长的聚乳酸链并降低聚乳酸的平均分子质量[36]。紫外线辐射导致聚乳酸聚合物中的酯键断裂,从而导致聚乳酸分子质量降低和脆性增加[37]。自1970年以来,聚乳酸已被用作外科缝合线[38]。一些术前紫外线消毒和术后放射线照相检查(例如CT)可能会影响聚乳酸。SAKAI等[39]指出了紫外线辐射对左旋聚乳酸薄膜降解的影响,发现发生一次主链断裂反应,左旋聚乳酸暴露于紫外线40 min后分子质量显著降低,在8周的时间内紫外线辐射使聚乳酸塑料薄膜降解了55%-97%。紫外线辐射可以加速聚乳酸的降解速度,使其Mw、玻璃化转变温度和断裂伸长率降低得更快。TSUJI等[40]观察到聚乳酸膜暴露于紫外线下长达200 h时,其分子质量分布Mw/Mn增加,但大多数拉伸性能可保持不变。JANORKAR等[41]发现经紫外线照射12 h后,聚乳酸的分子质量从约110 000 g/mol显著降低到约4 000 g/mol,当暴露于紫外线的时间增加时其降解速度更快。毫无疑问,聚乳酸在紫外线降解过程中不会产生新的基团,但酯基发生断裂。 除紫外线外,其他辐射(例如γ辐射、X射线)也对聚乳酸降解产生影响[42]。25 kGy的γ辐射是生物植入体灭菌的典型剂量[43],超高或低于该剂量都达不到材料的最佳灭菌效果及保持其原有性能。近年来,左旋聚乳酸的60Co-γ辐射灭菌已得到应用[44]。γ辐射聚乳酸使其在降解过程中会形成自由基,这是酯键断裂和聚乳酸主链中的甲烷夺氢的结果。由于聚合物的随机断链使样品变脆,γ射线辐照会降低右旋聚乳酸、左旋聚乳酸机械性能和分子质量。γ辐射主要发生在聚合物的非结晶区,并且随着γ射线辐照剂量的增加,左旋聚乳酸原料的球晶尺寸有所增大,更易结晶;而当剂量超高 15 kGy开始出现较为细小的球晶,归因于较高剂量的辐照使左旋聚乳酸发生了链段的裂解,从而形成细小的球晶[45]。因此,辐照的方式和剂量对聚乳酸降解的影响对该材料的使用性能和寿命也具有重要意义。 2.3 聚乳酸在骨修复的应用 得益于其优异的生物可降解性能,在生物医用材料领域聚乳酸已成为研究热点。同传统的金属类骨损伤固定件材料相比,聚乳酸及其复合材料有2大突出优点:一是能降解被人体代谢吸收,避免了愈合后的二次手术;二是随着聚乳酸在体内不断降解,其强度不断减弱克服了应力遮蔽,提高了骨修复效果。在开发和应用聚乳酸的早期阶段,鉴于其高昂的费用,它最初仅用作以骨科为代表的医学领域的生物医用材料,例如植入设备、组织工程支架等[33]。在1960年,聚乳酸因其机械强度和可生物降解性而首次在植入物和医疗设备领域用于替代生物医学金 属[37]。近年来,聚乳酸已在骨折固定装置、干涉螺钉、缝合锚钉、半月板修复、重建手术、血管移植物、关节软骨修复、骨移植替代物、硬脑膜替代物、皮肤替代物及组织增强和支架中应用[46]。纵观聚乳酸在骨科中的临床应用,主要又可以分为以下骨损伤固定器械和骨组织工程材料。 2.3.1 骨损伤固定及修复 聚乳酸是聚酯系列可承重的材料之一,由于高机械强度和优异的生物降解性在骨损伤修复中已开始逐步取代金属骨科内固定器械。聚乳酸在医学上发挥的主要作用有接合固定(夹钳、接骨材料、粘接剂)、辅助重建(皮肤、胸壁网络、韧带、血管)、填充保护(骨和软组织缺损部位填充剂、防止粘连、涂敷材料)、药物治疗(药物缓释包衣、微胶囊、植入片),其中常用的骨科内固定有骨钉、螺钉、髓内钉和微型骨板[47-48]。文章列出了典型的聚乳酸及其复合材料在骨科应用的示例,例如:骨骼肌健康解决方案公司ZimmerBiomet?生产的Bio-Statak?是一种由左旋聚乳酸制成的组织附着装置,具有吸收性,据报道其抗拉强度可与金属装置媲美[49];德国弗劳恩霍夫研究所的研究人员开发了聚乳酸复合螺钉,这些螺钉严格模拟了骨骼强度,可以替代钛合金外科植入物[50];其他以Arthrex?、Phusis、Gunze、Takiron和Linvatec为代表的公司已将聚乳酸医疗设备商业化,用作干涉螺钉、微孔板、杆[37](表3)。"

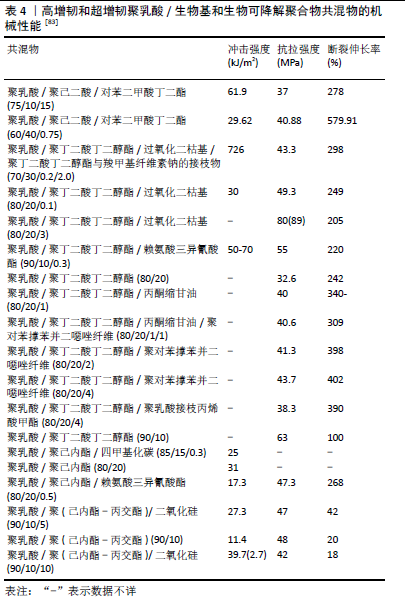
与传统金属骨钉相比,左旋聚乳酸骨钉术后有更好的愈合效果。类似地,对比左旋聚乳酸和不锈钢骨板植入兔股骨8-40周后的机械强度,发现金属骨板的应力遮蔽效应导致了骨质疏松,而左旋聚乳酸骨板的强度在25周后减小至零,未发生应力遮蔽现象[53]。左旋聚乳酸髓内钉可以通过拉伸技术制备,直径为3.2 mm和拉伸比为2.5∶1的超高强度左旋聚乳酸髓内钉的最初弯曲强度和模量分别为240 MPa和 13 GPa。左旋聚乳酸髓内钉的弯曲强度比人密质骨更大,其强度可在骨髓腔内维持8周不变[54]。聚乳酸骨内固定材料的降解性和生物相容性在过去的十几年被广泛研究,相比聚乙醇酸,聚乳酸的降解速率很低,所以很少有不良的组织反应。将左旋聚乳酸螺钉植入小猪骨裂模型中3年未出现肉芽肿瘤和瘘管,螺钉在两三年内充分降解,3年后仅在巨噬细胞中发现了少量残留的聚乳酸降解产物[55]。不仅如此,近期研究发现聚乳酸材料还有抗菌活性[56]。抗菌实验表明,经固态热拉伸后的聚乳酸对金黄色葡萄球菌和副溶血性弧菌的抑制作用均随材料拉伸比的增加先增加后降低,在拉伸比为600%时具有最优的抗菌活性。 2.3.2 骨组织工程材料 组织工程材料是将体外培养的组织、细胞吸附于一种生物相容性良好并可被人体逐步降解吸收的生物材料上,形成细胞-生物材料复合物,能够对病损组织进行形态、结构和功能的重建[57]。与之相对应的骨组织工程的目的是建立种子细胞和生物支架材料的复合体,通过体外培养形成具有一定结构和功能的组织,然后植入体内实现缺损部位的完美修复[58]。 聚乳酸及其一些复合材料在本体性质上符合组织工程材料要求,工艺上也能制成各种与组织匹配的形状[59]。例如,聚乳酸基基质中保留了其超强吸收能力,从而促进了溶胀,产生了非常高的孔隙率[60];将软骨细胞种植在聚乳酸基体内生成了软骨组织[61];基于聚乳酸的复合多孔支架具有巨大的骨再生潜力,并且通过掺入不同含量的生物活性玻璃可以调节支架的降解速率匹配新骨的再生[62];无机的羟基磷灰石与有机的聚乳酸复合成支架作为骨固定材料,表现出优异的骨损伤修复能力[63]。同时进一步的研究发现,羟基磷灰石的填充增加了聚乳酸支架的表面积,增强了聚乳酸的热稳定性,并减少了聚合物的热降解[64]。通过与羟基磷灰石的复合聚乳酸基材料优势更加突出,具体表现在:该复合材料的力学强度比聚乳酸材料更优,同时羟基磷灰石的掺入也降低了聚乳酸的降解速度,延长了材料的降解周期,与骨愈合周期更加匹配;该复合材料既有生物可吸收性又有生物活性,伴随着聚乳酸的降解,羟基磷灰石也逐渐释放出钙离子和磷酸根离子,促进了新骨组织的形成;该复合材料植入动物体内6周后,骨折处已基本愈合,没有关节积液和窦道形成,且未出现迟发性无菌性炎症,具有较强的骨结合能力。 作为骨修复最佳的候选材料之一,医用聚乳酸基复合材料在骨组织工程中的研究也在不断深入展开。VELIOGLU等[65]运用3D打印技术制备的聚乳酸支架与天然骨在孔径、孔隙率和机械特性方面具有相似的特征,并且支架表面的人骨髓间充质干细胞在孔径为1.25 mm的支架上增殖效果很好,该研究证明3D打印聚乳酸支架似乎是用于骨骼修复和再生的候选替代品。FAIRAG等[66]也借助3D打印机设计和制造具有不同孔径(500,750和1 000 μm)的微孔聚乳酸支架,研究发现成骨细胞在支架上显示出高增殖率和代谢活性且有成骨基质蛋白生成。进一步的实验表明,3D打印微孔聚乳酸支架对于临床接种到中等大小支架中的人间充质干细胞具有很强的成骨分化能力,适合作为修复骨缺损的骨替代物。也有研究发现,与羟基磷灰石相比,生物活性玻璃颗粒更多适用于生产用于骨骼再生的3D打印复合支架[63]。由于生物活性玻璃颗粒解离的离子对细胞的生物学反应和成骨作用的影响比羟基磷灰石更大,因此显示出更好的生物友好性和骨诱导性。3D打印技术与易于获得的医疗级聚乳酸和生物活性玻璃材料相结合,可生产针对患者的价格便宜、有效且快速的支架,以生产用于临床治疗骨缺损的支架。 2.4 聚乳酸的改性 尽管有许多优点,但由于缺乏特定的官能团,聚乳酸具有惰性的疏水表面及较低的自由表面能,影响细胞在其表面的附着和增殖,导致其生物相容性降低[67];聚乳酸在自然条件下降解速率较慢,降解酸性产物引起炎症,缺乏生物活性;伴随降解其力学强度有待进一步提高;除此之外,材料良好的抗菌性能也是其在骨科手术中亟需提升的性能之一。因此,聚乳酸功能化改性也是拓宽其应用范围及前景的热门研究内容,其中改性方法主要有共聚、交联、表面修饰等化学方法,以及共混、增塑等物理方法。 2.4.1 交联改性 交联改性是指在交联剂或者辐射作用下通过加入其他单体与聚乳酸发生交联反应,生成网状聚合物以改善其性能。聚乳酸的力学强度还不够高,适度的交联可以提高聚乳酸强度,满足一些强度要求较高的应用,适用于组织修复的骨固定材料[68]。除此之外,交联也是最便捷的提高材料细胞相容性的方法,聚乳酸可与某些亲水且生物相容的组分接枝,例如壳聚糖[69]、明胶[70]、胶原蛋白和其他细胞外基质蛋白等[37]。ALIPPILAKKOTTE等[71]通过用碱溶液处理聚乳酸膜以在其表面引入羧基,然后使用氟硼酸盐作为偶联剂共价接枝明胶。研究表明,通过NaOH的碱水解作用将聚乳酸表面上的羧基和羟基结合起来,再将明胶接枝到聚乳酸表面后,亲水性明胶与疏水性聚乳酸聚合物的组合可提供适当的拉伸强度、伸长率、顺应性、生物相容性和黏弹性,亲水部分提供生物相容性、抗菌活性和模拟黏弹性,而明胶则确保出色的机械强度和支架的稳定性。改性后的聚乳酸支架的拉伸强度为(0.85±0.14) MPa,并且其伸长率为 (41.0±1.61) %。明胶掺入的聚乳酸具有良好的研究结果,表明其在生物医学应用领域尤其是在伤口愈合中具有应用前景,并且还可广泛用于从心脏(血管移植物)到骨骼和皮肤的其他组织工程应用,交联的聚乳酸纤维也可用于韧带和腱重建。近期,KURZINA团队[67]借助离子注入技术,通过结合不同的离子使聚乳酸表面发生化学变化(断链、自由基形成、气体产物释放、交联和碳化),可以有效调控聚乳酸的某些物理化学性质,如亲水性、生物相容性、抗菌性等。研究发现,碳负离子的注入可以促进神经细胞的附着和神经线的再生;金和碳负离子的辐照可以控制表面形态。聚乳酸被广泛用于构建骨修复材料,将抗菌性能附加到聚合物材料上是当前的任务,可以通过将银离子引入材料的表面层来解决。类似地,也有研究通过使用等离子体处理来增强聚乳酸的抗菌活性,并结合抗菌剂进行了改性,从而可用于组织工程中[72]。 2.4.2 共混改性 共混改性是将2种或2种以上的聚合物进行混合,通过聚合物各组分性能的复合来达到改性的目的。共混改性工艺最为简单经济,如与壳聚糖、丙烯酸、聚氧乙烯和聚己内酯等共混可以改善聚乳酸的亲水性[73]。聚乳酸分子中的酯键对水、热等外界刺激较为敏感,其降解伴随着酯键断开形成乳酸,因此导致周围环境的酸性。成骨水平或者骨细胞的增殖与分化能力和微环境的pH值密切相关。SHEN等[74]发现成骨细胞的活性在pH值8-8.5时最佳,当pH值为6时活性较差。一般来说,弱碱性有利于成骨[75]。同样地,FU等[76]研究发现过高的pH值会造成骨细胞的增殖和分化能力变弱,不利于成骨,因此对于填充材料修复骨缺损,需要充分考虑到材料的降解性能以及其对pH值的影响。此外,不同的材料会产生不同的降解产物(小分子、离子等),导致成骨细胞最为适宜的pH值环境不尽相同。聚乳酸天然降解呈弱酸性,为了进一步拓展其在骨修复领域的应用,通常采用复合、改性等方式来调控。例如:与壳聚糖共混、表面碱处理改性,壳聚糖具有较好的亲水性,且水解产物呈弱碱性,可对聚乳酸的酸性产物起中和作用,在作为生物医用材料应用时可以减少聚乳酸降解后期出现的不良反应[77]。因而许多研究都已证明,壳聚糖与聚乳酸共混可以改善聚乳酸的降解性能且可提高其生物相容性,同时也可以根据共混比例调控复合材料的降解速度[78]。 聚乳酸是一种玻璃态聚合物,断裂伸长率不佳(<10%),这严重阻碍了其在许多领域中的应用,近年来对聚乳酸的增韧改性已成为众多研究的重点[79],已经开发了许多策略来提高聚乳酸的韧性。除此之外,用纳米材料复合而成的聚乳酸纳米复合材料也表现出很好的生物相容性、生物可降解性,与普通的聚乳酸相比,还具有良好的韧性和弹性、较高的强度和模量 、优良的力学和机械性能,使得聚乳酸纳米复合材料在医疗领域得到广泛应用。目前应用比较多的纳米颗粒有纳米蒙脱土、纳米二氧化硅、纳米管等。据KILIARIS等[80]研究,纳米填料(包括硅酸盐层,例如蒙脱土)、纳米管(主要是碳纳米管)、富勒烯、炭黑、金属氧化物(例如二氧化钛、氧化铁、氧化铝)、金属纳米颗粒[例如金、银、多面体低聚倍半硅氧烷,半导体(例如硫化铅、硫化镉),纳米金刚石等]可以增强纳米复合材料的热降解。FINNISS等[81]通过添加石墨烯纳米片作为共混填料提高了材料的耐久性。纳米复合材料热稳定性的提高通常归因于:曲折路径的产生,这是由于纳米粒子分散到聚合物基质中而导致的,减慢了所产生物质在材料中的扩散;碳质炭使材料绝缘并减慢分解产物的释放[82]。另一方面,可生物降解的聚合物共混物已成为材料科学非常活跃和重要的研究领域。通常,可以通过增强界面作用和细化相形态来获得具有完全可生物降解聚乳酸共混物,同时具有良好的拉伸韧性和冲击韧性,以及高增韧效率甚至超韧度的完全聚乳酸基可生物降解聚合物共混物。表4总结了高度和超增韧聚乳酸/生物基和可生物降解聚合物共混物的机械性能结果。"
| [1] HAMAD K, KASEEM M, AYYOOB M, et al. Polylactic acid blends: The future of green, light and tough. Prog Polym Sci. 2018;85:83-127. [2] FARAH S, ANDERSON DG, LANGER R. Physical and mechanical properties of PLA, and their functions in widespread applications - A comprehensive review. Adv Drug Deliv Rev. 2016;107(15):367-392. [3] ELMOWAFY EM, TIBONI M, SOLIMAN ME. Biocompatibility, biodegradation and biomedical applications of poly (lactic acid)/poly (lactic-co-glycolic acid) micro and nanoparticles. J Pharm Investig. 2019; 49:347-380. [4] WU CS, TSOU CH. Fabrication, characterization, and application of biocomposites from poly (lactic acid) with renewable rice husk as reinforcement. J Polym Res. 2019;26(2):44-53. [5] MURARIU M, DUBOIS P. PLA composites: From production to properties. Adv Drug Deliv Rev. 2016;107:17-46. [6] MONTICELLI O, CAVALLO D, BOCCHINI S, et al. A novel use of Ti-POSS as initiator of L-lactide ring-opening polymerization. J Polym Sci Pol Chem. 2011;49(22):4794-4799. [7] QI X, REN Y, WANG X. New advances in the biodegradation of Poly (lactic) acid. Int Biodeter Biodegr. 2017;117:215-223. [8] PRETULA J, SLOMKOWSKI S, PENCZEK S. Polylactides-Methods of synthesis and characterization. Adv Drug Deliv Rev. 2016;107:3-16. [9] DELPOUVE N, SAITER-FOURCIN A, COIAI S, et al. Effects of organo-LDH dispersion on thermal stability, crystallinity and mechanical features of PLA. Polymer. 2020;208:122952. [10] LARRAÑAGA A, LIZUNDIA E. A review on the thermomechanical properties and biodegradation behaviour of polyesters. Eur Polym J. 2019;121:109296. [11] BHIOGADE A, KANNAN M, DEVANATHAN S. Degradation kinetics study of Poly lactic acid (PLA) based biodegradable green composites. Mater Today Proc. 2020;24(2):806-814. [12] XU Y, KIM CS, SAYLOR DM, et al. Polymer degradation and drug delivery in PLGA-based drug-polymer applications: A review of experiments and theories. J Biomed Mater Res B Appl Biomater. 2017;105:1692-1716. [13] SAHA SK, TSUJI H. Effects of molecular weight and small amounts of d-lactide units on hydrolytic degradation of poly (l-lactic acid) s. Polym Degrad Stabil. 2006;91(8):1665-1673. [14] GORRASI G, PANTANI R. Hydrolysis and Biodegradation of Poly (lactic acid). Adv Polym Sci. 2017;279:119-151. [15] TSUJI H, IKADA Y. Properties and morphology of poly(L-lactide) 4. Effects of structural parameters on long-term hydrolysis of poly(L-lactide) in phosphate-buffered solution. Polym Degrad Stabil. 2000; 67(1):179-189. [16] LI Z, TAN BH, LIN T, et al. Recent advances in stereocomplexation of enantiomeric PLA-based copolymers and applications. Prog Polym Sci. 2016;62:22-72. [17] SAHA SK, TSUJI H. Hydrolytic Degradation of Amorphous Films of L-Lactide Copolymers with Glycolide and D-Lactide. Macromol Mater Eng. 2006;291:357-368. [18] DRIESKENS M, PEETERS R, MULLENS J, et al. Structure versus properties relationship of poly (lactic acid). I. Effect of crystallinity on barrier properties. J Polym Sci Polym Phys. 2010;47:2247-2258. [19] PORFYRIS A, VASILAKOS S, ZOTIADIS C, et al. Accelerated ageing and hydrolytic stabilization of poly (lactic acid) (PLA) under humidity and temperature conditioning. Polym Test. 2018;68:315-332. [20] KARAMANLIOGLU M, PREZIOSI R, ROBSON GD. Abiotic and biotic environmental degradation of the bioplastic polymer poly (lactic acid): A review. Polym Degrad Stabil. 2017;137:122-130. [21] HOGLUND A, ODELIUS K, ALBERTSSON AC. Crucial differences in the hydrolytic degradation between industrial polylactide and laboratory-scale poly(L-lactide). ACS Appl Mater Interfaces. 2012;4:2788-2793. [22] ELSAWY MA, KIM KH, PARK JW, et al. Hydrolytic degradation of polylactic acid (PLA) and its composites. Renew Sust Energ Rev. 2017; 79:1346-1352. [23] LYU S, UNTEREKER D. Degradability of polymers for implantable biomedical devices. International J Mol Sci. 2009;10:4033-4065. [24] YU K, REN L, TAN Y, et al. Wireless Magnetoelasticity-Based Sensor for Monitoring the Degradation Behavior of Polylactic Acid Artificial Bone In Vitro. Appl Sci. 2019;9(4):739-751. [25] GORRASI G, PANTANI R. Effect of PLA grades and morphologies on hydrolytic degradation at composting temperature: Assessment of structural modification and kinetic parameters. Polym Degrad Stabil. 2013;98(5):1006-1014. [26] 房美函,王碧峤,吕志前,等.PGA,PLA,PGLA碱处理改性及降解性能[J].东华大学学报(自然科学版),2012,38(4):390-395. [27] SEDNICKOVA M, PEKAROVA S, KUCHARCZYK P, et al. Changes of physical properties of PLA-based blends during early stage of biodegradation in compost. Int J Biol Macromol. 2018;113:434-442. [28] JARM V. Nazivlje za biosrodne polimere i njihovu primjenu (Preporuke IUPAC 2012.). Kemija U Industriji. 2014;63:411-432. [29] HOU B, LI Y, LUO Q, et al. The Effect of oligomer in poly (L-lactic Acid) on hydrolysis performance. China Plastics Industry. 2019;47:36-39. [30] NAMPOOTHIRI KM, NAIR NR, JOHN RP. An overview of the recent developments in polylactide (PLA) research. Bioresour Technol. 2010; 101(22):8493-8501. [31] JEONG SI, KIM BS, KANG SW, et al. In vivo biocompatibilty and degradation behavior of elastic poly(L-lactide-co-epsilon-caprolactone) scaffolds. Biomaterials. 2004;25(28):5939-5946. [32] MAINIL-VARLET P, CURTIS R, GOGOLEWSKI S. Effect of in vivo and in vitro degradation on molecular and mechanical properties of various low-molecular-weight polylactides. J Biomed Mater Res. 1997;36:360-380. [33] MIDDLETON JC, TIPTON AJ. Synthetic biodegradable polymers as orthopedic devices. Biomaterials. 2000;21(23):2335-2346. [34] LITAUSZKI K, KOVÁCS Z, MÉSZÁROS L, et al. Accelerated photodegradation of poly(lactic acid) with weathering test chamber and laser exposure – A comparative study. Polym Test. 2019;76:411-419. [35] ATTIA MF, BRUMMEL BR, LEX TR, et al. Recent advances in polyesters for biomedical imaging. Adv Healthc Mater. 2018;7(22):1-12. [36] JEON HJ, KIM MN. Biodegradation of poly(l-lactide) (PLLA) exposed to UV irradiation by a mesophilic bacterium. Int Biodeter Biodegrad. 2013; 85:289-293. [37] CASTRO-AGUIRRE E, INIGUEZ-FRANCO F, SAMSUDIN H, et al. Poly (lactic acid)-Mass production, processing, industrial applications, and end of life. Adv Drug Deliv Rev. 2016;107:333-366. [38] DA SILVA D, KADURI M, POLEY M, et al. Biocompatibility, biodegradation and excretion of polylactic acid (PLA) in medical implants and theranostic systems. Chem Eng J. 2018;340:9-14. [39] SAKAI W, SADAKANE T, NISHIMOTO W, et al. Photosensitized degradation and crosslinking of linear aliphatic polyesters studied by GPC and ESR. Polymer. 2002;43(23):6231-6238. [40] TSUJI H, ECHIZEN Y, NISHIMURA Y. Photodegradation of biodegradable polyesters: A comprehensive study on poly(l-lactide) and poly(ɛ-caprolactone). Polym Degrad Stabil. 2006;91(5):1128-1137. [41] JANORKAR AV, METTERS AT, HIRT DE. Degradation of poly(L-lactide) films under ultraviolet-induced photografting and sterilization conditions. J Appl Polym Sci. 2007;106(2):1042-1047. [42] LEX TR, BRUMMEL BR, ATTIA MF, et al. Iodinated polyesters with enhanced X-ray contrast properties for biomedical imaging. Sci Rep. 2020;10(1):1508-1518. [43] ASHRAF SS, FROUNCHI M, DADBIN S. Gamma irradiated electro-conductive polylactic acid/polyaniline nanofibers. Synthetic Met. 2020; 259(116204):1-7. [44] 张伟,韩颖,张娇娇,等.60Co-γ辐照灭菌对食品和医疗器械的不良影响[J].中国医疗器械信息,2019,25(1):52-53. [45] 刘晓玉,田孟超,陈金周,等.γ-辐照对PLLA分子量及结晶形态的影响[J].高分子通报,2010(1):81-84. [46] HAGHIGHAT F, RAVANDI SAH. Mechanical properties and in vitro degradation of PLGA suture manufactured via electrospinning. Fibers Polym. 2014;15(1):71-77. [47] YEON YK, PARK HS, LEE JM, et al. New concept of 3D printed bone clip (polylactic acid/hydroxyapatite/silk composite) for internal fixation of bone fractures. J Biomater Sci Polym Ed. 2018;29:894-906. [48] SANGEETHA VH, DEKA H, VARGHESE TO, et al. State of the art and future prospectives of poly (lactic acid) based blends and composites. Polym Composite. 2018;39:81-101. [49] LUXIANG Z, LUZHU Z, DONGMEI H, et al. Clinical and Radiologic Follow-Up of Zimmer Biomet Stock Total Temporomandibular Joint Replacement After Surgical Modifications. J Oral Maxillofac Surg. 2018; 76:2518-2524. [50] EGLIN D, ALINI M. Degradable polymeric materials for osteosynthesis: Tutorial. Eur Cell Mater. 2008;16:80-91. [51] NARAYANAN G, VERNEKAR VN, KUYINU EL, et al. Poly (lactic acid)-based biomaterials for orthopaedic regenerative engineering. Adv Drug Deliv Rev. 2016;107:247-276. [52] CALORI IR, BRAGA G, PRISCILA DA COSTA CARVALHO DE JESUS B, et al. Polymer scaffolds as drug delivery systems. Eur Polym J. 2020;129: 109621. [53] POITOUT DG. Biomechanics and biomaterials in orthopedics. Springer, 2016. [54] MATSUSUE Y, YAMAMURO T, OKA M, et al. In vitro and in vivo studies on bioabsorbable ultra-high-strength poly(L-lactide) rods. J Biomed Mater Res A. 2010;26(12):1553-1567. [55] HASEGAWA Y, SAKANO S, IWASE T, et al. The long-term behavior of poly-L-lactide screws in a minipig fracture model: preliminary report. J Biomed Mater Res. 2002;63(6):679-685. [56] LI Z, LIU L, RAO Y, et al. Mechanical and antibacterial properties of oriented poly (lactic acid). Polym Eng Sci. 2019;59(10):2121-2127. [57] DAWSON DR, EL-GHANNAM A, VAN SICKELS JE, et al. Tissue Engineering. Dent Clin North Am. 2019;63:433-445. [58] KOONS GL, DIBA M, MIKOS AG. Materials design for bone-tissue engineering. Nat Rev Mater. 2020;5:584-603. [59] LIU S, QIN S, HE M, et al. Current applications of poly (lactic acid) composites in tissue engineering and drug delivery. Compos. B. Eng. 2020;199:108238. [60] SARTORE L, PANDINI S, DEY K, et al. A versatile cell-friendly approach to produce PLA-based 3D micro-macro-porous blends for tissue engineering scaffolds. Materialia. 2020;9:100615. [61] 汪帅伊.3D打印聚乳酸纳米纤维支架与软骨细胞交联体对大鼠软骨基质损伤修复的研究[D].杭州:浙江大学,2019. [62] MAO D, LI Q, LI D, et al. Fabrication of 3D porous poly (lactic acid)-based composite scaffolds with tunable biodegradation for bone tissue engineering. Mater Design. 2018;142:1-10. [63] ALKSNE M, KALVAITYTE M, SIMOLIUNAS E, et al. In vitro comparison of 3D printed polylactic acid/hydroxyapatite and polylactic acid/bioglass composite scaffolds: Insights into materials for bone regeneration. J Mech Behav Biomed Mater. 2020;104:103641. [64] KAREEM MM, TANNER KE. Optimising micro-hydroxyapatite reinforced poly (lactide acid) electrospun scaffolds for bone tissue engineering. J Mater Sci Mater Med. 2020;31(4):1-13. [65] VELIOGLU ZB, PULAT D, DEMIRBAKAN B, et al. 3D-printed poly (lactic acid) scaffolds for trabecular bone repair and regeneration: scaffold and native bone characterization. Connect Tissue Res. 2019;60(3): 274-282. [66] FAIRAG R, ROSENZWEIG DH, RAMIREZ-GARCIALUNA JL, et al. Three-Dimensional Printed Polylactic Acid Scaffolds Promote Bone-like Matrix Deposition in Vitro. ACS Appl Mater Interfaces. 2019;11(17): 15306-15315. [67] KURZINA I A, LAPUT OA, ZUZA DA, et al. Surface property modification of biocompatible material based on polylactic acid by ion implantation. Surf Coat Tech. 2020;388:125529. [68] BERGER K, GREGOROVA A. Thermal stability of modified end-capped poly (lactic acid). J Appl Polym Sci. 2015;131(22):547-557. [69] CUI YL, QI AD, LIU WG, et al. Biomimetic surface modification of poly (l-lactic acid) with chitosan and its effects on articular chondrocytes in vitro. Biomaterials. 2003;24:3859-3868. [70] CUI Y, GAO X, TIAN J, et al. Biomimetic surface modification of poly (L-lactic acid) with gelatin and its effects on articular chondrocytesin vitro. J Biomed Mater Res A. 2003;66(4):770-778. [71] ALIPPILAKKOTTE S, SREEJITH L. Benign route for the modification and characterization of poly (lactic acid) (PLA) scaffolds for medicinal application. J Appl Polym Sci. 2018;135(13):46056. [72] POPELKA A, ABDULKAREEM A, MAHMOUD AA, et al. Antimicrobial modification of PLA scaffolds with ascorbic and fumaric acids via plasma treatment. Surf Coat Technol. 2020;400:126216. [73] CHOI KM, LIM SW, CHOI MC, et al. Thermal and mechanical properties of poly (lactic acid) modified by poly (ethylene glycol) acrylate through reactive blending. Polym Bull. 2014;71(12):3305-3321. [74] SHEN YH, LIU WC, WEN C, et al. Bone regeneration: importance of local pH—strontium-doped borosilicate scaffold. J Mater Chem. 2012; 22(17):8662-8670. [75] LIU W, WANG T, YANG C, et al. Alkaline biodegradable implants for osteoporotic bone defects—importance of microenvironment pH. Osteoporosis Int. 2016;27(1):93-104. [76] FU S, LIU W, LIU S, et al. 3D printed porous beta-Ca2SiO4 scaffolds derived from preceramic resin and their physicochemical and biological properties. Sci Technol Adv Mater. 2018;19(1):495-506. [77] TANASE CE, SPIRIDON I. PLA/chitosan/keratin composites for biomedical applications. Mater Sci Eng C Mater Biol Appl. 2014;40:242-247. [78] ZUO DY, LI HJ. Structure and Properties of Chitosan/Poly-Lactic Acid Blend Scaffold and Chitosan Powder/Poly-Lactic Acid Blend Scaffold. Adv Mater Res. 2013;647:9-15. [79] YANG Y, ZHANG L, XIONG Z, et al. Research progress in the heat resistance, toughening and filling modification of PLA. Sci China Chem. 2016;59(11):1355-1368. [80] KILIARIS P, PAPASPYRIDES CD. Polymer/layered silicate (clay) nanocomposites: An overview of flame retardancy. Prog Polym Sci. 2010;35(7):902-958. [81] FINNISS A, AGARWAL S, GUPTA R. Retarding hydrolytic degradation of polylactic acid: Effect of induced crystallinity and graphene addition. J Appl Polym Sci. 2016;133(43):44166. [82] DARIE RN, PÂSLARU E, SDROBIS A, et al. Effect of Nanoclay Hydrophilicity on the Poly (lactic acid)/Clay Nanocomposites Properties. Ind Eng Chem Res. 2014;53(19):7877-7890. [83] ZHAO X, HU H, WANG X, et al. Super tough poly (lactic acid) blends: a comprehensive review. RSC Adv. 2020;10:13316-13368. [84] CHOI KM, LIM SW, CHOI MC, et al. Properties of poly (ethylene glycol)-grafted poly (lactic acid) PLA sticized with poly (ethylene glycol). Macromol Res. 2014;22(12):1-8. |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Xu Feng, Kang Hui, Wei Tanjun, Xi Jintao. Biomechanical analysis of different fixation methods of pedicle screws for thoracolumbar fracture [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1313-1317. |
| [3] | Jiang Yong, Luo Yi, Ding Yongli, Zhou Yong, Min Li, Tang Fan, Zhang Wenli, Duan Hong, Tu Chongqi. Von Mises stress on the influence of pelvic stability by precise sacral resection and clinical validation [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1318-1323. |
| [4] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [5] | Zhang Yu, Tian Shaoqi, Zeng Guobo, Hu Chuan. Risk factors for myocardial infarction following primary total joint arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1340-1345. |
| [6] | Wei Wei, Li Jian, Huang Linhai, Lan Mindong, Lu Xianwei, Huang Shaodong. Factors affecting fall fear in the first movement of elderly patients after total knee or hip arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1351-1355. |
| [7] | Wang Jinjun, Deng Zengfa, Liu Kang, He Zhiyong, Yu Xinping, Liang Jianji, Li Chen, Guo Zhouyang. Hemostatic effect and safety of intravenous drip of tranexamic acid combined with topical application of cocktail containing tranexamic acid in total knee arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1356-1361. |
| [8] | Xiao Guoqing, Liu Xuanze, Yan Yuhao, Zhong Xihong. Influencing factors of knee flexion limitation after total knee arthroplasty with posterior stabilized prostheses [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1362-1367. |
| [9] | Huang Zexiao, Yang Mei, Lin Shiwei, He Heyu. Correlation between the level of serum n-3 polyunsaturated fatty acids and quadriceps weakness in the early stage after total knee arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1375-1380. |
| [10] | Zhang Chong, Liu Zhiang, Yao Shuaihui, Gao Junsheng, Jiang Yan, Zhang Lu. Safety and effectiveness of topical application of tranexamic acid to reduce drainage of elderly femoral neck fractures after total hip arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1381-1386. |
| [11] | Wang Haiying, Lü Bing, Li Hui, Wang Shunyi. Posterior lumbar interbody fusion for degenerative lumbar spondylolisthesis: prediction of functional prognosis of patients based on spinopelvic parameters [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1393-1397. |
| [12] | Lü Zhen, Bai Jinzhu. A prospective study on the application of staged lumbar motion chain rehabilitation based on McKenzie’s technique after lumbar percutaneous transforaminal endoscopic discectomy [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1398-1403. |
| [13] | Chen Xinmin, Li Wenbiao, Xiong Kaikai, Xiong Xiaoyan, Zheng Liqin, Li Musheng, Zheng Yongze, Lin Ziling. Type A3.3 femoral intertrochanteric fracture with augmented proximal femoral nail anti-rotation in the elderly: finite element analysis of the optimal amount of bone cement [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1404-1409. |
| [14] | Du Xiupeng, Yang Zhaohui. Effect of degree of initial deformity of impacted femoral neck fractures under 65 years of age on femoral neck shortening [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1410-1416. |
| [15] | Zhang Shangpu, Ju Xiaodong, Song Hengyi, Dong Zhi, Wang Chen, Sun Guodong. Arthroscopic suture bridge technique with suture anchor in the treatment of acromioclavicular dislocation [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1417-1422. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||