牙髓干细胞
-
图1|牙周膜干细胞(PDLSCs)的分离培养、鉴定

应用经典酶消化法获得PDLSCs,细胞在分离培养5 d后顺利贴壁生长,细胞排列稀疏、不规则,呈散在的纺锤样结构,胞体形态丰满,胞核呈卵圆性,见图1A。细胞传代实验和克隆形成实验均显示细胞增殖生长的速度相较于初期呈明显的几何级数增长,约3 d就可增长到培养器皿底面的95%,见图1B;单克隆实验显示有显著的细胞集落群形成,呈漩涡状,见图1C。同期,流式细胞仪检测培养的PDLSCs可阳性表达间充质干细胞表面标记物STRO-1(15.6%)、CD146(42.85%);阴性表达血小板内皮细胞标志分子CD31(0.527%)及白细胞共同抗原CD45(1.61%),见图1D。细胞经成骨及成脂向分化诱导培养后,经相应的染色处理,各组细胞可分别呈现粉染的碱性磷酸酶、红染的钙结节和胆红素串珠样的脂滴,成骨和成脂相关基因均较空白对照组呈上升趋势,提示实验培养的细胞具有骨向分化和脂肪向分化的潜能,见图1E-I。以上结果证实课题组分离、培养的细胞符合PDLSCs的生物学性能,培养成功。
图3|构建过表达和干扰Lin28A表达的牙周膜干细胞(PDLSCs)模型

构建过表达和干扰Lin28A表达的慢病毒载体,转染至PDLSCs。荧光显微镜下显示:除空白对照组外,各组PDLSCs均不同程度显示出明显的绿色荧光,表明重组慢病毒载体转染细胞成功,见图3A。qRT-RCR检测转染72 h后各组PDLSCs中Lin28A的表达水平,过表达Lin28A组的表达量明显增高(P < 0.01),干扰Lin28A组细胞的表达量显著下降(P < 0.01),差异有显著性意义;而转染过表达空载体和干扰表达空载体的这两组细胞其Lin28A的表达量与空白对照组比较无明显差异,见图3B。上述结果说明过表达及干扰表达的效率与空载体及空白对照组比较有明显差异,符合正反两个方面的PDLSCs模型构建,可为后续相关分子机制研究提供实验基础。
图4|过表达Lin28A和干扰Lin28A表达的牙周膜干细胞(PDLSCs)经成骨诱导后成骨指标的表达变化
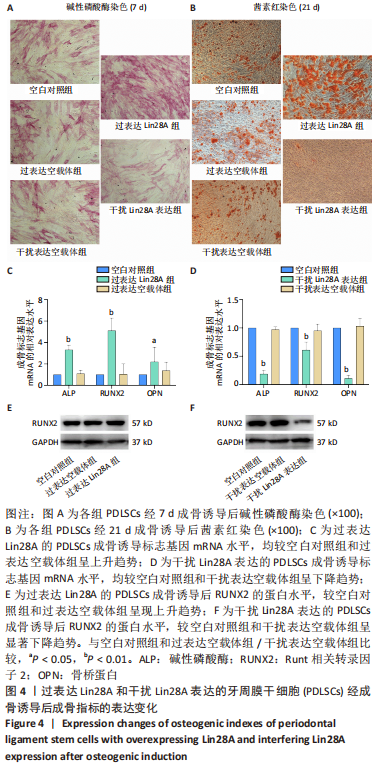
经不同慢病毒载体转染的PDLSCs模型给予相应的成骨诱导。成骨诱导7 d,早期指标碱性磷酸酶染色结果显示,过表达Lin28A组的细胞染色较深,而干扰Lin28A表达组碱性磷酸酶染色较少,成骨能力较弱,过表达空载体组和干扰表达空载体组的染色结果与空白对照组基本一致,没有明显的染色差异,见图4A。各组细胞在成骨诱导21 d后,成骨晚期茜素红染色结果显示:过表达Lin28A组细胞红染的钙结节明显、量多;而干扰Lin28A表达组钙结节形成较少,镜下视野呈现出量少或几乎没有的状态,成骨能力显著降低;同期,过表达空载体组和干扰表达空载体组的钙化结节形成量与空白对照组无明显差别,见图4B。收集骨向诱导14 d的各组细胞总RNA,检测每组细胞中成骨标志基因的mRNA表达水平,仍以GAPDH为参照基因。与空白对照组相比较,转染过表达Lin28A载体的PDLSCs成骨基因碱性磷酸酶、Runt相关转录因子2及骨桥蛋白的表达量显著升高,而转染过表达空载体的PDLSCs成骨基因表达水平与空白对照组相比无明显差异,说明过表达Lin28A可以促进PDLSCs成骨向分化各项成骨指标高表达;转染干扰Lin28A表达载体的PDLSCs其成骨基因的表达水平显著下降,转染干扰表达空载体的PDLSCs成骨基因的表达水平与空白对照组比较无明显差异,说明干扰Lin28A表达后PDLSCs的骨向分化能力减弱,得出与过表达Lin28A相反的结果,见图4C,D。经成骨诱导分化,5组细胞的成骨相关蛋白Runt相关转录因子2的表达趋势与成骨基因表现的趋势一样,即过表达Lin28A组的Runt相关转录因子2蛋白表达相较空白对照和空载体对照组显著增高(P < 0.05),见图4E;而干扰Lin28A表达后,PDLSCs的成骨相关蛋白Runt相关转录因子2的表达量明显降低(P < 0.01),见图4F。