中国组织工程研究 ›› 2012, Vol. 16 ›› Issue (49): 9209-9213.doi: 10.3969/j.issn.2095-4344.2012.49.016
• 干细胞移植 stem cell transplantation • 上一篇 下一篇
骨髓间充质干细胞修复Wistar大鼠的脊髓损伤
贾全章1,李东君2,陈玉丙3,孙景海1,王风华1,徐 爽1,刘丽萍3,高德萱2,姜大伟2
- 1解放军第208医院,吉林省长春市 130062;2延边大学医学部,吉林省延吉市 133002;3吉林大学附属第二医院,吉林省长春市 130041
Bone marrow mesenchymal stem cells repair Wistar rat spinal cord injury
Jia Quan-zhang1, Li Dong-jun2, Chen Yu-bing3, Sun Jing-hai1, Wang Feng-hua1, Xu Shuang1, Liu Li-ping3, Gao De-xuan2, Jiang Da-wei2
- 1No.208 Hospital of Chiinese Liberation Army, Changchun 130062, Jilin Province, China; 2Department of Medicine, Yanbian University, Yanji 133002, Jilin Province, China; 3The Second Affiliated Hospital of Jilin University, Changchun 130062, Jilin Province, China
摘要:
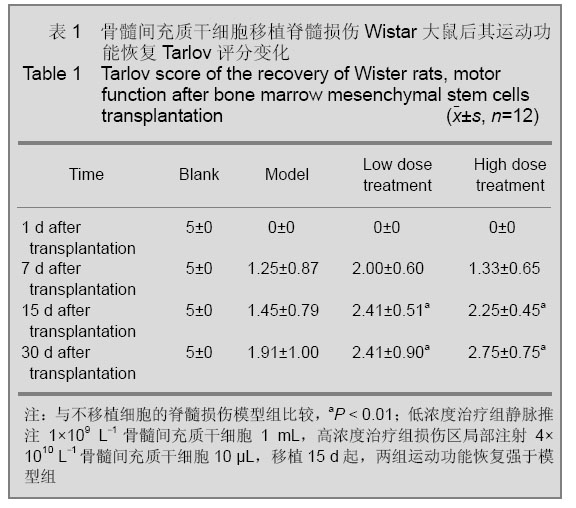
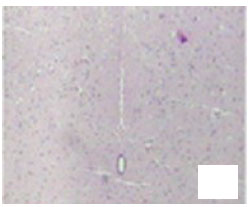
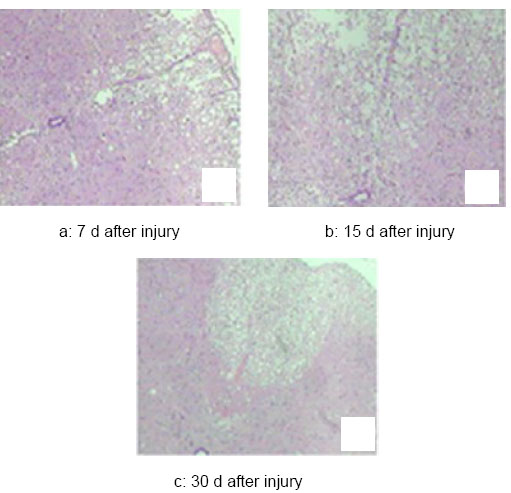
背景:研究表明,骨髓间充质干细胞移植治疗脊髓损伤已取得疗效。 目的:观察骨髓间充质干细胞移植对脊髓损伤大鼠脊髓功能的影响。 方法:120只大鼠随机数字表法分为4组:空白组不造模,于脊髓损伤后当天损伤区局部注射生理盐水10 μL;模型组采用改良的Allen’s打击法造成脊髓损伤模型,不做任何治疗;低浓度治疗组行脊髓损伤后当天经尾静脉注射浓度为1×109 L-1骨髓间充质干细胞1 mL;高浓度治疗组行脊髓损伤后当天损伤区局部注射浓度为4×1010 L-1骨髓间充质干细胞10 μL。 结果与结论:损伤后1 d模型组和两治疗组均无恢复迹象,运动评分低于空白组(P < 0.01);损伤7 d,两治疗组运动功能有所恢复,行为学评分均高于模型组,但差异无显著性意义(P > 0.05);损伤15,30 d,两治疗组行为学评分均明显高于模型组(P < 0.01)。移植后7,15,30 d脊髓病理切片显示治疗组较模型组均有显著恢复。提示骨髓间充质干细胞对脊髓损伤模型大鼠的脊髓功能有修复作用。
中图分类号: