中国组织工程研究 ›› 2023, Vol. 27 ›› Issue (19): 3011-3016.doi: 10.12307/2023.640
• 牙髓及牙周膜干细胞 Dental pulp and periodontal ligament stem cells • 上一篇 下一篇
白藜芦醇促进人乳牙牙髓干细胞的增殖和成骨分化
岳海云1,孙银雪2,毕迎春3
- 解放军第九六〇医院,1基础医学实验室,3口腔科,山东省济南市 250031;2山东中医药大学第一临床医学院,山东省济南市 250355
Resveratrol promotes the proliferation and osteogenic differentiation of stem cells from human exfoliated deciduous teeth
Yue Haiyun1, Sun Yinxue2, Bi Yingchun3
- 1Department of Basic Medical Sciences, 960 Hospital of Chinese PLA, Jinan 250031, Shandong Province, China; 2First Clinical Medical College of Shandong University of Chinese Medicine, Jinan 250355, Shandong Province, China; 3Department of Stomatology, 960 Hospital of Chinese PLA, Jinan 250031, Shandong Province, China
摘要:
文题释义:
白藜芦醇:是广泛存在于葡萄、坚果、蓝莓等植物中的天然非黄酮类多酚化合物,能促进骨膜和骨髓来源间充质干细胞的增殖和成骨分化,抑制破骨细胞的活性和生成。乳牙牙髓干细胞:人乳牙牙髓干细胞来源于人替换的乳牙牙髓,具有较高的增殖率、端粒酶活性以及多向分化潜能,其分化能力受细胞因子、小分子化合物等诸多因素的调节。
背景:白藜芦醇是一种天然非黄酮类多酚化合物。研究表明,白藜芦醇具有抗氧化、抗炎、抗衰老和抗肿瘤等多种生物活性,并且能促进骨髓间充质干细胞的成骨分化,但其是否能调节乳牙牙髓干细胞的成骨分化尚不清楚。
目的:研究白藜芦醇对人乳牙牙髓干细胞增殖和成骨分化能力的影响。
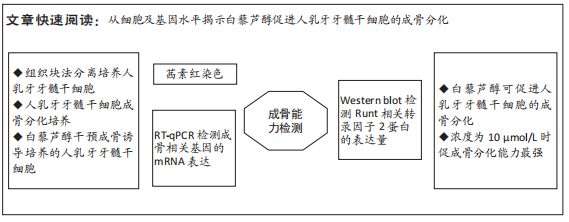
方法:组织块法分离培养人乳牙牙髓干细胞,不同浓度的白藜芦醇处理成骨诱导的人乳牙牙髓干细胞,CCK-8检测细胞活性,茜素红染色检测矿化结节数量,RT-qPCR检测成骨相关基因的mRNA表达及Western blot检测Runt相关转录因子2的蛋白水平。
结果与结论:①CCK-8 检测结果显示,处理第3天时,较高浓度(20,40,80,100 μmol/L)白藜芦醇显著抑制细胞增殖,因此,后续实验中选用1,5,10 μmol/L白藜芦醇处理乳牙牙髓干细胞,检测其对成骨分化的作用;②与成骨诱导对照组相比,10 μmol/L白藜芦醇组乳牙牙髓干细胞的矿化结节数量显著增多;③与成骨诱导对照组相比,10 μmol/L白藜芦醇组乳牙牙髓干细胞的碱性磷酸酶、Runt相关转录因子2和骨钙素的mRNA表达量升高;④与成骨诱导对照组相比,白藜芦醇组乳牙牙髓干细胞的Runt相关转录因子2蛋白水平呈浓度依赖性增加;⑤结果表明,适宜浓度的白藜芦醇可提高人乳牙牙髓干细胞的增殖和成骨分化能力。
https://orcid.org/0000-0002-7529-8716 (岳海云)
中图分类号: